有机化学课件-多环芳烃
有机化学课件-多环芳烃

NH2
Zn
HCl
a. 萘的化学性质 1. 亲电取代反应 c. 磺化
由于热力学与动力学上的不同导致产物不同的例子: 1、共轭二烯烃与氯化氢的加成反应—是1,2还是1,4加成 2、甲苯的磺化反应 动力学在邻位,热力学在对位。 3、萘的磺化反应。
SO 3H
40-80 C
o
o
96%
-磺化为主
160 C H2SO4 + H2SO4 160 C
内容回顾
§6.6 苯环上亲电取代反应的定位规律
苯环上取代基对亲电取代反应的影响 取代基对反应活性的影响及定位作用的理论解释 双取代基的定位作用,位阻对定位的影响
取代基的定位作用在合成中的应用
第七章 多环芳烃和非苯芳烃
§7.1 多环芳烃的分类与命名
§7.2 联苯及其衍生物
§7.3 稠环芳烃:萘、蒽 §7.4 非苯芳烃(休克尔规则)
§7.3 稠环芳烃
§7.3.1 萘、蒽的结构
b. 蒽的结构 sp2杂化, 平面结构,
键长不均等(与普通的单双键不同)
表达式
§7.3 稠环芳烃
§7.3.2 萘、蒽的化学性质
a. 萘的化学性质 1. 亲电取代反应
具有芳香性,易发生亲电取代, 但比苯易发生氧化及加成反应。
萘的亲电取代反应活性大于苯,-位比-位更易发生亲电取代反应。 共振论的解释
反式,十氢化萘
Na (or Li) NH3-C2H5OH (4mol)
§7.3 稠环芳烃
§7.3.2 萘、蒽的化学性质 b. 蒽的化学性质 蒽比萘更容易反应,位最活泼。 (A) 加成反应: 9,10 位加成
+ H2
H + Br2
CCl4
多环芳烃 (2)

多环芳烃什么是多环芳烃?多环芳烃(Polycyclic Aromatic Hydrocarbons,简称PAHs)是一类由苯环和其它碳氢环组成的有机化合物。
它们在自然界中广泛存在,源自于燃烧和热解过程,也可以由石化工业、炼油厂、汽车尾气等排放物中检测到。
多环芳烃具有高稳定性和高残留性,对环境和人类健康具有潜在的危害。
多环芳烃的结构和分类多环芳烃通常由两个或更多个苯环组成,并被称为环间连通的芳烃。
根据多环芳烃的结构,它们可以分为三类:1. 两环芳烃两环芳烃是最简单的多环芳烃,由两个苯环组成。
最常见的两环芳烃是萘(naphthalene)和菲(phenanthrene)。
这些化合物常在燃烧和热解过程中产生。
2. 三环芳烃三环芳烃是由三个苯环组成的多环芳烃,例如芘(pyrene)和蒽(anthracene)。
这些化合物较为稳定,常在化石燃料的燃烧中生成。
3. 四环以上芳烃四环以上芳烃是由四个或更多个苯环组成的多环芳烃,例如苯并(a)芘(benz[a]anthracene)和苯并(a)蒽(benz[a]anthracene)。
这些芳烃在环境中普遍存在,并被认为是环境中的污染物。
多环芳烃的来源和污染多环芳烃的主要来源是燃烧和热解过程。
例如,汽油和柴油的燃烧过程中会产生大量的多环芳烃,其中一些化合物(如苯并(a)芘和苯并(a)蒽)被认为是致癌物质。
此外,石化工业、炼油厂、焚烧厂以及某些工业过程中也会生成多环芳烃。
这些化合物通过大气、水和土壤的传播,进入到环境中。
多环芳烃在环境中的残留时间较长,它们可以在空气中悬浮、沉积在土壤中,甚至进入水体中。
这些污染物可能对人类健康和环境造成危害。
多环芳烃的环境影响多环芳烃对环境具有广泛的影响。
它们可能对水体生态系统产生毒性作用,影响水生生物的生长和繁殖。
多环芳烃在土壤中残留的时间较长,会导致土壤的污染,并对农作物的生长和产量产生负面影响。
除了对环境的直接影响外,多环芳烃还具有生物积累性。
第六章 多环芳烃(化学)
无
π 符合4n+2,由于环较大,内部氢斥力小,能共平面 有 π 符合4n+2,由于环较大,内部氢斥力小,能共平面 有 [26]轮烯 π 超过[26]轮烯,由于环太大,难保持共平面,虽符合4n+2规则,也无芳香性。
18 18 22 22 26 26
符合4n+2,由于环较大,内部氢斥力小,能共平面
有
富勒烯(Fullerenes)
NO2 HNO3- H2SO 4 30-60 度 95% Fe + HCl NH2
-硝基萘主要用于制备-萘胺,它是染料、医药和农药中间体。
(3) 磺化
同苯一样,萘用浓硫酸的磺化也是可逆的。因位比位活泼,所 以用浓硫酸在较低温磺化时,主要得-萘磺酸。但如果在较高 温下磺化时,则主要得-萘磺酸。并且实验发现,将-萘磺酸 与硫酸在较高温下加热,它也能转变为-萘磺酸。
CH3
(2) 原来取代基为第二类定位基时,则钝化芳环,主要发生异环 -位取代。如: NO
2
NO2
萘亲电取代的定位规律
但是,萘的亲电取代反应有的不遵循定位规律,如:
CH3 92% H SO 2 4 HO3S
CH3
7.3 蒽和菲
除了萘,蒽和菲是较重要的稠环芳烃,它们和萘一起存 在于煤焦油中,蒽和菲是同分异构体,命名时有固定 的编号。 8 9 1
于光生伏特电池、光电二极管等高科技领域。
富勒烯
C60和一些有机化合物的结合,或在C60内嵌入某种放射性元 素,则有可能在医学的某些领域,如清除体内自由基、治疗 癌症等方面发挥其独特的作用。 目前,C60及其衍生物的研究正方兴未艾,而开拓这一新领域 的三位科学家—柯尔、斯莫利和克罗托,也因“发现碳的球 状结构——即富勒式结构,开创了化学研究的新领域”而共 同荣获了1996年的诺贝尔化学奖。
《有机化学》课件第07章 多环芳烃和非苯芳

环丙烯碳正离子的芳香性
14
环戊二烯负离子与环庚三烯正离子
15
环戊二烯负离子与环庚三烯正离子
16
Aromaticity of azulene
17
(Azulene) 的芳香性
Azulene
=1.08D
18
8
十氢化萘的构象
H H
顺十氢化萘
H
H
反十氢化萘
9
萘的反应-氧化
10
蒽的反应
(蒽醌)
11
蒽醌类染料和偶氮类染料
O
O
NN
蒽醌 (Anthraquinone)
偶氮苯 (Azobenzene)
12
环状共轭体系分子轨道示意图
反键 非键 成键
休克尔规则 单环共轭体系的电子数为4n+2时该化合物具有芳香性
《有机化学》课件第07章 多环芳烃 和非苯芳
稠环芳烃-萘及其衍生物
8 7
1 2
6 5
3 4
NO 2
萘 (Naphthalene)
Cl
1-硝基萘
2-氯萘
Br
1-溴萘
2
稠环芳烃-蒽、菲和其它化合物
蒽(Anthrathene)
菲(Phenanthrene)
芘(Pyrene)
蒄(Coronene,非蔻)3Βιβλιοθήκη 稠环芳烃的结构-萘的轨道图
4
萘的反应-亲电取代
5
萘-位和-位亲电反应的活性比较
HE
+
HE
+
反应在-位时碳正离子中间体的结构
+H E
反应在-位时碳正离子中间体的结构
6
萘磺化反应的动力学控制和热力学控制
高校化工-有机化学-课件-Org_Ch07 多环芳烃等

-硝基萘 (79 %) •萘的硝化反应速度比苯的硝化要快几百倍. •-硝基萘是黄色针状晶体,熔点61℃,不溶于水而溶于 有机溶剂. 常用于制备 -萘胺(合成偶氮染料的中间体):
NO 2 Zn + HCl [H] NH2
-萘胺
18
(c) 磺化 •萘的磺化也是可逆反应. •磺酸基进入的位置和反应温度有关.
11
萘的分子轨道示意图 • 每个碳原子还有一个p轨道,这些对称轴平行的p轨道 侧面相互交盖,形成包含10个碳原子在内的分子轨道. • 在基态时,10个电子分别处在5个成键轨道上. • 所以萘分子没有一般的碳碳单键也没有一般的碳碳双 键,而是特殊的大键. • 由于电子的离域,萘具有255kJ/mol的共振能(离域能).
(2) 此外,环上有给电子基时“同环定位”;环上有吸电子 基时是“异环定位”。
27
OH CH3
一、上述讨论的 仅仅是一般原则, 幻化时就有例外。 二、有关异环定 位规律苯教材没 有详细论述主产 物的位置,详见 刑其毅基础有机 化学
同 环 定 位 : 1)首 先 看 取 代 基 对 苯 环 的 定 位 2)再 看 a-定 位 NO2 NO2
第七章作业(157)
2、 3、 5、 6、 7。
1
第七章 多环芳烃和非苯芳烃 (Polycyclic Aromatic Hydrocarbon and Nonbenzenoid Aromatic Hydrocarbon )
2
本章重点与难点
• 萘的结构; • 萘的性质; • 芳香性的判断。
3
按照苯环相互联结方式,多环芳烃可分为三种: (1) 联苯和联多苯类 (2) 多苯代脂烃类 (3) 稠环芳烃
16
*萘的位比位活性高的解释 • 萘的位取代时,中间体碳正离子的共振结构式:
有机化学课件(徐寿昌 全)7

3. 萘环的取代规律 • 萘衍生物进行取代反应的定位作用要比苯衍生物复 杂. • 原则上 第二取代基的位置要由原有取代基的性质和 原则上:第二取代基的位置要由原有取代基的性质和 位置以及反应条件来决定.但由于 位的活性高,在一般 但由于α 位置以及反应条件来决定 但由于 α位的活性高 在一般 条件下,第二取代基容易进入 第二取代基容易进入α 条件下 第二取代基容易进入α位. • 此外 环上的原有取代基还决定发生 “ 同环取代 ” 还 此外,环上的原有取代基还决定发生 同环取代” 环上的原有取代基还决定发生“ 异环取代” 是“异环取代”.
NO2 Zn + HCl [H] NH2
(c) 磺化
萘的磺化也是可逆反应. 萘的磺化也是可逆反应 磺酸基进入的位置和反应温度有关. 磺酸基进入的位置和反应温度有关
热力学控制? 热力学控制? 动力学控制? 动力学控制?
SO3H 100 %H2SO4
96 %
165℃ H2SO4 ℃
<80℃ ℃
SO3H
SO3H 对甲萘磺酸
NO2 1,5-二硝基萘 二硝基萘
2. 萘的性质 萘为白色晶体,熔点 熔点80.5℃,沸点 ℃,有特殊气味 沸点218℃ 有特殊气味 ☆萘为白色晶体 熔点 ℃ 沸点 (常用作防蛀剂 易升华 常用作防蛀剂),易升华 常用作防蛀剂 易升华. 不溶于水,而易溶于热的乙醇和乙醚 而易溶于热的乙醇和乙醚. ☆不溶于水 而易溶于热的乙醇和乙醚 萘在染料合成中应用很广,大部分用来制造 大部分用来制造邻苯 ☆萘在染料合成中应用很广 大部分用来制造邻苯 二甲酸酐. 二甲酸酐 • 萘 具 有 2 5 5 kJ/mol 的 共 振 能 ( 离 域 能 ) , 苯 具 有 1 5 2 kJ/mol, 所以萘的稳定性比苯弱 萘比苯容易发生加成 所以萘的稳定性比苯弱,萘比苯容易发生加成 和氧化反应,萘的取代反应也比苯容易进行 萘的取代反应也比苯容易进行. 和氧化反应 萘的取代反应也比苯容易进行
多环芳烃的降解ppt课件

在整堂课的教学中,刘教师总是让学 生带着 问题来 学习, 而问题 的设置 具有一 定的梯 度,由 浅入深 ,所提 出的问 题也很 明确
不同的菌属对不同的PAHs的降解能力存在着很大的差别, 降解产物和途径也大不相同。
在整堂课的教学中,刘教师总是让学 生带着 问题来 学习, 而问题 的设置 具有一 定的梯 度,由 浅入深 ,所提 出的问 题也很 明确
影响因素
环境中PAHs的生物降解过程主要涉及到微生物、PAHs污 染物和环境,所以可将直接或间接影响PAHs生物降解性能的 因素分为三个大的方面,即基质的影响、微生物活性和环境 因子的影响。 1.基质的影响主要是指PAHs的生物可利用性。污染物的浓度 、化学结构、毒性、溶解性和吸附性能都影响PAHs的生物可 利用性。 2.影响PAHs生物降解的环境因子包括PAHs的存在状态、温度 、溶解氧、营养盐、pH、盐度等。 3.微生物的活性强烈地影响生物降解的效果。生物降解的成 功与否很大程度上取决于降解微生物群落在环境中的数量及 生长繁殖速率。
几种多环芳烃的结构
在整堂课的教学中,刘教师总是让学 生带着 问题来 学习, 而问题 的设置 具有一 定的梯 度,由 浅入深 ,所提 出的问 题也很 明确
二、来源
天然来源主要是陆地和水生生物的合成、森林和草原火灾、火山爆发等,在 这些过程中均会产生PAHs。
人为来源环境中多环芳烃的主要来源包括化学工业污染源、交通运输污染 源、生活污染源和其他人为源。主要是由各种矿物燃料(如煤、石油、天 然气等)、木材、纸以及其他含碳氢化合物的不完全燃烧或在还原气氛下 热解形成的。
多环芳烃

多环芳烃(PAHs)是环境常见的污染物之一,其来源于有机物热解和不完全燃烧, 在空气、水、土壤中广泛分布。
由于食品产地环境受到污染, 致使PAHs在食品中存在,同时加工方式不同, 也会影响食品中PAHs的含量。
长期食用含有PAHs的食物对健康将产生潜在威胁[2-5]。
不同国家和地区, 烹饪方法和饮食习惯不同,从食品中摄入的PAHs量也不相同。
不同食品中含有不同种类和浓度的多环芳烃,其主要来源有以下3方面: (1)自然界天然存在的,如植物、细菌、藻类的内源性合成,使得森林、土壤、海洋沉积物中存在多环芳烃类化合物; (2)环境污染造成的,现代工业生产和其它许多方面要使用和产生多环芳烃类化合物;这些物质难免会有一些排放到食品的生产环境如水源、土壤、空气、海洋中,从而对食品造成污染,这是目前食品中多环芳烃最主要的来源;(3)食品加工和包装过程中产生的,如食品的烤、炸、熏制和包装材料、印刷油墨中多环芳烃污染,这也是食品中多环芳烃的重要来源。
目前,各类食品已检测出20余种PAHs,其中以熏烤类食品污染最严重:如熏肉吉有屈、苯并[b]荧蒽、苯并[e]芘、苯并[k]荧蒽、苯并[a]芘、1,2,5,6-二苯并蒽、茚[1,2,3-cd]并芘等PAHs。
王绪卿评价了14种熏烤肉中PAHs的污染水平,并在19份腊昧肉中全部测出屈、苯并[e]芘、苯并[k]荧蒽,其中9份样品苯并[a]芘量为0.34~27.56μg/kg。
另据报道,尼日利亚各种熏烤鱼中均含有PAHs。
比较了现代烤炉与传统烤炉熏烤物中13种PAHs含量,前PAHs<4.5μg/kg。
后者苯并[a]芘为0.2~4.1μg/kg(湿质量)。
食用植物油及其加热产物中均含有PAHs[6-7],而且加热后PAHs含量显著增加。
实验表明,食用植物油加温后B(a)P含量是加温前的2.33倍,1,2,5,6-二苯并蒽为4.17倍,而且油烟雾中其含量更高,厨房空气气态样品中PAHs种类与含量均大于颗粒物,说明厨房空气中PAHs可能主要是由于食品,特别是动植物蛋白以热油烹炸过程中形成。
多环芳烃ppt课件

但是,
“湾区理论”没有提出PAH致癌活性的定量判据,因而缺乏预测能力。
32
四、多环芳烃的结构与致癌性
双区理论
戴乾圜在总结“K区理论”、“湾区理论”的基础上,用PMO法计算了 49个PAH的K区碳原子和湾区碳原子的离域能及分子中各个碳原子的Dewar 指数,并以PAH在生物体内的代谢试验资料为依据,对计算数据进行数学处 理,提出了“双区理论”。
德国:食物、接触食物、可能会放入口中的产品以及儿童用品, 111111苯并(a)芘<0.1mg/kg, 16种PAHs总和<1mg/kg 有人估计,成年人每年从食物中摄取的PAHs总量为1~2mg,如果累积摄 入PAHs超过80mg即可能诱发癌症,因此建议每人每天的摄入总量不可 超过10μg。
18
三、多环芳烃在环境中的迁移转化
5 、“湾区理论”认为 PAH 的致癌机理是:“
湾区碳正离子”具有很强的亲电性,它可以与生物
大分子 DNA 的负电中心结合,生成共价化合物, 导致基因突变,形成癌症。
31
四、多环芳烃的结构与致癌性
湾区理论
“湾区理论”是建立在PAH在生物体内代谢实验基础上的,它解释了除 苯并[a]蒽和苯并[a]芘之外,多数PAH的致癌性,证明了“湾区环氧化物”在 致癌过程中起了重要作用。
论”,他们把PAH分子结构中的不同位置划分为“湾区”、A区、B区和K
区:
12 A区 9 8 7
29
1 2 3 4
11 10
6
5
四、多环芳烃的结构与致癌性
湾区理论
A区是最先被氧化的区域;B区是最终被氧化的区域; K区的位置与“K
区理论”中的K区相同,湾区理论要点如下:
1、PAH分子中存在“湾区”是其具有致癌性的主要原因。 2、在湾区的角环“B区”容易生成环氧化物, 它能自发地转变成“湾区碳正离子”。
有机化学:第二节 多环芳烃

(1)蒽和菲的结构和命名
α
γ
α
89
1
β7
2β
β6
3β
5 10 4
αγ
α
3
4
2
5
6
1
7 8
10 9
蒽
菲
蒽 的 离 域 能 为 349kJ/mol; 菲 的 离 域 能 为 381.63kJ/mol;菲的芳香性比蒽强。
Br
9-溴蒽
SO3H
5-硝基-2-蒽磺酸
NO2
9-溴菲
Br
3. 其它稠环芳烃
茚
芴
芘
b. 有4n 个p电子的环烯烃具有反芳香性和非芳香性
问题:环辛四烯有没有芳香性?
环烯烃
P电子数 4
稳定性 << 开链烯烃
是否具芳香性 反芳香性
4 + 2 >>开链烯烃
芳香性
4 + 4 接近开链烯烃 非芳香性
4 + 2 >>开链烯烃
芳香性
4 + 2 >>开链烯烃
芳香性
能量
π*
反键轨道
非键轨道
π
成键轨道
一平面内,无芳香性。
HH
HH
[14]-轮烯有芳香性
HH
HH
[16]-轮烯无芳香性
HHH HH H
[18]-轮烯有芳香性
5.并联环系:
-+
薁
μ=3.335×10-30 C﹒m
薁可以看成是环戊二烯负离子和环庚三烯正离 子稠合而成,具有较大偶极距,是典型非苯芳烃。
第二节 多环芳烃
多环芳烃可分为三类
(1)联苯和联多苯类:
第七章多环芳烃
H
2
165度
SO
4
H2SO4 165度
SO3H
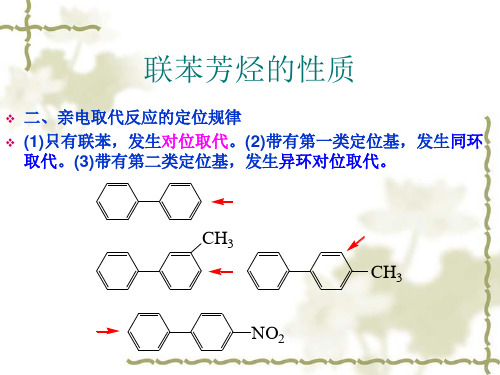
萘的磺化
出现上述现象是由于在-萘磺酸中 由于磺酸基体积较大,与邻环8位上 H
的氢原子距离较近,存在着范德华
SO3H
H SO3H
张力。而在-萘磺酸中,这种空间
H
斥力较小,因此-萘磺酸比-萘磺酸稳定。所以在高温下-
萘磺酸是主要产物。但 由于-位电子云密度较高,反应活化
HH
H
H
K2Cr2O7 + H2SO4
OO 9,10-菲醌
9,10-菲醌是一种农药,可防治小麦莠病和红薯黑斑病等。
7.4 非苯芳烃
在有机化合物中,除苯系芳烃外,还有一些环状烯烃及离子和一 些轮烯等,它们虽然不含有苯环,但却具有闭合的离域大键, 它们的性质也和苯相似,不易加成和氧化,易发生亲电取代反 应,即具有芳香性。常把这类不含苯环的,具有芳香性的环状 多烯化合物叫非苯芳烃。
7.3 蒽和菲
除了萘,蒽和菲是较重要的稠环芳烃,它们和萘一起存
在于煤焦油中,蒽和菲是同分异构体,命名时有固定
的编号。 8 9 1
7
2
6
3
5 10 4
9 8
10 1
7
2
6 5 43
一、蒽和菲的结构
一、蒽和菲的结构
蒽和菲都是平面型分子,C为SP2杂化,都存在一个闭
π 合的离域大键(
14 14
)。但它们与苯和萘相比,
COCH3
+ CH3COCl
AlCl 3 CH2Cl2 0度
-萘乙酸是一个重要的植物生长调节剂。
2. 萘的还原反应
萘比苯更易进行加成和还原,但比烯烃难。如:
有机化学多环芳烃和非苯芳烃PPT学习教案

[10]轮烯——C10H10
HH
环癸五烯
π电子数10,n=2,但由 于轮内氢原子间斥力大, 使环发生扭转,不能共面 ,故无芳香性。
第22页/共26页
[14]轮烯——C14H14
H HH H
环十四碳七烯 [18] 轮烯——C18H18
π电子数14,n=3,但 仍无芳香性。
H HH HH
H
环十八 碳九烯
命名时不论取代基位置如何编号都要从一个位开始并经过该环编到另一个1072萘的结构命名和性质22硝基萘硝基萘硝基萘硝基萘1616二硝基萘二硝基萘clch萘的结构萘的结构并不相等并不相等说明萘环中说明萘环中各各碳原子的碳原子的pp轨道重叠程轨道重叠程度不完全相同度不完全相同由此导致由此导致其中其中某些原子某些原子性质活泼性质活泼易发生化学反易发生化学反01404nm01365nm01424nm01393nm分子式为c10是大键体系
7-3 蒽
命名
分子式C14H10,命名与萘相 似,蒽环也有固定的编号次序.
8
9
1
7
2
CH3
9-甲基蒽
6 51
3 4
1,4,5,8位—0—位
2,3,6,7位——位
9, 10 位——γ位
-甲基蒽
C2H5 2-乙基蒽
-乙基蒽
第13页/共26页
7-3 蒽
蒽的结构
平面结构, 所有碳原
0.1408 nm 子为sp2杂化, 是大π键
有机化学多环芳烃和非苯芳烃
会计学
1
7-1 联苯
3′ 2′ 2 3
1′ 1
4′
4
5′ 6′
65
O2N
O2N
2,4′-二硝基联苯
多环芳烃化合物PPT演示文稿

contamination and prevention of ploycyclic aromatic hydrocarbons (PAH) in food
1
多环芳烃化合物
1. 分类: 一类:苯环与苯环之间各由一个碳原子
相连,如联苯。
另一类:相邻的苯环至少有两个共用的 碳原子的碳氢化合物,如萘,苯并(a) 芘,也称为稠环芳烃。
0.03—0.9
煤
0.09—0.19
电
0.06—0.072
香肠
煤电热空气 0.66-1.08
煤直接烘
0.42—0.74
电直接烘
0.32—0.38
13
不同加工方法肉制品B(a)P 含量
种类
B(a)P 含量(μg/Kg )
一般烤肉或烤香肠 0.11——0.63
碳火烤肉 冰岛家庭熏肉
2.6 ——11.2 23
范围(μg/Kg ) 平均值
0—16.6
2.56
0—12.7
2.43
0—10.0
2.69
1.9—47.5
14.0
1.3—15.2
6.09
0.5—3.5
1.35
3.0—7.0
4.38
1.4—11.0
3.18
12
不同热源熏制烤肉制品B(a)P 含量(μg/Kg)
制品
热源(燃料) B(a)P 含量
烤猪
茅草
18
苯并(a)芘
3. 预防措施
(1) 防止污染
A 加强环境治理,减少环境污染。 B 改进食品加工方式 C 粮食、油料种子不在柏油马路上晾晒 D 机械化生产食品要防止润滑油污染食
有机化学课件--第五章芳烃

NO2
N O 2 95oC
+H N O 3( 发 烟 ) + H 2S4 O ( 浓 )
NO2 NO2
+
NO2
NO2
+
NO2
NO2
6%
93%
1%
2019/10/30
课件
32
C H 3
+H N O 3( 浓 )+H 2S4 O ( 浓 )
1
: 1.5
30oC
CH3 NO2
+
58%
CH3
CH3
+
NO2
2019/10/30
课件
9
2. 分子轨道理论
E
2019/10/30
课件
反键轨道
成键轨道
10
3. 共振论
Ⅰ
Ⅱ
贡献大
键长,键角完全 相等的等价结构
Ⅲ
Ⅳ
Ⅴ
贡献小
键长、键角不等 的不等价结构
2019/10/30
课件
11
(二)苯衍生物的同分异构、 命名和物理性质
苯(Benzene) 苯基(phenyl) 苄基(benzyl) (phenyl methyl)
Br
NH2
3-氨基-5-溴苯酚
2019/10/30
课件
14
芳香化合物命名中保留的母体及其名称
CH3
甲苯 Toulene
苯乙烯 Styrene
例如:
CH3
3-乙基甲苯(3-ethyltoulene)
不叫做3-甲基乙苯
C H 2C H 3
2019/10/30
课件
15
物理性质
芳香烃不溶于水,但溶于有机溶剂。 一般芳香烃均比水轻。沸点随相对分子质 量升高而升高。熔点除与相对分子质量有 关外,还与结构有关,通常对位异构体由 于分子对称,熔点较高。
简介多环芳烃ppt课件

3. 多环芳烃的来源
多环芳烃的来源可分为天然源与人为源两 种, 后者是多环芳烃污染的主要来源 。
• 天然源主要是火山爆发、森林火灾和生物合 成等自然因素所形成的污染。
• 人为源包括各种矿物燃料(如煤、石油、天 然气等)、木材、纸以及其他含碳氢化合物 的不完全燃烧或在还原状态下热解而形成的 有毒物质污染。
“雪亮工程"是以区(县)、乡(镇) 、村( 社区) 三级综 治中心 为指挥 平台、 以综治 信息化 为支撑 、以网 格化管 理为基 础、以 公共安 全视频 监控联 网应用 为重点 的“群 众性治 安防控 工程” 。
1. 什么是多环芳烃?
多环芳烃 ( Polycyclic Aromatic Hydrocarbons,PAHs)是指两个以 上苯环以稠环形式相连的化合 物,是目前环境中普遍存在的污 染物质。其中结构最简单的萘 就是我们日常生活中用来防蛀 虫的樟脑丸的主要成分,而在 多数情况下更复杂的多环芳烃 如芘、苯并芘等却是一种致癌 物质,在厨房油烟、有机燃料 燃烧或抽烟时产生的烟雾和烟 尘中就存在这种物质。此类化 合物对生物及人类的毒害主要 是参与机体的代谢作用,具有致 癌、致畸、致突变和生物难降 解的特性。
“雪亮工程"是以区(县)、乡(镇) 、村( 社区) 三级综 治中心 为指挥 平台、 以综治 信息化 为支撑 、以网 格化管 理为基 础、以 公共安 全视频 监控联 网应用 为重点 的“群 众性治 安防控 工程” 。
主要体现在以下几个方面:
污染范围
生活
大气、乡(镇) 、村( 社区) 三级综 治中心 为指挥 平台、 以综治 信息化 为支撑 、以网 格化管 理为基 础、以 公共安 全视频 监控联 网应用 为重点 的“群 众性治 安防控 工程” 。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
§7.1.1 命名
a.联苯及衍生物
3 2 2' 3'
3 2 2' 3' 2" 3"
4
1 1'
4' 4
1 1'
4' 1"
4"
5 6 6' 5'
联苯
5 6 6' 5' 6" 5"
对联三苯
Cl Cl
32
2' 3'
4
1 1'
4'
5 6 6' 5'
3 2 NO2 2' 3'
4
1 1'
4' NO2
5 6 6' 5'
与苯环不同处:键长不均等 (但与普通的单双键不同)
§7.3 稠环芳烃 §7.3.1 萘、蒽的结构
b. 蒽的结构
表达式
sp2杂化, 平面结构, 键长不均等(与普通的单双键不同)
§7.3 稠环芳烃 §7.3.2 萘、蒽的化学性质
具有芳香性,易发生亲电取代, 但比苯易发生氧化及加成反应。
a. 萘的化学性质 1. 亲电取代反应
萘
稠环共用原子不编号,与螺环化合物区别(螺碳编号)。
蒽
菲
8 7
6 5
1 2 3
4
1,4,5,8 称为位 2,3,6,7 称为位
SO3H
- 萘磺酸
8 91
7
2
6
3
5 10 4
1,4,5,8 称为位 2,3,6,7 称为位 9,10称为γ位
6 54 3
7
2
8
1
9 10
有五种不同的位置
1, 8;2, 7;3, 6;
内容回顾
§6.6 苯环上亲电取代反应的定位规律
苯环上取代基对亲电取代反应的影响 取代基对反应活性的影响及定位作用的理论解释 双取代基的定位作用,位阻对定位的影响 取代基的定位作用在合成中的应用
第七章 多环芳烃和非苯芳烃
§7.1 多环芳烃的分类与命名 §7.2 联苯及其衍生物 §7.3 稠环芳烃:萘、蒽 §7.4 非苯芳烃(休克尔规则)
萘的亲电取代反应活性大于苯,-位比-位更易发生亲电取代反应。
共振论的解释
EH
HE
+
+
两个共振式都有完整的苯环
+E
E
H
H +
只有一个共振式有完整的苯环
a. 萘的化学性质 1. 亲电取代反应
a. 卤代 -卤代为主
b. 硝化 -硝化为主
萘比苯环上容易发生取代反应
Br
+ Br2 CCl4
+ HBr
72~75%
O2N
HNO3 H2SO4
O2N O2N
NO2
主
次
还
NO2
原
2
NO2 Zn+ NaOH
NN HH
HCl H2N
NH2
氢化偶氮苯
联苯胺重排
§7.3 稠环芳烃
§7.3.1 萘、蒽的结构 §7.3.2 萘、蒽的化学性质
§7.3 稠环芳烃 §7.3.1 萘、蒽的结构
a. 萘的结构
表达式
sp2杂化, 平面结构,
2,2’-二氯联苯 2,4’-二硝基联苯 单键连接的芳香碳原子为1号位
§7.1 多环芳烃的分类与命名 §7.1.1 命名
b.多苯代脂肪烃 多苯代脂肪烃命名时,一般把苯基作为取代基。
CH2
二苯甲烷
CH
三苯甲烷
CH2CH2
1,2-二苯乙烷
§7.1 多环芳烃的分类与命名
§7.1.1 命名 c.稠环芳烃
主产物
OH SO3H
CH3 HNO3 , CH3COOH
50~700C
NO2 CH3 +
10 : 1
CH3 NO2
CH3
H2SO 4
HO3S
CH3
80%
a. 萘的化学性质 2. 氧化反应 萘比苯容易氧化
O
O O
V2O5 200-500oC
CrO3-HOAc 10-15oC
O
CH3
CrO3-HOAc 25oC
+ HNO3 H2SO4
NH2 Zn
HCl
NO2 + H2O
79%
a. 萘的化学性质
由于热力学与动力学上的不同导致产物不同的例子: 1、共轭二烯烃与氯化氢的加成反应—是1,2还是1,4加成 2、甲苯的磺化反应 动力学在邻位,热力学在对位。 3、萘的磺化反应。
1. 亲电取代反应
SO3H
c. 磺化
40-80oC + H2SO4
§7.2.1 衍生物的立体异构
NO2 O2N
HOOC COOH
NO2 O2N COOH
HOOC
含手性轴化合物R、S构型的确定方法:
将化合物竖放,下方的两个基团中较小的基团放在视线远方,这时上面的两个基团呈现 水平,如果按基团优先顺序从较大基团指向较小基团,如箭头从左到右,则为R构型,
如是从右到左,则为S构型。
a. 萘的化学性质 1. 亲电取代反应 d. 萘环上取代基的定位规律
G(o,p) 次
活化基团: 同环取代 原取代基在位,则在同环另一位取代;
主 原取代基在位,则在同环相邻位。
G(o,p)
主
主 G(m)
次
主
钝化基团:异环取代,且发生在异环的位
G(m)
主
主
萘环取代反应实例
OH
H2SO 4
OH +
SO3H
§7.2.2 制备
a. 工业
2
700~800℃/铁管
H
b. 实验室 (乌尔曼反应) 2
I + 2Cu
+ H2 + 2CuI
§7.2 联苯及其衍生物苯环上已有基团若为钝化基团,第二个取代基进入 异环的对位;若已有基团为活化基团则进入同环邻位。
§7.2.3 化学性质
取代基主要进入苯基的对位
HNO3 H2SO4
△
某磺酸的水解性能
1、烷基硫酸在酸性条件下,发生磺酸基的离去得到醇。P53,烯烃的加成 2、苯磺酸的水解反应 a、在酸性条件下(如稀硫酸作用下)磺酸基与质子交换,重新变为苯环。 b、在碱性条件下(如氢氧化钠)得到苯酚钠,进一步酸解得到苯酚。 3、萘磺酸碱性条件下(如氢氧化钠)得到萘酚钠,进一步酸解得到萘酚。
下次课:杂环化合物
§7.1 多环芳烃的分类与命名 §7.1.1 分类
(1) 联苯和联多苯类 苯环通过单键相连
(2) 多苯代脂肪烃类
CH2CH2
CH2
苯环通过脂肪烃基相连
(3) 稠环芳烃 苯环通过共用两个相临碳原子相连
8 7
6 5
8 91
7
2
6
3
5 10 4
1 2 3
4
6 54 3
7
2
8
1
9 10
§7.1 多环芳烃的分类与命名
160oC
96%
-磺化为主
160oC H2SO4
SO3H
85%
-磺化为主
位阻大 动力学控制产物
位阻小 热力学控制产物
a. 萘的化学性质
1. 亲电取代反应 c. 磺化 萘磺化的应用:-萘酚、萘胺的制备
SO3H
NaOH
H+
OH
3000C
OH (NH4)2SO3 ,PNΒιβλιοθήκη 2NH2 NaHSO3/H2O
OH
4, 5;9,10。
含有多个取代基的稠环芳烃,
OH
命名按阿拉伯数字编号来。
- 萘酚
§7.2 联苯及其衍生物
§7.2.1 衍生物的立体异构 §7.2.2 联苯的制备 §7.2.3 化学性质
联接两个苯环的碳原子的邻位都有取代基时,因为
位阻效应使得δ不能够自由旋转,而出现立体异构 §7.2 联苯及其衍生物
