纯化水检验原始记录(2020版药典)
中国药典2020版二部纯化水微生物检查

中国药典2020版二部纯化水微生物检查我国药典2020版二部纯化水微生物检查一、前言我国药典2020版二部纯化水微生物检查是当前药品行业中的重要标准之一。
纯化水作为制药过程中不可或缺的重要原料,其微生物检查的质量标准直接关系到药品的安全性和有效性。
本文将围绕我国药典2020版二部纯化水微生物检查这一主题展开讨论,通过全面评估和深入分析,帮助读者对该标准有更深入的理解。
二、我国药典2020版二部纯化水微生物检查的内容概述1. 我国药典2020版中纯化水微生物检查的重要性在药品制造中,纯化水被广泛应用于药品配制、清洁消毒等生产工艺中。
然而,在疫苗、注射剂、眼用制剂等高风险药品中使用的水质则对微生物污染的敏感度要求更高。
我国药典2020版二部纯化水微生物检查作为衡量纯化水质量的重要标准,对保障药品生产过程和药品质量安全具有重要意义。
2. 我国药典2020版中纯化水微生物检查的具体内容我国药典2020版二部中对纯化水微生物检查的内容主要包括微生物总数检查、大肠菌群检查和致病菌检查。
这些检查项目的严格执行,能够有效地保障纯化水的微生物污染水平处于合理的范围内,符合药品生产的要求。
三、对我国药典2020版二部纯化水微生物检查的深入分析1. 微生物总数检查微生物总数检查是评价水质中微生物总体污染水平的重要指标。
根据我国药典2020版二部的相关规定,微生物总数检查采用膜过滤法,通过将一定容积的水样过滤到膜上,再将膜培养于富含营养物质的培养基中,最终统计出微生物菌落总数。
这一检查项目的严谨性和科学性直接关系到纯化水的微生物质量。
2. 大肠菌群检查大肠菌群检查是评价水质中是否存在粪肠道致病菌的关键指标之一。
我国药典2020版二部中对大肠菌群检查的相关要求十分严格,如规定了检测方法、培养基的配制等方面的内容。
这一检查项目的合格与否,直接影响着纯化水的可靠性和安全性。
3. 致病菌检查致病菌检查是对纯化水中致病菌的检测和评价。
纯化水验证检验原始记录
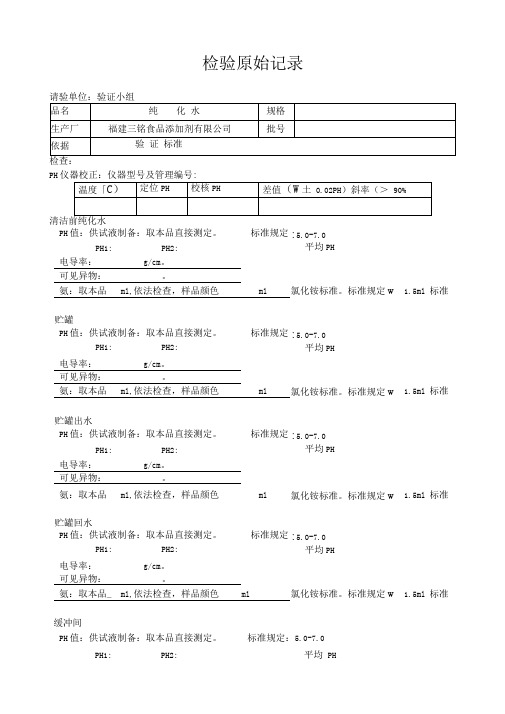
检验原始记录
检查:
PH
清洁前纯化水
PH值:供试液制备:取本品直接测定。
标准规定:5.0-7.0
PH1: PH2: 平均PH
电导率:g/cm。
可见异物:。
氨:取本品ml,依法检查,样品颜色ml 氯化铵标准。
标准规定w 1.5ml 标准
贮罐
PH值:供试液制备:取本品直接测定。
标准规定:5.0-7.0
PH1: PH2: 平均PH
电导率:g/cm。
可见异物:。
氨:取本品ml,依法检查,样品颜色ml 氯化铵标准。
标准规定w 1.5ml 标准
贮罐出水
PH值:供试液制备:取本品直接测定。
标准规定:5.0-7.0
PH1: PH2: 平均PH
电导率:g/cm。
可见异物:。
氨:取本品ml,依法检查,样品颜色ml 氯化铵标准。
标准规定w 1.5ml 标准
贮罐回水
PH值:供试液制备:取本品直接测定。
标准规定:5.0-7.0
PH1: PH2: 平均PH
电导率:g/cm。
可见异物:。
氨:取本品_ml,依法检查,样品颜色ml 氯化铵标准。
标准规定w 1.5ml 标准
缓冲间
PH值:供试液制备:取本品直接测定。
标准规定:5.0-7.0
PH1: PH2: 平均PH
结论:该样品_______ 标准。
检验:核对:年月日请验
年月日出报。
纯化水理化检测原始记录表
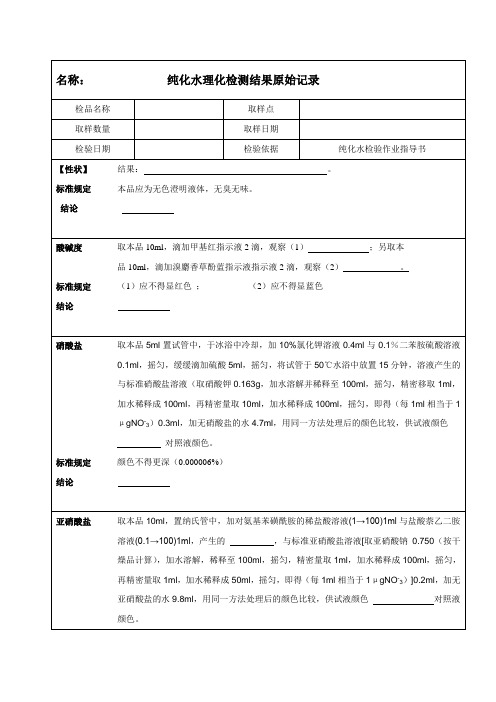
硝酸盐取本品5ml置试管中,于冰浴中冷却,加10%氯化钾溶液0.4ml与0.1%二苯胺硫酸溶液0.1ml,摇匀,缓缓滴加硫酸5ml,摇匀,将试管于50℃水浴中放置15分钟,溶液产生的与标准硝酸盐溶液(取硝酸钾0.163g,加水溶解并稀释至100ml,摇匀,精密移取1ml,加水稀释成100ml,再精密量取10ml,加水稀释成100ml,摇匀,即得(每1ml相当于1μgNO-3)0.3ml,加无硝酸盐的水4.7ml,用同一方法处理后的颜色比较,供试液颜色
标准规定颜色不得更深(0.000002%)
结论
电导率使用在线或离线电导率仪完成。电导率µS/cm。
标准规定不超过4.3µS/cm
结论
氨取本品50ml,加碱性碘化汞钾试液2ml,放置15分钟;如显色,与氯化铵溶液1.5ml,加无氨水48ml与碱性碘化汞钾试液2ml制成对照液比较,供试液颜色对照液颜色。
名称:纯化水理化检测结果原始记录
检品名称
取样点
取样数量
取样日期
检验日期
检验依据
纯化水检验作业指导书
【性状】结果:。
标准规定本品应为无色澄明液体,无臭无味。
结论
酸碱度取本品10ml,滴加甲基红指示液2滴,观察(1);另取本
品10பைடு நூலகம்l,滴加溴麝香草酚蓝指示液指示液2滴,观察(2)。
标准规定(1)应不得显红色;(2)应不得显蓝色
标准规定颜色不得更深(0.00001%)
结论
记录人:审核人:
日期:日期:
对照液颜色。
标准规定颜色不得更深(0.000006%)
结论
亚硝酸盐取本品10ml,置纳氏管中,加对氨基苯磺酰胺的稀盐酸溶液(1→100)1ml与盐酸萘乙二胺溶液(0.1→100)1ml,产生的,与标准亚硝酸盐溶液[取亚硝酸钠0.750(按干燥品计算),加水溶解,稀释至100ml,摇匀,精密量取1ml,加水稀释成100ml,摇匀,再精密量取1ml,加水稀释成50ml,摇匀,即得(每1ml相当于1μgNO-3)]0.2ml,加无亚硝酸盐的水9.8ml,用同一方法处理后的颜色比较,供试液颜色对照液颜色。
中国药典2020版二部纯化水微生物检查

中国药典2020版二部纯化水微生物检查(原创版)目录1.中国药典 2020 版二部纯化水微生物检查的概述2.微生物检查的方法和标准3.微生物检查的重要性和应用正文1.中国药典 2020 版二部纯化水微生物检查的概述中国药典是我国药品和医疗器械行业最为重要的法规之一,其中包含了各种药品的质量标准和检测方法。
在 2020 版的中国药典二部中,纯化水的微生物检查是一项重要的内容。
纯化水是制药过程中最为常见的一种溶剂,它的质量直接关系到药品的质量和安全性。
因此,对纯化水进行微生物检查是十分必要的。
2.微生物检查的方法和标准微生物检查的方法主要包括细菌总数检查、霉菌和酵母菌检查、细菌内毒素检查等。
其中,细菌总数检查是微生物检查中最为常见的一种方法。
这种方法主要是通过在纯化水中加入一定量的营养琼脂,然后在一定温度下培养一定时间,最后通过计数平板上的菌落数量来确定细菌总数。
霉菌和酵母菌检查则是通过在纯化水中加入一定量的霉菌和酵母菌培养基,然后在一定温度下培养一定时间,最后通过计数培养基上的菌落数量来确定霉菌和酵母菌总数。
细菌内毒素检查则是通过检测纯化水中的内毒素含量来判断微生物污染的程度。
这些检查方法都有相应的标准,比如细菌总数的标准一般不应超过100CFU/ml,霉菌和酵母菌总数的标准一般不应超过 10CFU/ml。
3.微生物检查的重要性和应用微生物检查的重要性不言而喻,它直接关系到药品的质量和安全性。
如果纯化水中的微生物污染严重,那么药品中就有可能出现微生物污染,这对于患者的健康会造成严重的威胁。
微生物检查的应用也十分广泛,它不仅应用于药品的制备过程中,还应用于医疗器械的清洗和消毒过程中,甚至应用于医院的感染防控中。
纯化水检验原始记录(2020版药典)

纯化水检验原始记录(2020版药典) XXXXXXXXXXXX检验原始记录记录编号:检验日期:年月日;检品名称:车间:取样点:纯化水报告日期:全检检品编号:取样日期:检验依据:《中国药典》2020年版二部检验项目:性状】:本品为,无臭。
标准规定:本品为无色的澄清液体,无臭。
)检查】检查方法:取本品10ml,加甲基红指示液2滴,(标准规定:不得显红色)另取本品10ml,加溴麝香草酚蓝指示液5滴,(标准规定:不得显蓝色)硝酸盐检查方法:取本品5ml置试管中,于水浴中冷却,加10%氯化钾溶液0.4ml与0.1%二苯胺硫酸溶液0.1ml,摇匀,缓缓滴加硫酸5ml,摇匀,将试管于50℃水浴中放置15分钟,溶液产生的蓝色与标准硝酸盐溶液液[取硝酸钾0.163g,加水溶解并稀释至100ml,摇匀,精密量取lml,加水稀释成100ml,再精密量取10ml,加水稀释成100ml,摇匀,即得(每1ml相当于1μgNO3)]0.3ml,加无硝酸盐的水 4.7ml,用同一方法处理后的颜色比较,供试品溶液。
(标准规定:不得更深0.%)亚硝酸盐搜检办法:取本品10ml,置纳氏管中,加对氨基苯磺酰胺的稀盐酸溶液﹙1→100﹚1ml与盐酸萘乙二胺溶液﹙0.1→100﹚1ml,产生的粉红色,与标准亚硝酸盐溶液[取亚硝酸钠0.750g(按枯燥品计算),加水溶解,稀释至100ml,摇匀,邃密精美量取lml,加水稀释成100ml,摇匀,再邃密精美量取lml,加水稀释成50ml,摇勻,即得(每1ml相当于1μgNO2)]0.2ml,加无硝酸盐的水9.8ml,用同一办法处理后的颜色比较,供试品溶液。
标准划定:不得更深0.%)氨搜检办法:取本品50ml,加碱性碘化汞钾试液2ml,安排15分钟,溶液;如显色,供试品颜色比比较液氯化铵溶液。
(标准划定:如显色与比较液氯化铵溶液﹙取氯化铵31.5mg,加无氨水适量使溶解并稀释成1000ml﹚1.5ml,加无氨水48ml 与碱性碘化汞钾试液2ml制成的比较液比较,不得更深0.%)XXXXXXXXXXXX检验原始记录记实编号:电导率检查方法:取本品照制药用水电导率测定法标准操作规程25℃测得电导率为μS/cm。
纯化水检验原始记录
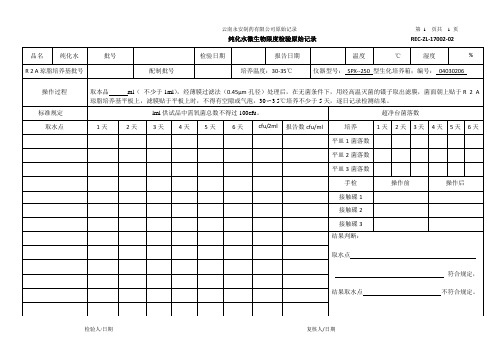
云南永安制药有限公司原始记录第1 页共 1 页
纯化水微生物限度检验原始记录REC-ZL-17002-02
品名纯化水批号检验日期报告日期温度℃湿度% R 2 A琼脂培养基批号配制批号培养温度:30-35℃仪器型号:SPX--250 型生化培养箱;编号:04030206
操作过程取本品ml(不少于1ml),经薄膜过滤法(0.45μm孔径)处理后,在无菌条件下,用经高温灭菌的镊子取出滤膜,菌面朝上贴于R 2 A 琼脂培养基平板上,滤膜贴于平板上时,不得有空隙或气泡,30〜3 5℃培养不少于5天,逐日记录检测结果。
标准规定lml供试品中需氧菌总数不得过100cfu。
超净台菌落数取水点1天2天3天4天5天6天cfu/2ml 报告数cfu/ml 培养1天2天3天4天5天6天
平皿1菌落数
平皿2菌落数
平皿3菌落数
手检操作前操作后
接触碟1
接触碟2
接触碟3
结果判断:
取水点
符合规定,
结果取水点不符合规定。
检验人/日期复核人/日期。
(完整版)纯化水原始记录

纯化水(全检)取水点:批号:共页第1页【性状】实验室环境:温度;湿度。
本品为(标准:无色澄清)液体;(标准:无臭),(标准:无味)。
本项结论规定检验者日期. 【检查】实验室环境:温度;湿度。
酸碱度取本品(标准:10ml),加甲基红指示液(标准:2滴)(标准:不得显红色);另取(标准:10ml),加溴麝香草酚蓝指示液(标准:5滴)(标准:不得显蓝色)。
本项结论规定检验者日期. 硝酸盐实验室环境:温度;湿度。
取本品(标准:5m1)置试管中,于冷浴中冷却,加10%氯化钾溶液(标准:0.4ml)与0.1%二苯胺硫酸溶液(标准:0.1ml),摇匀,缓缓滴加(标准:硫酸5ml),将试管于(标准:50℃)水浴中放置(标准:l5分钟),溶液产生的(标准:蓝色)与标准硝酸盐溶液[取硝酸钾0.163g,加水溶解并稀释至100ml,摇匀,精密量取1ml,加水稀释成100ml,再精密量取10ml,加水稀释成100ml,摇匀,即得(每1ml相当于1μg NO3)]0.3ml,加无硝酸盐的水(标准:4.7ml),同一方法处理后的颜色比较(标准:不得更深)(0.000006%)。
本项结论规定检验者日期. 亚硝酸盐实验室环境:温度;湿度。
取本品(标准:l0ml),置比色管中,加对氨基苯磺酰胺的稀盐酸溶液(1→100)(标准:1ml)与盐酸萘乙二胺溶液(0.1→100)(标准:1ml),产生的(标准:粉红色)与标准亚硝酸盐溶液[取亚硝酸钠0.750g(按干燥品计算),加水溶解,稀释至100ml,摇匀,精密量取1ml,加水稀释成100ml,摇匀,再精密量取1ml,加水稀释成50ml,摇匀,即得(每1ml相当于1μg NO2)]0.2ml,加无亚硝酸盐的水(标准:9.8ml),用同一方法处理后的颜色比较(标准:不得更深)(0.000002%)。
本项结论规定检验者日期. 氨实验室环境:温度;湿度。
纯化水(全检)取水点:批号:共页第2页取本品(标准:50ml),加碱性碘化汞钾试液(标准:2ml),放置(标准:15分钟),溶液(标准:不显色);如显色,与氯化铵溶液(取氯化铵31.5mg,加无氨水适量使溶解并稀释成1000ml)1.5ml,加无氨水(标准:48ml)与碱性碘化汞钾试液(标准:2ml)制成的对照液比较(标准:不得更深)(0.00003%)。
纯化水检测记录

加溴麝香草酚蓝指示液 5 滴,不得显蓝色,测得结果为:□显蓝色□未显蓝色。
mL (10mL),
【电导率】取两份 30mL 待测水样于 50mL 小烧杯中,将电导电极置于其中搅动,待数值稳定后(即 25℃时),读取电导率测试值不得
超过 5.1μs/cm,测得结果分别为: 1)
μs/c录
QC-JL-030-00
取样点
仪器设备 仪器编号 校验有效期至
取样日期
电子天平
电热恒温培养 箱(细菌)
检测依据
鼓风干燥箱
恒温水浴锅
【性状】待测水样目测为
(无色澄明液体),嗅为
电导率仪
检测频次 1 次/周 电热恒温培养箱 (霉菌)
(无臭、无味)。
【酸碱度】取待测水样
mL(10mL),加甲基红指示液 2 滴,不得显红色,测得结果为:□显红色□未显红色;另取
【微生物限度】取待测水样 1)
mL 2)
中需氧菌总数不得过 100cfu,实测结果为:1)
mL(1mL),分别采用薄膜过滤法处理后,经 30~35℃培养 5 天,1mL 纯化水
cfu/mL; 2)
cfu/mL。
检测结论:
备注: 编号
检验人/日期:
复核人/日期:
纯化水检验记录

取样日期:________________ 检验日期:_________________ 1样品信息2纯化水性状检验2.1可接受标准:本品应为无色澄明液体;无臭。
2.2检验结果注:检查结果表中“+”为合格;“-”为不合格。
如有不合格项在“不合格项”框内填写不合格具体内容,如无不合格项在框内“/”表示。
检验人/日期复核人/日期3酸碱度检验3.1物料与设备3.1.1试液3.2实验操作过程:取本品 ml,加甲基红指示液2滴;另取 ml,加溴麝香草酚蓝指示液5滴。
3.3实验结果3.3.1可接受标准:样品加甲基红指示液后不得显红色,加溴麝香草酚蓝指示液后不得显蓝色。
3.3.2实验结果:检验人/日期复核人/日期4硝酸盐检验4.1物料与设备管:25ml/管、50ml/管、制冰机4.2实验操作过程:4.2.1标准硝酸盐工作溶液配制:量取水中NO3-离子溶液标准物质(100µg/ml)100µl,置10ml量瓶中,加水稀释至刻度,摇匀,即得(每1ml相当于1µg的NO3)。
本溶液仅供当日使用。
4.2.2取本品ml置纳氏比色管中,于冰浴中冷却,加10%氯化钾溶液____ml与0.1%二苯胺硫酸溶液____ml,摇匀,缓缓滴加硫酸____ml,摇匀,将纳氏比色管于50±1℃水浴放置15分钟,放入电热恒温水浴锅时显示温度: ℃,时间: ,取出时显示温度: ℃,时间: ,样品组溶液若发生变色。
与标准硝酸盐溶液____ml,加无硝酸盐的水____ml,用同一方法处理后的对照管比较。
4.3实验结果4.3.1接受标准:样品管不得比对照管颜色更深(0.000006%)日期日期5亚硝酸盐检测5.1物料与设备5.1.1试液瓶5.2实验操作过程:5.2.1标准亚硝酸盐工作溶液配制:精密量取标准亚硝酸盐溶液1ml,加水稀释成100ml,摇匀,再精密量取1ml,加水稀释成50ml,摇匀,即得。
5.2.2取本品ml置比色管中,加对氨基苯磺酰胺的稀盐酸溶液(1→100)_____ml及盐酸萘乙二胺溶液(0.1→100)_____ml,产生的粉红色,与标准亚硝酸盐溶液_____ml,加无氨水_____ml,用同一方法处理后的颜色比较。
中国药典2020版二部纯化水微生物检查

中国药典2020版二部纯化水微生物检查
摘要:
一、前言
二、中国药典2020 版二部纯化水微生物检查的标准
三、检查方法与步骤
四、结果判断与处理
五、总结
正文:
一、前言
中国药典2020 版二部纯化水微生物检查是药品生产过程中重要的质量控制环节,对于保证药品的安全性和有效性具有重要意义。
本文将对中国药典2020 版二部纯化水微生物检查的相关内容进行详细阐述。
二、中国药典2020 版二部纯化水微生物检查的标准
根据中国药典2020 版二部,纯化水微生物检查主要包括细菌总数、霉菌总数、酵母菌总数和大肠埃希氏菌等指标。
检查要求在药品生产过程中使用的纯化水应符合一定的微生物学标准,以确保药品生产过程不受污染。
三、检查方法与步骤
1.取样:从药品生产过程中使用的纯化水中取样。
2.增菌:将样品接种到适当的培养基中,进行增菌培养。
3.分离:将增菌后的菌落进行分离,以便进行进一步的鉴定。
4.鉴定:对分离后的菌落进行形态学观察和生化试验,以鉴定菌种。
5.计数:对鉴定后的菌落进行计数,以得出各种微生物的数量。
四、结果判断与处理
1.如果检查结果不符合标准要求,应查找原因并采取相应的措施,如更换纯化水来源或改进生产工艺等。
2.对于超标的情况,应严格按照相关规定进行处理,如报废不合格产品或进行重新检测等。
五、总结
中国药典2020 版二部纯化水微生物检查是药品生产过程中的关键环节,对于保证药品的质量和安全具有重要意义。
(完整版)纯化水全性能检测报告及原始记录

性状
无色澄明液体,无臭,无味
合格
合格
电导率
≤2µs/cm
合格
合格
酸碱度
纯化水
加甲基红不得显红色,加溴麝香草酚兰不得显蓝色
合格
——
注射用水
pH值应为5.0~7.0
——
合格
氯化物
硫酸盐
钙盐
不得发生浑浊
合格
合格
硝酸盐
颜色不得更深
合格
合格
亚硝酸盐
颜色不得更深
合格
合格
氨
如显色,显色不得超过对照液
1.00µs/cm
酸碱度
纯化水
加甲基红不得显红色,加溴麝香草酚兰不得显蓝色
取本品10ml,加甲基红指示液2滴,不得显红色;另取10ml,加溴麝香草酚兰指示液5滴,不得显蓝色
符合规定
注射用水
pH值应为5.0~7.0
取本品40ml,用酸度计测PH值
——
氯化物
硫酸盐
钙盐
不得发生浑浊
取3只试管分别加入50ml本品,第一管加硝酸5滴与硝酸银试液1ml,第二管加氯化钡试液2ml,第三管加草酸铵试液2ml
未超过标准液
亚硝酸盐
颜色不得更深
取本品10ml,置纳氏管中,加对氨基苯磺酰胺的稀盐酸溶液1ml及盐酸萘乙二胺溶液1ml,产生的粉红色,与标准亚硝酸盐溶液0.2ml,加无硝酸盐的水9.8ml,用同一方法处理的颜色比较
未超过标准液
氨
如显色,显色不得超过对照液
取本品50ml,加碱性碘化汞钾试液2ml,放置15min,如显色,与氯化铵溶液1.5ml(注射用水则取1.0ml),加无氨水48ml与碱性碘化汞钾试液2ml制成的对照液比较
中国药典2020版二部纯化水微生物检查

中国药典2020版二部纯化水微生物检查【原创实用版】目录1.概述2.中国药典 2020 版二部纯化水微生物检查的标准3.微生物检查的方法4.微生物检查的注意事项5.结论正文1.概述纯化水是制药工业中常用的一种水质,其微生物质量对于药品的质量和安全性至关重要。
为了保证纯化水的微生物质量,我国制定了一系列的标准和方法。
本文将介绍中国药典 2020 版二部纯化水微生物检查的相关内容。
2.中国药典 2020 版二部纯化水微生物检查的标准中国药典 2020 版二部对于纯化水的微生物检查有严格的标准。
其中,纯化水的微生物限度要求如下:- 细菌总数:≤10cfu/ml- 霉菌和酵母菌:≤1cfu/ml- 细菌内毒素:≤0.25EU/ml3.微生物检查的方法微生物检查通常包括以下几个步骤:- 采样:在纯化水的生产过程中随机采样,保证样品具有代表性。
- 培养:将样品在适当的培养基中进行培养,以便微生物生长和繁殖。
- 计数:在适当的时间点对培养基中的微生物进行计数,以了解样品中微生物的数量。
- 鉴定:通过显微镜观察和生化试验等方法,对微生物进行鉴定,以确定其种类。
4.微生物检查的注意事项在进行纯化水微生物检查时,应注意以下几点:- 采样时应保证样品的无菌性,避免样品被污染。
- 选择适当的培养基和培养条件,以保证微生物的生长和繁殖。
- 在进行微生物计数时,要保证计数方法的准确性和精度。
- 定期对纯化水微生物检查的设备和方法进行验证,以确保检查结果的可靠性。
5.结论通过对中国药典 2020 版二部纯化水微生物检查的研究,我们可以了解到,我国对于纯化水的微生物质量有着严格的要求。
微生物检查的方法和注意事项也需要我们在实际操作中严格遵守,以保证药品的质量和安全性。
纯化水检验记录
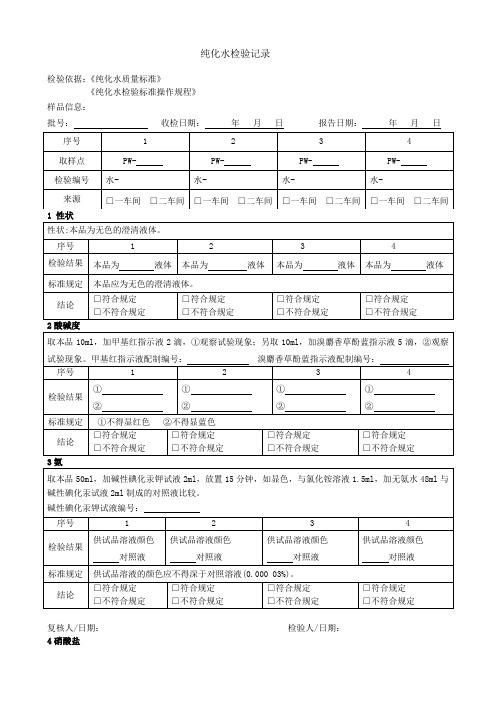
培养箱型号及编号:
、
培养基配制批号: 培养时间:5 天
序号
1天
2天
3天
4天
5天
1
计数结果
2
( cfu/ml)
3
4
阴性对照
观察人/日期 序
需氧菌总数 号
结论
1
cfu/ml 本品按照《中国药典》2015 版二部检验上述项目,结果 □符合规定 □不符合规定
2
cfu/ml 本品按照《中国药典》2015 版二部检验上述项目,结果 □符合规定 □不符合规定
□符合规定
□符合规定
□不符合规定
□不符合规定
□符合规定 □不符合规定
□符合规定 □不符合规定
复核人/日期: 8 不挥发物
检验人/日期:
—
2
精选文档
取本品 100ml,置 105℃恒重的蒸发皿中,在水浴上蒸干,并在 105℃干燥至恒重,计算遗留残渣量。
电子天平型号及编号□:
、
其他:□
干燥箱型号及编号□:
序号
1
2
3
4
供试品溶液颜色
检验结果
于对照液
供试品溶液颜色 于对照液
供试品溶液颜色 于对照液
供试品溶液颜色 于对照液
标准规定 结论
6 电导率
供试品溶液的颜色应不得深于对照溶液 (0.000 002%)。
□符合规定 □不符合规定
□符合规定 □不符合规定
□符合规定 □不符合规定
□符合规定 □不符合规定
照《中国药典》2015 年版四部(通则 0681)测定。
□符合规定 □不符合规定
复核人/日期: 4 硝酸盐
检验人/日期:
精选文档
中国药典2020版二部纯化水微生物检查

我国药典2020版二部纯化水微生物检查我国药典2020版二部是我国药典发布的最新版本,其中包含了对纯化水微生物检查的相关规定和检测方法。
本文将从深度和广度两方面来全面评估我国药典2020版二部对纯化水微生物检查的内容,并探讨其在药品生产和质量控制中的重要性。
1. 纯化水微生物检查的重要性纯化水是药品生产中不可或缺的重要物质,它广泛应用于药品的生产、清洗、冲洗及设备、容器和容器弥补之用。
然而,纯化水中的微生物污染可能会对药品的质量和安全造成严重影响,因此对纯化水中微生物的检查成为药品生产过程中至关重要的一环。
2. 我国药典2020版二部对纯化水微生物检查的规定我国药典2020版二部对纯化水微生物检查的规定主要包括了微生物总数的检查方法、大肠菌裙的检查方法和其他微生物的检查方法。
其中针对微生物总数的检查方法包括了膜过滤法和涂布计数法,大肠菌裙的检查方法采用MPN法和膜过滤法,其他微生物的检查方法则包括了酵母菌和霉菌的检查方法等。
这些规定的制定和执行,有助于保障纯化水的微生物质量,保证药品生产过程中的安全性和合规性。
3. 个人观点和理解笔者认为,我国药典2020版二部对纯化水微生物检查的规定和方法的发布,体现了我国药典对于药品质量和安全的高度重视。
在药品生产过程中,严格执行纯化水微生物检查的规定,不仅可以确保药品质量的稳定性和可靠性,也有助于提升我国药品生产的国际竞争力和知名度。
总结我国药典2020版二部对纯化水微生物检查的规定和检测方法的发布,标志着我国在药品质量控制和安全监管方面迈出了重要的一步。
严格按照我国药典的规定执行纯化水微生物检查,不仅是对药品质量的保障,也是对患者安全的保障,对促进整个医药行业的快速健康发展具有重要意义。
通过对我国药典2020版二部对纯化水微生物检查的全面评估和探讨,相信读者对于这一主题已经有了更深入的了解。
在药品生产和质量控制中,无论是制药企业还是监管部门,都应该严格遵循我国药典的规定,确保纯化水的微生物质量,以推动整个医药行业的健康发展。
纯化水检验原始记录

纯化水检验原始记录纯化水是指经过各种净化手段处理后的水,其中去除了大部分或所有悬浮物、有机物、离子和微生物。
在实验室和工业生产中,纯化水经常被用作实验试剂和工业原料。
为了确保纯化水的质量和纯度符合要求,在生产和使用过程中需要对纯化水进行检验。
本次实验将对纯化水的质量进行检验,并记录实验结果。
实验名称:纯化水检验实验目的:1.检验纯化水的质量和纯度是否符合要求;2.验证纯化水的各项指标是否在规定范围内。
实验器材:1.纯化水;2.pH计;3.电导率仪;4.紫外可见分光光度计;5.毛细管;6.干燥皿;7.温度计;8.纸巾;9.手套;10.安全护目镜。
实验步骤:1.戴上手套和安全护目镜,确保实验操作的安全性。
2.取得一瓶纯化水样品。
3.进行外观检查:观察纯化水的颜色、透明度和悬浮物是否存在。
4.进行pH值检测:将pH电极插入纯化水中,待数值稳定后记录pH 值。
5.进行电导率检测:将电导率仪探头插入纯化水中,待数值稳定后记录电导率。
6.进行紫外可见光谱检测:取一定量的纯化水样品,通过纸巾过滤去除悬浮物,倒入紫外可见分光光度计中,扫描波长范围,记录吸光度值。
7.进行溶解氧检测:将毛细管插入纯化水样品中,尽量避免气泡产生,待读数稳定后记录溶解氧值。
8.进行温度检测:使用温度计测量纯化水的温度,记录温度值。
9.进行高纯度指标检测:依照高纯水的要求,检测纯化水的指标是否符合要求,如溶解无机离子、有机物含量等。
10.做好实验记录和整理实验数据。
实验结果:1.外观检查:纯化水呈无色透明,无悬浮物存在。
2.pH值检测:纯化水的pH值为7,符合中性。
3. 电导率检测:纯化水的电导率为0.05 μS/cm,低于规定的标准值。
4.紫外可见光谱检测:纯化水在紫外可见光谱范围内无吸光峰,表明无有机物存在。
5. 溶解氧检测:纯化水的溶解氧为8.0 mg/L,高于规定的标准值。
6.温度检测:纯化水的温度为25°C,符合要求。
纯化水检验原始记录
试样温度:25℃电导率限度值为5.1us.cm-1
电导率:(1)(2)平均
结论
(电导率值应小于限度值)
7.易氧化物取本品100ml,加稀硫酸10ml,煮沸后,加高锰酸钾滴定液(0.02mol/L)0.10ml,再煮沸10分钟,粉红色。
结论
(粉红色应不得完全消失)
2.酸碱度取本品10ml,加甲基红指示液2滴,色。另取10ml,加溴麝香草酚蓝指示液5滴,色。 结论
3.硝酸盐取本品5ml置试管中,于冰浴中冷却,加10%氯化钾溶液0.4ml与0.1%二苯胺硫酸溶液0.1ml,摇匀,缓缓加硫酸5ml,摇匀,将试管于50℃水浴中放置15分钟,溶液产生的蓝色与标准硝酸盐溶液[取硝酸钾0.163g,加水溶解并稀释至100ml,摇匀,精密量取1ml,加水稀释至100ml,再精密量取10ml,加水稀释至100ml,摇匀,即得(每1ml相当于1µgNO3)]0.3ml,加无硝酸盐的水4.7ml,用同一方法处理后的颜色比较,
8.不挥发物取本品100ml置105℃恒重的蒸发皿中,在水浴上蒸干,并在105℃干燥至恒重
实验仪器:天平型号编号温度湿度
烘箱型号编号
空蒸发皿恒重:2hg 1hg 1hg
残渣加蒸发皿恒重:hg 1hg 1hg
计算: 遗留残渣:×103= (mg)
结论(不得过1mg)
9.重金属取本品100ml,加水19ml,蒸发至20ml,放冷,加醋酸盐缓冲液(PH3.5)2ml与水适量成25ml,加硫代乙酰胺试液2ml,摇匀,放置2分钟,与标准铅溶液(浓度为10μg/ml)[精密量取标准铅溶液贮备液(浓度为100μg/ml)10ml加水水稀释成100ml,摇匀,即得]1.0ml,加水19ml用同一方法处理后的颜色比较。
QR824-17纯化水检测记录

纯化水检测记录
取样点: 检验日期:
项目
标准过程
记录
结论
性状
应为无色的澄清液体;无臭,无味
酸碱度
1.取本品10ml,加甲基红指示液2滴,观察颜色;
2.取10ml,加溴麝香草酚蓝指示液5滴,观察颜色。
硝酸盐
取本品5ml置试管中,于冰浴中冷却,加10%氯化钾溶液0.4ml与0.1%二苯胺硫酸溶液0.1ml,摇匀,缓缓滴加硫酸5ml,摇匀,将试管于50℃水浴中放置15分钟,溶液产生的蓝色与标准硝酸盐溶 液0.3ml,加无硝酸盐的水4.7ml,用同一方法处理后的颜色比较。
电导率
取本品100ml,按电导率仪的使用操作规程测定电导率,应附合附录1要求
易氧化物
取本品100ml,加稀硫酸10ml,煮沸后,加高锰酸钾滴定液(0.02mol/L)0.10ml,再煮沸10分钟,粉红色不得完全消失。
不挥发物
取本品100ml,置105℃恒重的蒸发皿中,在水浴上蒸干,并在105℃干燥至恒重,遗留残渣不得过1mg。
总体结论
检验人: 复核:
重金属
取本品100ml,加水19ml,蒸发至20ml,放冷,加醋酸盐缓冲液(pH3.5)2ml与水适量使成25ml,加硫代乙酰胺试液2ml,摇匀,放置2分钟,与标准铅溶液1.0ml加水19ml用同一方法处理后的颜色比较
微生物
取本品,采用薄膜过滤法处理后,按中国药典附录XI J检查,细菌、霉菌和酵母菌总数每1ml不得过,培养时间3天。霉菌和酵母菌总数检查:玫瑰红钠琼脂培养基,培养温度23~28℃,培养时间5天
亚硝酸盐
取本品10ml,置纳氏管中,加对氨基苯磺酰胺的稀盐酸溶液(1→100)1ml及盐酸萘乙二胺溶液(0.1→100)1ml,产生的粉红色,与标准亚硝酸盐溶液0.2ml,加无亚硝酸盐的9.8ml,用同一方法处理后的颜色比较
纯化水检查记录表

氯化物
检测方法:采用滴定法或电 导率仪测量
检测目的:确保纯化水中氯 化物含量符合标准,保障产 品质量和安全性
正常范围:一般应小于 1mg/L
注意事项:检测时应避免污 染,保证仪器的准确性和可
靠性
硫酸盐
检测方法:按照中国药典2020版规定的方法进行检测
正常范围:≤0.015mg/L 异常结果处理:超过正常范围,应重新进行检测,如仍不符合要求,应停止使用该批纯化 水,并追溯调查原因 注意事项:检测时应避免阳光直射,防止空气中二氧化碳对检测结果的影响
培训计划与实施
培训目标:确保相关责任人掌握纯化水检查的技能和知识 培训内容:纯化水检查的标准操作流程、注意事项和安全要求 培训方式:理论授课、实操演练和考核评估相结合 培训周期:每年至少进行一次培训和考核
考核与奖惩机制
考核内容:操作 技能、理论知识、 工作态度等
考核方式:定期 考核、抽查考核、 自查考核等
06
相关责任人及培训 管理
责任人职责与分工
责任人:负责纯化水检查记录表的审核和批准
培训管理:定期对相关人员进行培训和考核,确保其具备足够的技能和知识
分工:明确各责任人的职责和工作内容,避免工作重复和遗漏 监督与检查:对纯化水检查记录表的管理和执行情况进行定期监督和检查,确保其符合相 关法规和标准
纯化水检查记录表
单击此处添加副标题
汇报人:XX
目录
纯化水检查项目 检查结果记录与报告 纯化水系统维护与保养
检查周期与频率 纯化水使用情况记录 相关责任人及培训管理
01
纯化水检查项目
微生物限度
定义:纯化水中 微生物的数量和 种类是否符合规 定标准
检测方法:培养 法、计数法等
(完整版)检验原始记录(纯化水)
检品编号:共3 页第1 页[性状] 本品为(规定:应为无色的澄清液体;无臭,无味)单项结论:[检查]酸碱度取本品10ml,加甲基红指示液2滴,___________;另取10ml,加溴麝香草酚蓝指示液5滴,____________。
(规定:检品与两种指示液均不得显色)单项结论:硝酸盐取本品5ml置试管中,于冰浴中冷却,加10%氯化钾溶液0.4ml与0.1%二苯胺硫酸溶液0.1ml,摇匀,缓缓滴加硫酸5ml,摇匀,将试管于50℃水浴中放置15分钟,溶液产生的蓝色与标准硝酸盐溶液【取硝酸钾0.163g,加水溶解并稀释至100ml,摇匀,精密量取1ml,加水稀释成100ml,再精密量取10ml,加水稀释成100ml,摇匀,即得(每1ml相当于1μgNO3)】0.3ml,加无硝酸盐的水4.7ml,用同一方法处理后的颜色比较____________。
(规定:检品与对照品用同一方法处理后的颜色比较,不得更深)单项结论:亚硝酸盐取本品10ml,置纳氏管中,加对氨基苯磺酰胺的稀盐酸溶液(1 → 100)1ml与盐酸萘乙二胺溶液(0.1 → 100)1ml,产生的粉红色,与标准亚硝酸盐溶液[取亚硝酸钠0.750g(按干燥品计算),加水溶解,稀释至100ml,摇匀,精密量取1ml,加水稀释成100ml,摇匀,再精密量取1ml,加水稀释成50ml摇匀,即得(每1ml相当于1μgNO2)]0.2ml,加无亚硝酸盐的水9.8ml,用同一方法处理后的颜色比较,_______________。
(规定:检品与对照品用同一方法处理后的颜色比较,不得更深)单项结论:检验者:核对者:年月日年月日检品编号:共3 页第2 页氨取本品50ml,加碱性碘化汞钾试液2ml,放置15分钟;如显色,与氯化铵溶液(取氯化铵31.5mg,加无氨水适量使溶解并稀释成1000ml)1.5ml,加无氨水48ml与碱性碘化汞钾试液2ml制成的对照液比较,_________________。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
检查方法:取本品10ml,置纳氏管中,加对氨基苯磺酰胺的稀盐酸溶液﹙1→100﹚1ml与盐酸萘乙二胺溶液﹙0.1→100﹚1ml,产生的粉红色,与标准亚硝酸盐溶液[取亚硝酸钠0.750g(按干燥品计算),加水溶解,稀释至100ml,摇匀,精密量取lml,加水稀释成 100ml,摇匀 ,再精密量取lml,加水稀释成 50ml,摇勻,即得(每1ml相当于1μg NO2)]0.2ml,加无硝酸盐的水9.8ml,用同一方法处理后的颜色比较,供试品溶液。
硝酸盐
检查方法:取本品5ml置试管中,于水浴中冷却,加10%氯化钾溶液0.4ml与0.1%二苯胺硫酸溶液0.1ml,摇匀,缓缓滴加硫酸5ml,摇匀,将试管于50℃水浴中放置15分钟,溶液产生的蓝色与标准硝酸盐溶液液[取硝酸钾0.163g ,加水溶解并稀释至100ml,摇匀,精密量取lml,加水稀释成100ml,再精密量取10ml,加水稀释成100ml,摇匀,即得 (每1ml相当于1μgNO3)]0.3ml,加无硝酸盐的水4.7ml,用同一方法处理后的颜色比较,供试品溶液。 (标准规定:不得更深0.000006%)
电导率
检查方法:取本品照制药用水电导率测定法标准操作规程25℃测得电导率为μS/cm 。 (标准规定:25℃不得大于5.1μSl,加稀硫酸10ml,煮沸后,加高锰酸钾滴定液﹙0.02mol/L﹚0.10ml,再煮沸10分钟,溶液的粉红色消失。
(标准规定:粉红色不得完全消失)
检验日期: 年 月 日;
检品名称:
纯化水
检品编号:
车 间:
取样日期:
取 样 点:
报告日期:
检验依据:
《中国药典》2020年版二部
检验项目:
全检
【性状】:本品为,无臭。
(标准规定:本品为无色的澄清液体,无臭。)
【检查】
检查方法:取本品10ml,加甲基红指示液2滴,(标准规定:不得显红色)
另取本品10ml,加溴麝香草酚蓝指示液5滴,(标准规定:不得显蓝色)
(标准规定:不得更深0.000002%)
氨
检查方法:取本品50ml,加碱性碘化汞钾试液2ml,放置15分钟,溶液;如显色,供试品颜色比对照液氯化铵溶液。(标准规定:如显色与对照液氯化铵溶液﹙取氯化铵31.5mg,加无氨水适量使溶解并稀释成1000ml﹚1.5ml,加无氨水48ml与碱性碘化汞钾试液2ml制成的对照液比较,不得更深0.00003%)
不挥发物
检查方法:取本品100ml,置105℃恒重的蒸发皿中,在水浴上蒸干,并在105℃干燥至恒重,称重,计算:
105℃空蒸发皿恒重: 第一次称重:
第二次称重:
105℃蒸发皿和残渣恒重: 第一次称重:
第二次称重:
不挥发物量: (标准规定:不得过1mg)
重金属
检查方法:取本品100ml,加水19ml,蒸发至20ml,放冷,加醋酸盐缓冲液﹙PH3.5﹚2ml与水适量使成25ml,加硫代乙酰胺试液2ml,摇匀,放置2分钟,与标准铅溶液1.0ml加水19ml用同一方法处理后的颜色比较,。
(标准规定:不得更深0.00001%)
异常情况或偏差处理:
