粘液表皮样癌
粘液表皮样癌护理查房课件

谁会受到影响? 临床表现
患者可能表现为皮肤肿块、溃疡或局部淋巴 结肿大。
定期自我检查有助于早期发现异常。
谁会受到影响? 确诊方法
通过病理组织学检查和影像学检查确诊。
早期诊断能够提高治疗效果。
何时进行护理干预?
何时进行护理干预?
入院评估
患者入院后,需进行全面的身体评估和病史采集 。
患者反馈对于改善护理质量至关重要。
护理中的挑战与解决方案
护理中的挑战与解决方案 常见挑战
患者的心理压力、疼痛管理和药物副作用是护理 中的主要挑战。
护理人员需具备处理这些问题的能力。
ቤተ መጻሕፍቲ ባይዱ
护理中的挑战与解决方案
解决方案
通过提供心理支持、疼痛管理方案和教育患者用 药知识来应对挑战。
与患者建立良好的沟通关系,促进患者的依从性 。
如何实施护理计划?
如何实施护理计划?
制定个性化护理方案
根据患者的具体情况,制定个性化的护理计 划。
护理计划应包含生理、心理和社会支持的各 个方面。
如何实施护理计划? 实施护理干预
定期进行血液检查、影像学检查,监测肿瘤 指标。
通过多学科协作提高护理质量。
如何实施护理计划? 评估护理效果
护理人员应定期评估护理效果,并根据需要 调整护理计划。
什么是粘液表皮样癌? 发病机制
具体的发病机制尚不完全明确,与遗传因素和环 境因素可能有关。
早期诊断和治疗对于改善预后至关重要。
什么是粘液表皮样癌? 流行病学
此类癌症相对少见,通常见于中老年人群体。
性别和种族在发病率上可能存在差异。
谁会受到影响?
谁会受到影响? 高风险人群
粘液表皮样癌的科普知识

粘液表皮样癌的预后与随访 随访检查
术后定期随访非常重要,以监测复发或转移的风 险。
一般建议每3-6个月进行一次随访检查。
粘液表皮样癌的预后与随访
患者支持
患者及家属可寻求心理支持和社交支持,以帮助 应对治疗过程中的挑战。
参加相关支持小组,分享经验可以减轻心理负担 。
谢谢观看
通过影像学检查(如CT、MRI)和组织活检来确 诊粘液表皮样癌。
早期诊断对预后至关重要。
粘液表皮样癌的治疗
粘液表皮样癌的治疗
手术治疗
手术切除是治疗粘液表皮样癌的主要方法, 尽量保证切缘阴性。
手术后可能需要进行放疗或化疗,以降低复 发风险。
粘液表皮样癌的治疗 放疗
放疗可以作为辅助治疗,帮助控制局部肿瘤 或减轻症状。
粘液表皮样癌科普知识
演讲人:
目录
1. 什么是粘液表皮样癌? 2. 粘液表皮样癌的病因 3. 粘液表皮样癌的症状 4. 粘液表皮样癌的治疗 5. 粘液表皮样癌的预后与随访
什么是粘液表皮样癌?
什么是粘液表皮样癌?
定义
粘液表皮样癌是一种稀有的恶性肿瘤,通常发生 在唾液腺、乳腺和其他腺体中。
它的特征是粘液和鳞状细胞的混合组织,导致其 在显微镜下呈现独特的结构。
病毒的具体作用机制尚需进一步研究。
粘液表皮样癌的症状
粘液表皮样癌的症状 早期症状
早期可能没有明显症状,偶尔可感到局部肿块或 肿胀。
定期检查有助于早期发现。
粘液表皮样癌的症状 晚期症状
肿瘤增大可能导致疼痛、吞咽困难或面部麻木等 症状。
如出现这些症状,应及时就医检查。
粘液表皮样癌的症状 诊断方法
什么是粘液表皮样癌? 分类
根据肿瘤的细胞类型和分化程度,粘液表皮样癌 可以分为低分化型和高分化型。
粘液表皮样癌的预后好吗?

粘液表皮样癌的预后好吗?
一、概述
癌症是一种致命的恶心肿瘤之一,如果出现了癌症,要及早的到正规的医院进行检查和治疗,有的时候可能会出现身体不适的症状,可能会诱发一些肿瘤性疾病,一般的情况下,良性肿瘤是可以很好的治疗的,而且这个过程中不会出现严重的并发症,但是大多数癌症都属于一种比较严重的恶性肿瘤,粘液表皮样癌早期可以通过药物进行治疗,也可以通过手术治疗。
二、步骤/方法:
1、患了粘液表皮样癌,这样的疾病要及早发现,及早治疗,这
样对于患者的生命安全有一定的保障作用,一般患上这个疾病,人体的面部神经会受到一定的影响,粘液表皮样癌生长发展是比较缓慢的,所以要定期体检才可以发现.
2、很多疾病早期并不影响到日常的生活和工作,有的时候患了
粘液表皮样癌这个疾病,肿块的界限并不清楚,患者在早期并没有发现一些不适的感觉,所以平时要注意身体方面的保健,避免出现严重的疾病。
3、患了粘液表皮样癌症,这个疾病平时一定要注意饮食方面的
调节,最好要饮食清淡,适当的吃一些蔬菜和水果,有助于提高自身的免疫力,平时一定要注意自己的个人卫生,合理搭配膳食有助于疾病的治疗。
三、注意事项:
以上某同事讲了一下,粘液表皮样癌的预后好吗等方面的事情,一般疾病手术治疗之后,要按照医生的建议进行饮食的搭配,预后效果都是不错的.。
黏液表皮样癌(mucoepidermoid carcinoma,MEC)

黏液表皮样癌(mucoepidermoid carcinoma,MEC)黏液表皮样癌是最常见的涎腺肿瘤,在大、小涎腺发生率相似。
MEC 有3种类型细胞组成:黏液细胞通常较大和类似杯状,经常衬覆于囊壁;非角化表皮样细胞,甚至可能看起来是鳞状上皮;中间细胞则更像基底样或立方细胞。
非典型性少见,表皮样/鳞状细胞倾向类似于正常黏膜上皮。
临床上,使用FISH检测MAML2重排对几种情况有帮助。
在低级别MEC病例中,鉴别诊断需考虑良性肿瘤如Wathin瘤的化生性变型,或更罕见的疾病,如淋巴腺瘤。
在这种情况下,对MAML2重排的检测可以确认MEC的诊断。
在MEC 嗜酸细胞亚型的这种特殊情形中,MAML2 的FISH检测非常有用,因为其中突出的嗜酸细胞形态学可以掩盖表皮样表型,并类似WT、嗜酸细胞囊腺瘤或AciCC。
虽然在许多情况下出现p63阳性反应提示MEC,但对MAML2重排的检测可确认MEC。
尽管许多需与良性肿瘤(WT或嗜酸细胞囊腺瘤)鉴别的嗜酸细胞MEC 是低级别和转移风险较低,但恶性嗜酸细胞MEC由于复发风险较高,对其的诊断诊断仍很重要。
在瘤谱的另一端,高级别MEC可以类似各种其他高级别癌。
在这种情况下MAML2重排的确定对MEC具有诊断性,而且可能很重要,因为在腮腺部位能排除转移的可能性。
高级别MEC中的MAML2重排少见,因此没有重排也不能排除MEC的诊断。
鉴别诊断需要考虑下列肿瘤,包括SDC、腺鳞癌、甚至鳞状细胞癌;一般而言,所有这些肿瘤都比高级别MEC预后更差。
SDC通常由雄激素受体(AR)阳性而p63阴性,与MEC形成对照,后者通常为AR阴性,并至少具有p63的局灶阳性。
腺鳞癌和鳞状细胞癌一般认为源自表面上皮,与MEC对比,后者没有表面原位癌成分。
多灶角化的存在有利于鳞状细胞癌的诊断而非MEC。
MAML2基因断裂探针黏液表皮样癌有特征性的 t(11;19)易位,导致形成 MAML2-CRTC1 融合蛋白。
粘液表皮样癌的影像诊断与鉴别诊断

淋巴瘤
谢谢
粘液表皮样癌的影像诊断 与鉴别诊断
概述
➢ 最常见的腮腺恶性肿瘤,中青年多见。 ➢ 无痛性肿块,膨隆浸润性生长,体积较大。 ➢ 不规则、分叶状、边界不清,可见坏死。 ➢ 大部分位于腮腺浅叶。 ➢ 侵犯神经时可引起面瘫;可伴有淋巴结转移。
影像表现
• 分化不同,恶性程度不同,影像表现差异大。 • 高分化型呈良性特征,可见囊变、出血,含有粘液成分
鉴别诊断
淋巴瘤: 原 发 少 见 , 继 发 较 多 , 多 为 N H L 。 可 双 侧 发 病 。 多 数 表 现 多 发 结 节 , T 1 W I 等 信 号 , T 2 W I 稍 高 信 号 , 信 号 较
均匀,坏死囊变少,DWI高信号,ADC低信号。 中度均匀强化。 常 伴 周 围 淋 巴 结 肿 大 。
围侵袭。 • 很少发生淋巴结转移。
❖囊实性多见,体积较大时内部呈筛状 改变。
❖T1WI等或低信号,T2WI等或高信号, 可见分隔状改变。
❖增强扫描可见中或明显强化,病灶常 有线状强化的完整或不完整的包膜。
腺样囊性癌
鉴别诊断
腺泡细胞癌: 中 年 以 上 发 病 率 高 。 是 腮 腺 恶 性 肿 瘤 中 预 后 最 好 的 , 属 于 低 度 恶 性 , 但 常 侵 犯 包 膜 。 可 双 侧 发 病 。 多 数 表 现 为 良 性 特 点 , 与 多 形 性 腺 瘤 难 鉴 别 。 晚 期 发 生 淋 巴 结 转 移 或 血 行 转 移 。 转 移 部 位 常 见 于 肺 和 骨 , 骨 转 移 多 发 生 在 椎 骨 。 长 T 1 长 T 2 , 明 显 强 化 。
较多时,T2WI稍高信号,T1WI低信号。 • 低分化型浸润性生长,实性成分多,粘液少,T2WI信号
粘液表皮样癌是最常见的唾液腺恶性肿瘤

粘液表皮样癌是最常见的唾液腺恶性肿瘤。
我们和其他人的研究共同表明,CRTC1-MAML2基因融合是临床病理学中常见的肿瘤特征之一。
最近,在对粘液表皮样癌的研究中,科学家们报道了一种罕见的新型CRTC3-MAML2基因融合。
这种新型的基因融合的发生频率和临床病理学意义尚不明朗。
科学家们对101例粘液表皮样癌和89例非粘液表皮样癌的唾液标本进行了分析,并对被福尔马林固定和石蜡镶嵌过的标本进行了RNA提取。
CRTC又分为分为CRTC1、CRTC2和CRTC3三种,我们对CRTC1-NAML2、CRTC2-NAML2和CRTC3-NAML2分别进行了RT-PCR检测,并从病人的临床记录中获得了其临床病理学数据。
在101例粘液表皮样癌病例中,分别有34例和6例表现出CRTC1-NAML2和CRTC3-NAML2阳性。
而在89例粘液表皮样癌病例中,则没有以上任何一种基因融合显示为阳性。
在以往的病例分析中,我们知道CRTC1-NAML2和CRTC3-NAML2是相互排斥的,而CRTC2-NAML2则尚未被检测到。
我们证实了CRTC1-NAML2阳性的粘液表皮样癌的临场病理学特征表现为惰性过程(indolent course)。
而CRTC3-NAML2阳性的粘液表皮样癌的临场病理学特征则表现为进行肿瘤切除术后所有临场病例表现为低级的临床阶段(less-advanced clinic stage)、负节点新陈代谢过程(negative nodal metastasis)、无高阶肿瘤组织学(high-grade tumor histology)、无肿瘤再生或肿瘤相关死亡。
值得注意的是,CRTC3-NAML2患者的平均年龄(36岁)要远低于CRTC1-NAML2患者(55岁)和阴性患者(58岁)。
综上所述,CRTC3-NAML2融合的发生概率被发现要高于较早研究的结果,对于存在CRTC3-NAML2融合的粘液表皮样癌常会伴随某些特定的临床病理学特征,且发病人群的平均年龄要远低于CRTC1-NAML2型或阴性粘液表皮样癌。
涎腺粘液表皮样癌的治疗及预后

涎腺粘液表皮样癌的治疗及预后*导读:粘液表皮样癌来源于涎腺导管上皮,在涎腺恶性肿瘤中比较多见,约占所有涎腺肿瘤的10%,涎腺恶性肿瘤的30%。
……粘液表皮样癌来源于涎腺导管上皮,在涎腺恶性肿瘤中比较多见,约占所有涎腺肿瘤的10%,涎腺恶性肿瘤的30%。
病理上可分为高度恶性及低度恶性二类。
组织学上以含有粘液细胞、表皮样细胞和中间型细胞为特征。
有时还可见到透明细胞及嗜酸细胞。
高分化者粘液细胞及表皮样细胞较多,中间细胞少;低分化者主要为表皮样细胞和中间细胞,而粘液细胞少。
许多文献报道,粘液表皮样癌的预后与肿瘤的病理学分型密切相关。
低分化型粘液表皮样癌侵袭性强,转移率高,并可发生远处转移[1]。
粘液表皮样癌的治疗目前仍主要以传统的手术、放疗和化疗为主,尤其是低分化型粘液表皮样癌,患者5年生存率很低[2]。
因此,许多学者在探索新的疗法,以期提高对粘液表皮样癌的疗效。
1 粘液表皮样癌的治疗1.1 粘液表皮样癌的放射治疗刘斌等对人粘液表皮样癌 MEC-1细胞放射敏感性的研究发现,MEC -1 细胞与其它两种细胞 (人舌癌 Tca8113细胞和人腺样囊性癌Sacc-83细胞 )比较具有较高的放射敏感性[3]。
刘斌等在研究HMBA联合辐射对人粘液表皮样癌MEC-1细胞的抑制作用时发现,1或2mmol/L的HMBA能增强MEC-1细胞系乏氧细胞的辐射敏感性,增敏比分别为 1.28和 1.14,表明小剂量 HMBA与辐射联合应用对MEC-1细胞具有协同抑制作用[4]。
Winslow等研究表明,儿童小涎腺粘液表皮样癌的治疗方案以局部广泛切除加放疗为佳[5]。
1.2 粘液表皮样癌的化学治疗粘液表皮样癌的化学治疗方面也有一些新的进展。
吴军正等在粘液表皮样癌细胞对抗肿瘤药物敏感性研究中发现,粘液表皮样癌普遍对阿霉素、表阿霉素、氟脲嘧啶、长春新碱、维甲酸及干扰素敏感性较强,而对阿糖胞苷、补骨脂素及尼莫通的敏感性低[6]。
贺福长等发现平阳霉素对体外培养的人粘液表皮样癌MEC-1 细胞系细胞生长有较强的抑制作用,而与 0.25T恒定强磁场联合应用后,抑制作用明显增强,两者有相加作用。
腮腺黏液表皮样癌分化标准

腮腺黏液表皮样癌分化标准
腮腺黏液表皮样癌(MEC)是一种罕见的恶性程度较高的癌症,主要发生在腮腺。
它的命名和分类可能会因不同的病理学家和病理学组织学指南而有所不同。
在病理学中,肿瘤的分化程度通常用来描述肿瘤细胞在结构和功能上的成熟程度。
分化程度越高,肿瘤细胞越接近正常细胞,恶性程度相对较低。
相反,分化程度越低,肿瘤细胞越不像正常细胞,恶性程度相对较高。
对于腮腺黏液表皮样癌,病理学家通常会关注以下几点:
1. 肿瘤细胞的形态:肿瘤细胞是否保持正常的形态和大小,是否有明显的异型性(即细胞的大小、形状和极性不一致)。
2. 肿瘤细胞的排列方式:肿瘤细胞是否按照正常的层次和顺序排列,是否有明显的无序或混乱排列。
3. 肿瘤细胞的核质比例:肿瘤细胞的核大小和形状是否正常,核质比例是否合适。
4. 肿瘤细胞的核仁:肿瘤细胞的核仁是否明显,大小和形状是否正常。
5. 肿瘤细胞的染色质:肿瘤细胞的染色质是否密集或疏松,是否分布均匀。
6. 肿瘤细胞的核膜:肿瘤细胞的核膜是否明显,是否有连续或断裂。
7. 肿瘤细胞的胞质:肿瘤细胞的胞质是否清晰,是否有明显的颗粒或粘液池。
这些因素的综合考虑可以用来评估肿瘤的分化程度,从而确定其恶性程度和治疗策略。
然而,这些标准并不是绝对的,不同的病理学家可能会根据他们的经验和理解有不同的判断。
黏液表皮样癌分级标准

黏液表皮样癌的分级标准主要基于细胞的分化程度,可以将其分为三个级别:
1.一级(高分化型):当黏液细胞分化占50%以上时,被划分为一级黏液表皮样癌,此时表皮样癌细胞分化良好,中间细胞较少,无核异形,有丝分裂极少或没有。
2.二级(中分化型):如果黏液细胞分化在10%以下,且在50%以上,被划分为二级黏液表皮样癌,此时常较多实性和细胞间变,偶有神经侵犯。
3.三级(低分化型):当黏液细胞分化低于10%时,被划分为三级黏液表皮样癌,此时肿瘤系中间细胞或表皮样细胞形成的实性团块,瘤细胞间变明显,可见核异形及较多的有丝分裂像,肿瘤呈浸润性生长,质地均匀,完全无包膜,切面呈灰白色,或形成大小不等囊腔,内含拉丝状黏稠液体或血液,淋巴结转移率较高,且可出现血行性转移。
此外,另一种黏液表皮样癌分级方法是通过特定的组织学特征进行评分,如囊腔比例、神经侵犯、坏死、核分裂等,然后根据总分进行分级,低级别为0-4分,中级别为5-6分,高级别为7分以上。
这些分级标准有助于医生评估疾病的严重程度,制定合适的治疗方案,并预测患者的预后。
但请注意,具体的分级标准可能会因不同的医疗机构或专家建议而略有差异。
因此,
在制定具体的治疗方案时,应根据患者的具体情况和医生的建议来确定。
肺原发性黏液表皮样癌(pulmo...

肺原发性黏液表皮样癌(pulmo...粘液表皮样癌(mucoepidermoid carcinoma, MEC)是由不同比例的表皮样细胞、粘液细胞和中间细胞组成的恶性肿瘤,黏液表皮样癌主要发生在涎腺,其中约一半(53%)发生在大涎腺,其中腮腺占45%,颌下腺为7%,舌下腺为1%。
口腔内最常见的发生部位是腭和颊黏膜。
在肺内也可以发生与涎腺肿瘤相似的上皮性肿瘤,原发于肺部的较为少见,肺原发性黏液表皮样癌(pulmonary mucoepidermoid carcinoma,PMEC)是一种罕见的肿瘤(如图1)。
由smetana等人1952年首次报道,一般认为起源于气管及支气管浆液腺和黏液腺的Kulchitsky细胞。
PMEC占支气管肿瘤的1%-5%,全部肺肿瘤0.1%-0.2%。
融合蛋白MECT1-MAML2被认为是唾液腺和 PMEC中的致病性遗传事件。
有研究发现88%的PMEC与MECT1-MAML2融合转录相关,并且MAML2基因重排的存在可以支持PMEC的诊断。
t(11;19) (12;P13)融合蛋白MECT1-MAML2被认为是涎腺和支气管肺黏液表皮样癌的驱动基因事件。
也可发生在皮肤、乳腺和宫颈等部位。
大约6%的病例存在CRTC3-MAML2基因融合,而非MECT1-MAML2基因融合。
有研究表明,存在基因融合的黏液表皮样癌预后更好。
图1:肿瘤位于支气管粘膜下,肿瘤细胞巢状分布,部分细胞内有粘液,可见片状肿瘤性坏死。
临床特征:PMEC可发生于任何年龄段,但患者总体发病年龄较轻,国内文献报道平均年龄在40岁左右,青少年患者也屡见不鲜。
通常认为发病无性别差异,有研究显示大于40岁男性以低级别多见,而高级别多见于年轻女性。
PEMC大体可分为四型: 腔内息肉型、腔内外肿块型、管壁全层浸润型、外周型,而腔内息肉型最多见。
CT检查是一种无创且有效的方法。
Kim等人总结以下征象:①肿瘤长径与所属肺叶或肺段气道平行;②常伴远端肺叶的阻塞性肺炎或肺不张;③“空气新月征”,即病灶部分阻塞气道所形成周围含气的空腔。
儿童支气管黏液表皮样癌一例

较前增生,后转至外 科 于 全 身 麻 醉 下 行 胸 腔 镜 右 肺 下 叶 切
性增生。免疫 组 织 化 学:CK (- ),D2
40 (- ), 八 因 子
癌。出院后随访 2 年患儿情况良好。
高分辨 CT 示 右 肺 下 叶 炎 症,右 肺 下 叶 支 气 管 内 软 组 织 影。
胸部增强 CT 示 右 肺 肺 门、 右 肺 下 叶 病 变, 右 下 叶 支 气 管
ohe
b
e
i@s
i
na c
om
【
Ab
s
t
r
a
c
t】 Br
onch
i
a
l muc
oep
i
de
rmo
i
dc
a
r
c
i
nomai
n ch
i
l
d
r
eni
sr
e
l
a
t
i
ve
l
a
r
ei
nc
l
i
n
i
c
a
l
yr
r
a
c
t
i
c
e and i
t
s symp
t
oms a
r
e no
t spe
c
i
f
i
c Th
i
sd
i
s
e
a
s
ei
下叶基底段肿物
镜技术限制,患儿于 2016 年 1 月 4 日转至 上 级 医 院, 行 胸
部增强 CT+ 重建,右肺门下极、右下叶支气管起始段区域
粘液表皮样癌的并发症及其危害了解并预防

疼痛
疼痛部位:粘液表皮样癌病灶周围或转移部位 疼痛性质:持续性、剧烈、难以忍受 疼痛原因:肿瘤压迫神经、侵犯骨骼、引起炎症等 缓解方法:药物治疗、放射治疗、手术治疗等
压迫症状
吞咽困难:肿瘤压迫食道, 导致吞咽困难
呼吸困难:肿瘤压迫气管, 导致呼吸困难
疼痛:肿瘤压迫神经,导致 疼痛
声音嘶哑:肿瘤压迫喉返神 经,导致声音嘶哑
出血等并发症,增加治疗难度。
增加治疗难度
添加 标题
粘液表皮样癌的并发症可能会导致肿瘤的扩散和转移,导致患者的身体机能下降,影响治疗效果。
添加 标题
并发症可能会导致患者的生活质量下降,增加治疗难度。
添加 标题
并发症可能会导致患者的心理压力增加,影响治疗效果。
降低生存率
添加标题
保持良好的生活习惯
保持良好的饮食习惯,多吃蔬菜水果,少 吃高脂肪、高糖、高盐的食物
保持良好的作息习惯,保证充足的睡眠, 避免熬夜
保持良好的运动习惯,每周至少进行三次 有氧运动,如跑步、游泳、瑜伽等
保持良好的心理状态,避免过度焦虑、抑 郁等负面情绪
定期进行体检,及时发现并治疗疾病,避 免并发症的发生
活质量。
加重病情
01 粘液表皮样癌的并发症可能会
导致病情加重,甚至危及生命。
04 并发症可能会导致患者出现器官
功能障碍,影响患者的身体健康。
并发症可能会导致患者出现疼痛、
02 肿胀、发热等症状,影响患者的生
活质量。
05 并发症可能会导致患者出现心
理压力,影响患者的心理健康。
03 并发症可能会导致患者出现感染、
定期进行身体检查,及时发 现疾病征兆
避免接触致癌物质,如吸烟、 饮酒等
鉴别粘液表皮样癌分三步走

鉴别粘液表皮样癌分三步走
一、概述
白刃给人的身心带来极大的威胁,如果出现了癌症,最常见的治疗方法就是化疗,在坏的过程中,可能放一些刺激性比较大的药品,很多患者都抵抗不住化疗的药品的刺激,有的患者甚至会出现放弃治疗的情况,所以如果出现了一些恶性的肿瘤,要早治疗,一般治疗的越早,治愈的效果就越好,不会给患者的身心造成严重的影响,而且可以更好的治愈疾病。
二、步骤/方法:
1、
粘液表皮样癌是一种特异性肿瘤中最常见的一种癌症,这种疾病给您的生活带来极大的影响,一般出现嘴痛,也会出现牙周炎等方面的症状,患者可能在饮食和这几家的过程中出现一定的障碍。
2、
一般粘液表皮样癌这个疾病发生于中年人的几率比较大,有的患者经常发生在胰腺方面的疾病,而且这个疾病患病时间比较长,病症比较缓慢,和一般的肿瘤有一定的相似之处,所以容易误诊。
3、
鉴别黏液表皮癌这个疾病的方法比较多,一般出现了这个疾病会出现比较明显的腮腺疾病的历史,有的患者早期可以出现面部疼痛或者面谈等方面的症状,要及时到医院进行详细的检查,做到早治疗早治愈。
三、注意事项:
以上我讲了一下,鉴别粘液表皮样癌分三步走等方面的事情,有的时候要认清自己的症状,这样才能够很好的治疗,避免在治疗的过程中出现误诊的现象。
肺粘液表皮样癌1例报告
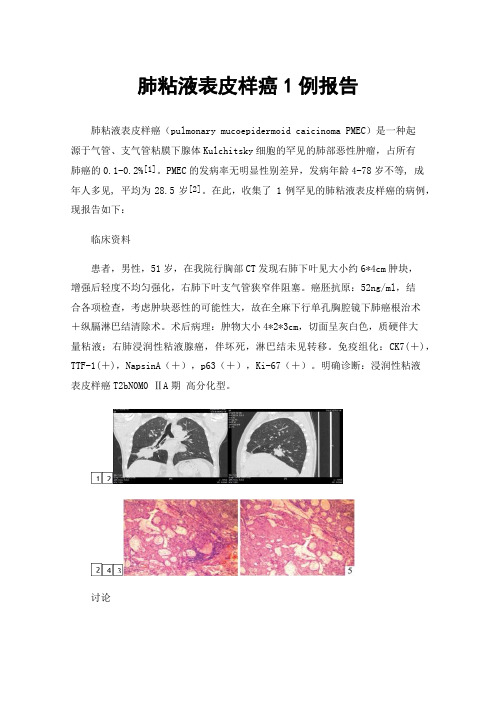
肺粘液表皮样癌1例报告肺粘液表皮样癌(pulmonary mucoepidermoid caicinoma PMEC)是一种起源于气管、支气管粘膜下腺体Kulchitsky细胞的罕见的肺部恶性肿瘤,占所有肺癌的0.1-0.2%[1]。
PMEC的发病率无明显性别差异,发病年龄4-78岁不等, 成年人多见, 平均为28.5岁[2]。
在此,收集了 1例罕见的肺粘液表皮样癌的病例,现报告如下:临床资料患者,男性,51岁,在我院行胸部CT发现右肺下叶见大小约6*4cm肿块,增强后轻度不均匀强化,右肺下叶支气管狭窄伴阻塞。
癌胚抗原:52ng/ml,结合各项检查,考虑肿块恶性的可能性大,故在全麻下行单孔胸腔镜下肺癌根治术+纵膈淋巴结清除术。
术后病理:肿物大小4*2*3cm,切面呈灰白色,质硬伴大量粘液;右肺浸润性粘液腺癌,伴坏死,淋巴结未见转移。
免疫组化:CK7(+),TTF-1(+),NapsinA(+),p63(+),Ki-67(+)。
明确诊断:浸润性粘液表皮样癌T2bN0M0 ⅡA期高分化型。
讨论PMEC是一种源于支气管的恶性肿瘤,主要由分泌黏液细胞,表皮样细胞和未特殊分化中间细胞组成[3],病理上分为高分化黏液样癌和低分化黏液样癌,Ki-67指数可作为高分化和低分化的鉴别指标[4],指数越高,低分化的可能性越大,恶性的可能性越高。
高分化黏液表皮样癌是以黏液细胞为主,细胞异型性不明显,肿瘤多无坏死区域,可见钙化,行手术切除,预后良好;低分化黏液表皮样癌较少见,以中间细胞为主,异型细胞核分裂像和坏死表现及区域淋巴结转移为特征,可远处转移,手术切除,预后不佳。
免疫组化:P63、Ki-67, NapsinA、CK7和TTF-1及FISH检测MAML2可以识别PMEC,其中普遍认为t(11;19)(q21;p13)染色体易位形成的MAML2与粘液表皮样癌的发生相关,且具有高度特异性[10-11],因此成为了PMEC研究方向,并用于MAML2阳性的患者的靶向治疗。
粘液表皮样癌的治疗方法有哪些了解最新医学进展

靶向治疗
靶向治疗的原理:通过特异性识别和攻击肿瘤细胞,减少对正常细胞的损害 靶向治疗的优势:精准度高,副作用小,治疗效果显著 靶向治疗的药物:如EGFR抑制剂、VEGF抑制剂等 靶向治疗的临床应用:已在多种肿瘤治疗中取得良好效果,包括粘液表皮样癌
03 医学进展
新的治疗药物
免疫疗法:通过激活患者自身的免疫系统来攻击肿瘤细胞 靶向治疗:针对肿瘤细胞的特定基因或蛋白质进行治疗
粘液表皮样癌的治疗 方法及医学进展
,
汇报人:
目录 /目录
01
点击此处添加 目录标题
02
粘液表皮样癌 的治疗方法
03
医学进展Βιβλιοθήκη 2粘液表皮样癌的治疗方 法
手术切除
标题
手术切除是治疗粘液表皮样癌的主要方法之一
标题
手术切除包括局部切除和广泛切除两种方式
标题
局部切除适用于早期、低度恶性的粘液表皮样癌
标题
大适应症范围
个体化治疗的发展
基因检测技术的发展,为 个体化治疗提供了基础
靶向药物的研发,提高了 个体化治疗的效果
免疫疗法的兴起,为个体 化治疗提供了新的选择
精准医学的发展,推动了 个体化治疗的普及和应用
基因编辑技术的应用
CRISPR-Cas9技 术:通过基因编 辑,实现对粘液 表皮样癌的精准
治疗
基因编辑技术在 粘液表皮样癌治 疗中的应用:通 过基因编辑,实 现对粘液表皮样
癌的精准治疗
基因编辑技术在 粘液表皮样癌治 疗中的应用:通 过基因编辑,实 现对粘液表皮样
癌的精准治疗
基因编辑技术在 粘液表皮样癌治 疗中的应用:通 过基因编辑,实 现对粘液表皮样
癌的精准治疗
添加标题
粘液表皮样癌

粘液表皮样癌*导读:粘液表皮样癌(mucoepidermoidcarcinoma)也称粘液表皮样肿瘤(mucoepidermoidtumor),在涎腺肿瘤中占5%~10%。
Stewart等根据其临床特点和组织学特征将其称为粘液表皮样肿瘤,并又分为良性及恶性两类。
……【概述】粘液表皮样癌(mucoepidermoid carcinoma)也称粘液表皮样肿瘤(mucoepidermoid tumor),在涎腺肿瘤中占5%~10%。
Stewart 等根据其临床特点和组织学特征将其称为粘液表皮样肿瘤,并又分为良性及恶性两类。
WHO也曾采用粘液表皮样瘤的名称,但以后许多学者认为这种命名分类并不恰当,认为此肿瘤全部为恶性,应称为粘液表皮样癌,并根据癌细胞分化程度的高低和生物学行为,将其分为低度恶性和高度恶性粘液表皮样癌。
WHO1990年修订的涎腺肿瘤的命名及分类已采用这种分类方法。
虽然“粘液表皮样”一词并不完全合适,但基本上反映了肿瘤的主要成分为粘液样细胞和表皮样细胞。
粘液表皮样癌来源于腺管的上皮细胞。
【诊断】一般需经术冰冻切片检查后方能确诊。
发生在腮腺者,腮腺造影可见侵蚀性破坏,导管缺损或中断,远端导管出现部分或完全不充盈,管壁不光滑,也可能出现分支导管破坏,碘油外漏等恶性肿瘤表现。
CT检查可见边界不清楚的肿块,腮腺腺体破坏或被挤压移位。
【治疗措施】粘液表皮样癌原发灶的处理主要是区域性根治性切除。
为防止复发,手术应在距肿瘤1cm以外的正常组织内进行肿瘤切除。
腮腺高分化粘液表皮样癌首次手术治疗者,不管病期如何,一般采用保留面神经的腮腺全切除术;低分化型浸润面神经的机会较多,如面神经受累,应行牺牲面神经的腮腺全切术,如果及的面神经长度较大,可以在切除一段神经后做神经移植。
发生在颌下腺的粘液表皮样癌,应行颌下三角清扫术。
发生在腭部者,应做部分上颌骨切除术。
如肿瘤已侵犯周围组织,应做扩大切除术。
粘液表皮样癌的区域淋巴结转移率较低,除低分化型可考虑选择性颈淋巴清扫术,高分化者一般不做选择性颈淋巴清扫术。
黏液表皮样癌(mucoepidermoid carcinoma,MEC)

黏液表皮样癌(mucoepidermoid carcinoma,MEC)黏液表皮样癌是最常见的涎腺肿瘤,在大、小涎腺发生率相似。
MEC 有3种类型细胞组成:黏液细胞通常较大和类似杯状,经常衬覆于囊壁;非角化表皮样细胞,甚至可能看起来是鳞状上皮;中间细胞则更像基底样或立方细胞。
非典型性少见,表皮样/鳞状细胞倾向类似于正常黏膜上皮。
临床上,使用FISH检测MAML2重排对几种情况有帮助。
在低级别MEC病例中,鉴别诊断需考虑良性肿瘤如Wathin瘤的化生性变型,或更罕见的疾病,如淋巴腺瘤。
在这种情况下,对MAML2重排的检测可以确认MEC的诊断。
在MEC 嗜酸细胞亚型的这种特殊情形中,MAML2 的FISH检测非常有用,因为其中突出的嗜酸细胞形态学可以掩盖表皮样表型,并类似WT、嗜酸细胞囊腺瘤或AciCC。
虽然在许多情况下出现p63阳性反应提示MEC,但对MAML2重排的检测可确认MEC。
尽管许多需与良性肿瘤(WT或嗜酸细胞囊腺瘤)鉴别的嗜酸细胞MEC 是低级别和转移风险较低,但恶性嗜酸细胞MEC由于复发风险较高,对其的诊断诊断仍很重要。
在瘤谱的另一端,高级别MEC可以类似各种其他高级别癌。
在这种情况下MAML2重排的确定对MEC具有诊断性,而且可能很重要,因为在腮腺部位能排除转移的可能性。
高级别MEC中的MAML2重排少见,因此没有重排也不能排除MEC的诊断。
鉴别诊断需要考虑下列肿瘤,包括SDC、腺鳞癌、甚至鳞状细胞癌;一般而言,所有这些肿瘤都比高级别MEC预后更差。
SDC通常由雄激素受体(AR)阳性而p63阴性,与MEC形成对照,后者通常为AR阴性,并至少具有p63的局灶阳性。
腺鳞癌和鳞状细胞癌一般认为源自表面上皮,与MEC对比,后者没有表面原位癌成分。
多灶角化的存在有利于鳞状细胞癌的诊断而非MEC。
MAML2基因断裂探针黏液表皮样癌有特征性的 t(11;19)易位,导致形成 MAML2-CRTC1 融合蛋白。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
粘液表皮样癌基本概述粘液表皮样癌(mucoepidermoid carcinoma)也称粘液表皮样肿瘤(mucoepidermoid tumor),在涎腺肿瘤中占5%~10%。
Stewart等根据其临床特点和组织学特征将其称为粘液表皮样肿瘤,并又分为良性及恶性两类。
WHO也曾采用粘液表皮样瘤的名称,但以后许多学者认为这种命名分类并不恰当,认为此肿瘤全部为恶性,应称为粘液表皮样癌,并根据癌细胞分化程度的高低和生物学行为,将其分为低度恶性和高度恶性粘液表皮样癌。
WHO1990年修订的涎腺肿瘤的命名及分类已采用这种分类方法。
虽然“粘液表皮样”一词并不完全合适,但基本上反映了肿瘤的主要成分为粘液样细胞和表皮样细胞。
粘液表皮样癌来源于腺管的上皮细胞。
[1]发病原因肿瘤的主要成分为粘液样细胞和表皮样细胞。
粘液表皮样癌来源于腺管的上皮细胞。
[2]临床表现粘液表皮样癌发生在腮腺者最多,约占70%以上。
小涎腺者常见于腭部,其他部位,如磨牙后区、颊部、上唇、下唇等部位则少有发生。
可发生于任何年龄,以30~50岁多见,女性多于男性,约为1.5∶1。
高分化者常呈无痛苦性肿块,生长缓慢。
肿瘤大小不等,边界可清或不清,质地中等偏硬,表面可呈结节状。
腮腺肿瘤侵犯面神经时,可出现面瘫。
手术后可以复发,但颈部淋巴结转移率低,血道转移更为少见。
与高分化者相反,低分化黏液表皮样癌生长较快,可有疼痛,边界不清,与周围组织粘连。
腮腺肿瘤常累及面神经,颈淋巴结转移率高,且可出现血到转移。
术后易于复发。
因此,高分化黏液表皮样癌术低度恶性肿瘤,而低分化黏液表皮样癌属高度恶性肿瘤。
前者较常见,后者少见。
粘液表皮样癌的临床表现与临床的分化程度关系密切。
高分化型,占多数,一般为无痛性肿块,生长较慢,病程较长。
肿瘤体积大小不一,边界清楚,质偏硬,活动,表面光滑或呈结节状。
可为囊性,亦可为实性。
发生于腭部或磨牙后区者,可见肿块在粘膜下呈淡蓝色或暗紫色,粘膜光滑,质地软,穿刺可抽出少量血性紫黑色液体。
低分化型肿瘤生长较快,常伴疼痛。
边界不清楚,呈弥散性,与周围组织有粘连,可破溃而继发感染,形成经久不愈的溃烂面,并有淡黄色粘稠分泌物。
有时可形成涎瘘。
发生于腮腺者,累及面神经时可发生面神经瘫痪症状及面肌抽搐症状。
发生于腭部者,可能破坏硬腭。
[3]一般需经术冰冻切片检查后方能确诊。
发生在腮腺者,腮腺造影可见侵蚀性破坏,导管缺损或中断,远端导管出现部分或完全不充盈,管壁不光滑,也可能出现分支导管破坏,碘油外漏等恶性肿瘤表现。
CT检查可见边界不清楚的肿块,腮腺腺体破坏或被挤压移位。
(一)大体形态:粘液表皮样癌高分化者与混合瘤相似,呈圆形,肿瘤较小,直径多为2~3cm,少数超过5cm。
有的有被膜,但多数不完整,甚至完全无被膜。
剖面呈灰白色或浅粉色,偶见分叶,可有多少不等的小囊,内含粘液。
低分化者完全缺乏包膜,界限不清,侵犯邻近组织。
切面呈灰白色,不分叶,质地均匀,可有散在的小囊及半透明的小灶。
(二)镜检:粘液表皮样癌由粘液样细胞、表皮样细胞和中间细胞组成。
粘液样细胞分化成熟时呈杯状或柱状,胞浆透明,核在基底部;分化不成熟时,似腺癌细胞,胞浆内含粘液,胭脂红染色阳性。
表皮样细胞类似口腔粘膜的复层鳞状上皮,可见细胞间桥,偶见角化。
中间细胞呈立方形,体积较小,大小一致,胞浆少,类似上皮的基底细胞。
中间细胞可向粘液样细胞和表皮样细胞演变。
高分化者,粘液样细胞和表皮样细胞较多,中间细胞较少,瘤细胞可形成不规则的片状,但常形成大小不等的囊腔,囊壁衬里常见粘液细胞。
粘液样细胞可覆盖于表皮样细胞上,也可夹杂在表皮样细胞之间。
较大的囊腔可有乳头突入,腔内有红染的粘液。
低分化者,主要为表皮样细胞和中间细胞,而粘液样细胞较少,瘤细胞间变明显,可见核分裂,实质性上皮团块多,囊腔少,并可见肿瘤向周围组织侵犯。
(三)生物学特点:粘液表皮样癌常呈浸润性生长,复发率较高,可发生淋巴结转移,转移到骨、脑、肺者较少,但高分化者可有完整包膜,完整切除后复发较少。
[4]治疗措施粘液表皮样癌原发灶的处理主要是区域性根治性切除。
为防止复发,手术应在距肿瘤1cm以外的正常组织内进行肿瘤切除。
腮腺高分化粘液表皮样癌首次手术治疗者,不管病期如何,一般采用保留面神经的腮腺全切除术;低分化型浸润面神经的机会较多,如面神经受累,应行牺牲面神经的腮腺全切术,如果及的面神经长度较大,可以在切除一段神经后做神经移植。
发生在颌下腺的粘液表皮样癌,应行颌下三角清扫术。
发生在腭部者,应做部分上颌骨切除术。
如肿瘤已侵犯周围组织,应做扩大切除术。
粘液表皮样癌的区域淋巴结转移率较低,除低分化型可考虑选择性颈淋巴清扫术,高分化者一般不做选择性颈淋巴清扫术。
Perzik等强调,只有在切除原发肿瘤时确定颈淋巴结有转移者,才做颈淋巴结清扫术。
粘液表皮样癌对放射治疗不敏感,但对低分化型术后可配合使用放射治疗,有可能提高疗效或减少复发。
[6]100%,而低分化型的5年、10年生存率则分别为39%和11%。
Spiro等报告367例,其中高分化型5年、10年及15年生存率分别为92%、90%及82%;低分化型则分别为49%、42%及33%。
原发于腮腺及小涎腺者较发生于颌下腺者为好。
林国础等报告189例,局部复发率为13.57%,5年、10年、15年生存率分别为91.66%、89.87%、66.61%。
治疗及预后粘液表皮样癌来源于涎腺导管上皮,在涎腺恶性肿瘤中比较多见,约占所有涎腺肿瘤的10%,涎腺恶性肿瘤的30%。
病理上可分为高度恶性及低度恶性二类。
组织学上以含有粘液细胞、表皮样细胞和中间型细胞为特征。
有时还可见到透明细胞及嗜酸细胞。
高分化者粘液细胞及表皮样细胞较多,中间细胞少;低分化者主要为表皮样细胞和中间细胞,而粘液细胞少。
许多文献报道,粘液表皮样癌的预后与肿瘤的病理学分型密切相关。
低分化型粘液表皮样癌侵袭性强,转移率高,并可发生远处转移[1]。
粘液表皮样癌的治疗目前仍主要以传统的手术、放疗和化疗为主,尤其是低分化型粘液表皮样癌,患者5年生存率很低[2]。
因此,许多学者在探索新的疗法,以期提高对粘液表皮样癌的疗效。
1 粘液表皮样癌的治疗1.1 粘液表皮样癌的放射治疗刘斌等对人粘液表皮样癌 MEC-1细胞放射敏感性的研究发现,MEC -1 细胞与其它两种细胞 (人舌癌 Tca8113细胞和人腺样囊性癌Sacc-83细胞 )比较具有较高的放射敏感性[3]。
刘斌等在研究HMBA联合辐射对人粘液表皮样癌MEC-1细胞的抑制作用时发现,1或2mmol/L的HMBA能增强MEC-1细胞系乏氧细胞的辐射敏感性,增敏比分别为 1.28和 1.14,表明小剂量 HMBA与辐射联合应用对MEC-1细胞具有协同抑制作用[4]。
Winslow等研究表明,儿童小涎腺粘液表皮样癌的治疗方案以局部广泛切除加放疗为佳[5]。
1.2 粘液表皮样癌的化学治疗粘液表皮样癌的化学治疗方面也有一些新的进展。
吴军正等在粘液表皮样癌细胞对抗肿瘤药物敏感性研究中发现,粘液表皮样癌普遍对阿霉素、表阿霉素、氟脲嘧啶、长春新碱、维甲酸及干扰素敏感性较强,而对阿糖胞苷、补骨脂素及尼莫通的敏感性低[6]。
贺福长等发现平阳霉素对体外培养的人粘液表皮样癌MEC-1 细胞系细胞生长有较强的抑制作用,而与 0.25T恒定强磁场联合应用后,抑制作用明显增强,两者有相加作用。
在随后平阳霉素磁性脂质体对人粘液表皮样癌的体内抗瘤作用研究中发现,平阳霉素磁性脂质体,对人粘液表皮样癌的移植瘤有显著抑制作用,抑瘤率为81.1%,显著高于平阳霉素脂质体 (60.9% )和游离平阳霉素(45.5% ),而且对正常组织 (主要是肺脏 )的毒副作用明显减轻[7]。
金军等发现10mg/L 阿霉素可以诱导MEC-1细胞系细胞发生凋亡,光镜、电镜下MEC-1细胞形态上显现一系列典型的凋亡特征性变化,并用流式细胞仪检测到细胞DNA的变化,同时免疫组化发现 p53蛋白表达增强,提示阿霉素诱导的MEC-1细胞凋亡为 p53依赖性的[8]。
1.3 粘液表皮样癌的分化诱导治疗目前,国内一些学者在粘液表皮样癌的分化诱导治疗方面,做了许多有益的基础研究。
司徒镇强等应用1 mmol/L六亚甲基二乙酰胺 (HMBA )诱导MEC-1细胞,经细胞动力学、细胞DNA含量、核仁区嗜银蛋白染色、抑瘤率、荷瘤后生命延长率及光镜、电镜细胞形态学指标观察,发现MEC-1细胞有向成熟细胞分化趋势,主要表现为嗜银颗粒数目变少( P < 0.01 ),MEC-1细胞大小趋于一致,胞浆丰富,核浆比例减小,胞核异形性降低,微绒毛减少,细胞器趋于成熟,核形态规整,胞浆出现代表分泌功能的成熟酶原颗粒,抑瘤率下降到71.7%,生命延长率 29.6%等[9]。
常用分化诱导剂二甲基亚砜(DMSO)诱导 MEC -1细胞发现, MEC-1细胞异型性降低,有向成熟细胞分化的趋势,抑瘤率下降到75% (对照组 100 %,P < 0.01 ),诱导组肿瘤细胞生长缓慢,快速生长期肿瘤倍增时间延长(P<0.05),诱导组裸鼠生存期较长。
用平面极性化合物环组乙酰胺(cAHB)作为分化诱导剂,对 MEC-1细胞进行体外分化诱导,发现诱导后 MEC-1细胞染色体数目和畸度率均下降,并出现二倍体细胞。
分化诱导剂HMBA与丝裂霉素(MMC)合用能提高 MEC-1细胞对丝裂霉素的敏感性,并且联合应用可有效地增强MMC对原来耐药的 MEC-1细胞抑制生长效果。
而HMBA与 5-Fu联合应用抑制肿瘤生长呈现协同作用,联合用药组的抑瘤率及生命延长率均高于单独用药组。
2 粘液表皮样癌的预后Inagaki等对下颌骨粘液表皮样癌研究表明,利用全口曲面断层及CT检查可将发生在下颌骨的粘液表皮样癌分为三型:囊肿型、骨小梁轻度改变型及浸润型,根据分型的不同,肿瘤的预后也不一样[10]。
俞光岩等认为,癌胚抗原表达的研究可作为粘液表皮样癌病理分级的补充,对于诊断为粘液表皮样癌者,在进行病理分级的同时,观察癌胚抗原的表达特征,可获得更多的信息,更全面地了解肿瘤的生物学行为及预测患者的预后[11]。
张中仪等对8例粘液表皮样癌作了回顾性形态测量及 DNA倍体值测定,其中1 例高度恶性者 DNA倍体 > 5c,占 20.99%,3例中度恶性 DNA倍体 >5c,平均8%,4例低度恶性DNA 倍体 > 5c,平均为3.5%,因此提出,粘液表皮样癌切片Feulgen染色后,应用图象分析进行核形态及 DNA倍体测定,与组织学定性分析同步进行,对粘液表皮样癌的分级有重要价值,对估计预后也有一定意义[12]。
Press和 Cho等研究发现大约1/3的涎腺粘液表皮样癌有HER-2/neu和 c-erbB-2基因过度表达和 /或扩增,HER-2/neu和 c-erbB-2的扩增和 /或过度表达可以作为粘液表皮样癌预后不良诊断的一个独立指标[13,14]。
