干细胞和免疫细胞的差别,您有必要了解一下
干细胞基础知识

干细胞概述干细胞的定义干细胞(Stem cell,SC)是一类具有自我更新(self-renewing)能力的多潜能细胞,即干细胞保持未定向分化状态和具有增殖能力,在合适的条件或给予合适的信号,它可以分化成多种功能细胞或组织器官,医学界称其为“万用细胞”,也有人通俗而形象地称其为“干什么都行的细胞”。
干细胞来源于胚胎、胎儿组织和成年组织。
来自胚胎和胎儿组织的胚胎干细胞具有多潜能分化特性,可分化为成熟个体体内几乎全部200多种以上的成熟细胞类型。
而成年个体组织来源的成体干细胞(adult stem cell)有造血干细胞、神经干细胞和胰腺干细胞等。
人类很多疾病诸如心肌梗塞、糖尿病、帕金森病等,均涉及细胞(如脑细胞、心肌细胞、胰岛细胞)的死亡。
干细胞技术最显著的作用就是:能再造一种全新的、正常的甚至更年轻的细胞、组织或器官,用以治疗诸如脑瘫、中风、白血病、心肌梗塞、糖尿病、帕金森氏病等多种用传统方法难以治愈的疾病,具有不可估量的医学价值,给人们带来了希望。
干细胞的分类干细胞具有自我更新(self-renewing)的能力,在一定条件下下,它可以分化成各种功能细胞。
按分化潜能的大小,干细胞基本上可分为以下三种类型。
(1)全能性干细胞(Totipotent stem cells) 它具有形成完整个体的分化潜能。
如胚胎干细胞(Embryonic stem cells,ESC),具有与早期胚胎细胞相似的形态特征和很强的分化能力,可以无限增殖并分化成为全身200多种细胞类型,进一步形成机体的所有组织、器官。
(2)多能性干细胞(Pluripotent stem cells) 这种干细胞具有分化出多种组织细胞的潜能,但却失去了发育成完整个体的能力,发育潜能受到一定的限制。
骨髓多能造血干细胞是典型的例子,它可分化出至少12种血细胞,但不能分化出造血系统以外的其它细胞。
(3)单能干细胞也称专能或偏能干细胞(Unipotent stem cells)。
干细胞-免疫细胞相关知识(1)

产品技术产品技术2.免疫细胞技术u DC/CIK u NK u NKT u CAPRI(链式cik)u CTL 1.干细胞技术u 脐带间充质干细胞u 脂肪干细胞u 牙髓干细胞u 毛囊干细胞u 胰岛干细胞u 自体成纤 3.抗衰老技术u 全身抗衰老:NK细胞、CIK细胞、干细胞(脐带间充干,自体脂肪细胞)u 局部年轻化:脂肪干细胞,自体成纤维细胞干细胞干细胞干细胞来源干细胞医学价值干细胞临床病例干细胞临床标准干细胞使用注意事项干细胞的“干”译自英文“Stem”,意为“树干”和“起源”。
自我更新增殖和多向分化干细胞分类根据发育阶段可分为:1、胚胎干细胞:ES细胞。
2、成体干细胞EG细胞:神经干细胞、血液干细胞、骨髓间充质干细胞、表皮干细胞)等。
根据其分化潜能可分为:1、全能干细胞:可分化成人体的各种细胞,从而组成各种组织和器官,最终发肓成为一个完整的生物体(受精卵)2、多能干细胞:具有分化多种组织的潜能,但失去了发肓成完整个体的能力(间充质干细胞)3、专能干细胞:由多能干细胞分化而来,只能向一种类型的细胞分化(肝脏干细胞等)干细胞的四大特性Ø自我更新:干细胞可以通过自我复制,产生与亲本完全相同的子代细胞,以保持干细胞数量的恒定可通过分裂维持自身细胞的特性和大小;Ø多向分化:干细胞在一定条件下可以进入分化程序,可进一步多向(或定向)分化为逐步成熟的次级子代细胞,最终形成功能特异的组织细胞,在组织修复和新陈代谢中起重要作用;Ø自动归巢:干细胞在体内定向迁移至特定的组织部位,在不同环境的诱导下,依赖性地分化为特定的组织细胞。
Ø免疫原性低:脐带、胎盘来源的干细胞表面抗原不明显,免疫原性低,不存在免疫排斥的特性。
生活中的几个现象1、擦伤日常生活中,我们的皮肤经常会擦伤,7-8天后,受伤的部位会自动愈合,恢复受伤之前的样子。
这是什么原因呢?2、献血一次性抽出200-400ml血液,相当于人体总血量的1/10左右。
第七章-免疫细胞课件

B2细胞(CD5-)受外来抗原刺激,经活化,克隆扩增,发生体细胞突变,产生高亲和性特异性抗体。 而CD5+B1细胞对外原抗原只产生有限的应答,主要对一些自己抗原产生应答,其应答特征是不依赖T细胞的,其产生的抗体也无亲和性成熟。故CD5+B细胞产生的抗体为低亲和性和多反应性的IgM型自身抗体,及一些天然抗体。
T细胞亚群的分类:
根据TCRαβT细胞的功能可将其分为二类: 一类为调节性T细胞 辅助性T细胞 (helper T lymphocyte, TH) 抑制性T细胞 (suppressor T lymphocyte, TS) 另一类为效应性T细胞 杀伤性T细胞 (cytolytic T cell, CTL或Tc) 迟发型超敏T细胞 (delayed type hypersensitivity T lymphocyte, TDTH)
胸腺微环境
T细胞在胸腺的分化发育过程
三个阶段: 早期T发育为双阴性细胞阶段 其主要表型为CD4-和CD8-,故称为双阴性细胞(double negative, DN) 第二阶段为不成熟胸腺细胞 由DN细胞经单阳性细胞(CD4-,CD8+)进行分化为双阳性(CD4+,CD8+)细胞(double positive, DP)。 第三阶段为由DP细胞选择分化为只表达CD4+或CD8+的单阳细胞(single positive, SP),然后迁出胸腺,移居周围淋巴器官。
第七章 免疫细胞
第一节 造血干细胞
各种血细胞都起源于 共同的祖先细胞——造血干细胞
在人和动物周围血中,存在形态不同,功能各异的多种血细胞: 生命周期 红细胞 120天 粒细胞 20-60小时 血小板 5-10天 单核细胞 存在于骨髓 约为5天 存在周围血 可超过200天 淋巴细胞 数月至数年
第十二章造血干细胞及免疫细胞的生成

第十二章造血干细胞及免疫细胞的生成免疫细胞都属于血细胞,所有血细胞都来源于造血干细胞。
因此在一定意义上讲,免疫细胞的发育分化就是造血干细胞分化成熟的过程。
第一节 造血干细胞的特性和分化一、造血干细胞的起源和表面标记(一)造血干细胞的起源哺乳动物的造血最早发生在卵黄囊,随后转移到胎肝,胚胎发育中期以后以及出生后,骨髓成为主要的造血场所,并为B细胞发育的中枢免疫器官;胸腺是T淋巴细胞的分化成熟的中枢免疫器官。
早期的造血干细胞是多能造血干细胞(pluripotent hematopoietic stem cell),具有自我更新(self−renewing)和分化(differentiation)两种重要的潜能,赋予机体在整个生命过程中始终保持造血能力。
多能造血干细胞最初分化为共同淋巴样祖细胞和共同髓样祖细胞等等。
(二)造血干细胞的表面标记白细胞分化抗原和单克隆抗体技术的应用,为造血干细胞表面标记的研究及其分离纯化提供了重要的理论和实验依据。
人造血干细胞的主要表面标记为CD34和c-kit (CD117),不表达谱系(lineage)特异性标记。
(1)CD34:CD34是一种高度糖基化跨膜蛋白,有1%~4%骨髓细胞表达CD34,其中包括了造血干细胞,是造血干细胞的一种重要标记,应用CD34单克隆抗体可从骨髓、胎肝或脐血中分离、富集造血干细胞。
随着造血干细胞的分化成熟,CD34表达水平逐渐下降,成熟血细胞不表达CD34。
(2)CD117:CD117是干细胞因子(stem cell factor,SCF)的受体,是原癌基因c−kit的编码产物Kit。
CD117是属于含有酪氨酸激酶结构的生长因子受体,胞膜外区结构属IgSF。
CD117+细胞约占骨髓细胞的1%~4%,50%~70%CD117+骨髓细胞表达CD34,因此,CD117也是多能造血干细胞的重要标记。
(3)Lin-细胞:应用针对T细胞、B细胞、NK细胞、单核细胞、巨噬细胞、巨核细胞、髓系以及红系等多种谱系相应单克隆抗体的混合抗体(CD2、CD3、CD14、CD16、CD19、CD24、CD56、CD66b和血型糖蛋白A等抗体)结合免疫磁珠分离的方法,除去骨髓、胎肝单个核细胞中上述各个谱系发育不同阶段的细胞,所留下的细胞称为谱系阴性(Lin-)细胞,主要为早期造血干细胞。
免疫细胞
Developmental time course of TCR gene expression
T细胞发育的阳性选择
早期胸腺细胞为CD2+CD5+CD4-CD8-, TCRβ基因重排和表达,继而发育成双阳 性CD4+CD8+(DP) 机制:如DP细胞的TCRαβ能与胸腺基质 细胞表面的MHC-I和MHC-II类分子高亲 和力结合,被选择继续发育,否则凋亡
脑
神经元、胶质细胞、血细胞
间质干细胞
骨髓
肌肉细胞、骨骼、脂肪细胞
造血干细胞的生物学特征
1.自我更新(self-renewal) 造血干细胞 不对称有丝分裂 子代细胞1(早期祖细胞):继续分化 子代细胞2(自我更新):
(维持造血干细胞的全部生物学特征: 维持干细胞池大小、干细胞数量/质量不变。)
2.多向分化 * 造血干细胞早期祖细胞 对称性有丝分裂多向分化
T细胞的发育过程
造血干细胞(PHSC) 前体T细胞(有TdT)
成熟T细胞
效应T细胞
CD4+
CD8+
T细胞在胸腺内的发育
骨髓:pro-T 早期阶段:DN
CD4-CD8-
第二阶段:DP
CD4+CD8+
第三阶段:SP
CD4+CD8- 或CD4-CD8+
T细胞受体的发育
最早表达CD3δ基因
随即出现pTα的mRNA, TCRβ的胚系转录本
组织专一干细胞
* 是特定组织的起源细胞,具发育潜能; * 动物成体多数组织中保留有部分干细胞;
不同组织来源的干细胞可能互相转化。
神 经
骨髓环境
干
细 胞
脑部
干细胞变为免疫细胞的原理

干细胞变为免疫细胞的原理干细胞是一类具有自我更新和多分化能力的细胞。
它们可以分化成多种不同细胞类型,包括心脏细胞、神经细胞和免疫细胞等。
其中,干细胞转化为免疫细胞的过程涉及多个复杂的细胞信号通路和分化因子的调控。
下面我将详细讨论干细胞转化为免疫细胞的原理。
首先,为了使干细胞向免疫细胞分化,需要提供相应的信号分子来启动和促进细胞分化过程。
这些信号分子主要来自周围环境中的细胞和细胞外基质,它们通过与细胞表面的受体结合来传递信号。
例如,造血干细胞(HSCs)可以分化为免疫细胞,主要受到造血微环境中多种细胞类型和细胞外基质的影响。
例如,造血干细胞途径中的细胞外基质成分,如纤维蛋白原、胶原等,能够通过与整合素受体互作,调控干细胞增殖和分化。
而造血干细胞则受到周围环境细胞所释放的细胞因子的影响,如干扰素(IFN)、肿瘤坏死因子(TNF)等能够促进干细胞向免疫细胞的分化。
其次,干细胞分化为免疫细胞还需要依赖于多个调控分化过程的因子。
在造血系统中,一系列调控免疫细胞分化的因子得到了广泛研究,例如,GATA-1、GATA-2、PU.1和Erg等转录因子在造血系统的分化和成熟过程中发挥关键作用。
这些转录因子能够通过调控特定的基因表达来促进干细胞分化为免疫细胞。
例如,PU.1被广泛认为是一个免疫细胞特异性的转录因子,它在干细胞向粒细胞系列、单核细胞系列等免疫细胞分化过程中发挥重要作用。
实验证据表明,通过改变PU.1的表达水平,可以显著调控干细胞向免疫细胞分化的能力。
另外,细胞的外界环境对干细胞分化为免疫细胞也具有重要影响。
适当的细胞外环境可以为干细胞提供分化所需的信号和条件。
例如,骨髓中的造血微环境通过提供支持细胞、细胞因子和细胞外基质等成分,为造血干细胞的分化提供了良好的条件。
在干细胞转化为免疫细胞的过程中,细胞因子的作用也是十分重要的。
例如,肿瘤坏死因子(TNF)、干扰素(IFN)和白细胞介素(IL)等能够调控干细胞的增殖和分化。
免疫细胞的发育和功能

免疫细胞的发育和功能免疫系统是人体抵御外界病原体入侵的重要防线,而免疫细胞则是免疫系统的重要组成部分。
免疫细胞主要包括白细胞、淋巴细胞、巨噬细胞、粒细胞等,它们在体内扮演着关键的防御作用。
然而,在胚胎发育的早期,免疫细胞却是一个相对较为薄弱的环节,它们的发育和功能需要在经过一定的过程之后才能较为完善地展现出来。
一、免疫细胞的发育免疫细胞是由骨髓和胸腺等器官生成的。
最初,体内的免疫细胞都是从一个干细胞中分化出来的。
这个干细胞可以分化为不同类型的细胞,包括T细胞、B细胞、自然杀伤细胞等。
这些分化出来的细胞再经过进一步的分化和成熟,成为体内不同种类的免疫细胞。
免疫细胞的发育过程主要包括以下几个阶段:1. 骨髓中的干细胞分化。
在骨髓中,有一类非常原始的细胞,它们可以分化为不同类型的免疫细胞。
这些细胞叫做多能干细胞或者造血干细胞。
它们可以分化为T细胞、B细胞、巨噬细胞、粒细胞等不同类型的免疫细胞。
2. 免疫细胞的成熟和分化。
干细胞经过分化之后会成为原始免疫细胞。
原始免疫细胞随后会分化和成熟,最终成为不同类型的免疫细胞。
比如,原始免疫细胞可以分化为T细胞和B细胞。
B细胞会分泌一种叫做抗体的分子,可以直接识别和清除体内的病原体。
而T细胞则主要扮演着辨识和杀死体内受感染细胞的重要角色。
3. 免疫细胞在体内的定位和巡视。
成熟的免疫细胞会在体内不同的组织中巡视,以寻找并清除病原体。
比如,巨噬细胞和自然杀伤细胞会在体内不同的组织中活动,有效地清除体内的一些感染病原体。
而T细胞和B细胞则会在淋巴组织中定位,以便与病原体相遇并进行攻击。
二、免疫细胞的功能免疫细胞在人体的免疫防御中扮演着非常重要的角色,其功能也相当复杂和多样。
下面简单介绍一下免疫细胞常见的几种功能:1. 免疫识别和攻击。
当人体遭受感染或受到病原体入侵的时候,免疫细胞能够识别出外来物质和病原体,进而对其进行攻击。
比如,自然杀伤细胞可以识别和杀死一些肿瘤细胞和病原体感染的细胞;而T细胞和B细胞则会攻击和消灭体内的病原体。
免疫细胞的特征及分类

免疫细胞的特征及分类
免疫细胞的特征及分类如下:
1、特征:免疫细胞俗称白细胞,具有识别抗原、产生特异性免疫应答的能力。
2、分类:
(1)非特异性免疫细胞:包括吞噬细胞、自然杀伤细胞等。
(2)特异性免疫细胞:包括T淋巴细胞、B淋巴细胞等。
此外,根据功能的不同,免疫细胞还可以分为以下几种:
1、吞噬细胞:具有吞噬功能的细胞,是免疫战斗中反应最快,最先奔赴前线的“先头部队”,特点是全面杀敌、作用迅速。
2、特异性细胞:包括淋巴细胞(T淋巴细胞和B淋巴细胞)、浆细胞、抗原呈递细胞等。
其中淋巴细胞是人体免疫系统的主要组成部分,包括T淋巴细胞和B淋巴细胞,它们能够识别抗原、产生特异性免疫应答,并具有调节免疫应答、参与免疫记忆等功能。
浆细胞能够产生抗体,参与体液免疫。
抗原呈递细胞能够摄取和处理抗原,并将其呈递给淋巴细胞,是启动免疫应答的关键步骤。
免疫学与细胞治疗技术的结合

免疫学与细胞治疗技术的结合我的免疫学知识告诉我,免疫系统是人体内一支强大的防御力量,能够识别和消灭病原体、肿瘤细胞等异常细胞。
然而,在某些疾病状态下,免疫系统的作用受到抑制,导致病情恶化。
为了解决这一问题,我将免疫学原理应用于细胞治疗技术,以增强免疫系统的功能。
细胞治疗技术是一种利用细胞来治疗疾病的方法。
在我的研究中,我主要关注两种类型的细胞:干细胞和免疫细胞。
干细胞具有多能性,可以分化为各种类型的细胞,从而修复受损的组织和器官。
免疫细胞,如T细胞、B细胞和自然杀伤细胞(NK细胞),则具有识别和消灭异常细胞的能力。
我将免疫学原理与细胞治疗技术相结合,从患者身上采集免疫细胞,经过体外培养和修饰,使其具有更高的识别和消灭异常细胞的能力。
然后,将这些修饰后的免疫细胞回输到患者体内,以增强其免疫系统。
我还将干细胞与免疫细胞结合,利用干细胞的分化能力,修复受损的免疫系统,进一步提高患者的免疫功能。
在我的研究中,免疫学与细胞治疗技术的结合已经取得了一系列突破性成果。
这种结合可以用于治疗癌症。
通过修饰T细胞,使其具有识别和消灭肿瘤细胞的能力,可以有效降低肿瘤负荷,提高患者生存率。
结合干细胞治疗,可以修复受损的免疫系统,进一步提高治疗效果。
除了癌症治疗,免疫学与细胞治疗技术的结合还可以应用于其他疾病。
例如,在自身免疫性疾病中,通过调节免疫细胞的活性,可以减轻炎症反应,缓解病情。
在移植医学中,结合免疫细胞治疗,可以降低移植排斥反应,提高移植成功率。
尽管免疫学与细胞治疗技术的结合取得了一系列成果,但仍然面临一些挑战。
细胞治疗技术的疗效和安全性需要进一步验证。
免疫细胞的修饰和培养过程需要优化,以提高其识别和消灭异常细胞的能力。
个体化的治疗方案也需要进一步研究,以适应不同患者的需求。
免疫学与细胞治疗技术的结合,为现代医学领域带来了一场革命。
作为这一领域的忠实拥护者,我深感其潜力无限,为众多疾病患者带来了希望之光。
在这里,我将以第一人称的视角,深入探讨免疫学与细胞治疗技术结合的原理、应用及其前景。
医学免疫学(第八版)免疫细胞

概述
巨噬细胞能够吞噬并消化多种抗原,并将抗原信息通过MHC分子转递给淋巴细胞。
功能
巨噬细胞通过其表面的受体识别并吞噬抗原,然后在细胞内将抗原降解成短肽,与MHC分子结合后表达于细胞表面,供T细胞识别。
作用机制
巨噬细胞
B淋巴细胞抗原提呈细胞是B淋巴细胞的特化亚型,能够摄取并转递抗原信息给T细胞。
分类
免疫细胞的定义和分类
免疫细胞能够识别并清除侵入机体的外来抗原,如细菌、病毒等。
识别和清除外来抗原
B淋巴细胞能够产生特异性抗体,参与体液免疫应答;T淋巴细胞能够产生多种细胞因子,调节免疫应答。
产生抗体和细胞因子
NK细胞等非特异性免疫细胞能够识别并杀伤受损或异常的自身细胞,维持内环境稳定。
杀伤和清除受损细胞
作用机制
抗原提呈细胞通过其表面的受体识别并摄取抗原,然后在细胞内将抗原降解成短肽,与MHC分子结合后表达于细胞表面,供T细胞识别。这一过程对于免疫应答的启动和调控至关重要。
抗原提呈细胞的功能和作用机制
04
CHAPTER
粒细胞和单核细胞
总结词
主要负责非特异性免疫的防御机制
功能和作用机制
中性粒细胞是白细胞中的主要成分,通过吞噬作用清除病原体和坏死组织。它们在感染、炎症和组织损伤等情况下迅速到达受损部位,发挥非特异性免疫作用。
功能和作用机制
B淋巴细胞可分为前B淋巴细胞和成熟B淋巴细胞。前者在骨髓中分化,后者则迁移到外周淋巴器官。
分类
NK细胞是固有免疫应答的重要组成部分,能够直接杀伤某些肿瘤细胞和被病毒感染的细胞。
功能和作用机制
活性调节
其他功能
关于干细胞的知识点总结

关于干细胞的知识点总结### 1. 干细胞的基本知识#### 1.1 干细胞的定义干细胞是一种具有自我更新和分化为多种细胞类型潜能的细胞。
它们可以通过不同的分化途径产生特定类型的细胞,例如心脏细胞、神经元和肌肉细胞。
干细胞的特点是具有自我更新的能力,即可以不断地分裂产生新的干细胞,同时可以分化为多种不同的细胞类型。
#### 1.2 干细胞的来源干细胞可以从多种来源获得,包括胚胎、胎儿、成体组织和实验室中的细胞。
胚胎干细胞是最早被发现的干细胞类型,它们来自胚胎内部的内细胞团,具有最广泛的分化潜能。
成体干细胞来源于成熟组织或器官中的特定位置,具有较为有限的分化潜能。
实验室中可以通过诱导多能干细胞(iPSCs)技术将成体细胞重新编程成具有干细胞特性的细胞。
#### 1.3 干细胞的分类根据其潜能和来源,干细胞可以分为多种类型。
根据其分化潜能可分为全能干细胞(pluripotent stem cells)、多能干细胞(multipotent stem cells)和单能干细胞(unipotent stem cells)。
全能干细胞能够分化为除胎盘细胞外的所有体细胞类型,如胚胎干细胞和诱导多能干细胞。
多能干细胞只能分化为某一种或某几种细胞类型,如造血干细胞和神经干细胞。
单能干细胞只能分化为同一种细胞类型,如肝细胞和皮肤细胞。
### 2. 干细胞的应用#### 2.1 干细胞在医学上的应用干细胞在医学上有广泛的应用,可以用于治疗各种疾病和损伤。
例如,造血干细胞可以用于治疗白血病和其他血液疾病,神经干细胞可以用于治疗神经退行性疾病,肌肉干细胞可以用于肌肉再生和修复。
胚胎干细胞和诱导多能干细胞还可以用于体外器官的再生和修复。
#### 2.2 干细胞在科研中的应用干细胞在科研中也有重要的应用,可以用于研究细胞分化和发育、基因调控、疾病模型和药物筛选。
通过对干细胞的培养和分化,可以获得大量的特定细胞类型,为细胞和分子生物学研究提供了重要的工具。
什么叫干细胞(细胞生物学)(二)

引言概述:干细胞是一类具有自我复制和分化能力的细胞,它们能够分化成多种细胞类型,并具备修复和再生受损组织的潜力。
本文将深入探讨什么叫干细胞,探索其在细胞生物学中的重要性和用途。
正文内容:一、干细胞的定义及特点:1.干细胞的定义:干细胞是具有自我复制和多向分化能力的细胞,能够产生多个不同类型的细胞。
2.干细胞的特点:自我复制、分化能力、长寿性等。
二、干细胞的来源:1.胚胎干细胞:来自胚胎早期的内细胞团,具备全能性,即能分化成体内的各种细胞类型。
2.成体干细胞:存在于成体组织中的一类细胞,如骨髓干细胞、脂肪干细胞等,具有有限的分化潜能。
3.诱导多能性干细胞(iPS细胞):通过基因重编程技术将成体细胞重新转化为类似胚胎干细胞的多能性细胞。
三、干细胞的分类:1.基于分化能力:全能性干细胞和多能性干细胞。
2.基于来源:胚胎干细胞和成体干细胞。
3.基于特征:表面标记和基因表达特征等。
四、干细胞的应用领域:1.组织工程和再生医学:利用干细胞修复和再生受损组织,为疾病治疗提供新的替代方案。
2.药物开发与筛选:干细胞可用于体外模型建立,加速药物的研发,毒性筛选等。
3.疾病研究:干细胞可以用于模拟疾病发生和发展过程,解析疾病机制。
4.基础研究:干细胞作为研究细胞生物学和发育生物学的重要工具,用于探究细胞分化、分裂与发育等过程。
5.个体化医疗:利用干细胞技术针对个体的特殊需求进行定制化治疗,提高治疗效果。
五、干细胞研究的挑战与前景:1.挑战:伦理问题、安全性问题、细胞纯度问题等。
2.前景:干细胞在医学和科学领域的广泛应用前景巨大,将为人类健康事业带来深刻的变革。
结论:干细胞作为一类具有自我复制和分化能力的细胞,在细胞生物学中起着重要作用。
通过研究干细胞的定义、特点、来源、分类以及应用领域,我们可以更好地理解干细胞的重要性和潜力,并为干细胞研究的发展提供参考和指导。
虽然干细胞研究还面临一些挑战,但展望未来,干细胞技术将为医学和科学领域带来革命性的突破,为人类的健康问题提供更有效的解决方案。
免疫细胞包括哪三类

免疫细胞包括哪三类
免疫细胞有淋巴细胞、肥⼤细胞、单核吞噬细胞系统。
免疫细胞主要是指能识别抗原,产⽣特异性免疫应答的淋巴细胞,因免疫细胞的存在我们才能够⾃我恢复,并杀死外来的⼀些抗原物质等,从⽽达到保护⾃⾝机能的作⽤。
1免疫细胞
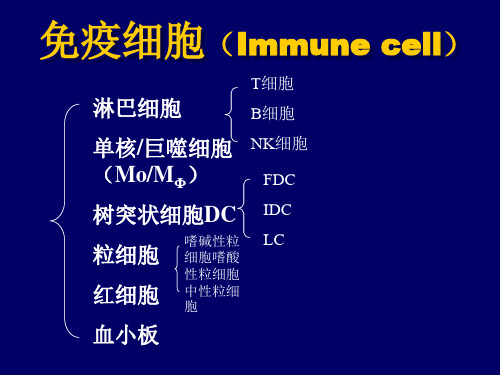
淋巴细胞
淋巴细胞是免疫系统的基本成分,在体内分布很⼴泛,主要是T淋巴细胞、B淋巴细胞受抗原刺激⽽被活化,分裂增殖、发⽣特异性免疫应答。
除T淋巴细胞和B淋巴细胞外,还有K淋巴细胞和NK淋巴细胞,共四种类型。
T淋巴细胞是⼀个多功能的细胞群。
除淋巴细胞外,参与免疫应答的细胞还有浆细胞、粒细胞、肥⼤细胞、抗原呈递细胞及单核吞噬细胞系统的细胞。
肥⼤细胞结构:细胞呈圆形或卵圆形,细胞核⼩,呈圆形或椭圆形,染⾊浅,位于细胞中央。
细胞常成堆或单个分布于⾎管附近。
细胞呈圆形或卵圆形,细胞质中充满⼤⼩⼀致、染成蓝紫⾊的颗粒,均匀分布在核周围。
功能:分泌多种细胞因⼦,参与免疫调节(TB细胞,APC细胞活化)。
表达MHC分⼦,B7分⼦,具有APC功能。
表达⼤量的IgEFc受体,释放过敏介质。
具有弱吞噬功能。
吞噬细胞:具有吞噬功能,包括巨噬细胞和中性粒细胞。
①巨噬细胞:具有强⼤的吞噬功能,可吞噬和杀伤体内病原体(细菌、真菌、寄⽣⾍、病毒)和清除体内凋亡的细胞和异物。
②中性粒细胞:有很强的吞噬和清除作⽤,且对化脓性细菌吞噬作⽤强。
⾎液中有⼤量的中性粒细胞存在,且能通过⾎循环迅速动员⾄病原体⼊侵部位。
机体在细菌感染尤其是化脓菌感染时,中性粒细胞数量往往快速增加。
免疫细胞介绍

T细胞的亚群及功能
Th1
Th2
产生的细胞因子
IL-2
++++
—
IL-4
—
++++
IL-5
—
++++
IL-10
—
+++
IFN-
++++
—
TNF-
+++
—
增殖所需细胞因子 IL-2源自IL-2/IL-4辅助作用
形成IgG促进DTH 形成IgE/IgA
抑制作用
Th2
Th1
Th1细胞分泌细胞因子的作用
FasL基因
CTL
粒酶
FasL
Fas
TCR 穿孔素
未活化ICE
靶细胞
活化ICE
ICE底物
P34cdc2 (凋亡)
CTL的细胞毒作用机制
Ts细胞的特性
抑制性T细胞(Ts)直接作用于CD4T细胞,B细胞和抗原提呈细胞 (TsF)
对胸腺内不能形成耐受的自身反应性T细胞克 隆有抑制作用
CD4与CD8细胞的效应特性
T细胞表面受体TCR-CD3
T细胞的其它受体
绵羊红细胞受体(CD2或IFA-2) 细胞因子受体
IL-1R IL-2R IL-4R IL-6R IL-7R
丝裂原受体(COn-A PHA PWM) HIV受体(CD4)
T细胞受体的相应CD分子
细胞因子受体 CD25(IL-2 R)、CD115(M-CSFR)、CDw116(GM-CSFR) CDw119(IFN-R)、CD120(TNF-R)、CDw121(IL-1R) CD122(IL-2R)、CDw124(IL-4R)、CD126(IL-6R)
细胞医疗知识点总结

细胞医疗知识点总结一、细胞医疗的基本概念细胞医疗是一种基于细胞的治疗手段,通过利用患者自身的细胞或来源于外部的细胞来治疗疾病。
它与传统的药物治疗相比,具有针对性强、副作用小、疗效持久等优势。
细胞医疗的核心就是利用细胞的自我修复、增殖以及功能发挥的能力,来实现对疾病的治疗。
二、细胞医疗的应用领域细胞医疗在临床上有着广泛的应用领域,包括但不限于以下几个方面:1. 干细胞治疗:干细胞可以分化为多种细胞类型,包括心肌细胞、神经细胞、肝细胞等,因此在心脑血管疾病、神经系统疾病以及肝脏疾病的治疗中具有重要作用。
2. 免疫细胞治疗:免疫细胞包括T细胞、B细胞、自然杀伤细胞等,它们在免疫系统的监控和调节中发挥着关键作用,因此在免疫缺陷病、肿瘤、传染病等方面具有重要价值。
3. 肝细胞移植:对于患有严重肝病的患者,通过移植健康的肝细胞可以帮助患者重建肝脏功能。
4. 其他:除了上述的几个方面,细胞医疗还可以应用于骨髓移植、糖尿病治疗、软骨修复、皮肤再生等领域。
三、细胞医疗的主要技术细胞医疗的主要技术包括干细胞培养、细胞工程、基因编辑、细胞移植等。
其中,干细胞培养是细胞医疗的基础技术,通过培养和扩增干细胞,可以获得足够数量且具有特定功能的细胞;细胞工程技术则是对细胞进行功能性改造,以实现特定治疗目的;基因编辑技术则是对细胞进行基因的修饰和调控,以增强其治疗效果;细胞移植技术则是将培养好的细胞移植到患者体内,实现疾病治疗。
四、细胞医疗的发展现状目前,细胞医疗已经在一些领域取得了突破性进展。
比如,干细胞治疗已经成功应用于心肌梗死、帕金森病等疾病的治疗;免疫细胞治疗在肿瘤领域也取得了一定的成果;基因编辑技术更是开启了治愈一些遗传性疾病的大门。
此外,细胞医疗还在临床试验阶段探索应用于更多的疾病领域。
五、细胞医疗的前景展望随着科技的不断进步和临床经验的积累,细胞医疗将有望在更多领域发挥作用,甚至成为治愈一些难治疾病的关键手段。
未来,细胞医疗还会面临一些挑战与问题,比如治疗效果的长期观察、安全性问题、成本问题等,需要不断的研究和探索解决方案。
造血干细胞及免疫细胞的生成

B细胞在骨髓的发育
B细胞发育 的两个阶段
免疫应答的特异性 (specificity)
抗原受体基因结构及其重排
TCR和BCR(Ig)的胚系基因结构 淋巴细胞发育过程中抗原受体基因重排
人免疫球蛋白基因定位
定位于非淋巴组织 血液脾脏中有
记忆性T 细胞的产生
Tcm:来源于刚活化Tn---Ta---无适当刺激信号---不成为 Te---无AICD---返回静息状态并存活成为Tcm.
Tn—IL-2(高)—分泌IFN-—Tc Tn—IL-2(低)或IL-15(高)—维持中间状态,保 留CCR7—Tcm Tem:Ag 刺激—Ta—95%AICD,少部分细胞缺乏抗原的 持续刺激,难于启动 AICD得以存活,成为记忆细胞。 如脑膜炎病毒刺激 T细胞研究发现:病毒滴度高: 有强的初次应答,弱的回忆反应,原因是AICD导致 CD8Tc过度耗竭;病毒滴度低,有弱的初次应答,强的 回忆反应。
MHC-I →DP细胞表面CD8分子结合
导致CD4分子 表达关闭
CD4-CD8+细胞
MHC-II →DP细胞表面CD4分子结合
导致CD8分子 表达关闭
CD4+CD8-细胞
T细胞发育的阴性选择-获得自 身耐受性
树突状细胞和巨噬细胞表达高水平的 MHC-I和MHC-II类抗原,并与自身抗原 形成复合物,SP细胞如能识别自身抗原 肽-MHC复合物,即发生凋亡,否则继续 发育成熟,保证进入外周淋巴器官的T细 胞库中不含有针对自身抗原成分的T细胞。
Ig的合成和肽链转运
TCR基因重排
围绕TCR成熟发生一系列基因的有序表达 和关闭:
第十二章-造血干细胞及免疫细胞的生成

CD3+ CD4‾ CD8+ TCRgd+
CD3+ CD4‾ CD8‾ TCRgd+
CD3+ CD4+ CD8+ TCRab+
CD3+ CD4‾ CD8‾ TCRgd+
CD3+ CD4+ CD8‾ TCRab+
CD3+ CD4‾ CD8+ TCRab+
10/31/2024
CD3+ TCRgd+
CD3+ CD4+ TCRab+ CD3+ CD8+ TCRab+
人造血干细胞的主要表面标记为CD34和 c-kit(CD117),无谱系特异性标记(Lin-):
1.CD34 是造血干细胞的一种重要标记分
子,为高度糖基化跨膜蛋白,包括造血干 细胞,有1%~4%骨髓细胞表达CD34。应 用CD34可从造血组织中分离造血干细胞, 成熟血细胞不表达此分子。
10/31/2024
单位10/31(/202C4 FU-MeG)
▶定向干细胞及其分化 :
1.髓样干细胞及其分化:
Ⅲ 粒单系:GM-CSF、 SCF、IL-3起作用。
髓样干细胞→具有产生粒细胞系、 红细胞系、巨核细胞系和单核巨噬细胞系潜能的集落形成单位 (CFU-GEMM)→(在GCSF/M-CSF/GM-CSF、SCF、 IL-3存在下)→中性粒细胞或单 核/巨噬细胞。
10/31/2024
▶定向干细胞及其分化 :
1.髓样干细胞及其分化:
Ⅳ嗜酸性粒细胞: GMCSF、IL-5、IL-3起作 用。
髓样干细胞→CFU-GEMM(在 GM-CSF、IL-5、IL-3存在下) →嗜酸粒细胞集落形成 单位 (CFU-Eos) →嗜酸性粒细胞
干细胞库,免疫细胞与干细胞的区别

什么是干细胞库,干细胞实体库,干细胞资料库?干细胞库是在约为-196℃液氮中(深低温)储存干细胞或相关资料的场所。
一个完善的干细胞库应具备随时随地将健康干细胞提供临床使用的能力。
按所储存的干细胞来源和采集方式,干细胞库分为脐血干细胞库、骨髓和外周血干细胞库。
脐血干细胞库所做的工作是将新生儿的脐血采集后经过分离冷冻并储存起来。
在每份脐血中,大约含数百万个干细胞,足够供一个幼儿或少年患者使用。
如果是在成年后发病,一份脐血所提供的干细胞数量就不够用了,但是将来可以通过干细胞的扩增技术得到解决。
骨髓和外周血干细胞库可分为资料库和实物库。
资料库所做的工作是将健康者提供的骨髓或外周血干细胞进行HLA配型和资料登记,待需要时再采集其骨髓。
实物库则是在进行细胞配型和资料登记的同时,采集和储存健康提供者可供移植用的骨髓或外周血干细胞。
干细胞库按提供方式又分为公共库和自体库。
公共库所储存的干细胞是他人的干细胞,以满足需要移植但自体干细胞没有被保存的病人的需求。
自体库则是储存在自己出生或健康时采集的部分干细胞,以备自己生病时用。
目前,自体脐血储存多由父母为子女来做。
目前我国的干细胞库主要有中国造血干细胞捐献者资料库和脐血库。
这两类干细胞库的不同在于,中国造血干细胞捐献者资料库(中华骨髓库)是中国红十字会发起建立的,主要对自愿捐献者进行白细胞抗原配型和资料登记,将来需要时再采集骨髓,是一种资料库。
脐血库是实物库,即通过对新生儿脐血进行配型和资料登记,同时采集储存可供移植用的干细胞,一旦需要,这些干细胞即可用于临床移植。
资料库的建库方法,主要是对捐献者进行白细胞抗原配型,HLA抗原(白细胞抗原)是人类主要组织相容性复合物抗原。
它们与同种异体移植中的排斥反应有密切关系。
HLA是由 HLA基因复合体所编码的产物,HLA复合体是人类中最复杂的基因复合体,其遗传主要特点是共显性复等位基因遗传,是调节人体免疫反应和异体移植排斥作用的一组基因,位于第六号染色体的短臂上。
什么是干细胞

什么是干细胞作者:伟东生物干细胞因有如同树干能够分化的超强属性,以此又称之为“万能细胞”。
当我们的人体还在成长时,干细胞作为细胞王国的建设者,通过分化源源不断提供新生细胞,增加我们身体细胞的数量;当我们成年后,人体外形基本固定,无需再继续增长时,干细胞又会承担起细胞王国维护者的角色,及时替换和更新衰老或受损的细胞。
免疫细胞是防卫者免疫细胞作为王国内部的防卫兵,则是起到内清叛变(正常细胞突变成的癌细胞)外剿夙敌的作用,当有外敌入侵,如细菌和病毒,免疫细胞就会扮演细胞王国的军队,快速反应,将其清除。
如果细胞王国中出现叛变分子,如正常细胞突变为癌细胞,免疫细胞就会扮演安保系统,将其识别并清除。
然而,当外敌入侵过多,或王国内叛变分子太多,免疫细胞没有能力全部清除时,我们的身体就会生病。
不幸的是,当我们不断变老(30岁以后),体内干细胞和免疫细胞的数量及活力均会不断减弱。
幸运的是,科学家开发了基于干细胞和免疫细胞的生物医学技术,为我们的健康保驾护航。
综上,我们的身体生病的原因大致也就是两种,敌人太强或者自己太弱。
为了更好的建设及保卫细胞王国,干细胞和免疫细胞内部商议后进行了更详尽的职能细分。
按照分化潜能分类,干细胞分为:全能干细胞、多能干细胞和专能干细胞。
如果把人体比喻为一棵树,深埋大地的种子就是全能干细胞,就如同种子可以发育成长为一颗参天大树;大树的主要枝干可以比喻为多能干细胞,主要成员间充质干细胞,可以分化为神经细胞、心肌细胞、肝细胞、肌肉细胞、软骨细胞、成骨细胞、脂肪细胞、血管内皮细胞等多系统的功能细胞,就如同每个树冠能生出的葱郁的枝桠、树叶和果实;末端的枝干是专能干细胞,例如上皮组织基底层干细胞、肌肉中的成肌细胞等,这批干细胞专项供给给未端枝干充足的能量用以开枝散叶。
人体成熟的功能细胞,如皮肤细胞,心肌细胞、肾细胞等,就如同大树枝桠末端的叶子和果实,随着季节的变化不断凋零,需要干细胞不断分化补充和更新,以维持生命的运转。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
干细胞和免疫细胞的差别,您有必要了解一下!
我们的身体是一个由细胞构成的王国,极其精密复杂,同时又高度有序。
任何伟大的王国都既需要能干建设者,也需要勇猛防卫兵。
我们身体细胞王国也不例外。
简单来说,干细胞就是建设者,免疫细胞则是防卫兵!
干细胞是建设者
干细胞是构筑人类形态的原始细胞,通过分化源源不断地提供新生细胞,根据需要发育成人体内各种类型的组织和器官。
当我们成年后身体不再成长,干细胞又会扮演细胞王国的维护者,及时替换和更新衰老或受损的细胞。
因为数量非常丰富,可塑性极强,又被医学界称为“万能细胞”。
免疫细胞是防卫兵
当有外敌入侵,如细菌和病毒,免疫细胞就会扮演细胞王国的军队,快速反应,将其清除。
如果细胞王国中出现叛变分子,如正常细胞突变为癌细胞,免疫细胞就会扮演安保系统,将其识别并清除。
但是,当外敌入侵过多,或王国内叛变分子太多,免疫细胞没有能力全部清除时,我们的身体就会生病。
不幸的是,当我们慢慢衰老,体内干细胞和免疫细胞的数量及活力均会不断减弱。
幸运的是,科学家开发了基于干细胞和免疫细胞的生物医学技术,为我们的健康保驾护航。
①干细胞与免疫细胞提取方式有何不同?
干细胞可以从多种人体组织中提取。
以目前临床应用最广泛的间充质干细胞为例,最初是从骨髓中提取的,后来在新生儿脐带、脂肪、牙髓等多种人体组织都能提取到。
研究发现,新生儿出生后带来的脐带胎盘中有非常丰富的干细胞,使用和提取对新生儿和妈妈都没有任何伤害,并且在用于治疗各类难治重病时,有非常好的效果和潜力。
而牙髓干细胞可以来自小孩的乳牙或成人的智齿等,相较于一生只能存储一次的脐带间充质干细胞,给大家提供了更多的存储机会。
目前,免疫细胞的来源主要是血液,包括成人的外周血和婴儿的脐带血。
血液中含有大量功能成熟的免疫细胞,在我们的身体内不停循环,时刻保护我们的健康。
其用途广泛,前景广阔,为未来免疫细胞技术研究突破储备生命资源。
②干细胞储存or免疫细胞储存
这两种细胞都是体内的活细胞,如果要长期保存它们的细胞活性就需要低温存储。
也就是存放在-196℃的液氮中,它们的技术是相同而且成熟的。
干细胞干细胞主要是修复与再生功能。
提取出来的间充质干细胞冷冻保存后仍具有多向分化潜能,可作为理想的种子细胞,用于衰老和病变引起的组织器官损伤修复。
干细胞保健,就是把之前冻存的干细胞拿出来,像种子一样进行复苏,扩增培养,用来修复机体的一些功能,当然也包括抗衰老。
干细胞在多个方面参与抗衰老,包括分化成免疫细胞,对抗内外环境的干扰;参与代谢调节,维持机体的内在平衡;通过控制炎症和修复组织,预防各种慢性疾病。
免疫细胞自体免疫细胞储存是指采用细胞冻存技术把健康成人最佳状态的优质免疫细胞储存起来,保存年轻时的活力,一旦机体免疫系统需要,体外复苏细胞,通过相关生长因子刺激、诱导,大量扩增后回输体内,帮助机体调理免疫系统并恢复健康。
免疫细胞保健,就是把存储好的自己的免疫细胞,扩增回输到体内,提高免疫技能。
总之,不管是免疫细胞还是干细胞,都有能力影响我们的衰老和健康,使亚健康和疾病远离我们。
换句话说,只要保持我们体内的细胞持续更新,足够强壮,就可以实现延缓衰老和健康长寿的目的。
即使是自然衰老,也能使衰老的过程变得更加健康和快乐。
