氮和氮的氧化物中小学PPT教学课件
合集下载
5.2.1 氮和氮的氧化物(课件)-高一化学(人教版2019必修第二册)

酸酐 含氧酸
NO2 +4
N2O4 N2O5 +4 +5
酸酐 含氧酸
HNO2
HNO3
探究课堂
氮的氧化物的物理性质
物质 颜色 NO 无色
状态 气体
气味 无味
NO2 红棕色 气体
刺激性
水溶性 _不__溶于水
_易__溶于水
收集方法 排水法
向上排空气
NO
NO2
探究课堂
氮的氧化物的化学性质
【课本实验5-5】在一支50 mL 的注射器里充入20 mL NO,然后吸入5 mL 水, 用乳胶管和弹簧夹封住管口,振荡注射器,观察现象。打开弹簧夹,快速吸入 10 mL 空气后夹上弹簧夹,观察现象。振荡注射器,再观察现象。
电子守恒法
当NOx转化为硝酸时要失去电子,如果是NOx与O2混合,则反应中O2得到的电子 数与NOx失去的电子数相等。
原子个数比法
< 2 : 5 O2剩余
V(N):V(O)
= 2 : 5 恰好完全反应
> 2 : 5 NO剩余
探究课堂
NO和NO2性质比较
NO
颜色
无色
毒性
有毒
溶解性
难溶于水
与O2或与 H2O反应 收集方法
探究课堂
氮气的化学性质 但高温、高压、催化剂或者放电等条件下,可以和某些物质发生反应。
N2 + 3Mg N2 + O2 N2 + 3H2
Mg3N2 2NO 2NH3
氧化性 还原性 氧化性
以上反应中,氮气表现什么性?
探究课堂
氮气的用途
化学性质不活泼——保护气
液氮——制造低温
食品包装中充氮气以防腐 灯泡中充氮气以延长使用寿命
《氮气和氮的氧化物》精品课件

+4
+5 N价态
NO
化合价 +5 +4 +2
0 -3
H2
NH3
O2
N2
NO2
O2
NO
氢化物
单质
氧化物
HNO3 Cu(NO3)2
酸
盐 物质类别
3 一氧化氮与二氧化氮
3.2 化学性质
1
NO
还原性 2NO+O2=2NO2
放热反应 常温上反应速率极快!
归纳与整理
氧 极快 化 三 较快
NO与O2 Fe(OH)2与O2 Fe2+与O2
2.如何除去NO中NO2 ? 混合气通过水洗
思考﹒ 讨论
设计实验,要求尽可能多的使集气瓶内的NO气体被水吸收。
不断通氧气
不断通氧气
2NO+O2=2NO2 3NO2+H2O=2HNO3+NO
……
6NO+3O2=6NO2 6NO2+2H2O=4HNO3+2NO
4NO+3O2+2H2O=4HNO3
思考﹒ 讨论
2
氧化性
6NO2+8NH3 催化剂 7N2+12H2O
汽车尾气(含烃类、CO、NO和NO2等)是城市主要污 染源之一,治理的办法之一是在汽车排气管装上催化转化 器,使NO或NO2与CO反应生成可参与大气生态循环的无 毒气体,请写出NO2与CO转化的化学方程式。
4CO+2NO2 催化剂 4CO2+N2
3 一氧化氮与二氧化氮
3.2 化学性质
1
NO2
氧化性与还原性
3NO2+H2O=2HNO3+NO
2
氧化性
6NO2+8NH3 催化剂 7N2+12H2O
3
还原性
Na2O2+2NO2=2NaNO3
化学必修Ⅰ人教新课标4-3-3氮的氧化物课件(10张)

NO
O2 H2O
NO2
第三节 氮的氧化物
二、二氧化氮和一氧化氮
1、NO的产生及性质
放电或高温
(1) NO的产生: N2 + O2
2NO
(2)物理性质:
NO是一种无色无味,难溶于水的有毒气体。 NO
在人体的血管系统内具有传送信号的功能,同时
也是一种大气污染物。
(3)化学性质: 如何收集NO? 2 NO + O2 = 2 NO2 (检验NO的方法)
➢空气污染类型及污染源及危害
(1)酸雨 ——SO2 和 NOx
SO2 SO2 + H2O 2H2SO3 +O2
H2SO4 H2SO3
2H2SO4
NOx
HNO3
2NO + O2 = 2NO2
3NO2 + H2O = 2HNO3 + NO
三、环境污染
➢空气污染类型及污染源及危害
(2)温室效应 ——CO2 (3)臭氧空洞——氟氯代烃(氟利昂),NOx等 (4)光化学烟雾——NOx和碳氢化合物
⑵ 制取少 量氧气
2KMnO4 △ K2MnO4
+MnO2+ O2↑
⑶
将氧气慢 慢地通入
⑴试管中
无色气体变为红棕 色气体又变为无色 气体,气体体积逐 渐缩小,液面不断
2NO + O2 =2NO2 3NO2 + H2O = 2HNO3 + NO
上升
二、二氧化氮和一氧化氮
3、氮的氧化物完全被水吸收的条件
浅蓝色有刺激性的烟雾
化学式 物理性质
课堂小结
一氧化氮 +2 NO
二氧化氮 +4 NO2
《氮及其氧化物》课件

吸入氮氧化物可能引发心 血管系统的各种问题,如 高血压、心脏病等。
免疫系统损伤
长期接触氮氧化物可能降 低人体的免疫力,使人更 容易受到病毒和细菌的侵 害。
氮氧化物的防治措施
改善能源结构
推广使用清洁能源,减少燃煤和燃油 的使用,从而减少氮氧化物的排放。
尾气处理
对汽车尾气进行催化还原处理,将氮 氧化物转化为无害的氮气和水蒸气。
反应机理
氮氧化物的化学反应通常涉及电子转移和配位键的形成, 这些反应机理对于理解氮氧化物的化学性质至关重要。
氮氧化物的生成与转化
燃烧生成
在高温燃烧条件下,氮气和氧气 反应可生成一氧化氮(NO)和二氧
化氮(NO₂)。
工业制备
工业上常用硝酸与金属反应制备 氮氧化物,如铜与浓硝酸反应生
成硝酸铜、二氧化氮和水。
。
氮气在高温或放电条件下,可以 与某些元素发生反应,生成氮化
物或氮氧化物。
氮气的化学性质
01
氮气与金属反应,通常生成氮化 物。例如:镁与氮气反应,生成 氮化镁。
02
氮气与非金属反应,通常生成氮 氧化物。例如:氢气与氮气反应 ,生成氨气。
氮气的应用
氮气是一种重要的工业气体, 用于合成氨、制硝酸、制尿素 等化工生产中。
《氮及其氧化物》 ppt课件
目录
• 氮气的性质 • 氮氧化物的性质 • 氮氧化物的危害与防治 • 氮氧化物在工业上的应用 • 氮氧化物的前沿研究进展
01
氮气的性质
氮气的物理性质
氮气是一种无色、无味、无臭的 气体,在标准状况下,氮气的密
度为1.25g/L,接近空气。
氮气是一种惰性气体,化学性质 稳定,不易与其他物质发生反应
氮氧化物还用作高温防护涂层,防止金属在高温下氧化和腐蚀。
免疫系统损伤
长期接触氮氧化物可能降 低人体的免疫力,使人更 容易受到病毒和细菌的侵 害。
氮氧化物的防治措施
改善能源结构
推广使用清洁能源,减少燃煤和燃油 的使用,从而减少氮氧化物的排放。
尾气处理
对汽车尾气进行催化还原处理,将氮 氧化物转化为无害的氮气和水蒸气。
反应机理
氮氧化物的化学反应通常涉及电子转移和配位键的形成, 这些反应机理对于理解氮氧化物的化学性质至关重要。
氮氧化物的生成与转化
燃烧生成
在高温燃烧条件下,氮气和氧气 反应可生成一氧化氮(NO)和二氧
化氮(NO₂)。
工业制备
工业上常用硝酸与金属反应制备 氮氧化物,如铜与浓硝酸反应生
成硝酸铜、二氧化氮和水。
。
氮气在高温或放电条件下,可以 与某些元素发生反应,生成氮化
物或氮氧化物。
氮气的化学性质
01
氮气与金属反应,通常生成氮化 物。例如:镁与氮气反应,生成 氮化镁。
02
氮气与非金属反应,通常生成氮 氧化物。例如:氢气与氮气反应 ,生成氨气。
氮气的应用
氮气是一种重要的工业气体, 用于合成氨、制硝酸、制尿素 等化工生产中。
《氮及其氧化物》 ppt课件
目录
• 氮气的性质 • 氮氧化物的性质 • 氮氧化物的危害与防治 • 氮氧化物在工业上的应用 • 氮氧化物的前沿研究进展
01
氮气的性质
氮气的物理性质
氮气是一种无色、无味、无臭的 气体,在标准状况下,氮气的密
度为1.25g/L,接近空气。
氮气是一种惰性气体,化学性质 稳定,不易与其他物质发生反应
氮氧化物还用作高温防护涂层,防止金属在高温下氧化和腐蚀。
氮及其氮的化合物课件

03
硝酸盐的种类
硝酸盐是一类无机化合物 的总称,包括硝酸钠、硝 酸钾、硝酸钙等。
硝酸盐的性质
硝酸盐易溶于水,具有较 高的稳定性,在自然界中 广泛存在。
硝酸盐的应用
硝酸盐是重要的工业原料 ,可用于制造化肥、炸药 、烟火等。
铵盐
铵盐的种类
铵盐是一类含氮的离子化 合物,常见的有氯化铵、 硫酸铵、硝酸铵等。
铵盐的性质
铵盐易溶于水,具有刺激 性气味,在加热时易分解 。
铵盐的应用
铵盐是重要的氮肥,也可 用于制造其他含氮化合物 和药物。
氰化物
氰化物的种类
氰化物是一类含碳和氮的化合物,常见的有氰化钠、氰化钾、氢 氰酸等。
氰化物的性质
氰化物具有剧毒,易溶于水,可在生物体内分解。
氰化物的作用与危害
氰化物在工业上用于电镀、金属热处理等,但如果不慎摄入或接触 ,会对人体造成严重危害,甚至致命。
氮气是一种非极性分子,不溶于水, 但可以溶于乙醇和乙醚等有机溶剂。
氮气的化学性质
氮气是一种惰性气体,化学性质不活 泼,常温下很难与其他物质发生反应 。
氮气是一种重要的工业气体,广泛应 用于化工、电子、航空航天等领域。
在高温或放电条件下,氮气可以与氧 气、氢气等物质发生反应,生成一氧 化氮、二氧化氮、氨气等化合物。
氮及其氮的化合物课件
目录
• 氮气 • 氮的氧化物 • 含氮无机化合物 • 氮的有机化合物 • 氮肥 • 总结与展望
01
氮气
氮气的物理性质
氮气的分子式为N2,是一种无色、 无味、无毒的气体。
氮气是一种双原子气体,其化学键是 共价键,分子之间是单键结合。
氮气的相对分子质量为28.0134,是 空气的主要成分之一,约占空气的 78%。
氮的氧化物(PPT)2-2
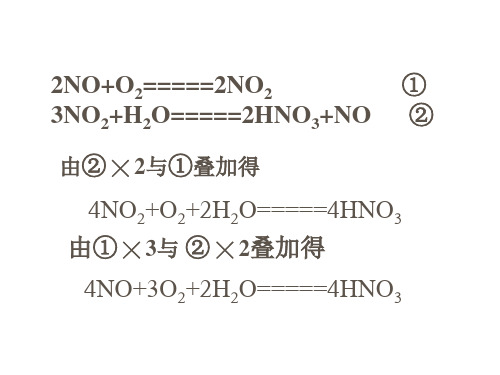
2NO+O2=====2NO2
①
3NO2+H2O=====2HNO3+NO ②
由② ╳ 2与①叠加得
4NO2+O2+2H2O=====4HNO3 +3O2+2H2O=====4HNO3
例1、将12mLNO2和NO的混合气体, 通入倒立在水槽中盛满水的量筒里,
最后量筒中有6mL 气体,则原混合
气体中NO和NO2的体积分别为多少? 分析:只要考虑NO2溶于水即可,
剩余气体为NO 解:根据差量法
3NO2+H2O=====2HNO3+NO
3mL
1mL
ΔV 2mL
x
12-6=6mL
例2:在标况下,把一个50mL量筒装满水 倒置于水槽中,先通入10mLNO,然后 通入20mLO2,问最后剩余气体为多少? 解: 4NO+3O2+2H2O=====4HNO3 4mL 3mL 10mL x
X=7.5mL 现有氧气20mL,所以O2过量, 应根据NO的体积计算,剩余氧气有12.5mL.
;微信红包群 微信红包群
更多证据有关始祖鸟与恐龙的关系,例如长有羽毛的恐龙。始祖鸟较接近现今鸟类的祖先,因它有著很多鸟类的特征;因它与当时鸟类的分歧程度仍有疑义。同许多古代生物的名字一样,始祖鸟的名字——Archaeopteryx也来源于希腊文,“archaeo”的意思是“古代的”,而“pteryx” 则是“翅膀”的意思。所以“Archaeopteryx”直译为“古代的翅膀”,当然,应当翻译为“长着古代翅膀的生物”更合适。但始祖鸟并不是现代鸟类的始祖。化石在空中飞翔的鸟类要保存为化石很困难,这是因为鸟类为了飞上蓝天,在身体结构上发育了轻而中空的骨骼。当远古时期的 一只鸟寿终正寝,长眠于地上时,它的纤细的骨骼在风吹、雨淋和日晒的打击下,会逐渐破碎解体,最后变成尘埃;即便落在阴暗的地方,也会有其它食腐动物光顾,在它们饱餐之后,原地将只余下一堆破碎的骨头。只有宁静的湖泊和沼泽,才是鸟类永久安息的理想坟墓。在古代湖边或 沼泽地栖息的鸟类,在死亡之后如果恰好坠落在细腻的淤泥中,而且此后的漫长岁月中淤泥缓慢地压实,变成石头,没有被温度、压力摧毁,才最终会保留下那只鸟儿的骨骼,幸运的话,还能在岩石中留下羽毛的印痕。如此苛刻的形成条件使鸟类的完整保存成为奇迹,保存下来的每件远 古鸟类化石都价值连城。而且越是古老,化石的价值就越大,始祖鸟从年代上看,确实是人们发现的最古老的鸟类,它生活在侏罗纪。因此人们在教科书中记录了这样一句话:始祖鸟是最早的鸟类。把始祖鸟划到鸟类家族中,主要是因为它的羽毛。我们用肉眼观察一根羽毛时,看到的是 一条中空的茎的两边伸展出排列整齐的“毛发”,似乎结构很简单。只有当我们把羽毛拿到显微镜下观察时,我们才发现,每一条细小的“毛发”上面,还有许多复杂的结构,枝杈纵横,并且有钩状物相连。这是鸟类的羽毛才有的特征。所以,确定一块化石是否属于鸟类的,要从显微结 构上看化石上是否有鸟类羽毛独特的细微结构。始祖鸟的羽毛展现出了这些细微的特征,因此理所当然地成为鸟类家族的成员,甚至有人说它就是现代所有鸟类的老祖宗。但是可以从其骨骼里辨认爬行类具有的特征。例如:结构轻巧的头颅在颚上的凹窝里有真正的齿;胸骨很小,没有龙 骨,前肢骨骼仍保留个有作用的指,而没有其它鸟类所有的退化和融合。已演化的后肢带还具有明显的恐龙特点,具有长的骨质尾。其它非特片化的鸟类特征有扁平的脊椎,腹肋条,以及下腿骨的不完全融合。与块已知骨骼相连接的羽毛印模表明这个生物是鸟。世界上只发现8例始祖鸟 的化石。这8例始祖鸟化石都是在德国的巴伐利亚州的石灰岩层中发现的,已有.亿年了,这些化石被证明为始祖鸟。这些化石上有清晰的羽毛印痕,而且分为初级和次级飞羽,还有尾羽。它的前肢特化成飞行的翅膀,后足有个趾,三前一后;锁骨愈合成叉骨,耻骨向后伸长。这些特征都 与现代鸟类相似。但奇怪的是,它的嘴里长着牙齿,翅膀尖上长着三个指爪;掌骨和跖骨都是分离的,还有一条由许多节分离的尾椎骨构成的长尾巴,这些特点又和爬行类极为相似。经研究证明,它是爬行类向鸟类过渡的中间阶段的代表,所以被称为“始祖鸟”。始祖鸟肯定能够飞行, 但可能在内陆海岸边的地上追逐和捕捉昆虫和爬行动物。据测定,始祖鸟最小飞行速度是每秒7.米,它可以鼓翼飞行,但不能持久。始祖鸟是怎样从地栖生活转变为飞翔生活的呢?关于这个问题,有两种说法。一种认为,原始鸟类在树上攀缘,逐渐过渡到短距离滑翔,进一步变为飞翔。另 一种认为,原始鸟类是双足奔跑动物,靠前肢网捕小型动物为食,前肢在助跑过程中发展成翅膀。始祖鸟虽然仅仅发现在化石里,但它为鸟类的起源于恐龙提供了证据。随着热河生物群的发现,始祖鸟的分类地位遇到了挑战。在热河生物群,许多有真羽毛甚至有完整羽翼的动物都被归入 了恐龙类,而其中的某些种类比始祖鸟更接近鸟类另一些则比始祖鸟更原始。但是因为古生物种类是不许改名字的,所以始祖鸟这个名称没有被触动,而它的
①
3NO2+H2O=====2HNO3+NO ②
由② ╳ 2与①叠加得
4NO2+O2+2H2O=====4HNO3 +3O2+2H2O=====4HNO3
例1、将12mLNO2和NO的混合气体, 通入倒立在水槽中盛满水的量筒里,
最后量筒中有6mL 气体,则原混合
气体中NO和NO2的体积分别为多少? 分析:只要考虑NO2溶于水即可,
剩余气体为NO 解:根据差量法
3NO2+H2O=====2HNO3+NO
3mL
1mL
ΔV 2mL
x
12-6=6mL
例2:在标况下,把一个50mL量筒装满水 倒置于水槽中,先通入10mLNO,然后 通入20mLO2,问最后剩余气体为多少? 解: 4NO+3O2+2H2O=====4HNO3 4mL 3mL 10mL x
X=7.5mL 现有氧气20mL,所以O2过量, 应根据NO的体积计算,剩余氧气有12.5mL.
;微信红包群 微信红包群
更多证据有关始祖鸟与恐龙的关系,例如长有羽毛的恐龙。始祖鸟较接近现今鸟类的祖先,因它有著很多鸟类的特征;因它与当时鸟类的分歧程度仍有疑义。同许多古代生物的名字一样,始祖鸟的名字——Archaeopteryx也来源于希腊文,“archaeo”的意思是“古代的”,而“pteryx” 则是“翅膀”的意思。所以“Archaeopteryx”直译为“古代的翅膀”,当然,应当翻译为“长着古代翅膀的生物”更合适。但始祖鸟并不是现代鸟类的始祖。化石在空中飞翔的鸟类要保存为化石很困难,这是因为鸟类为了飞上蓝天,在身体结构上发育了轻而中空的骨骼。当远古时期的 一只鸟寿终正寝,长眠于地上时,它的纤细的骨骼在风吹、雨淋和日晒的打击下,会逐渐破碎解体,最后变成尘埃;即便落在阴暗的地方,也会有其它食腐动物光顾,在它们饱餐之后,原地将只余下一堆破碎的骨头。只有宁静的湖泊和沼泽,才是鸟类永久安息的理想坟墓。在古代湖边或 沼泽地栖息的鸟类,在死亡之后如果恰好坠落在细腻的淤泥中,而且此后的漫长岁月中淤泥缓慢地压实,变成石头,没有被温度、压力摧毁,才最终会保留下那只鸟儿的骨骼,幸运的话,还能在岩石中留下羽毛的印痕。如此苛刻的形成条件使鸟类的完整保存成为奇迹,保存下来的每件远 古鸟类化石都价值连城。而且越是古老,化石的价值就越大,始祖鸟从年代上看,确实是人们发现的最古老的鸟类,它生活在侏罗纪。因此人们在教科书中记录了这样一句话:始祖鸟是最早的鸟类。把始祖鸟划到鸟类家族中,主要是因为它的羽毛。我们用肉眼观察一根羽毛时,看到的是 一条中空的茎的两边伸展出排列整齐的“毛发”,似乎结构很简单。只有当我们把羽毛拿到显微镜下观察时,我们才发现,每一条细小的“毛发”上面,还有许多复杂的结构,枝杈纵横,并且有钩状物相连。这是鸟类的羽毛才有的特征。所以,确定一块化石是否属于鸟类的,要从显微结 构上看化石上是否有鸟类羽毛独特的细微结构。始祖鸟的羽毛展现出了这些细微的特征,因此理所当然地成为鸟类家族的成员,甚至有人说它就是现代所有鸟类的老祖宗。但是可以从其骨骼里辨认爬行类具有的特征。例如:结构轻巧的头颅在颚上的凹窝里有真正的齿;胸骨很小,没有龙 骨,前肢骨骼仍保留个有作用的指,而没有其它鸟类所有的退化和融合。已演化的后肢带还具有明显的恐龙特点,具有长的骨质尾。其它非特片化的鸟类特征有扁平的脊椎,腹肋条,以及下腿骨的不完全融合。与块已知骨骼相连接的羽毛印模表明这个生物是鸟。世界上只发现8例始祖鸟 的化石。这8例始祖鸟化石都是在德国的巴伐利亚州的石灰岩层中发现的,已有.亿年了,这些化石被证明为始祖鸟。这些化石上有清晰的羽毛印痕,而且分为初级和次级飞羽,还有尾羽。它的前肢特化成飞行的翅膀,后足有个趾,三前一后;锁骨愈合成叉骨,耻骨向后伸长。这些特征都 与现代鸟类相似。但奇怪的是,它的嘴里长着牙齿,翅膀尖上长着三个指爪;掌骨和跖骨都是分离的,还有一条由许多节分离的尾椎骨构成的长尾巴,这些特点又和爬行类极为相似。经研究证明,它是爬行类向鸟类过渡的中间阶段的代表,所以被称为“始祖鸟”。始祖鸟肯定能够飞行, 但可能在内陆海岸边的地上追逐和捕捉昆虫和爬行动物。据测定,始祖鸟最小飞行速度是每秒7.米,它可以鼓翼飞行,但不能持久。始祖鸟是怎样从地栖生活转变为飞翔生活的呢?关于这个问题,有两种说法。一种认为,原始鸟类在树上攀缘,逐渐过渡到短距离滑翔,进一步变为飞翔。另 一种认为,原始鸟类是双足奔跑动物,靠前肢网捕小型动物为食,前肢在助跑过程中发展成翅膀。始祖鸟虽然仅仅发现在化石里,但它为鸟类的起源于恐龙提供了证据。随着热河生物群的发现,始祖鸟的分类地位遇到了挑战。在热河生物群,许多有真羽毛甚至有完整羽翼的动物都被归入 了恐龙类,而其中的某些种类比始祖鸟更接近鸟类另一些则比始祖鸟更原始。但是因为古生物种类是不许改名字的,所以始祖鸟这个名称没有被触动,而它的
氮气及氮的氧化物课件
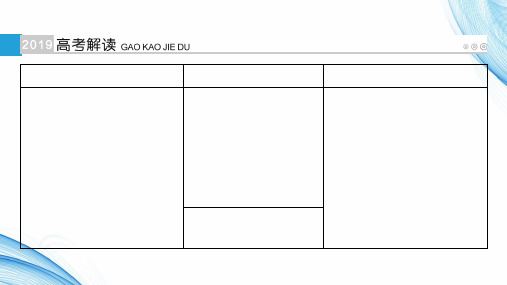
• [例1] 工业上利用氨氧化获得的高浓度NOx气体(含NO、NO2)制备NaNO2、NaNO3, 工艺流程如下:
• 已知:Na2CO3+NO+NO2===2NaNO2+CO2。
• (1)中和液所含溶质除NaNO2及少量Na2CO3外,还有____________(填化学式)。
• (2)中和液进行蒸发Ⅰ操作时,应控制水的蒸发量,避免浓度过大,目的是 _________________。蒸发Ⅰ产生的蒸气中含有少量NaNO2等有毒物质,不能直 接排放,将其冷凝后用于流程中的____________(填操作名称)最合理。
• ②NO与NO2按物质的量之比1:1被足量的NaOH溶液完全吸收后只得到一种钠盐, 该钠盐的化学式是______N_a_N__O_2_。
解析 (1)V(NO)+V(NO2)=3.0 L,23V(NO)+43V(NO2)=3.5 L,则 V(NO)=0.75 L, V(NO2)=2.25 L,V(NO)∶V(NO2)=1∶3。(2)②NO 中氮的化合价为+2,NO2 中氮 的化合价为+4,利用电子守恒,二者按 1∶1 混合时与 NaOH 反应生成盐的化合价 必然为+3 价,即为 NaNO2。
• (4)标准状况下,6.72 L NO2与水充分反应转移的电子数目为0.1NA。 ( ×)
• (5)常温常压下,92 g的NO2和N2O4混合气体含有的原子数为6NA。(
)√ ×
• (6)溴蒸气和NO2都为红棕色气体,用湿润的淀粉-KI试纸可以鉴别。( )
• 2.下列说法正确的是 ( )B • A.CO、NO、NO2都是大气污染气体,在空气中都能稳定存在 • B.NO可用于某些疾病的治疗 • C.常温下,N2既能与O2反应又能与H2反应 • D.汽车尾气的主要污染成分包括NO、CO和N2
氮的氧化物ppt3 人教课标版

作业:
• 1、默写下列方程式:
N2
① ②
NO
④
⑤
NO2
③
HNO3
• 2、课后:10题
祝你进步
• • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • •
41、从现在开始,不要未语泪先流。 42、造物之前,必先造人。 43、富人靠资本赚钱,穷人靠知识致富。 44、顾客后还有顾客,服务的开始才是销售的开始。 45、生活犹如万花筒,喜怒哀乐,酸甜苦辣,相依相随,无须过于在意,人生如梦看淡一切,看淡曾经的伤痛,好好珍惜自己、善待自己。 46、有志者自有千计万计,无志者只感千难万难。 47、苟利国家生死以,岂因祸福避趋之。 48、不要等待机会,而要创造机会。 49、如梦醒来,暮色已降,豁然开朗,欣然归家。痴幻也好,感悟也罢,在这青春的飞扬的年华,亦是一份收获。犹思“花开不是为了花落,而是为了更加灿烂。 50、人活着要呼吸。呼者,出一口气;吸者,争一口气。 51、如果我不坚强,那就等着别人来嘲笑。 52、若不给自己设限,则人生中就没有限制你发挥的藩篱。 53、希望是厄运的忠实的姐妹。 54、辛勤的蜜蜂永没有时间悲哀。 55、领导的速度决定团队的效率。 56、成功与不成功之间有时距离很短只要后者再向前几步。 57、任何的限制,都是从自己的内心开始的。 58、伟人所达到并保持着的高处,并不是一飞就到的,而是他们在同伴誉就很难挽回。 59、不要说你不会做!你是个人你就会做! 60、生活本没有导演,但我们每个人都像演员一样,为了合乎剧情而认真地表演着。 61、所谓英雄,其实是指那些无论在什么环境下都能够生存下去的人。 62、一切的一切,都是自己咎由自取。原来爱的太深,心有坠落的感觉。 63、命运不是一个机遇的问题,而是一个选择问题;它不是我们要等待的东西,而是我们要实现的东西。 64、每一个发奋努力的背后,必有加倍的赏赐。 65、再冷的石头,坐上三年也会暖。 66、淡了,散了,累了,原来的那个你呢? 67、我们的目的是什么?是胜利!不惜一切代价争取胜利! 68、一遇挫折就灰心丧气的人,永远是个失败者。而一向努力奋斗,坚韧不拔的人会走向成功。 69、在真实的生命里,每桩伟业都由信心开始,并由信心跨出第一步。 70、平凡的脚步也可以走完伟大的行程。 71、胜利,是属于最坚韧的人。 72、因害怕失败而不敢放手一搏,永远不会成功。 73、只要路是对的,就不怕路远。 74、驾驭命运的舵是奋斗。不抱有一丝幻想,不放弃一点机会,不停止一日努力。 75、自己选择的路,跪着也要走完。 76、当你的希望一个个落空,你也要坚定,要沉着! 77、蚁穴虽小,溃之千里。 78、我成功因为我志在成功! 79、凡真心尝试助人者,没有不帮到自己的。 80、相信自己,你能作茧自缚,就能破茧成蝶。 81、偶尔,只需要一个鼓励的微笑,就可以说服自己继续坚强下去。 82、年轻是本钱,但不努力就不值钱。 83、一时的忍耐是为了更广阔的自由,一时的纪律约束是为了更大的成功。 84、在你不害怕的时间去斗牛,这不算什么;在你害怕时不去斗牛,也没有什么了不起;只有在你害怕时还去斗牛才是真正了不起。 85、能把在面前行走的机会抓住的人,十有八九都会成功。 86、天赐我一双翅膀,就应该展翅翱翔,满天乌云又能怎样,穿越过就是阳光。 87、活鱼会逆流而上,死鱼才会随波逐流。 88、钕人总是把男人的谎言当作誓言去信守。 89、任何业绩的质变都来自于量变的积累。 90、要战胜恐惧,而不是退缩。
氮及其化合物PPT课件

溶解性
N2 无色 NO 无色
无味 无毒 比空气稍小 难溶于水 无味 有毒 比空气稍大 不溶于水
NO2
红棕色
有刺激 性气味
有毒
比空气大
与水发 生反应
2.化学性质 (1)氮气
(2)NO与O2反应:2NO+O2===2NO2。 (3)NO2与H2O反应:3NO2+H2O===2HNO3+NO。 3.氮氧化物对环境的影响 (1)形成硝酸型酸雨。 (2)形成光化学烟雾。
(2)形成喷泉后,甲烧瓶内液体呈________色,原因是
_______________________________________________ _________________________
(用化学方程式说明);乙烧瓶内液体呈________色,原 因是________________________(用化学方程式说明)。
答案:(1)× (2)√ (3)√ (4)√ (5)× (6)× (7)× (8)× (9)×
4.同温同压下,在甲、乙两个等体积的干燥圆底烧瓶 中分别充满NH3、NO2进行喷泉实验。如图:
(1) 实 验 室 制 备 NH3 的 化 学 方 程 式 为 : ____________________________________________________。
1.了解氮单质及其重 要化合物的主要性质和应 用。
2.了解氮单质及其 重要化合物对环境质量的 影响。
1.氮的化合物NOx对环境 的污染及治理。
2.以HNO3的强氧化性 考查氧化还原反应。
3.以NH3及铵盐考查 弱电解质的电离及盐类的水 解。
一、氮气及氮的氧化物 1.物理性质
颜色 气味 毒性 密度
3NO2+H2O===2HNO3+NO (3)等于
第五章第二节氮及其化合物第1课时氮和氮的氧化物课件-高一化学人教版(2019)必修第二册

2、下列叙述与氮的固定无关的是( B ) A.工业上氮气与氢气化合成氨 B.工业上将氨转化为硝酸和其他含氮化合物 C.豆科植物的根瘤菌把空气中的氮气转化为含氮化合物 D.电闪雷鸣的雨天,空气中的氮气会与氧气发生反应并最终转化为硝酸盐被植物吸收
【课堂同步练习】
3.下列转化属于工业固氮的是( A )
A.N2 NH3 B.NH4HCO3 NH3 C.NH3 NH4Cl
现 象
无明显现象
___________
__无__色__气__体_变__红__棕__色__,振荡 后__红__棕__色_变__为__无__色___
无色气体变红棕色 2NO + O2 = 2NO2
红棕色变为无色 3NO2 + H2O = 2HNO3 + NO
结论: 在一定条件下,NO 与 NO2 可以相互转化。
氮原子的最外电子层有5个电子,既不容易得到3个电子,也不容易失去5个电子
因此,氮原子一般通过共用电子对与其他原子相互结合构成物质。
主要化合价:-3、0、+2、+4、+5
一、氮气与氮的固定
2.氮气 (1)物理性质:无色、无味的气体,密度与空气接近,难溶于水
液氮可用于 冷冻治疗
食品等
氮气 熔点:-210 ℃ 沸点:-196 ℃ 密度:1.25 g/L
D.N2 NO
2、化学性质
毒性
NO 有毒
NO2
与水反应
3NO2 + H2O = 2HNO3 + NO与O2反应Βιβλιοθήκη 2NO + O2 = 2NO2
(工业上利用这一原理生产硝酸)
一氧化氮用排水法收集 二氧化氮用向上排气法收集
【思考与讨论】 【思考】NO2转化为NO的变化中,NO2只能作氧化剂吗?
【课堂同步练习】
3.下列转化属于工业固氮的是( A )
A.N2 NH3 B.NH4HCO3 NH3 C.NH3 NH4Cl
现 象
无明显现象
___________
__无__色__气__体_变__红__棕__色__,振荡 后__红__棕__色_变__为__无__色___
无色气体变红棕色 2NO + O2 = 2NO2
红棕色变为无色 3NO2 + H2O = 2HNO3 + NO
结论: 在一定条件下,NO 与 NO2 可以相互转化。
氮原子的最外电子层有5个电子,既不容易得到3个电子,也不容易失去5个电子
因此,氮原子一般通过共用电子对与其他原子相互结合构成物质。
主要化合价:-3、0、+2、+4、+5
一、氮气与氮的固定
2.氮气 (1)物理性质:无色、无味的气体,密度与空气接近,难溶于水
液氮可用于 冷冻治疗
食品等
氮气 熔点:-210 ℃ 沸点:-196 ℃ 密度:1.25 g/L
D.N2 NO
2、化学性质
毒性
NO 有毒
NO2
与水反应
3NO2 + H2O = 2HNO3 + NO与O2反应Βιβλιοθήκη 2NO + O2 = 2NO2
(工业上利用这一原理生产硝酸)
一氧化氮用排水法收集 二氧化氮用向上排气法收集
【思考与讨论】 【思考】NO2转化为NO的变化中,NO2只能作氧化剂吗?
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
氮族元素的化学性质
小
氮的存在
结
氮气的物理性质
氮 氮气的化学性质
氮气的用途
氮的固定
氮的主要氧化物:NO 和 NO2
作业:
教材第八页: 一、1 、3 、4 、7 、8 二、1 、2 、3 、4 、6
练习1: 在NO2与水的反应中, NO2 ( C )
A. 只是氧化剂 B. 只是还原剂 C. 既是氧化剂,又是还原剂 D. 既不是氧化剂,又不是还原剂
1936 年参加 “二二六” 兵变的日 本青年军 官
1936年广田弘毅 上台组阁,标志着 日本建立了军事法 西斯专政。
1937年日军发动卢沟桥事变,占领卢沟桥。
说一说,法 西斯统治为什么 应受到谴责?
P.28 课中题 参考答案
法西斯对内实行恐怖统治、对外扩军备战。例如: 1、对内实行恐怖统治。A制造国会纵火案,大肆逮 捕共产党人和进步人士,人数多达六七万;B.推行种 族灭绝政策,疯狂迫害犹太人,约有600万犹太人惨屠 杀。C.严密控制思想和文化教育,对宣传舆论界实行 专制,进步书籍均被付之一炬,全部的文化生活都要符 合纳粹思想。2、对外扩军备战。A.国民经济军事化: 急剧增加军费开支,1935一1936年为62亿马克,1938 一1939年猛增到160亿马克。B.实施普遍义务兵役制, 欲将后备军扩充到600万。C.悍然进军莱茵非军事区。 D.疯狂扩军备战,成为欧洲战争策源地。1939年9月 进攻波兰,挑起了第二次世界大战。
四、“柏林—罗马—东京轴心”的形成
1.《德意议定书》和《反共产国际协定》 2.“柏林—罗马—东京轴心”的形成
墨索里尼和希特勒在一起
轴心国的侵略野心
日本发动全面侵华战 争之前进行了哪些侵略 中国的活动?
P.29 温故知新 参考答案
1、19世纪70年代,日本曾侵略台湾。2、 1894年发动甲午战争,强迫清政府签订 《马关条约》。3、19世纪末,把福建占为 势力范围。4、1900年参与八国联军侵华。 5、1904-1905年发动日俄战争,与俄国争 夺中国东北。6、1915年与袁世凯签订灭 亡中国的“二十一条”。7、1931年发动 九一八事变,侵占中国东北。8、1932年制 造一•二八事变,侵略上海。9、1937年制 造卢沟桥事变,发动了全面侵华战争。
请概括德国法西斯政权的内外政策。
对内 恐怖 独裁
制造“国会纵火案”,取缔其他政党 疯狂迫害犹太人 严密控制文化思想和文化教育
对外 扩军 备战
实行国民经济军事化 1935年撕毁《凡尔赛和约》实行普遍 义务兵役制 1936年开进莱茵非军事区
“国会纵火案”是怎么一回事?
庭
上 揭
季
露米
事特
件洛
真夫
相在
。法
℃
-209.9 44.1 (白磷) 817
630.7
271.3
沸点
℃
-195.8 280
(白磷) 613
1750
1560
由以上数据分析可知:随着氮族元素核电荷
数的增加,它们的密度逐渐增大,熔点和沸点由小 到大,再由大到小。
3、氮族元素的原子结构特点
元素 名称
氮 磷
元素 符号
相同点
最外层电 子数
核电 荷数
1929—1933年危机中的德国
工业生产下降40.6% 农业生产下降30% 对外贸易缩减69.1% 失业工人占1/3,达600万人
希特勒
(1889—1945)
纳粹党臂带
1933年1月希特
勒出任德国总理。
德国总统兴登堡任命
希特勒为总理后,接见希 特勒的合影。
图为1934年兴登堡逝世。此后,希特勒 集总统、总理大权于一身,称国家元首。
无色在无通味常,情难况溶于下水,氮,气比的空化气学稍轻性。 3.氮生质气化不的学活分反泼子应,很式.而难、氮与电原其子子他式较物、活质结泼发构. 式
分子式
电子式
结构式
N2
:N ‥‥‥N:
N≡ N
4.氮气的化学性质
(1) 氧化性
a. 氮气与氢气的反应
N2 +3H2
高温高压 催化剂
2NH3
b. 氮气与金属反应
氮
磷 砷 锑 铋
元素 符号
N P As Sb Bi
核电 荷数
颜色和状态 (常态)
单质的性质 密度
g.cm-3
7
无色气体
0.00125
15
白磷:白色或黄色固体 1.82 (白磷) 红磷:红棕色固体 2.34 (红磷)
33
灰砷:灰色固体
5.727
51
银白色金属
6.684
83 银白色或微红色金属
9.80
熔点
德国国会纵火事件
受到迫害的犹太人
纳粹分子强迫犹 太人佩戴的标志
德国法西斯为什么要迫害犹太人?
1935年,德国撕毁《凡尔赛和约》,疯狂扩充军备。
在攫 取权力 后,希 特勒迅 速重建 德国的 军事力 量。
1936年,德军开进莱茵非军事区。
三、日本法西斯化 1.经济危机对日本的影响 2.军部法西斯专政的逐步建立 3.亚洲战争策源地的形成
德、日法西斯专政 建立的途径有什么不 同?
P.30 问题讨论 参考答案
在德国,以希特勒为头子的法西斯组织纳 粹党,通过蛊惑人心的宣传,骗取了各阶层的广 泛支持,从而成为国会第一大党。希特勒被授 权组阁,出任德国总理,建立起法西斯专政。在 日本,为摆脱严重的经济危机和政治危机,以军 部为主力的法西斯好战势力迅速抬头。通过 对外发动战争,使军部势力更加强大。1936年 二二六兵变之后,军部控制了新上台的内阁,建 立起军部法西斯专政
点燃
N2+3Mg
Mg3N2 (淡黄色)
(2) 还原性: 氮气与氧气的反应
放电
N2+O2
2NO
5. 氮气的用途
(1) 合成氨、制氮肥、硝酸(工业上) (2) 作保护气(通常状况下氮气的化学 性质很不活泼) (3) 作冷冻剂(医学上,常用液氮作冷冻 剂,在冷冻麻醉条件下做手术等)
6. 氮的固定
(1) 定义:将游离的氮(N2)转变为氮的 化合物的过程.
3NO2+H2O = 2HNO3+NO 注意:
(l)NO2不能用排水法收集,只能用排空气法.
(2) 鉴别NO2和溴蒸气.可用加CCl4法或加AgNO3 溶液法.
(3)氮的氧化物都是大气污染物,其中NO2是造成 光化学污染的主要因素.
元素周期表中的位置 (VA)
氮族元素 氮族元素单质的物理性质
氮族元素的原子结构特点
国 的 最希 高特 统勒 治走 宝上 座纳 。粹
德 有人说,没有希特勒,德国就不会出 现法西斯专政。你同意这种说法吗?
P.27 课中题 参考答案
不同意。这种观点过分夸大了 个人在历史中的作用。经济危机引 起政治危机,垄断资产阶级寻求出 路,妄图通过建立强权政府来巩固 其统治。这是垄断资本主义发展的 需要所决定的,并非受某个人的所 左右,所以没有希特勒,德国当时 也会出现法西斯专政。
课件使用说明
采用非线性结构,方便老师调用 鼠标左键或键盘任意键可逐步显示屏幕内容 单击各种按钮、热字可实现交互跳转 任意时刻均可按 练习 可进入练习 任意时刻均可按 End 结束
氮族元素
张掖中学
1. 氮族元素在元素周期表中的位V置A
N P As Sb Bi
2、氮族元素单质的物理性质
元素 名称
1929—1933年危机中的日本
工业生产下降1/3 进出口贸易下降50% 失业工人达300万人 在业工人工资下降1/3以上 1/3的农民失去土地 工人农民斗争不断
什么是军部?
军部是指当时日本庞大的军事 官僚机构,包括陆军省、海军省、 陆军最高指挥部参谋本部、海军最 高指挥部军令部等。
1931年日本发动九一八事变,进攻沈阳。
N
5
7
P
5
15
不同点
电子 原子半径 层数 nm
2
0.075
3
0.110
砷 As
5
33
4
0.121
锑 Sb
5
51
5
0.141
铋 Bi
5
83
6
0.152
4、氮族元素的化学性质
(1)相似性 a. 主要化合价:-3,+3,+5(Sb和Bi只有+3,+5) 。
b.最高价氧化物通式为R2O5,对应水化物除 HNO3外其它均为H3RO4。 c.气态氢化物通式为RH3。
End
练习2:下列关于氮的叙述中不正确的是 ( B )
A. 氮分子为非极性分子 B. 氮气的化学性质活泼,在常温下能与 H2 、
O2等非金属反应 C. 液氮可作冷冻剂 D. 氮有多种化合物
End
练习3:指出下列物质中氮的化合价
物
质 N2O NO N2O3 NO2 N2O4 N2O5
氮的化合价 +1 +2 +3 +4 +4 +5
授课人 嘉禾五中 李刚武
学习重点
1、慕尼黑会议 2、1939年德国进攻波兰,第二次世界大战 爆发 3、德国入侵苏联,第二次世界大战扩大; 日本偷袭珍珠港,太平洋战争爆发;第二次 世界大战进一步扩大 4、美、苏、英、中等国在华盛顿签署《联 合国家宣言》,世界反法西斯联盟建立
一、意大利法西斯专政的建立 1.墨索里尼建立法西斯专政的背景 2.法西斯专政在意大利建立 3.意大利法西斯专政的恐怖统治
练习4:下列气体中不能用排空气法收集的是 ( D )
A. CO2 C. NO2
B. H2 D. NO
End
金 张 掖 土
塔
卫
士
