FDA新药许可申请审核以及管理简介
fda的审查、运作程序和要求

fda的审查、运作程序和要求FDA(美国食品药品监督管理局)作为美国的主要药品和食品监管机构,负责确保美国市场上的药品和食品安全、有效。
为了实现这个目标,FDA拥有一套严格的审查、运作程序和要求。
FDA的审查程序包括多个步骤,以确保药品和食品符合相关法规和标准。
审查程序的第一步是申请提交,申请人需要提交详细的产品信息和数据。
然后,FDA对提交的申请进行评估,包括对药品的安全性、有效性和质量进行评估,对食品的成分和生产过程进行评估。
在评估过程中,FDA可能会要求补充信息或进行进一步的研究。
最后,FDA会根据评估结果作出决策,决定是否批准申请。
FDA的运作程序包括监督和检查,以确保药品和食品的质量和安全。
FDA会定期检查制药厂和食品生产商的生产设施,包括生产过程、设备和员工培训等方面。
他们还会对药品和食品进行抽样检测,以确保其符合相关标准。
如果发现问题,FDA会采取相应的措施,包括警告信、产品召回和制裁等。
FDA对药品和食品的要求非常严格。
对于药品,FDA要求申请人提供充分的证据证明其安全性和有效性。
对于食品,FDA要求食品生产商遵守好制造规范,并确保食品的成分和标签准确无误。
此外,FDA还要求药品和食品生产商报告任何不良事件和副作用,以便及时采取措施保护公众健康。
总结起来,FDA的审查、运作程序和要求确保了美国市场上药品和食品的安全和质量。
通过严格的审查程序,FDA确保药品和食品符合相关法规和标准。
通过监督和检查,FDA确保药品和食品生产商遵守规定,并采取措施保护公众健康。
通过严格的要求,FDA确保药品和食品的安全性、有效性和质量。
这些措施和要求使得美国市场上的药品和食品能够得到公众的信任和使用。
【医疗药品管理】FDA新药申请指南
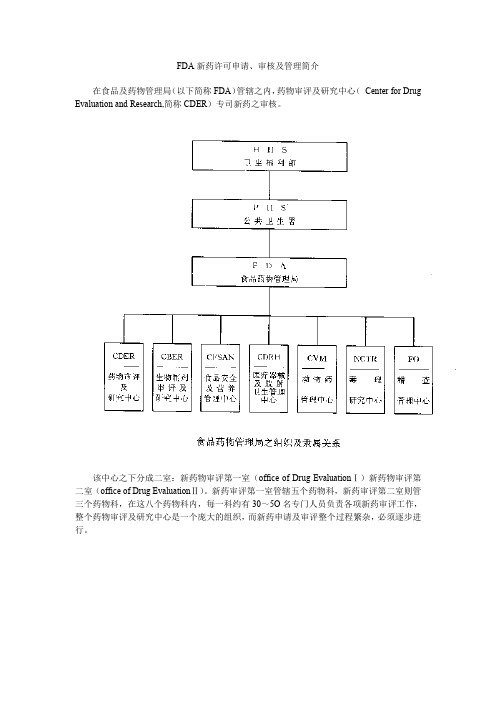
FDA新药许可申请、审核及管理简介在食品及药物管理局(以下简称FDA)管辖之内,药物审评及研究中心(Center for Drug Evaluation and Research,简称CDER)专司新药之审核。
该中心之下分成二室:新药物审评第一室(office of Drug EvaluationⅠ)新药物审评第二室(office of Drug EvaluationⅡ)。
新药审评第一室管辖五个药物科,新药审评第二室则管三个药物科,在这八个药物科内,每一科约有30~5O名专门人员负责各项新药审评工作,整个药物审评及研究中心是一个庞大的组织,而新药申请及审评整个过程繁杂,必须逐步进行。
药物审评及研究中心(Center for Drug Evalution and Research,CDER)之组织说明如下:1.秘书室(Executive Secretariant Staff)2.总务室(Office of Management)(l)药物资记中心(Drug Information Resource)(2)医学图书馆(Medical Library)(3)总务及王计(Management and Budget)(4)资讯系统设计(Information System Design)3.专业进修室(Professional Development)4.顾问团(Advisors and Consultants Staff)5·前导性新药审评(Pilot Drug Evaluation)6.非处方药审评室(office of OTC Drug Evaluation)(1)单篇非处方药审评室(MonograPh Review Staff)(2)非处方药政策性科(OTC Drug Policy Staff)(3)医学审评科(Medical Review Staff)7.非专利处方药室(office of Generic Drugs)(1)化学第一科(ChemistryⅠ)(2)化学第二科(ChemistryⅡ)(3)生体相等性科(Bioequivalence)8.研究发展室(Office of Research Resources)(1)研究及试验科(Research and Testing)(2)药品分析科(Drug Analysis)(3)生体药学科(Biopharmaceutics)(4)临床药理科(Clinical pharmacology)9.新药标准室(Office of Drug Standards)(l)新药市场广告及信息科(Drug Marketing,Advertising and Communications)10.新药合法性室(Office of Compliance)(1)新药信息科(Drug Labeling Compliance)(2)新药品质审核科(Drug Quality Evaluation)(3)新药产品及制造品质科(Mahufacturing and Product Quality)(4)科学性侦查科(Scientific Investigations)(5)新药管理科(Regulatory Affairs)11.新药流行学及统计生物学室(Office of Epidemiology and Biostatistics)(1)流行学及监视科(Epidemiology and Surveillances)(2)生物统计科(Biometrics)12.新药审评第一室(Office of Drug EvaluationⅠ,ODEI)(1)心脏药物科(Division of Cardio-Renal Drug Products)(2)神经药物科(Division of Neuropharmacological Drug Products)(3)肿瘤肺药物科(Division of Oncology and Pulmonary Drug Products)(4)影像、手术及牙药物科(Division of Medical Imaging Surgical and Dental Drug Products)(5)胃肠及凝血药物科(Division of Gastrointestinal and Coagulation Drug Products)13.新药审评第二室(Office of Drug Evaluation Ⅱ, ODE Ⅱ)(1)新陈代谢及内分泌药物科(Division of Metabolism and Endocrine Drug ProductS)(2)抗传染药物科(Division of Anti-Infective Drug Products )(3)抗病毒药物科(Division of Anti—Viral Drug ProductS)二、新药申请(一)药物的定义依据联邦食品药物及化妆品法第二章第201节,药物的定义如下:l.美国药典,同种治疗法药典,或者国家处方集(National Formulary)中所列的物质。
FDA新药审批流程简述

FDA新药审批流程简述FDA(美国食品药品监督管理局)负责监管并审批新药的上市。
下面将对FDA新药审批流程进行简述。
1.阶段Ⅰ临床试验:新药首先在健康志愿者身上进行,评估药物的安全性和耐受性,并确定药物的剂量范围。
2.阶段Ⅱ临床试验:新药在患者身上进行,评估药物的疗效和副作用。
试验时间较长,研究人员需要收集更多的数据,以确定新药的安全性和效力。
3.阶段Ⅲ临床试验:新药在大规模患者群体身上进行,以证明其疗效和安全性是否持久有效,并与现有的治疗方法进行比较。
4.新药申请:药企将试验结果提交给FDA,并申请新药上市批准。
包括药物的数据和试验结果,使用方法等。
FDA会评估申请材料。
5.NDA审批:NDA(新药申请)包括对药物研究的细节、试验结果等的描述。
FDA对NDA进行评估,确定药物是否符合上市标准。
此过程可能需要数月或数年。
6.审查:FDA将药物进行详细审查,并与药企进行沟通,以充分了解药物的性质和潜在的风险。
7.审查会议:FDA可能会召开药物审查会议,邀请专家、学者和公众就药物的疗效和风险发表意见。
8.确认上市:如果FDA认为新药符合上市标准,将发出批准通知,允许药企将新药投入市场销售。
以上是FDA新药审批流程的简要概述。
在流程中,FDA扮演着保障公众健康和安全的角色,确保新上市的药物是安全有效的。
FDA New Drug Approval Process OverviewThe FDA (U.S. Food and Drug Administration) is responsible for regulating and approving new drugs for market. The following is an overview of the FDA's new drug approval process.1. Phase I Clinical Trials: The new drug is first tested on healthy volunteers to assess its safety and tolerability and determine the dosage range.5. NDA Approval: The NDA (New Drug Application) includes a detailed description of the drug's research, trial results, etc. The FDA evaluates the NDA to determine if the drug meets the approval standards. This process can take months or years.7. Review Meetings: The FDA may hold drug review meetings where experts, scholars, and the public are invited to provide opinions on the drug's efficacy and risks.9. Post-Market Surveillance: The FDA continues to monitor the drug's safety and effectiveness, collects feedback from the market, and takes necessary actions, including further research and updating warning labels.The above is a brief overview of the FDA's new drug approval process. Throughout the process, the FDA plays a crucial role insafeguarding public health and safety, ensuring that newly marketed drugs are safe and effective.。
FDA新药审批流程简述

FDA新药审批流程简述FDA(美国食品药品监督管理局)是负责监督和管理美国食品和药品安全的联邦机构。
它负责确保市场上的药品是安全有效的,并且符合严格的审批标准。
新药审批是FDA的主要职责之一,它是一个复杂且漫长的过程,通常包括以下几个步骤:1.提交新药申请(NDA)首先,药物制造商需要通过NDA向FDA提交有关新药的完整资料。
这些资料通常包括药物的化学成分、制造工艺、药理学研究、临床试验数据以及用于治疗的适应症等信息。
此外,还需要提供药物的质量、安全和有效性的证据。
2.评估申请文件一旦FDA收到NDA,会对申请文件进行评估。
这个过程通常包括对文件的完整性和合规性的审查,例如核实所有必需的资料是否齐全。
如果缺少必要的信息,FDA可能会要求制造商提供补充材料。
3.优先审批对于一些药物,FDA可能会给予优先审批待遇。
例如,对于治疗一些严重疾病的新药,FDA可能会加快审批速度,以符合患者的迫切需求。
4.临床试验阶段一旦FDA确认NDA文件完整无误,药物制造商可以开展临床试验。
临床试验是评估药物疗效和安全性的关键步骤,通常分为三个阶段(I、II、III)。
这些试验需要遵守严格的方案和伦理规定,以确保患者的安全和药物的有效性。
5.申请审核委员会的审查在临床试验结束后,药物制造商将向FDA提交试验结果,并要求FDA审核审查委员会对其进行审查。
审查委员会是由FDA专家组成的独立机构,他们会仔细评估试验结果以及相关数据和文献,并发表意见。
这些意见对于FDA的最终决策具有重要影响。
6.申请批准在经过临床试验和审查后,FDA将根据收集到的数据和顾问委员会的意见,决定是否批准新药上市。
如果FDA认为药物的风险和益处之间的平衡是积极的,它将批准新药,并颁发批准证书。
7.监督上市后安全性一旦新药获得批准,FDA对其进行监督,以确保其安全性和真实性。
制造商需要持续向FDA提供有关药物的安全性和有效性的信息。
此外,FDA还通过药物安全盛会进行监测,并与制造商和医疗专业人员合作,收集和分析有关药物的副作用和其他安全问题的信息。
FDA新药申请

美国的新药申请制度根据现行法律,所有新药在被批准上市前除了安全性之外,还需有证明其有效性的证据。
但没有一种药是绝对安全的,认识这一点很重要。
不良反应多少总是有的,只有当一种药的利大于弊时,FDA才会认为该药足够安全,因而批准上市。
事实上,仅仅25年前,美国药品法才开始具有权衡利弊的观念,而现在这种观念已成为新药审评中的关键。
1938年《联邦食品、药品和化妆品法案》首次要求新药在上市前应提供其安全性的证据,但直到《1962年药品修正案》才要求生产厂家证明药品的有效性。
现在任何药品上市之前FDA都要在彻底审评的基础上尽快地决定资助人(通常为生产厂家)提交的研究报告是否证明了该药是安全的,并且对其预期用途是有效的。
1987年5月,FDA颁布了一项法规,放宽有前途的实验药物的使用,以便那些患绝症和垂死的病人与以往相比能够早几年从那些药物中受益。
FDA的评审员仔细审查新药申请中数目庞大的信息资料以评价新药的有效性和安全性。
一个新药当资助人在临床实验开始前向FDA提交研究用新药申请(IND)的时候就首次受到审查。
在30天之内,FDA必须让资助人知道,据FDA判断,所提交的试验是否足够安全。
如果是的话,IND就被认为可行,临床研究就能进行;如果不是,在资助人做出必要的修正之前,FDA将此研究暂时搁置一边。
在人体试验的最后阶段,也就是大规模对照试验开始前,鼓励资助人与FDA 会面。
在会谈中,FDA就资助人有研究计划的设计给予指导,以保证试验被人们接受。
正如FDA官员所说的:在发现和排除计划中那些以后在新药申请审查中会给我们带来麻烦的缺陷方面,我们是很有经验的。
我们不希望人们进行庞大的而又不可能被认为是充分的而且也无良好对照性的研究。
依照法律,在FDA接到新药申请(NDA)的那一天,“审评钟”就开始运行了。
FDA 有180天审查新药申请的时间,结论是批准或否决。
但是从第一天到批准的那天,其间的时间跨度几乎总是多于 180天。
欧美新药注册介绍和案例

欧美新药注册介绍和案例欧美新药注册是指将新的药物推向市场之前,必须经过一系列严格的审查和验证程序,确保其安全性、有效性和质量。
在欧美,新药注册通常需要进行临床试验、获得批准、监测和报告等步骤。
本文将介绍欧美新药注册的整体流程,并通过案例分析其具体应用情况。
欧美新药注册流程通常分为以下几个主要阶段:1.预临床阶段:在试验室和动物模型中评估药物的毒理学、药代动力学、药物相互作用等特性。
这一阶段的目标是确定药物是否具有潜力用于治疗人类疾病,并确定其安全性。
2.临床试验阶段:将药物用于人体进行试验,以确定其安全性和有效性。
临床试验分为三个阶段:(1)第I期试验:在健康志愿者中进行,主要评估药物的药代动力学、毒理学和耐受性。
(2)第II期试验:在患者中进行,主要评估药物的疗效、剂量反应关系和副作用。
(3)第III期试验:在大量患者中进行,用于确认药物的疗效和安全性,并与现有治疗方案进行比较。
3.注册申请:在完成临床试验后,药企可以向监管机构提交注册申请。
这些申请文件通常包括药物的质量控制、制造过程、药代动力学、毒理学和临床数据等。
4.批准和监管:监管机构将对注册申请进行评估,并根据药物的疗效、安全性和质量决定是否批准上市。
注册通过后,监管机构会继续监督药物的安全性和有效性,药企需要定期提交监测和报告。
下面我们通过一个案例来了解具体的欧美新药注册流程。
以美国食品药品监督管理局(FDA)为例,根据其官方网站提供的信息,我们了解到Imfinzi(durvalumab)是一种用于治疗晚期肺癌的免疫治疗药物。
1.预临床阶段:Imfinzi在机体内的药物动力学和毒性特性通过预临床评估得到初步验证,并显示出潜力用于治疗晚期肺癌。
2.临床试验阶段:Imfinzi进行了一系列的临床试验,其中包括:(1)第I期试验:对健康志愿者进行试验,验证药物的安全性和药代动力学。
(2)第II期试验:对晚期肺癌患者进行试验,评估药物的疗效和副作用。
FDA新药审批流程简述

FDA新药审批流程美国的新药审批可以说是世界上最严格和规范的,作为一个公司通常需要花费5亿美元资金,用 12到15年的时间才能将一个新药从试验室走入市场。
在5000个临床前化合物中大约只有5个化合物可以进入临床试验(Clinical Trials),而这5个化合物中只有一个才能被批准用于临床治疗病人,成为真正的药物。
从一个实验室发现的新化合物发展成为一个治疗疾病的药物,需要经过如下开发阶段:一、临床前试验将一个新发现的化合物经过实验室和动物试验,证明该化合物针对特定目标疾病具有生物活性,并且要评估该化合物的安全性。
二、新药临床研究申请当一个化合物通过了临床前试验后,需要向FDA提交新药临床研究申请,以便可以将该化合物应用于人体试验。
如果在提交申请后30天内FDA没有驳回申请,那么该新药临床研究申请即被视为有效,可以进行人体试验。
新药临床研究申请需要提供先前试验的材料;以及计划将在什么地方,由谁以及如何进行临床试验的说明;新化合物的结构;投药方式;动物试验中发现的所有毒性情况;该化合物的制造生产情况。
所有临床方案必须经过机构审评委员会(Institutional Revuew Board,IRB)的审查和通过。
每年必须向FDA 和IRB 汇报一次临床试验的进程和结果。
三、一期临床试验这一阶段的临床试验一般需要征集20-100名正常和健康的志愿者进行试验研究。
试验的主要目的是提供该药物的安全性资料,包括该药物的安全剂量范围。
同时也要通过这一阶段的临床试验获得其吸收、分布、代谢和排泄以及药效持续时间的数据和资料。
四、二期临床试验这一期的临床试验通常需要征集100-500名相关病人进行试验。
其主要目的是获得药物治疗有效性资料。
五、三期临床试验这一期的临床试验通常需1000-5000名临床和住院病人,多在多个医学中心进行,在医生的严格监控下,进一步获得该药物的有效性资料和鉴定副作用,以及与其他药物的相互作用关系。
fda审核流程

fda审核流程
FDA审核流程是指美国食品药品监督管理局(Food and Drug Administration)对药品、医疗器械、食品等产品进行审查和批准的程序。
这一审核流程严格遵循法律法规,旨在保障公众健康和安全。
下面将对FDA审核流程进行详细介绍。
FDA审核流程通常包括以下几个主要步骤:申请提交、审核准备、审核、批准或拒绝。
申请提交阶段是指申请人向FDA提交申请表格和相关资料,包括药品或医疗器械的化学成分、制造工艺、药效学和临床试验数据等。
审核准备阶段是指FDA的专家团队对申请资料进行初步评估和准备工作,确定审核重点和计划。
接下来是审核阶段,FDA专家团队对申请资料进行详细审查,包括药品或医疗器械的安全性、有效性、质量控制和生产工艺等方面。
他们可能会要求申请人提供额外资料或进行补充试验。
一旦审核完成,FDA将作出批准或拒绝的决定。
如果通过审核,产品将获得上市许可,否则将被拒绝上市。
在审核流程中,FDA还会进行现场检查和监督,确保生产厂家和研究机构符合相关标准和法规。
此外,FDA还会进行市场监测,监测已上市产品的安全性和质量,及时处理投诉和安全事件。
需要注意的是,FDA审核流程非常严格,时间长、成本高。
一般来说,从申请提交到最终批准,可能需要数年时间和数百万美元的投
入。
因此,申请人需要充分准备和配合,以确保审核顺利进行。
FDA审核流程是一个严格、科学的程序,旨在保障公众健康和安全。
只有通过严格审核和监督,才能确保药品、医疗器械和食品的质量和有效性。
希望本文能帮助读者更好地了解FDA审核流程,增强对药品安全的认识和信心。
FDA新药审评

美国FDA CDER新药质量审评部简介除非处方药典药(O T Cmonograph drugs)及临床试验药(Investigational New Drugs,IND)以外,在美国上市的所有新药都必须遵守美国相关新药申请(New Drug Application)法规,事先接受美国食品药品管理局(US Food and Drug Administration,FDA)的审理并取得其批准。
FDA 下属的化学类药物评价与研究中心(Center for Drug Evaluation and Research,CDER)是其属下的五个中心之一。
此中心的职责为审评并批准申请在美上市的化学类药品及某些生物类药品的安全性、有效性及质量可控性。
新药申请材料中相当一部分涉及药品的药物化学、药品生产以及生产和质量监控(Chemistry,M a n u f a c t u r e a n d C o n t r o l ,CMC)。
而这部分的审评则为CDER下属的新药质量评审部(Office of New Drug Quality Assessment,ONDQA)的主要职责,生物药品的这部分则属于生物科技产品部的职责。
需要补充说明的是国际会议协调组织(InternationalConference Harmonization,I C H )将C M C 部分统称为质量(Quality),在其网址上对此有细述。
关于新药质量审评部此部目前的机构设置建于2005年10月。
该设置便于实施新的药物质量评审体系(PharmaceuticalQuality Assessment System,PQAS)。
此系统的详细讨论和描述可见于发表在2004年FDA白皮书上的论文“21世纪药品生产质量管理规范——一种以风险为考量的模式”(cGMP for the 21st century– A Risk Based Approach)。
美国新药申请审评程序

美国新药申请审评程序在美国, 一个普通的新化合物从最初的发现到申请上市, 大约需要经过15 年的时间, 其中FDA用于审评的时间大约为6~12 个月。
FDA 将最终决定该新药能否进入市场, 因此除了实施有效的新药开发计划外, 熟悉FDA 的新药审评程序对于申请人来说也是非常重要的一个环节。
美国创新药物的申请包括两个步骤:①新药研究申请(investigational new drug application , IND) , 相当于我国的临床研究申请。
②新药申请( new drugapplication , NDA) , 相当于我国的新药上市申请,在三期临床结束后提出。
本文介绍的是FDA 对新药申请(即NDA) 的审评程序。
1、预备会议(pre - NDA meeting)在三期临床结束后, 申请人就可以进行新药申请, 在申请人提交NDA 之前, FDA 新药审评部门通常会和申请人举行一次会议。
在会议上, 申请人提交临床试验的概述报告, 让FDA 及评阅人员了解所申请新药的NDA 格式和内容。
2、新药申请的审评程序 (New Drug Application review process)2.1 、申请书的受理(filing of NDA)在收到新药申请书以后的60 天内, FDA 首先会对新药申请书的完整性作出评价。
如果FDA 认为申请书的内容完整可以受理作进一步的评价, 则书面通知申请人。
如果FDA 发现申请书中存在下列任何原因, 将拒绝受理此申请书, 并书面告知相关理由:①没有完成FDA 申请表(356h 表) ;②申请书不符合规定的格式;③申请书不完整, 所要求的一项或多项内容缺失;④缺少一份完整的环境评估报告, 或申请人请求FDA 放弃对此部分内容的要求,但没有能够提交充分的信息来说服FDA ;⑤对于非英语的申请书, 没有准确而完整的英文译本;⑥没有指出是否在符合GLP 的条件下开展每个非临床试验;⑦没有指出每个临床试验是否符合伦理委员会规定(institutional review board regulations) 和知情同意书规定(informed consent regulations) ;⑧FDA 已经批准了该新药的申请书或简化申请书;⑨对于应该用简化申请书的形式来递交的新药, 如果申请人想以NDA 的形式来递交, 那么可以在30 天内书面要求和FDA 就此问题举行一次讨论会。
FDA新药许可申请审核以及管理简介

FDA新药许可申请、审核及管理简介在食品及药物管理局(以下简称FDA)管辖之内,药物审评及研究中心(Center for Drug Evaluation and Research,简称CDER)专司新药之审核。
该中心之下分成二室:新药物审评第一室(office of Drug EvaluationⅠ)新药物审评第二室(office of Drug EvaluationⅡ)。
新药审评第一室管辖五个药物科,新药审评第二室则管三个药物科,在这八个药物科内,每一科约有30~5O名专门人员负责各项新药审评工作,整个药物审评及研究中心是一个庞大的组织,而新药申请及审评整个过程繁杂,必须逐步进行。
药物审评及研究中心(Center for Drug Evalution and Research,CDER)之组织说明如下:1.秘书室(Executive Secretariant Staff)2.总务室(Office of Management)(l)药物资记中心(Drug Information Resource)(2)医学图书馆(Medical Library)(3)总务及王计(Management and Budget)(4)资讯系统设计(Information System Design)3.专业进修室(Professional Development)4.顾问团(Advisors and Consultants Staff)5•前导性新药审评(Pilot Drug Evaluation)6.非处方药审评室(office of OTC Drug Evaluation)(1)单篇非处方药审评室(MonograPh Review Staff)(2)非处方药政策性科(OTC Drug Policy Staff)(3)医学审评科(Medical Review Staff)7.非专利处方药室(office of Generic Drugs)(1)化学第一科(ChemistryⅠ)(2)化学第二科(ChemistryⅡ)(3)生体相等性科(Bioequivalence)8.研究发展室(Office of Research Resources)(1)研究及试验科(Research and Testing)(2)药品分析科(Drug Analysis)(3)生体药学科(Biopharmaceutics)(4)临床药理科(Clinical pharmacology)9.新药标准室(Office of Drug Standards)(l)新药市场广告及信息科(Drug Marketing,Advertising and Communications)10.新药合法性室(Office of Compliance)(1)新药信息科(Drug Labeling Compliance)(2)新药品质审核科(Drug Quality Evaluation)(3)新药产品及制造品质科(Mahufacturing and Product Quality)(4)科学性侦查科(Scientific Investigations)(5)新药管理科(Regulatory Affairs)11.新药流行学及统计生物学室(Office of Epidemiology and Biostatistics)(1)流行学及监视科(Epidemiology and Surveillances)(2)生物统计科(Biometrics)12.新药审评第一室(Office of Drug EvaluationⅠ,ODEI)(1)心脏药物科(Division of Cardio-Renal Drug Products)(2)神经药物科(Division of Neuropharmacological Drug Products)(3)肿瘤肺药物科(Division of Oncology and Pulmonary Drug Products)(4)影像、手术及牙药物科(Division of Medical Imaging Surgical and Dental Drug Products)(5)胃肠及凝血药物科(Division of Gastrointestinal and Coagulation Drug Products)13.新药审评第二室(Office of Drug Evaluation Ⅱ, ODE Ⅱ)(1)新陈代谢及内分泌药物科(Division of Metabolism and Endocrine Drug ProductS)(2)抗传染药物科(Division of Anti-Infective Drug Products )(3)抗病毒药物科(Division of Anti—Viral Drug ProductS)二、新药申请(一)药物的定义依据联邦食品药物及化妆品法第二章第201节,药物的定义如下:l.美国药典,同种治疗法药典,或者国家处方集(National Formulary)中所列的物质。
FDA新药申请程序

FDA新药申请程序FDA(美国食品药品监管局)是负责确保美国公众获得安全和有效药物的监管机构。
为了确保药物的安全性和疗效,FDA对新药申请进行了严格的审查和批准程序。
新药开发是一个复杂和昂贵的过程,通常需要多次临床试验和大量数据收集。
下面将详细介绍FDA新药申请的程序。
1.基础研究和药物发现阶段:在此阶段,科学家通过实验室研究、细胞培养和动物实验等方法鉴定出一种具有潜在治疗作用的新药物。
2.预临床研究(药物毒理学和药代动力学研究):在此阶段,新药物的体内代谢、毒理学和药代动力学特性进行评估。
该阶段的研究数据将用于设计后续临床试验。
3.临床试验:临床试验是评估新药疗效和安全性的关键步骤。
该阶段分为三个阶段:I期、II期和III期。
I期试验旨在评估药物在人体内的代谢和安全性。
II期试验考察药物对特定疾病的疗效。
III期试验是最后一个阶段,目的是确定药物的疗效、剂量和安全性。
5.NDA审查:一旦NDA被提交给FDA,它将分配给一个专门的评审团队进行审查。
该团队会仔细审查文档中的所有数据和信息,并进行评估。
他们将对药物的质量、安全性和疗效进行评估,并提出问题和需要进一步证明的地方。
审查的时限通常为10个月,但在一些情况下可能会延长。
6.审查结果:FDA会向药企发出一封通知信,信中解释审查团队的评估和意见。
如果药物符合FDA的安全性和有效性要求,FDA将批准NDA,并核发许可证。
如果存在问题或缺失,FDA可能要求补充信息或重新评估。
7.药物上市:一旦FDA批准了新药的NDA,该药物即可在美国市场上市销售。
药企将开始生产、推广和销售药物,并严格遵守FDA的监管要求。
8.后续监管:药物上市后,FDA将继续监督其安全性和有效性。
FDA在市场上设立了不同的监测系统,包括药理学、药效学和不良事件报告。
如果出现安全问题或重大风险,FDA有权采取必要的措施,包括药品召回、警告公告和流行病学调查等。
总之,FDA的新药申请程序旨在确保药物的安全性和疗效。
fda审核流程

fda审核流程FDA审核流程FDA(美国食品药品监督管理局)是负责监管美国食品、药品、医疗器械和化妆品的联邦机构。
FDA审核流程是指FDA对新药品、新医疗器械或新治疗方案进行审核和批准的流程。
1. 临床试验阶段在开始进行FDA审核流程前,需要进行临床试验来评估药品或医疗器械的安全性和有效性。
临床试验通常分为三个阶段:第一阶段:小规模试验,目的是评估药品的安全性和耐受性。
第二阶段:中等规模试验,目的是进一步评估药品的安全性和有效性。
第三阶段:大规模试验,目的是评估药品的安全性和有效性,并与常规治疗方案进行比较。
2. 提交申请当临床试验成功后,申请者可以向FDA提交新药品申请(NDA)或新医疗器械申请(PMA)。
如果申请得到批准,药品或医疗器械将获得FDA许可证。
3. 审核过程申请提交后,FDA会对申请进行评估和审核。
这个过程包括以下几个步骤:① 预审:FDA会对申请进行预审,以确定文件是否齐全和符合FDA的要求。
② 审核:FDA会对申请进行详细的审核,包括研究数据、药品或医疗器械的制造工艺、标签和说明书等。
③ 评估:FDA会评估申请的内容,包括药品或医疗器械的安全性和有效性、是否符合FDA的标准等。
④ 决策:FDA会根据评估结果,决定是否批准申请,并在批准后发布批准信。
4. 后续监管一旦药品或医疗器械获得FDA许可证,申请者需要遵守FDA的监管要求,并定期向FDA提交更新的数据和信息。
FDA还会对药品或医疗器械进行定期检查,以确保它们的安全性和有效性。
FDA审核流程是一个严格的过程,旨在确保药品或医疗器械的安全性和有效性,并保护公众的健康和安全。
美国FDA简略新药申请(ANDA)概览

美国FDA简略新药申请(ANDA)概览摘要:本文通过对美国简略新药申请流程,原料药、制剂技术审评要求及部分注册资料关键控制点进行介绍以构建出美国FDA简略新药申请(ANDA)的概览。
关键词 FDA ANDA 简略新药申请1.背景介绍美国食品药品监督管理局(U.S. Food & Drug Administration)简称FDA,是药品监管相当严苛的市场,只有经过FDA批准的药品,才可以在美国上市销售。
简略新药申请(Abbreviated New Drug Application)简称ANDA,与新药申请(New Drug Application,简称NDA)相比新药申请(New Drug Application,简称NDA)不需要开展非临床试验研究及临床试验研究。
美国负责ANDA审评的机构为FDA下属的仿制药办公室(Office of Generic Drugs, OGD)。
新化合物(New Chemical Entity,简称NCE)专营期从NDA获批开始计时,用于阻止ANDA和505(b)(2)含有此化合物产品进入市场。
5年NCE专营期内FDA不接受ANDA递交,或者4年后,ANDA可以通过专利挑战来递交申请。
按照《药品价格竞争和专利期恢复法》法案,对挑战专利的、首个仿制药申请可能获得180天专营期。
180天的计算开始时间是申请人开始商业上市的日期,或法院判决专利无效、不侵权的日期,两者中较早的时间。
通用技术文件(Common Technical Document,简称 CTD),FDA要求ANDA以CTD格式提交注册资料。
CTD是人用药品注册技术要求国际协调会(The International Council for Harmonisation of Technical Requirements for Pharmaceuticals for Human Use,简称ICH)为协调ICH地区注册申报资料的格式而制定的,其实施的目的是规范注册申请,统一技术格式要求,减少不必要浪费。
FDA新药审核流程

FDA新药审核流程FDA(美国食品药品监督管理局)是美国联邦政府的一个机构,负责审批并监督所有食品、药品、医疗器械、化妆品和其他消费品的安全性和有效性。
新药审核是FDA的一个重要职责,涉及多个环节和步骤。
下面将详细介绍FDA新药审核的流程。
1. 前期准备:在提交新药申请(New Drug Application,NDA)之前,药厂需要进行大量的研发工作,包括药物的预临床实验、临床试验、效力和安全性评估等。
这个过程通常持续数年。
2.提交NDA:一旦药厂认为新药具备了提交FDA审批的条件,他们将向FDA提交NDA。
NDA需要包含大量的数据和信息,包括药物的化学成分、制备方法、质量控制等。
3.优先审查:FDA对一些新药进行优先审查,这些药物通常是用于治疗罕见病或临床需求紧迫的药物。
优先审查可以缩短FDA的审批时间。
4.首次评审:FDA将对NDA进行首次评审,评估药物的有效性和安全性。
评审小组通常由FDA的药物评审员和其他专家组成。
5.补充材料:在首次评审之后,FDA可能会要求药厂提供额外的数据和信息,以填补信息不完整或不足的方面。
6.药物评估:FDA的药物评审员将针对NDA中的各个方面进行全面评估,包括活性成分、药物代谢、药动学、药效学、不良反应等。
评审员还会研究临床试验数据,以评估药物的效果和安全性。
8.二次评审:在考虑了所有相关数据和信息之后,FDA可能会对NDA进行二次评审,并向药厂提供评审意见和建议。
此时,FDA可能会提出一些需要满足的条件,才能最终批准该药物上市。
9.批准与上市:如果通过了二次评审,FDA将批准新药上市,并授予该药物一个专利保护期。
这意味着在一定的时间内,其他药厂不能生产和销售相同的药物。
10.监测与后市场研究:一旦药物上市,FDA将继续监测该药物的有效性和安全性。
药厂也需要承担监测和报告药物的不良反应的责任。
此外,FDA可能要求药厂进行后市场研究,以更好地了解药物的效果和安全性。
FDA认证程序及其要求

FDA认证程序及其要求FDA(美国食品药品监督管理局)是美国联邦政府机构,负责监管和审核食品、药品、医疗器械、化妆品、药店以及其他相关产品的安全性和有效性。
为了确保产品的质量和安全,FDA实施了一系列认证程序及其要求。
本文将介绍FDA认证程序及其要求,以帮助企业了解相关内容。
1.新药审批程序:FDA要求在美国市场上销售的新药必须经过严格的审查和审批程序。
该程序包括“临床试验阶段”、“确证安全性和有效性阶段”以及“上市许可阶段”。
企业需要提交完整的药理毒理学数据、临床试验数据和生产工艺等信息,以证明新药的安全性和有效性。
3.医疗器械510(k)认证程序:设备制造商在销售新的医疗器械之前需要获得FDA的510(k)认证。
该认证要求企业证明所销售的医疗器械与已经获得FDA认可的同类产品相似,其安全性和有效性也得到保证。
4.药品质量管理认证程序:制药企业需要遵守严格的药品质量管理规定。
FDA要求制药企业建立完善的质量体系,保证药品在生产、贮存和配送过程中的质量和安全。
5.生物药物许可认证程序:企业在销售生物药物之前需要获得FDA的许可。
此过程包括临床试验、制造工艺控制、产品质量控制等,以确保生物药物的安全性和有效性。
6. 药店及批发商许可认证程序:所有在美国提供药店和药品批发服务的企业需要获得FDA的许可。
该认证要求实体店铺满足GMP(Good Manufacturing Practices)的标准,以确保药物的质量和安全性。
以上是FDA认证程序及其要求的简要介绍。
请注意,这些程序和要求可能会因具体产品的不同而有所差异。
因此,在申请认证之前,企业应仔细阅读FDA的要求和指南,确保了解和满足相应的要求。
在整个认证过程中,与FDA进行有效的沟通和合作也是至关重要的。
只有获得FDA的认证,企业才能在美国市场上合法销售相关产品,建立良好的声誉,并提高消费者对产品的信任度。
FDA新药申请程序

FDA新药申请程序美国食品药品监督管理局(FDA)是负责监管和批准新药上市的机构。
在美国,所有新药都必须经过FDA的审查和批准程序,以确保其安全性和有效性。
以下是FDA新药申请程序的详细步骤:第一步:发现和基础研究新药的开发通常从科学家对疾病的基础研究开始。
在这个阶段,科学家会尝试理解疾病的发生机制,并尝试找出治疗该疾病的潜在药物。
第二步:临床前研究在将药物应用于人体之前,需要进行大量的临床前研究。
这些研究包括体外和动物试验,以评估药物的安全性和有效性。
如果临床前研究表明药物有治疗潜力,并且不会对人体造成严重的安全风险,那么可以开始提交FDA新药申请。
第三步:IND(Investigational New Drug)申请IND申请是一份详细的文件,其中包含了新药的临床前研究数据、药物特性、疾病的治疗需求以及计划进行的临床试验的详细计划。
一旦IND申请被FDA接受,开发者可以开始进行临床试验。
第四步:临床试验临床试验是确定新药是否安全、有效以及对疾病产生治疗效果的关键步骤。
它分为三个不同的阶段:I期、II期和III期。
在这些试验中,药物将被应用于患者身上,并且监测其效果和副作用。
临床试验的设计必须符合FDA的规定,并且需要得到患者的知情同意。
第五步:申请审查在临床试验结束后,开发者将提交新药申请(NDA)给FDA。
NDA是一份详细的文件,其中包含了从临床试验中获得的所有数据,包括药物的安全性和有效性数据。
这些数据需要经过严密的分析和解释,以证明药物的治疗效果。
第六步:审查过程一旦NDA被提交,FDA将进行审查。
审查过程包括多个阶段,包括初步审查、详细审查和面板审查。
FDA将评估所有提供的数据,并就药物的安全性、有效性和适应症提出问题。
在这个过程中,开发者和FDA之间可能会进行多次的沟通和交流,以澄清问题和提供进一步的信息。
第七步:批准和上市经过审查过程,如果FDA认为新药是安全有效的,并且对疾病产生治疗效果,那么他们将批准其上市。
FDA生物制品的申报许可流程及要求

FDA生物制品的申报许可流程及要求FDA对新药在美国上市销售前的监管和审批始于1938年。
所有在美国上市的新药需遵循新药上市的评审程序,FDA将会对充分证明了药品安全性和有效性的申请者颁发许可执照,只有成功通过新药申请的制造商才能在美国市场销售新医药制品。
FDA认为新药的申请应具备明确的研究目的、恰当的试验设计、确切定义患者对治疗反应的评价方法、有科学依据的患者筛选方法以及具备适当的措施能够将偏向性减到最小,在具备了上诉要求并且证明了药品效益大于风险的情况下便可以批准其上市销售。
而对于剂型、安全性、浓度、给药途径、质量、疗效和适应症与原研药一致的仿制药,在美国上市需提交FDA 仿制药申请,获批后只要不与原研药的专利保护和独享权冲突,申请者可以生产并上市该仿制药。
1. 药品审批类别FDA将人用药品大致分为了4大类,分别为处方药、非处方药、植物药以及生物制品。
生物制品按照类别的不同以及监管属性的不同,主要以处方药和生物制品两类途径进行上市申请。
处方药分为创新药(New drug)和仿制药(Generics)两大类,创新药需经过特定的FDA新药上市前审批,而仿制药的上市则采用《联邦食品、药品和化妆品法》(FD&C Act)505(j)规定的简化新药申请(ANDA)的批准程序。
非处方药(OTC)采用“OTC专论”(OTC Monographs)的法规管理系统,列入该专论系统的非处方药上市无须经过上市前审批。
未列入OTC专论的药品上市途径主要有:(1) 向FDA递交请愿,要求列入OTC专论;(2) 首先申请作为新处方药上市,销售多年后再申请转为OTC资格;(3) 按照仿制药申请程序(ANDA)上市。
在植物药的类别中,一些具有悠久历史的植物药成分已归入OTC 专论,而新的植物药则必须经新药审批途径上市。
生物制品中的低风险类生物制品无需通过新药申请上市,生物仿制药(biosimilars)有其特殊的351(k)申请途径,而治疗性新生物医药制品等一类具有较高风险的制品需经过新药审批后方可上市。
FDA新药审批流程简述

FDA新药审批流程简述FDA(美国食品药品监督管理局)是负责监督和监管美国药品市场的机构,负责确保新药的安全性和有效性。
FDA的新药审批流程是一系列的评估和审查过程,由多个部门和专业人士参与。
以下是FDA新药审批流程的简要描述:1.前临床研究阶段:药物研发者在动物模型和离体实验中对新药进行测试,以确定其安全性和毒性潜力。
这个阶段主要是为了确认新药的潜在效果和毒副作用。
2.临床试验阶段:分为三个阶段进行人体临床试验。
第一阶段是在健康志愿者身上测试新药的安全性和药代动力学特性。
第二阶段是在病人身上测试新药的安全性和疗效。
第三阶段是在大量患者身上进行随机、双盲、安慰剂对照的试验,以证明新药的效果和安全性。
3.NDA(新药申请)提交:如果临床试验结果积极,研发者将提交一份完整的NDA给FDA,包括对药物的详细描述,药理学、临床试验和毒性数据,以及质量和制造信息。
4.NDA审评:FDA的药物评估员将对NDA进行评估,包括审查药物的临床试验结果、药代动力学和毒性数据,评估药物的有效性和安全性。
5.审查周期:FDA有一定的审查周期,这在一定程度上取决于药物的治疗领域和创新性。
优先审查的新药可以加速审批过程。
在审查期间,FDA可能会要求额外的信息或进行进一步的讨论。
6.FDA决策:经过审查后,FDA将就新药的批准做出决定。
如果批准,FDA将发布一份新药批准信函,并告知制药公司其药品在市场上的条件和限制。
7.药品上市:获得FDA批准的药物可以在市场上销售和推广。
然而,一些药物可能会接受后续的监管和追踪,以进一步评估其长期安全性和效果。
需要注意的是,这个简述只是新药审批流程的概述,并且过程可能因药物类型、治疗领域和创新性而略有不同。
此外,FDA还有其他途径可以加速新药的审批过程,例如优先审查、快速通道和条件批准等。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
FDA新药许可申请、审核及管理简介
在食品及药物管理局(以下简称FDA)管辖之内,药物审评及研究中心(Center for Drug Evaluation and Research,简称CDER)专司新药之审核。
该中心之下分成二室:新药物审评第一室(office of Drug EvaluationⅠ)新药物审评第二室(office of Drug EvaluationⅡ)。
新药审评第一室管辖五个药物科,新药审评第二室则管三个药物科,在这八个药物科内,每一科约有30~5O名专门人员负责各项新药审评工作,整个药物审评及研究中心是一个庞大的组织,而新药申请及审评整个过程繁杂,必须逐步进行。
药物审评及研究中心(Center for Drug Evalution and Research,CDER)之组织说明如下:1.秘书室(Executive Secretariant Staff)
2.总务室(Office of Management)
(l)药物资记中心(Drug Information Resource)
(2)医学图书馆(Medical Library)
(3)总务及王计(Management and Budget)
(4)资讯系统设计(Information System Design)
3.专业进修室(Professional Development)
4.顾问团(Advisors and Consultants Staff)
5•前导性新药审评(Pilot Drug Evaluation)
6.非处方药审评室(office of OTC Drug Evaluation)
(1)单篇非处方药审评室(MonograPh Review Staff)
(2)非处方药政策性科(OTC Drug Policy Staff)
(3)医学审评科(Medical Review Staff)
7.非专利处方药室(office of Generic Drugs)
(1)化学第一科(ChemistryⅠ)
(2)化学第二科(ChemistryⅡ)
(3)生体相等性科(Bioequivalence)
8.研究发展室(Office of Research Resources)
(1)研究及试验科(Research and Testing)
(2)药品分析科(Drug Analysis)
(3)生体药学科(Biopharmaceutics)
(4)临床药理科(Clinical pharmacology)
9.新药标准室(Office of Drug Standards)
(l)新药市场广告及信息科(Drug Marketing,Advertising and Communications)10.新药合法性室(Office of Compliance)
(1)新药信息科(Drug Labeling Compliance)
(2)新药品质审核科(Drug Quality Evaluation)
(3)新药产品及制造品质科(Mahufacturing and Product Quality)
(4)科学性侦查科(Scientific Investigations)
(5)新药管理科(Regulatory Affairs)
11.新药流行学及统计生物学室(Office of Epidemiology and Biostatistics)
(1)流行学及监视科(Epidemiology and Surveillances)
(2)生物统计科(Biometrics)
12.新药审评第一室(Office of Drug EvaluationⅠ,ODEI)
(1)心脏药物科(Division of Cardio-Renal Drug Products)
(2)神经药物科(Division of Neuropharmacological Drug Products)
(3)肿瘤肺药物科(Division of Oncology and Pulmonary Drug Products)
(4)影像、手术及牙药物科(Division of Medical Imaging Surgical and Dental Drug Products)
(5)胃肠及凝血药物科(Division of Gastrointestinal and Coagulation Drug Products)13.新药审评第二室(Office of Drug Evaluation Ⅱ, ODE Ⅱ)
(1)新陈代谢及内分泌药物科(Division of Metabolism and Endocrine Drug ProductS)(2)抗传染药物科(Division of Anti-Infective Drug Products )
(3)抗病毒药物科(Division of Anti—Viral Drug ProductS)
二、新药申请
(一)药物的定义
依据联邦食品药物及化妆品法第二章第201节,药物的定义如下:
l.美国药典,同种治疗法药典,或者国家处方集(National Formulary)中所列的物质。
2.任何物质用于人或动物以利诊断、治愈、治疗、预防疾病。
3.任何物质用于改变人体或动物构造或功能。
4.任何物质属于上述1、2或3的一部分。
药物定义范围广泛,本文着重于人用新药,不包括生物制剂在内。
(二)新药申请手续
新药申请可分为两个阶段,即新药临床试验申请。
(Investigational New Drug Application,简称IND)及新药上市许可申请(New Drug Application,简称NDA)。
1.新药临床试验申请(IND)
一般新药试验申请的目的是请求FDA核准进行第一次人体临床试验,不管是否已在美国之外其他各国进行人体试验,只要是在美国申请,需填Form FDA1571表。
及Form FDA1572表。
新药试验申请所提出的内容应包括新药的物理化学性质、临床前(preclinical)或非临床(nonclinical),以及健康志愿者(healthy volunteer)或病人使用的经验[若是已在美国以外之国家取得人体试验结果,最重要的资料是第一次在美国进行人体试验的计划书(clinical protocol)]。
进一步说明,新药试验申请至少应包括下列资料:
(1)药物的化学名称、分子式、构造、投药方式(口服、注射或其他方法),如无商标名称trade name)亦可先用公司暗码名称(code name)代替。
(2)主要成分及所知之非主要成分(没作用的成分)及所测得之杂物(impurities),并列出成分组成。
(3)供应药物公司的地址。
(4)药物来源,工厂设备(facilities)及质量控制(controls)的资料以说明如何制造、包装等,以确保药物的认定(identity)、效力(strength)、质量(quality)及纯度(purity)。
(5)所有临床前之动物药理实验、毒性试验资料、动物毒性试验,须遵照优良实验室规范(GLP)。
若未遵照是项规定,则应加以说明。
(6)一份依据临床前动物实验的结果—确定该新药物第一次用于人体实验相当安全(reasonably safe)的声明。
(7)一份提供所有相关资料—包括其可能发生副作用之临床研究员手册(Clinical Investigator’s Brochure)。
(8)一份第一次在美国进行人体试验计划书(Protocol)—该计划书应阐明实验目的、实验手续、药物授予法、参加实验者合格条件及不合格条件(inclusion and exclusion criteria)、处理特别反应或过度反应之方式、实验室血液及尿液检查等.
(9)一份说明书(包括提供学历、经历及医学经验等文件)—证明医生及专业人员有足够能力执行人体试验。
(10)经过研究机构审评委员会(Institutional Review Board)的核准,进行人体试验计划之文件。
(11)一份同意于向FDA提出人体试验申请日起30天开始进行人体试验之声明书。
正如Form FDA1571规定,除非经FDA特准,一般而言,FDA收到新药试验申请日起30天内是不能进行人体试验的。
新药试验申请送达相关的药物审评科评审后,如无问题,FDA 也不会通知公司,亦即新药试验公司于30天期限未收到FDA通知有任何异议(objection)时此新药试验申请(IND)即开始生效(in effect)。
换言之食品药物管理局并非“核准”(Approve)IND,而是“反对”而已。
如FDA对该新药申请之临床试验持不同意见,则有临床试验暂缓进行(Clinical hold)之判定,此时公司应充分合作,而补足FDA所要求的资料或实验。
新药试验如无法确定向FDA那一科(Division)申请时,可先以电话查询。
如申请之新药试验有两种药物,一般依具主要疗效(Primary mode。
fuction)之药物来决定。
如药物与生物制剂(biologics)或医疗器材(medical device)合并使用时,大致亦依主要疗效(Pri -mary mode fuction),或经过不同的中心(CDER,CBER或CDRH)讨论而决定管辖权,详细情况请参考,Federal Register,Docket No.91N—0257 Vol 56,No.225 November 21,1991。
