武汉科技大学2020年《814冶金原理》考研专业课真题试卷【答案】
武汉科技大学考研真题之冶金原理(A卷)2013年专业课考研真题

法拉第常数 F=96500C/mol, 气体常数 R=8.314J/(mol· K) 一、 (36 分)简答题: 1. 某金属元素 M( s)的熔化热为△ fusH0m,正常熔点为 Tm。写出溶解反应 M( s)→[M] 在温度 T 时的标准溶解吉布斯能△ G0 的表达式,其中 [M]选纯液态 M( l)为标准态。 2. 3. 某反应的ቤተ መጻሕፍቲ ባይዱ布斯能 G 越负,是否该反应速率越快?简述理由。 三元相图上某一相界线可以一段为共晶线、一段为转熔线,对否?请分别写出相图内二元 共晶线、二元转熔线上的反应式。 4. 高炉炼铁渣系的 3 个主要氧化物组元是什么?其碱性强弱顺序?此时高炉渣碱度表述公 式? 5. 某高碱度熔渣由 CaO 与 SiO2 混合组成, (1)按照熔渣的分子结构理论,熔渣中存在哪些 基本质点(不考虑 CaO 与 SiO2 之间的相互作用)?(2)按照熔渣离子结构理论,熔渣 中存在哪些基本质点?炉渣中 CaO 的光学碱度值为多少? 6. 在 FeO, Fe3O4, Fe2O3, 2FeO· SiO2 中, 1273K 时还原的难易顺序?1273K 分解压大小顺序? 570 C 以下不能稳定存在的是哪一个?
二 O 一三年招收硕士研究生入学考试试题
考试科目代码及科目名称: 814 冶金原理
可使用的常用工具:直尺,计算器,铅笔,橡皮 答题内容写在答题纸上,写在试卷或草稿纸上一律无效。考完后试题随答题纸交回。 考试时间 3 小时,总分值 150 分。
注意:本试题可能用到的基本数据如下:
2C+O2=2CO C+O2=CO2
六、 (共 16 分)在高炉内冶炼钛磁铁矿,还原出来的 Ti 溶解于铁水中,同时伴随有 TiC(s) 析出,存在于熔渣-铁液界面上。如果铁水温度为 1400oC,不考虑其它溶解元素的影响。求: 1. 铁水中碳为 3%时与[C]呈平衡的 a Ti ( a Ti 取质量 1%溶液为标准态) ; 2. 铁水中碳饱和时与[C]呈平衡的 a Ti ( a Ti 取质量 1%溶液为标准态) 。
武汉科技大学2017年《814冶金原理》考研专业课真题试卷【含参考答案】

A 卷参考答案及评分标准
一、 名词解释(共 5 小题,每小题 3 分,共 15 分)
1、拉乌尔定律:在溶液中当组分 B 的 xB 趋向于 1 时,它的蒸气压与其浓度 xB 成线性关系:pB=pb*×xB 2、标准溶解吉布斯自由能:纯液态物质标准态转变为溶解标准态的吉布斯自由能的变量称为标准
准考证号码: 密封线内不要写题
2017 年全国硕士研究生招生考试初试自命题试题
科目名称:冶金原理(□√ A 卷□B 卷)科目代码:814 考试时间:3 小时 满分 150 分
可使用的常用工具:□无 □√ 计算器 □√ 直尺 □圆规(请在使用工具前打√)
注意:所有答题内容必须写在答题纸上,写在试题或草稿纸上的一律无效;考 完后试题随答题纸交回。 一、名词解释(共 5 小题,每小题 3 分,共 15 分)
核心的半径 r 的计算式。
第2页共5页
六、计算题(13 分)矿球被 CO 还原反应的速率位于外扩散范围内,Sh 方程为:
Sh=2+0.16Re2/3 ,矿球直径 d=2×10-3 m,气流速度 u=0.5m/s,黏度 v=2×10-4 m2/s。还原 气体的 D=2.0×10-4 m2/s。试求 CO 的传质系数及扩散边界层厚度。 舍伍德准数 Sh=βd/D,雷诺数 Re=ud/v
压
二、 简述题(共 10 小题,每小题 6 分,共 60 分)
1、反应可能性(方向)、平衡(限度)等问题 2、不是;左边:标准态,右边:平衡态;仅数值相等而已(标准态与平衡态的数据互换) 3、B0;fB;B 或 GBex(超额函数)
4、 dcA dt
k ,则 cA
kt c0
5、CaO-SiO2-FeO,碱性最强的氧化物是 CaO 6、高碱度、高氧化性、大渣量、低温。 7、1; 1/x[C]
武汉科技大学2020年《819机械原理》考研专业课真题试卷【答案】
4.对于转速很高的凸轮机构,为了减小冲击和振动,从动件运动规律最好采用
D 运动规律。
A.等速
B.等加速等减速
C.余弦加速度
D.正弦加速度
5.在由若干机器串联构成的机组中,若这些机器的单机效率均不相同,其中最高效
ห้องสมุดไป่ตู้
率和最低效率分别为max 和min ,则机组的总效率 必有如下关系: A 。
A. min B. min
2020 年全国硕士研究生招生考试初试自命题试题 ( A 卷) (参考答案)
科目代码: 819 科目名称: 机械原理
注意:所有答题内容必须写在答题纸上,写在试题或草稿纸上的一律无效;考 完后试题随答题纸交回。
一、单项选择题(共 10 小题,每小题 2 分,共 20 分,错选、多选均无分)
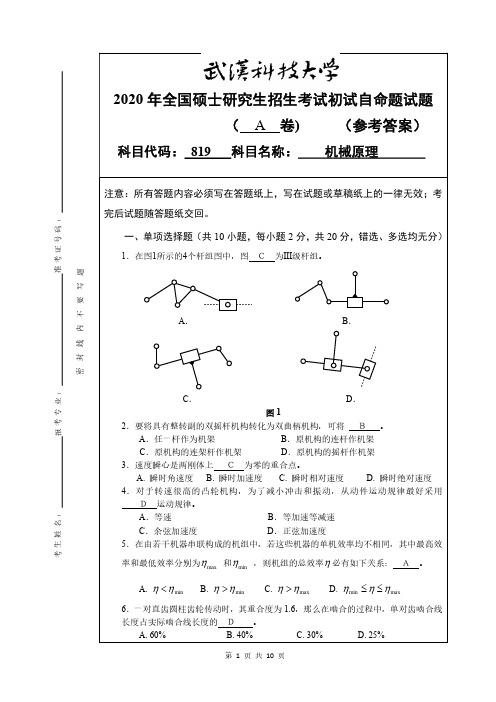
1.在图1所示的4个杆组图中,图 C 为III级杆组。
A.
B.
准考证号码:
密封线内不要写 题
报考专业:
考生姓名:
C.
D.
图1
2.要将具有整转副的双摇杆机构转化为双曲柄机构,可将 B 。
A.任一杆作为机架
B.原机构的连杆作机架
C.原机构的连架杆作机架
D.原机构的摇杆作机架
3.速度瞬心是两刚体上 C 为零的重合点。
A. 瞬时角速度 B. 瞬时加速度 C. 瞬时相对速度 D. 瞬时绝对速度
C. max
D. min max
6.一对直齿圆柱齿轮传动时,其重合度为 1.6,那么在啮合的过程中,单对齿啮合线
长度占实际啮合线长度的 D 。
A. 60%
B. 40%
C. 30%
D. 25%
第 1 页 共 10 页
(完整word版)武汉科技大学-《冶金概论》-试卷及答案

模拟试题一一选择题1.高炉生产的产品有:A)生铁B)炉渣C)高炉煤气D)炉尘2.高炉干式除尘的方法有:A)文氏管B)布袋除尘C)电除尘D)洗涤塔3.高炉内对煤气阻力最大的区域为:A)块状带B)滴落带C)软熔带D)风口回旋区4.炼钢过程的主要反应是:A)碳的氧化B)硅的氧化C)锰的氧化D)磷的氧化5.常用的氧枪喷头类型为:A)直孔型B)拉瓦尔型C)螺旋型D)扇型6.炼钢终点控制主要控制:A)钢水成分B)钢水温度C)冶炼时间D)终渣量7.碱性电弧炉炼钢按工艺方法可分为:A)双渣留渣法B)返回吹氧法C)氧化法D)不氧化法8.氧枪的常用冷却保护介质为:A)水B)气态碳氢化合物C)燃料油D)植物油9.采用顶吹氧底复合吹炼时,底部吹入的可能是:A)N2 B)Ar C)O2 D)H210高炉中配加焦炭的作用是:A)作还原剂B)燃烧后产生热量C)作料柱骨架,起支撑料柱作用D)氧化剂1:A、B、C、D 2:B、C 3:C 4:A 5:B6:A、B 7:B、C 8:A 9:A、B、C 10:A、B、C二名词解释1)冶金学2)热脆3)硫负荷4)烧结矿5)炉外精炼1、冶金学是一门研究如何经济地从矿石或其它原料中提取金属或金属化合物,并用一定加工方法制成具有一定性能的金属材料的科学。
2、钢材在轧制和锻造时,由于温度升高,晶界上的富含硫化物的网状结构又变成液态,在力的作用下,就会引起这些富硫液相沿晶界滑动,造成钢材的破裂,产生了所谓的热脆现象3、冶炼一吨生铁由炉料带入高炉硫的总量称为“硫负荷”4、将各种粉状铁,配入适宜的燃料和熔剂,均匀混合,然后放在烧结机上点火烧结。
在燃料燃烧产生高温和一系列物理化学变化作用下,部分混合料颗粒表面发生软化熔融,产生一定数量的液相,并润湿其它未融化的矿石颗粒。
冷却后,液相将矿粉颗粒粘结成块。
这一过程叫是烧结,所得到的块矿叫烧结矿。
5、炉外精炼是对炼钢炉的钢水在钢包或专用容器中进行再次精炼,又称“二次精炼”。
武汉科技大学814冶金原理2011--2020(都有答案)考研真题

54 二O 一一年招收硕士研究生入学考试试题 考试科目及代码:冶金原理 808 适用专业: 冶金物理化学、钢铁冶金、有色金属冶金 可使用的常用工具:直尺,计算器,铅笔,橡皮 答题内容写在答题纸上,写在试卷或草稿纸上一律无效考完后试题随答题纸交回。
考试时间3小时,总分值 150 分。
姓名:报考学科、专业:准考证号码:密封线内不要写题 可能用到的基本数据: 元素原子量M Si =28,M Mn =55,M Fe =56,M O =16。
CaO (s )+CO 2=CaCO 3(s ) ∆G 0=-170577+144.19T J/mol 。
一、 简答题(4⨯4+6⨯6=52分) 1. 氧化物MO 的溶解反应MO (s )→(MO ),其中(MO )的活度标准态分别选纯固态MO (s )与纯液态MO (l ),(MO )的活度值是否相等?在什么条件下能相等? 2. 如何定义铁液中活度的相互作用系数e B K ?若e B K < 0, 表示第3组元K 对组元B 在铁液中的溶解度有何影响? 3. 已知基元反应A B 的速率微分式为A A kC dt dC =-,问该反应为几级反应?设反应物的初始浓度为C 0,请写出该反应速率积分式的表达式。
4. 熔渣中氧化物CaO 、SiO 2、Fe 2O 3、FeO 酸碱性高低顺序是什么? 5. 利用下述结构的固体电解质电池测定钢液溶解氧含量: Mo 丝| [O]Fe | ZrO 2(MgO )| Mo (s )+MoO 2(s ) | Mo 丝 请写出电极反应、电池反应。
6. 请用公式表出化学反应的速率常数k 与温度T 的关系,并注明公式中其他量的物理意义。
7. 简述熔渣的完全离子溶液模型。
请评价该模型在熔渣理论中的地位。
8. 在氧势图(Ellingham 图)中, 2C+O 2=2CO 的氧势线倾斜向上,还是倾斜向下?为什么?其在冶金中的意义如何? 9. 请在你所学知识中,列举至少3个衡量氧化物稳定性大小的方法。
2020年武汉科技大学考研真题814冶金原理B硕士研究生专业课考试试题

第 3 页 共 3 页 考生姓名:报考专业:准考证号码:密封线内不要写题2020年全国硕士研究生招生考试初试自命题试题 ( B 卷) 科目代码: 814 科目名称: 冶金原理 注意:所有答题内容必须写在答题纸上,写在试题或草稿纸上的一律无效;考完后试题随答题纸交回。
一、简述题(共10小题,每小题 6分,共60分) 1. 1450︒C 下进行反应 Fe(s)+O 2(g) = FeO(l),该反应吉布斯能的变化∆G 与标准吉布斯能的变化∆G 0之间的关系式如何?二者在什么条件下可以相等? 2. 写出下列固体电解质电池的电极反应、电池反应:Ni+NiO |ZrO 2(MgO )| Mo+MoO 2 3. 有效边界层内是否存在对流扩散?请用公式表述流体内组元传质系数β与扩散系数D 以及有效边界层厚度δ的关系,并注明式中各量国际制单位。
4. 已知基元反应A → B 的速率微分式为k dt dC A =-(k 为反应速率常数),问该反应为几级反应?请指出k 的国际制单位。
设反应物A 的初始浓度为C 0,请写出该反应速率积分式的表达式。
5. 设一定温度下溶质B 在相互接触、互不相溶的平衡共存两液相I 和II 中的活度分别为B(I)a 和B(II)a ,定义分配系数B B(II)B(I)/L a a =。
试通过组元B 的化学势证明:当活度标准态确定后,L B 为一常数,不随浓度而变。
6. 钢水脱碳反应,一氧化碳气泡要均相形核需要克服的外力分别是什么? 7. 请分别说明沉淀脱氧和扩散脱氧的优缺点各是什么? 8. 改写成离子方程式:(1)2(MnO )+[Si]=2[Mn]+(SiO 2),(2)[C]+(FeO )= CO+[Fe] 9. 适用于转炉炼钢渣的基本三元系相图由哪3个主要氧化物组元构成?其中碱性最强的氧化物是哪一个? 10. 请在你所学知识中,列举至少3个衡量氧化物稳定性大小的方法。
二、分析题(共 7 小题,共 43 分) 分析炼钢过程中某液-液相反应动力学过程:[M] +b (B) = e [E] +d (D),回答下列问题: 1. (4分)请分别指出反应式中[ ]、( )符号的含义。
武汉科技大学《814冶金原理》考研专业课真题试卷【含参考答案】

1. (4 分)在图上标出组元 A、B、C 及化合物
D 的初晶区。
2. (3 分)图中表明 D 为不稳定化合物的特征? 3. (7 分)标出浓度三角形中 Pe4,PE,e3e4
线温度下降方向,写出 Pe4,PE 线上的相变 反应式(不含 P、E 点)并注明相变反应名称。
改写成离子反应式。
2. (5 分)在分子反应式中,[Mn]与(MnO)的活度标准态一般如何选取?
据此活度标准态写出该反应包含组元[Mn]与(MnO)浓度的平衡常数 K 的
第2页共6页
表达式。
3. ( 3 分 ) 基 于 K 的 表 达 式 , 写 出 Mn 在 渣 - 铁 间 平 衡 分 配 比
L’Mn=x(MnO)/w[Mn]的表达式。
准考证号码: 密封线内不要写题
2016 年攻读硕士学位研究生入学考试试题
科目名称:冶金原理(■A 卷□B 卷)科目代码:814 考试时间:3 小时 满分 150 分
可使用的常用工具:□无 □计算器 直尺 □圆规(请在使用工具前打√)
注意:所有答题内容必须写在答题纸上,写在试题或草稿纸上的一律无
效;考完后试题随答题纸交回。
可以发生,但为什么在单一的铁液中很难发生?
报考专业:
二、(共 12 分)利用下述结构的固体电解质电池测定钢液溶解氧含量:
Mo 丝| [O]Fe| ZrO2(CaO)| Mo,MoO2 | Mo 丝 在温度为 T K 时,测得电池的电动势为 E V。另外,可查到下述反应的基本热力 学数据:
Mo(s)+O2=MoO2(s), f Gm0 J/mol;
4. (9 分)基于 L’Mn 的表达式,说明采取哪些措施可有利于 Mn 的氧化。 5. (8 分)一般用哪种动力学模型处理该动力学过程较为合理?根据该模型,
武汉科技大学研究生招生初试自主命题试卷(含答案)-814冶金原理2019统招-A

姓名:报考专业: 准考证号码:密封线内不要写题2019年全国硕士研究生招生考试初试自命题试题科目名称:冶金原理(□√A 卷□B 卷)科目代码:814考试时间:3小时 满分 150 分可使用的常用工具:□无 □√计算器 □√直尺 □圆规(请在使用工具前打√)注意:所有答题内容必须写在答题纸上,写在试题或草稿纸上的一律无效;考完后试题随答题纸交回。
一、名词解释(共 5 小题,每小题4分,共20分)1、活度2、分子扩散3、二元共晶反应4、酸性氧化物5、沉淀脱氧二、简述题(共 10 小题,每小题 6 分,共 60 分)1、 钢铁冶金从铁矿石开始到生产出连铸坯的过程主要工序有哪些。
2、请简述热力学第一定律。
3、拉乌尔定律表达式p B =p B *⋅x B 中p B *的含义?4、球团矿的还原反应应该采用什么动力学模型进行描述,此反应由那些环节组成?5、熔渣中4个组元:CaO 、TiO 2、K 2O 、FeO, 请说明酸碱性强弱顺序。
其中光学碱度大于1的氧化物是哪一个?6、如果忽略压力对相平衡体系的影响,相律的表达式为 ,其中C 和ϕ分别表示什么?7、钢水脱磷反应式为:2[P]+5(FeO )=(P 2O 5)+5[Fe] ,请改写为离子方程式。
8、氧势图中2Cu +O 2=2CuO 线为何倾斜向上?C (石)+O 2=CO 2线为何近似水平?9、简述温度、渣的碱度以及氧化性对炼钢脱磷的影响? 10、请简述熔渣分子结构理论?三、计算题(共15分)700℃时测得Cd —Sn 合金的镉蒸汽压与镉浓度关系如1f C ϕ=-+%Cd 1 50 100Pc d (mmHg) 5 150 250试分别以纯物质和重量1%溶液为标准态,确定含镉50%的Cd —Sn 合金中镉的活度和活度系数。
(已知M Cd =112.4,M Sn =118.7)四、相图分析题(共30分)下图为具有一个二元中间化合物D 的三元系相图,看图在答题纸上回答问题:1、(4分)D 是稳定的中间化合物还是不稳定中间化合物,为什么?2、(6分)分别写出P 、E 点发生的相变反应名称及反应式。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
B 卷参考答案及评分标准
一、简述题(共 10 小题,每小题 6 分,共 60 分)
1、2
01ln O G G RT p ∆=∆+;O 2(g)分压在标准态压力100 kPa 条件下。
2、正极:MoO 2+4e=2Mo+2O 2-;负极:2Ni+2O 2-=2NiO+4e ;电池反应: 2Ni+MoO 2=2NiO+Mo
3、是。
δβD
=。
单位:β-m ⋅ s -1;D -m 2⋅s -1;δ-m
4、0级,mol/(m 3·s),C A =-kt +C 0
5、证明: 平衡时化学势相等,则
L B 分配常数,在一定温度下与组分B 在两相内的标准态有关,不随浓度而变。
6、需要克服大气压力、钢渣静压力、钢水静压力以及形核表面张力。
7、沉淀脱氧优点:脱氧速率快,脱氧彻底。
缺点:容易引入新的夹杂
扩散脱氧优点:不易引入新的杂质,脱氧后钢水纯净度高。
缺点:脱氧速度慢。
8、(1)2(Mn 2+) +4(O 2-) +[Si] =2[Mn]+ (SiO 44-) (2) [C]+(Fe 2+)+(O 2-)= CO+[Fe]
9、CaO-SiO 2-FeO ,碱性最强的氧化物是CaO
10、氧化物生成反应的标准吉布斯和氧势以及分解反应的分解压。
在一定温度下,生成反应
的标准吉布斯能愈负,氧势小,分解压小,氧化物稳定性大。
二、看图回答问题(43分)
1. (4分)[ ]金属相、()渣相
2.(3分)渣金反应:[Mn]+(FeO )= [Fe]+(MnO )
3.(13分)双膜理论,反应物M 在钢液侧的有效边界层内向钢-渣界面扩散;反应物B 在熔渣侧的有效边界层内向渣-钢界面扩散;钢渣界面化学反应;界面生成的E 在钢液侧的有效边界层内向钢液本体内扩散;界面生成的D 在熔渣侧的有效边界层内向熔渣本体内扩散。
4. (6分)对于可逆反应净反应速率:b e d M B E D v k c c k c c +−=−。
当反应达到平衡时,v =0。
故()=e d E D b M B
k c c K k c c +−=平衡 5.(6分)界面化学反应;相等;不能
6. (3分)各环节混合控制
7. (8分)能。
(3分)
1n J A t ∂=−∂=x C D ∂∂−=()C C β*− )(0)()(B )(0)()(B ln ln II B II B II I B I B I a RT a RT +=+=μμμμRT L a a II B I B I B II B 0)(0)(B )()(ln ln μμ−==)()(B II B I μμ=。
