高中化学溶解性表
化学常用物质溶解性表及沉淀颜色

化学溶解性表盐类溶解性表的规律可编成如下口诀记忆:钾、钠铵盐都可溶,硝盐遇水影无踪;硫(酸)盐不溶铅和钡,氯(化)物不溶银、亚汞。
氢气还原氧化铜实验,操作顺序可编成如下口诀记忆:氢气应早去晚归,酒精灯迟到早退,试管口下倾水滴。
氧化一还原反应的定义、性质、特征可编成如下口诀记忆:升失氧,降得还;若说剂,两相反。
盐类水解规律可编成如下口诀记忆:无“弱”不水解,谁“弱”谁水解;愈“弱”愈水解,又“弱”剧水解;谁“强”显谁性,双“弱”由K定。
盐类水解离子方程式的书写可编成如下口诀:左边水写分子式,中间符号写可逆,右边不写“↑”和“↓”。
溶解性口诀一钾钠铵盐溶水快,①硫酸盐除去钡铅钙。
②氯化物不溶氯化银,硝酸盐溶液都透明。
③口诀中未有皆下沉。
④注:①钾钠铵盐都溶于水;②硫酸盐中只有硫酸钡、硫酸铅、硫酸钙不溶;③硝酸盐都溶于水;④口诀中没有涉及的盐类都不溶于水;溶解性口诀二钾、钠、铵盐、硝酸盐;氯化物除银、亚汞;硫酸盐除钡和铅;碳酸、磷酸盐,只溶钾、钠、铵。
说明,以上四句歌谣概括了8类相加在水中溶解与不溶的情况。
溶解性口诀三钾钠铵硝皆可溶、盐酸盐不溶银亚汞;硫酸盐不溶钡和铅、碳磷酸盐多不溶。
多数酸溶碱少溶、只有钾钠铵钡溶溶解性口诀四钾、钠、硝酸溶,(钾盐、钠盐和硝酸盐都溶于水。
)盐酸除银(亚)汞,(盐酸盐里除氯化银和氯化亚汞外都溶。
)再说硫酸盐,不容有钡、铅,(硫酸盐中不溶的是硫酸钡和硫酸铅。
)其余几类盐,(碳酸盐、亚硫酸盐、磷酸盐、硅酸盐和硫化物)只溶钾、钠、铵,(只有相应的钾盐、钠盐和铵盐可溶)最后说碱类,钾、钠、铵和钡。
(氢氧化钾、氢氧化钠、氢氧化钡和氨水可溶)另有几种微溶物,可单独记住。
溶解性口诀五钾钠铵盐硝酸盐完全溶解不困难氯化亚汞氯化银硫酸钡和硫酸铅生成沉淀记心间氢硫酸盐和碱类碳酸磷酸硝酸盐可溶只有钾钠铵钾钠铵盐溶水快,①硫酸盐除去钡铅钙。
②氯化物不溶氯化银,硝酸盐溶液都透明。
③口诀中未有皆下沉。
高中化学晶体知识点

高中化学晶体知识点高中化学教材中的晶体内容是微观分子、原子结构与宏观物质产生联系的桥梁。
为了帮助高中生掌握晶体知识点,下面店铺为高中生整理化学晶体知识点,希望对大家有所帮助。
高中化学晶体知识点石墨――混合型晶体石墨晶体为层状结构,层与层之间的作用力为范德华力,每一层内C原子间以共价键形成正六边形结构(见图8)。
由于层内C原子以较强的共价键相结合,所以石墨有较高的熔点。
但由于层间的范德华力较弱,层间可以滑动,故石墨的硬度较小。
因此石墨晶体又称为过渡型晶体或混合型晶体。
石墨品体中每个C原子只拥有其所连接的3个C-C键的1/2(3/2个),因此晶体中C原子与C-C键数之比为2:3。
干冰――分子晶体干冰晶体中的CO2分布在立方体的顶点和面心上,分子间由分子间作用力结合形成晶体(见图7)。
C02分子内存在共价键,因此晶体中既有分子间作用力,又有共价键,但熔、沸点的高低由分子间的作用力决定,影响分子间作用力的主要因素是相对分子质量,从晶胞的结构可知与一个CO2分子距离最近且相等的CO2分子共有12个。
金刚石、二氧化硅――原子晶体(1) 金刚石是一种具有空间网状结构的原子晶体。
每个C原子以共价键与其他4个C原子紧邻,由5个碳子形成正四面体的结构单元,由共价键构成的最小环结构中有6个碳原子(见图4),由于每个C原子拥有所连4个C-C键的1/2(2个),所以碳原子个数与C-C键数之比为1:2。
(2) 二氧化硅晶体可以看成是金刚石结构中,C原子被Si原子代替,且在C-C键之间插入O原子后形成的,即每个硅原子与周围的四个氧原子构成一个正四面体,构成二氧化硅晶体结构的最小环是由12个原子构成椅式环,键角∠(O-Si-O)=109°28'(见图5)。
每个Si原子拥有所连4个O原子的1/2(2个)(见图6),因此si、O原子个数比为1:2,即化学式表示为SiO2。
氯化钠、氯化铯晶体——离子晶体由于离子键无饱和性与方向性,所以离子晶体中无单个分子存在。
(完整)高中化学有机化合物知识点总结

高中化学有机物知识点总结一、重要的物理性质1.有机物的溶解性(1)难溶于水的有:各类烃、酯、绝大多数高聚物、高级的(指分子中碳原子数目较多的,下同)醇、醛、羧酸等。
(2)易溶于水的有:低级的[一般指N(C)≤4]醇、醛、羧酸及盐、氨基酸及盐、单糖、二糖。
(3)具有特殊溶解性的:①乙醇是一种很好的溶剂,既能溶解许多无机物,又能溶解许多有机物。
②乙酸乙酯在饱和碳酸钠溶液中更加难溶,同时饱和碳酸钠溶液还能通过反应吸收挥发出的乙酸,溶解吸收挥发出的乙醇,便于闻到乙酸乙酯的香味。
③有的淀粉、蛋白质可溶于水形成胶体..。
蛋白质在浓轻金属盐(包括铵盐)溶液中溶解度减小,会析出(即盐析,皂化反应中也有此操作)。
④线型和部分支链型高聚物可溶于某些有机溶剂,而体型则难溶于有机溶剂。
2.有机物的密度小于水的密度,且与水(溶液)分层的有:各类烃、酯(包括油脂)3.有机物的状态[常温常压(1个大气压、20℃左右)](1)气态:①烃类:一般N(C)≤4的各类烃注意:新戊烷[C(CH3)4]亦为气态②衍生物类:一氯甲烷(...HCHO....,沸点为...).....-.21℃.....).甲醛(...-.24.2℃.....CH..3.Cl..,.沸点为(2)液态:一般N(C)在5~16的烃及绝大多数低级衍生物。
如,己烷CH3(CH2)4CH3甲醇CH3OH甲酸HCOOH 乙醛CH3CHO★特殊:不饱和程度高的高级脂肪酸甘油酯,如植物油脂等在常温下也为液态(3)固态:一般N(C)在17或17以上的链烃及高级衍生物。
如,石蜡C12以上的烃饱和程度高的高级脂肪酸甘油酯,如动物油脂在常温下为固态4.有机物的颜色☆绝大多数有机物为无色气体或无色液体或无色晶体,少数有特殊颜色☆淀粉溶液(胶)遇碘(I2)变蓝色溶液;☆含有苯环的蛋白质溶胶遇浓硝酸会有白色沉淀产生,加热或较长时间后,沉淀变黄色。
5.有机物的气味许多有机物具有特殊的气味,但在中学阶段只需要了解下列有机物的气味:☆甲烷无味☆乙烯稍有甜味(植物生长的调节剂)☆液态烯烃汽油的气味☆乙炔无味☆苯及其同系物芳香气味,有一定的毒性,尽量少吸入。
高中化学会考必背知识要点总结

高中化学会考必背知识要点总结高中化学会考必背知识要点总结虽然高中的化学会考难度不大但是会考所涉及到的化学知识点还是比较多的,对于文科生而言,最重要的无非就是知识点的记忆。
下面是店铺为大家整理的高中化学会考重要的知识,希望对大家有用!高中化学会考必背知识要点总结11、掌握一图(原子结构示意图)、五式(分子式、结构式、结构简式、电子式、最简式)、六方程(化学方程式、电离方程式、水解方程式、离子方程式、电极方程式、热化学方程式)的正确书写。
2、最简式相同的有机物:① CH:C2H2和C6H6② CH2:烯烃和环烷烃③ CH2O:甲醛、乙酸、甲酸甲酯④ CnH2nO:饱和一元醛(或饱和一元酮)与二倍于其碳原子数和饱和一元羧酸或酯;举一例:乙醛(C2H4O)与丁酸及其异构体(C4H8O2)3、一般原子的原子核是由质子和中子构成,但氕原子(1H)中无中子。
4、元素周期表中的每个周期不一定从金属元素开始,如第一周期是从氢元素开始。
5、ⅢB所含的元素种类最多。
碳元素形成的化合物种类最多,且ⅣA族中元素组成的晶体常常属于原子晶体,如金刚石、晶体硅、二氧化硅、碳化硅等。
6、质量数相同的原子,不一定属于同种元素的原子,如18O与18F、40K与40Ca7. ⅣA~ⅦA族中只有ⅦA族元素没有同素异形体,且其单质不能与氧气直接化合。
8、活泼金属与活泼非金属一般形成离子化合物,但AlCl3却是共价化合物(熔沸点很低,易升华,为双聚分子,所有原子都达到了最外层为8个电子的稳定结构)。
9、一般元素性质越活泼,其单质的性质也活泼,但N和P相反,因为N2形成叁键。
10、非金属元素之间一般形成共价化合物,但NH4Cl、NH4NO3等铵盐却是离子化合物。
11、离子化合物在一般条件下不存在单个分子,但在气态时却是以单个分子存在。
如NaCl。
12、含有非极性键的化合物不一定都是共价化合物,如Na2O2、FeS2、CaC2等是离子化合物。
13、单质分子不一定是非极性分子,如O3是极性分子。
人教版高中化学选三溶解性、手性
服/务/教/师 免/费/馈/赠
返回菜单
新课标化学·选修3 物质结构与性质
3.从碘水中提取碘,可供选择的有机溶剂是( )
A.苯、酒精
B.汽油、甘油
C.四氯化碳、汽油 D.二硫化碳、乙醇 【解析】 从碘水中提取碘要求碘在该有机溶剂(萃取剂)中
的溶解度比在水中的溶解度大,且有机溶剂与水互不相溶,只
服/务/教/师 免/费/馈/赠
返回菜单
新课标化学·选修3 物质结构与性质
【解析】
A
中
32
BrCH2CHOH
1
CH2OH,2
号碳原子是饱和碳
原子,且连有 BrCH2—、H—、—OH、—CH2OH 四个不同的原
子或原子团,所以存在手性异构体;B 中
带
圈 的 碳 原 子 是 饱 和 碳 原 子 , 且 连 有 —C2H5 、 —CH2OH 、 —CH===CH2、—COOH 四个不同的原子团,所以存在手性异 构体;C 中C3 H3C2 HOHC1 OOH,2 号碳原子是饱和碳原子,且连 有—CH3、H—、—OH、—COOH 四个不同的原子或原子团, 所以存在手性异构体;D 中饱和碳原子没有一个原子符合连有四
有这样才能使碘转移到有机溶剂中与水分离。碘属于非极性分
子,易溶于苯、汽油、CCl4、乙醇等有机溶剂,但甘油、酒精 由于分子中存在—OH,能与水互溶,所以不能用作萃取剂,故
答案为C。 【答案】 C
服/务/教/师 免/费/馈/赠
返回菜单
新课标化学·选修3 物质结构与性质
4.下列物质中不存在手性异构体的是( )
D.以上说法都不对
【解析】 Br2、I2是非极性分子,它们易溶于非极性溶剂
——CCl4,而在极性溶剂——水中的溶解度较小。 【答案】 C
人教版新课标高中化学目录各册大全

人教版新课标高中化学目录各册大全编辑整理:尊敬的读者朋友们:这里是精品文档编辑中心,本文档内容是由我和我的同事精心编辑整理后发布的,发布之前我们对文中内容进行仔细校对,但是难免会有疏漏的地方,但是任然希望(人教版新课标高中化学目录各册大全)的内容能够给您的工作和学习带来便利。
同时也真诚的希望收到您的建议和反馈,这将是我们进步的源泉,前进的动力。
本文可编辑可修改,如果觉得对您有帮助请收藏以便随时查阅,最后祝您生活愉快业绩进步,以下为人教版新课标高中化学目录各册大全的全部内容。
普通高中课程标准实验教科书化学必修1第一章从实验学化学第一节化学实验基本方法第二节化学计量在实验中的应用归纳与整理第二章化学物质及其变化第一节物质的分类第二节离子反应第三节氧化还原反应归纳与整理第三章金属及其化合物第一节金属的化学性质第二节几种重要的金属化合物第三节用途广泛的金属材料归纳与整理第四章非金属及其化合物第一节无机非金属材料的主角--—硅第二节富集在海水中的元素—-—氯第三节硫和氮的氧化物第四节硫酸、硝酸和氨归纳与整理附录Ⅰ 相对原子质量表附录Ⅱ 部分酸、碱和盐的溶解性表(20℃)附录Ⅲ 一些常见元素中英文名称对照表元素周期表普通高中课程标准实验教科书化学必修2第一章物质结构元素周期律第一节元素周期表第二节元素周期律第三节化学键归纳与整理第二章化学反应与能量第一节化学能与热能第二节化学能与电能第三节化学反应的速率和限度归纳与整理第三章有机化合物第一节最简单的有机化合物-—--甲烷第二节来自石油和煤的两种基本化工原料第三节生活中两种常见的有机物归纳与整理第四章化学与可持续发展第一节开发利用金属矿物和海水资源第二节化学与资源综合利用、环境保护归纳与整理结束语附录Ⅰ 相对原子质量表附录Ⅱ 部分酸、碱和盐的溶解性表(20℃)附录Ⅲ 一些常见元素中英文名称对照表普通高中课程标准实验教科书化学与生活选修1第一章关注营养平衡第一节生命的基础能源--—糖类第二节重要的体内能源———油脂第三节生命的基础—--蛋白质归纳与整理第二章促进身心健康第一节合理选择饮食第二节正确使用药物归纳与整理第三章探索生活材料第一节合金第二节金属的腐蚀和防护第三节玻璃、陶瓷和水泥第四节塑料、纤维和橡胶归纳与整理第四章保护生存环境第一节改善大气质量第二节爱护水资源第三节垃圾资源化归纳与整理附录Ⅰ 我国居民膳食中某些元素每日的适宜摄入量或推荐摄入量附录Ⅱ 环境空气质量标准附录Ⅲ 我国生活饮用水水质标准普通高中课程标准实验教科书化学与技术选修2第一单元走进化学工业课题1化学生产过程中的基本问题课题2人工固氮技术──合成氨课题3纯碱的生产归纳与整理练习与实践第二单元化学与资源开发利用课题1获取洁净的水课题2海水的综合利用课题3石油、煤和天然气的综合利用归纳与整理练习与实践第三单元化学与材料的发展课题1无机非金属材料课题2金属材料课题3高分子化合物与材料归纳与整理练习与实践第四单元化学与技术的发展课题1化肥和农药课题2表面活性剂精细化学品归纳与整理练习与实践结束语迎接化学的黄金时代元素周期表普通高中课程标准实验教科书物质结构与性质选修3第一章原子结构与性质第一节原子结构第二节原子结构与元素的性质归纳与整理复习题第二章分子结构与性质第一节共价键第二节分子的立体结构第三节分子的性质归纳与整理复习题第三章晶体结构与性质第一节晶体的常识第二节分子晶体与原子晶体第三节金属晶体第四节离子晶体归纳与整理复习题开放性作业普通高中课程标准实验教科书化学反应原理选修4第一章化学反应与能量第一节化学反应与能量的变化第二节燃烧热能源第三节化学反应热的计算归纳与整理第二章化学反应速率和化学平衡第一节化学反应速率第二节影响化学反应速率的因素第三节化学平衡第四节化学反应进行的方向归纳与整理第三章水溶液中的离子平衡第一节弱电解质的电离第二节水的电离和溶液的酸碱性第三节盐类的水解第四节难溶电解质的溶解平衡归纳与整理第四章电化学基础第一节原电池第二节化学电源第三节电解池第四节金属的电化学腐蚀与防护归纳与整理附录部分酸、碱和盐的溶解性表(20℃)后记普通高中课程标准实验教科书有机化学基础选修5引言第一章认识有机化合物第一节有机化合物的分类第二节有机化合物的结构特点第三节有机化合物的命名第四节研究有机化合物的一般步骤和方法归纳与整理复习题第二章烃和卤代烃第一节脂肪烃。
离子反应表

推荐一张实用性很强的表 ——部分离子反应表酸、碱、盐等物质间的复分解反应实质是离子之间的反应,它一直是初、高中化学的重点、难点。
酸、碱、盐等化合物数量非常多,它们间的反应特别多,反应规律相当复杂,使用频率相当高的“部分酸、碱、盐的溶解性表”也不容易被学生熟练的掌握。
针对这种情况,笔者通过多年的教学摸索,总结出一张“部分离子反应表”,该表能使学生们轻轻松松驾驭酸、碱、盐之间的各类复分解反应,现推荐给同学们。
部分离子反应表OH NO Cl SO CO H H O NH K Na Ca Ba Zn Mg Mn Fe Cu Al Fe Ag -----++++++++++++++↑↑3423224222222233关于上表的几点说明:(1)该表是在初、高中化学教材中“部分酸、碱、盐的溶解性表(20℃)”的基础上发展起来的,它用简洁明快的线条代替了原表中的文字,并补充了一些新的内容使之更富有实用性。
更有意义的是学生经过训练之后只需30~40秒的时间就能将该表勾画出来直观的使用。
(2)熟练按序地阅读表中的阴、阳离子是正确迅速勾画该表的关键。
纵行阳离子读为:一价氢铵钾钠根(为了表的美观性,Ag +仍然写在最下面)二价钙钡锌镁锰亚铁铜(谐音:盖被 心美梦 亚铁铜) 三价铝铁横行阴离子读为: 负一氢氧硝酸氯 负二硫酸碳酸根(3)表中记号表示的意义:(a )“↓”表示相应位置处,阴、阳离子在水溶液中相互作用将有难溶于水的沉淀生成。
例如:()()Cu OH Cu OH Ag OH AgOH AgOH Ag O H OAl CO H O Al OH CO 22223322322223323+-+-+-+=↓+=↓=↓+++=↓+↑有趣的是表中第一纵行氢氧化物沉淀从锌(心)即氢氧化锌开始沉淀,到最后一纵行碳酸钙(即石灰石的主要成分)开始沉淀,最终一块石头落地了。
(b )“”表示相应位置处,阴、阳离子相互结合形成微溶于水的化合物,当水中这些阴、阳离子浓度较大时,它们相互作用也会生成沉淀。
人教版新课标高中化学目录各册大全(K12教育文档)

人教版新课标高中化学目录各册大全(word版可编辑修改)编辑整理:尊敬的读者朋友们:这里是精品文档编辑中心,本文档内容是由我和我的同事精心编辑整理后发布的,发布之前我们对文中内容进行仔细校对,但是难免会有疏漏的地方,但是任然希望(人教版新课标高中化学目录各册大全(word版可编辑修改))的内容能够给您的工作和学习带来便利。
同时也真诚的希望收到您的建议和反馈,这将是我们进步的源泉,前进的动力。
本文可编辑可修改,如果觉得对您有帮助请收藏以便随时查阅,最后祝您生活愉快业绩进步,以下为人教版新课标高中化学目录各册大全(word版可编辑修改)的全部内容。
普通高中课程标准实验教科书化学必修1 第一章从实验学化学第一节化学实验基本方法第二节化学计量在实验中的应用归纳与整理第二章化学物质及其变化第一节物质的分类第二节离子反应第三节氧化还原反应归纳与整理第三章金属及其化合物第一节金属的化学性质第二节几种重要的金属化合物第三节用途广泛的金属材料归纳与整理第四章非金属及其化合物第一节无机非金属材料的主角———硅第二节富集在海水中的元素-—-氯第三节硫和氮的氧化物第四节硫酸、硝酸和氨归纳与整理附录Ⅱ部分酸、碱和盐的溶解性表(20℃)附录Ⅲ一些常见元素中英文名称对照表元素周期表普通高中课程标准实验教科书化学必修2第一章物质结构元素周期律第一节元素周期表第二节元素周期律第三节化学键归纳与整理第二章化学反应与能量第一节化学能与热能第二节化学能与电能第三节化学反应的速率和限度归纳与整理第三章有机化合物第一节最简单的有机化合物—-—-甲烷第二节来自石油和煤的两种基本化工原料第三节生活中两种常见的有机物归纳与整理第四章化学与可持续发展第一节开发利用金属矿物和海水资源第二节化学与资源综合利用、环境保护结束语附录Ⅰ相对原子质量表附录Ⅱ部分酸、碱和盐的溶解性表(20℃)附录Ⅲ一些常见元素中英文名称对照表普通高中课程标准实验教科书化学与生活选修1第一章关注营养平衡第一节生命的基础能源—-—糖类第二节重要的体内能源——-油脂第三节生命的基础-——蛋白质归纳与整理第二章促进身心健康第一节合理选择饮食第二节正确使用药物归纳与整理第三章探索生活材料第一节合金第二节金属的腐蚀和防护第三节玻璃、陶瓷和水泥第四节塑料、纤维和橡胶归纳与整理第一节改善大气质量第二节爱护水资源第三节垃圾资源化归纳与整理附录Ⅰ我国居民膳食中某些元素每日的适宜摄入量或推荐摄入量附录Ⅱ环境空气质量标准附录Ⅲ我国生活饮用水水质标准普通高中课程标准实验教科书化学与技术选修2第一单元走进化学工业课题1化学生产过程中的基本问题课题2人工固氮技术──合成氨课题3纯碱的生产归纳与整理练习与实践第二单元化学与资源开发利用课题1获取洁净的水课题2海水的综合利用课题3石油、煤和天然气的综合利用归纳与整理练习与实践课题1无机非金属材料课题2金属材料课题3高分子化合物与材料归纳与整理练习与实践第四单元化学与技术的发展课题1化肥和农药课题2表面活性剂精细化学品归纳与整理练习与实践结束语迎接化学的黄金时代元素周期表普通高中课程标准实验教科书物质结构与性质选修3第一章原子结构与性质第一节原子结构第二节原子结构与元素的性质归纳与整理复习题第二章分子结构与性质第一节共价键第二节分子的立体结构复习题第三章晶体结构与性质第一节晶体的常识第二节分子晶体与原子晶体第三节金属晶体第四节离子晶体归纳与整理复习题开放性作业普通高中课程标准实验教科书化学反应原理选修4第一章化学反应与能量第一节化学反应与能量的变化第二节燃烧热能源第三节化学反应热的计算归纳与整理第二章化学反应速率和化学平衡第一节化学反应速率第二节影响化学反应速率的因素第三节化学平衡第四节化学反应进行的方向第三章水溶液中的离子平衡第一节弱电解质的电离第二节水的电离和溶液的酸碱性第三节盐类的水解第四节难溶电解质的溶解平衡归纳与整理第四章电化学基础第一节原电池第二节化学电源第三节电解池第四节金属的电化学腐蚀与防护归纳与整理附录部分酸、碱和盐的溶解性表(20℃)后记普通高中课程标准实验教科书有机化学基础选修5引言第一章认识有机化合物第一节有机化合物的分类第二节有机化合物的结构特点第三节有机化合物的命名复习题第二章烃和卤代烃第一节脂肪烃第二节芳香烃第三节卤代烃归纳与整理复习题第三章烃的含氧衍生物第一节醇酚第二节醛第三节羧酸酯第四节有机合成归纳与整理复习题第四章生命中的基础有机化学物质第一节油脂第二节糖类第三节蛋白质和核酸归纳与整理复习题第五章进入合成有机高分子化合物的时代第一节合成高分子化合物的基本方法第二节应用广泛的高分子材料第三节功能高分子材料归纳与整理复习题普通高中课程标准实验教科书实验化学选修6第一单元从实验走进化学课题一实验化学起步课题二化学实验的绿色追求第二单元物质的获取课题一物质的分离和提纯课题二物质的制备第三单元物质的检测课题一物质的检验课题二物质含量的测定第四单元研究型实验课题一物质性质的研究课题二身边化学问题的探究课题三综合实验设计人教版新课标高中化学目录各册大全(word版可编辑修改) 附录I 化学实验规则附录II 化学实验种的一些常用仪器附录III 部分盐、氧化物、碱融解性表附录IV 常见离子和化合物的颜色附录V 实验室常用酸、碱溶液的配制方法附录V I 一些酸、碱溶液中溶质的质量分数和溶液的密度附录VII 几种仪器分析方法简介后记11。
溶解度表

溶解度表维基百科,自由的百科全书跳转到:导航, 搜索关于高中阶段使用的用于判断溶解性的简易表格,请参见溶解性表。
溶解度表以化学品中特征元素的拼音顺序排列。
所有数据都为1atm下的数据,单位为g/100cm3。
内容列表:锕、氨、铵、钯、钡、铋、铂、钚、氮、镝、铒、钒、钆、钙、锆、镉、铬、汞、钴、硅、铪、氦、钬、镓、钾、金、钪、镧、锂、硫、镥、铝、镁、锰、钠、镍、钕、硼、铍、钋、镨、氢、铅、铷、铯、钐、砷、铈、锶、铊、碳、铽、锑、铁、铜、钍、锡、氙、锌、溴、氩、氧、铟、钇、镱、银、铀、铕、有机化合物物质化学式0°C 10°C20°C30°C40°C50°C60°C70°C80°C90°C100°C氢氧化锕(III)Ac(OH)30.0022氨NH388.5 70 56 44.5 34 26.5 20 15 11 8 7叠氮化铵NH4N316 25.3 37.1苯甲酸铵NH4C7H5O220碳酸氢铵NH4HCO311.9 16.1 21.7 28.4 36.6 59.2 109 170 354溴化铵NH4Br60.6 68.1 76.4 83.2 91.2 108 125 135 145碳酸铵(NH4)2CO3100氯酸铵NH4ClO328.7氯化铵NH4Cl29.4 33.2 37.2 41.4 45.8 50.4 55.3 60.2 65.6 71.2 77.3氯铂酸铵(NH4)2PtCl60.289 0.374 0.499 0.637 0.815 1.44 2.16 2.61 3.36铬酸铵(NH4)2CrO425 29.2 34 39.3 45.3 59 76.1重铬酸铵(NH4)2Cr2O718.2 25.5 35.6 46.5 58.5 86 115 156砷酸二氢铵NH4H2AsO433.7 48.7 63.8 83 107 122磷酸二氢铵NH4H2PO422.7 39.5 37.4 46.4 56.7 82.5 118 173氟硅酸铵(NH4)2SiF618.6甲酸NH4HCO2102 143 204 311 533铵磷酸一氢铵(NH4)2HPO442.9 62.9 68.9 75.1 81.8 97.2硫酸氢铵NH4HSO4100酒石酸氢铵NH4HC4H4O61.882.7碘酸铵NH4IO32.6碘化铵NH4I155 163 172 182 191 209 229 250硝酸铵NH4NO3118 150 192 242 297 421 580 740 871高碘酸铵(NH4)5IO62.7草酸铵(NH4)2C2O42.23.214.45 6.09 8.18 14 22.4 27.9 34.7高氯酸铵NH4ClO412 16.4 21.7 37.7 34.6 49.9 68.9高锰酸铵NH4MnO40.8磷酸铵(NH4)3PO426.1硒酸铵(NH4)2SeO496 105 115 126 143 192硫酸铵(NH4)2SO470.6 73 75.4 78 81 88 95 103亚硫酸铵(NH4)2SO347.9 54 60.8 68.8 78.4 104 144 150 153酒石酸铵(NH4)2C4H4O645 55 63 70.5 76.5 86.9硫氰酸铵NH4SCN120 144 170 208 234 346硫代硫酸铵(NH4)2S2O32.15钒酸铵NH4VO30.48 0.84 1.32 2.42(II)10-10氢氧化钯(IV)Pd(OH)45.247×10-14乙酸钡Ba(C2H3O2)258.862 72 7578.575 74 74.8砷酸钡Ba3(AsO4)22.586×10-9叠氮化钡Ba(N3)212.516.1 17.4溴酸钡Ba(BrO3)20.290.44 0.65 0.951.312.273.520.951.31溴化钡BaBr298 101 104 109 114 123 135 149碳酸钡BaCO31.409×10-3氯酸钡Ba(ClO3)220.326.9 33.9 41.649.766.784.8105氯化钡BaCl231.233.5 35.8 38.140.846.252.555.859.4氯酸钡Ba(ClO2)243.944.6 45.447.953.866.680.8铬酸钡BaCrO42.775×10-4氰化钡Ba(CN)280亚铁氰化钡Ba2Fe(CN)69.732×10-3氟化钡BaF20.1590.160.162氟硅酸钡BaSiF62.8×10-2甲酸钡Ba(HCO2)226.228 31.9 3438.644.247.651.3磷酸氢钡BaHPO41.3×10-2亚磷酸氢钡BaHPO30.687氢氧化钡Ba(OH)2·8H2O1.672.483.89 5.598.2220.9101碘酸钡Ba(IO3)23.5×4.6×5.7×10-210-210-2碘化钡BaI2182 201 223 250 264 291 301钼酸钡BaMoO46×10-3硝酸钡Ba(NO3)24.956.67 9.02 11.514.120.427.234.4亚硝酸钡Ba(NO2)250.360 72.8 102 151 222 261 325草酸钡BaC2O4·2H2O3×10-3氧化钡BaO 3.8高氯酸钡Ba(ClO4)2239 336 416 495 575 653高锰酸钡Ba(MnO4)21.5×10-2焦磷酸钡Ba2P2O79×10-3硒酸钡BaSeO45×10-3硫酸钡BaSO42.448×10-4硫化钡BaS2.884.89 7.86 10.414.927.749.967.360.3砷酸铋BiAsO47.298×10-4氢氧化铋Bi(OH)32.868×10-7碘化铋BiI37.761×10-4磷酸铋BiPO41.096×10-10硫化铋Bi2S31.561×10-20氢氧化铂(II)Pt(OH)23.109×10-11溴化铂(IV)PtBr41.352×10-7物质化学式°C10°C 20°C 30°C 40°C 50°C 60°C 70°C 80°C 90°C 100°C 一氧化氮NO5.6×10-3一氧化二氮N 2O0.112铬酸镝(III )Dy 2(CrO 4)3·10H2O0.663(III )·9H2O氢氧化钆(III )Gd(OH)31.882×10-5硫酸钆(III )Gd2(SO4)33.98 3.3 2.6 2.32氯化钙CaCl259.5 64.7 74.5 100 128 137 147 154 159乙酸钙Ca(C2H3O2)2·2H2O37.4 36 34.7 33.8 33.2 32.7 33.531.129.7砷酸钙Ca3(AsO4)23.629×10-3叠氮化钙Ca(N3)245苯甲酸钙Ca(C7H5O2)2·3H2O2.32 2.45 2.723.02 3.424.71 6.878.558.7碳酸氢钙Ca(HCO3)216.1 16.6 17.1 17.5 17.9 18.4溴酸钙Ca(BrO3)2230溴化钙CaBr2125 132 143 213 278 295 312霰石CaCO3-霰石7.753×10-4方解石CaCO3-方解石6.170×10-4氯酸钙Ca(ClO3)2209铬酸钙CaCrO44.5 2.25 1.83 1.49 0.83磷酸二氢钙Ca(H2PO4)21.8氟化钙CaF28.575×10-3氟硅酸钙CaSiF60.518甲酸钙Ca(HCO2)216.1 16.6 17.1 17.5 17.9 18.4磷酸氢钙CaHPO44.303×10-3氢氧化钙Ca(OH)20.1890.1820.1730.160.1410.1218.6×10-27.6×10-2碘酸钙Ca(IO3)29×10-20.24 0.38 0.52 0.65 0.660.67碘化钙CaI264.6 66 67.6 70.8 74 78 81钼酸钙CaMoO44.099×10-3硝酸钙Ca(NO3)2·4H2O102 115 129 152 191 358 363亚硝酸钙Ca(NO2)2·4H2O63.9 84.5 104 134 151 166 178草酸钙CaC2O46.7×10-4高氯酸钙Ca(ClO4)2188高锰酸钙Ca(MnO4)2338磷酸钙Ca3(PO4)22×10-3硒酸钙CaSeO4·2H2O 9.73 9.77 9.22 8.79 7.14硫酸钙CaSO4·2H2O0.2230.2440.2550.2640.2650.2440.2340.205钨酸钙CaWO42.387×10-3氟化锆ZrF41.32硫酸锆Zr(SO4)2·4H2O52.5砷酸镉Cd3(AsO4)27.091×10-6苯甲酸镉Cd(C7H5O2)22.81溴酸镉Cd(BrO3)2125溴化镉CdBr256.3 75.4 98.8 129 152 153 156 160碳酸镉CdCO33.932×10-5氯酸镉Cd(ClO3)2299 308 322 348 376 455氯化镉CdCl2100 135 135 135 135 136 140 147氰化镉Cd(CN)22.2×10-2亚铁氰化镉Cd2Fe(CN)68.736×10-5氟化镉CdF24甲酸镉Cd(HCO2)28.3 11.1 14.4 18.6 25.3 59.5 80.585.294.6氢氧化镉Cd(OH)22.697×10-4碘酸镉Cd(IO3)29.7×10-2碘化镉CdI278.7 84.7 87.9 92.1 100 111 125硝酸镉Cd(NO3)2122 136 150 194 310 713草酸镉CdC2O4.3H2O6.046×10-3高氯酸镉Cd(ClO4)2180 188 195 203 221 243 272磷酸镉Cd3(PO4)26.235×10-6硒酸镉CdSeO472.5 68.4 64 58.9 55 44.2 32.527.222硫酸镉CdSO475.4 76 76.6 78.5 81.8 66.763.160.8硫化镉CdS1.292×10-12钨酸镉CdWO44.642×10-2硝酸铬Cr(NO3)3108 124 130 152高氯酸铬Cr(ClO4)3104 123 130硫酸铬Cr2(SO4)3·18H2O220叠氮化亚汞Hg2(N3)22.727×10-2溴化亚汞Hg2Br21.352×10-6碳酸亚汞Hg2CO34.351×10-7氯化亚汞Hg2Cl23.246×10-5铬酸亚汞Hg2CrO42.313×10-3氰化亚汞Hg2(CN)22.266×10-12高氯酸亚汞Hg2(ClO4)2)282 325 407 455 499 541 580硫酸亚汞Hg2SO44.277×10-2乙酸汞Hg(C2H3O2)225苯甲酸汞Hg(C7H5O2)2·H2O1.1溴酸汞Hg(BrO3)2·2H2O0.08溴化汞HgBr20.3 0.4 0.56 0.66 0.91 1.68 2.77 4.9氯酸汞Hg(ClO3)225氯化汞HgCl23.634.82 6.57 8.34 10.2 16.3 30 61.3氰化汞Hg(CN)29.3碘酸汞Hg(IO3)22.372×10-3碘化汞HgI26×10-3草酸汞HgC2O41.1×10-2硫化汞HgS2.943×10-25硫氰酸汞Hg(SCN)26.3×10-2溴酸钴Co(BrO3)2·6H2O45.5溴化钴CoBr291.9 112 128 163 227 241 257氯酸钴Co(ClO3)2135 162 180 195 214 316氯化钴CoCl243.5 47.7 52.9 59.7 69.5 93.8 97.6 101 106氟化钴CoF21.36氟硅酸钴CoSiF6·6H2O118碘酸钴Co(IO3)2·2H2O1.02 0.9 0.88 0.82 0.73 0.7碘化钴CoI2203硝酸钴Co(NO3)284 89.6 97.4 111 125 174 204 300亚硝酸钴Co(NO2)27.6×0.24 0.4 0.61 0.85物质化学式°C10°C20°C30°C40°C50°C60°C70°C80°C90°C100°C氢氧化铪(III )Hf(OH)34.50305×10-4氢氧化铪(IV)Hf(OH)44.503×10-6氦He0.6 氢氧化钬(III )Ho(OH)32.519×10-5物质化学式0°C10°C20°C30°C40°C50°C60°C70°C80°C90°C100°C氢氧化镓Ga(OH)38.616×10-9草酸镓Ga2(C2O4)3·42O0.4硒酸镓Ga2(SeO4)3·16H2O18.1乙酸钾KC2H3O2216 233 256 283 324 350 381 398砷酸钾K3AsO419叠氮化KN341.446.250.855.861 106钾苯甲酸钾KC7H5O265.870.776.782.1溴酸钾KBrO33.094.726.919.6413.122.734.149.9溴化钾KBr53.659.565.370.775.485.594.999.2104溴铂酸钾K2PtBr61.89碳酸钾K2CO3105 109 111 114 117 127 140 148 156氯酸钾KClO33.3 5.2 7.310.113.923.837.546 56.3氯化钾KCl2831.234.237.240.145.848.851.353.956.3铬酸钾K2CrO456.360 63.766.767.870.174.5氰化钾KCN50 重铬酸钾K2Cr2O74.7 7 12.318.126.345.673砷酸二氢钾KH2AsO419磷酸二氢钾KH2PO414.818.322.6 2835.550.270.483.5铁氰化钾K3Fe(CN)630.238 46 5359.370 91亚铁氰化钾K4Fe(CN)614.321.128.235.141.454.866.971.574.2氟化钾KF44.753.594.9 108 138 142 150甲酸钾KHCO2313 337 361 398 471 580 658碳酸氢钾KHCO322.527.433.739.947.565.6磷酸一氢钾K2HPO4150硫酸氢钾KHSO436.248.654.36176.496.1122氢氧化钾KOH95.7103 112 126 134 154 178碘酸钾KIO34.66.278.0810.312.618.324.832.3碘化钾KI128 136 144 153 162 168 176 192 198 206 硝酸钾KNO313.921.931.645.361.3106 167 203 245亚硝酸钾KNO2279 292 306 320 329 348 376 390 410草酸钾K2C2O425.531.936.439.943.853.263.669.275.3高氯酸钾KClO40.761.061.682.563.737.313.417.722.3高碘酸钾KIO40.170.280.420.651 2.1 4.4 5.9高锰酸钾KMnO42.834.316.349.0312.622.1过二硫酸钾K2S2O84.7磷酸钾K3PO481.592.3 108 133硒酸K2SeO4107 109 111 113 115 119 121 122钾硫酸钾K2SO47.4 9.3 11.1 1314.818.221.422.924.1四苯硼钾KBC24H201.8×10-5硫氰酸钾KSCN177 198 224 255 289 372 492 571 675硫代硫酸钾K2S2O396 155 175 205 238 293 312钨酸钾K2WO451.5三氯化金AuCl368三碘化金AuI31.295×10-10镧×10-2钼酸镧La2(MoO4)32.473×10-3硝酸镧La(NO3)3100 136 168 247硒酸镧La2(SeO4)350.545 45 45 4518.55.4 2.2硫酸镧La2(SO4)332.722.33 1.91.671.260.910.790.68钨酸镧La2(WO4)3·3H2O 6.06乙酸锂LiC2H3O231.235.140.850.668.6叠氮化锂LiN361.364.267.271.275.486.6100苯甲酸锂LiC7H5O238.941.644.753.8溴酸锂LiBrO3154 166 179 198 221 269 308 329 355溴化锂LiBr143 147 160 183 211 223 245 266 碳酸Li2CO3 1.5 1.4 1.33 1.2 1.1 1.0 1.00.80.72锂 4 3 6 7 8 1 5氯酸锂LiClO3241 283 372 488 604 777氯化锂LiCl69.274.583.586.289.898.4112 121 128铬酸锂Li2CrO4.2H2O142重铬酸锂Li2Cr2O7.2H2O151磷酸二氢锂LiH2PO4126氟化锂LiF0.16氟硅酸锂Li2SiF6.2H2O73甲酸锂LiHCO232.335.739.344.149.564.792.7116 138亚磷酸氢锂Li2HPO34.439.977.617.116.03氢氧化锂LiOH12.712.712.812.913.13.313.815.317.5碘化锂LiI151 157 165 171 179 202 435 440 481钼酸锂Li2MoO482.679.579.578 73.9硝酸锂LiNO353.460.870.1 138 152 175亚硝酸锂LiNO270.982.596.8 114 133 177 233 272 324草酸锂Li2C2O48高氯酸锂LiClO442.749 56.163.672.392.3128 151高锰酸锂LiMnO471.4磷酸锂Li3PO43.821×10-2硒化锂Li2Se57.7亚硒酸锂Li2SeO32523.321.519.617.914.711.911.19.9硫酸锂Li2SO436.135.534.834.233.732.631.430.9酒石酸锂Li2C4H4O64231.827.126.627.229.5硫氰酸锂LiSCN114 131 153钒酸锂LiVO32.5 4.826.284.382.67二氧化硫SO29.4氢氧化镥(III )Lu(OH)31.164×10-5硫酸镥(III )Lu2(SO4)3·8H2O57.9氯化铝AlCl343.944.945.846.647.348.148.649氟化铝AlF30.560.560.670.780.911.11.321.72硝酸铝Al(NO3)36066.773.981.888.7106 132 153 160高氯酸铝Al(ClO4)3122 128 133物质化学式0°C10°C20°C30°C40°C50°C60°C70°C80°C90°C100°C乙酸镁Mg(C2H3O2)256.759.753.468.675.7118苯甲酸镁Mg(C7H5O2)2·H2O 5溴酸镁Mg(BrO3)2·6H2O58溴化镁MgBr298 99 101 104 106 112 125碳酸镁MgCO33.9×10-2氯酸镁Mg(ClO3)2114 123 135 155 178 242 268氯化镁MgCl252.953.654.655.857.56166.169.573.3铬酸镁MgCrO4·7H2O137氟化镁MgF27.325×10-3氟硅酸镁MgSiF626.330.834.944.4甲酸镁Mg(HCO2)21414.214.414.915.917.920.522.222.9氢氧化镁Mg(OH)29.628×10-4碘酸镁Mg(IO3)27.2 8.6 1011.715.215.515.6碘化镁MgI2120 140 173 186钼酸镁MgMoO413.7硝酸镁Mg(NO3)262.166 69.573.678.978.991.6106草酸镁MgC2O40.104高氯酸镁Mg(ClO4)249.6磷酸镁Mg3(PO4)22.588×10-4硒酸镁MgSeO42030.438.344.348.655.8亚硒酸镁MgSeO35.454×10-2硫酸镁MgSO42228.233.738.944.554.655.852.950.4硫代硫酸镁MgS2O350溴化锰MnBr2127 136 147 157 169 197 225 226 228碳酸锰MnCO34.877×10-5氯化锰MnCl263.468.173.980.888.5109 113 114 115亚铁氰化锰Mn2Fe(CN)61.882×10-3氟化锰MnF210.60.670.440.48氟硅酸锰MnSiF6·6H2O140氢氧化锰Mn(OH)23.221×10-4硝酸锰Mn(NO3)2102 118 139 206草酸锰MnC2O4·2H22×10-22.4×10-22.8×10-23.3×10-2硫酸锰MnSO452.959.762.962.96053.645.640.935.3物质化学式0°C10°C20°C30°C40°C50°C60°C70°C80°C90°C100°C乙酸钠CH3COONa36.240.846.454.665.6139 153 161 170叠氮化钠NaN338.939.940.8苯甲酸钠NaC7H5O253.0溴酸钠NaBrO324.230.336.442.648.862.675.790.8溴化钠NaBr80.285.290.898.4107 118 120 121 121碳酸钠Na2CO3712.521.539.749 4643.943.9氯酸钠NaClO379.687.695.9 105 115 137 167 184 204氯化钠NaCl35.735.835.936.136.437.13838.539.2铬酸Na2CrO431.50.84 88 96 115 125 126钠7 1氰化钠NaCN40.848.158.771.2水解重铬酸钠Na2Cr2O7163 172 183 198 215 269 376 405 415磷酸二氢钠NaH2PO456.569.886.9 107 133 172 211 234氟化钠NaF3.664.064.224.44.684.895.08甲酸钠HCOONa43.962.581.2 102 108 122 138 147 160碳酸氢钠NaHCO37 8.1 9.611.112.716氢氧化钠NaOH98 109 119 129 174碘酸钠NaIO32.484.598.0810.713.319.826.629.533碘化钠NaI159 167 178 191 205 257 295 302钼酸钠Na2MoO444.164.765.366.968.671.8硝酸钠NaNO37380.887.694.9102 122 148 180亚硝酸钠NaNO271.275.180.887.694.9111 113 160草酸钠Na2C2O42.693.053.413.814.184.935.716.5高氯酸钠NaClO4167 183 201 222 245 288 306 329高碘酸钠NaIO41.835.6 10.319.930.4磷酸钠Na3PO44.5 8.2 12.116.320.220.96068.177焦磷酸钠Na4P2O72.26硒酸钠Na2SeO413.325.226.9 7781.878.674.873 72.7硫酸钠Na2SO44.9 9.1 19.540.848.845.343.742.742.5硫代硫酸钠Na2S2O371.57377.690.897.2溴酸镍Ni(BrO3)2·6H2O28溴化镍NiBr2113 122 131 138 144 153 154 155碳酸镍NiCO39.643×10-4氯酸镍Ni(ClO3)2111 120 133 155 181 221 308氯化镍NiCl253.456.366.870.673.281.286.687.6氟化镍NiF22.552.562.562.59碘酸镍Ni(IO3)20.746.2×10-21.43碘化镍NiI2124 135 148 161 174 184 187 188硝酸镍Ni(NO3)279.294.2 105 119 158 187 188高氯酸镍Ni(ClO4)2105 107 110 113 117焦磷酸镍Ni2P2O71.017×10-3硫酸镍NiSO4·6H2O44.446.649.255.664.570.176.7乙酸钕(III )Nd(C2H3O2)3·H2O26.2溴酸钕(III )Nd(BrO3)343.959.275.695.2116氯化钕(III )NdCl396.79899.6102 105钼酸钕(III )Nd2(MoO4)31.9×10-3硝酸钕(III )Nd(NO3)3127 142 145 159 211硒酸钕(III )Nd2(SeO4)345.244.641.839.939.943.97 3.3硫酸钕(III Nd2(SO4)313 9.7 7.1 5.3 4.1 2.8 2.2 1.2物质化学式0°C10°C20°C30°C40°C50°C60°C70°C80°C90°C100°C硼酸H3BO35.7三氧化二硼B2O32.2碳酸铍BeCO30.218氯化铍BeCl242 42钼酸铍BeMoO43.02硝酸铍Be(NO3)297 102 108 113 125 178草酸铍BeC2O4·3H2O63.5高氯酸铍Be(ClO4)2147硒酸BeSeO4·4H2O49硫酸铍BeSO43737.639.141.445.853.167.282.8硫化钋(II)PoS2.378×10-14乙酸镨(III )Pr(C2H3O2)3·H2O32溴酸镨(III )Pr(BrO3)355.973 91.8 114 144氯化镨(III )PrCl3104钼酸镨(III )Pr2(MoO4)31.5×10-3硝酸镨(III )Pr(NO3)3112 162 178硫酸镨(III Pr2(SO4)319.815.612.69.892.565.043.5 1.1 0.91物质化学式0°C10°C20°C30°C40°C50°C60°C70°C80°C90°C100°C砷化氢AsH38×10-2氯化氢HCl81 75 7065.56157.553 50 47 43 40硫化氢H2S0.33乙酸铅Pb(C2H3O2)219.829.544.369.8116叠氮化铅Pb(N3)22.49×10-2溴酸铅Pb(BrO3)27.92溴化PbBr20.450.630.861.121.52.293.323.864.55碳酸铅PbCO37.269×10-5氯酸铅Pb(ClO3)23.7×10-2氯化铅PbCl20.670.821 1.2 1.42 1.94 2.542.883.2铬酸铅PbCrO41.71×10-5亚铁氰化铅PbFe(CN)65.991×10-4氟化铅PbF24.634×10-2氟硅酸铅PbSiF6190 222 403 428 463磷酸氢PbHPO43.457×10-4亚磷酸氢铅PbHPO32.187×10-2氢氧化铅Pb(OH)21.615×10-4碘酸铅Pb(IO3)22.4×10-3碘化铅PbI24.4×10-25.6×10-26.9×10-29×10-20.1240.1930.2940.42钼酸铅PbMoO41.161×10-5硝酸铅Pb(NO3)237.546.254.363.472.1 91.6 111 133草酸铅PbC2O46.495×10-4高氯酸Pb(ClO4)2·3H2O440硒酸铅PbSeO41.31×10-2硫酸铅PbSO43.836×10-3硫化铅PbS6.767×10-13酒石酸铅PbC4H4O62.5×10-3硫氰酸铅Pb(SCN)20.553硫代硫酸铅PbS2O32.02×10-2钨酸铅PbWO42.838×10-2氢氧化Pb(OH)47.229×物质化学式0°C10°C20°C30°C40°C50°C60°C70°C80°C90°C100°C乙酸铷RbC2H3O286溴酸铷RbBrO33.6 5.1溴化铷RbBr90 99 108 119 132 158 氯酸铷RbClO32.13.1 5.4 8 11.6 22 38 49 63氯化铷RbCl77 84 91 98 104 115 127 133 143 铬酸铷Rb2CrO462 67.5 73.6 78.9 85.6 95.7重铬Rb2Cr2O75.9 10 15.2 32.3铷氟化铷RbF300 氟硅酸铷Rb2SiF60.157甲酸铷RbHCO2443 554 614 694 900碳酸氢铷RbHCO3110氢氧化铷RbOH180 碘酸铷RbIO31.96碘化铷RbI144硝酸RbNO319.5 33 52.9 81.2 117 200 310 374 452物质化学式0°C10°C20°C30°C40°C50°C60°C70°C80°C90°C100°C乙酸铯CsC2H3O21010叠氮化铯CsN3307溴酸铯CsBrO30.213.664.535.3。
高中化学方程式总结及公式大全(完整版)

高中化学方程式总结及公式大全(完整版)高中化学的方程式注意不能死记硬背,要根据公式去配平,这样不仅不容易出错,而且记忆效果也比较好。
以下是整理的一些高中化学方程式总结及公式大全,欢迎阅读参考。
高中化学方程式记忆窍门1:实验联想法从生动直观到抽象思维,化学方程式是化学实验的忠实和本质的描述,是实验的概括和总结。
因此,依据化学实验来记忆有关的化学反应方程式是最行之有效的。
例如,在加热和使用催化剂(MnO2)的条件下,利用KClO3分解来制取氧气。
只要我们重视实验之情景,联想白色晶体与黑色粉末混和加热生成氧气这个实验事实,就会促进对这个化学反应方程式的理解和记忆。
2:反应规律法化学反应不是无规律可循。
化合、分解、置换和复分解等反应规律是大家比较熟悉的,这里再强调一下氧化——还原反应规律。
如,FeCl3是较强的氧化剂,Cu是不算太弱的还原剂,根据氧化——还原反应总是首先发生在较强的氧化剂和较强的还原剂之间这一原则,因而两者能发生反应:2FeCl3+Cu=CuCl2+2FeCl2而相比之下,CuCl2与FeCl2是较弱的氧化剂与还原剂,因而它第1页共7页们之间不能反应。
3:编组法索引能概括全体,而编组能突出局部,是一种主题鲜明、有针对性的表现形式。
两者相互补充,异曲同工。
例如,关于铝元素的一组方程式是:①AlCl3+3NH3·H2O=Al(OH)3↓+3NH4Cl②Al2O3+2NaOH=2NaAlO2+H2O③2Al+2NaOH+2H2O=2NaAlO2+3H2↑④Al(OH)3+NaOH=NaAlO2+2H2O⑤Al2S3+6H2O=3H2S↑+2Al(OH)3↓⑥2Al3++3CO32-+3H2O=2Al(OH)3↓+3CO2⑦2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-4:索引法索引法是从总体上把学过的方程式按章节或按反应特点,分门别类地编号、排队,并填写在特制的卡片上,这样就组成一个方程式系统。
高中化学有机化合物知识点总结

高中化学有机物知识点总结一、重要的物理性质1.有机物的溶解性(1)难溶于水的有:各类烃、酯、绝大多数高聚物、高级的(指分子中碳原子数目较多的,下同)醇、醛、羧酸等。
(2)易溶于水的有:低级的[一般指N(C)≤4]醇、醛、羧酸及盐、氨基酸及盐、单糖、二糖。
(3)具有特殊溶解性的:①乙醇是一种很好的溶剂,既能溶解许多无机物,又能溶解许多有机物。
②乙酸乙酯在饱和碳酸钠溶液中更加难溶,同时饱和碳酸钠溶液还能通过反应吸收挥发出的乙酸,溶解吸收挥发出的乙醇,便于闻到乙酸乙酯的香味。
③有的淀粉、蛋白质可溶于水形成胶体..。
蛋白质在浓轻金属盐(包括铵盐)溶液中溶解度减小,会析出(即盐析,皂化反应中也有此操作)。
④线型和部分支链型高聚物可溶于某些有机溶剂,而体型则难溶于有机溶剂。
⑤氢氧化铜悬浊液可溶于多羟基化合物的溶液中,如甘油、葡萄糖溶液等,形成绛蓝色溶液。
2.有机物的密度小于水的密度,且与水(溶液)分层的有:各类烃、酯(包括油脂)3.有机物的状态[常温常压(1个大气压、20℃左右)](1)气态:①烃类:一般N(C)≤4的各类烃注意:新戊烷[C(CH3)4]亦为气态②衍生物类:一氯甲烷(....,沸点为...HCHO...).....-.21℃...-.24.2℃.....CH..3.Cl..,.沸点为.....).甲醛((2)液态:一般N(C)在5~16的烃及绝大多数低级衍生物。
如,己烷CH3(CH2)4CH3甲醇CH3OH甲酸HCOOH 乙醛CH3CHO★特殊:不饱和程度高的高级脂肪酸甘油酯,如植物油脂等在常温下也为液态(3)固态:一般N(C)在17或17以上的链烃及高级衍生物。
如,石蜡C12以上的烃饱和程度高的高级脂肪酸甘油酯,如动物油脂在常温下为固态4.有机物的颜色☆绝大多数有机物为无色气体或无色液体或无色晶体,少数有特殊颜色☆多羟基有机物如甘油、葡萄糖等能使新制的氢氧化铜悬浊液溶解生成绛蓝色溶液;☆淀粉溶液(胶)遇碘(I2)变蓝色溶液;☆含有苯环的蛋白质溶胶遇浓硝酸会有白色沉淀产生,加热或较长时间后,沉淀变黄色。
高中人教版化学选择性必修二:溶解性 手性 无机含氧酸分子的酸性

二、手性与无机含氧酸的酸性 1.手性: (1)手性异构体:具有完全相同的_组__成__和__原__子__排__列__的一对分子,如同左手与右手 一样互为_镜__像__,却在三维空间里不能_重__叠__,互称手性异构体。 (2)手性分子:有_手__性__异__构__体__的分子叫做手性分子。 (3)手性碳原子:在有机物分子中,连有_四__个__不__同__基__团__或__原__子__的碳原子。含有手 性碳原子的分子是手性分子,如
【合作探究】 (1)极性分子一定易溶于极性溶剂,非极性分子一定易溶于非极性溶剂吗? 提示:不一定,相似相溶原理只是一般性规律,也有例外情况。如CO、NO均为极性 分子,但难溶于水;CO2为非极性分子,但在苯中溶解度不大。 (2)下列物质在水中有较大的溶解度,最主要的原因分别是什么?①HF ②HCl ③Cl2。 提示:影响物质的溶解性有多种因素,如形成氢键、分子的极性相似相溶、分子 结构相似相溶、发生反应溶解度增大。其中HF易溶于水最主要原因是能与水分 子间形成氢键;HCl因为是极性分子,与水相似相溶;Cl2是因为能与水反应。
【典例示范】 【典例】(2020·泉州高二检测)判断含氧酸酸性强弱的一条经验规律是含氧酸 分子结构中含非羟基氧原子数越多,该含氧酸的酸性越强。如表所示: 含氧酸酸性强弱与非羟基氧原子数的关系
次氯酸
磷酸
硫酸
高氯酸
含氧酸
Cl—OH
非羟基氧 原子数
酸性
0 弱酸
1 中强酸
2 强酸
3 最强酸
(1)亚磷酸H3PO3和亚砷酸H3AsO3分子式相似,但它们的酸性强弱相差很大,H3PO3 是中强酸,H3AsO3既有弱酸性又有弱碱性。由此可知它们的结构式分别为 ①______________________, ②________________。 (2)H3PO3和H3AsO3与过量的NaOH溶液反应的化学方程式分别是 ①______________________________________________________________, ②______________________________________________________________。 (3)在H3PO3和H3AsO3中分别加入浓盐酸,分析反应情况________________,写出反 应的化学方程式________________________________ __。
高中化学盐溶解性表及元素周期表
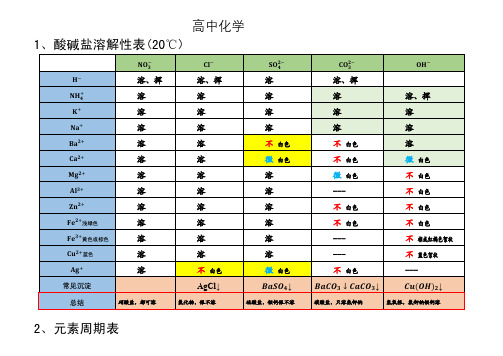
高中化学盐溶解性表及元素周期表
1、酸碱盐溶解性表(20℃)
−
−
−
−
−
−
溶、挥
溶、挥
溶
溶、挥
+
溶
溶
溶
溶
溶、挥
+
溶
溶
溶
溶
溶
+
溶
溶
溶
溶
溶
+
溶
溶
不
白色
不
白色
溶
&色
不
白色
微
白色
+
溶
溶
溶
微
白色
不
白色
+
溶
溶
溶
---
不
白色
+
溶
溶
溶
不
白色
不
白色
+ 浅绿色
溶
溶
溶
不
白色
不
白色
+ 黄色或棕色
溶
溶
溶
---
不
棕或红褐色絮状
+ 蓝色
溶
溶
溶
---
不
蓝色絮状
溶
不
不
---
+
AgCl↓
常见沉淀
总结
白色
硝酸盐,都可溶
2、元素周期表
氯化物,银不溶
微
白色
↓
高中化学常见物质特殊性质归纳

常见物质特殊性质归纳:一. 极易溶于水地气体:NH3,HCl,HBr,易溶于水地气体:NO2,SO2,能溶于水地气体:CO2,Cl2,H2S,难溶于水地气体:H2,CO,C2H2,C2H4,O2,NO,能和水反应地气体:Cl2,F2,Br2,NH3,NO2,CO2,SO2.2. 易液化地气体:NH3,Cl2,SO23. 有毒有害地气体:F2,O2,HF,Cl2,H2S,SO2,CO,NO,NO2,Br2蒸汽4. 有颜色地气体:NO2,Cl2,F2(淡黄绿色),Br25. 有气味地气体:NH3,NO2,SO2,H2S6. 有还原性气体:H2,CO,NH3,H2S,HCl,SO2有氧化性气体:O2,Cl2,NO2,CO2,Br2,F2,O37. 常见地单质气体:H2,O2,N2,Cl28. 有漂白性地气体:Cl2(潮湿),SO2,O39. 能使澄清石灰水变浑浊地气体:CO2,SO2,HF,变浑浊后又能澄清地气体:CO2,SO2一0. 能使石蕊变红色地气体:HX,H2S,SO2,CO2,NO2,Br2,特别地:Cl2先变红,后褪色一一. 能使Br2水,酸性KMnO4褪色地气体:H2S,SO2,C2H2,C2H4一2. 能和AgNO3反应生成沉淀地气体:Cl2,Br2,H2S,HCl,HI,NH3一3. 能使无水CuSO4变色:H2O一4. 遇氨气有白烟现象产生地物质:HCl,HNO3,[Cl2(可以)]一5. 在空气中产生白雾地气体:HF,HCl,HBr一6. 能使淀粉KI试纸变蓝色地物质:[Cl2,Br2,NO2,O3](气体),[FeCl3溶液,酸性KMnO4溶液,HNO3溶液](其他)一7. 能使湿润地Pb(NO3)2或PbAc2试纸变黑色地气体:H2S一8. 能使湿润地品红试纸褪色地气体:SO2,Cl2一9. 可燃烧地气体:H2,CO,H2S,C2H2,C2H4,CH4,20. 在空气中燃烧时,火焰呈淡蓝色或蓝色地物质:H2,CO,CH4,H2S,S,C2H5OH2一. 在空气中因氧化变质地气体;NO,22. 常作为保护气体地气体:N2,Ar,23. 不用H2SO4干燥地气体:NH3,H2S,HBr,HI,不能用无水CaCl2干燥地气体:NH3(生成CaCl2·8NH3)24. 只用排水集气法收集地气体:CO,N2,NO,C2H4只用排空气法收集地气体:NO2,NH3,HCl用饱和盐溶液收集地气体:Cl2(排饱和NaCl),CO2(排饱和NaHCO3),H2S(排饱和NaHS)25. 使用启普发生器制取地气体:H2,CO2,H2S26. 常温下由于发生反应而不能共存地气体:H2S/SO2,Cl2/H2S,HI/Cl2,NH3/HCl,NO/O2,F2/H2,Cl2/NH3焰色反应:钠Na 黄锂Li 紫红钾K浅紫铷Rb 紫铯Cs 紫红钙Ca 砖红色锶Sr 洋红铜Cu 绿钡Ba 黄绿稀有气体放电颜色:He 粉红Ne 鲜红Ar 紫Xe 蓝常见物质地物理性质归纳:一.颜色地规律:(一)常见物质颜色①以红色为基色地物质红色:难溶于水地Cu,Cu2O,Fe2O3,HgO等。
人教版高中化学选修4《难溶电解质的溶解平衡》

难溶电解质的溶解平衡一、难溶电解质的溶解平衡1.固体物质的溶解度(S)与溶解性的关系溶解性难溶微溶可溶易溶S的范围S<0.01 g 0.01 g<S<1 g 1 g <S<10 g S>10 g 2. 溶解平衡状态:在一定温度下,固体溶质在水中形成饱和溶液时,溶液中溶质质量保持不变的状态,该状态下,固体溶质溶解的速率和溶液中溶质分子结晶的速率达到相等,但溶解和结晶仍在进行。
3.沉淀溶解平衡(1)概念在一定温度下,当沉淀溶解和生成的速率相等时,即建立了动态平衡,叫做难溶电解质的溶解平衡。
如AgCl溶于水的溶解平衡表示为:(2)特征逆:沉淀的溶解是一个过程动:动态平衡等:溶解速率和沉淀速率相等定:平衡状态时,溶液中离子的浓度保持不变变:当外界条件改变时,溶解平衡发生移动练习:1.已知溶解平衡Mg(OH)2 Mg2+(aq)+2OH-(aq),请分析当下列条件改变时,对该溶解平衡的影响,填写下表,并归纳其影响因素。
条件改变移动方向c(Mg2+) c(OH-)加水向右减小减小升温向右增大增大加MgCl2(s) 向左增大减小2.从物质类别、变化过程角度分析沉淀溶解平衡与弱电解质的电离平衡有何区别?答案(1)从物质类别看,难溶电解质可以是强电解质,也可以是弱电解质[如BaSO4是强电解质,而Al(OH)3是弱电解质],而难电离物质只能是弱电解质。
(2)从变化的过程来看,沉淀溶解平衡是指已溶解的溶质与未溶解的溶质之间形成沉淀与溶解的平衡状态;而电离平衡则是指已经溶解在溶液中的弱电解质分子与离子之间的转化达到平衡状态。
二、影响沉淀溶解平衡的因素:(1)内因:溶质本身的性质。
绝对不溶的物质是没有的;同是微溶物质,溶解度差别也很大;易溶溶质只要是饱和溶液也存在溶解平衡。
(2)外因:①浓度:加水,平衡向溶解方向移动。
②温度:升温,多数平衡向溶解方向移动;少数平衡向生成沉淀的方向移动,如Ca(OH)2的溶解平衡。
③同离子效应:向平衡体系中加入相同的离子,使平衡向生成沉淀的方向移动。
使用溶解性表书写离子方程式问题例析

非常道Җ㊀甘肃㊀石兴龙㊀㊀在高中化学离子反应 教学和高考复习中,常要借助教材中 部分酸㊁碱和盐的溶解性表(室温) (以下简称 表 )中物质溶解性书写离子方程式,从学生平时练习和考前检测中常出现的错误可以看出,学生在使用 表 时常感到困惑,出现了不少问题.现以近几年部分高考选择题解答为例,进行问题讨论,点评小结,让学生明晰产生错误的原因,以减少问题的发生.1㊀应用物质溶解性书写离子方程式1 1㊀注意微溶物处理例1㊀下列离子方程式书写是否正确(㊀㊀).(2017年浙江卷)澄清石灰水中通入过量C O 2:C O 2+OH -=H C O -3.分析㊀澄清石灰水中微溶物C a (O H )2电离成C a2+和OH -,书写离子方程式时要改写成离子.通入少量C O 2离子方程式为C a 2++2O H -+C O 2=C a C O 3ˌ+H 2O ;通入过量C O 2时,C O 2与H 2O ㊁C O 2-3反应生成H C O -3,使c (C O 2-3)减小,C a C O 3沉淀溶解平衡移动,生成能溶于水的C a (H C O 3)2,离子方程式为C O 2+OH -=H C O -3,该离子方程式正确.B a (O H )2溶液通入少量㊁足量C O 2㊁S O 2的离子方程式写法与本题相似.教材中的 表 显示M g C O 3㊁C a S O 4㊁A g 2S O 4是微溶物,如纯碱溶液中滴入氯化镁溶液,离子方程式为M g 2++C O 2-3=M g C O 3ˌ;硫酸钠溶液加入澄清石灰水,离子方程式为C a 2++S O 2-4=C a S O 4ˌ;硝酸银溶液中加入硫酸钾溶液,离子方程式为2A g ++S O 2-4=A g 2S O 4ˌ.表 中没有列出的物质(如M g S O 3㊁P b C l 2㊁H g 2S O 4)也是微溶物,一些没有列出或说明溶解性的(如C a (H C O 3)2㊁C a (H S O 3)2㊁B a (H C O 3)2㊁B a (H S O 3)2㊁磷酸氢盐(除B a H P O 4㊁C a H P O 4)㊁磷酸二氢盐等能溶于水),这些物质的溶解性在书写离子方程式时要注意学习应用.写离子方程式时,反应物中微溶物的澄清溶液要改写成离子,悬浊液写化学式,生成物中的微溶物写化学式;如果弱酸酸式盐溶于水,要改写成离子,但弱酸酸式酸根不能拆写;强酸酸式盐(如N a H S O 4)在水中完全溶解电离,要拆写成离子(N a +㊁H +㊁S O 2-4).1 2㊀注意难溶物沉淀转化例2㊀下列离子方程式书写是否正确(㊀㊀).(2018年江苏卷)饱和N a 2C O 3溶液与C a S O 4固体反应:C O 2-3+C a S O 4=C a C O 3+S O 2-4.分析㊀C a C O 3是难溶物,C a S O 4是微溶物,结合C a 2+能力:C O 2-3>S O 2-4,使c (C a 2+)和c (C O 2-3)减小,促使微溶物C a S O 4沉淀溶解平衡移动,生成难溶的C a C O 3,离子方程式为:C O 2-3+C a S O 4=C a C O 3+S O 2-4,反应前后均出现微溶物或难溶物,不标ˌ,该离子方程式正确.相似的离子反应有,向F e C l 3溶液中加入M g (O H )2:3M g (O H )2+2F e 3+=2F e (O H )3+3M g 2+.反应中M g (O H )2和F e (O H )3都是难溶物,但K s p [F e (O H )3]更小,F e (O H )3溶解性更小,所以生成更难溶的F e (O H )3.C a 2+㊁M g 2+的碳酸氢盐与碱溶液(如澄清石灰水㊁B a (O H )2等)也会发生沉淀转化,产物与碱的用量有关.如M g (H C O 3)2溶液加入少量石灰水:M g 2++2OH -=M g (O H )2ˌ;M g (H C O 3)2溶液加入足量石灰水虽有M g C O 3微溶物生成,但在O H -足量时转化为M g (O H )2;比较K s p 大小,M g (O H )2㊁C a C O 3比M g C O 3更难溶㊁更稳定,所以离子方程式为M g 2++2H C O -3+2C a 2++4O H -=M g (O H )2ˌ+2C a C O 3ˌ+2H 2O.C a (H C O 3)2溶液中加入少量B a (O H )2溶液:C a 2++2H C O -3+B a 2++2O H -=C a C O 3ˌ+B a C O 3ˌ+2H 2O ;C a (H C O 3)2溶液加入足量B a (O H )2溶液:B a 2++H C O -3+OH -=B a C O 3ˌ+H 2O.B a 2+过量时,主要生成B a C O 3沉淀.表 中没有列出或说明的除含K +㊁N a +㊁N H +4的硅酸盐㊁亚硫酸盐㊁硫化物㊁磷酸盐能溶于水外,其他金属离子的盐大多难溶于水,这些物质的溶解性,在学习中要逐步掌握应用.应用 表 时要把 表 中标 不 的物质理解为难 ,因难溶物在水中存在沉淀溶解平衡,溶解量虽少,但总能溶解一部分,要把物质溶解性大小与碱性强弱㊁电解质强弱区分开来.如在 表 中标 不 的76非常道M g (O H )2,难溶于水,事实上M g (OH )2是中强碱,也是强电解质; 表 中标 不 的B a C O 3㊁B a S O 4等难溶物,虽难溶于水,但都是强电解质.若反应中出现几种难溶物,要考虑沉淀溶解平衡移动和沉淀转化,依据物质在常温下水中溶度积常数K s p 来比较溶解性大小,K s p 越小,溶解性越小.2㊀水解反应的离子方程式书写2 1㊀注意水解规律的应用例3㊀下列反应的离子方程式是否正确(㊀㊀).(2019年天津卷)向沸水中滴加饱和氯化铁溶液得到红褐色液体:F e 3++3H 2O=F e (O H )3+3H +.分析㊀F e (O H )3是难溶物,含F e 3+的可溶性强酸盐溶液水解显弱酸性,p H<7,存在水解平衡,受热水解反应加剧,形成胶体,两边用 ә连接,离子方程式为F e 3++3H 2O әF e (O H )3(胶体)+3H +,该离子方程式错误.明矾净水原理为A l 3++3H 2O⇌A l (O H )3(胶体)+3H +.含C O 2-3㊁S O 2-3㊁P O 3-4㊁H P O 2-4可溶性强碱盐溶液水解显弱碱性,主要以第一步为主,两边用 ⇌连接;如N a 2C O 3溶液中C O 2-3水解,分步写为C O2-3+H 2O⇌H C O -3+O H -,H C O -3+H 2O ⇌H 2C O 3+O H -,由此可判断出N a 2C O 3溶液中离子种类和浓度大小.含H C O -3㊁H 2P O -4的可溶性强碱盐溶液中存在微弱水解和电离,水解程度大于电离程度,溶液显弱碱性,p H>7,离子方程式写法相似;但H S O -3可溶性强碱盐溶液显弱酸性,因溶液中H S O -3的电离程度大于水解程度.表 中没有列出N a 2S ㊁K 2S ㊁B a S ㊁C a S 在水溶液中易水解,放出有毒H2S 气体,要注意密封保存.含弱碱根㊁弱酸根或弱酸酸式根离子的可溶性盐在溶液中发生水解,水参加反应,离子方程式两边用 ⇌ 连接;书写时注意水解规律(如谁强显谁性㊁越弱越水解㊁越热越水解)应用.2 2㊀注意溶液中发生的双水解反应例4㊀下列反应的离子方程式是否正确(㊀㊀).(2017年海南卷)向硫酸铝溶液中滴加碳酸钠溶液:2A l 3++3C O 2-3=A l 2(C O 3)3ˌ.分析㊀C O 2-3是二元弱酸根,与A l 3+在溶液中发生双水解反应:2A l 3++3C O 2-3+3H 2O =2A l (O H )3ˌ+3C O 2ʏ,双水解较为彻底,用 = 连接,沉淀标ˌ,气体标ʏ,该离子方程式错误.表 中标 - 的含F e 3+㊁F e 2+㊁A l 3+㊁C O 2-3或H C O -3的盐在溶液中发生双水解;在 表 中没有列出的(N H 4)2S ,在溶液中发生双水解,放出N H 3和有毒H 2S 气体,取用时要注意密封保存. 表 中标 - 的含C u 2+与C O 2-3的盐在溶液中既生成沉淀,又发生水解;生成沉淀:C u 2++C O 2-3=C u C O 3ˌ;发生双水解:C u 2++C O 2-3+H 2O =C u (O H )2ˌ+C O 2ʏ,总反应为2C u 2++2C O 2-3+H 2O=C u 2(O H )2C O 3ˌ+C O 2ʏ. 表 中标 - 的金属阳离子(如H g +㊁H g 2+㊁A g +)与O H -反应,产物不稳定,发生分解.如A g +与O H -生成白色沉淀,能短暂存在,久置分解成棕褐色A g 2O ,离子方程式为A g ++O H -=A g OHˌ,2A g O H=A g 2O+H 2O.含弱碱根㊁弱酸根或弱酸酸式根离子组成的盐在溶液中发生双水解反应,反应较为彻底,仍用 = 连接,沉淀标ˌ,气体标ʏ,H 2O 参加反应,不能漏写.3㊀反应物浓度、性质影响反应产物的离子方程式书写例5㊀下列反应的离子方程式是否正确(㊀㊀).(2019年天津卷)氧化亚铁溶于稀HN O 3:F e O+2H +=F e 2++H 2O.分析㊀H N O 3表现酸性和氧化性,稀HN O 3被还原,放出无色N O 气体,浓H N O 3被还原,放出红棕色N O 2气体;F e O 溶于稀H N O 3㊁浓H N O 3离子方程式分别为3F e O+10H ++N O -3=3F e 3++N Oʏ+5H 2O ,F e O+4H ++N O -3=F e 3++N O 2ʏ+2H 2O ,该离子方程式错误.随浓度增大,H N O 3的氧化性增强,HN O 3的性质如强氧化性㊁不稳定性㊁挥发性都是考试的热点,要引起重视.在 表 中盐酸㊁碳酸㊁硝酸用 溶㊁挥 标示,但要根据具体性质理解应用.把浓盐酸㊁浓硝酸试剂瓶盖打开,瓶口出现 白雾 ,说明具有挥发性;盐酸挥发放出H C l 气体,盐酸要密封低温保存;实际反应中C O 2-3与少量H +反应生成H C O -3,与足量H +反应生成不稳定的H 2C O 3,挥发放出的是H 2C O 3分解后的C O 2;HN O 3见光或受热易分解,实际上硝酸挥发气体成分中有HN O 3蒸气㊁N O 或N O2气体,硝酸要密封低温避光保存.受反应物浓度㊁性质影响,反应现象㊁生成物也会发生变化;书写时注意元素化合物性质知识的应用;涉及氧化还原反应,书写时注意检查是否符合 三守恒 规律.86非常道4㊀反应物用量影响反应产物的离子方程书写例6㊀下列反应的离子方程式是否正确(㊀㊀).(2020年浙江卷)(N H 4)2F e (S O 4)2溶液与少量B a (O H )2溶液反应:S O 2-4+B a 2+=B a S O 4ˌ.分析㊀(N H 4)2F e (S O 4)2溶于水,完全电离,与少量B a (O H )2溶液反应:F e 2++S O 2-4+Ba 2++2O H -=B a S O 4ˌ+F e (O H )2ˌ;与足量B a (O H )2溶液反应时,O H -与N H +4生成N H 3 H 2O :2NH +4+F e 2++2S O 2-4+2B a 2++4O H -=2B a S O 4ˌ+F e (O H )2ˌ+2N H 3 H 2O ,该离子方程式错误.N H +4与O H -的反应产物,在 表 中用 溶㊁挥 标示.实际上N H+4与足量O H -反应,稀溶液中产物主要是N H 3 H 2O ,浓度很大或加热时挥发放出的是N H 3,标ʏ.含A l3+的可溶性盐溶液与含O H -的碱溶液反应,生成 表 中标 不 的难溶物A l (O H )3,实际反应与O H -量有关.O H -少量时,生成物为A l (O H )3,当O H -过量时,A l (O H )3发生酸式电离,生成偏铝酸盐而溶解;A l (O H )3与强酸发生碱式电离,生成铝酸盐而溶解,表现两性[Z n (O H )2性质与A l (O H )3相似,也表现两性].A l (O H )3难溶于弱酸(如H 2C O 3)㊁弱碱(如N H 3 H 2O ),可用于制取A l (O H )3,分解后的A l 2O 3,在熔融状态电解得到金属A l .一些特殊的离子反应与用量有关,虽然 表 中没有列出或标示,但在学习中要注意掌握应用.如A g +㊁C u 2+与浓氨水,A g O H ㊁C u (O H )2溶于过量浓氨水发生配位反应,生成[A g (N H 3)2]+和[C u (N H 3)4]2+,产物与氨水浓度和用量有关.书写与量有关的离子方程式,把少量反应物化学计量数设定为 1,再判定另一种足量反应物化学计量数;拆写时,注意反应物用量㊁反应现象和产物对应关系;与量有关的氧化还原反应,注意强先弱后规律应用.5㊀相同类型反应的离子方程式书写例7㊀下列反应的离子方程式是否正确(㊀㊀).(2017年江苏卷)向氢氧化钡溶液加入稀硫酸:B a 2++O H -+H ++S O 2-4=B a S O 4ˌ+H 2O.分析㊀反应中O H -㊁H +和H 2O 计量数都是2,但B a 2+㊁S O 2-4㊁B a S O 4计量数是1,不能将2约去,离子方程式应写为B a 2++2O H -+2H ++S O 2-4=B a S O 4ˌ+2H 2O ,该离子方程式错误.若N a H S O 4溶液中滴入B a (O H )2溶液反应至中和B a 2++2O H -+2H ++S O 2-4=B a S O 4ˌ+2H 2O ;N a H S O 4溶液中滴入B a (O H )2溶液至S O 2-4完全沉淀,O H -过量,应写为B a 2++OH -+H ++S O 2-4=B a S O 4ˌ+H 2O.含B a 2+和S O 2-4可溶性盐反应生成 表 中标 不 的难溶物B a S O 4,可用B a C l 2㊁B a (N O 3)2溶液与N a 2S O 4或K 2S O 4溶液反应,也可用B a (O H )2溶液与稀H 2S O 4㊁B a (O H )2溶液与N a H S O 4或K H S O 4溶液反应生成.同样,N a H C O 3溶液中加入足量B a (O H )2溶液反应㊁B a (H C O 3)2溶液中加入少量N a O H 溶液反应的离子方程式相同,都写为H C O -3+B a 2++O H -=B a C O 3ˌ+H 2O.N a H C O 3溶液中加入足量的澄清石灰水㊁C a (H C O 3)2溶液中加入少量Na O H 溶液反应的离子方程式相同,都为H C O -3+C a 2++O H -=C a C O 3ˌ+H 2O.含B a 2+和C O 2-3可溶性盐反应生成 表 中标 不 的难溶物B a C O 3,可采用N a 2C O 3㊁K 2C O 3溶液与B a C l 2或B a (N O 3)2溶液反应生成,也可采用N a H C O 3溶液与B a (O H )2溶液反应生成.生成难溶物C a C O 3的方法与此相似.不同反应物交换离子成分,虽反应物用量不同,但产物㊁离子方程式相同,书写时灵活应用表 ,注意反应物用量与产物对应关系.对离子反应方程式相同的离子反应,可写出反应物不同的化学方程式.生产中可应用物质性质设计出制取某种物质的可行途径.学生进入高中化学学习阶段,教材内容拓展加深,要掌握的知识点多,而现行高中化学实验教材中表 的内容少,有些物质的溶解性在 表 中没有标示或说明,需要在平时进一步学习掌握.学生在使用 表 书写离子方程式时既要参考,又不能依赖,更不能照搬,要结合所掌握知识,灵活应用;不仅要比较反应物质溶解性差异,还要具体分析判断参加反应物质的不同浓度㊁用量㊁性质㊁反应现象等;要仔细拆写,掌握规律方法,平时多练习体会,提高准确率,以避免或减少问题的发生.(作者单位:甘肃省高台县第一中学)96。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
高中化学溶解性表
溶:该物质易溶于水。
不:该物质不溶于水。
难:难溶于水(溶解度小于0.01g,几乎可以看成不溶,但实际溶解了极少量,绝对不溶于水的物质几乎没有)
微:微溶于水
挥:易挥发或易分解
—:该物质不存在或遇水发生水解
红褐色:Fe(OH)3
沉淀鉴别
沉淀;Cu2O 红色沉淀;Fe2O3红棕色沉淀;FeO 黑色沉淀FeS2黄色沉淀;PbS 黑色沉淀;FeCO3灰色沉淀;
Ag2CO3白色沉淀(制作过程中Ag2CO3易分解成褐色Ag2O,混合物常常为黄色);Cu2(OH)2CO3暗绿色沉淀;BaCO3白色沉淀(且有CO2生成);CaCO3白色沉淀(且有CO2生成);
BaSO4白色沉淀;不溶的碳酸盐白色沉淀(且有CO2生成);
不溶的碱、金属氧化物白色沉淀(且有CO2生成);Fe(OH)2为白色絮状沉淀(在空气中很快变成灰绿色,再变成Fe(OH)3红褐色沉淀)
溶解性口诀:
钾、钠、硝酸溶,(钾盐、钠盐和硝酸盐都溶于水。
)
盐酸除银(亚)汞,(盐酸盐里除氯化银和氯化亚汞外都溶。
)
硫酸盐除钡、铅,(硫酸盐中不溶的是硫酸钡和硫酸铅。
)
其余几类盐,(碳酸盐、亚硫酸盐、磷酸盐、硅酸盐和硫化物);只溶钾、钠、铵,(只有相应的钾盐、钠盐和铵盐可溶)
碱类中,钾、钠、铵、钡溶。
(氢氧化钾、氢氧化钠、氢氧化钡和氨水可溶)
另有几种微溶物,可单独记住(见上表)。
