(完整版)八年级化学方程式大全
初中必须掌握的化学方程式90条

2KMnO4=△K2MnO4+MnO2+O2↑2H2O2=MnO22H2O+O2↑2KClO3=△MnO22KCl+3O2↑CaCO3+2HCl=CaCl2+H2O+CO2↑Zn+H2SO4=ZnSO4+H2↑4P+5O2=点燃2P2O5S+O2=点燃SO24Al+3O2=2Al2O33Fe+2O2=点燃Fe3O42Cu+O2=△2CuO2Mg+O2=点燃2MgO2Hg+O2=△2HgO2H2+O2=点燃2H2OS+O2=点燃SO22CO+O2=点燃2CO2C+O2(充足)=点燃CO22C+O2(不充足)=点燃2CO2HgO=△2Hg+O2↑CH4+2O2=点燃CO2+2H2O 252点燃22实验室制取气体有氧气参加的反应H2CO3=H2O+CO2↑NH4HCO3=△NH3↑+H2O+CO2↑2HgO=△2Hg+O2↑Cu2(OH)2CO3=△2CuO+H2O+CO2↑CaCO3=高温CaO+CO2↑2H2O=通电2H2↑+O2↑Fe+H2SO4=FeSO4+H2↑Mg+H2SO4=MgSO4+H2↑2Al+3H2SO4=Al2(SO4)3+3H2↑Zn+2HCl=ZnCl2+H2↑Fe+2HCl=FeCl2+H2↑Mg+2HCl=MgCl2+H2↑2Al+6HCl=2AlCl3+3H2↑2Al+3CuSO4=Al2(SO4)3+3Cu Fe+CuSO4=FeSO4+Cu Zn+CuSO4=ZnSO4+Cu Cu+Hg(NO3)2=Cu(NO3)2+Hg Cu+2AgNO3=Cu(NO3)2+2AgCO2+C=高温2CO3CO+Fe2O3=高温2Fe+3CO24CO+Fe3O4=高温3Fe+4CO2分解反应金属与酸反应置换反应还原反应3C+2Fe 2O 3=高温4Fe+3CO 2↑ 2C+Fe 3O 4=高温3Fe+2CO 2↑ Fe 2O 3+3H 2=△2Fe+3H 2O Fe 3O 4+4H 2=△3Fe+4H 2O 2CuO+C =高温2Cu+CO 2↑ CuO+CO =△Cu+CO 2CuO+H 2=△Cu+H 2O 2Al+Fe 2O 3=高温2Fe+Al 2O 3 2Mg+CO 2=点燃2MgO+C 4Na+3CO 2=点燃2Na 2CO 3+C Fe 2O 3+6HCl =2FeCl 3+3H 2O Fe 2O 3+3H 2SO 4=Fe 2(SO 4)3+3H 2O CuO+2HCl =CuCl 2+H2O CuO+H 2SO 4=CuSO 4+H 2O MgO+H 2SO 4=MgSO 4+H 2O MgO+2HCl =MgCl 2+H 2O CaO+2HCl =CaCl 2+H 2O CaO+H 2SO 4=CaSO 4↓+H 2O CO 2+H 2O =H 2CO 3 2Na+2H 2O =2NaOH+H 2↑ CaO+H 2O =Ca(OH)2 Na 2O+H 2O =2NaOH SO 3+H 2O =H 2SO 4 氧化物与酸反应 还原反应与水化合CuSO4+5H2O=CuSO4·5H2O CuSO4+2NaOH=Cu(OH)2↓+Na2SO4 H2SO4+2NaOH=Na2SO4+2H2O H2SO4+2KOH=K2SO4+2H2OH2SO4+Cu(OH)2=CuSO4+2H2O 3H2SO4+2Fe(OH)3=Fe2(SO4)3+6H2OHNO 3+NaOH=NaNO3+H2O CaCO3+2HCl=CaCl2+H2O+CO2↑Na2CO3+2HCl=2NaCl+H2O+CO2 AgNO3+HCl=AgCl↓+HNO3Na2CO3+H2SO4=Na2SO4+H2O+CO2↑Na2CO3+Ca(OH)2=CaCO3↓+2NaOH3NaOH+FeCl3=Fe(OH)3↓+3NaCl NaCl+AgNO3=AgCl↓+NaNO32NaOH+CO2=Na2CO3+H2O2NaOH+SO2=Na2SO3+H2O2NaOH+SO3=Na2SO4+H2OCa(OH)2+CO2=CaCO3↓+H2OCa(OH)2+SO2=CaSO3↓+H2OHCl+NaOH=NaCl+H2OHCl+KOH=KCl+H2O2HCl+Cu(OH)2=CuCl2+2H2O2HCl+Ca(OH)2=CaCl2+2H2O3HCl+Fe(OH)3=FeCl3+3H2O3HCl+Al(OH)3=AlCl3+3H2O其它酸碱盐反应。
初二化学方程式

初二化学方程式初二化学方程式汇总1、镁在空气中燃烧:2Mg+O2点燃2MgO2、铁在氧气中燃烧:3Fe+2O2点燃Fe3O43、铝在空气中燃烧:4Al+3O2点燃2Al2O34、氢气在空气中燃烧:2H2+O2点燃2H2O5、红磷在空气中燃烧:4P+5O2点燃2P2O56、硫粉在空气中燃烧:S+O2点燃SO27、碳在氧气中充分燃烧:C+O2点燃CO28、碳在氧气中不充分燃烧:2C+O2点燃2CO9、二氧化碳通过灼热碳层:C+CO2高温2CO10、一氧化碳在氧气中燃烧:2CO+O2点燃2CO211、二氧化碳和水反应(二氧化碳通入紫色石蕊试液):CO2+H2O===H2CO312、生石灰溶于水:CaO+H2O===Ca(OH)213、无水硫酸铜作干燥剂:CuSO4+5H2O====CuSO4?5H2O14、钠在氯气中燃烧:2Na+Cl2点燃2NaCl分解反应15、实验室用双氧水制氧气:2H2O2MnO22H2O+O2↑16、加热高锰酸钾:2KMnO4加热K2MnO4+MnO2+O2↑17、水在直流电的作用下分解:2H2O通电2H2↑+O2↑18、碳酸不稳定而分解:H2CO3===H2O+CO2↑19、高温煅烧石灰石(二氧化碳工业制法):CaCO3高温CaO+CO2↑置换反应20、铁和硫酸铜溶液反应:Fe+CuSO4==FeSO4+Cu21、锌和稀硫酸反应(实验室制氢气):Zn+H2SO4==ZnSO4+H2↑22、镁和稀盐酸反应:Mg+2HCl===MgCl2+H2↑23、氢气还原氧化铜:H2+CuO加热Cu+H2O24、木炭还原氧化铜:C+2CuO高温2Cu+CO2↑25、甲烷在空气中燃烧:CH4+2O2点燃CO2+2H2O26、水蒸气通过灼热碳层:H2O+C高温H2+CO27、焦炭还原氧化铁:3C+2Fe2O3高温4Fe+3CO2↑28、氢氧化钠溶液与硫酸铜溶液反应:2NaOH+CuSO4==Cu(OH)2 +Na2SO429、甲烷在空气中燃烧:CH4+2O2点燃CO2+2H2O30、酒精在空气中燃烧:C2H5OH+3O2点燃2CO2+3H2O31、一氧化碳还原氧化铜:CO+CuO加热Cu+CO232、一氧化碳还原氧化铁:3CO+Fe2O3高温2Fe+3CO233、二氧化碳通过澄清石灰水(检验二氧化碳):Ca(OH)2+CO2====CaCO3 +H2O34、氢氧化钠和二氧化碳反应(除去二氧化碳):2NaOH+CO2====Na2CO3+H2O35、石灰石(或大理石)与稀盐酸反应(二氧化碳的实验室制法):CaCO3+2HCl===CaCl2+H2O+CO2↑36、碳酸钠与浓盐酸反应(泡沫灭火器的原理):Na2CO3+2HCl===2NaCl+H2O+CO2↑一.物质与氧气的反应:(1)单质与氧气的反应:1.镁在空气中燃烧:2Mg+O2点燃2MgO2.铁在氧气中燃烧:3Fe+2O2点燃Fe3O43.铜在空气中受热:2Cu+O2加热2CuO4.铝在空气中燃烧:4Al+3O2点燃2Al2O35.氢气中空气中燃烧:2H2+O2点燃2H2O6.红磷在空气中燃烧:4P+5O2点燃2P2O57.硫粉在空气中燃烧:S+O2点燃SO28.碳在氧气中充分燃烧:C+O2点燃CO29.碳在氧气中不充分燃烧:2C+O2点燃2CO(2)化合物与氧气的反应:10.一氧化碳在氧气中燃烧:2CO+O2点燃2CO211.甲烷在空气中燃烧:CH4+2O2点燃CO2+2H2O12.酒精在空气中燃烧:C2H5OH+3O2点燃2CO2+3H2O二.几个分解反应:13.水在直流电的作用下分解:2H2O通电2H2↑+O2↑14.加热碱式碳酸铜:Cu2(OH)2CO3加热2CuO+H2O+CO2↑15.加热氯酸钾(有少量的二氧化锰):2KClO3====2KCl+3O2↑16.加热高锰酸钾:2KMnO4加热K2MnO4+MnO2+O2↑17.碳酸不稳定而分解:H2CO3===H2O+CO2↑18.高温煅烧石灰石:CaCO3高温CaO+CO2↑三.几个氧化还原反应:19.氢气还原氧化铜:H2+CuO加热Cu+H2O20.木炭还原氧化铜:C+2CuO高温2Cu+CO2↑21.焦炭还原氧化铁:3C+2Fe2O3高温4Fe+3CO2↑22.焦炭还原四氧化三铁:2C+Fe3O4高温3Fe+2CO2↑23.一氧化碳还原氧化铜:CO+CuO加热Cu+CO224.一氧化碳还原氧化铁:3CO+Fe2O3高温2Fe+3CO225.一氧化碳还原四氧化三铁:4CO+Fe3O4高温3Fe+4CO2四.单质、氧化物、酸、碱、盐的相互关系(1)金属单质+酸--------盐+氢气(置换反应)26.锌和稀硫酸Zn+H2SO4=ZnSO4+H2↑27.铁和稀硫酸Fe+H2SO4=FeSO4+H2↑28.镁和稀硫酸Mg+H2SO4=MgSO4+H2↑29.铝和稀硫酸2Al+3H2SO4=Al2(SO4)3+3H2↑30.锌和稀盐酸Zn+2HCl===ZnCl2+H2↑31.铁和稀盐酸Fe+2HCl===FeCl2+H2↑32.镁和稀盐酸Mg+2HCl===MgCl2+H2↑33.铝和稀盐酸2Al+6HCl==2AlCl3+3H2↑(2)金属单质+盐(溶液)-------另一种金属+另一种盐34.铁和硫酸铜溶液反应:Fe+CuSO4===FeSO4+Cu35.锌和硫酸铜溶液反应:Zn+CuSO4===ZnSO4+Cu36.铜和硝酸汞溶液反应:Cu+Hg(NO3)2===Cu(NO3)2+Hg(3)碱性氧化物+酸--------盐+水37.氧化铁和稀盐酸反应:Fe2O3+6HCl===2FeCl3+3H2O38.氧化铁和稀硫酸反应:Fe2O3+3H2SO4===Fe2(SO4)3+3H2O39.氧化铜和稀盐酸反应:CuO+2HCl====CuCl2+H2O40.氧化铜和稀硫酸反应:CuO+H2SO4====CuSO4+H2O41.氧化镁和稀硫酸反应:MgO+H2SO4====MgSO4+H2O42.氧化钙和稀盐酸反应:CaO+2HCl====CaCl2+H2O(4)酸性氧化物+碱--------盐+水43.苛性钠暴露在空气中变质:2NaOH+CO2====Na2CO3+H2O44.苛性钠吸收二氧化硫气体:2NaOH+SO2====Na2SO3+H2O45.苛性钠吸收三氧化硫气体:2NaOH+SO3====Na2SO4+H2O46.消石灰放在空气中变质:Ca(OH)2+CO2====CaCO3 +H2O47.消石灰吸收二氧化硫:Ca(OH)2+SO2====CaSO3 +H2O(5)酸+碱--------盐+水48.盐酸和烧碱起反应:HCl+NaOH====NaCl+H2O49.盐酸和氢氧化钾反应:HCl+KOH====KCl+H2O50.盐酸和氢氧化铜反应:2HCl+Cu(OH)2====CuCl2+2H2O51.盐酸和氢氧化钙反应:2HCl+Ca(OH)2====CaCl2+2H2O52.盐酸和氢氧化铁反应:3HCl+Fe(OH)3====FeCl3+3H2O53.氢氧化铝药物治疗胃酸过多:3HCl+Al(OH)3====AlCl3+3H2O54.硫酸和烧碱反应:H2SO4+2NaOH====Na2SO4+2H2O55.硫酸和氢氧化钾反应:H2SO4+2KOH====K2SO4+2H2O56.硫酸和氢氧化铜反应:H2SO4+Cu(OH)2====CuSO4+2H2O57.硫酸和氢氧化铁反应:3H2SO4+2Fe(OH)3====Fe2(SO4)3+6H2O58.硝酸和烧碱反应:HNO3+NaOH====NaNO3+H2O(6)酸+盐--------另一种酸+另一种盐59.大理石与稀盐酸反应:CaCO3+2HCl===CaCl2+H2O+CO2↑60.碳酸钠与稀盐酸反应:Na2CO3+2HCl===2NaCl+H2O+CO2↑61.碳酸镁与稀盐酸反应:MgCO3+2HCl===MgCl2+H2O+CO2↑62.盐酸和硝酸银溶液反应:HCl+AgNO3===AgCl +HNO363.硫酸和碳酸钠反应:Na2CO3+H2SO4===Na2SO4+H2O+CO2↑64.硫酸和氯化钡溶液反应:H2SO4+BaCl2====BaSO4 +2HCl(7)碱+盐--------另一种碱+另一种盐65.氢氧化钠与硫酸铜:2NaOH+CuSO4====Cu(OH)2 +Na2SO466.氢氧化钠与氯化铁:3NaOH+FeCl3====Fe(OH)3 +3NaCl67.氢氧化钠与氯化镁:2NaOH+MgCl2====Mg(OH)2 +2NaCl68.氢氧化钠与氯化铜:2NaOH+CuCl2====Cu(OH)2 +2NaCl69.氢氧化钙与碳酸钠:Ca(OH)2+Na2CO3===CaCO3 +2NaOH(8)盐+盐-----两种新盐70.氯化钠溶液和硝酸银溶液:NaCl+AgNO3====AgCl +NaNO371.硫酸钠和氯化钡:Na2SO4+BaCl2====BaSO4 +2NaCl五.其它反应:72.二氧化碳溶解于水:CO2+H2O===H2CO373.生石灰溶于水:CaO+H2O===Ca(OH)274.氧化钠溶于水:Na2O+H2O====2NaOH75.三氧化硫溶于水:SO3+H2O====H2SO476.硫酸铜晶体受热分解:CuSO4?5H2O加热CuSO4+5H2O 77.无水硫酸铜作干燥剂:CuSO4+5H2O====CuSO4?5H2化学方程式反应现象应用2Mg+O2点燃或Δ2MgO剧烈燃烧.耀眼白光.生成白色固体.放热.产生大量白烟白色信号弹2Hg+O2点燃或Δ2HgO银白液体、生成红色固体拉瓦锡实验2Cu+O2点燃或Δ2CuO红色金属变为黑色固体4Al+3O2点燃或Δ2Al2O3银白金属变为白色固体3Fe+2O2点燃Fe3O4剧烈燃烧、火星四射、生成黑色固体、放热4Fe+3O2高温2Fe2O3C+O2点燃CO2剧烈燃烧、白光、放热、使石灰水变浑浊S+O2点燃SO2剧烈燃烧、放热、刺激味气体、空气中淡蓝色火焰.氧气中蓝紫色火焰2H2+O2点燃2H2O淡蓝火焰、放热、生成使无水CuSO4变蓝的液体(水)高能燃料4P+5O2点燃2P2O5剧烈燃烧、大量白烟、放热、生成白色固体证明空气中氧气含量CH4+2O2点燃2H2O+CO2蓝色火焰、放热、生成使石灰水变浑浊气体和使无水CuSO4变蓝的液体(水)甲烷和天然气的燃烧2C2H2+5O2点燃2H2O+4CO2蓝色火焰、放热、黑烟、生成使石灰水变浑浊气体和使无水CuSO4变蓝的液体(水)氧炔焰、焊接切割金属2KClO3MnO2Δ2KCl+3O2↑生成使带火星的木条复燃的气体实验室制备氧气2KMnO4ΔK2MnO4+MnO2+O2↑紫色变为黑色、生成使带火星木条复燃的气体实验室制备氧气2HgOΔ2Hg+O2↑红色变为银白、生成使带火星木条复燃的气体拉瓦锡实验2H2O通电2H2↑+O2↑水通电分解为氢气和氧气电解水Cu2(OH)2CO3Δ2CuO+H2O+CO2↑绿色变黑色、试管壁有液体、使石灰水变浑浊气体铜绿加热NH4HCO3ΔNH3↑+H2O+CO2↑白色固体消失、管壁有液体、使石灰水变浑浊气体碳酸氢铵长期暴露空气中会消失Zn+H2SO4=ZnSO4+H2↑有大量气泡产生、锌粒逐渐溶解实验室制备氢气Fe+H2SO4=FeSO4+H2↑有大量气泡产生、金属颗粒逐渐溶解Mg+H2SO4=MgSO4+H2↑有大量气泡产生、金属颗粒逐渐溶解2Al+3H2SO4=Al2(SO4)3+3H2↑有大量气泡产生、金属颗粒逐渐溶解Fe2O3+3H2Δ2Fe+3H2O红色逐渐变为银白色、试管壁有液体冶炼金属、利用氢气的还原性Fe3O4+4H2Δ3Fe+4H2O黑色逐渐变为银白色、试管壁有液体冶炼金属、利用氢气的还原性WO3+3H2ΔW+3H2O冶炼金属钨、利用氢气的还原性MoO3+3H2ΔMo+3H2O冶炼金属钼、利用氢气的还原性2Na+Cl2Δ或点燃2NaCl剧烈燃烧、黄色火焰离子化合物的形成、H2+Cl2点燃或光照2HCl点燃苍白色火焰、瓶口白雾共价化合物的形成、制备盐酸CuSO4+2NaOH=Cu(OH)2 +Na2SO4蓝色沉淀生成、上部为澄清溶液质量守恒定律实验2C+O2点燃2CO煤炉中常见反应、空气污染物之一、煤气中毒原因2CO+O2点燃2CO2蓝色火焰煤气燃烧C+CuO高温2Cu+CO2↑黑色逐渐变为红色、产生使澄清石灰水变浑浊的气体冶炼金属2Fe2O3+3C高温4Fe+3CO2↑冶炼金属Fe3O4+2C高温3Fe+2CO2↑冶炼金属C+CO2高温2COCO2+H2O=H2CO3碳酸使石蕊变红证明碳酸的酸性H2CO3ΔCO2↑+H2O石蕊红色褪去Ca(OH)2+CO2=CaCO3 +H2O澄清石灰水变浑浊应用CO2检验和石灰浆粉刷墙壁CaCO3+H2O+CO2=Ca(HCO3)2白色沉淀逐渐溶解溶洞的形成,石头的风化Ca(HCO3)2ΔCaCO3 +H2O+CO2↑白色沉淀、产生使澄清石灰水变浑浊的气体水垢形成.钟乳石的形成2NaHCO3ΔNa2CO3+H2O+CO2↑产生使澄清石灰水变浑浊的气体小苏打蒸馒头CaCO3高温CaO+CO2↑工业制备二氧化碳和生石灰CaCO3+2HCl=CaCl2+H2O+CO2↑固体逐渐溶解、有使澄清石灰水变浑浊的气体实验室制备二氧化碳、除水垢Na2CO3+H2SO4=Na2SO4+H2O+CO2↑固体逐渐溶解、有使澄清石灰水变浑浊的`气体泡沫灭火器原理Na2CO3+2HCl=2NaCl+H2O+CO2↑固体逐渐溶解、有使澄清石灰水变浑浊的气体泡沫灭火器原理MgCO3+2HCl=MgCl2+H2O+CO2↑固体逐渐溶解、有使澄清石灰水变浑浊的气体CuO+COΔCu+CO2黑色逐渐变红色,产生使澄清石灰水变浑浊的气体冶炼金属Fe2O3+3CO高温2Fe+3CO2冶炼金属原理Fe3O4+4CO高温3Fe+4CO2冶炼金属原理WO3+3CO高温W+3CO2冶炼金属原理CH3COOH+NaOH=CH3COONa+H2O2CH3OH+3O2点燃2CO2+4H2OC2H5OH+3O2点燃2CO2+3H2O蓝色火焰、产生使石灰水变浑浊的气体、放热酒精的燃烧Fe+CuSO4=Cu+FeSO4银白色金属表面覆盖一层红色物质湿法炼铜、镀铜Mg+FeSO4=Fe+MgSO4溶液由浅绿色变为无色Cu+Hg(NO3)2=Hg+Cu(NO3)2Cu+2AgNO3=2Ag+Cu(NO3)2红色金属表面覆盖一层银白色物质镀银Zn+CuSO4=Cu+ZnSO4青白色金属表面覆盖一层红色物质镀铜Fe2O3+6HCl=2FeCl3+3H2O铁锈溶解、溶液呈黄色铁器除锈Al2O3+6HCl=2AlCl3+3H2O白色固体溶解Na2O+2HCl=2NaCl+H2O白色固体溶解CuO+2HCl=CuCl2+H2O黑色固体溶解、溶液呈蓝色ZnO+2HCl=ZnCl2+H2O白色固体溶解MgO+2HCl=MgCl2+H2O白色固体溶解CaO+2HCl=CaCl2+H2O白色固体溶解NaOH+HCl=NaCl+H2O白色固体溶解Cu(OH)2+2HCl=CuCl2+2H2O蓝色固体溶解Mg(OH)2+2HCl=MgCl2+2H2O白色固体溶解Al(OH)3+3HCl=AlCl3+3H2O白色固体溶解胃舒平治疗胃酸过多Fe(OH)3+3HCl=FeCl3+3H2O红褐色沉淀溶解、溶液呈黄色Ca(OH)2+2HCl=CaCl2+2H2OHCl+AgNO3=AgCl +HNO3生成白色沉淀、不溶解于稀硝酸检验Cl—的原理Fe2O3+3H2SO4=Fe2(SO4)3+3H2O铁锈溶解、溶液呈黄色铁器除锈Al2O3+3H2SO4=Al2(SO4)3+3H2O白色固体溶解CuO+H2SO4=CuSO4+H2O黑色固体溶解、溶液呈蓝色ZnO+H2SO4=ZnSO4+H2O白色固体溶解MgO+H2SO4=MgSO4+H2O白色固体溶解2NaOH+H2SO4=Na2SO4+2H2OCu(OH)2+H2SO4=CuSO4+2H2O蓝色固体溶解Ca(OH)2+H2SO4=CaSO4+2H2OMg(OH)2+H2SO4=MgSO4+2H2O白色固体溶解2Al(OH)3+3H2SO4=Al2(SO4)3+3H2O白色固体溶解2Fe(OH)3+3H2SO4=Fe2(SO4)3+3H2O红褐色沉淀溶解、溶液呈黄色Ba(OH)2+H2SO4=BaSO4 +2H2O生成白色沉淀、不溶解于稀硝酸检验SO42—的原理BaCl2+H2SO4=BaSO4 +2HCl生成白色沉淀、不溶解于稀硝酸检验SO42—的原理Ba(NO3)2+H2SO4=BaSO4 +2HNO3生成白色沉淀、不溶解于稀硝酸检验SO42—的原理Na2O+2HNO3=2NaNO3+H2O白色固体溶解CuO+2HNO3=Cu(NO3)2+H2O黑色固体溶解、溶液呈蓝色ZnO+2HNO3=Zn(NO3)2+H2O白色固体溶解MgO+2HNO3=Mg(NO3)2+H2O白色固体溶解CaO+2HNO3=Ca(NO3)2+H2O白色固体溶解NaOH+HNO3=NaNO3+H2OCu(OH)2+2HNO3=Cu(NO3)2+2H2O蓝色固体溶解Mg(OH)2+2HNO3=Mg(NO3)2+2H2O白色固体溶解Al(OH)3+3HNO3=Al(NO3)3+3H2O白色固体溶解Ca(OH)2+2HNO3=Ca(NO3)2+2H2OFe(OH)3+3HNO3=Fe(NO3)3+3H2O红褐色沉淀溶解、溶液呈黄色3NaOH+H3PO4=3H2O+Na3PO43NH3+H3PO4=(NH4)3PO42NaOH+CO2=Na2CO3+H2O吸收CO、O2、H2中的CO2、2NaOH+SO2=Na2SO3+H2O2NaOH+SO3=Na2SO4+H2O 处理硫酸工厂的尾气(SO2)FeCl3+3NaOH=Fe(OH)3 +3NaCl溶液黄色褪去、有红褐色沉淀生成AlCl3+3NaOH=Al(OH)3 +3NaCl有白色沉淀生成MgCl2+2NaOH=Mg(OH)2 +2NaClCuCl2+2NaOH=Cu(OH)2 +2NaCl溶液蓝色褪去、有蓝色沉淀生成CaO+H2O=Ca(OH)2白色块状固体变为粉末、生石灰制备石灰浆Ca(OH)2+SO2=CaSO3 +H2O有白色沉淀生成初中一般不用Ca(OH)2+Na2CO3=CaCO3 +2NaOH有白色沉淀生成工业制烧碱、实验室制少量烧碱Ba(OH)2+Na2CO3=BaCO3 +2NaOH有白色沉淀生成Ca(OH)2+K2CO3=CaCO3 +2KOH有白色沉淀生成CuSO4+5H2O=CuSO4?H2O蓝色晶体变为白色粉末CuSO4?H2OΔCuSO4+5H2O白色粉末变为蓝色检验物质中是否含有水AgNO3+NaCl=AgCl +NaNO3白色不溶解于稀硝酸的沉淀(其他氯化物类似反应)应用于检验溶液中的氯离子BaCl2+Na2SO4=BaSO4 +2NaCl白色不溶解于稀硝酸的沉淀(其他硫酸盐类似反应)应用于检验硫酸根离子CaCl2+Na2CO3=CaCO3 +2NaCl有白色沉淀生成MgCl2+Ba(OH)2=BaCl2+Mg(OH)2 有白色沉淀生成CaCO3+2HCl=CaCl2+H2O+CO2↑MgCO3+2HCl=MgCl2+H2O+CO2↑NH4NO3+NaOH=NaNO3+NH3↑+H2O生成使湿润石蕊试纸变蓝色的气体应用于检验溶液中的铵根离子NH4Cl+KOH=KCl+NH3↑+H2O生成使湿润石蕊试纸变蓝色的气体【初二化学方程式汇总】。
八年级考试必会化学方程式

MnO 2△MnO 2初中化学方程式大全一、 氧气的性质:(1)单质与氧气的反应:(化合反应) 镁在空气中燃烧:2Mg + O 2点燃2MgO铁在氧气中燃烧:3Fe + 2O 2 点燃Fe 3O 4 铜在空气中受热:2Cu + O 2△2CuO 铝在空气中燃烧:4Al + 3O 2点燃2Al 2O 3 氢气中空气中燃烧:2H 2 + O 2 点燃2H 2O红磷在空气中燃烧 4P + 5O 2 点燃2P 2O 5 硫粉在空气中燃烧: S + O 2点燃SO 2碳在氧气中充分燃烧:C + O 2点燃CO 2碳在氧气中不充分燃烧:2C + O 2 点燃2CO(2)化合物与氧气的反应: 一氧化碳燃烧2CO + O 2 点燃2CO 2甲烷燃烧CH 4 + 2O 2点燃CO 2 + 2H 2O酒精燃烧C 2H 5OH+3O 2 点燃2CO 2+3H 2O(3)氧气的来源:玻义耳研究空气的成分:HgO Hg+ O 2↑ 高锰酸钾制氧气2KMnO4+K2MnO4 MnO2+O2↑过氧化氢制氧气2H 2O 2 2H 2O+ O 2↑氯酸钾制氧气2K ClO 3 2K Cl+3O 2↑电解水 2H 2O通电2H 2↑+O 2 ↑△生石灰溶于水:CaO + H2O == Ca(OH)2二氧化碳可溶于水:H2O + CO2==H2CO3二、质量守恒定律:镁燃烧2Mg + O2点燃 2MgO铁和硫酸铜溶液Fe+CuSO4==FeSO4+Cu 氢气还原氧化铜H2+CuO△Cu+H2O镁还原氧化铜Mg+CuO △ Cu + MgO 三、碳和碳的氧化物:(1)碳的化学性质碳充分燃烧:C + O2点燃CO2炭还原氧化铜C+2CuO高温2Cu + CO2↑炭还原氧化铁3C+2Fe2O3高温4Fe+3CO2↑(2)煤炉中发生的三个反应:(化合反应)煤炉的底层:C + O2点燃 CO2煤炉的中层:CO2 + C 高温 2CO煤炉的上部蓝色火焰2CO+O2点燃2CO2(3)二氧化碳的制法与性质:实验室制二氧化碳CaCO3 + 2HCl == CaCl2 + H2O + CO2↑碳酸分解H2CO3 == H2O + CO2↑二氧化碳溶于水H2O + CO2== H2CO3工业制二氧化碳CaCO3高温CaO + CO2↑石灰水与二氧化碳反应鉴别二氧化碳:Ca(OH)2 + CO2 === CaCO3↓+ H2O(4)一氧化碳的性质:一氧化碳还原氧化铜CO+CuO△Cu+CO2一氧化碳的可燃性2CO+O2点燃2CO2其它反应:36.碳酸钠与稀盐酸反应(灭火器的原理):Na2CO3 + 2HCl == 2NaCl + H2O + CO2↑四、燃料及其利用:酒精在空气中燃烧C2H5OH+3O2点燃2CO2+3H2O(1)金属与氧气反应:镁在空气中燃烧:2Mg + O2点燃2MgO铁在氧气中燃烧:3Fe + 2O2点燃 Fe3O4铜在空气中受热:2Cu + O2△ 2CuO铝在空气中形成氧化膜4Al+3O2=2Al2O3(标注成红色的必会)三常见混合物的重要成分四常见物质俗称五物质的检验1、氧气:带火星的木条放入瓶中,若木条复燃,燃起火:上红下蓝,则是氧气.2、氢气:在玻璃尖嘴点燃气体,罩一干冷小烧杯,观察杯壁是否有水滴,往烧杯中倒入澄清的石灰水,若不变浑浊,则是氢气.3、二氧化碳:通入澄清的石灰水,若变浑浊则是二氧化碳.但二氧化碳过量浑浊的石灰水又会变回澄清。
八年级化学方程式总汇

八年级化学方程式总汇1.镁在空气中燃烧:2Mg + O 2 点燃 2MgO2.铁在氧气中燃烧:3Fe + 2O 2 点燃 Fe 3O 43.氢气中空气中燃烧:2H 2 + O 2 点燃 2H 2O4.红磷在空气中燃烧:4P + 5O 2 点燃 2P 2O 55.硫粉在空气中燃烧: S + O 2 点燃 SO 26.碳在氧气中充分燃烧:C + O 2 点燃 CO 27.碳在氧气中不充分燃烧:2C + O 2 点燃 2CO8.一氧化碳在氧气中燃烧:2CO + O 2 点燃 2CO 29.甲烷在空气中燃烧:CH 4 + 2O 2 点燃 CO 2 + 2H 2O10.酒精在空气中燃烧:C 2H 5OH + 3O 2 点燃 2CO 2 + 3H 2O11.水在直流电的作用下分解:2H 2O 通电 2H 2↑+ O 2 ↑12.过氧化氢分解:2H 2O 2 二氧化锰 2H 2O+ O 2 ↑13.加热氯酸钾(有少量的二氧化锰):2KClO 3 2 ↑ 14.加热高锰酸钾:2KMnO 4 加热 K 2MnO 4 + MnO 2215.大理石与稀盐酸反应:CaCO 3 + 2HCl === CaCl 2 + H 2O + CO 2↑16.高温煅烧石灰石:CaCO 3 高温 CaO + CO 2↑17.生石灰溶于水:CaO + H 2O === Ca(OH)218.消石灰放在空气中变质:Ca(OH)2 + CO 2 ==== CaCO 3 ↓+ H 2O19.二氧化碳溶解于水:CO 2 + H 2O === H 2CO 320.碳酸不稳定而分解:H2CO3 === H2O + CO2↑八年级化学方程式总汇1.镁在空气中燃烧:2.铁在氧气中燃烧:3.氢气中空气中燃烧:4.红磷在空气中燃烧:5.硫粉在空气中燃烧:6.碳在氧气中充分燃烧:7.碳在氧气中不充分燃烧:8.一氧化碳在氧气中燃烧:9.甲烷在空气中燃烧:10.酒精在空气中燃烧:11.水在直流电的作用下分解:12.过氧化氢分解:13.加热氯酸钾(有少量的二氧化锰):14.加热高锰酸钾:15.大理石与稀盐酸反应:16.高温煅烧石灰石:17.生石灰溶于水:18.消石灰放在空气中变质:19.二氧化碳溶解于水:20.碳酸不稳定而分解:。
初中常见50个化学方程式

初中常见50个化学方程式1、2H₂+ O₂→2H₂O(氢气与氧气生成水)2、2Na + Cl₂→2NaCl(钠与氯气生成氯化钠)3CH₄+ 2O₂→CO₂+ 2H₂O(甲烷燃烧生成二氧化碳和水)4、CaCO₃→CaO + CO₂(碳酸钙分解生成氧化钙和二氧化碳)5、HCl + NaOH →NaCl + H₂O(盐酸与氢氧化钠中和生成氯化钠和水)6、Fe + S →FeS(铁与硫化合生成硫化铁)7、2H₂O →2H₂+ O₂(水分解生成氢气和氧气)8、CuSO₄+ Zn →ZnSO₄+ Cu(硫酸铜与锌反应生成硫酸锌和铜)9、C₃H₈+ 5O₂→3CO₂+ 4H₂O(丙烷燃烧生成二氧化碳和水)10、2AgNO₃+ Cu →2Ag + Cu(NO₃)₂(硝酸银与铜反应生成银和硝酸铜)11、2Na + 2H₂O →2NaOH + H₂(钠与水反应生成氢氧化钠和氢气)12、Fe + CuSO₄→FeSO₄+ Cu(铁与硫酸铜反应生成硫酸亚铁和铜)13、H₂SO₄+ 2NaOH →Na₂SO₄+ 2H₂O(硫酸与氢氧化钠中和生成硫酸钠和水)14、Zn + 2HCl →ZnCl₂+ H₂(锌与盐酸反应生成氯化锌和氢气)15、Ca(OH)₂+ 2HCl →CaCl₂+ 2H₂O(氢氧化钙与盐酸反应生成氯化钙和水)16、2Mg + O₂→2MgO(镁与氧气反应生成氧化镁)17、C + O₂→CO₂(碳与氧气反应生成二氧化碳)18、2Al + 6HCl →2AlCl₃+ 3H₂(铝与盐酸反应生成氯化铝和氢气)19、2NaHCO₃→Na₂CO₃+ CO₂+ H₂O(碱式碳酸氢钠分解生成碳酸钠、二氧化碳和水)20、2K + 2H₂O →2KOH + H₂(钾与水反应生成氢氧化钾和氢气)21、2HCl + Ca(OH)₂→CaCl₂+ 2H₂O(盐酸与氢氧化钙反应生成氯化钙和水)22、2Na + 2H₂O →2NaOH + H₂(钠与水反应生成氢氧化钠和氢气)23、CH₃COOH + NaHCO₃→CH₃COONa + CO₂+ H₂O(醋酸与碱式碳酸氢钠反应生成乙酸钠、二氧化碳和水)24、H₂O + CO₂→H₂CO₃(二氧化碳溶解在水中生成碳酸)25、CuO + H₂→Cu + H₂O(氧化亚铜与氢气反应生成铜和水)26、2HgO →2Hg + O₂(氧化汞分解生成汞和氧气)27、4Fe + 3O₂→2Fe₂O₃(铁与氧气反应生成氧化铁)28、2H₂O₂→2H₂O + O₂(过氧化氢分解生成水和氧气)29、Ca + 2H₂O →Ca(OH)₂+ H₂(钙与水反应生成氢氧化钙和氢气)30、2AgNO₃+ Na₂S →Ag₂S + 2NaNO₃(硝酸银与硫化钠反应生成硫化银和硝酸钠)31、Al + Cl₂→AlCl₃(铝与氯气反应生成氯化铝)32、C₃H₈+ 5O₂→3CO₂+ 4H₂O(丙烷燃烧生成二氧化碳和水)33、2HNO₃+ Ba(OH)₂→Ba(NO₃)₂+ 2H₂O(硝酸与氢氧化钡反应生成硝酸钡和水)34、Zn + H₂SO₄→ZnSO₄+ H₂(锌与硫酸反应生成硫酸锌和氢气)35、2Mg + 2HCl →MgCl₂+ H₂(镁与盐酸反应生成氯化镁和氢气)36、2C₄H₁₀+ 13O₂→8CO₂+ 10H₂O(戊烷燃烧生成二氧化碳和水)37、Na₂O + H₂O →2NaOH(氧化钠与水反应生成氢氧化钠)38、CaO + H₂O →Ca(OH)₂(氧化钙与水反应生成氢氧化钙)39、2Fe + 3Cl₂→2FeCl₃(铁与氯气反应生成氯化铁)40、NH₃+ HCl →NH₄Cl(氨气与盐酸反应生成氯化铵)41、Mg + 2H₂O →Mg(OH)₂+ H₂(镁与水反应生成氢氧化镁和氢气)42、C₂H₅OH + O₂→CO₂+ H₂O(乙醇燃烧生成二氧化碳和水)43、2Ag + S →Ag₂S(银与硫反应生成硫化银)44、2Al + 3CuCl₂→2AlCl₃+ 3Cu(铝与氯化亚铜反应生成氯化铝和铜)45、2NH₄NO₃→2N₂+ 4H₂O + O₂(硝酸铵分解生成氮气、水和氧气)46、KClO₃→KCl + O₂(高氯酸钾分解生成氯化钾和氧气)47、C₆H₁₂O₆→2C₂H₅OH + 2CO₂(葡萄糖发酵生成乙醇和二氧化碳)48、Ca + 2HCl →CaCl₂+ H₂(钙与盐酸反应生成氯化钙和氢气)49、2H₂O + O₂→2H₂O₂(水和氧气反应生成过氧化氢)50、4NH₃+ 5O₂→4NO + 6H₂O(氨气与氧气反应生成一氧化氮和水)。
初中化学方程式大全
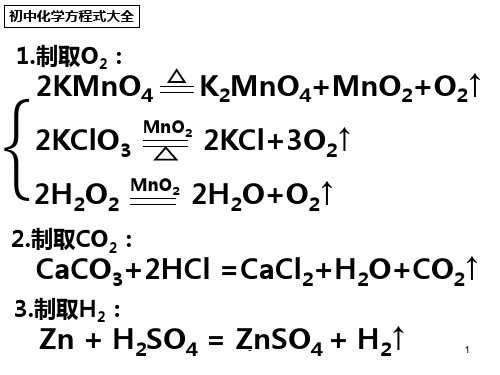
等等。。。
-
13
15、碱与铵盐反应: Ca(OH)2+2NH4Cl =CaCl2+2NH3↑+2H2O
Ca(OH)2+2NH4NO3=Ca(NO3)2+2NH3↑+2H2O
Ca(OH)2+(NH4)2SO4 =CaSO4+2NH3↑+2H2O Ca(OH)2+(NH4)2CO3 =CaCO3+2NH3↑+2H2O
7、还原反应:(C、CO、H2具有还原性)
Fe2O3+3CO 高温 2Fe +3CO2 (炼铁原理)
2Fe2O3+3C 高温 4Fe +3CO2 Fe2O3+3H2 高温 2Fe +3H2O
CuO+CO △ Cu +CO2 CuO+H2 △ Cu +H2O
2CuO+C 高温 2Cu +CO2 (两种黑色固体反
-
7
活泼金属与稀盐酸或稀硫酸的反应:
Mg+2HCl =MgCl2+H2↑
Zn+2HCl =ZnCl2+H2↑ Fe+2HCl =FeCl2+H2↑ 2Al+6HCl =2AlCl3+3H2↑ Mg+H2SO4 =MgSO4 +H2↑ Zn+H2SO4 =ZnSO4 +H2↑ Fe+H2SO4 =FeSO4 +H2↑ 2Al+3H2SO4 =Al-2(SO4)3+3H2↑ 8
-பைடு நூலகம்
10
化学方程式(8年级全)

反应名称
化学方程式
反应现象
1
加热碱式碳酸铜(俗称铜绿)
Cu2(OH)2CO3=== 2CuO + H2O + CO2加热
绿色粉末逐渐变为黑色,试管口有水滴生成,生成的气体能使澄清的石灰水变浑浊。
2
加热高锰酸钾制取氧气
2KMnO4===K2MnO4+ MnO2+ O2加热
高锰酸钾是暗紫色固体,其水溶液为紫红色,二氧化锰是黑色粉末不溶于水
C2H5OH + 3O2点燃2CO2+ 3H2O
大理石或石灰石(主要成分为CaCO3)表面有大量气泡生成且逐渐溶解
22
检验二氧化碳气体
CO2+ Ca(OH)2=== H2CO3
澄清石灰水变浑浊
23
二氧化与水生成碳酸
CO2+ H2O === H2CO3
注:CO2通入紫色石蕊试液中是CO2与水生成的碳酸使石蕊试液由紫变红
24
碳酸不稳定分解
H2CO3=== H2O + CO2加热
6
木炭的充分燃烧
C + O2点燃CO2
木炭在空气中燃烧时红热;在氧气中燃烧得更旺,发出白光;倒入燃烧后集气瓶中的澄清石灰水变浑浊。
7
硫的燃烧
S + O2点燃SO2
硫在空气中燃烧发出淡蓝色火焰;在氧气中燃烧得更旺,发出蓝紫色火焰;都放出大量的热,都生成了具有刺激性气味的气体。
8
铁丝在氧气中燃烧
3Fe + 2O2点燃Fe3O4
铁丝在氧气中剧烈燃烧,活性四射,放出大量的热,生成了黑色固体。
9
镁条在空气中燃烧
2Mg + O2点燃2MgO
(完整版)八年级化学方程式大全

八年级化学方程式大全1、2Mg+O22MgO 剧烈燃烧.耀眼白光.生成白色固体.放热.产生大量白烟白色信号弹2、2Hg+O22HgO 银白液体、生成红色固体拉瓦锡实验3、2Cu+O22CuO 红色金属变为黑色固体4、4Al+3O22Al2O3银白金属变为白色固体5、3Fe+2O2 Fe3O4剧烈燃烧、火星四射、生成黑色固体、放热6、C+O2 CO2剧烈燃烧、白光、放热、使石灰水变浑浊7、S+O2SO2剧烈燃烧、放热、刺激味气体、空气中淡蓝色火焰.氧气中蓝紫色火焰8、2H2+O2 2H2O 淡蓝火焰、放热、生成使无水CuSO4变蓝的液体(水)高能燃料9、4P+5O2 2P2O5剧烈燃烧、大量白烟、放热、生成白色固体证明空气中氧气含量10、二氧化碳和水反应(二氧化碳通入紫色石蕊试液):CO2+H2O==H2CO311、加热氯酸钾: 2 KClO3 2 KCl + 3 O2(加热)12、实验室用双氧水制氧气:2H2O22H2O+O2↑13、加热高锰酸钾:2KMnO4K2MnO4+MnO2+O2↑14、水在直流电的作用下分解:2H2O2H2↑+O2↑ 15、碳酸不稳定而分解:H2CO3==H2O+CO2↑16.氢氧化钠溶液与硫酸铜溶液反应:2NaOH+CuSO4==Cu(OH)2↓+Na2SO417、甲烷在空气中燃烧:CH4+2O2CO2+2H2O18、二氧化碳通过澄清石灰水(检验二氧化碳):Ca(OH)2+CO2==CaCO3↓+H2O19、氢氧化钠和二氧化碳反应(除去二氧化碳):2NaOH+CO2==Na2CO3+H2O20、石灰石(或大理石)与稀盐酸反应(二氧化碳的实验室制法):CaCO3+2HCl==CaCl2+H2O+CO2↑。
(完整版)初中化学方程式汇总(整理)

初中化学方程式汇总、基本反应类型(一)、化合反应2Mg + O2 点燃2MgO3Fe + 202 Fe3O44Al + 30 2 2A12O32H2 + O2 些2H2O4P + 5O2 点燃2P2O5S + O2 SO2C + O2 CO22C + O2 点燃2COC + CO2 2CO 11、二氧化碳和水反应(二氧化碳通入紫色石蕊试液)12、生石灰溶于水:CaO + H2O === Ca(OH)213、无水硫酸铜作干燥剂:CuSO4 + 5H2O === CuSO 4 5H2O14、钠在氯气中燃烧:2Na + Cl2 座夏2NaCl15、氧化钠溶于水:Na2O + H2O === 2NaOH16、三氧化硫溶于水:SO3 + H2O === H 2SO4(二)、分解反应17、实验室用双氧水制氧气:2H2O2 MnO2 2H2O +。
2,18、加热高镒酸钾:2KMnO4 △ K2MnO4 + MnO2 + O2 f19、水在直流电的作用下分解:2H2O 2H2f + O2 f20、碳酸不稳定而分解:H2CO3 H2O + CO2f21、高温燧烧石灰石(二氧化碳工业制法):CaCO3回!CaO + CO2?22、加热碱式碳酸铜:Cu2(OH)2CO3 △2CuO + H 2。
+ CO2T23、加热氯酸钾(有少量的二氧化猛):2KC1O 3 MnC_2和八2KC1 + 3O 2 f24、硫酸铜晶体受热分解:CuSO4 5H2O 八CuSO4 + 5H2O(三)、置换反应25、铁和硫酸铜溶液反应:Fe + CuSO4 === FeSO4 + Cu 26、锌和稀硫酸反应(实验室制氢气):Zn + H2SO4 === ZnSO 4 + H2 f27、镁和稀盐酸反应: Mg + 2HC1 === MgCl 2 + H2 f28、氢气还原氧化铜:H2 + CuO Cu + H2O29、木炭还原氧化铜: C + 2CuO 2Cu + CO 2 f30、水蒸气通过灼热碳层:H2O + C 也L H2 + CO31、焦炭还原氧化铁:3C + 2Fe2O34Fe + 3CO2?(四)、复分解反应一32、盐酸和烧碱起反应:HCl + NaOH === NaCl + H 2O33、盐酸和氢氧化钾反应:HCl + KOH === KCl + H 2O34、盐酸和氢氧化铜反应:2HCl + Cu (OH) 2 === CuCl 2 + 2H2O35、盐酸和氢氧化钙反应:2HCl + Ca (OH) 2 === CaCl2 + 2H2O36、盐酸和氢氧化铁反应:3HCl + Fe(OH) 3 === FeCl 3 + 3H 2O37、氢氧化铝药物治疗胃酸过多:3HCl + Al(OH) 3 === AlCl 3 + 3H2O38、硫酸和烧碱反应: H 2SO4 + 2NaOH === Na 2SO4 + 2H 2O39、硫酸和氢氧化钾反应:H2SO4 + 2KOH === K 2SO4 + 2H 2O40、硫酸和氢氧化铜反应:H2SO4 + Cu(OH) 2 === CuSO 4 + 2H 2O41、硫酸和氢氧化铁反应:3H2SO4 + 2Fe(OH)3 === Fe2(SO4)3 + 6H2O42、硝酸和烧碱反应:HNO3 + NaOH === NaNO 3+H2O43、大理石与稀盐酸反应:CaCO3 + 2HCl === CaCl 2 + H 2O + CO 2 f44、碳酸钠与稀盐酸反应:Na2CO3 + 2HCl === 2NaCl + H 2O + CO2 f45、碳酸镁与稀盐酸反应:MgCO 3 + 2HCl === MgCl 2 + H2O + CO2T46、盐酸和硝酸银溶液反应:HCl + AgNO 3 === AgCl $ + HNO47、硫酸和碳酸钠反应: Na2CO3 + H2SO4 === Na2SO4 + H2O + CO2 f48、硫酸和氯化根溶液反应:H 2SO4 +BaCl 2 === BaSO 4 $ + 2HCl + CuSO 4=== Cu(OH) 2 $ + NOSO4+ FeCl 3 === Fe(OH) 3 $ + 3NaCl+ MgCl 2 === Mg(OH) 2 $ + 2NaCl+ CuCl 2 === Cu(OH) 2 $ + 2NaCl2 + Na2CO3 === CaCO3 $ + 2NaOH54、氯化钠溶液和硝酸银溶液:NaCl + AgNO 3 === AgCl $ + NaNO55、硫酸钠和氯化彻: Na2SO4 + BaCl 2 === BaSO 4 $ + 2NaCl1、镁在空气中燃烧:2、铁在氧气中燃烧:3、铝在空气中燃烧:4、氢气在空气中燃7、碳在氧气中充分燃烧:8、碳在氧气中不充分燃烧:10、一氧化碳在氧气中燃烧: 2CO + O2 2CO2:CO2 + H2O === H2CO349、氢氧化钠与硫酸铜:2NaOH50、氢氧化钠与氯化铁:3NaOH51、氢氧化钠与氯化镁:2NaOH52、氢氧化钠与氯化铜:2NaOH53、氢氧化钙与碳酸钠:Ca56、甲烷在空气中燃烧: CH4 + 2O2 CO2 + 2H2O(五)、其它2Mg + O2 点燃2MgO3Fe + 2O2 Fe3O42Cu + O2 2CuO4Al + 3O2 2Al2O32H2 + O2 2H2O4P + 5O2 点燃2P2O5 S + O2 SO28、碳在氧气中充分燃烧:C + O2CO29、碳在氧气中不充分燃烧:2C + O2点燃2CO(二)、化合物与氧气的反应3、镁和稀硫酸:Mg + H 2SO4 === MgSO 4 + H2 f4、铝和稀硫酸:2AI + 3H 2SO4 === Al 2(SO4)3 + 3H2 f5、锌和稀盐酸: Zn + 2HC1 === ZnCl 2 + H2 f6、铁和稀盐酸: Fe + 2HCl === FeCl 2 + H2 f7、镁和稀盐酸:Mg + 2HCl === MgCl 2 + H2T 8、铝和稀盐酸:2Al + 6HCl === 2AlCl 3 + 3H2?(二)、金属单质+盐(溶液)—另一种金属+另一种盐9、铁和硫酸铜溶液反应:Fe + CuSO4 === FeSO4 + Cu10、锌和硫酸铜溶液反应:Zn + CuSO 4=== ZnSO 4 + Cu11、铜和硝酸汞溶液反应:Cu + Hg(NO3)2 === Cu(NO 3)2 + Hg(三)、碱性氧化物+酸K盐+水Fe2O3 + 6HCl === 2FeCl 3 + 3H 2OFe2O3 + 3H 2SO4 === Fe2(SO4)3 + 3H 2OCuO + 2HCl === CuCl 2 + H 2OCuO + H 2SO4 === CuSO4 + H 2OMgO + H 2SO4 === MgSO 4 + H2OCaO + 2HCl === CaCl 2 + H2O1、氢气还原氧化铜:H2 + CuO △ Cu + H 2。
初中必背化学方程式

初中必背100个化学方程式
一、置换反应:
1.镁与稀盐酸反应:Mg + 2HCl = MgCl2 + H2↑
二、酸和碱反应生成盐和水的中和反应
2.盐酸和氢氧化钠反应:HCl + NaOH = NaCl + H2O
三、酸与碱的中和反应
3.硫酸与氢氧化钠反应:H2SO4 + 2NaOH = Na2SO4 + 2H2O
四、金属氧化物与酸反应生成盐和水
4.氧化钙与稀盐酸反应:CaO + 2HCl = CaCl2 + H2O
五、非金属氧化物与碱反应生成盐和水
5.二氧化碳与氢氧化钠反应:CO2 + 2NaOH = Na2CO3 + H2O
六、碱与盐反应生成新碱和新盐
6.氢氧化钠与硫酸铜反应:2NaOH + CuSO4 = Cu(OH)2↓ + Na2SO4
七、盐与盐反应生成两种新盐
7.氯化钠与硝酸银反应:NaCl + AgNO3 = AgCl↓ + NaNO3
八、金属与酸反应生成盐和氢气
8.铁与稀盐酸反应:Fe + 2HCl = FeCl2 + H2↑
九、非金属与氢气反应生成非金属单质
9.碳与氢气反应:C + H2= CH4↑
十、有沉淀生成的复分解反应
10.硫酸铜溶液与氢氧化钠溶液反应:CuSO4 + 2NaOH = Cu(OH)2↓+ Na2SO4
十一、中和反应的离子方程式
11.盐酸和氢氧化钠反应:H+ + OH- = H2O。
初二化学反应方程式大全

(1)反应1.铁在氧气中燃烧:3Fe+2O2点燃Fe3O42.红磷在空气(氧气)中燃烧:4P+5O2点燃2P2O53.硫粉在空气(氧气)中燃烧:S+O2点燃SO24.碳在氧气中充分燃烧:C+O2点燃CO25.碳在氧气中不充分燃烧:2C+O2点燃2CO6.一氧化碳在氧气中燃烧:2CO+O2点燃2CO27.甲烷在空气(氧气)中燃烧:CH4+2O2点燃CO2+2H2O8.酒精在空气(氧气)中燃烧:C2H5OH+3O2点燃2CO2+3H2O9.铝在空气(氧气)中燃烧:4Al+3O2点燃2Al2O310.氢气中空气(氧气)中燃烧:2H2+O2点燃2H2O11.镁在空气(氧气)中燃烧:2Mg+O2点燃2MgO12.铜在空气(氧气)中受热:2Cu+O2∆2CuO13.铁放在氧气中:4Fe+3O2==2Fe2O314.亚硫酸放在空气(氧气)中:H2SO3+O2==H3SO4(2)其他14.水在直流电的作用下分解:2H2O通电2H2↑+O2↑(3)制取15.加热高锰酸钾:2KMnO4∆K2MnO4+MnO2+O2↑16.加热氯酸钾:2KClO3∆2MnO2KCl+3O2↑17.分解过氧化氢(双氧水):2H2O22MnO2H2O+O2↑二、二氧化碳(1)制取18.大理石(碳酸钙)与稀盐酸反应:CaCO3+2HCl==CaCl2+H2O+CO2↑19.碳酸钠与稀盐酸反应:Na2CO2+2HCl==2NaCl+H2O+CO2↑20.硫酸和碳酸钠反应:Na2CO3+H2SO4==Na2SO4+H2O+CO2↑21.高温煅烧石灰石(碳酸钙):CaCO3高温CaO+CO2↑22.熟石灰(氢氧化钙)放在空气中变质(通入二氧化碳):Ca(OH)2+CO2==CaCO3↓+H2O23.烧碱(氢氧化钠)放在空气中变质(通入二氧化碳):2NaOH+CO2==Na2CO3+H2O24.二氧化碳溶解于水:CO2+H2O==H2CO3(3)其他25.碳酸受热分解:H2CO3∆CO2↑+H2O26.烧碱(氢氧化钠)暴露在空气中变质:2NaOH+CO2==Na2CO3+H2O27.生石灰和二氧化碳反应:CaO+CO2==CaCO3三、其他28.盐酸和硝酸银溶液反应:HCl+AgNO3==AgCl↓+HNO329.硫酸和大理石(碳酸钙)反应:H2SO4+CaCO3==CaSO4+H2O30.盐酸和氢氧化钙反应:2HCl+Ca(OH)2==CaCl2+2H2O31.硫酸和水反应:SO2+H2O==H2SO332.生石灰溶于水:CaO+H2O==Ca(OH)235.加热使氯酸钾与二氧化锰反应:2KClO3+MnO2∆K2MnO4+Cl2↑+2O2↑36.氢氧化钡与氯化铵反应:Ba(OH)2+2NH4Cl==BaCl2+2NH3↑+2H2O37.硫酸铜晶体受热分解:CuSO4•5H2O∆CuSO4+5H2O38.无水硫酸铜作干燥剂:CuSO4+5H2O==CuSO4•5H2O。
八年级化学方程式

八年级化学方程式【文章导读】化学方程式,也称为化学反应方程式,是用化学式表示化学反应的式子。
化学方程式反映的是客观事实。
下面是关于八年级化学方程式,欢迎阅读参考!一.物质与氧气的反应:(1)单质与氧气的反应:1.镁在空气中燃烧:2mg+o22.铁在氧气中燃烧:3fe+2o23.铜在空气中受热:2cu+o24.铝在空气中燃烧:4al+3o25.*气中空气中燃烧:2h2+o26.红*在空气中燃烧:4p+5o27.硫粉在空气中燃烧:s+o28.碳在氧气中充分燃烧:c+o29.碳在氧气中不充分燃烧:2c+o2(2)化合物与氧气的反应:10.一氧化碳在氧气中燃烧:2co+o211.**在空气中燃烧:ch4+2o212.酒精在空气中燃烧:c2h5oh+3o2二.几个分解反应:13.水在直流电的作用下分解:2h2o14.用过氧化*制氧气:2h2o22h2↑+o2↑2mgofe3o42cuo2al2o32h2o2p2o5so2co22co2c o2co2+2h2o2co2+3h2o2h2o+o2↑15.用**钾制取氧气(有少量的二氧化锰):2kclo32kcl+3o2↑16.用高锰*钾制氧气:2kmno4k2mno4+mno2+o2↑17.碳*不稳定而分解:h2co3===h2o+co2↑18.高温煅烧石灰石:caco3三.几个氧化还原反应:19.*气还原氧化铜:h2+cuo20.木炭还原氧化铜:c+2cuocao+co2↑cu+h2o2cu+co2↑21.焦炭还原氧化铁:3c+2fe2o322.焦炭还原四氧化三铁:2c+fe3o423.一氧化碳还原氧化铜:co+cuo4fe+3co2↑3fe+2co2↑cu+co22fe+3co224.一氧化碳还原氧化铁(炼铁):3co+fe2o325.一氧化碳还原四氧化三铁:4co+fe3o43fe+4co2四.单质、氧化物、*、碱、盐的相互关系(1)金属单质+*--------盐+*气(置换反应)26.实验室用锌与稀硫*反应制取*气zn+h2so4=znso4+h2↑27.铁和稀硫*fe+h2so4=feso4+h2↑28.镁和稀硫*mg+h2so4=mgso4+h2↑29.铝和稀硫*2al+3h2so4=al2(so4)3+3h2↑30.锌和稀盐*zn+2hcl=zncl2+h2↑31.铁和稀盐*fe+2hcl=fecl2+h2↑32.镁和稀盐*mg+2hcl===mgcl2+h2↑33.铝和稀盐*2al+6hcl==2alcl3+h2↑(2)金属单质+盐(溶液)-------另一种金属+另一种盐34.铁和硫*铜溶液反应:fe+cuso4====cu+feso435.锌和硫*铜溶液反应:zn+cuso4===znso4+cu36.铜和***溶液反应:cu+hg(no3)2===cu(no3)2+hg铜和**银溶液反应:cu+2agno3===cu(no3)2+2ag(3)碱*氧化物+*--------盐+水37.氧化铁和稀盐*反应(除铁锈):fe2o3+6hcl===2fecl3+3h2o38.氧化铁和稀硫*反应(除铁锈):fe2o3+3h2so4===fe2(so4)3+3h2o39.氧化铜和稀盐*反应:cuo+2hcl====cucl2+h2o40.氧化铜和稀硫*反应:cuo+h2so4====cuso4+h2o41.氧化镁和稀硫*反应:mgo+h2so4====mgso4+h2o42.氧化钙和稀盐*反应:cao+2hcl====cacl2+h2o(4)**氧化物+碱--------盐+水43.*氧化*暴露在空气中变质(除去二氧化碳)2naoh+co2=na2co3+h2o44.苛**吸收二氧化硫气体:2naoh+so2====na2so3+h2o 45.苛**吸收三氧化硫气体:2naoh+so3====na2so4+h2o 46.用石灰水检验二氧化碳/石灰水在空气中变质/用石灰浆粉刷墙壁:ca(oh)2+co2====caco3↓+h2o47.消石灰吸收二氧化硫:ca(oh)2+so2====caso3↓+h2o(5)*+碱--------盐+水48.盐*和烧碱起反应:hcl+naoh====nacl+h2o49.盐*和*氧化铜反应:2hcl+cu(oh)2====cucl2+2h2o50.盐*和*氧化钙反应:2hcl+ca(oh)2====cacl2+2h2o51.盐*和*氧化铁反应:3hcl+fe(oh)3====fecl3+3h2o52.*氧化铝*物治疗胃*过多:3hcl+al(oh)3====alcl3+3h2o53硫*和烧碱反应:h2so4+2naoh====na2so4+2h2o(6)*+盐--------另一种*+另一种盐54.实验室制取二氧化碳(大理石与稀盐*反应):caco3+2hcl===cacl2+h2o+co2↑55.碳**与稀盐*反应:na2co3+2hcl===2nacl+h2o+co2↑56.碳*镁与稀盐*反应:mgco3+2hcl===mgcl2+h2o+co2↑57.盐*和**银溶液反应:hcl+agno3===agcl↓+hno358.硫*和碳**反应:na2co3+h2so4===na2so4+h2o。
初二科学化学方程式大全

科学化学式一、氧气的性质:(1)单质与氧气的反应:(化合反应)1.镁在空气中燃烧:2Mg+O2点燃2MgO2.铁在氧气中燃烧:3Fe+2O2点燃Fe3O43.铜在空气中受热:2Cu+O2加热2CuO4.铝在空气中燃烧:4Al+3O2点燃2Al2O35.氢气中空气中燃烧:2H2+O2点燃2H2O6.红磷在空气中燃烧(研究空气组成的实验):4P+5O2点燃2P2O57.硫粉在空气中燃烧:S+O2点燃SO28.碳在氧气中充分燃烧:C+O2点燃CO29.碳在氧气中不充分燃烧:2C+O2点燃2CO(2)化合物与氧气的反应:10.一氧化碳在氧气中燃烧:2CO+O2点燃2CO211.甲烷在空气中燃烧:CH4+2O2点燃CO2+2H2O12.酒精在空气中燃烧:C2H5OH+3O2点燃2CO2+3H2O(3)氧气的来源:13.玻义耳研究空气的成分实验2HgO加热Hg+O2↑14.加热高锰酸钾:2KMnO4加热K2MnO4+MnO2+O2↑(实验室制氧气原理1)15.过氧化氢在二氧化锰作催化剂条件下分解反应:H2O2MnO22H2O+O2↑(实验室制氧气原理2)二、自然界中的水:16.水在直流电的作用下分解(研究水的组成实验):2H2O通电2H2↑+O2↑17.生石灰溶于水:CaO+H2O==Ca(OH)218.二氧化碳可溶于水:H2O+CO2==H2CO3三、质量守恒定律:19.镁在空气中燃烧:2Mg+O2点燃2MgO20.铁和硫酸铜溶液反应:Fe+CuSO4===FeSO4+Cu21.氢气还原氧化铜:H2+CuO加热Cu+H2O22.镁还原氧化铜:Mg+CuO加热Cu+MgO四、碳和碳的氧化物:(1)碳的化学性质23.碳在氧气中充分燃烧:C+O2点燃CO224.木炭还原氧化铜:C+2CuO高温2Cu+CO2↑25.焦炭还原氧化铁:3C+2Fe2O3高温4Fe+3CO2↑(2)煤炉中发生的三个反应:(几个化合反应)26.煤炉的底层:C+O2点燃CO227.煤炉的中层:CO2+C高温2CO28.煤炉的上部蓝色火焰的产生:2CO+O2点燃2CO2(3)二氧化碳的制法与性质:29.大理石与稀盐酸反应(实验室制二氧化碳):CaCO3+2HCl==CaCl2+H2O+CO2↑30.碳酸不稳定而分解:H2CO3==H2O+CO2↑31.二氧化碳可溶于水:H2O+CO2==H2CO332.高温煅烧石灰石(工业制二氧化碳):CaCO3高温CaO+CO2↑33.石灰水与二氧化碳反应(鉴别二氧化碳):Ca(OH)2+CO2===CaCO3↓+H2O(4)一氧化碳的性质:34.一氧化碳还原氧化铜:CO+CuO加热Cu+CO235.一氧化碳的可燃性:2CO+O2点燃2CO2其它反应:36.碳酸钠与稀盐酸反应(灭火器的原理):Na2CO3+2HCl==2NaCl+H2O+CO2↑五、燃料及其利用:37.甲烷在空气中燃烧:CH4+2O2点燃CO2+2H2O38.酒精在空气中燃烧:C2H5OH+3O2点燃2CO2+3H2O39.氢气中空气中燃烧:2H2+O2点燃2H2O六、金属(1)金属与氧气反应:40.镁在空气中燃烧:2Mg+O2点燃2MgO41.铁在氧气中燃烧:3Fe+2O2点燃Fe3O413.铜在空气中受热:2Cu+O2加热2CuO14.铝在空气中形成氧化膜:4Al+3O2=2Al2O3(2)金属单质+酸--------盐+氢气(置换反应)15.锌和稀硫酸Zn+H2SO4=ZnSO4+H2↑16.铁和稀硫酸Fe+H2SO4=FeSO4+H2↑17.镁和稀硫酸Mg+H2SO4=MgSO4+H2↑18.铝和稀硫酸2Al+3H2SO4=Al2(SO4)3+3H2↑19.锌和稀盐酸Zn+2HCl==ZnCl2+H2↑20.铁和稀盐酸Fe+2HCl==FeCl2+H2↑21.镁和稀盐酸Mg+2HCl==MgCl2+H2↑51.铝和稀盐酸2Al+6HCl==2AlCl3+3H2↑(3)金属单质+盐(溶液)-------新金属+新盐24.铁和硫酸铜溶液反应:Fe+CuSO4==FeSO4+Cu25.锌和硫酸铜溶液反应:Zn+CuSO4==ZnSO4+Cu26.铜和硝酸汞溶液反应:Cu+Hg(NO3)2==Cu(NO3)2+Hg(3)金属铁的治炼原理:55.3CO+2Fe2O3高温4Fe+3CO2↑。
八年级化学方程式汇总

化学方程式汇总点燃1.镁在空气中燃烧:2Mg + O2 === 2MgO点燃2. 铁在氧气中燃烧:3Fe + 2O2 === Fe3O4点燃3. 铝在空气中燃烧:4Al + 3O2 === 2Al2O3点燃4. 氢气中空气中燃烧:2H2 + O2 === 2H2O点燃5.磷在空气中燃烧:4P + 5O2 === 2P2O5点燃6. 硫粉在空气中燃烧: S + O2 === SO2点燃7. 木炭在氧气中燃烧:C + O2 === CO2通电8.水的电解:2H2O ==== 2H2↑+ O2↑MnO29.实验室制取氧气:加热氯酸钾:2KClO3 ==== 2KCl + 3O2↑△△加热高锰酸钾:2KMnO4 === K2MnO4 + MnO2 + O2↑(高锰酸钾)(锰酸钾)MnO2分解过氧化氢(双氧水)2H2O2====2H2O+O2↑10.实验室制取二氧化碳:大理石(石灰石)与稀盐酸反应:CaCO3 + 2HCl === CaCl2 + H2O + CO2↑11. 二氧化碳溶解于水:CO2 + H2O === H2CO3△(碳酸)12. 碳酸不稳定而分解:H2CO3 == H2O + CO2↑13.石灰水放在空气中变质:Ca(OH)2 + CO2 == CaCO3↓+ H2O(鉴定CO2的方法)(白色沉淀)高温14.工业上制取 CO2(高温煅烧石灰石):CaCO3 ===CaO + CO2↑酶15.生物呼吸作用:C6H12O6+6O2===6CO2+6H2O+能量(葡萄糖)光16.植物光合作用:6 CO2 + 6 H2O ==== C6H12O6 + 6O2叶绿体化学方程式汇总点燃1.镁在空气中燃烧:2Mg + O2 === 2MgO点燃2. 铁在氧气中燃烧:3Fe + 2O2 === Fe3O4点燃3. 铝在空气中燃烧:4Al + 3O2 === 2Al2O3点燃4. 氢气中空气中燃烧:2H2 + O2 === 2H2O点燃5.磷在空气中燃烧:4P + 5O2 === 2P2O5点燃6. 硫粉在空气中燃烧: S + O2 === SO2点燃7. 木炭在氧气中燃烧:C + O2 === CO2通电8.水的电解:2H2O ==== 2H2↑+ O2↑MnO29.实验室制取氧气:加热氯酸钾:2KClO3 ==== 2KCl + 3O2↑△△加热高锰酸钾:2KMnO4 === K2MnO4 + MnO2 + O2↑(高锰酸钾)(锰酸钾)MnO2分解过氧化氢(双氧水)2H2O2====2H2O+O2↑10.实验室制取二氧化碳:大理石(石灰石)与稀盐酸反应:CaCO3 + 2HCl === CaCl2 + H2O + CO2↑11. 二氧化碳溶解于水:CO2 + H2O === H2CO3△(碳酸)12. 碳酸不稳定而分解:H2CO3 == H2O + CO2↑13.石灰水放在空气中变质:Ca(OH)2 + CO2 == CaCO3↓+ H2O(鉴定CO2的方法)(白色沉淀)高温14.工业上制取 CO2(高温煅烧石灰石):CaCO3 ===CaO + CO2↑酶15.生物呼吸作用:C6H12O6+6O2===6CO2+6H2O+能量(葡萄糖)光16.植物光合作用:6 CO2 + 6 H2O ==== C6H12O6 + 6O2叶绿体。
初二化学方程式大全总结

初二化学方程式的总结一、化合反应1.镁在氧气中燃烧:2Mg+O2=点燃2MgO2.铁和稀盐酸反应:Fe+2HCl=FeCl2+H2↑3.铜和硝酸银反应:Cu+2AgNO3=Cu(NO3)2+2Ag4.氧化钙和水反应:CaO+H2O=Ca(OH)25.二氧化碳和水反应:CO2+H2O=H2CO36.氢氧化钠和二氧化碳反应:2NaOH+CO2=Na2CO3+H2O7.硫酸和氢氧化钠反应:H2SO4+2NaOH=Na2SO4+2H2O8.碳酸钙和稀盐酸反应:CaCO3+2HCl=CaCl2+H2O+CO2↑9.一氧化碳还原氧化铁:3CO+Fe2Fe+3CO210.二氧化碳和氢氧化钙反应:CO2+Ca(OH)2=CaCO3↓+H2O11.二氧化硫和水反应:SO2+H2O=H2SO312.氢氧化钙和二氧化碳反应:Ca(OH)2+CO2=CaCO3↓+H2O13.二氧化碳和氢氧化钠反应:CO2+2NaOH=Na2CO3+H2O14.一氧化碳还原氧化铜:CO+CuOCu+CO215.一氧化碳还原氧化铁:3CO+Fe2Fe+3CO216.一氧化碳还原四氧化三铁:4CO+Fe3Fe+4CO217.金属铝和稀盐酸反应:2Al+6HCl=2AlCl3+3H2↑18.金属铝和稀硫酸反应:2Al+3H2SO4=Al2(SO4)3+3H2↑19.金属铝和稀盐酸反应:2Al+6HCl=2AlCl3+3H2↑二、分解反应1.水在直流电的作用下分解:2H=通电H↑+O↑2.过氧化氢在二氧化锰的催化作用下分解:H=MnOH↑+O↑3.高锰酸钾在加热条件下分解:KMnOK Mn―△+MnO +O4.碳酸不稳定而分解:H=△H↑+CO↑5.碳酸氢铵受热分解:NH=N△+H +CO ↑三、置换反应1.氢气与氧化铜反应:H2+CuO―△Cu+H2O2.实验室用氢气还原氧化铜:H2+CuO―△Cu+H2O3.一氧化碳还原氧化铜:CO+CuO―△Cu+CO24.一氧化碳还原氧化铁:3CO+Fe2Fe+3CO2四、其他反应类型一、中和反应:酸与碱作用生成盐和水的反应。
八年级化学方程式汇总

1、呼吸作用:C 6H 2G 6 + 602亠6CQ + 6 H 2O +能量八年级化学方程式汇总有关氧气的化学性质的化学方程式:点燃、木炭在氧气中燃烧生成二氧化碳:C+O 2 C02 占桝 、硫在氧气中燃烧生成二氧化硫:S+0 2 -------------------- SQ 点燃 、铁在氧气中燃烧生成四氧化三铁:3Fe+2O 2 Fe 3G 4 点燃 、红磷在氧气中燃烧生成五氧化二磷: 4P+5O 2 2P2Q 点燃 、镁在氧气中燃烧生成氧化镁: 2Mg + 0 2 2Mg0 、铝在氧气中燃烧生成氧化铝: 4AI + 30 2 — 2AI 20点燃 、氢气在氧气中燃烧生成水: 2H 2 + 02 2H 20 、甲烷在空气中燃烧生成二氧化碳和水: CH 4 + 20 2 一— C02 + 2H 20 点燃、蜡烛燃烧的文字表达式:石蜡+氧气 二氧化碳+水 实验室制取氧气的化学方程式:| △ | 、加热高锰酸钾制氧气: 2KMnQ ------------ K 2Mn0+MnQ + 02 f、氯酸钾与二氧化锰共热制氧气: 2KCI0 —- — 2KCI + 30 2 f氧化碳能使澄清石灰水变浑浊(或者是用来鉴定二氧化碳的存在的化学方程式)C02 + Ca (O H) 2 = CaCO J + H 2O1 2 3 456 78 9 _ 、 1 23 三、 1 234 四、 、过氧化氢和二氧化锰混合制氧气: Mn0 22HQ 2H 2O + 02 f 有关二氧化碳的化学方程式:、实验室制取二氧化碳的化学方程式:CaC0+2HCI = CaCl 2 + CQ f + H 2O 、二氧化碳溶于水:CO +、碳酸不稳定受热易分解: HO = H 2C0 2C0CO f + HO光合作用和呼吸作用:1、呼吸作用:C6H2G6 + 602 亠6CQ + 6 H2O +能量2、光合作用:6CO + 6 HaO 叶绿体a C6H1Q + 602光电解五、电解水产生氢气和氧气:2HO •2H T + O a f六、氧气和臭氧的转化:(详见课本第65页)。
初中化学方程式大全列表

初中化学方程式大全列表碳酸氢铵受热分解:NH 4HCO 3===NH 3↑+H 20+CO 2↑ 碱式碳酸铜受热分解:Cu 2(OH)2CO 3===2CuO+H 20+CO 2↑一、初中化学方程式总结(1—7单元) 化合反应1.镁在空气中燃烧:2Mg + O 2点燃2MgO 2、铁在氧气中燃烧:3Fe +2O 2点燃Fe 3O 4 3、铝在空气中燃烧:4Al + 3O 2点燃2Al 2O 3 4、氢气在空气中燃烧:2H 2 + O 2点燃2H 2O 5、红磷在空气中燃烧:4P + 5O 2点燃2P 2O 56、硫粉在空气中燃烧: S + O 2点燃SO 2 7、碳在氧气中充分燃烧:C + O 2点燃CO 28、碳在氧气中不充分燃烧:2C + O 2点燃2CO 9、二氧化碳通过灼热碳层: C +CO 2高温2CO 10、一氧化碳在氧气中燃烧:2CO + O 2点燃2CO 2 11、二氧化碳和水反应(二氧化碳通入紫色石蕊试液):CO 2 + H 2O = H 2CO 3 12、生石灰溶于水:CaO + H 2O = Ca(OH)2 13、无水硫酸铜作干燥剂:CuSO 4 + 5H 2O ===CuSO 4•5H 2O 14、钠在氯气中燃烧:2Na + Cl 2点燃2NaCl分解反应 15、实验室用双氧水制氧气:2H 2O 2 2H 2O+O 2↑ 16、加热高锰酸钾:2KMnO 4 △2MnO 4 + MnO 2 + O 2↑ 17、水在直流电的作用下分解:2H 2O通电2H 2↑+ O 2 ↑ 18、碳酸不稳定而分解:H 2CO 3 = H 2O + CO 2↑19、高温煅烧石灰石(二氧化碳工业制法):CaCO 3高温CaO + CO 2↑ 置换反应20、铁和硫酸铜溶液反应:Fe + CuSO 4===FeSO 4 + Cu 21、锌和稀硫酸反应(实验室制氢气):Zn + H 2SO 4===ZnSO 4 + H 2↑ 22、镁和稀盐酸反应:Mg+2HCl = MgCl 2 + H 2↑ 23、氢气还原氧化铜:H 2 + CuO △2O 24、木炭还原氧化铜:C+2CuO高温2Cu + CO 2↑ 25、甲烷在空气中燃烧:CH 4 +2O 2点燃CO 2 + 2H 2O 26、水蒸气通过灼热碳层:H 2O + C高温H 2 + CO27、焦炭还原氧化铁:3C+2Fe 2O 3高温4Fe + 3CO 2↑ 其他 28、氢氧化钠溶液与硫酸铜溶液反应:2NaOH + CuSO 4===Cu(OH)2↓+ Na 2SO 4 29、甲烷在空气中燃烧:CH 4 + 2O 2点燃CO 2 + 2H 2O 30、酒精在空气中燃烧:M ====C2H5OH + 3O2点燃2CO2+ 3H2O 31、一氧化碳还原氧化铜:CO+CuO △232、一氧化碳还原氧化铁:3CO+Fe2O3高温2Fe +3CO233、二氧化碳通过澄清石灰水(检验二氧化碳):Ca(OH)2+ CO2===CaCO3↓+ H2O 34、氢氧化钠和二氧化碳反应(除去二氧化碳):2NaOH + CO2===Na2CO3 + H2O 35、石灰石(或大理石)与稀盐酸反应(二氧化碳的实验室制法):CaCO3 + 2HCl = CaCl2 + H2O + CO2↑36、碳酸钠与浓盐酸反应(泡沫灭火器的原理): Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑一.物质与氧气的反应:(1)单质与氧气的反应: 1. 镁在空气中燃烧:2Mg + O2点燃2MgO 2. 铁在氧气中燃烧:3Fe + 2O2点燃Fe3O4 3.铜在空气中受热:2Cu + O2△2CuO 4. 铝在空气中燃烧:4Al +3O2点燃2Al2O3 5. 氢气中空气中燃烧:2H2 + O2点燃2H2O 6. 红磷在空气中燃烧:4P + 5O2点燃2P2O57. 硫粉在空气中燃烧:S + O2点燃SO28. 碳在氧气中充分燃烧:C + O2点燃CO29. 碳在氧气中不充分燃烧:2C + O2点燃2CO (2)化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:2CO + O2点燃2CO211. 甲烷在空气中燃烧:CH4 + 2O2点燃CO2 + 2H2O 12. 酒精在空气中燃烧:C2H5OH + 3O2点燃2CO2 + 3H2O 二.几个分解反应:13. 水在直流电的作用下分解:2H2O 通电2H2↑+ O2↑14. 加热碱式碳酸铜:Cu2(OH)2CO3△2CuO + H2O + CO2↑15. 加热氯酸钾(有少量的二氧化锰):2KClO3MnO2△2KCl + 3O2↑16. 加热高锰酸钾:2KMnO4△K2MnO4 + MnO2 + O2↑17. 碳酸不稳定而分解:H2CO3 =H2O + CO2↑18. 高温煅烧石灰石:CaCO3高温CaO + CO2↑三.几个氧化还原反应:19. 氢气还原氧化铜:H2 + CuO△2O 20. 木炭还原氧化铜:C+2CuO 高温2Cu + CO2↑21. 焦炭还原氧化铁:3C+2Fe2O3高温4Fe + 3CO2↑22. 焦炭还原四氧化三铁:2C+Fe3O4高温3Fe + 2CO2↑23. 一氧化碳还原氧化铜:CO+CuO △Cu + CO224. 一氧化碳还原氧化铁:3CO+Fe2O3高温2Fe+ 3CO225. 一氧化碳还原四氧化三铁:4CO+Fe3O4高温3Fe + 4CO2四.单质、氧化物、酸、碱、盐的相互关系(1)金属单质+ 酸盐+ 氢气(置换反应)26. 锌和稀硫酸Zn + H2SO4 = ZnSO4 + H2↑27. 铁和稀硫酸Fe + H2SO4 = FeSO4 + H2↑28. 镁和稀硫酸Mg + H2SO4 = MgSO4 + H2↑29. 铝和稀硫酸2Al +3H2SO4 = Al2(SO4)3 +3H2↑30. 锌和稀盐酸Zn + 2HCl = ZnCl2 + H2↑31. 铁和稀盐酸Fe + 2HCl = FeCl2 + H2↑32. 镁和稀盐酸Mg+2HCl = MgCl2 + H2↑33. 铝和稀盐酸2Al + 6HCl===2AlCl3+ 3H2↑(2)金属单质+ 盐(溶液)另一种金属+ 另一种盐34. 铁和硫酸铜溶液反应:Fe + CuSO4 = FeSO4 + Cu 35. 锌和硫酸铜溶液反应:Zn + CuSO4= ZnSO4+ Cu 36. 铜和硝酸汞溶液反应:Cu + Hg(NO3)2 = Cu(NO3)2 + Hg (3)碱性氧化物+酸盐+ 水37. 氧化铁和稀盐酸反应:Fe2O3 + 6HCl = 2FeCl3 + 3H2O 38. 氧化铁和稀硫酸反应:Fe2O3 + 3H2SO4 = Fe2(SO4)3 + 3H2O 39. 氧化铜和稀盐酸反应:CuO + 2HCl===CuCl2+ H2O 40. 氧化铜和稀硫酸反应:CuO + H2SO4===CuSO4+ H2O 41. 氧化镁和稀硫酸反应:MgO + H2SO4===MgSO4+ H2O 42. 氧化钙和稀盐酸反应:CaO + 2HCl===CaCl2 + H2O (4)酸性氧化物+碱盐+ 水43.苛性钠暴露在空气中变质:2NaOH + CO2===Na2CO3+ H2O 44.苛性钠吸收二氧化硫气体:2NaOH + SO2===Na2SO3 + H2O 45.苛性钠吸收三氧化硫气体:2NaOH + SO3===Na2SO4+ H2O 46.消石灰放在空气中变质:Ca(OH)2+ CO2===CaCO3↓+ H2O 47. 消石灰吸收二氧化硫:Ca(OH)2+ SO2===CaSO3↓+ H2O (5)酸+ 碱盐+ 水48.盐酸和烧碱起反应:HCl + NaOH===NaCl +H2O 49. 盐酸和氢氧化钾反应:HCl + KOH===KCl +H2O 50.盐酸和氢氧化铜反应:2HCl + Cu(OH)2===CuCl2+ 2H2O 51. 盐酸和氢氧化钙反应:2HCl + Ca(OH)2===CaCl2+ 2H2O 52. 盐酸和氢氧化铁反应:3HCl + Fe(OH)3===FeCl3+ 3H2O 53.氢氧化铝药物治疗胃酸过多:3HCl + Al(OH)3===AlCl3+ 3H2O 54.硫酸和烧碱反应:H2SO4+ 2NaOH===Na2SO4+ 2H2O 55.硫酸和氢氧化钾反应:H2SO4+ 2KOH===K2SO4+ 2H2O 56.硫酸和氢氧化铜反应:H2SO4+ Cu(OH)2===CuSO4+ 2H2O 57. 硫酸和氢氧化铁反应:3H2SO4+ 2Fe(OH)3===Fe2(SO4)3+ 6H2O 58. 硝酸和烧碱反应:HNO3+NaOH===NaNO3+H2O (6)酸+ 盐另一种酸+ 另一种盐59.大理石与稀盐酸反应:CaCO3 + 2HCl = CaCl2 + H2O + CO2↑60.碳酸钠与稀盐酸反应: Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑61.碳酸镁与稀盐酸反应: MgCO3 + 2HCl = MgCl2 + H2O + CO2↑62.盐酸和硝酸银溶液反应:HCl + AgNO3= AgCl↓+ HNO363.硫酸和碳酸钠反应:Na2CO3+ H2SO4= Na2SO4+ H2O + CO2↑64.硫酸和氯化钡溶液反应:H2SO4+ BaCl2===BaSO4↓+ 2HCl (7)碱+ 盐另一种碱+ 另一种盐65.氢氧化钠与硫酸铜:2NaOH + CuSO4===Cu(OH)2↓ + Na2SO466.氢氧化钠与氯化铁:3NaOH + FeCl3===Fe(OH)3↓ + 3NaCl 67.氢氧化钠与氯化镁:2NaOH + MgCl2===Mg(OH)2↓ + 2NaCl 68. 氢氧化钠与氯化铜:2NaOH + CuCl2===Cu(OH)2↓+ 2NaCl 69. 氢氧化钙与碳酸钠:Ca(OH)2+ Na2CO3= CaCO3↓+ 2NaOH (8)盐+ 盐两种新盐70.氯化钠溶液和硝酸银溶液:NaCl + AgNO3===AgCl↓ + NaNO371.硫酸钠和氯化钡:Na2SO4+ BaCl2===BaSO4↓+ 2NaCl 五.其它反应:72.二氧化碳溶解于水:CO2 + H2O = H2CO373.生石灰溶于水:CaO + H2O = Ca(OH)274.氧化钠溶于水:Na2O + H2O ===2NaOH 75.三氧化硫溶于水:SO3+ H2O===H2SO476.硫酸铜晶体受热分解:CuSO4•5H2O===CuSO4+ 5H2O 77.无水硫酸铜作干燥剂:CuSO4+ 5H2O===CuSO4•5H2O 化学方程式、反应现象、应用2Mg+O2点燃2MgO 剧烈燃烧.耀眼白光.生成白色固体.放热.产生大量白烟白色信号弹2Hg+O2△2HgO 银白液体、生成红色固体拉瓦锡实验2Cu+O2△2CuO 红色金属变为黑色固体4Al+3O2点燃2Al2O3银白色金属变为白色固体3Fe+2O2点燃Fe3O4剧烈燃烧、火星四射、生成黑色固体、放热4Fe + 3O2高温2Fe2O3C+O2点燃CO2剧烈燃烧、白光、放热、使石灰水变浑浊S+O2点燃SO2剧烈燃烧、放热、刺激味气体、空气中淡蓝色火焰.氧气中蓝紫色火焰2H2+O2点燃2H2O 淡蓝火焰、放热、生成使无水CuSO4变蓝的液体(水)高能燃料4P+5O2点燃2P2O5剧烈燃烧、大量白烟、放热、生成白色固体证明空气中氧气含量CH4+2O2点燃2H2O+CO2蓝色火焰、放热、生成使石灰水变浑浊气体和使无水CuSO4变蓝的液体(水)甲烷和天然气的燃烧2C2H2+5O2点燃2H2O+4CO2蓝色火焰、放热、黑烟、生成使石灰水变浑浊气体和使无水CuSO4变蓝的液体(水)氧炔焰、焊接切割金属2KClO3MnO2△2KCl +3O2↑生成使带火星的木条复燃的气体实验室制备氧气2KMnO4△K2MnO4+MnO2+O2↑紫色变为黑色、生成使带火星木条复燃的气体实验室制备氧气2HgO △2Hg+O2↑红色变为银白、生成使带火星木条复燃的气体拉瓦锡实验2H2O 通电2H2↑+O2↑水通电分解为氢气和氧气电解水Cu2(OH)2CO3△2CuO+H2O+CO2↑绿色变黑色、试管壁有液体、使石灰水变浑浊气体铜绿加热NH4HCO3△NH3↑+ H2O +CO2↑白色固体消失、管壁有液体、使石灰水变浑浊气体碳酸氢铵长期暴露空气中会消失Zn+H2SO4=ZnSO4+H2↑有大量气泡产生、锌粒逐渐溶解实验室制备氢气Fe+H2SO4=FeSO4+H2↑有大量气泡产生、金属颗粒逐渐溶解Mg+H2SO4 =MgSO4+H2↑有大量气泡产生、金属颗粒逐渐溶解2Al+3H2SO4=Al2(SO4)3+3H2↑有大量气泡产生、金属颗粒逐渐溶解Fe2O3+3H2△2Fe+3H2O 红色逐渐变为银白色、试管壁有液体冶炼金属、利用氢气的还原性Fe3O4+4H2△3Fe+4H2O 黑色逐渐变为银白色、试管壁有液体冶炼金属、利用氢气的还原性WO3+3H2高温W +3H2O 冶炼金属钨、利用氢气的还原性MoO3+3H2高温Mo +3H2O 冶炼金属钼、利用氢气的还原性2Na+Cl2点燃2NaCl 剧烈燃烧、黄色火焰离子化合物的形成、H2+Cl22HCl 点燃苍白色火焰、瓶口白雾共价化合物的形成、制备盐酸CuSO4+2NaOH=Cu(OH)2↓+Na2SO4蓝色沉淀生成、上部为澄清溶液质量守恒定律实验2C +O2点燃2CO 煤炉中常见反应、空气污染物之一、煤气中毒原因2CO+O2点燃2CO2蓝色火焰煤气燃烧 C + CuO高温2Cu+CO2↑黑色逐渐变为红色、产生使澄清石灰水变浑浊的气体冶炼金属2Fe2O3+3C高温4Fe+3CO2↑冶炼金属Fe3O4+2C高温3Fe + 2CO2↑冶炼金属 C + CO2高温2CO CO2 + H2O = H2CO3碳酸使石蕊变红证明碳酸的酸性H2CO3△CO2↑+ H2O 石蕊红色褪去Ca(OH)2+CO2= CaCO3↓+ H2O 澄清石灰水变浑浊应用CO2检验和石灰浆粉刷墙壁CaCO3+H2O+CO2 = Ca(HCO3)2白色沉淀逐渐溶解溶洞的形成,石头的风化Ca(HCO3)2△CaCO3↓+H2O+CO2↑白色沉淀、产生使澄清石灰水变浑浊的气体水垢形成.钟乳石的形成2NaHCO3△Na2CO3+H2O+CO2↑产生使澄清石灰水变浑浊的气体小苏打蒸馒头CaCO3高温CaO+CO2↑工业制备二氧化碳和生石灰CaCO3+2HCl=CaCl2+H2O+CO2↑固体逐渐溶解、有使澄清石灰水变浑浊的气体实验室制备二氧化碳、除水垢Na2CO3+H2SO4=Na2SO4+H2O+CO2↑固体逐渐溶解、有使澄清石灰水变浑浊的气体泡沫灭火器原理Na2CO3+2HCl=2NaCl+H2O+CO2↑固体逐渐溶解、有使澄清石灰水变浑浊的气体泡沫灭火器原理MgCO3+2HCl=MgCl2+H2O+CO2↑固体逐渐溶解、有使澄清石灰水变浑浊的气体CuO +CO △Cu + CO2黑色逐渐变红色,产生使澄清石灰水变浑浊的气体冶炼金属Fe2O3+3CO 高温2Fe+3CO2冶炼金属原理Fe3O4+4CO高温3Fe+4CO2冶炼金属原理WO3+3CO高温W+3CO2冶炼金属原理CH3COOH+NaOH=CH3COONa+H2O2CH3OH+3O2点燃2CO2+4H2O C2H5OH+3O2点燃2CO2+3H2O 蓝色火焰、产生使石灰水变浑浊的气体、放热酒精的燃烧Fe+CuSO4=Cu+FeSO4银白色金属表面覆盖一层红色物质湿法炼铜、镀铜Mg+FeSO4= Fe+MgSO4溶液由浅绿色变为无色Cu+Hg(NO3)2=Hg+Cu(NO3)2Cu+2AgNO3=2Ag+Cu(NO3)2红色金属表面覆盖一层银白色物质镀银Zn+CuSO4= Cu+ZnSO4青白色金属表面覆盖一层红色物质镀铜Fe2O3+6HCl=2FeCl3+3H2O 铁锈溶解、溶液呈黄色铁器除锈Al2O3+6HCl=2AlCl3+3H2O 白色固体溶解Na2O+2HCl=2NaCl+H2O 白色固体溶解CuO+2HCl=CuCl2+H2O 黑色固体溶解、溶液呈蓝色ZnO+2HCl=ZnCl2+H2O 白色固体溶解MgO+2HCl=MgCl2+H2O 白色固体溶解CaO+2HCl=CaCl2+H2O 白色固体溶解NaOH+HCl=NaCl+H2O 白色固体溶解Cu(OH)2+2HCl=CuCl2+2H2O 蓝色固体溶解Mg(OH)2+2HCl=MgCl2+2H2O 白色固体溶解Al(OH)3+3HCl=AlCl3+3H2O 白色固体溶解胃舒平治疗胃酸过多Fe(OH)3+3HCl=FeCl3+3H2O 红褐色沉淀溶解、溶液呈黄色Ca(OH)2+2HCl=CaCl2+2H2O HCl+AgNO3= AgCl↓+HNO3生成白色沉淀、不溶解于稀硝酸检验Cl-的原理Fe2O3+3H2SO4= Fe2(SO4)3+3H2O 铁锈溶解、溶液呈黄色铁器除锈Al2O3+3H2SO4= Al2(SO4)3+3H2O 白色固体溶解CuO+H2SO4=CuSO4+H2O 黑色固体溶解、溶液呈蓝色ZnO+H2SO4=ZnSO4+H2O 白色固体溶解MgO+H2SO4=MgSO4+H2O 白色固体溶解2NaOH+H2SO4=Na2SO4+2H2OCu(OH)2+H2SO4=CuSO4+2H2O 蓝色固体溶解Ca(OH)2+H2SO4=CaSO4+2H2OMg(OH)2+H2SO4=MgSO4+2H2O 白色固体溶解2Al(OH)3+3H2SO4=Al2(SO4)3+3H2O 白色固体溶解2Fe(OH)3+3H2SO4=Fe2(SO4)3+3H2O 红褐色沉淀溶解、溶液呈黄色Ba(OH)2+H2SO4=BaSO4↓+2H2O 生成白色沉淀、不溶解于稀硝酸检验SO42-的原理BaCl2+H2SO4=BaSO4↓+2HCl 生成白色沉淀、不溶解于稀硝酸检验SO42-的原理Ba(NO3)2+H2SO4=BaSO4↓+2HNO3生成白色沉淀、不溶解于稀硝酸检验SO42-的原理Na2O+2HNO3=2NaNO3+H2O 白色固体溶解CuO+2HNO3=Cu(NO3)2+H2O 黑色固体溶解、溶液呈蓝色ZnO+2HNO3=Zn(NO3)2+H2O 白色固体溶解MgO+2HNO3=Mg(NO3)2+H2O 白色固体溶解CaO+2HNO3=Ca(NO3)2+H2O 白色固体溶解NaOH+HNO3=NaNO3+H2OCu(OH)2+2HNO3=Cu(NO3)2+2H2O 蓝色固体溶解Mg(OH)2+2HNO3=Mg(NO3)2+2H2O 白色固体溶解Al(OH)3+3HNO3=Al(NO3)3+3H2O 白色固体溶解Ca(OH)2+2HNO3=Ca(NO3)2+2H2OFe(OH)3+3HNO3=Fe(NO3)3+3H2O 红褐色沉淀溶解、溶液呈黄色3NaOH + H3PO4=3H2O+Na3PO43NH3+H3PO4=(NH4)3PO4 2NaOH+CO2=Na2CO3+H2O 吸收CO、O2、H2中的CO2、2NaOH+SO2=Na2SO3+H2O 2NaOH+SO3=Na2SO4+H2O 处理硫酸工厂的尾气(SO2)FeCl3+3NaOH=Fe(OH)3↓+3NaCl 溶液黄色褪去、有红褐色沉淀生成AlCl3+3NaOH=Al(OH)3↓+3NaCl 有白色沉淀生成MgCl2+2NaOH = Mg(OH)2↓+2NaCl CuCl2+2NaOH = Cu(OH)2↓+2NaCl 溶液蓝色褪去、有蓝色沉淀生成CaO+H2O = Ca(OH)2白色块状固体变为粉末、生石灰制备石灰浆Ca(OH)2+SO2=CaSO3↓+ H2O 有白色沉淀生成初中一般不用Ca(OH)2+Na2CO3=CaCO3↓+2NaOH 有白色沉淀生成工业制烧碱、实验室制少量烧碱Ba(OH)2+Na2CO3=BaCO3↓+2NaOH 有白色沉淀生成Ca(OH)2+K2CO3=CaCO3↓+2KOH 有白色沉淀生成CuSO4+5H2O= CuSO4•5H2O 蓝色晶体变为白色粉末CuSO4•5H2O===CuSO4+5H2O 白色粉末变为蓝色检验物质中是否含有水AgNO3+NaCl = AgCl↓+NaNO3白色不溶解于稀硝酸的沉淀(其他氯化物类似反应)应用于检验溶液中的氯离子BaCl2 + Na2SO4 = BaSO4↓+2NaCl 白色不溶解于稀硝酸的沉淀(其他硫酸盐类似反应)应用于检验硫酸根离子CaCl2+Na2CO3= CaCO3↓+2NaCl 有白色沉淀生成MgCl2+Ba(OH)2=BaCl2+Mg(OH)2↓有白色沉淀生成CaCO3+2HCl=CaCl2+H2O+CO2↑MgCO3+2HCl= MgCl2+H2O+CO2↑NH4NO3+NaOH=NaNO3+NH3↑+H2O 生成使湿润石蕊试纸变蓝色的气体应用于检验溶液中的铵根离子NH4Cl+KOH= KCl+NH3↑+H2O 生成使湿润石蕊试纸变蓝色的气体。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
八年级化学方程式大全
1、2Mg+O22MgO 剧烈燃烧.耀眼白光.生成白色固体.放热.产生大量白烟白色信号弹
2、2Hg+O22HgO 银白液体、生成红色固体拉瓦锡实验
3、2Cu+O22CuO 红色金属变为黑色固体
4、4Al+3O22Al2O3银白金属变为白色固体
5、3Fe+2O2 Fe3O4剧烈燃烧、火星四射、生成黑色固体、放热
6、C+O2 CO2剧烈燃烧、白光、放热、使石灰水变浑浊
7、S+O2SO2剧烈燃烧、放热、刺激味气体、空气中淡蓝色火焰.氧气中蓝紫色火焰
8、2H2+O2 2H2O 淡蓝火焰、放热、生成使无水CuSO4变蓝的液体(水)高能燃料
9、4P+5O2 2P2O5剧烈燃烧、大量白烟、放热、生成白色固体证明空气中氧气含量
10、二氧化碳和水反应(二氧化碳通入紫色石蕊试液):CO2+H2O==H2CO3
11、加热氯酸钾:2 KClO3 2 KCl + 3 O2(加热)
12、实验室用双氧水制氧气:2H2O22H2O+O2↑
13、加热高锰酸钾:2KMnO4K2MnO4+MnO2+O2↑
14、水在直流电的作用下分解:2H2O2H2↑+O2↑
15、碳酸不稳定而分解:H2CO3==H2O+CO2↑
16.氢氧化钠溶液与硫酸铜溶液反应:2NaOH+CuSO4==Cu(OH)2↓+Na2SO4
17、甲烷在空气中燃烧:CH4+2O2CO2+2H2O
18、二氧化碳通过澄清石灰水(检验二氧化碳):Ca(OH)2+CO2==CaCO3↓+H2O
19、氢氧化钠和二氧化碳反应(除去二氧化碳):2NaOH+CO2==Na2CO3+H2O
20、石灰石(或大理石)与稀盐酸反应(二氧化碳的实验室制法):CaCO3+2HCl==CaCl2+H2O+CO2↑。
