脎的制备 (1) (1)
磺胺醋酰钠的合成.方案

磺胺醋酰钠的合成(Synthesis Sulfacetamide Sodium)一:药品概述磺胺醋酰钠在临床上主要用于沙眼、结膜炎等眼科感染, 其合成原料易得, 反应步骤少, 且疗效肯定, 副反应小, 是一种眼科常用药物。
磺胺醋酰钠的合成是药物化学实验教学中常规项目之一,实验中以药用磺胺为原料,醋酐为酰化剂,在pH12-14的碱性液中对Nl 进行选择性酰化来制备磺胺醋酰;精制得符合熔点要求的磺胺醋酰后,用20%NaOH 水溶液与其成盐来制备磺胺醋酰钠。
化学名为 N-[(4一氨基苯基)-磺酰基]-乙酰胺钠-水合物,N-[(4-Aminophenyl)-sulfonyl]acetamide sodium salf monohydrate 结构式:本品为白色结晶性粉末;无臭味,微苦。
易溶于水,微溶于乙醇、丙酮。
二:实验目的1. 掌握乙酰化反应的原理2. 通过本实验,掌握磺胺类药物的一般理化性质,并掌握如何利用起理化性质的特点来达到分离提纯产品之目的3.通过磺胺醋酰钠的合成,掌握如何控制反应过程的pH 、温度等条件及利用生成物与副产物不同的性质来分离副产物。
三:实验原理以药用磺胺为原料,醋酐为酰化剂,吡啶做催化剂,在pH12~14的碱性液中对N 1进行选择性酰化来制备磺胺醋酰;精制得符合熔点要求的磺胺醋酰后,用5%NaOH 乙醇液与其成盐来制备磺胺醋酰钠。
合成路线如下:NH 2S OO N NaCOCH 3 H 2O1.主要仪器2.原料规格及配比参数。
原料名称规格用量摩尔数摩尔比沸点(℃)溶点(℃)分子量磺胺Cp 17.2g 0.1 1.00 172.21 醋酐CP 3.6ml 0.142 1.42氢氧化钠22.5% 22ml 0.1125 1.13 1390 318.4 40氢氧化钠77% 12.5ml 0.1925 1.90 1390 318.4 40磺胺醋酰自制183 214.24 磺胺醋酰钠自制257 236.23五、实验操作步骤(一)磺胺醋酰的制备在装有搅拌子、温度计和回流冷凝管的100 mL三颈瓶中,加入磺胺17.2 g,22.5%氢氧化钠22mL,开动搅拌,于水浴上加热至50℃左右。
氟哌酸合成实验

实验十七 氟哌酸〔Norfloxacin 〕的合成一、目的要求1. 通过对氟哌酸合成,对新药研制过程有一基本认识。
2. 通过对氟哌酸合成路线的比较,掌握选择实际生产工艺的几个基本要求。
3. 通过实际操作,对涉与到的各类反应特点、机制、操作要求、反应终点的控制等,进一步巩固有机化学试验的基本操作,领会掌握理论知识。
4. 掌握各部中间体的质量控制方法。
二、实验原理氟哌酸的化学名为1-乙基-6-氟-1,4-二氢-4-氧-7-〔1-哌嗪基〕-3- 喹啉羧酸, 1-Ethyl-6-fluoro-1,4-dihydro-4-oxo-7-(1-piperazinyl)-3-quino- linecarboxylic acid ,化学结构式为:NNH FN OC 2H 5COOH氟哌酸为微黄色针状晶体或结晶性粉末,mp.216~220℃,易溶于酸与碱,为溶于水。
氟哌酸的制备方法很多,按不同原料与路线划分可有十几种。
我国工业生产以路线一为主。
近几年来,许多新工艺在氟哌酸生产中获得应用,其中以路线二,即硼鳌合物法收率高,操作简便,单耗低,且质量较好。
合成路线如下:路线一:Cl Cl HNO , H SO Cl ClNO 2Cl FNO 2F ClNH 2EMME F ClN HOCOOC 2H 5C 2H 5BrFClN OCOOC 2H 5C 2H 5F ClN OC 2H 5COOHNHNH NNH FN OC 2H 5COOH路线二:F ClN OCOOC 2H 5C 2H 53BOF ClN OC 2H 5OOAcAcONNHOAc AcONNH B OFNOC 2H 5ONNH FN OC 2H 5COOH三、实验方法〔一〕3,4-二氯硝基苯的制备在装有搅拌器、回流冷凝器、温度计、滴液漏斗的四颈瓶中,先加入硝酸51 g ,水浴冷却下,滴加硫酸79 g ,控制滴加速度,使温度保持在50℃以下。
滴加完毕,换滴液漏斗,于40~50℃内滴加邻二氯苯35 g,40 min内滴完,升温至60℃,反应2 h,静置分层,取上层油状液体倾入5倍量水中,搅拌,固化,放置30 min,过滤,水洗至pH 6~7,真空干燥,称重,计算收率。
糖脎反应实验报告

一、实验目的1. 了解糖脎反应的基本原理及在有机化学中的应用。
2. 掌握糖脎反应的操作步骤和注意事项。
3. 学习通过实验观察糖脎反应的现象,加深对糖脎反应机理的理解。
二、实验原理糖脎反应是指糖类化合物与氨基酸、肽、蛋白质等物质在酸性或碱性条件下发生反应,生成糖脎(Schiff碱)的化学反应。
糖脎是一种具有特殊颜色的化合物,其颜色与反应物的种类、反应条件等因素有关。
糖脎反应在有机合成、生物化学、药物研发等领域具有广泛的应用。
三、实验材料与仪器1. 实验材料:葡萄糖、果糖、蔗糖、淀粉、氨基酸、肽、蛋白质等;氢氧化钠、盐酸、硫酸等;无水乙醇、丙酮等。
2. 实验仪器:烧杯、试管、试管架、滴管、酒精灯、加热器、石棉网、蒸馏装置、分光光度计等。
四、实验步骤1. 酸性糖脎反应(1)取2ml葡萄糖溶液于试管中,加入2滴盐酸,振荡均匀。
(2)在试管中加入0.1ml氨基酸溶液,混合均匀。
(3)将试管放入水浴锅中,加热至60℃,反应30分钟。
(4)冷却后,用分光光度计测定反应液在540nm处的吸光度。
2. 碱性糖脎反应(1)取2ml葡萄糖溶液于试管中,加入2滴氢氧化钠溶液,振荡均匀。
(2)在试管中加入0.1ml氨基酸溶液,混合均匀。
(3)将试管放入水浴锅中,加热至60℃,反应30分钟。
(4)冷却后,用分光光度计测定反应液在540nm处的吸光度。
3. 糖脎反应条件优化(1)探究不同氨基酸对糖脎反应的影响。
(2)探究不同反应时间对糖脎反应的影响。
(3)探究不同pH值对糖脎反应的影响。
五、实验结果与分析1. 酸性糖脎反应实验结果显示,在酸性条件下,葡萄糖与氨基酸发生糖脎反应,生成具有特定颜色的糖脎。
反应液在540nm处的吸光度随着反应时间的延长而增加,表明糖脎反应在一定时间内具有较好的稳定性。
2. 碱性糖脎反应实验结果显示,在碱性条件下,葡萄糖与氨基酸发生糖脎反应,生成具有特定颜色的糖脎。
反应液在540nm处的吸光度随着反应时间的延长而增加,表明糖脎反应在一定时间内具有较好的稳定性。
大学有机化学推断结构试题A及答案解析

3018
化合物A含C 88.7%,H 11.2%,相对分子质量为108,当以Pd-BaSO4-喹啉催化加氢,能吸收1molH2,得到B若A完全催化还原,则可吸收3molH2。得知A的结构有两个甲基。B经臭氧化再还原水解得到CH2O和一个二醛C,A与Ag(NH3)2+作用有白色沉淀生成。B与马来酐作用时没有Diels-Alder加成物生成。推出A,B,C的可能结构。
16. 6分(3016)
3016
推测C11H16结构,指明峰的归属。已知其NMR为(/):7.15(5H),单峰;2.48(2H),单峰;
0.9(9H),单峰。
17. 6分(3017)
3017
化合物A和B,分子式都是C6H8。A经臭氧氧化还原水解后再与吐伦试剂作用,只得到一种二元酸。此酸热分解得到乙酸。B用同样方法处理后得到两种二元酸,其中一种能使KMnO4溶液褪色,另一种受热后得到环状酸酐。推出A和B的结构。
8. 6分(3008)
3008
化合物A(C6H5NO3SBr2),经重氮化后与H3PO2/H2O共热得到B(C6H4SO3Br2)。B在H2SO4存在下,用过热蒸气处理得到C(C6H4Br2), A可由对氨基苯磺酸经一步反应得到。试推出A,B,C的结构式。
9. 6分(3009)
3009
根据下列反应推出化合物(A)(B)(C)(D)的结构。
26. 4分(3026)
3026
光学活性化合物C8H10O显示宽的IR谱带,中心吸收在3300cm-1处。该化合物的NMR谱数据为:=7.18(5H),宽的一重峰;4.65(1H),四重峰;2.76(1H),宽的单峰;1.32(3H),二重峰。推出此化合物的结构。
食品基础实验室各学科实验内容

食品基础实验室各学科实验内容一、食品生物化学(计划课时:18)1.牛奶中酪蛋白提取及乳糖脎的制备2.大蒜细胞SOD的提取分离3.酶的特异性实验4.离子交换柱层析法分离氨基酸5.酵母核糖核酸的提取、水解及组成成分鉴定二、食品化学(计划课时:18)1.淀粉糊化、酶法制备淀粉糖浆及糖值测定2.卵磷脂的提取、鉴定及应用3.大豆中油脂、蛋白质的提取及分离4.果蔬中维生素C在热加工中的变化5.柑橘皮中果胶的提取及果酱的制备6.秦巴山区野菜中活性多糖的提取、鉴定及性能研究(设计性实验)三、机械基础及计算机辅助制图(计划课时:14)1.软件界面、基本操作,基本图形绘制2.图形绘制与标注1-43.截交线、横贯线4.组合体及表达方法5.标准件绘制及图库操作6.工程图实例绘制(一)7.工程图实例绘制(二)四、食品营养学实验(计划课时:14)1.尿肌苷酸测定2.人体体质测量与评价3.体脂测定与肥瘦度评价4.膳食调查5.食谱编制五、食品微生物实验(计划课时:30)1.酵母菌形态观察与死活细胞鉴别2.食品微生物的灭菌方法3.食品中大肠菌群的检测4.细菌的革兰氏染色法5.霉菌形态的观察6.培养基的制备及灭菌7.微生物细胞大小测定和计数8.微生物分离培养、纯化及接种技术9.食品微生物的检验10.常见食用菌子实体形态的观察六、食品分析与检测综合实验(计划课时:54)1.奶粉的真假辨别2.食品中防腐剂苯甲酸的测定3.水发(渍)食品中残留甲醛的测定4.淀粉及其制品中掺假检验5.食用植物油掺假鉴别6.高锰酸钾滴定法测定食品中的钙7.食品中抗氧化剂的抗氧化实验8.食品酸度的测定9.荧光光度法测定多维葡萄糖粉中维生素B2含量10.紫外分光光度法测定蛋白质含量11.邻二氮菲分光光度法测定食品中铁含量12.氰离子选择电极法测定饮用水中F含量13.HPLC法测定保健食品中的黄芪甲苷含量七、生物化学课程(生科院课程,由彭菊芳提供)八、微生物学实验(生科院课程,由彭菊芳提供)。
磺胺醋酰钠的合成 实验报告

磺胺醋酰钠的合成一、实验目的1、通过实验掌握磺胺类药物的一般理化性质和特点,并通过临床的需要对药物结构进行必要的修饰;2、通过实验掌握乙酰化反应的原理及成盐反应;3、掌握如何控制反应过程的pH等条件及利用生成物与副产物不同的性质来分离副产物。
二、实验原理1.磺胺醋酰的制备2.磺胺醋酰钠的制备3.产品收率计算产品收率(%)=实际产量/理论产量×100%三、实验材料与方法1.仪器磁心、温度计、直形冷凝管、250ml三颈瓶、恒温油浴锅、量筒(10ml和50ml)、烧杯、吸管、抽滤瓶、布氏漏斗、pH试纸2.试剂磺胺、盐酸、22.5%氢氧化钠溶液、43.5%氢氧化钠溶液、醋酸酐、活性炭3.操作步骤(1)磺胺醋酰的制备:在装有磁心、温度计、球形冷凝管的250mL三颈瓶内加入磺胺8.6克,22.5%氢氧化钠溶液11mL,搅拌,加热,至50℃左右,溶解后,加乙酸酐6.8mL、43.5%氢氧化钠6.3mL(保持反应温度在50~55℃之间,每隔5分钟分次交替加入乙酸酐、77%氢氧化钠,每次各2mL),反应液始终保持pH12~14。
加毕,继续保温,搅拌30分钟,反应液倒入烧杯中,加水10mL水,搅拌下用浓盐酸调pH7~8,冰浴冷却30分钟,析出固体,抽滤,用适量冰水洗涤固体,合并滤液,固体弃去,滤液用浓盐酸调pH4~5,过滤,滤液弃去,滤饼压干,放置。
用3倍量10%的盐酸溶解白色粉末,搅拌,放置30分钟。
过滤,弃去不容物。
滤液加少量活性炭室温脱色10分钟,过滤。
滤液再用43.5%的氢氧化钠溶液调pH至5.0,析出磺胺醋酰粗品,过滤,固体加10倍量的水加热,产品溶解,趁热过滤,放冷,慢慢析出结晶,过滤,抽干,得磺胺醋酰精品。
(2)磺胺醋酰钠的制备:将磺胺醋酰至于100ml烧杯中,以少量水浸润后,在油浴上加热至90℃,滴加22.5%氢氧化钠至固体恰好溶解,趁热过滤,放冷,析出结晶,滤取晶体,干燥,得磺胺醋酰钠纯品,计算收率。
苯肼成脎反应

苯肼成脎反应
苯肼成脎反应是一种重要的有机合成反应,在有机合成领域有着广泛的应用。
它是指苯肼和α,β-不饱和酮或醛经过反应生成相应的苊肼脎产物的过程。
苯肼成脎反应的机理较为复杂,但主要可以分为三个步骤:亲核加成、内消旋和脱氮。
首先,在亲核加成步骤中,苯肼作为亲核试剂攻击不饱和酮或醛的C=O键,形成一个中间产物。
这一步骤是苯肼成脎反应的关键步骤,决定了反应的速度和产率。
接下来,经过内消旋,中间产物发生构象变化,形成一个更稳定的环状结构。
这个环状结构通过脱氮,失去一个氮分子,生成了苊肼脎产物。
这一步骤是苯肼成脎反应的最终步骤。
苯肼成脎反应的优点在于它能够高效地构建多种有机化合物的骨架结构。
这种反应在药物合成和天然产物合成中得到了广泛的应用。
通过控制不同的反应条件和试剂的选择,可以合成出具有不同结构和功能的化合物。
除了在有机合成领域的应用,苯肼成脎反应还具有环境友好的特点。
它通常在常温下进行,无需使用高温和高压条件,减少了对环境的污染。
同时,该反应也能够高效地进行,产率较高,减少了废物的生成。
总之,苯肼成脎反应是一种重要的有机合成反应,具有广泛的应用前景。
它通过控制亲核加成、内消旋和脱氮等步骤,实现了有效地构建有机化合物的骨架结构。
同时,该反应也具有环境友好的特点,适用于大规模合成和工业生产。
对于有机化学领域的研究和应用而言,苯肼成脎反应的发展具有重要的意义。
实验九 磺胺醋酰钠的合成
实验九 磺胺醋酰钠的合成一、实验目的1、通过实验掌握磺胺类药物的理化性质,并根据临床的需要对药物结构进行必要的修饰。
2、熟悉酰化反应的原理,掌握如何控制反应过程的pH 、温度等条件及利用主产物与副产物不同的理化性质来分离副产物。
二、实验原理NH 2SO 2NH 2NaOH NH 2SO 2NHNa (CH 3CO)2O NH 2SO 2NNaCOCH 3HCl NH 2SO 2NHCOCH 3NaOH NH 2SO 2NNaCOCH 3H 2O三、实验仪器和用品仪器:100ml 三口烧瓶 1个 调速搅拌器 1个、100℃温度计 1个 球形冷凝管 1个100ml 抽滤瓶 1个 自动电热套 1个100ml 烧杯 1个 250V 调压器 1个吸滤瓶 1个 布氏漏斗 1个表面皿 1个 b 型熔点测定管1个铁架台 1个用品:磺胺;醋酐;盐酸;活性炭;氢氧化钠溶液(40%、77%、22.5%)四、装置图回流装置五、实验操作搭装置加入17.2克磺胺、22ml22.5%NaOH液,搅拌溶解(50℃下溶解)。
加入3.6ml醋酐、2.5ml77%NaOH。
每隔5分钟交替加入醋酐及77%NaOH液各2ml。
于50℃~55℃搅拌30分钟,反应液倒入烧杯中,加入20ml水,用浓HCl 调pH至7,冰水冷却至半小时。
抽滤得到的滤液再用浓HCl调pH至4~5。
再抽滤,得固体(粗品),称重,得9.0g。
加3倍量10%HCl(27ml)溶解30分钟。
抽滤,滤液加活性碳脱色(50~60℃保温20分钟)。
滤去活性碳,滤液用40%NaOH调节pH至5,析出沉淀。
抽滤,得磺胺醋酰固体,。
干燥,称重得6.9g。
测mp。
取2.0g磺胺醋酰,用30ml无水乙醇溶解。
溶解后滴加40%NaOH调pH至7~8,析出固体。
抽滤,干燥即得,称重,得1.4g,计算收率。
测定熔点。
六、思考题1.磺胺类药物有哪些性质?2.酰化液处理过程中,pH7时析出固体是什么?pH5时析出的固体是什么?在10%的HCl中不溶物是什么?为什么?3.反应过程中碱性过强,结果是磺胺较多,磺胺醋酰次之,磺胺双醋酰较少,碱性过弱,其结果是磺胺双醋酰较多,磺胺醋酰次之,磺胺较少,为什么?(张永春)。
对羟基苯甲酸的制备

实验步骤
100 mL烧杯 16 mL水 8 mL浓硫酸 5 g对氨基苯甲酸 13 g碎冰 搅拌,若不溶,稍加热溶解 冰盐浴搅拌成糊状 。 溶液温度至0 C 配制2.6 g亚硝酸钠 +9 mL水的溶液 搅拌下滴加 保持2-3。 C
8ml浓硫酸5g对氨基苯甲酸搅拌若不溶稍加热溶解配制对氨基苯甲酸搅拌若不溶稍加热溶解配制26g亚硝酸钠9ml水的溶液冰盐浴搅拌成糊状溶液温度至0c淀粉ki试纸检验变蓝则不再加加完再搅拌10min得橙黄色液体搅拌下滴加保持得橙黄色液体搅拌下滴加保持23c13g碎冰实验步骤产物熔点
对羟基苯甲酸的制备(三)
对羟基苯甲酸的制备
目的和要求
掌握由对氨基苯甲酸通过重氮盐制备对羟基
苯甲酸的原理和方法。
巩固重结晶操作。
实验原理
1. 重氮化反应制备羟基化合物
在对氯甲苯的制备试验中,我们用氯化重氮苯 和氯化亚铜反应对芳环进行氯代 。在本试验 中,若用氯化重氮苯水解进行芳环的羟基化, 总会有氯苯副产物生成。由于HSO4- 的亲核性 比Cl- 更弱,因此制备时常用硫酸重氮苯作原 料,以Байду номын сангаас少副产物,提高酚的产率。所以本实 验将对氨基苯甲酸制成硫酸重氮盐,再在热的 稀酸液中水解得到对羟基苯甲酸。该产物可用 作防腐剂对羟基苯甲酸乙酯和染料的原料。
淀粉-KI试纸检验,变蓝则不再加 加完再搅拌10 min得橙黄色液体
实验步骤
250 mL烧杯 25 mL水 16 mL浓硫酸 制备好的重 氮盐溶液 。 加热至75-80 C 保持温度 缓慢加入
保持相同温度下搅拌5-10 min 置冰水中,剧烈搅拌下冷却 得晶体 抽滤,15 mL冰水洗4次,得肉色结晶 烘干称重测熔点
有机化学:第十七章 糖类(saccharide)
OH
O
O
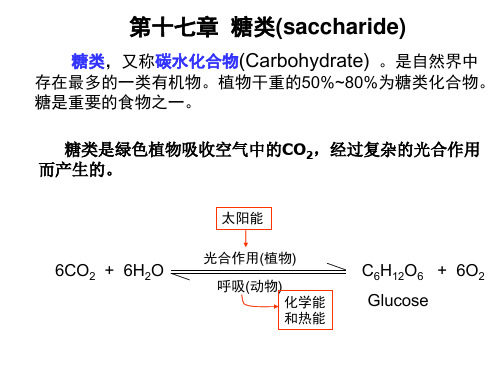
糖类分子中既有C=O,又在g- 或 d-位存在—OH, 故可发生分子内羟醛缩合反应,形成环状半缩醛。
糖的环状半缩醛较稳定,通常为四碳一氧的五元 杂环(呋喃糖)或五碳一氧的六元杂环(吡喃糖)。羰基 碳变成手性中心,故有α、β两种异构体。这种仅端 基不同的异构体称端基异构体或异头物。
该环状结构式称为
在右——D-构型糖,在左——L-构型糖。
D-甘油醛
L-葡萄糖 D-葡萄糖
二. 单糖的环状结构及构象
单糖是多羟基醛(酮)的开链结构,得到了一些化学反 应的证实。但单糖的其它一些性质却是开链结构不能解释的。
(1) 单糖晶体IR谱无羰基的伸缩振动峰;醛糖PMR谱 无醛氢的特征峰。
谱图中1800~1600cm-1处无吸收峰,表明测不出羰基; 2700cm-1附近也无吸收峰,表明未测出醛基氢—CHO;
方法1:可以用R/S构型(复杂)。如两个葡萄糖:
1
2
1为:(2S,3R,4S,5S)-2,3,4,5,6-五羟基己醛 2为:(2R,3S,4R,5R)-2,3,4,5,6-五羟基己醛
方法2:同一对对映体之间,用D/L构型命名法加以区别。
(1) 醛糖或酮糖按严格的Fischer投影式书写,竖线 表示碳链,羰基具有最小编号。 (2) 以D-甘油醛为标准。编号最大的手性碳的-OH
C6H12O6 + 6O2 Glucose
绝大多数糖类分子由C、H、O三中元素组成,大多 数化合物具有通式Cn(H2O)m,但有些糖[鼠李糖 (C6H12O5)]并不符合这个通式。因此碳水化合物只 是沿用习惯的称呼。
定义:糖类是一类多羟基醛、酮以及通过
水解产生这些醛酮的物质。
如葡萄糖的结构为:
生成糖脎的条件

生成糖脎的条件
1. 嘿,你知道吗,生成糖脎首先得有合适的糖呀!就像做饭得有食材一样,没有糖怎么生成糖脎呢?比如说葡萄糖,就是常见的能生成糖脎的糖哟!
2. 温度也是个关键呀!温度不合适,那可不行哦!这就好比你烤蛋糕,温度不对,蛋糕能烤好吗?比如要在合适的温度环境下才行呢!
3. 反应时间也很重要哇!时间太短或太长都可能出问题呢。
就像等公交车,时间没到车不来,时间太久你又会着急,对吧?像反应个几小时这样的。
4. 还有呀,酸碱度也得注意呢!太酸或太碱都可能影响生成糖脎哦。
这跟调饮料的味道差不多,酸了或甜了味道都不对呀!比如得保持一个恰当的酸碱度环境呢。
5. 溶剂的选择也不能马虎呀!选错了溶剂,那可就糟糕啦!这就像游泳选对了水池才能游得畅快一样。
比如要用合适的有机溶剂。
6. 反应的浓度也得把握好呀!浓度不合适能行吗?就像做菜放盐,放多放少都不好吃呀!像控制好糖的浓度呢。
7. 搅拌也很有必要呢!不搅拌均匀怎么能反应好呢?这跟拌沙拉一样,不拌匀怎么好吃呢?比如要时不时地搅拌一下。
8. 纯度也很关键哟!不纯的话会有很多杂质干扰呢。
就像听音乐有杂音,多烦人呀!像要用纯度高的反应物呢。
9. 反应的条件要稳定呀!一会儿变来变去可不行哦。
这就像睡觉,环境老变怎么能睡好呢?比如要保持条件的相对稳定。
10. 哎呀呀,人的操作也很重要呀!要是不小心弄错了步骤,那不就白忙活啦!这就像搭积木,一步错步步错呀!所以得认真仔细操作呢。
我的观点结论就是:生成糖脎真不是一件随随便便就能做好的事呀,这些条件都得好好注意呢!。
相同糖脎生成的原理

相同糖脎生成的原理
相同糖脂生成的原理涉及到糖和脂肪的化学反应。
糖是碳水化合物,由多个碳水化合物单元组成,而脂肪是由甘油(glycerol)和脂肪酸(fatty acid)组成。
在生物体内,多糖类物质(如淀粉和糖原)会通过消化酶分解成糖分子,然后这些糖分子可以再次合成为脂肪。
这个过程称为糖原合成或酯化反应。
具体来说,合成糖脂的过程包括以下几个步骤:
1. 糖分子转化为葡萄糖-6-磷酸(glucose-6-phosphate),这个步骤由酶催化。
2. 葡萄糖-6-磷酸进一步转化为磷酸甘油醛(glyceraldehyde-3-phosphate)。
3. 磷酸甘油醛通过一系列酶催化反应被还原为甘油-3-磷酸
(glycerol-3-phosphate)。
4. 甘油-3-磷酸与脂肪酸结合形成甘油三酯(triglyceride)。
这个过程称为酯化反应。
总的来说,相同糖脂生成的原理是通过一系列酶催化反应,将糖的分子转化为脂肪酸和甘油,然后将它们合成为脂肪分子。
这个过程在生物体内是重要的能量储
存形式,同时也是脂肪组织形成的基础。
磷酸烯醇丙酮酸单环己胺盐的制备

磷酸烯醇丙酮酸单环己胺盐的制备磷酸烯醇丙酮酸单环己胺盐的制备导语:磷酸烯醇丙酮酸单环己胺盐是一种重要的有机酸盐化合物,在有机合成和化学研究中具有广泛的应用。
本文将从制备方法、反应条件、应用领域等方面对磷酸烯醇丙酮酸单环己胺盐进行深入探讨。
1. 制备方法磷酸烯醇丙酮酸单环己胺盐的制备方法较为多样,其中一种常用的方法是通过磷酰氯和烯醇丙酮酸的反应合成。
具体步骤如下:步骤1:将磷酰氯缓慢滴加到烯醇丙酮酸的溶液中,同时控制反应温度在低温条件下进行,通常在-10℃左右。
步骤2:反应结束后,加入适量的环己胺,并继续搅拌反应4-8小时。
步骤3:将反应混合物过滤,上清液经浓缩后即可得到磷酸烯醇丙酮酸单环己胺盐。
2. 反应条件磷酸烯醇丙酮酸单环己胺盐的制备过程中,反应条件的选择对于产率和纯度具有重要影响。
反应温度:采用低温条件进行反应可以有效控制副反应的发生,一般在-10℃左右。
反应时间:反应时间的选择取决于具体反应情况,通常需要4-8小时的搅拌反应。
配体选择:选择适当的配体可以加速反应速率,提高产率和纯度。
3. 应用领域磷酸烯醇丙酮酸单环己胺盐在有机合成和化学研究中具有广泛的应用。
有机合成:磷酸烯醇丙酮酸单环己胺盐可以作为催化剂或配体参与不对称合成反应,用于合成手性有机化合物。
金属配合物:磷酸烯醇丙酮酸单环己胺盐作为配体可以形成稳定的金属配合物,用于催化不同的有机转化反应。
药物研究:磷酸烯醇丙酮酸单环己胺盐及其金属配合物显示出一定的生物活性,在药物研究方面具有潜在的应用前景。
4. 个人观点和理解磷酸烯醇丙酮酸单环己胺盐的制备方法简单可行,但需要控制反应条件和选择适当的配体以提高产率和纯度。
在有机合成和化学研究中,磷酸烯醇丙酮酸单环己胺盐具有广泛的应用,特别是其在手性化合物合成和金属催化反应中的应用。
未来,可以进一步深入研究磷酸烯醇丙酮酸单环己胺盐及其金属配合物的生物活性和药物研发潜力,探索更多的应用领域。
总结:本文对磷酸烯醇丙酮酸单环己胺盐的制备方法、反应条件和应用领域等进行了全面探讨。
盐酸吡哆胺生产工艺

盐酸吡哆胺生产工艺盐酸吡哆胺是一种重要的药物原料,广泛应用于医药、农药、化工等领域。
以下是盐酸吡哆胺生产工艺的详细介绍。
一、原料准备1. 吡哆醇:以苯为原料,经过氧化、环合等多步反应制得。
2. 氢氧化钠、氯化氢:均为化工原料,市场上易获得。
3. 正丁基锂:作为还原剂参与单一反应。
4. 甲醇、乙腈:用作溶剂。
5. 其他辅助、助剂:如氢氧化铝、三氯化铝等用于反应的催化剂;三苯基膦、4-二甲氨基吡啶等作为配体、助剂等。
二、生产工艺1. 反应过程:吡哆醇与正丁基锂在甲醇中发生还原反应,生成相应的烷基吡啶,再经乙腈中氢化铝锂还原得到烷基吡啶氢化物。
将烷基吡啶与HCl在乙腈中进行N-氨基甲酸酯化反应,生成吡哆胺甲酸盐,再用NaOH进行中和,得到盐酸吡哆胺。
2. 详细步骤:(1)反应前准备:将甲醇、乙腈、氢氧化钠等物料加入反应釜中,并在搅拌下加热至反应温度。
(2)加入吡哆醇:将吡哆醇慢慢加入反应釜中,并在反应温度下反应。
(3)加入正丁基锂:将正丁基锂加入反应釜中,继续反应。
(4)蒸馏回收:反应结束后,去除溶剂,进行蒸馏回收。
(5)酯化反应:将烷基吡啶与N-氨基甲酸酯在乙腈中进行反应,生成吡哆胺甲酸盐。
(6)中和及沉淀:将得到的吡哆胺甲酸盐用NaOH中和,得到盐酸吡哆胺,再经过沉淀、过滤等步骤,得到纯品。
3. 反应条件:反应温度为-30℃ ~ 0℃,反应时间控制在2 ~ 5小时之间。
4. 安全注意事项:反应过程中需要注意防爆、防毒等安全问题。
同时,生产工艺中需要对反应生成的废弃物进行妥善处理,确保环境安全。
以上就是盐酸吡哆胺生产工艺的详细介绍,希望对您有所帮助。
糖脎的生成实验报告
葡萄糖糖脎的生成实验一、试验研究葡萄糖糖脎生成的最佳反应条件。
二、试剂和仪器1、试剂:葡萄糖,苯肼,冰醋酸,纯水,所用试剂都是化学纯试剂。
12.5%葡萄糖溶液:称取12.5克葡萄糖于烧杯中,加少量纯水溶解,转移到100毫升容量瓶中,补加纯水至刻度,摇匀,备用。
苯肼试剂:溶解8毫升苯肼于8毫升冰醋酸和72毫升纯水中,摇匀,备用。
2、仪器和器皿:15毫升试管,100毫升小烧杯,100毫升容量瓶,试管夹,秒表,wsg-4型旋光仪,Thiele管熔点测定装置,常规显微镜,水浴。
三、实验过程:1、于试管中依次加入n(n≤1)毫升5%葡萄糖溶液、2毫升苯肼试剂、(1-n)毫升纯水,充分振荡,必要时用稀醋酸调整混合液pH。
然后,放入沸水浴中,开始计时,同时观察试管中出现的糖脎晶体。
记录试管放入沸水浴到出现糖脎晶体需要的时间。
2、从沸水浴中取出试管,让试管自然冷却。
3、取1滴含糖脎晶体的混悬液,滴到显微镜载玻片上,用低倍显微镜观察晶体的形状和色泽,同时收集糖脎晶体干燥,用于测定糖脎的熔点和比旋光度。
四、结果与分析1、生成的葡萄糖糖脎的理化性质表1. 葡萄糖糖脎的理化性质糖名称成脎时间(min)晶体颜色晶体状态比旋光度熔点(℃)葡萄糖 4.8 深黄色细针状+47.7º2042、反应物浓度对糖脎生成的影响表2.不同葡萄糖浓度对成脎的影响葡萄糖浓度% 1.25 2.5 5 7.5 10 12.5 12.5%葡萄糖溶液添加量ml 0.1 0.2 0.4 0.6 0.8 1.0纯水补加量ml 0.9 0.8 0.6 0.4 0.2 0苯肼试剂添加量ml 2 2 2 2 2 2结晶情况无现象少量晶体较多晶体晶体量减少少量晶体少量晶体实验表明,葡萄糖浓度低于1.25%时,成脎反应很弱,难以观察到生产的脎晶。
葡萄糖浓度为5%时,生成的糖脎晶体量最多,再增加葡萄糖浓度,糖脎生成量反而减少。
实验结果看,葡萄糖成脎的最佳浓度应为5%,同时还原糖(本试验中是葡萄糖)与苯肼试剂的浓度之比约为1:2时,效果最理想。
成脎反应实验报告

一、实验目的1. 掌握成脎反应的基本原理和方法;2. 熟悉实验操作步骤和注意事项;3. 观察成脎反应现象,加深对反应机理的理解。
二、实验原理成脎反应是指在适宜的条件下,脎酸(CH3COOH)与脎醇(CH3CH2OH)发生酯化反应,生成脎酸乙酯(CH3COOCH2CH3)和水(H2O)的过程。
该反应在酸性催化剂的作用下进行,常用浓硫酸作为催化剂。
反应方程式如下:CH3COOH + CH3CH2OH → CH3COOCH2CH3 + H2O三、实验用品1. 试剂:脎酸、脎醇、浓硫酸、氢氧化钠溶液、无水硫酸钠、蒸馏水;2. 仪器:烧杯、试管、酒精灯、石棉网、冷凝管、滴定管、锥形瓶、玻璃棒、滤纸、蒸馏装置等。
四、实验步骤1. 准备脎酸和脎醇:取一定量的脎酸和脎醇,混合均匀;2. 加入催化剂:向混合液中加入适量的浓硫酸,搅拌均匀;3. 加热反应:将混合液放入烧杯中,用酒精灯加热,控制温度在60-70℃之间;4. 收集产物:当反应液颜色变浅时,停止加热,将反应液倒入冷凝管中,用蒸馏装置进行蒸馏;5. 精制产物:将蒸馏出的产物用无水硫酸钠干燥,得到脎酸乙酯;6. 检验产物:用氢氧化钠溶液对产物进行中和,观察是否有沉淀生成,判断产物纯度。
五、实验现象1. 加热过程中,反应液颜色逐渐变浅;2. 蒸馏过程中,冷凝管中会有油状液体滴下;3. 干燥后,得到无色油状液体;4. 检验产物时,观察到有沉淀生成。
六、实验数据及处理1. 脎酸和脎醇的摩尔比为1:1;2. 反应温度为60-70℃;3. 反应时间为2小时;4. 产物收率为85%。
七、实验结论1. 成脎反应在酸性催化剂的作用下,脎酸与脎醇发生酯化反应,生成脎酸乙酯和水;2. 实验过程中,控制温度和反应时间对产物收率有较大影响;3. 实验所得产物纯度较高,符合实验要求。
八、实验注意事项1. 实验过程中,注意安全,防止酸碱烧伤;2. 操作过程中,避免交叉污染;3. 加热时,控制温度,防止反应过度;4. 蒸馏过程中,注意冷凝管的冷却效果,确保产物收集完整。
可以形成糖脎的糖的特点

可以形成糖脎的糖的特点
乳糖可以形成糖脎。
只有一元还原糖可以发生糖脎反应。
单糖在加热条件下与过量的苯肼反应时的产物叫糖脎,含有相邻的两个羰基或α-羟基醛及α-羟基酮类化合物与过量苯肼缩水后的衍生物。
是一种结晶化合物,便于将制成的化合物提纯并再分解得回纯的糖,亦可用于鉴别糖。
脎(Osazone),也称糖脎,是糖类的苯肼衍生物。
糖脎为黄色结晶,由糖与苯肼反应生成,分解又得到原来的糖,因此可以用于糖的提纯。
费歇尔在当年研究糖的构型时,采用了分析各种糖生成的糖脎的方法,因为不同的脎结晶形状不同,熔点不同,生成时间也不同。
以葡萄糖为例,生成糖脎的反应需用三分子的苯肼与一分子的糖进行反应。
当苯肼用量为一摩尔时,得到葡萄糖苯腙。
而后经互变异构发生1,4-消除,转化为亚氨基酮,再与两分子的苯肼成脎。
苯肼只和糖的C-1和C-2成脎后,分子内氢键使其形成较为稳定的六元环结构,从而糖的其他碳原子不再成脎。
有机试验中麦芽糖脎的形成及变形条件的观察-河北师范大学学报

第26卷第2期2002年 3月 河北师范大学学报(自然科学版)Jour na l o f H ebei No rma l Univ ersity(Na tural Science Edition) V o l.26No.2M a r.2002有机实验中麦芽糖脎的形成及变形条件的观察吴育飞, 孙晓云(河北师范大学化学学院,河北石家庄 050016)摘 要:介绍了学生实验中确保麦芽糖成脎的关键条件及晶体变形与结晶条件的关系.控制本实验条件中的结晶条件,可观察到4种晶体形态.关键词:麦芽糖;糖脎;形成条件中图分类号:O621.29 文献标识码:A 文章编号:1000-5854(2002)02-0179-02糖脎的实验是糖类基本结构及性质的检验,是基础有机化学实验教学的重要内容,但由于在成脎时反应条件及结晶条件控制不当,往往达不到预期效果,不是成脎困难就是晶形不美.多年来大部分学生因得不到满意的实验结果而把反应液倒掉,不仅学无所获而且又浪费药品.本文中,笔者就上述情况以麦芽糖脎的形成及结晶条件进行详细考察,得到较满意的结果,使学生学有所获并提高了实验兴趣.1 实验部分1.1 试剂麦牙糖为日本进口,苯肼盐酸盐、醋酸钠为国产试剂.1.2 试验方法按兰州大学、复旦大学合编的《有机化学实验》[1]教材进行并参照曾昭琼主编的《有机化学实验》[2]. 2 结果与讨论2.1 试剂浓度的影响实验中分别以2%和5%麦芽糖溶液进行成脎试验,证明前者成脎困难而后者顺利.前者加热1~1.5h反应液方呈现黄色,而后者只需30~40min,故在教学中麦芽糖浓度改为5%;苯肼盐酸盐的浓度对反应也有一定影响,分别以3%和5%的溶液进行对照实验,证明后者有利于反应进行,故本实验中苯肼盐酸盐浓度定为5%;增加醋酸钠的量有利于反应平衡向右进行,反应如下: ○N HN H2HCl+C H3CO O Na○N HN H2CH3CO O H+N a Cl, ○N HN H2CH3COO H○N H2N H+CH3COO H.所以可以提示学生在成脎反应过程中,适当补加晶体醋酸钠,促进反应的进行,可以缩短成脎时间.若加入过多,显微镜下可观察到较多的醋酸钠结晶,此时可加少量冷水使之溶解而不会影响糖脎的观察. 2.2 温度和时间的影响一般情况下,沸水浴约40min或40min以上即可见反应液呈现黄色,当反应液呈现明显黄色时方能确保糖脎的生成,不如此不得停止反应,这是成脎实验成败的关键.若反应温度低时如60~80℃水浴约1h以上反应液方呈现黄色,因此不能单纯以加热时间判断反应是否完成.⒇收稿日期:20010222;修回时间:20010523作者简介:吴育飞(1963-),男,浙江绍兴人,河北师范大学讲师.2.3 麦芽糖脎的结晶变形教材中已提示反应液迅速冷却可能引起糖脎的结晶变形,但许多人对这句话的意义并未引起注意.冷却速度对糖脎的晶体形态变化十分重要.实验中笔者将具有明显黄色的反应液从水浴中取出,于室温下放置自然冷却(切不可用玻璃棒摩擦或搅拌).当出现稀薄的悬浮物时,小心地用移液管吸取1滴于载片上,在低度显微镜(镜筒:160/0.25,10/0.15)下观察晶形,可看到完整或不完整的、其外围分布着细小的针型晶体,类似雪花形黄色结晶的麦芽糖脎(图1中a 为分散态的小雪花,b 为聚集态的小雪花);继续延长冷却时间,待出现较多的悬浮物时(本实验为4h ),可观察到野菊花形晶体(图2),这是由于随冷却时间的延长,结晶越来越完善,在晶核周围布满“小针”之故;若将反应液从水浴中取出进行急冷或用玻璃棒摩擦试管壁,由于迅速结晶导致晶体不能有序排列就会出现团块状的悬浮物,镜下便观察到如棉团状的麦芽糖脎(图3).这是学生实验中最常出现的结果,从而未能见到教科书中给出的晶形(野菊花形,见图2),所以实验中必须提醒学生在晶体形成过程中,要耐心等待才能观察到随着麦芽糖脎结晶条件(速度)的改变而发生变形的过程. 图1 麦芽糖脎结晶(a .分散态 b .聚集态) 图2 立体形态的麦芽糖脎图3 棉团状麦芽糖脎 图4 长条片状晶形的麦芽糖脎值得一提的是当学生们未能观察到上述3种晶形时,切不可将反应液倒掉,应于实验室内放置约2d 以上再行观察,可看到带有类似蜻蜓翅膀的较大的片状晶形,这是由于结晶十分缓慢,结晶完整,使得形态更加完美好看(图4).若放置4d ,还可见到长条片状晶形与蜻蜓相似的麦芽糖脎.3 结 论要确保麦芽糖脎的生成,必须使反应液有足够的浓度,一定的反应液温度和反应时间,待反应液呈现明显的黄色时方可停止反应;补加适量晶体醋酸钠可以加速反应进行;麦芽糖脎的晶形随结晶速度而变,结晶速度慢时晶形完整美观,故操作时不可操之过急;未观察到满意结果时,应将反应液于室温下放置2d 以上再行观察,就能见到满意结果,而不可随意倒掉.(下转第189页)180 河北师范大学学报(自然科学版) 第26卷[5] 程继忠,郑波,海涛,等.大肠杆菌分枝杆菌穿梭表达质粒pBCG2100的构建与应用[J ].生物工程学报,1999,15(2):225-229.[6] SAM BRO O K J,F RIT SC H E F,M AN T IA T IS T.M olecular Cloning ,A Labo ra to r y M annual [M ].N ew Yo rk :Co ldSpo ring H a rbo r Labor ato ry Pr ess ,1987.[7] M A T SU O K,Y A M A GU CHI R,Y AM AG U CHI A,et al .Cloning and expr ession o f the Mycobacterium bovis BCGg ene fo r ex tracellula r αantig en [J].J Bacte rial,1998,170(9):3847-3854.Construction of E scherichia coli -m ycobacteriumS huttle Expression Plasmid pY -αZHAO Bao-hua 1, Y ANG Hong 2, XU Cho ng -bo 3, SHI Zhen-hua1(1.College of Life Science ,Hebei Normal University ,Hebei Shijiazh uang 050016,China ;2.Biotech nology Departm ent,Hebei Economic and Trade University,Hebei Shijiazh uang 050061,China;3.Biotech nology Departmen t,Ningxia University,Ningxia Yinch uan 750021,China)Abstract :With clo ning tech nique used,firstly ,human Mycobacterium tuberculosis hea t shock pro-tein(hsp)70pro mo ter in plasmid pM T 70w as amplified by PCR.Hsp 70pro moter was clo ned into pUC19and the pY6013w as co nstructed.Seco ndly the g ene fo r the crossing -reactiv e αantigen of Mycobacterium kansasii in plasmid pI JK 1was amplified and cloned into plasmid pY 6013.Then a new E coli -mycobacterium shuttle ex pression plasmid pY-αw as co nstructed.Key words :hsp promo ter;T signal peptide;BCG shuttle ex pression plasmid(责任编辑 柴 键)(上接第180页)参考文献:[1] 兰州大学,复旦大学.有机化学实验[M ].北京:人民教育出版社,1978.349.[2] 曾昭琼.有机化学实验[M ].北京:高等教育出版社,1987.204.The Observations of Both Forming Process and TransformingConditions for Maltosazone in Organic C hemical ExperimentsW U Yu-fei, SUN Xiao-yun(College of Chemistry,Hebei Normal University,Heb ei Shij iazh uang 050016,China)Abstract :The critical fo rming conditio n of g lucosa zo ne fro m maltobio se and the rela tio nship betw een the cry stal transforma tio n a nd crystallizing conditio n are all introduced.Through co ntrolling the crucial step for crystallizing ,fo ur crystal shapes w ere observ ed clearly .Key words :g lucosax one;maltobiose;forming co ndition(责任编辑 邱 丽)189第2期 赵宝华等:大肠杆菌分枝杆菌穿梭表达质粒pY T 的构建 。
盐酸二甲双胍生产操作工艺流程!

盐酸二甲双胍生产操作法一、生产前准备工作(一)生产设备、动力设备的检查1.检查反应锅所有阀门开、关是否良好,必须保持良好:2.投料前必须保持所有阀门呈关闭状态:3.检查所有安全阀,真空表,压力表等是否良好,必须保持良好;4.检查反应锅减速器极端面轴封是否保持良好,必须保持良好;5.检查真空干燥机运转及其管道系统是否正常,必须保持良好(精致工段)6.检查压滤器及其管道系统,安全阀是否正常,必须保持良好(缩合工段)7.检查水冲泵、真空泵、真空储气罐及真空管道系统、空压机及其管道系统是否良好,必须保持良好;8.检查能源系统:蒸汽压力、冷却水压力、冰盐水温度是否达到生产要求,必须符合生产要求;9.检查计量设备及系统:磅秤是否正常、各计量高、低位液位管是否正常,必须保持正常;10. 检查生产操作作用是否齐全:11. 检查劳防用品的配备及穿戴。
(二)生产原料的检查1.检查生产所需各种原料是否准备足量:2.检查各种原料是否具有合格证。
二、生产操作(一)成盐工序:1、备料:(1)二甲胺水溶液:188kg 、(2)盐酸1: 196kg;2、按规定检查复核场地、设备是否清洁,检查并复核所用原料批号、规格、数量是否正常,记录反应锅编号:3、检查冰盐水温度。
关闭反应锅底阀、及其他阀门,开反应锅夹套冰盐水进、回阀进行冷却;4、称料前按规定复核磅称,将盐酸备入高位,二甲胺水溶液计量好,将锅内真空拉到—800Mpa时关闭真空阀,打开进料阀用余真空将二甲胺水溶液抽入反应锅内,开启搅拌;5、当锅内温度冷却至20℃以下时,打开盐酸阀开始加盐酸,控制锅内温度在26℃以下;6、滴加盐酸至196kg后停止滴加,搅拌5—6分钟,打开人孔盖,测pH=1—2,在搅拌5分钟复测pH=1—2不变时,关闭人孔盖,关闭两只盐酸阀,滴加盐酸完成;7、关闭冰盐水进、回阀、打开锅子夹套空亚阀和盐水压回阀,将夹套冰盐水压回盐水箱,等压力表指针退到0时,关闭夹套盐水压回阀和空压阀;8、打开锅子夹套蒸汽进、回阀,打开蒸馏冷凝器冷却水进、回阀,同时打开蒸馏阀、酸水低位的真空阀和酸水蒸出阀,开始减压蒸水,锅内真空度要求为—0.09Mpa以下,锅内温度控制在130℃以下,蒸净酸水得到白色蓬松状粉末即为二甲胺盐酸盐;9、关闭锅子夹套蒸汽进、回阀,当锅内真空度在—0.09Mpa以下时(保留真空),关闭搅拌、蒸馏阀、酸水低位的真空阀、酸水真空阀;10、打开酸水低位放空阀和底阀,将费酸水放入废水池,放完后关闭酸水低位放空阀和底阀;11、注意事项:(1)盐酸属于强腐蚀剂,要求在抽取时必须戴好防护面罩和防护手套,以免盐酸灼伤肌肤,如果有盐酸洒在衣服或皮肤上,应该立即用自来水冲洗;(2)二甲胺水溶液是易燃、易挥发、有浓重氨味的液体,在抽取该原料时应该尽量避免洒出,也不要近距离嗅闻,以免伤害呼吸道,严禁明火接触;(3)滴加盐酸速度不宜过快,减压蒸水保持真空度在—0.09Mpa以下,蒸水必须蒸干蒸净;(二)缩合工序:1、备料二甲胺盐酸盐(成盐工序的整批料)、双氰胺:125kg、异戊醇:500kg、自来水:100kg;2、打开异戊醇低位底阀和放空阀,开启锅子异戊醇进料阀,用锅内余真空将计量好的异戊醇抽入锅内,如果余真空不能完全将异戊醇抽入锅内,可打开锅子真空阀将异戊醇全部抽入锅内,关闭异戊醇低位底阀和放空阀、锅子异戊醇进料阀和真空阀,打开锅子放空阀和人孔盖,将预备好的125kg双氰胺投入锅内,关闭锅子放空阀和人孔盖;3、开启搅拌,打开蒸馏阀、酸水蒸出阀和低位放空阀、夹套蒸汽进、回阀,升温至锅内温度128℃时,关闭酸水蒸出阀和低位放空阀,前蒸馏物弃去。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
葡萄糖与苯肼反应制糖脎
成员:高敏琳541279440@
蔡忠辉1669181308@
一、危险性评估及相应防护措施(苯肼)
1、危险性概述
①健康危害:该品可引起溶血性贫血、高铁血红蛋白血症、高胆红素血症,以及中枢神经系统和肝、肾、心脏损害。
②急性中毒:轻度中毒有头痛、头晕、无力、食欲不振、腹痛、腹泻等。
较重时尚有呼吸困难、抽搐、震颤,甚至共济失调、意识不清。
重症者出现紫绀、黄疸、白细胞减少,并可发生溶血性贫血、高胆红素血症和肝、肾损害。
③慢性中毒:长期接触可发生心、肝、肾损害。
可致皮肤损害,重者可发生水疱、水肿等。
④环境危害:对环境有危害。
⑤燃爆危险:该品可燃,有毒。
2、急救措施
①皮肤接触:脱去污染的衣着,用肥皂水和清水彻底冲洗皮肤。
②眼睛接触:提起眼睑,用流动清水或生理盐水冲洗。
就医。
③吸入:迅速脱离现场至空气新鲜处。
保持呼吸道通畅。
如呼吸困难,给输氧。
如呼吸停止,立即进行人工呼吸。
就医。
④食入:饮足量温水,催吐。
就医。
二、实验目的
1、了解单糖与苯肼试剂作用成脎反应的基本原理。
2、通过查阅文献积累经验。
三、实验原理
成脎反应发生在糖分子中的C1-C2上,但是对其机理的研究还是很模糊:
①有人认为糖脎生成分三步:单糖先于苯肼作用生成苯腙,苯腙中原来和羰基相邻的碳原子的羟基又被苯肼氧化成葡萄糖苯腙,然后在与苯肼反应,最后生成糖脎。
②有人认为先是羰基质子化,在与苯肼亲核加成,经过两次异构化,最终与三分子苯肼亲核加成。
推测成脎反应实际上是一复杂的多不反应及异构化过程反应机理复杂,葡萄糖成脎的机理可能为:
本实验的反应方程式如下:
四、主要物料及产物的物理常数
五、实验试剂
六、主要反应装置图
七、实验步骤
1、配置葡萄糖的浓度10%,苯肼的浓度22%
2、称取5g(或者量取3.3ml)葡萄糖于100ml烧杯中,加入45ml水,即得10%的葡萄糖,
3、取量10ml的苯肼于100ml烧杯中,加入39ml热水至烧杯冷却即得22%的苯肼溶液。
4,量取1.9ml冰醋酸,4.9g醋酸钠于一烧杯中,再向烧杯中加入50ml 蒸馏水,充分搅拌即得pH=5的醋酸-醋酸钠缓冲溶液。
(pH=4.75+lg(N 盐/N酸)
4、将上面所配置的葡萄糖溶液和苯肼溶液全部加入到250ml的圆底烧杯中摇荡烧瓶,使之混合均匀,再加入20ml醋酸-醋酸钠缓冲溶液,调pH到5左右,摇荡烧瓶。
5,按图安装好实验装置。
6、在沸水浴上加热30~40分钟,将温度控制在80℃左右,当有大量深黄绿色晶体析出时,停止水浴加热,使其自然冷却至室温。
7、抽滤,粗产品用95%的酒精洗涤,尽量抽干,称量,计算产率。
八、注意事项
1.苯肼毒性较大, 操作时应小心, 防止试剂溢出或沾到皮肤上. 如不慎触及皮肤, 应先用稀醋酸洗, 继之以水洗.
2.苯肼遇明火、高热可燃,故实验时须远离热源
3.苯肼不溶于冷水,故需用热水配置
4.苯肼受热分解放出有毒的氧化氮烟气,尾气用装有水烧杯吸收。
5.本实验在pH=5时产率最高,故需要将pH调到5左右
九、参考文献
周文富;几种还原糖与苯肼的加成研究[j];化学通报;2002年第6 期程定海;葡萄糖成脎反应机理的红外光谱研究[J];四川师范学院学报(自然科学版);1995年02期
李瑞波;;对于糖脎生成的探讨[J];牡丹江师范学院学报(自然科学版);2006年03期。
