分子晶体与原子晶体
分子晶体和原子晶体

学与问
1、怎样从原子结构角度理解金刚石、硅 和锗的熔点和硬度依次下降?
解释:结构相似的原子晶体,原子半径越小, 键长越短,键能越大,晶体熔点越高 金刚石 > 碳化硅 > 晶体硅
2、“具有共价键的晶体叫做原子晶体”。这 种说法对吗?为什么?
知识拓展-石墨
一种结晶形碳,有天然出产的矿物。铁黑 色至深钢灰色。质软具滑腻感,可沾污手指成 灰黑色。有金属光泽。六方晶系,成叶片状、 鳞片状和致密块状。密度2.25g/cm3,化学性 质不活泼。具有耐腐蚀性,在空气或氧气中强 热可以燃烧生成二氧化碳。石墨可用作润滑剂, 并用于制造坩锅、电极、铅笔芯等。
因此,比较分子晶体的熔、沸点高低, 实际上就是比较分子间作用力(包括范力 和氢键)的大小。
(1)组成和结构相似的物质,
分子量越大,熔沸点越高。 ___________________________________
烷烃、烯烃、炔烃、饱和一元醇、醛、 羧酸等同系物的沸点均随着碳原子数的增 加而升高。
因为CO2是分子晶体,SiO2是原子晶体, 所以熔化时CO2是破坏范德华力而SiO2是破 坏化学键。所以SiO2熔沸点高。
破坏CO2分子与SiO2时,都是破坏共价 健,而C-O键能>Si-O键能,所以CO2分子更 稳定。
4、原子晶体熔、沸点比较规律 在共价键形成的原子晶体中,原子半
径小的,键长短,键能大,晶体的熔、沸 点高。如:金刚石 > 碳化硅 > 晶体硅
2 、分子晶体和原子晶体
一、分子晶体
1、概念 分子间以分子间作用力(范德华力,氢键)相 结合的晶体叫分子晶体。
构成分子晶体的粒子是分子,
粒子间的相互作用是分子间作用力 .
分子晶体有哪些物理特性,为什么?
分子晶体与原子晶体PPT课件

② 分子晶体熔化时一般只破坏分子间作 用力,不破坏化学键,也有例外,如S8
(2)较小的硬度;
(3)一般都是绝缘体,熔融状态也不导电。 有些在水溶液中可以导电.
➢原因:分子间作用力较弱
.
14
5、典型的分子晶体:
(1)所有非金属氢化物:H2O,H2S,NH3, CH4,HX
(1)范德华力
(2)分子间氢键
.
26
讨论
CO2和SiO2的一些物理性质如下所示,通过 比较,判断SiO2晶体是否属于分子晶体。
CO2 SiO2
熔点/oC -56.2 1723
状态(室温) 气态 固态
结论:SiO2不是分子晶体。 那么SiO2是什么晶体呢?
.
27
二、原子晶体
1、定义:原子间以共价键相结合而形成 的空间网状结构的晶体。
.
24
〖思考2〗为何干冰的熔沸点比冰低,密度却 比冰大?
由于冰中除了范德华力外还有氢键作用, 破坏分子间作用力较难,所以熔沸点比干冰 高。
由于分子间作用力特别是氢键的方向性, 导致晶体冰中有相当大的空隙,所以相同状 况下体积较大
由于CO2分子的相对分子质量>H2O,所 以干冰的密度大。
.
25
〖归纳要点〗分子的密度取决于晶体 的体积,取决于紧密堆积程度,分子 晶体的紧密堆积由以下两个因素决定:
7
一、分子晶体
一、概念
分子间以分子间作用力(范德华力,氢 键)相结合的晶体叫分子晶体。
构成分子晶体的粒子:分子,
粒子间的相互作用:分子间作用力。
分子晶体熔化时:
一般只破坏分子间作用力,
分子晶体与原子晶体

晶胞类型 观察同一种点,如观察空心圆点 Cl-,正
六面体的 8 个顶点和各面的中心,均有一个。所以为面心
立方晶胞。
整理课件
23
小结、晶体结构的基本单元 --晶胞
1、 晶胞是晶体的最小结构重复单元。
晶胞是从晶体结构中截取出来的大小、形状完 全 相同的平行六面体。
晶体是晶胞“无隙并置”而成 2、 晶胞必须符合两个条件: 一是代表晶体的化学组成;二是代表晶体的对称性, 即与晶体具有相同的对称元素 —— 对称轴,对称面 和对称中心 ) 。
3
Ti
8=1 Ca:1
整理课件
O
40
现有甲、乙、丙、丁四种晶胞(如图2-8所
示 比)为_,_1可_:_1推_;知乙:晶甲体晶的体化中学A与式B为的_C_离_2子_D_个;数丙 晶体的化学式为_E__F___;丁晶体的化学式 为_X__Y__2_Z。
整理课件
41
巩固练习:
某晶胞结 构如图所示, 晶胞中各微粒 个数分别为:
整理课件
14
干冰晶体结构
整理课件
碘晶体结构 15
二﹑晶胞 组成晶体的细胞 1. 晶胞:描述晶体结构的基本单元
蜂巢与蜂室
铜晶体
铜铜晶晶胞胞
晶体与晶胞的关系可用蜂巢与峰室的关系比 喻
整理课件16Fra bibliotek 晶体与晶胞整理课件
17
NaCl晶体结构和晶胞
整理课件
18
干冰的晶体结构图 将图中的CO2分子换成I2分子 即为碘晶体的结构图
二 氧 化 碳 分 子
整理课件
19
CsCl晶体
整理课件
20
1、体心——全部 2、面心——1/2 3、棱上的点——1/4 4、顶点(具体问题具体分析)
高中化学选修3之知识讲解_晶体的常识 分子晶体与原子晶体_基础-

晶体的常识分子晶体与原子晶体【学习目标】1、初步了解晶体的知识,知道晶体与非晶体的本质差异,学会识别晶体与非晶体的结构示意图;2、知道晶胞的概念,了解晶胞与晶体的关系,学会通过分析晶胞得出晶体的组成;3、了解分子晶体和原子晶体的特征,能以典型的物质为例描述分子晶体和原子晶体的结构与性质的关系;4、知道分子晶体与原子晶体的结构粒子、粒子间作用力的区别。
【要点梳理】要点一、晶体与非晶体【分子晶体与原子晶体#晶体与非晶体】1、概念:①晶体:质点(分子、离子、原子)在空间有规则地排列成的、具有整齐外型、以多面体出现的固体物质。
晶体具有的规则的几何外形源于组成晶体的微粒按一定规律周期性的重复排列。
②非晶体:非晶态物质内部结构没有周期性特点,而是杂乱无章地排列,如:玻璃、松香、明胶等。
非晶体不具有晶体物质的共性,某些非晶态物质具有优良的性质要点诠释:晶体与非晶体的区分:晶体是由原子或分子在空间按一定规律周期性地重复排列构成的固体物质。
周期性是晶体结构最基本的特征。
许多固体的粉末用肉眼是看不见晶体的,但我们可以借助于显微镜观察,这也证明固体粉末仍是晶体,只不过晶粒太小了。
晶体的熔点较固定,而非晶体则没有固定的熔点。
区分晶体和非晶体最可靠的科学方法是对固体,进行X—射线衍射实验,X射线透过晶体时发生衍射现象。
特别注意:一种物质是否晶体,是由其内部结构决定的,而非由外观判断。
2、分类:说明:①自范性:晶体能自发性地呈现多面体外形的性质。
所谓自范性即“自发”进行,但这里要注意,“自发”过程的实现仍需一定的条件。
例如:水能自发地从高处流向低处,但若不打开拦截水流的闸门,水库里的水不能下泻;②晶体自范性的条件之一:生长速率适当;③晶体自范性的本质:是晶体中粒子微观空间里呈现周期性的有序排列的宏观表象。
4、晶体形成的途径:①熔融态物质凝固,例:熔融态的二氧化硅,快速冷却得到玛瑙,而缓慢冷却得到水晶。
②气态物质冷却不经液态直接凝固(凝华);③溶质从溶液中析出。
无机化学——原子晶体与分子晶体
B
B
C A
A
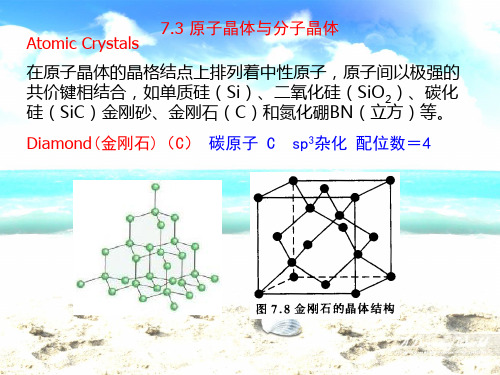
面心立方 紧密堆积
六方紧密堆积
Body-centered cubic cell (BCC)
体心立方紧密堆积 CN=12,利用率 =68% K、Rb、Cs、Li、 Na A B
A
体心立方 紧密堆积
7.4.2 金属键 金属键:金属原子的价电子可以完全失去成为自由电子,并在 晶格中运动,自由电子把金属阳离子胶合成金属晶体,这种胶 合作用就叫金属键。金属键无饱和性和方向性。
氯化氢、氨、三氯化磷、冰等由极性键构成的极性分子,晶体 中分子间存在色散力、取向力、诱导力,有的还有氢键,所以 它们的结点上的粒子间作用力大于分子量相近的非极性分子之 间的引力。
分子晶体的特性 分子晶体是以独立的分子出现的 ,化学式就是分子式。
分子晶体可以是非金属单质,如卤素、H2、N2、O2; 非金属化合物,如CO2、H2S、HCl、HN3等 绝大多数有机化合物,稀有气体的晶体
7.6.3 离子极化对物质性质的影响 一、离子的电子构型
外层电子结构 电子构型 阳离子实例
ns2np6
8
Na+, Mg2+,Al3+,Ti4+
ns2np6 nd1-9
9-17
Cr3+,Mn2+,Fe3+,Cu2+
ns2np6 nd10
18
Ag+,Zn2+,Cd2+,Hg2+
s2p6d10ns2
18+2
7.3 原子晶体与分子晶体 Atomic Crystals
在原子晶体的晶格结点上排列着中性原子,原子间以极强的 共价键相结合,如单质硅(Si)、二氧化硅(SiO2)、碳化 硅(SiC)金刚砂、金刚石(C)和氮化硼BN(立方)等。
分子晶体和原子晶体

分子晶体和原子晶体
1、分子晶体和原子晶体区别:
(1)单体结构不同。
分子晶体一般是有物质分子构成,而原子晶体一般有单个原子构成;
(2)晶体内作用力不同。
分子晶体一般是通过分子间范德华力作用形成,而原子晶体一般通过原子共价键作用形成;
(3)物理性质不同。
分子晶体一般硬度、熔点较低,而原子晶体一般硬度、熔点很高。
比如白糖属于分子晶体,而钻石属于原子晶体,二者硬度、熔点差别很大;
(4)存在形式有差异。
分子晶体一般有固、液、气三种存在形式,而原子晶体一般只有固体存在形式。
分子晶体典型代表:
1、所有非金属氢化物;
2、大部分非金属单质(稀有气体形成的晶体也属于分子晶体),如:卤素(X2)、氧气、硫(S8)、氮(N2)、白磷(P4)、C60等(金刚石,和单晶硅等是原子晶体);
3、部分非金属氧化物,如:CO2、SO2、SO3、P4O6、P4O10等(如SiO2是原子晶体) ;
4、几乎所有的酸;
5、绝大多数有机化合物,如:苯、乙酸、乙醇、葡萄糖等 ;
6、所有常温下呈气态的物质、常温下呈液态的物质(除汞外)、
易挥发的固态物质。
原子晶体类型:
1、某些金属单质:晶体锗(Ge)等;
2、某些非金属化合物:氮化硼(BN)晶体、碳化硅、二氧化硅等;
3、非金属单质:金刚石、晶体硅、晶体硼等。
原子晶体 分子晶体

原子晶体分子晶体
原子晶体和分子晶体都是固体的一种形式,它们之间的主要区别在于它们的基本构建单位。
1. 原子晶体:
•构建单位:在原子晶体中,基本的构建单位是原子。
这些原子通过离子键、共价键或金属键等方式相互结合,形成均匀的晶体结构。
•例子:金属晶体(如铁、铜)、离子晶体(如氯化钠NaCl)是原子晶体的例子。
在金属晶体中,金属原子通过金属键结合,形成具有电子云的电子海。
在离子晶体中,正负离子通过离子键相互吸引形成晶体结构。
2. 分子晶体:
•构建单位:在分子晶体中,基本的构建单位是分子。
分子通过分子间的力(如范德华力、氢键、共价键等)相互结合,形成晶体结构。
•例子:葡萄糖、水合铜硫酸是分子晶体的例子。
在葡萄糖中,分子是由碳、氢、氧原子组成的葡萄糖分子,它们通过共价键结合在一起。
在水合铜硫酸中,分子是由铜、氧、硫、氢和水分子组成,它们通过范德华力等相互结合。
总的来说,原子晶体和分子晶体的区别在于它们构建晶体结构的基本单位:是原子还是分子。
在实际应用中,这两种类型的晶体具有不同的性质和特征。
第二节 分子晶体与原子晶体

第三章第二节分子晶体与原子晶体第一课时分子晶体教学目标1、使学生了解分子晶体的组成粒子、结构模型和结构特点及其性质的一般特点。
2、使学生了解晶体类型与性质的关系。
3、使学生理解分子间作用力和氢键对物质物理性质的影响。
4、知道一些常见的属于分子晶体的物质类别。
5、使学生主动参与科学探究,体验研究过程,激发他们的学习兴趣。
教学重点、难点重点掌握分子晶体的结构特点和性质特点难点是氢键的方向性和氢键对物体物理性质的影响从三维空间结构认识晶胞的组成、结构教学方法建议:运用模型和类比方法诱导、分析、归纳教学过程:[引入]我们已经知道,固体有晶体和非晶体之分,绝大多数常见的固体是晶体。
现在给出下列晶体的熔点:甲烷(-182.5℃)氮(-210.1℃)金刚石(3900℃)氧化铝(2030℃),氯化钠(801℃)同为晶体,为什么它们的熔点及其性质有如此大的差异呢?物质结构决定物质性质,我们需要探讨晶体的内部结构来回答这个问题。
分类研究是科学研究的基本方法之一,根据晶体结构的不同,我们把年个吨毫2分为若干类型,其中,只含分子的晶体称为分子晶体。
一、分子晶体1、定义:含分子的晶体称为分子晶体也就是说:分子间以分子间作用力相结合的晶体叫做分子晶体分子,就属于分子晶体问:还有哪些属于分子晶看图,如:碘晶体中只含有I2体?2、较典型的分子晶体有非金属氢化物,部分非金属单质,部分非金属氧化物,几乎所有的酸,绝大多数有机物的晶体。
3、分子间作用力和氢键过度:首先让我们回忆一下分子间作用力的有关知识阅读必修2 科学视野教师诱导:分子间存在着一种把分子聚集在一起的作用力叫做分子间作用力,也叫范徳华力。
分子间作用力对物质的性质有怎么样的影响?学生回答:一般来说,对于组成和结构相似的物质,相对分子量量越大分子间作用力越大,物质的熔、沸点也越高。
教师诱导:但是有些氢化物的熔点和沸点的递变却与此不完全符合,如:NH3、H2 O和HF的沸点就出现反常。
晶体结构(3, 原子晶体与分子晶体)
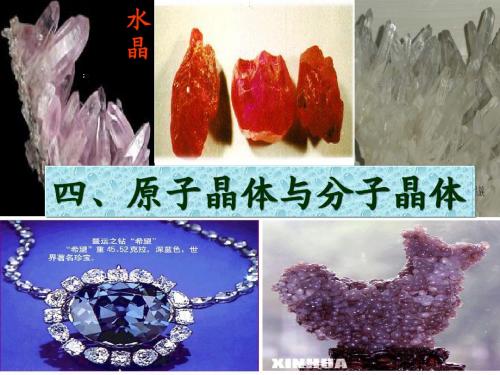
金刚石晶体
金刚石晶体
①每个碳 原子与 4 个碳原子 相连; 相连;
基本单元: 基本单元: 六元环
6 个碳
原子形成一 个六 元 环
金刚石晶体
②晶体中碳原子与C-C键数 晶体中碳原子与C 目比 1:2 。
SiO2晶体
①构成SiO2晶体的微粒是什么? 构成SiO 晶体的微粒是什么? Si原子和 原子和O Si原子和O原子
CO2
SiO2
课堂练习
° 1、 白磷分子中的键角为 60° ,分子的空间结 、 每个P原子与 构为正四面体 ,每个 原子与 3 个P原子结合成共 原子结合成共 价键。若将1分子白磷中的所有 分子白磷中的所有P-P键打开并各插 价键。若将 分子白磷中的所有 键打开并各插 个氧原子, 若每个P 入一个氧原子, 入一个氧原子,共可结合 6 个氧原子, 若每个P 原子上的孤对电子再与氧原子配位, 原子上的孤对电子再与氧原子配位,就可以得到 填分子式)。 磷的另一种氧化物 P4O10 (填分子式)。
SiO2晶体
④晶体中最小的环有 12 个 原子。 原子。
小结: 小结:三种化学键的比较
化学键 成键本质
由电子静电作用 键的方 影响键强弱 的因素 向性和 饱和性
金属键 金属阳离子和自 离子键 阴阳离子间的 静电作用 共价键 共用电子对
无 无 有
原子半径和 价电子数 离子半径和 离子电荷 键长
课堂练习 1、下列物质属于原子晶体的 化合物是 ( C ) A.金刚石 A.金刚石 B.NaOH C.二氧化硅 D.干冰 C.二氧化硅 D.干冰
小试牛刀】 【小试牛刀】
下列物质在变化过程中, 例1.下列物质在变化过程中,只需克服分子 下列物质在变化过程中 间作用力的是 ( C ) A.食盐溶解 食盐溶解 C.干冰升华 干冰升华 B.铁的熔化 铁的熔化 D.氯化铵的“升华” 氯化铵的“ 氯化铵的 升华”
分子晶体和原子晶体

分子晶体和原子晶体
图2-15 金刚石原子晶体示意图
分子晶体和原子晶体
二氧化碳和方石英都是第Ⅳ A元素化合物, 由于前者是分子晶体,后者是原子晶体,导致 物理性质差别较大。CO2在-78.5 ℃时即升华, 而SiO2的熔点却高达1610 ℃,说明晶体结构 不同,微粒间的作用不同,物质的物理性质也 不同。
分子晶体和原子晶体
在原子晶体中,不存在独立的小分子,而只能把整个晶体看成是 一个大分子,没有确定的相对分子质量。由于共价键具有饱和性和方 向性,所以原子晶体的配位数一般不高。以典型的金刚石原子晶体为 例,每一个碳原子在成键时以sp3等性杂化形成4个sp3共价键,构成 正四面体,所以碳原子的配位数为4。无数的碳原子相互连接构成, 如图2-15所示晶体结构。原子晶体中,原子间以共价键相连,所以 表现出有较高的硬度和较高的熔点(金刚石硬度最大,熔点为3849 K)。 通常这类晶体不导电、不导热,熔化时也不导电,但硅、碳化硅等具 有半导体性质,可以有条件地导电。
分子晶体和原子晶体
图2-14 CO2分子晶体示意图
分子晶体和原子晶体
二、 原子晶体
在晶格结点上排列的微粒为原子,原子之间以 共价键结合构成的晶体称为原子晶体,如碳(金刚 石)、硅(单晶硅)、锗(半导体单晶)及第Ⅳ A族元素 的单质都属于原子晶体,化合物中的碳化硅(SiC)、 砷化镓(GaAs)、方石英(SiO2)等也属于原子晶体。
无机化学
分子晶体和原子晶体
一、 分子晶体
在晶格结点上排列着分子,通过分子间力而形成的晶体, 称为分子晶体,如非金属单质和非金属元素之间的固体化合物 CO2是分子晶体,其晶体结构如图2-14所示。分子晶体中存在 着独立的分子,分子晶体内是共价键,分子晶体间的作用力是 分子间力,由于分子间力很弱,因此分子晶体的熔点低,具有 较大的挥发性,硬度较小,易溶于非极性溶剂,通常是电的不 良导体。若干极性分子晶体在水中解离生成离子,则其水溶液 导电,如HCl溶液。
分子晶体和原子晶体

HXC60P106, P1010都形成分子晶体,只有很少的一部分和______SiO2,碳化硅,第二节分子晶体和原子晶体一、分子晶体(一)、概念:分子间以______________________ (_____________ , ________________ )相结合的晶体叫分子晶体。
注意:(1)构成分子晶体的粒子是 ______________________ 。
(2 )在分子晶体中,分子内的原子间以结合,而相邻分子靠或相互吸引。
(3 )范德华力化学键的作用:(4 )分子晶体熔化破坏的是O(二)•分子晶体的物理特性:(1)___ 的熔点和沸点,(2) ______________ 的硬度,________ 挥发, _________ 升华(3)—般都是________ 体,固体和熔融状态都__________________ 导电。
(4)分子晶体的溶解性与溶质和溶剂的分子的___________________ 相关一一____________________思考:1、为什么分子晶体熔沸点低、易挥发、易升华、硬度小?原因:分子晶体发生这些变化时_只破坏 __________________________ , ________________ 很弱,克服它时需要的能量小。
所以分子晶体熔沸点低、易挥发、易升华、硬度小。
2、为什么分子晶体在晶体和熔融状态均不导电?它们在晶体和熔融状态均不存在_______________________ 。
部分分子晶体溶于水在水分子作用下发生_____________ 导电,如HCI, H2S04 ;有些溶于水与水反应生成_______________________________ 而导电,晶体硼等。
)(四)分子晶体结构特征1. ______________________________ __ 分子密堆积每个分子周围有______________ 个紧邻的分子,如:C60、干冰、12、02——不具有分子密堆积特征P1,CH4,2,冰中1个水分lmol冰周I韦]有mol氢键。
高中化学必修三 分子晶体和原子晶体

思考:你怎么理解 “巨分子” “共价晶体
”? 2、结构特点:
(1)构成粒子:原子。
三态变化、 化学反应 都破坏它
(2)粒子间的作用:共价键。
3、原子晶体的物理特性及影响因素:
–熔点和沸点很高 –硬度大(金刚石在自然界中硬度最大) –一般不导电 –难溶于一些常见的溶剂
分子的非密堆积 氢键具有方向性
氢键具有饱和性 冰的结构 冰中1个水分子周围有4个水分子
排列方式:冰晶体与C60、CO2相比,结构上有何特点? 对性质有何影响?
冰晶体
✓液态水中有无氢键?和冰在结构上有何区别? 这种区别导致冰融化成水时体积有何变化?密度呢?
6、分子晶体结构特征
(1)只有范德华力,无分子间氢键-分子密堆积
分子的密堆积
每个CO2分子周围有12个CO2分子
分子的密堆积
O2的晶体结构
C60的晶胞
(与每个分子距离最近的相同分子共有12个 )
6、分子晶体的结构特征
(1)只有范德华力,无分子间氢键-分子密堆积
分子密堆积-- 每个分子周围有 :C60、干冰 、O2
个紧邻的分子。 如
• 冰晶体中,每个水分子周围有几个紧邻的分子? 他们是什么样的空间关系?为什么会这样排列?
分子间: 分子间作用力(范德华力、氢键)
4、分子晶体物理性质的共性: 熔点低、易升华、硬度小
导电性: 通常,晶体本身不导电,熔融状态也 不能导电,但某些分子晶体的水溶液能导电。
溶解性: 相似相溶原理
思考:以下晶体中哪些属于分子晶体?
S、 H2SO4、 C60、 尿素、 He 、 NH3、 SiO2、 SO2、 P4O6、 P、 Cl2、 C(金刚石)、 H2S、 冰醋酸
原子晶体与分子晶体

2NA 。 (4)12克金刚石中C—C键数为_______
(2)二氧化硅 若在硅晶体结构中的每个Si-Si键中“插入”一个 氧原子,便可得到以硅氧四面体为骨架的SiO2晶体的 结构
Si O
109º 28´
共价键
Байду номын сангаас
Si O
注意:
原子晶体的化学式并不表示其实际的组成,只 基本结构单元: 正四面体 表示原子的个数比。 1 个Si连接____ 4 个 ,___ 2 个Si, (1)___ 1 个 连接____ 1:2 的比例组成的立体空间网状结构。 SiO 是由Si和O按_____
练习:
1.下列晶体中不属于原子晶体的是 (A ) A.干冰 B.金刚砂 C.金刚石 D.水晶
2、下列叙述正确的是 (AD ) A.离子晶体都是化合物 B.原子晶体都是单质 C.分子晶体内部都存在共价键 D.金属单质形成的晶体都是金属晶体
3.在金刚石的网状结构中,含有共价键形 成的碳原子 环,其中最小的环上,碳原子 数是 ( D ) A.2个 B.3个 C.4个 D.6个 4,下列各物质中,按熔点由低到高排列 正确的是( B ) A.O2、I2、Hg B.CO2、KCl、SiO2 C.Na、K、Rb D.SiC、NaCl、SiO2
12
。
氢键具有方向性 和饱和性
(3)冰
冰晶体主要是水分子依靠氢 键形成的(亦有范德华力)。 由于氢键的方向性和饱和性, 分子间距比较大,有很多空 隙,结构比较松散。每个水 分子周周有4个水分子,故 配位数为4。
(4)其他分子晶体
①硫黄:硫的同素异形体最稳定的是S8,不溶于水, 微溶于酒精和乙醚,易溶于CS2。 试管壁上的硫如何洗涤?
③ 一般都是绝缘体,熔融状态不导电。
原子晶体 分子晶体

原子晶体分子晶体
摘要:
一、原子晶体和分子晶体的概念
二、原子晶体和分子晶体的区别
三、原子晶体和分子晶体的性质和应用
正文:
原子晶体和分子晶体是两种常见的晶体类型,它们在结构、性质和应用上都有所不同。
原子晶体是由原子通过共价键以空间网状结构形成的晶体。
例如,金刚石、晶体硅和二氧化硅等物质都是原子晶体。
在原子晶体中,原子之间通过共价键结合在一起,形成一个三维的、有序的结构。
这种结构具有较高的熔点、沸点和硬度,因此在工业上具有广泛的应用。
分子晶体是由分子通过分子间作用力结合而成的晶体。
例如,冰、干冰和氧气等物质都是分子晶体。
在分子晶体中,分子之间通过范德华力或氢键结合在一起,形成一个二维的、无序的结构。
这种结构具有较低的熔点、沸点和硬度,因此在制冷、保鲜和运输等领域具有广泛的应用。
原子晶体和分子晶体的区别在于它们的结构和结合方式。
原子晶体是由原子通过共价键结合而成的,具有较高的熔点、沸点和硬度;分子晶体是由分子通过分子间作用力结合而成的,具有较低的熔点、沸点和硬度。
原子晶体和分子晶体的性质和应用也不同。
原子晶体具有较高的熔点、沸点和硬度,因此在工业上广泛应用于制造高强度、高硬度的材料,如切削刀
具、钻头和模具等。
分子晶体具有较低的熔点、沸点和硬度,因此在制冷、保鲜和运输等领域具有广泛的应用。
综上所述,原子晶体和分子晶体在结构、性质和应用上都有所不同。
第二节分子晶体与原子晶体

第二节分子晶体与原子晶体① C60②干冰:CO2的晶体。
分子间存在范德华力,熔点低,易升华,制冷剂。
〔2〕冰的晶体:氢键型晶体、每个水分子周围只有4个紧邻的水分子、正四面体形。
特点:4℃密度最大。
教学过程教学步骤、内容教学方法、手段、师生活动[引入]咱们在第二章中已学过分子间作用力,在必修中也学过离子键和共价键,有谁总结一下微粒间的作用力有哪些?〔讨论〕[师生共同总结]微粒间作用:微粒为分子:分子间作用力〔或范德华力〕或氢键;微粒为原子:极性共价键或非极性共价键;微粒为离子:离子键。
[过渡]今天我们开始研究晶体中微粒间的作用力。
[板书]第二节分子晶体与原子晶体一、分子晶体[讲]只含分子的晶体称为分子晶体。
如碘晶体只含I2分子,属于分子晶体。
在分子晶体中,分子内的原子间以共价键结合,而相邻分子靠分子间作用力相互吸引。
[板书]1、分子晶体:(1) 定义:由分子构成。
相邻分子靠分子间作用力相互吸引。
(2) 构成微粒:分子[讲]稀有气体为单原子分子。
也是分子晶体[板书](3) 微粒间的作用[讲]分子间作用力,部分晶体中存在氢键。
分子晶体采纳密堆积。
[设咨询]依照分子间作用力较弱的特点判定分子晶体的特性有哪些?参照表3-2。
[投影][讲]分子间作用力的大小决定了晶体的物理性质。
分子晶体要熔化、要汽化都要克服分子间的作用力。
分子的相对分子质量越大,分子间作用力越大,物质的熔沸点越高,硬度越大。
比如氧气分子间作用力比氮气分子间作用力大,氧气沸点比氮气沸点高。
工业上制氧气,确实是先把空气液化,然后使液态空气蒸发,氮气第一从液态空气中蒸发出来,剩下的要紧是液态氧气。
由于分子间作用用专门弱,克服分子间作用力使物质熔化、汽化所需要的能量较小,因此,分子晶体具有较低的熔沸点和较小的硬度。
分子晶体熔化时,一样只破坏分子间作用力,不破坏分子内的化学键,但也有例外。
如硫晶体熔化时,既破坏了分子间的作用力,同时部分S-S键断裂,形成更小的分子。
3.2 分子晶体和原子晶体

分子的密堆积
干 冰 的 晶 体 结 构 图 (与CO2分子距离最近的CO2分子共有12个 ) 分子距离最近的CO 分子共有12个 共有12
分子的非密堆积
冰的结构 冰中1个水分子周围有4个水分子 冰中1个水分子周围有4 当冰刚刚融化为液态水时, 当冰刚刚融化为液态水时,热运动使冰的结构部分解 水分子间的空隙减小,密度反而增大, 体,水分子间的空隙减小,密度反而增大,超过4 ℃时, 才由于热运动加剧,分子间距离加大,密度渐渐减小。 才由于热运动加剧,分子间距离加大,密度渐渐减小。 ( m=ρv )
[课堂练习] 课堂练习] 四氯化硅的结构和四氯化碳类似,对其性质的推断, 1、四氯化硅的结构和四氯化碳类似,对其性质的推断, 正确的是: 正确的是: ①四氯化碳晶体是分子晶体;②通常情况下为液态; 四氯化碳晶体是分子晶体; 通常情况下为液态; 熔点高于四氯化碳; 属于正四面体的分子构型。 ③熔点高于四氯化碳;④属于正四面体的分子构型。
)
可燃冰
思 考与交流 CO2和SiO2的一些物理性质如下表所 示,通过比较试判断SiO2晶体是否属于分子 晶体。
二、原子晶体(共价晶体) 原子晶体(共价晶体)
1、概念: 概念: 所有原子都以共价键相互结合, 所有原子都以共价键相互结合,整块晶体是一个 三维的共价键网状结构,是一个“巨分子” 三维的共价键网状结构,是一个“巨分子”,又称 共价晶体。 共价晶体。
只含有分子的晶体 分子 分子间作用力
2、构成晶体的微粒: 、构成晶体的微粒: 3、微粒间作用: 、微粒间作用:
4、气化或熔化时破坏的作用力: 分子间作用力 、气化或熔化时破坏的作用力:
5、典型的分子晶体
(1)所有非金属氢化物 (1)所有非金属氢化物: 所有非金属氢化物: (2)大部分酸 (2)大部分酸: 大部分 (3)部分非金属单质 (3)部分非金属单质: 部分非金属单质: H2O,H2S,NH3,CH4,HX H2SO4,HNO3,H3PO4 X2,O2,H2, S8,P4, C60
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
一、分子晶体
回顾:分子间作用力(分子与分子之间的相互作用),存在于分子之间。
分子间作用力
范德华力 氢键
分子间作用力大小的影响因素:
①相对分子质量:同类型分子,相对分子质量越大, 分子间作用力越大。
②分子的极性:分子的极性影响分子间作用力,极性>非极性。
分子通常指的是小分子,不是指高分子。
• 典型的分子晶体:
对于组成和结构相似、晶体中又不含氢键的物质来说,相对分子质量增大, 分子间作用力增强,熔沸点升高。
对于分子间不含氢键的物质来说,由于分子间的作用力无方向性也使得分子 在堆积时会尽可能利用空间并采取紧密堆积方式,这一点与金属晶体和离子晶体 相似,分子的形状、极性以及氢键的存在都会影响分子的堆积方式。
思考与交流
小结:怎么比较晶体的熔点呢?
三、晶体熔、沸点的比较 (1)不同类型晶体熔、沸点的比较: ①不同类型晶体的熔、沸点高低的一般规律:
原__子__晶__体_____>_离__子__晶__体____>_分__子__晶__体____。 ②金属晶体的熔、沸点差别很大,如钨、铂等熔、沸点
很高,汞、铯等熔、沸点很低。
晶胞
金刚石中 每个C原子都以SP3杂化轨道与周围4个碳原子以共价键结合,构成正四面体。 C—C键间的夹角为109.5°。因为中心原子周围排列的原子的数目是有限的,所以这 种比较松散的排列与金属晶体和离子晶体中的紧密堆积排列有很大的不同。
(1)每个碳与①________以共价键结合,形成正四面体结构 (2)键角均为②________ (3)最小碳环由③____个C组成且六原子不在同一平面内 (4)每个C参与4条C—C键的形成,C原子数与C—C键之比为④______
阴离子,如金属晶体。 (4)易误认为金属晶体的熔点比分子晶体的熔点高,其实不一定,如Na
的熔点为97 ℃,尿素的熔点为132.7 ℃。
一 晶体的结构和性质 1.分子晶体中如果只有范德华力,它的晶体一
般采取密堆积结构,原因是分子晶体中( A ) A.范德华力无方向性和饱和性 B.占据晶体结点的粒子是原子 C.化学键是共价键 D.三者都是
石墨晶体的结构
研究发现,石墨晶体具有呈层状结构。同层内每个C 原子用sp2杂化轨道与邻近的三个C原子以共价键相结 合,形成无限的六边形平面网状结构,共价键的键长 为0.142nm,键角为120°;每个C原子还有一个与碳 环平面垂直的未参与杂化的2p轨道,并含有一个未成 对电子。因此能够形成遍及整个平面的大π键。Π电子 可以在整个六边形网状平面上运动,因此石墨的大π键 具有金属键的性质,这就是石墨沿层的平行方向上导 电性强的原因。
而层与层之间以_分__子__间__作__用__力__结合,层与层之间 的距离为0.335nm。层与层之间容易滑动,有滑腻感。 所以石墨晶体虽然熔、沸点很高,但硬度不大。
在石墨晶体中平均每个正六边形拥有的碳原子个 数是2个。C原子与共价键的比值为2:3。
这样,石墨晶体中既有共价键,又有范德华力, 同时还有金属键的特性。我们将这种晶体称为混合键 型晶体。
原子晶体具有 很高 的熔点, 很大 的硬度;对结构相似 的原子晶体来说,原子半径 越小 ,键长 越短 ,键能 越大 , 晶体的熔点就越高。
高熔点、高硬度是原子晶体的特性!
常见的原子晶体有(1)某些单质,如硼、硅、锗、灰锡等; (2)某些非金属化合物,如氮化硼等。
联想.质疑
实验测定,石墨的熔点高达3850℃,高于金刚石的 熔点,这说明石墨晶体具有原子晶体的特点;但是, 石墨很软并且能导电,是非常好的润滑剂,这说明 它又不同于原子晶体。那么石墨究竟属于哪种类型 的晶体呢?
(4)其中既含有离子键又含有非极性共价键的离子晶体是 Na2S2 。 (5)其中含有极性共价键的原子晶体是___S_iO__2_、__S_iC_________。 (6)其中属于分子晶体的是___H__2_O_、__C__O_2_、__C_C__l4_、__C_2_H__2 ____。
5.下列物质的熔、沸点高低顺序中,正确的是( B )
• 非金属氢化物:H2O,H2S,NH3,CH4,HX • 酸:H2SO4,HNO3,H3PO4 • 部分非金属单质:X2,O2,H2, S8,P4, C60 • 大部分非金属氧化物: CO2, SO2, NO2, P4O6, P4O10 • 大多数有机物:乙醇,冰醋酸,蔗糖,烃类
只要存在小分子,其固体就是分子晶体。
第四节 分子晶体与原子晶体
什么是晶体?下列图片中所示是晶体吗?
雪花
冰糖
水晶
金刚石
你知道它们它们都有什么样的物理性质吗?是否属于同种类型?
一、分子晶体
冰和冰糖分别是由水分子、蔗糖分子构成的分子晶体; 水晶和金刚石是由Si、O原子和C原子构成的原子晶体。
❖ 分子晶体:是分子之间通过分子间作用力结合, 从而在三维空间呈有序排列形成的。
(2)同种晶体类型熔、沸点的比较: ①原子晶体:
小
短
大
高
如熔点:金刚石__>__碳化硅__>__硅。
②离子晶体:
a.一般地说,阴、阳离子的电荷数越_多___,离子半径越 _小___,则离子间的作用力就越_强___,其离子晶体的熔、 沸点就越__高__, 如熔点:MgO__>__MgCl2__>__NaCl__>__CsCl。
b.衡量离子晶体稳定性的物理量是晶格能。晶格能越_大___, 形成的离子晶体越_稳_定__,熔点越_高___,硬度越_大___。
③分子晶体:
a.分子间作用力越_大___,物质的熔、沸点越_高___;具有 氢键的分子晶体熔、沸点反常地_高___。 如H2O_>___H2Te__>__H2Se__>__H2S。
思考与交流:
观察下表中的数据可以发现,原子晶体大都具有较高的熔点和硬度,
这是为什么?讨论表中所给出的结构相似的原子晶体的熔点差别较
大的原因?
晶体
金刚石
碳化硅
晶体硅
键能(kJ·mol-1) (C—C)347 (C—Si)301 (Si—Si)226
熔点(℃)
3350
2600
1415
硬度
10
9
7
规律:
以干冰为例,了解分子晶体的物理性质。
分子晶体中分子之间的作用力很微弱。所以熔沸点低、 干冰分子的密堆积 易升华、硬度小、固态和熔融状态不导电。
(1)8个CO2分子构成立方体且在6个面心又各占据1个CO2分子 (2)每个CO2分子周围等距紧邻的CO2分子有____个
面心立方 只要不存在氢键就和干冰一样,密堆积。
(NH4)2S、CO2、CCl4、C2H2、SiO2、SiC、晶体硅、金刚石。
(1)其中只含有离子键的离子晶体是____N__a_C_l_、__N_a_2_S____。
(2)其中既含有离子键又含有极性共价键的离子晶体是_____ __N_a_O__H_、__(_N_H__4_)2_S__。
(3)其中既含有离子键又含有极性共价键和配位键的离子晶体 是___(_N_H__4)_2_S_____________。
构的晶体。 构成原子晶体的粒子是原子,原子间以较强的共价 键相结合。
2、原子晶体的物理特性
• 在原子晶体中,由于原子间以较强的共价键相结合, 而且形成空间立体网状结构,所以原子晶体的。
• 熔点和沸点高(熔化破坏的是共价键) • 硬度大 • 一般不导电 • 且难溶于一些常见的溶剂
3、常见的原子晶体
• CO2和SiO2的一些物理性质如下表所示,通过比较试判断SiO2 晶体是否属于分子晶体。
• 碳元素和硅元素处于元素周期表中同一主族,为什么CO2晶体 的熔、沸点很低,而SiO2晶体的熔沸点很高?
二氧化硅晶体结构示意图
Si
O
180º
109º28´
共价键
二.原子晶体(共价晶体)
1概念:相邻原子间以共价键相结合而形成空间立体网状结
b.组成和结构相似的分子晶体,相对分子质量越_大___, 熔、沸点越_高___,如SnH4_>___GeH4__>__SiH4___>_CH4。
c.组成和结构不相似的物质(相对分子质量接近),分子的极性越大, 其熔、沸点越高,如CO>N2,CH3OH>CH3CH3。
d.同分异构体,支链越多,熔、沸点越低。
(6)石墨的硬度比金刚石小,所以其熔点比金刚石低。( ) (7)干冰(CO2)晶体中包含的作用力为分子间力和共价键。( ) (8)SiO2晶体中包含的作用力只有共价键。( )
【提示】 (1)× (2)× (3)× (4)× (5)× (6)× (7)√ (8)√
易错警示
(1)常温下为气态或液态的物质,其晶体应属于分子晶体(Hg除外)。 (2)原子晶体一定含有共价键,而分子晶体可能不含共价键。 (3)含阴离子的晶体中一定含有阳离子,但含阳离子的晶体由不一定含
3.SiC晶体的结构
SiC是人工合成的无机非金属材料,SiC晶体的结构类似于 金刚石晶体结构,其中C原子和Si原子的位置是 交替的, 所以在整个晶体中Si原子与C原子个数比为 1:1 。
SiC硬度大,而且具有耐热性、耐氧化性和耐腐蚀性,它可以 做磨料、耐火材料、电热元件等,还可以用来制造机械工程 中的结构元件和化工中的密封件等。
分子中存在氢键,非密堆积。
(1)每个水分子与____个水分子相邻
(2)分子以氢键相连接,含1 mol H2O 的冰中,最多可形成________ mol “氢键”
由干冰和冰的晶体结构可以看出,分子晶体在熔化时,破坏的只是分子间作 用力,只需要外界提供较小的能量,因此分子晶体的熔点通常较低,硬度也较小, 具有较强的挥发性。
3.有关金属及金属键的说法正确的是( B )
A.金属键具有方向性与饱和性 B.金属键是金属阳离子与自由电子间的相互作用 C.金属导电是因为在外加电场作用下产生自由电子 D.金属具有光泽是因为金属阳离子吸收并放出可见光
