(完整)初中化学酸碱盐溶解性表以及口诀.doc
溶解性口诀总汇(附溶解性表)

溶解性口诀钾钠铵盐溶水快,①硫酸盐除去钡铅钙。
②氯化物不溶氯化银,硝酸盐溶液都透明。
③口诀中未有皆下沉。
④溶解性口诀二钾、钠、铵盐、硝酸盐;氯化物除银、亚汞;硫酸盐除钡和铅;碳酸、磷酸盐,只溶钾、钠、铵。
溶解性口诀三钾钠铵硝皆可溶、盐酸盐不溶银亚汞;硫酸盐不溶钡和铅、碳磷酸盐多不溶。
多数酸溶碱少溶、只有钾钠铵钡溶溶解性口诀四钾、钠、硝酸溶,(钾盐、钠盐和硝酸盐都溶于水。
)盐酸除银(亚)汞,(盐酸盐里除氯化银和氯化亚汞外都溶。
)再说硫酸盐,不容有钡、铅,(硫酸盐中不溶的是硫酸钡和硫酸铅。
)其余几类盐,(碳酸盐、亚硫酸盐、磷酸盐、硅酸盐和硫化物)只溶钾、钠、铵,(只有相应的钾盐、钠盐和铵盐可溶)最后说碱类,钾、钠、铵和钡。
(氢氧化钾、氢氧化钠、氢氧化钡和氨水可溶)另有几种微溶物,可单独记住。
溶解性口诀五钾钠铵盐硝酸盐完全溶解不困难氯化亚汞氯化银硫酸钡和硫酸铅生成沉淀记心间氢硫酸盐和碱类碳酸磷酸硝酸盐可溶只有钾钠铵记得有硝酸根的和有钠离子的全都溶于水碳酸根只有钡和钙不溶于水硫酸根只有钡不溶于水氯化物只有氯化银不溶于水氢氧根只有镁,铜,铁(包括亚铁)不溶于水初中化学知识顺口溜:高价无亚,低价有亚钾钠银氢正一价钙镁钡锌正二价氟氯溴碘负一价通常氧是负二价铜汞一二铝正三铁有正二和正三碳有正二和正四硫有负二正四六氢、硝、氯根负一价硫、碳酸根负二价磷酸根为负三价还有铵根正一价高锰根和锰酸根前负一来后负二常见金属的活动性顺序表:K Ca Na Mg Al Zn Fe Sn Pb ( H) Cu Hg Ag Pt Au 碱盐溶解性顺口溜:碱除钾钠钡和钙,其余都不溶于水;硝酸盐都溶于水;氯化物除氯化银,其余都可溶于水;硫酸盐除硫酸钡,其余都可溶于水;碳磷盐除钾钠铵,其余都不溶于水。
溶液pH值的测定顺口溜:紫色石蕊试液酸红碱蓝,无色酚酞试液酸无碱红。
小口决:钾钠铵盐都可溶,氯化物不溶氯化银硫酸盐钙银微溶钡不溶硝酸盐遇水影无踪碳酸盐除钾钠铵都不溶氢氧化钙是微溶钾钠钡钙碱可溶红褐铁,蓝絮铜其它沉淀呈白色酸碱盐的溶解性表Ca (+2) Mg (+2)Al(+2/+3 ) Mn (+2) Zn (+2) Fe (+2) Fe (+3) Cu (+2)Ag ( +1) 溶(AgNO 微(Ag2SO 不(Ag2CO不(AgCl ) 不3) 4) 3)THANKS !!!致力为企业和个人提供合同协议,策划案计划书,学习课件等等打造全网一站式需求欢迎您的下载,资料仅供参考。
部分酸碱盐的溶解性表

OH H+ NH4+ K+ Na+ Ba2+ Ca2+ Mg2+ Al3+ Mn2+ Zn2+ Fe2+ Fe3+ Cu2+ Ag+ 酸 1、三大强酸:HCl、HNO3、H2SO4 2、四大强碱:KOH、NaOH、Ba(OH)2、Ca(OH)2 3、可溶性碱:KOH、NaOH、Ba(OH)2、Ca(OH)2、NH3·H2O 4、不可溶性碱的颜色:Cu(OH)2蓝色、Fe(OH)3红褐色、其余不溶性碱为白色 5、盐类物质记忆口诀:钾钠氨盐都可溶;碳酸氢盐都可溶;硝酸盐遇水无影踪;氯化物不溶氯化银;硫酸盐不溶硫酸钡,微溶硫酸钙、硫 酸银;碳酸盐、磷酸盐只溶钾钠氨 溶、挥 溶 溶 溶 微 不 不 不 不 不 不 不
说明:溶表示可溶于水;不表示不溶于水;微表示微溶于水;挥表示挥发性
-
NO3
-
Cl
-
SO4
2-ห้องสมุดไป่ตู้
CO3
2-
O
2-
溶、挥 溶 溶 溶 溶 溶 溶 溶 溶 溶 溶 溶 溶 溶 碱
溶、挥 溶 溶 溶 溶 溶 溶 溶 溶 溶 溶 溶 溶 不
溶 溶 溶 溶 不 微 溶 溶 溶 溶 溶 溶 溶 微 盐
溶、挥 溶 溶 溶 不 不 微 溶 溶 溶 溶 不 不 不 不 不 不 不 不 不 不 不 不 氧化物
初中溶解性表背诵口诀 酸碱盐溶解性表顺口溜

初中溶解性表背诵口诀酸碱盐溶解
性表顺口溜
大家有没有觉得溶解性表很难记?下面
是X整理的初中溶解性表背诵口诀,希望可以帮助到大家。
初中溶解性表背诵口诀钾钠铵碱盐水中溶, (凡是含有K,Na,NH的碱和盐都可溶) 硝酸盐入水无影踪,(硝酸盐全都可溶于水)
盐酸盐除去氯化银,(Cl盐除AgCL外全都溶)
硫酸钡遇水酸不溶。
(硫酸盐除去BaSO4外全都溶,且硫酸钡不溶于酸)
另外碱还要记住Ba Ca也是可溶的。
拓展:化学元素周期表顺口溜
我是氢,我最轻,火箭靠我运卫星;
我是氦,我无赖,得失电子我最菜;
我是锂,密度低,遇水遇酸把泡起;
我是铍,耍赖皮,虽是金属难电离;
我是硼,有点红,论起电子我很穷;
我是碳,反应慢,既能成链又成环;
我是氮,我阻燃,加氢可以合成氨; 我是氧,不用想,离开我就憋得慌; 我是氟,最恶毒,抢个电子就满足; 我是氖,也不赖,通电红光放出来; 我是钠,脾气大,遇酸遇水就火大; 我是镁,最爱美,摄影烟花放光辉; 我是铝,常温里,浓硫酸里把澡洗; 我是硅,色黑灰,信息元件把我堆; 我是磷,害人精,剧毒列表有我名; 我是硫,来历久,沉淀金属最拿手; 我是氯,色黄绿,金属电子我抢去; 我是氩,活性差,霓虹紫光我来发; 我是钾,把火加,超氧化物来当家; 我是钙,身体爱,骨头牙齿我都在; 我是钛,过渡来,航天飞机我来盖; 我是铬,正六铬,酒精过来变绿色; 我是锰,价态多,七氧化物爆炸猛; 我是铁,用途广,不锈钢喊我叫爷; 我是铜,色紫红,投入硝酸气棕红; 我是砷,颜色深,三价元素夺你魂; 我是溴,挥发臭,液态非金我来秀; 我是铷,碱金属,沾水烟花钾不如;。
酸碱盐溶解性表和口诀(精华版)
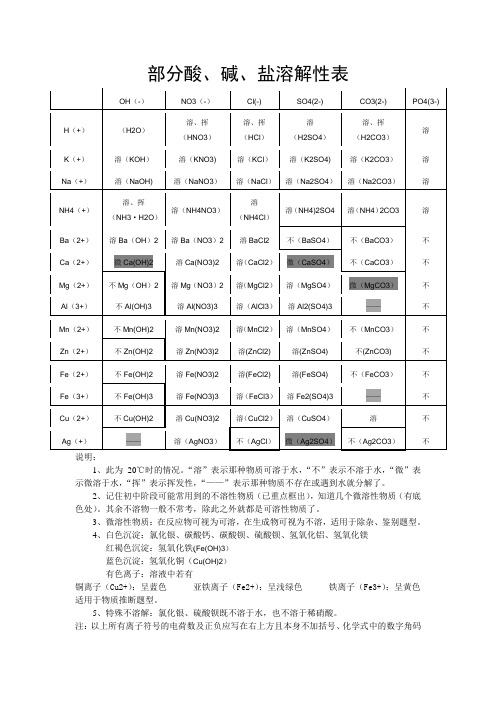
说明:
1、此为20℃时的情况。
“溶”表示那种物质可溶于水,“不”表示不溶于水,“微”表示微溶于水,“挥”表示挥发性,“——”表示那种物质不存在或遇到水就分解了。
2、记住初中阶段可能常用到的不溶性物质(已重点框出),知道几个微溶性物质(有底色处)。
其余不溶物一般不常考,除此之外就都是可溶性物质了。
3、微溶性物质:在反应物可视为可溶,在生成物可视为不溶,适用于除杂、鉴别题型。
4、白色沉淀:氯化银、碳酸钙、碳酸钡、硫酸钡、氢氧化铝、氢氧化镁
红褐色沉淀:氢氧化铁(Fe(OH)3)
蓝色沉淀:氢氧化铜(Cu(OH)2)
有色离子:溶液中若有
铜离子(Cu2+):呈蓝色亚铁离子(Fe2+):呈浅绿色铁离子(Fe3+):呈黄色适用于物质推断题型。
5、特殊不溶解:氯化银、硫酸钡既不溶于水,也不溶于稀硝酸。
注:以上所有离子符号的电荷数及正负应写在右上方且本身不加括号、化学式中的数字角码
应写在右下方,这里是为了方便打字,请谅解。
部分酸碱盐溶解性背诵口诀
①钾钠铵盐硝酸盐,
完全溶解不困难。
②硫酸盐中钡不溶,
盐酸盐中只银难,
硫酸钡和氯化银,
两种沉淀记心间。
③碳酸盐溶钾钠铵,
碳酸铝铁银碱无。
④硫酸钙银盐微溶,
微溶还有碳酸镁。
⑤碱有钾钠铵钡溶,
氢氧化钙是微溶,
其他全都不能溶。
⑥常见诸酸皆可溶,
记住挥酸盐硝碳。
注:口诀仅供参考,本身并不完全准确,但是能促进记忆。
酸碱盐的溶解性口诀大全

酸碱盐的溶解性口诀大全Document serial number【KK89K-LLS98YT-SS8CB-SSUT-SST108】酸碱盐的溶解性口诀大全溶解性用来判断复分解反应能否发生,如果生成物中有难溶性的物质而反应物中没有,那么反应就可以发生钾钠硝酸溶,铵盐也相同。
氯除银亚汞,硫酸除钡铅。
磷酸碳酸盐,钾钠氨才溶。
钾钠钡氨钙,溶碱有五种。
解释:就是钾盐、钠盐、硝酸盐、铵盐都是可溶的盐酸盐除了氯化银和氯化亚汞都是可溶的硫酸盐除硫酸钡和硫酸铅都可溶磷酸盐和碳酸盐除了含有钾、钠、铵根离子外都是不溶的氢氧化钾、氢氧化钠、氢氧化钡、氨水、氢氧化钙这五种碱溶于水钾钠铵盐皆可溶硝酸盐入水影无踪氯化物不溶氯化银硫酸盐不溶硫酸钡碳酸盐只溶钾钠铵可溶碱有四位钾钠和钙钡钾钠铵盐均可溶硝酸盐遇水无影踪盐酸盐不溶AgCl硫酸盐不溶BaSO4碳酸盐只溶钾钠铵带K+.NH4+.Na+离子菂盐都溶于水.带NO3+根离子菂盐都溶于水.带Cl-离子菂盐中只有AgCl不溶.带SO42-离子菂带CO32-离子菂盐中只有K2CO3.Na2CO3.(NH4)2CO3溶于水.例子BaCl2+Na2SO4===BaSO4↓+2NaCl(复分解反映条件为反应物都可溶.而生成物中一定要有气体或水.或沉淀)所以记溶解表最主要是明白什么和什么可以反映.什么和什么不能反映.而且除杂多数要把杂质以沉淀或者气体菂方式滤出或排出..背诵口诀1.钾钠铵盐都可溶,氯化物不溶氯化银硫酸盐钙银微溶钡不溶硝酸盐遇水影无踪碳酸盐除钾钠铵都不溶氢氧化钙是微溶钾钠钡钙碱可溶红褐铁,蓝絮铜其它沉淀白色呈注:1.初中用够了,红褐铁,代表铁盐沉淀为红褐色【fe(oh)2氢氧化亚铁除外】,蓝絮铜代表,铜盐为蓝色絮状沉淀。
2.氯化银【不溶酸】,碳酸钙,碳酸钡,硫酸钡【不溶酸】,氢氧化铝,氢氧化镁,为白色沉淀。
氢氧化铁(红褐色)氢氧化铜(蓝色)说明【】内为前一物质的特点2.钾钠铵盐全都溶碳酸除镁是微溶其他全都不能溶AgCl、BaSO4酸也不溶磷酸盐,更不溶3.钾钠铵硝溶氯化去银汞硫酸除钡铅碳酸多不溶溶碱有5种钾钠铵钡钙溶:氢氧铵钾钠钡钙,碳酸氢铵钾钠镁4.钾钠铵盐硝酸盐,全都溶于水中间;溶碱钾钠钡钙铵,碳酸只溶钾钠铵;硫酸盐中钡不溶,氯化物中银也难;常见诸酸皆可溶,记住挥酸盐硝碳。
酸碱盐的溶解性记忆口诀

酸碱盐的溶解性记忆口诀常见酸碱盐的溶解性表在我们中学化学教材每一册的附录中都有,它与元素周期表、金属活动顺序表一起称为中学化学中的三大工具表,本文是店铺整理酸碱盐的溶解性记忆口诀的资料,仅供参考。
酸碱盐的溶解性记忆口诀钾,钠,铵,盐,硝酸盐,都能溶解水中间.盐酸盐不容银,亚,汞,硫酸盐不容钡和铅,碳酸盐照顾溶钾钠铵溶解性口诀一钾钠铵盐溶水快,①硫酸盐除去钡铅钙。
②氯化物不溶氯化银,硝酸盐溶液都透明。
③口诀中未有皆下沉。
④注:①钾钠铵盐都溶于水;②硫酸盐中只有硫酸钡、硫酸铅、硫酸钙不溶;③硝酸盐都溶于水;④口诀中没有涉及的盐类都不溶于水;溶解性口诀二钾、钠、铵盐、硝酸盐;氯化物除银、亚汞;硫酸盐除钡和铅;碳酸、磷酸盐,只溶钾、钠、铵。
说明,以上四句歌谣概括了8类相加在水中溶解与不溶的情况。
溶解性口诀三钾钠铵硝皆可溶、盐酸盐不溶银亚汞;硫酸盐不溶钡和铅、碳磷酸盐多不溶。
多数酸溶碱少溶、只有钾钠铵钡溶溶解性口诀四钾、钠、硝酸溶, (钾盐、钠盐和硝酸盐都溶于水。
)盐酸除银(亚)汞, (盐酸盐里除氯化银和氯化亚汞外都溶。
)再说硫酸盐,不容有钡、铅,(硫酸盐中不溶的是硫酸钡和硫酸铅。
)其余几类盐, (碳酸盐、亚硫酸盐、磷酸盐、硅酸盐和硫化物)只溶钾、钠、铵, (只有相应的'钾盐、钠盐和铵盐可溶)最后说碱类,钾、钠、铵和钡。
(氢氧化钾、氢氧化钠、氢氧化钡和氨水可溶)另有几种微溶物,可单独记住。
溶解性口诀五钾钠铵盐硝酸盐完全溶解不困难氯化亚汞氯化银硫酸钡和硫酸铅生成沉淀记心间氢硫酸盐和碱类碳酸磷酸硝酸盐可溶只有钾钠铵酸碱盐溶解性酸盐,都能溶,钾.钠.铵盐也相同;碳酸盐只有钾.钠.铵,除此三种全不溶;硫酸盐多数溶,不溶只有钡.钙.银,最后剩下盐酸盐,沉淀只有氯化银;碱类多数都不溶,钾.钠.钡溶,钙微溶。
说的是所有的钾盐、钠盐、铵盐、硝酸盐都是可溶于水的,加入水中即可溶解;盐酸盐中除氯化银和氯化亚汞不溶于水,其它的都可以溶于水;硫酸盐中只有硫酸铅和硫酸钡不溶于水,其它硫酸盐都能溶于水,硫酸钙、硫酸银微溶于水。
溶解性口诀总汇(附溶解性表)

溶解性口诀一钾钠铵盐溶水快,①硫酸盐除去钡铅钙。
②氯化物不溶氯化银,硝酸盐溶液都透明。
③口诀中未有皆下沉。
④溶解性口诀二钾、钠、铵盐、硝酸盐;氯化物除银、亚汞;硫酸盐除钡和铅;碳酸、磷酸盐,只溶钾、钠、铵。
溶解性口诀三钾钠铵硝皆可溶、盐酸盐不溶银亚汞;硫酸盐不溶钡和铅、碳磷酸盐多不溶。
多数酸溶碱少溶、只有钾钠铵钡溶溶解性口诀四钾、钠、硝酸溶,(钾盐、钠盐和硝酸盐都溶于水。
)盐酸除银(亚)汞,(盐酸盐里除氯化银和氯化亚汞外都溶。
)再说硫酸盐,不容有钡、铅,(硫酸盐中不溶的是硫酸钡和硫酸铅。
)其余几类盐,(碳酸盐、亚硫酸盐、磷酸盐、硅酸盐和硫化物)只溶钾、钠、铵,(只有相应的钾盐、钠盐和铵盐可溶)最后说碱类,钾、钠、铵和钡。
(氢氧化钾、氢氧化钠、氢氧化钡和氨水可溶)还有几种微溶物,可单独记住。
溶解性口诀五钾钠铵盐硝酸盐完全溶解不困难氯化亚汞氯化银硫酸钡和硫酸铅生成沉淀记心间氢硫酸盐和碱类碳酸磷酸硝酸盐可溶只有钾钠铵记得有硝酸根的和有钠离子的全都溶于水碳酸根只有钡和钙不溶于水硫酸根只有钡不溶于水氯化物只有氯化银不溶于水氢氧根只有镁,铜,铁(包括亚铁)不溶于水初中化学知识顺口溜:高价无亚,低价有亚钾钠银氢正一价钙镁钡锌正二价氟氯溴碘负一价通常氧是负二价铜汞一二铝正三铁有正二和正三碳有正二和正四硫有负二正四六氢、硝、氯根负一价硫、碳酸根负二价磷酸根为负三价还有铵根正一价高锰根和锰酸根前负一来后负二常见金属的活动性顺序表:K Ca Na Mg Al Zn Fe Sn Pb (H)Cu Hg Ag Pt Au 碱盐溶解性顺口溜:碱除钾钠钡和钙,其余都不溶于水;硝酸盐都溶于水;氯化物除氯化银,其余都可溶于水;硫酸盐除硫酸钡,其余都可溶于水;碳磷盐除钾钠铵,其余都不溶于水。
溶液pH值的测定顺口溜:紫色石蕊试液酸红碱蓝,无色酚酞试液酸无碱红。
小口决:钾钠铵盐都可溶,氯化物不溶氯化银硫酸盐钙银微溶钡不溶硝酸盐遇水影无踪碳酸盐除钾钠铵都不溶氢氧化钙是微溶钾钠钡钙碱可溶红褐铁,蓝絮铜其它沉淀呈白色。
溶解性口诀总汇附溶解性表

溶解性口诀一钾钠铵盐溶水快,① 硫酸盐除去钡铅钙。
② 氯化物不溶氯化银,硝酸盐溶液都透明。
③ 口诀中未有皆下沉。
④ 溶解性口诀二钾、钠、铵盐、硝酸盐;氯化物除银、亚汞;硫酸盐除钡和铅;碳酸、磷酸盐,只溶钾、钠、铵。
溶解性口诀三钾钠铵硝皆可溶、盐酸盐不溶银亚汞;硫酸盐不溶钡和铅、碳磷酸盐多不溶。
多数酸溶碱少溶、只有钾钠铵钡溶溶解性口诀四钾、钠、硝酸溶,(钾盐、钠盐和硝酸盐都溶于水。
)盐酸除银(亚)汞,(盐酸盐里除氯化银和氯化亚汞外都溶。
)再说硫酸盐,不容有钡、铅,(硫酸盐中不溶的是硫酸钡和硫酸铅。
)其余几类盐,(碳酸盐、亚硫酸盐、磷酸盐、硅酸盐和硫化物)只溶钾、钠、铵,(只有相应的钾盐、钠盐和铵盐可溶)最后说碱类,钾、钠、铵和钡。
(氢氧化钾、氢氧化钠、氢氧化钡和氨水可溶)另有几种微溶物,可单独记住。
溶解性口诀五钾钠铵盐硝酸盐完全溶解不困难氯化亚汞氯化银硫酸钡和硫酸铅生成沉淀记心间氢硫酸盐和碱类碳酸磷酸硝酸盐可溶只有钾钠铵记得有硝酸根的和有钠离子的全都溶于水碳酸根只有钡和钙不溶于水硫酸根只有钡不溶于水氯化物只有氯化银不溶于水氢氧根只有镁,铜,铁(包括亚铁)不溶于水初中化学知识顺口溜:高价无亚,低价有亚钾钠银氢正一价钙镁钡锌正二价氟氯溴碘负一价通常氧是负二价铜汞一二铝正三铁有正二和正三碳有正二和正四硫有负二正四六氢、硝、氯根负一价硫、碳酸根负二价磷酸根为负三价还有铵根正一价高锰根和锰酸根前负一来后负二常见金属的活动性顺序表:K Ca Na Mg Al Zn Fe Sn Pb (H)Cu Hg Ag Pt Au碱盐溶解性顺口溜:碱除钾钠钡和钙,其余都不溶于水;硝酸盐都溶于水;氯化物除氯化银,其余都可溶于水;硫酸盐除硫酸钡,其余都可溶于水;碳磷盐除钾钠铵,其余都不溶于水。
溶液pH值的测定顺口溜:紫色石蕊试液酸红碱蓝,无色酚酞试液酸无碱红。
小口决:钾钠铵盐都可溶,氯化物不溶氯化银硫酸盐钙银微溶钡不溶硝酸盐遇水影无踪碳酸盐除钾钠铵都不溶氢氧化钙是微溶钾钠钡钙碱可溶红褐铁,蓝絮铜其它沉淀呈白色酸碱盐的溶解性表K ( +1) Na (+1) NH4( +1) Ba (+2) Ca (+2) Mg (+2)Al (+2/+3 ) Mn (+2) Zn (+2) Fe (+2) Fe (+3) Cu (+2)Ag (+1)。
溶解性口诀总汇(附溶解性表)

溶解性口诀一钾钠铵盐溶水快,①硫酸盐除去钡铅钙。
②氯化物不溶氯化银,硝酸盐溶液都透明。
③口诀中未有皆下沉。
④溶解性口诀二钾、钠、铵盐、硝酸盐;氯化物除银、亚汞;硫酸盐除钡和铅;碳酸、磷酸盐,只溶钾、钠、铵。
溶解性口诀三钾钠铵硝皆可溶、盐酸盐不溶银亚汞;硫酸盐不溶钡和铅、碳磷酸盐多不溶。
多数酸溶碱少溶、只有钾钠铵钡溶溶解性口诀四钾、钠、硝酸溶,(钾盐、钠盐和硝酸盐都溶于水。
)盐酸除银(亚)汞,(盐酸盐里除氯化银和氯化亚汞外都溶。
)再说硫酸盐,不容有钡、铅,(硫酸盐中不溶的是硫酸钡和硫酸铅。
)其余几类盐,(碳酸盐、亚硫酸盐、磷酸盐、硅酸盐和硫化物)只溶钾、钠、铵,(只有相应的钾盐、钠盐和铵盐可溶)最后说碱类,钾、钠、铵和钡。
(氢氧化钾、氢氧化钠、氢氧化钡和氨水可溶)另有几种微溶物,可单独记住。
溶解性口诀五钾钠铵盐硝酸盐完全溶解不困难氯化亚汞氯化银硫酸钡和硫酸铅生成沉淀记心间氢硫酸盐和碱类碳酸磷酸硝酸盐可溶只有钾钠铵记得有硝酸根的和有钠离子的全都溶于水碳酸根只有钡和钙不溶于水硫酸根只有钡不溶于水氯化物只有氯化银不溶于水氢氧根只有镁,铜,铁(包括亚铁)不溶于水初中化学知识顺口溜:高价无亚,低价有亚钾钠银氢正一价钙镁钡锌正二价氟氯溴碘负一价通常氧是负二价铜汞一二铝正三铁有正二和正三碳有正二和正四硫有负二正四六氢、硝、氯根负一价硫、碳酸根负二价磷酸根为负三价还有铵根正一价高锰根和锰酸根前负一来后负二常见金属的活动性顺序表:K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au 碱盐溶解性顺口溜:碱除钾钠钡和钙,其余都不溶于水;硝酸盐都溶于水;氯化物除氯化银,其余都可溶于水;硫酸盐除硫酸钡,其余都可溶于水;碳磷盐除钾钠铵,其余都不溶于水。
溶液pH值的测定顺口溜:紫色石蕊试液酸红碱蓝,无色酚酞试液酸无碱红。
小口决:钾钠铵盐都可溶,氯化物不溶氯化银(学习的目的是增长知识,提高能力,相信一分耕耘一分收获,努力就一定可以获得应有的回报)。
部分酸碱盐溶解性表记忆口诀
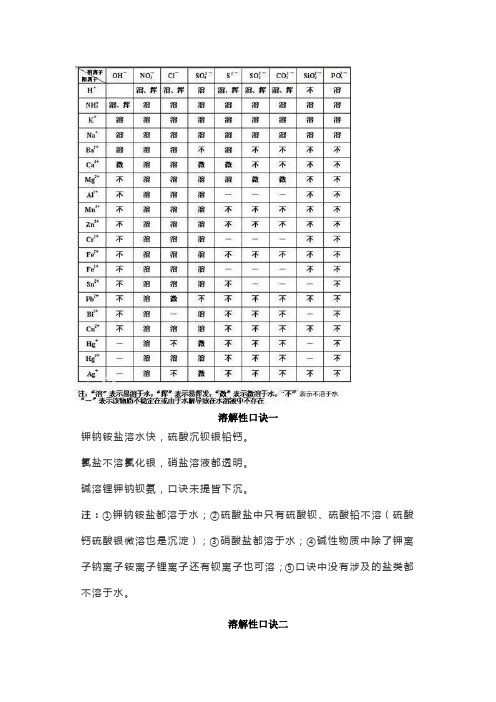
溶解性口诀一钾钠铵盐溶水快,硫酸沉钡银铅钙。
氯盐不溶氯化银,硝盐溶液都透明。
碱溶锂钾钠钡氨,口诀未提皆下沉。
注:①钾钠铵盐都溶于水;②硫酸盐中只有硫酸钡、硫酸铅不溶(硫酸钙硫酸银微溶也是沉淀);③硝酸盐都溶于水;④碱性物质中除了钾离子钠离子铵离子锂离子还有钡离子也可溶;⑤口诀中没有涉及的盐类都不溶于水。
溶解性口诀二钾、钠、铵盐、硝酸盐;氯化物除银、亚汞;硫酸盐除钡和铅;碳酸、磷酸盐,只溶钾、钠、铵。
说明:以上四句歌谣概括了8类相加在水中溶解与不溶的情况。
溶解性口诀三钾钠铵硝皆可溶,氯盐不溶银亚汞;硫酸盐不溶钡和铅,碳磷酸盐多不溶。
多数酸溶碱少溶,只有钾钠铵钡溶。
溶解性口诀四钾、钠、硝酸溶,(钾盐、钠盐和硝酸盐都溶于水。
)盐酸除银(亚)汞,(盐酸盐里除氯化银和氯化亚汞外都溶。
)再说硫酸盐,不溶有钡、铅,(硫酸盐中不溶的是硫酸钡和硫酸铅。
)其余几类盐,(碳酸盐、亚硫酸盐、磷酸盐、硅酸盐和硫化物)只溶钾、钠、铵,(只有相应的钾盐、钠盐和铵盐可溶)。
最后说碱类,钾、钠、铵和钡。
(氢氧化钾、氢氧化钠、氢氧化钡和氨水可溶)另有几种微溶物,可单独记住。
溶解性口诀五(适合初中化学课本后面的附录)钾钠铵盐硝酸盐①;氢氧根多钡离子②;硫酸盐除钡钙银③;碳酸溶氢钾钠铵④;生成沉淀氯化银⑤。
溶解性口诀六(初学记忆)钾、钠、铵、硝都可溶,氯化物里银不溶;硫酸盐里钡不溶,磷酸碳酸多不溶。
解释:①钾盐、钠盐、铵盐、硝酸盐都溶于水。
②除了以上四种,氢氧根和钡离子结合时也溶于水。
③硫酸根除了和钡离子、钙离子、银离子结合时不溶于水,其他都溶。
④碳酸根除了和氢离子、钾离子、钠离子和铵离子结合时溶于水,其他都不溶。
⑤氯离子只有和银离子结合时不溶于水⑥磷酸盐除钾钠铵都不溶。
溶解性口诀七铵钾钠钡氢氧溶①;碳酸只溶铵钾钠②;所有硝酸都能溶③;盐酸只有银不溶④;硫酸只有钡不溶⑤。
解释:①氢氧化铵,氢氧化钾,氢氧化钠,氢氧化钡都溶于水,其余带氢氧根的都不溶于水。
酸碱盐溶解性表

酸碱盐的溶解性表OH(-1 ) NO3(-Cl(-1)SO4(-CO3(-PO4(-1)2)2)3)H(+1)溶、挥溶、挥溶溶、挥溶K(+1)溶溶溶溶溶溶Na(+1)溶溶溶溶溶溶NH4(+ 溶、挥溶溶溶溶溶1)Ba(+2)溶溶溶不不不Ca(+2)微溶溶微不不Mg(+2)不溶溶溶微不Al(+3)不溶溶溶---不Zn(+2)不溶溶溶不不Fe(+2)不溶溶溶不不Fe(+3)不溶溶溶不不Cu(+2)不溶溶溶---不Ag(+1) ---溶不微不不说明:此为 20℃时的状况。
“溶”表示那种物质可溶于水,“不”表示不溶于水,“微”表示微溶于水,“挥”表示挥发性,“ --- ”表示那种物质不存在或碰到水就分解了背诵口诀1.钾钠铵盐都可溶,氯化物不溶氯化银硫酸盐钙银微溶钡不溶硝酸盐遇水影无踪碳酸盐除钾钠铵都不溶钾钠钡钙碱可溶红褐铁,蓝絮铜其余积淀白色呈注: 1. 初顶用够了,红褐铁,代表铁盐积淀为红褐色【f e(oh)2 氢氧化亚铁除外】,蓝絮铜代表,铜盐为蓝色絮状沉淀。
2. 氯化银【不溶酸】,碳酸钙,碳酸钡,硫酸钡【不溶酸】,氢氧化铝,氢氧化镁,为白色积淀。
氢氧化铁(红褐色)氢氧化铜(蓝色)说明【】内为前一物质的特色2.钾钠铵盐全都溶碳酸除镁是微溶其余全都不可以溶AgCl、 BaSO4酸也不溶磷酸盐,更不溶一、氧气的性质:(1)单质与氧气的反响:(化合反响)1.镁在空气中焚烧: 2Mg + O2 点燃 2MgO2.铁在氧气中焚烧: 3Fe + 2O2 点燃 Fe3O43.铜在空气中受热: 2Cu + O2 加热 2CuO4.铝在空气中焚烧: 4Al + 3O2 点燃 2Al2O35.氢气中空气中焚烧: 2H2 + O2 点燃 2H2O6.红磷在空气中焚烧(研究空气构成的实验): 4P + 5O2 点燃2P2O57.硫粉在空气中焚烧: S + O2 点燃 SO28.碳在氧气中充足焚烧: C + O2 点燃 CO29.碳在氧气中不充足焚烧: 2C + O2 点燃 2CO(2)化合物与氧气的反响:10.一氧化碳在氧气中焚烧: 2CO + O2 点燃 2CO211.甲烷在空气中焚烧: CH4 + 2O2 点燃 CO2 + 2H2O12.酒精在空气中焚烧: C2H5OH + 3O2点燃 2CO2 + 3H2O (3)氧气的根源:13.玻义耳研究空气的成分实验2HgO 加热 Hg+ O2 ↑14.加热高锰酸钾: 2KMnO4加热 K2MnO4 + MnO2 + O2↑(实验室制氧气原理 1)15.过氧化氢在二氧化锰作催化剂条件下分解反响:H2O2 MnO22H2O+ O2↑(实验室制氧气原理2)二、自然界中的水:16.水在直流电的作用下分解(研究水的构成实验):2H2O 通电2H2↑+ O2 ↑17.生石灰溶于水: CaO + H2O == Ca(OH)218.二氧化碳可溶于水:H2O + CO2==H2CO3三、质量守恒定律:19.镁在空气中焚烧: 2Mg + O2 点燃 2MgO20.铁和硫酸铜溶液反响: Fe + CuSO4 === FeSO4 + Cu 21.氢气复原氧化铜: H2 + CuO 加热 Cu + H2O22. 镁复原氧化铜: Mg + CuO 加热 Cu + MgO四、碳和碳的氧化物:(1)碳的化学性质23.碳在氧气中充足焚烧: C + O2 点燃 CO224.木炭复原氧化铜: C+ 2CuO高温 2Cu + CO2↑25.焦炭复原氧化铁: 3C+ 2Fe2O3 高温 4Fe + 3CO2↑(2)煤炉中发生的三个反响:(几个化合反响)26.煤炉的基层: C + O2 点燃 CO227.煤炉的中层: CO2 + C 高温 2CO28.煤炉的上部蓝色火焰的产生:2CO + O2 点燃 2CO2(3)二氧化碳的制法与性质:29.大理石与稀盐酸反响(实验室制二氧化碳):CaCO3 + 2HCl == CaCl2 + H2O + CO2↑30.碳酸不稳固而分解: H2CO3 == H2O + CO2↑31.二氧化碳可溶于水:H2O + CO2== H2CO332.高温煅烧石灰石(工业制二氧化碳):CaCO3高温 CaO + CO2↑33.石灰水与二氧化碳反响(鉴识二氧化碳):Ca(OH)2 + CO2 === CaCO3↓+ H2O(4)一氧化碳的性质:34.一氧化碳复原氧化铜: CO+ CuO加热 Cu + CO235.一氧化碳的可燃性: 2CO + O2 点燃 2CO2其余反响:36.碳酸钠与稀盐酸反响(灭火器的原理):Na2CO3 + 2HCl == 2NaCl + H2O + CO2↑五、燃料及其利用:37.甲烷在空气中焚烧: CH4 + 2O2 点燃 CO2 + 2H2O38.酒精在空气中焚烧: C2H5OH + 3O2点燃 2CO2 + 3H2O 39.氢气中空气中焚烧: 2H2 + O2 点燃 2H2O六、金属(1)金属与氧气反响:40.镁在空气中焚烧: 2Mg + O2 点燃 2MgO41.铁在氧气中焚烧: 3Fe + 2O2 点燃 Fe3O442.铜在空气中受热: 2Cu + O2 加热 2CuO43.铝在空气中形成氧化膜: 4Al + 3O2 = 2Al2O3(2)金属单质 + 酸 --------盐+氢气(置换反响)44.锌和稀硫酸 Zn + H2SO4 = ZnSO4 + H2↑45.铁和稀硫酸 Fe + H2SO4 = FeSO4 + H2↑46.镁和稀硫酸 Mg + H2SO4 = MgSO4 + H2↑47.铝和稀硫酸 2Al +3H2SO4 = Al2(SO4)3 +3 H2 ↑48.锌和稀盐酸 Zn + 2HCl == ZnCl2 + H2 ↑49.铁和稀盐酸 Fe + 2HCl == FeCl2 + H2 ↑50.镁和稀盐酸 Mg+ 2HCl == MgCl2 + H2 ↑51.铝和稀盐酸 2Al + 6HCl == 2AlCl3 + 3 H2↑(3)金属单质 + 盐(溶液) -------新金属+新盐52.铁和硫酸铜溶液反响: Fe + CuSO4 == FeSO4 + Cu53.锌和硫酸铜溶液反响: Zn + CuSO4 ==ZnSO4 + Cu54.铜和硝酸汞溶液反响: Cu + Hg(NO3)2 == Cu(NO3)2 + Hg (3)金属铁的治炼原理:55.3CO+ 2Fe2O3高温 4Fe + 3CO2↑七、酸、碱、盐1、酸的化学性质(1)酸 + 金属 --------盐+氢气(见上)(2)酸 + 金属氧化物 --------盐+水56.氧化铁和稀盐酸反响: Fe2O3 + 6HCl ==2FeCl3 + 3H2O57.氧化铁和稀硫酸反响: Fe2O3+ 3H2SO4== Fe2(SO4)3 + 3H2O58.氧化铜和稀盐酸反响: CuO + 2HCl ==CuCl2 + H2O59.氧化铜和稀硫酸反响: CuO + H2SO4 == CuSO4 + H2O (3)酸 + 碱 --------盐+水(中和反响)60.盐酸和烧碱起反响: HCl + NaOH == NaCl +H2O61.盐酸和氢氧化钙反响: 2HCl + Ca(OH)2 == CaCl2 + 2H2O62.氢氧化铝药物治疗胃酸过多: 3HCl + Al(OH)3 == AlCl3 +3H2O63. 硫酸和烧碱反响: H2SO4 + 2NaOH == Na2SO4 + 2H2O(4)酸 + 盐 --------另一种酸+另一种盐64.大理石与稀盐酸反响: CaCO3 + 2HCl == CaCl2 + H2O + CO2↑65.碳酸钠与稀盐酸反响 : Na2CO3+ 2HCl == 2NaCl + H2O+ CO2↑66.碳酸氢钠与稀盐酸反响: NaHCO3+ HCl== NaCl + H2O+ CO2↑67.硫酸和氯化钡溶液反响: H2SO4+ BaCl2 == BaSO4↓+2HCl 2、碱的化学性质(1)碱 + 非金属氧化物 --------盐+水68.苛性钠裸露在空气中变质: 2NaOH + CO2 == Na2CO3 + H2O69.苛性钠汲取二氧化硫气体: 2NaOH + SO2 == Na2SO3 + H2O 70.苛性钠汲取三氧化硫气体: 2NaOH + SO3 == Na2SO4 + H2O 71.消石灰放在空气中变质: Ca(OH)2 + CO2 == CaCO3↓+ H2O 72. 消石灰汲取二氧化硫: Ca(OH)2 + SO2 == CaSO3 ↓+ H2O (2)碱+酸--------盐+水(中和反响,方程式见上)(3)碱 + 盐 --------另一种碱 + 另一种盐73.氢氧化钙与碳酸钠: Ca(OH)2 + Na2CO3 == CaCO3↓+2NaOH 3、盐的化学性质(1)盐(溶液) + 金属单质 -------另一种金属+另一种盐74. 铁和硫酸铜溶液反响: Fe + CuSO4 == FeSO4 + Cu(2)盐 + 酸--------另一种酸+另一种盐75.碳酸钠与稀盐酸反响 : Na2CO3+ 2HCl == 2NaCl + H2O+ CO2↑碳酸氢钠与稀盐酸反响: NaHCO3 + HCl== NaCl + H2O + CO2↑(3)盐 + 碱 --------另一种碱+另一种盐76. 氢氧化钙与碳酸钠: Ca(OH)2 + Na2CO3 == CaCO3↓+ 2NaOH (4)盐 + 盐 -----两种新盐77.氯化钠溶液和硝酸银溶液: NaCl + AgNO3== AgCl↓ + NaNO3 78.硫酸钠和氯化钡: Na2SO4 + BaCl2 == BaSO4↓ + 2NaCl钾钠硝铵均可溶,盐酸盐不溶AgCl,硫酸盐不溶 BaSO4,碳酸盐能溶钾钠铵,钾钠钙钡可溶碱。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
盐的分类 :
盐酸盐硝酸盐碳酸盐硫酸盐钠盐NaCl NaNO3 Na2CO3 Na2SO4 钾盐kCl KNO3 K2CO3 K2SO4 +
镁盐钙MgCl2 Mg(NO3) 2 MgCO3 MgSO4 亚铁盐FeCl2 Fe(NO3) 2 FeCO3 FeSO4 铁盐FeCl3 Fe(NO3) 3 Fe2(CO3) 3 Fe 2(SO4) 3 钙盐CaCl2 Ca(NO) CaCO CaSO
3 3 4
部分酸碱盐溶解性表(
20℃ )
阳离子
阴离子
H
+
NH 4
K +
Na +
Ba 2+
Ca 2+
2+
Mg
Al 3+
2+ Mn
Zn 2+
Fe 2+
Fe 3+
Cu 2+
Ag +
-
3-
Cl -
4 2-
32-
OH NO SO CO
溶、挥
溶、挥 溶 溶、挥 溶、挥 溶 溶 溶 溶 溶 溶 溶 溶 溶 溶 溶 溶 溶 溶 溶 溶 溶 不 不 微 溶 溶 微 不 不 溶 溶 溶 微 不 溶 溶 溶 - 不 溶 溶 溶 不 不 溶 溶 溶 不 不 溶 溶 溶 不 不 溶 溶 溶 - 不 溶 溶 溶 不 -
溶
不
微
不
℃
记忆口诀 : 钾钠铵硝酸盐全溶 ,
盐酸盐只有 AgCl 不容,硫酸盐只有 BaSO 不容,
4
+
+
+ +
+
+2+
碳酸盐只溶 K 、Na
、NH , 碱类只溶 K
、Na
、NH
和 Ba
Ca(OH)
4
4
2、
CaSO Ag SO 微溶.
4、
2
4
阴离子
阳离子
酸类H+ 铵盐NH4+ 钾盐K+ 钠盐Na+ 钡盐Ba2+ 钙盐Ca2+
2+ 镁盐Mg 铝盐Al 3+
2+ 锰盐Mn 锌盐Zn2+
亚铁Fe2+ 盐
铁盐Fe3+ 铜盐Cu2+ 银盐Ag+ 物质的命名
酸碱盐溶解性表的分类解释
碱类硝酸盐盐酸盐硫酸盐碳酸盐
- -
Cl
- 2- 2- OH NO3 SO4 CO3
2
HNO HCl H2 SO H CO
H O 3 4 2 3
溶、挥溶、挥溶溶、挥NH3.H 2 O NH4NO3 NH4Cl (NH4) 2SO4 (NH4) 2CO3 溶、挥溶溶溶溶KOH KNO3 KCl K2 SO4 K2CO3 溶溶溶溶溶NaOH NaNO3 NaCl Na2SO4 Na2CO3 溶溶溶溶溶
Ba(OH)2 Ba(NO3 ) 2 BaCl 2 BaSO4 BaCO3 溶溶溶☆不☆不Ca(OH)2 Ca(NO3 ) 2 CaCl2 CaSO4 CaCO3 微溶溶微☆不Mg(OH)2 Mg(NO3) 2 MgCl2 MgSO4 MgCO3 ☆不溶溶溶微
Al(OH)
3
Al(NO
3
)
3
AlCl
3
Al (SO )
3
——
2 4
不溶溶溶——Mn(OH)2 Mn(NO3) 2 MnCl2 MnSO4 MnCO3 不溶溶溶不
Zn(OH)
2
Zn(NO )
2
ZnCl
2
ZnSO ZnCO
3 4 3
不溶溶溶不
Fe(OH)2 Fe(NO3 ) 2 FeCl 2 FeSO4 FeCO3 不溶溶溶不
Fe(OH)
3
Fe(NO )
3
FeCl
3
Fe (SO )
3
——
3 2 4
☆不溶溶溶——Cu(OH)2 Cu(NO3 ) 2 CuCl2 CuSO4 CuCO3 ☆不溶溶溶不——AgNO AgCl Ag SO Ag CO
3 2
4 2 3 ——溶☆不微不
氢氧化某硝酸某氯化某硫酸某碳酸某。
