性激素结合球蛋白检测作业指导书医学检验
检验医学SOP文件5--生化室作业指导书

生化室作业指导书文件编号:ABCD-3-SF-01~61第A版编制:审核:批准:生效日期:2015年4月8日ABCD人民医院检验科目录修订页血清总胆红素(T-BIL)测定1. 实验原理血清中的胆红素分为直接(结合)胆红素和间接(未结合)胆红素。
大多数方法是在1883年Ehrlich提出的重氮法胆红素测量法1,一些改良的方法已被用来增进反应。
这些改良的方法是使直接胆红素直接和重氮化合物进行反应,生成一种有颜色的化合物,而间接胆红素需要一种溶剂,如表面活性剂后才能进行反应。
申能总胆红素试剂是改良的重氮法。
使用一种稳定的重氮盐,2,4-二氯苯胺重氮盐(DCA),与胆红素反应,形成红色偶氮化合物,它在540nm吸光度最大。
在540/600nm时的吸光度与标本中总胆红素的浓度成正比。
胆红素+DCA 红色偶氮化合物表面活性剂2. 标本:2.1 病人准备:无特殊要求。
最好用禁食的标本以减少乳糜血的干扰。
2.2 类型:血清、肝素或EDTA血浆,应避光保存。
3. 标本存放:15~25℃保存可稳定2天;2~8℃保存可稳定7天;-20℃保存可稳定3个月,如冰冻保存,不可反复冻融!。
4. 标本运输:常温条件下避光保存运输。
5. 标本拒收标准:标本溶血、细菌污染、脂血、非避光保存运输的标本。
6. 实验材料6.1 试剂:申能总胆红素试剂盒(141 0817170 1 试剂1+试剂2)6.1.1 试剂组成试剂1:6×64 ml磷酸缓冲液40mmol/L氯化钠9g/L表面活性剂,稳定剂适量试剂2:6×16 ml2,4-二氯苯胺重氮盐1mmol/L盐酸30mmol/L表面活性剂适量6.1.2 试剂准备:试剂为即用式。
6.1.3 试剂稳定性与贮存试剂避光保存于2~8℃,若无污染,可稳定至失效期。
试剂有效期为18个月。
试剂2必需避光保存。
试剂不可冰冻。
6.1.4 变质指示:当试剂有浊度时,表明有细菌污染,不能继续使用。
医学检验·检查项目:性激素结合蛋白_课件模板

内容课件模板
医学检验·各论:性激素结合蛋白 >>>
简介:
SHBG能和睾酮及雌激素结合,睾酮 40%与SHBG结合,58%与白蛋白结合;而雌 激素75%与SHBG,20%和白蛋白结合,形成 的复合物主要在肝脏降解。
医学检验·各论:性激素结合蛋白 >>>
临床意义:
甲状腺功能亢进、使用过量的雌激素 与甲状腺激素、神经性厌食、肝硬变等患 者血清水平升高;而甲状腺功能低下、使 用睾酮过量、多毛症、肥胖、多囊水肿性 卵巢综合征等可降低。
医学检验·各论:性激素结合蛋白 >>>
正常值:
0 以上均为与睾酮结合的nmol/L (2)SHBG-BC硫酸铵沉淀法: 法定单位 (nmol/L) 血清 成人 男 41.5±10.2 女 65.0±24.1 (3)免疫分析法: 法定单位 (nmol/L) 血清成人 男 10~80 非孕妇 女 20~130 妊娠 10~15周 5
医学检验·各论:性激素结合蛋白 >>>
相关症状: 内分泌功能减退、乳房和生殖器萎缩、胡 子稀疏、汗毛过多、衰老加快、心理性性 功能障碍。
医学检验·各论:性激素结合蛋白 >>>
相关疾病:
性心理障碍、真两性畸形、特发性低促性 腺激素性性腺功能减退症、性早熟、小儿 46-XY单纯性腺发育不全综合征、小儿女 性性早熟、黄体囊肿、高催乳素血症、围 绝经期功能失调性子宫出血、围绝经期综 合征。
医学检验·各论:性激素结合蛋白 &g 20~25周 170~260 35~40周 321~456 羊水 12±4.0 nmol/L计算;按 每两聚体多肽链分子结合1分子类固醇计 (MW为59000)。
北京联众泰克性激素结合球蛋白(SHBG)测定试剂盒(电化学发光免疫分析法)产品技术要求
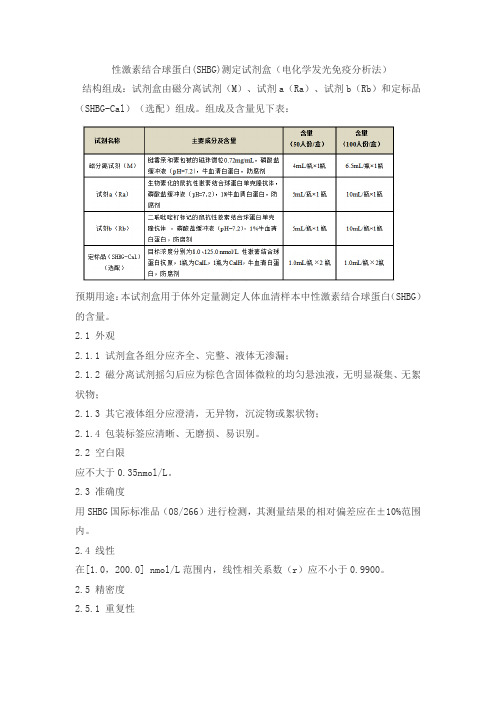
性激素结合球蛋白(SHBG)测定试剂盒(电化学发光免疫分析法)结构组成:试剂盒由磁分离试剂(M)、试剂a(Ra)、试剂b(Rb)和定标品(SHBG-Cal)(选配)组成。
组成及含量见下表:预期用途:本试剂盒用于体外定量测定人体血清样本中性激素结合球蛋白(SHBG)的含量。
2.1 外观2.1.1 试剂盒各组分应齐全、完整、液体无渗漏;2.1.2 磁分离试剂摇匀后应为棕色含固体微粒的均匀悬浊液,无明显凝集、无絮状物;2.1.3 其它液体组分应澄清,无异物,沉淀物或絮状物;2.1.4 包装标签应清晰、无磨损、易识别。
2.2 空白限应不大于0.35nmol/L。
2.3 准确度用SHBG国际标准品(08/266)进行检测,其测量结果的相对偏差应在±10%范围内。
2.4 线性在[1.0,200.0] nmol/L范围内,线性相关系数(r)应不小于0.9900。
2.5 精密度2.5.1 重复性在试剂盒的线性范围内,检测高、低两个水平的样品,检测结果的变异系数(CV)应不大于8%。
2.5.2 批间差在试剂盒的线性范围内,用3个批号试剂盒分别检测高、低两个水平的样品,检测结果的变异系数(CV)应不大于15%。
2.6 效期末稳定性本产品效期为15个月,试剂盒在2~8℃下保存至有效期末进行检测,检测结果应符合2.1、2.2、2.3、2.4、2.5.1的要求。
2.7 溯源性依据GB/T 21415-2008《体外诊断医疗器械生物样品中量的测量校准品和控制物质赋值的计量学溯源性》的要求提供性激素结合球蛋白(SHBG)定标品的来源、赋值过程以及测量不确定度等内容,定标品溯源至国际标准品(08/266)。
【指导】生长激素GH检测作业指导书医学检验

【关键字】指导《文件已阅声明表》《Procedure circulation form》文件修改记录页(Procedure amendment form)表号: KM-MP03•02•03文件信息表(Procedure information form)生长激素(GH)检测作业指导书(Standard operation procedure for analysis of Growth Hormone)1. 原理(Test principle):固相、双位点夹心法化学发光免疫量度检测。
固相(包被珠)包被有鼠单克隆hGH抗体,试剂含有碱性磷酸酶标记的兔抗hGH多克隆抗体。
试剂与样本中的hGH同时与包被有鼠单克隆hGH抗体的包被珠温育,形成抗体夹心复合物。
未结合的酶标记物经离心去除,最终加入化学发光底物,产生与结合酶成比例的光信号。
2. 样本收集和储存(Specimen Collection and Storage):标本收集(Specimen collection):类型(Ttype):血清(Serum);用量(V olume) 抽取0.4mL不抗凝血分离的血清,仪器加样量(Sampling volume) 50μl(样本杯中样本量要超过样本用量至少100μL)。
采集样本前,病人应空腹并休息30分钟。
拒收标本(Specimen rejection):推荐使用超速离心清除脂血(lipoprotein)样本。
溶血(hemolysis)样本提示样本在送达实验室之前处理不当,因此检测结果将受到影响,应予以注意。
血清(serum)样本在未充分凝集前离心将导致纤维蛋白的存在。
为躲免纤维蛋白对结果的影响必须确保离心处理前样本已经完全充分凝集。
对于正在接受抗凝剂治疗的病人样本,需要延长凝集时间。
源于不同生产商的血样收集试管,由于原材料和添加剂不同,包括凝胶或物理涂层、促凝剂和/或抗凝剂,可能导致得到不同的结果。
本试剂盒没有对所有可能应用的收集管类型进行测试。
医院检验微生物作业指导书

1.目的规范微生物实验室内部质量控制,确保临床报告的质量。
2.适用范围微生物实验室的所有检验项目。
3.职责实验室检验人员均需熟知并遵守本程序。
4.程序4.1分析前质量控制4.1.1检验申请单:临床医生应按照《微生物检验项目申请程序》申请临床微生物检测口头申请追加样本检验项目,必须在样本有效期内申请.并补正式的检验申请单。
4.1.2生成微生物检验标本标签:护士应在核对医嘱患者信息和检验申请信息后,按照《微生物检验标本条形码程序》生成申请单和微生物检验项目标签,并将微生物检验项目标签正确张贴于标本容器上。
4.1.3样本采集手册:实验室应制订样本采集手册,指导正确采集和处理样本。
4.1.4样本采集和运输:样本采集人员应按照《采样前患者识别程序》确认患者,按照《标本采集、运送、保存程序》采集样本,并在规定的时间和温度范围内,使用指定的运输培养基,安全运送到微生物室。
4.1.5样本的接收:样本接收人员应严格按照《标本接收、标识及信息录人程序》《标本拒收程序》对样本接收或拒收,并记录。
4.1.6微生物检验标本信息输人:微生物实验室接种岗位检验人员严格按照相关的微生物标本检验信息输,人程序录人,核对患者信息和标本信息等资料。
4.1.7样本储存:微生物实验室接种岗位检验人员按照相关的微生物标本检验前储存程序正确铺存未能及时处理的标本,已经检验的样本应在保证其性质稳定的条件下,将样本以适当的方式保留到规定时间内,以便能在出具结果报告后可以复查,成做补无检食。
4.2分析中质量控制4.2.1试剂的质量控制4.2.1.1所有试剂用于检测标本前,必须做质控以验证试剂性能并记录质控结果,只有质控合格才可使用(表2-1-1)。
质控应遵循以下原则。
4.2.1.1.1使用中的染色剂(革兰染色、特殊染色和荧光染色),至少每周(若检测频率小于每周1次,则实验当日)用已知阳性和阴性(适用时)的质控菌株检测。
4.2.1.2平行试验:新批号试剂使用前须用老试利或参考材料平行试验。
性激素结合球蛋白测定的方法学评价及相关性研究

【 要】 目的 摘
60 8) 1 0 1
对 性 激 素 结 合 球 蛋 白( HB 商 品 试 剂 盒 进 行 方 法 学 评 价 , S G) 以确 定 其 分 析 性 能 是 否 符 合 临床
实验 室应 用 的要 求 ; 立 S G 的 实验 室 参 考 范 围 , 分 析 其 与 睾 酮 、 二 醇 的相 关 性 。 方 法 依 据 美 国临 床 实验 建 HB 并 雌
s r m n t r cso l e r y e au t n a d t e l w i t d d t c i n a c r i g t h IEP 一 , 6 P f e . e u a d i p e iin,i a i v l a i n h o l s n t o mi e e t c o d n o t e CI 5 A EP 一 i s e o S l
T o s tup t e heSH BG e e e e r ng n lb. nay e t e c r lton o e t s e on s r dilt r f r nc a e i a To a lz h or ea i ft s o t r eorc ta o o SH BG . s ls Re u t
・
4 4・
坌堕墨堂皇 堕
!
笙! 塑 ! 查箜 :
! ! 』 ! 二 :. : : 三 .: . !
甲状腺球蛋白(Tg)作业指导书

检验科免疫室分析项目作业指导书第页,共页版本:A/0生效日期:2008-02-01 111.分析原理采用双抗体夹心法原理,整个过程18分钟完成。
·第1步:20μl标本、生物素化的抗甲状腺球蛋白单克隆抗体和钌(Ru)标记的抗甲状腺球蛋白单克隆抗体混匀,形成夹心复合物。
·第2步:加入链霉亲和素包被的微粒,让上述形成的复合物通过生物素与链霉亲和素间的反应结合到微粒上。
·第3步:反应混和液吸到测量池中,微粒通过磁铁吸附到电极上,未结合的物质被清洗液洗去,电极加电压后产生化学发光,通过光电倍增管进行测定。
检测结果由机器自动从标准曲线上查出。
此曲线由仪器通过2点定标校正,由从试剂条形码扫入仪器的原版标准曲线而得。
2.标本要求血清:按标准常规方法采集。
血浆:肝素、EDTA-K3、枸橼酸钠和氟化钠/草酸-K抗凝均可。
标本在15-25度可稳定24小时,2-8度可稳定3天,-20℃可稳定1个月。
标本只可冻融1次。
有沉淀的标本使用前需离心。
加热灭活的标本不可使用。
标本和质控品禁用叠氮钠防腐。
甲状腺球蛋白核实试验(抗甲状腺球蛋白中和试验)甲状腺球蛋白测定可受到患者血清中抗甲状腺球蛋白抗体(抗-Tg)和非特异性因素的干扰。
因此结果必须按以下步骤核查:在标本杯中加入200ul标本和50ul R3试剂,混匀,与不加入的标本作平行测定。
3.试剂、校准品、质控品和其他所需材料采用罗氏原装配套试剂。
试剂:M:链霉亲和素包被的微粒(透明瓶盖),1瓶,6.5ml。
粒子浓度0.72mg/ml,生物素结合能力: 470ng生物素/mg粒子。
含防腐剂。
R1:生物素化的抗甲状腺球蛋白单克隆抗体(灰盖),1瓶,10ml。
浓度0.7mg/l,磷酸缓冲液0.04mol/l,pH6.1含防腐剂。
R2:Ru(bpy)32+标记的抗甲状腺球蛋白单克隆抗体(黑盖),1瓶,10ml。
浓度1.0mg/l,磷酸缓冲液0.04mol/l,pH 6.1含防腐剂。
2024年检验类之临床医学检验技术(中级)通关考试题库带答案解析

2024年检验类之临床医学检验技术(中级)通关考试题库带答案解析单选题(共45题)1、临床上检测CK-MB多用于诊断A.肝脏疾病B.心脏疾病C.肾脏疾病D.大脑疾病E.胆囊疾病【答案】 B2、在某天的室内质量控制,其中有一水平质控品发生失控A.立即进行校准B.立即更换试剂C.立即更换质控品D.立即重新检测E.立即重新定标【答案】 C3、双缩脲测定血浆总蛋白,叙述正确的是A.反应复合物的吸收峰在540nm处B.反应复合物的吸收峰在650~750nm处C.反应物吸收峰在280nm,215~225nm处D.该方法是一种染料结合法E.该方法是一种散射比浊法【答案】 A4、为减少化疗和放疗对肿瘤患者的全身性伤害,药物靶向治疗已成为关注焦点。
制备肿瘤特异性的单克隆抗体,连接相应的毒性分子后可实现肿瘤的靶向治疗。
A.组合抗体库技术B.B细胞杂交瘤技术C.嗜菌体抗体技术D.T细胞杂交瘤技术E.基因工程抗体技术【答案】 D5、酶偶联法测定代谢物浓度时,指示酶反应呈()。
A.零级反应B.一级反应C.二级反应D.零级反应和一级反应的混合反应E.一级反应和二级反应的混合反应【答案】 B6、抗可溶性抗原的抗血清要长期保存,理想的方法是A.液体4℃B.低温C.加叠氮钠D.冷冻干燥E.室温即可【答案】 D7、用A型、B型、O型标准红细胞鉴定血型,结果分别为(-)、(+)、(-),则被鉴定的血型是()。
A.A型B.B型C.O型D.AB型E.A1亚型【答案】 A8、在2000年WHO血液肿瘤分型,将急性白血病诊断中骨髓原始细胞的数量规定为大于A.10%B.15%C.20%D.25%E.30%【答案】 C9、Ⅳ型超敏反应会出现()。
A.中性粒细胞浸润B.单核-巨噬细胞浸润C.B淋巴细胞浸润D.嗜酸性粒细胞浸润E.Th2型淋巴细胞浸润【答案】 B10、关于K-B纸片扩散法操作的描述,下列说法错误的是A.各纸片中心距离不小于24mmB.纸片距平板内缘不应大于15mmC.直径90mm的平皿可贴6张纸片D.纸片贴牢后避免移动E.35℃培养16~18小时后阅读结果【答案】 B11、患者男性,15岁。
人性激素结合球蛋白(SHBG)酶联免疫吸附测定试剂盒(精)

人性激素结合球蛋白(SHBG)酶联免疫吸附测定试剂盒使用说明书产品编号:E0396hUSCNLIFE TM 本试剂盒仅供体外研究使用、不用于临床诊断!预期应用ELISA法定量测定人血清、血浆或其它相关生物液体中SHBG含量。
实验原理用纯化的SHBG抗体包被微孔板,制成固相载体,往微孔中依次加入标本或标准品、生物素化的SHBG抗体、HRP标记的亲和素,经过彻底洗涤后用底物(TMB)显色。
TMB在过氧化物酶的催化下转化成蓝色,并在酸的作用下转化成最终的黄色。
颜色的深浅和样品中的SHBG呈正相关。
用酶标仪在450nm波长下测定吸光度(值),计算样品浓度。
试剂盒组成及试剂配制1、酶标板:一块(96孔)2、标准品(冻干品): 2瓶,请临用前15分钟内配制。
每瓶以样品稀释液稀释至1ml,盖好后室温静置大约10分钟,同时反复颠倒/搓动以助溶解,其浓度为500 nmol/L,然后做系列倍比稀释(注:不要直接在板中进行倍比稀释),分别配制成500 nmol/L,250 nmol/L,125 nmol/L,62.5 nmol/L,31.2 nmol/L,15.6 nmol/L,7.8 nmol/L,样品稀释液直接作为空白孔 0 nmol/L。
如配制250 nmol/L标准品:取0.5ml (不要少于0.5ml )500 nmol/L的上述标准品加入含有0.5ml样品稀释液的Eppendorf管中,混匀即可,其余浓度以此类推。
3、样品稀释液:1×20ml。
4、检测稀释液A:1×10ml。
5、检测稀释液B:1×10ml。
6、检测溶液A:1×120/瓶(1:100)。
临用前以检测稀释液A 1:100稀释(如:10 检测溶液A / 990检测稀释液A),充分混匀,稀释前根据预先计算好的每次实验所需的总量配制(100/孔),实际配制时应多配制 0.1-0.2ml。
7、检测溶液B:1×120/瓶(1:100)。
性激素结合球蛋白(SHBG)测定试剂盒(磁微粒化学发光法)产品技术要求利德曼生化
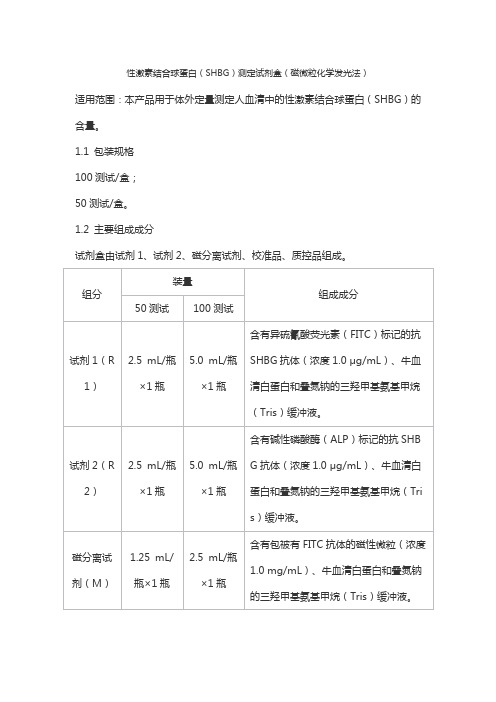
性激素结合球蛋白(SHBG)测定试剂盒(磁微粒化学发光法)适用范围:本产品用于体外定量测定人血清中的性激素结合球蛋白(SHBG)的含量。
1.1 包装规格100测试/盒;50测试/盒。
1.2 主要组成成分试剂盒由试剂1、试剂2、磁分离试剂、校准品、质控品组成。
注:校准品和质控品浓度具有批特异性,具体数值见瓶标签。
2.1外观2.1.1试剂盒各组分应齐全、完整、液体无渗漏;2.1.2磁分离试剂摇匀后为均匀悬浊液,无明显凝集;2.1.3液体组分应无沉淀或絮状物;2.1.4包装标签应清晰,易识别。
2.2准确度回收率应在85.0%-115.0%范围内。
2.3空白限应不大于0.35 nmol/L。
2.4线性在[0.50,200.00]nmol/L的测量范围内,试剂盒的相关系数r应≥0.9900。
2.5重复性用(10.00±2.00)nmol/L和(100.00±20.00)nmol/L的样本各重复检测10次,变异系数(CV)应不大于10.0%。
2.6批间差用三个批号的试剂盒分别检测(10.00±2.00)nmol/L和(100.00±20.00)nmol/L的样本,重复检测10次,其批间变异系数应≤15%。
2.7质控品的赋值有效性质控品的测量值应在质控范围内。
2.8 稳定性试剂盒2℃~8℃保存有效期为12个月,在有效期满后检测试剂盒的准确度、空白限、线性、重复性、质控品的赋值有效性,应符合2.2、2.3、2.4、2.5、2.7的要求。
2.9 分析特异性测定浓度为20.00μg/mL的5α-双氢睾酮(5α-DHT)、20.00μg/mL的睾酮(T)、5.00ng/mL的雌二醇(E2)样本,测定结果≤0.50nmol/L。
2.10溯源性根据GB/T 21415及有关规定提供校准品的来源、赋值过程以及不确定度等内容,性激素结合球蛋白校准品溯源至企业校准品,企业校准品已与上市产品比对赋值。
性激素结合球蛋白测定试剂盒(化学发光免疫分析法)产品技术要求新产业

2.性能指标
2.1外观和性状
试剂盒各组分应齐全、完整、液体无渗漏;包装标签应清晰,准确、牢固;试剂盒内组分(磁性微球溶液、校准品和质控品除外)应为澄清的液体,无沉淀、无悬浮物、无絮状物;对于以冻干粉形式保存的校准品和质控品,复溶后应为澄清的液体,不含异物、浑浊或摇不散的沉淀或颗粒。
2.2批内精密度
批内变异系数(CV)应≤10%。
2.3批间精密度
批间变异系数(CV)应≤15%。
2.4准确度
回收率应在(90.0%-110.0%)范围内。
2.5空白限
空白限应≤ 0.200 nmol/L。
2.6线性
在(0.800-250)nmol/L 浓度区间内,线性相关性系数(r)绝对值应≥ 0.9900。
2.7校准品均一性
校准品均一性(CV)应≤10%。
2.8质控品测量准确度
质控品测定结果在质控范围内(质控范围详见质控品标签)。
2.9质控品均一性
质控品均一性(CV)应≤10%。
2.10溯源性
本试剂盒校准品可以溯源至W HO标准品(2nd,NIBS C code:08/266)。
第 1 页共1 页。
性激素结合球蛋白

性激素结合球蛋白的研究进展与展 望
性激素结合球蛋白的研究现状
研究方向:性激素结合球蛋白的结构与功能研究
研究进展:发现了性激素结合球蛋白在生殖系统中的重要作用为相关疾病的治疗提供了新 的思路
研究成果:成功克隆了性激素结合球蛋白基因为进一步研究奠定了基础
研究展望:未来将深入研究性激素结合球蛋白的作用机制为相关疾病的预防和治疗提供更 多有效方案
性激素结合球蛋白 的检测方法有多种 可根据具体情况选 择合适的检测方式。
性激素结合球蛋白的检测与临床意 义
性激素结合球蛋白的检测方法
放射免疫分 析法
化学发光法
酶联免疫吸 附法
免疫透射比 浊法
性激素结合球蛋白检测的临床意义
评估性腺功能:性激素结合球蛋白与性腺功能密切相关检测其水平有助于评估性腺功能状态。
辅助诊断性早熟:通过检测性激素结合球蛋白水平有助于辅助诊断性早熟。
监测治疗反应:对于接受性腺相关治疗的患者检测性激素结合球蛋白水平有助于监测治疗反应和 调整治疗方案。
预测疾病风险:性激素结合球蛋白水平异常可能与某些生殖系统疾病的风险相关检测其水平有助 于预测疾病风险。
性激素结合球蛋白检测的注意事项
研究性激素结合 球蛋白与女性生 殖健康的关系有 助于深入了解女 性生殖系统的生 理和病理机制为 预防和治疗相关 疾病提供科学依 据。
性激素结合球蛋白与不孕不育
性激素结合球蛋白 与生殖健康密切相 关是评估女性生育 能力的重要指标。
性激素结合球蛋白 水平异常可能导致 不孕不育需及时就 医检查和治疗。
通过调整生活方式 和饮食习惯可以提 高性激素结合球蛋 白水平从而改善生 育能力。
性激素结合球蛋白的合成与分泌
性激素结合球蛋白的合成和 分泌受到多种因素的影响如 激素、生长因子等。
性激素结合球蛋白检测作业指导书医学检验

《文件已阅声明表》《Procedure circulation form》文件名称: 性激素结合球蛋白检测作业指导书表号: KM-MP03•02•02已阅声明:本人承诺已了解此文件中的相关内容,今后的工作中将严格按照此文件执行,不随意对外传阅此文件,如有因与文件不相符的操作,责任由本人承担。
(I have understood the relevant content of the document.I will keep the document secret and be responsible to properly perform procedure)阅读人签名表姓名(NAME)职务签名(SIGNATURE)签名日期(DATE)(POSITION)《文件修改记录页》《Procedure amendment form》序号NO.页码(Page)内容更改说明(Description ofModified contents)审批人(Approvedby )批准生效日期(Approveddate)1换版《文件信息表》《Procedure information form》文件名Title ofDOC.(Doc.Code)性激素结合球蛋白检测作业指导书(KM-SOP0300.317)版本号(Edition No.) Edition 3.0 生效日期(Operativedate)2008-03-13 文控部门(Doc. Control Dept.)实验室文控室回顾日期/签名 (Review date /signature ) 回顾日期(Reviewdate)回顾人员签名( Signature )替代文件(Replaces) 性激素结合球蛋白检测作业指导书(KM-SOP0300.317)Edition 2.0存放地点(Location)/持有人(Holder)No. Location(Holder) No. Location (Holder)1诊断部文控室(陈彬)2 发光室(段学成)作者签名/日期(Authorsignature/date)陈鲜美审批人签名/日期(Authorized by :Signature/Date)陈建波接收人签名/日期(Receiptor/Date)副本数(Copy No.) 本文件是第个文件拷贝 / 共发放 2 个文件拷贝。
大鼠(Rat)性激素结合球蛋白(SHBG)-NEWA

本试剂盒只能用于科学研究,不得用于医学诊断大鼠(Rat)性激素结合球蛋白(SHBG)ELISA检测试剂盒使用说明书检测原理试剂盒采用双抗体一步夹心法酶联免疫吸附试验(ELISA)。
往预先包被性激素结合球蛋白(SHBG)抗体的包被微孔中,依次加入标本、标准品、HRP标记的检测抗体,经过温育并彻底洗涤。
用底物TMB显色,TMB在过氧化物酶的催化下转化成蓝色,并在酸的作用下转化成最终的黄色。
颜色的深浅和样品中的性激素结合球蛋白(SHBG)呈正相关。
用酶标仪在450nm 波长下测定吸光度(OD 值),计算样品浓度。
样品收集、处理及保存方法1. 血清:使用不含热原和内毒素的试管,操作过程中避免任何细胞刺激,收集血液后,3000转离心10分钟将血清和红细胞迅速小心地分离。
2. 血浆:EDTA、柠檬酸盐或肝素抗凝。
3000转离心30分钟取上清。
3. 细胞上清液:3000转离心10分钟去除颗粒和聚合物。
4. 组织匀浆:将组织加入适量生理盐水捣碎。
3000转离心10分钟取上清。
5. 保存:如果样本收集后不及时检测,请按一次用量分装,冻存于-20℃,避免反复冻融,在室温下解冻并确保样品均匀地充分解冻。
自备物品1.酶标仪(450nm)2.高精度加样器及枪头:0.5-10uL、2-20uL、20-200uL、200-1000uL3.37℃恒温箱操作注意事项1. 试剂盒保存在2-8℃,使用前室温平衡20分钟。
从冰箱取出的浓缩洗涤液会有结晶,这属于正常现象,水浴加热使结晶完全溶解后再使用。
2. 实验中不用的板条应立即放回自封袋中,密封(低温干燥)保存。
3. 浓度为0的S0号标准品即可视为阴性对照或者空白;按照说明书操作时样本已经稀释5倍,最终结果乘以5才是样本实际浓度。
4. 严格按照说明书中标明的时间、加液量及顺序进行温育操作。
5. 所有液体组分使用前充分摇匀。
试剂盒组成名称96孔配置48孔配置 备注微孔酶标板 12孔×8条 12孔×4条 无标准品 0.3mL*6管 0.3mL*6管 无 样本稀释液 6mL 3mL 无 检测抗体-HRP 10mL 5mL 无 20×洗涤缓冲液 25mL 15mL 按说明书进行稀释底物A 6mL 3mL 无 底物B 6mL 3mL 无 终止液 6mL 3mL 无 封板膜 2张 2张 无 说明书 1份 1份 无自封袋1个1个无 注:标准品(S0-S5)浓度依次为:0、7.5、15、30、60、120 nmol/L试剂的准备20×洗涤缓冲液的稀释:蒸馏水按1:20稀释,即1份的20×洗涤缓冲液加19份的蒸馏水。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
《文件已阅声明表》《Procedure circulation form》文件名称: 性激素结合球蛋白检测作业指导书表号: KM-MP03•02•02已阅声明:本人承诺已了解此文件中的相关内容,今后的工作中将严格按照此文件执行,不随意对外传阅此文件,如有因与文件不相符的操作,责任由本人承担。
(I have understood the relevant content of the will keep the document secret and be responsible to properly perform procedure)阅读人签名表签名(SIGNATURE)签名日期(DATE)姓名(NAME)职务(POSITION)《文件修改记录页》《Procedure amendment form》序号NO.页码(Page)内容更改说明(Description ofModified contents)审批人(Approvedby )批准生效日期(Approveddate)1换版《文件信息表》《Procedure information form》文件名Title of DOC.性激素结合球蛋白检测作业指导书版本号(Edition No.) Edition 生效日期(Operativedate)2008-03-13 文控部门(Doc. Control Dept.)实验室文控室回顾日期/签名 (Review date /signature ) 回顾日期(Reviewdate)回顾人员签名( Signature )替代文件(Replaces) 性激素结合球蛋白检测作业指导书Edition存放地点(Location)/持有人(Holder)No. Location(Holder) No. Location (Holder)1诊断部文控室(陈彬)2 发光室(段学成)作者签名/日期(Authorsignature/date)陈鲜美审批人签名/日期(Authorized by :Signature/Date)陈建波接收人签名/日期(Receiptor/Date)副本数(Copy No.) 本文件是第个文件拷贝 / 共发放 2 个文件拷贝。
性激素结合球蛋白检测作业指导书(Analysis of SHBG by IMMULITE 1000)1. 原理(Test principle):固相、学发光免疫量度检测法(a solid-phase, chemiluminescent immunometricassay):包括免疫反应和化学反应,利用在化学反应中释放大量自由能产生激发态中间体,当其回到稳定的基态时,同时也发射出光子,利用发光信号测量仪对所发出的光量子进行定量测量。
2. 样本收集和储存(Specimen Collection and Storage):标本收集(specimen collection):血清(serum);单次用量(volume)200μl,仪器加样量(sampling volume)50μl(样本杯中加样量至少要超过检测总用量100μl)拒收标本(Specimen rejection):严重脂血(lipoprotein)样本应拒收。
脂血(lipoprotein)可能会干扰检测,推荐使用超速离心清除脂血(lipoprotein)样本。
溶血(hemolysis)样本提示样本在送达实验室之前处理不当,因此检测结果将受到影响,应予以注意。
血清(serum)样本在未充分凝集前离心将导致纤维蛋白的存在。
为避免纤维蛋白对结果的影响必须确保离心处理前样本已经完全充分凝集。
对于正在接受抗凝剂治疗的病人样本,需要延长凝集时间。
源于不同生产商的血样收集试管,由于原材料和添加剂不同,包括凝胶或物理涂层、促凝剂和/或抗凝剂,可能导致得到不同的结果。
本试剂盒没有对所有可能应用的收集管类型进行测试。
推荐使用超速离心法清除脂血样本.溶血样(hemolyzed sample)提示样本在送达实验室之前处理不当,因此检测结果将受到影响,应予以注意。
为避免纤维蛋白对结果的影响,必须确定离心处理前样本已经完全充分凝集。
对于正在接受抗凝剂治疗的病人样本,需要延长凝集时间。
标本储存条件(specimen storage conditions):(room temperature)24小时, 2-8℃7天; -20℃2个月;十天后处理标本。
3、试剂(Reagent):美国DPC IMMULITE 原装试剂。
3.1.1试剂内组份(Components):试剂盒组分必须成套使用,内包装盒上的条码标签为实验必需。
检测单位(SBG)每个带有条码的检测单位内有一个包被珠,包被有高纯度人anti-SHBG。
2~8℃可稳定至失效期。
LKSH1:100个,LKSH5:500个打开包装之前应恢复至室温,从包装顶部剪开,完整保留拉链隆起缘。
使用后将拉链重新封好,避免潮湿。
SHBGSAb试剂楔(LSH2)试剂楔带有条码。
碱性磷酸酶标记的anti-SHBG基质. 封盖低温保存:2~8℃可稳定至失效期,建议打开包装后在得示保存条件下30天内用完。
LKSH1:1套LKSH5:5套使用前将试剂楔顶部穿孔部位的胶条撕开,注意不要损坏条码。
揭掉试剂楔顶部的铝箔封条,将试剂楔滑盖的顶部搭扣在下方的斜坡上。
校正(LSHL,LSHH)两瓶(低、高)冻干的含SHBG自身抗体的人血清/缓冲液基质。
使用前至少提前30 min 复溶,复溶每瓶加 mL蒸馏水或去离子水。
轻轻翻转混匀,直至冻干粉完全溶解(不需要进一步稀释)。
分装并冷冻于密封塑料容器中。
避免反复冻融。
复溶后2~8℃可稳定保存30天,-20℃可以保存(分装)6个月。
LKSH1:1套LKSH5:2套LSHC1-2:SHBG质控每瓶加 mL蒸馏水或去离子水复溶后2~8℃可稳定保存30天,-20℃可以保存(分装)6个月。
SHBG稀释液(LSHZ4)用于人工稀释病人样本。
1:20倍稀释。
3.1.2未随试剂盒提供的组分L1KSHW1,5L1KSHW1:2套 L1KSHW5:10套LSUBX:化学发光底物LPWS2:探针清洗液LKPM:探针清洗试剂盒LCHX-Y:样本怀架(带条码)LSCP:样本怀(一次性)LSCC:样本怀盖(可选)DCHS:样品稀释管盖其它必需:样本加样吸管、蒸溜水或去离子水、质控。
试剂准备(Reagent preparation):将试剂从冰箱中取出并平衡至室温;不同批号的试剂不能混用;新试剂与前一批号试剂不同,则需做样本结果的比对,并记录,差异在允许范围内方可使用。
Put reagent from refrigeratory to room temperature for proper time;New reagent lots must be tested in parallel with old lots before or concurrently with being placed in service to ensure that the calibration of the new lot of reagent has maintained consistent results for patient specimens. Record the results.4 仪器(Instrument):美国DPC IMMULITE 1000.仪器准备(Prepare apparatus):使用前将仪器的液体与固体垃圾清空;加入足够的蒸馏水,清冼液,底物及样本杯。
然后运行仪器操作软件。
而后排水及底物,防止内有残留气柱。
将仪器的试剂盘中加入所需的试剂。
5.安全防范(Safety Precautions):操作时必须穿戴手套和工作服;工作后的台面应消毒擦洗;用过的加样枪头等耗材应作为医用垃圾处理;为了避免形成气溶胶,所有样品尽可能不要在空气当中暴露太长时间;遇到样本洒出,被污染的区域应立即用次氯酸钠溶液清洗,擦拭用的物品应丢弃在标有生物污染的垃圾筒中。
6校准(Calibration):校准品储存和使用(Calibration material storage and usage):美国DPC IMMULITE 1000 原装校准品。
要求在有效期内使用,过期的校准液应停止使用,保存于2-8℃可稳定到有效期。
Stop using overdue calibration it within expiration date,storage in 2-8℃复溶(Calibration material resolved):用复溶专用加样枪准确吸取3mL去离子水于瓶中,溶解静置1小时,混匀并用有盖小子弹头分装600μL/个,标明配制日期,校准品批号,配制人以及有效日期,于-20℃冻存备用。
Label confecting date ,calibration lot,person who confected, expiration复溶后校准品成分的稳定性:保存于15~25℃,可稳定8小时保存于2~8℃,可稳定2天保存于(-15)~(-25)℃,可稳定1个月(不可反复冻融)。
校准周期(Recommended Adjustment Interval):2周(2 weeks)。
当下列任何一种情况出现时,请重新校准:(If one of the two happens, recalibration )⑴试剂批号改变 (Reagent lot changes)⑵根据质控需要进行校准(Recalibration based on quality control problem) 厂商建议校准周期:2周(2 weeks)步骤:在计算机屏幕上选择Kit Entry项,用扫码器扫描药盒上的条码,选择Patient Entry项,输入SHBG校正信息.然后将两个样本杯中分别加入至少600ul的A,B校准品,放在加样履带上。
点击GO。
仪器自动识别校准是否通过,但是每次做校准后,必须跟做所有浓度的质控,如质控在控则校准通过。
7操作过程:(Procedural Steps)将从标本组取回的带有编号的血清标本,并按相应顺序将待测血清加入相应的样本管。
样本需稀释,稀释材料(Dilution material):SHBG diluents稀释倍数(Dilution times):1:20(10ul sample: 200ul diluents)取出空样本杯架,将已稀释好血清的并按相应顺序将待测血清加入相应的样本管,再将样品怀管放入对应的样本杯架中。
将样品杯放到进样链条的箭头处,其后放入SHBG反应杯。
