《医疗机构制剂许可证》验收标准 (1)
2023年-2024年执业药师之药事管理与法规精选试题及答案一

2023年-2024年执业药师之药事管理与法规精选试题及答案一单选题(共40题)1、关于药品安全风险的说法,正确的是()A.药品安全风险具有复杂性、可预见性和可控性B.药品安全风险管理的目的是使药品使用风险最小化C.药品安全的人为风险又称“必然风险”“固有风险”D.药品安全的自然风险主要来源于不合理用药、用药差错、药品质量问题等【答案】 B2、属于一级保护野生药材物种的是A.羚羊角B.熊胆C.人参D.穿山甲【答案】 A3、医疗器械使用单位对植入性医疗器械进货查验记录应当A.永久保存B.保存至医疗器械规定使用期限届满后2年或者使用终止后2年C.保存至医疗器械规定使用期限届满后3年或者使用终止后3年D.保存至医疗器械规定使用期限届满后5年或者使用终止后5年【答案】 A4、有关药品广告的说法,错误的是()A.药品广告不得说明治愈率或有效率B.药品广告应按批准的说明书说明适应证C.第二类精神药品不得做广告D.药品广告可以患者的名义作疗效证明【答案】 D5、根据《疫苗管理法》,关于疫苗上市许可和临床试验要求的说法,错误的是A.疫苗临床试验应当由符合国务院药品监督管理部门和国务院卫生健康主管部门规定条件的三级医疗机构或者省级以上疾病预防控制机构实施或者组织实施B.开展疫苗临床试验,应当取得受试者的书面知情同意,受试者为限制民事行为能力人的,只需要取得监护人的书面知情同意C.对疾病预防、控制急需的疫苗和创新疫苗,国务院药品监督管理部门应当予以优先审评审批D.国务院药品监督管理部门在批准疫苗注册申请时,对疫苗的生产工艺、质量控制标准和说明书、标签予以核准【答案】 B6、至少应当注明药品名称、贮藏、生产日期、产品批号、有效期、执行标准、批准文号、生产企业等内容的标签是A.药品的外标签B.药品的内标签C.用于运输、储藏的药品的包装标签D.原料药的标签【答案】 D7、某区药品监督管理部门对辖区内的某一药品零售企业(连锁药店)进行检查,检查人员发现其货架上销售的药品有艾司唑仑片10盒。
药物制剂留样制度与稳定性研究

3.1影响因素试验
(1)高温试验: 供试品开口置于适宜的洁净容器中,
60℃ 温度下放置 10 天,在第 5 天和第 10 天取样,按稳定性重点考察项目进行检测。若 供试品有明显变化(如含量下降5%),则在 40℃条件下同法进行试验。若 60℃无明显变化, 不再进行40℃试验。
3.1影响因素试验
(2)高湿度试验: 供试品置于恒湿密闭容器中,在25℃分别于相对湿 度90%±5%条件下放置10天,于第5天和第10天取样, 按稳定性重点考察项目要求检验,同时准确称量试 验前后供试品的重量,以考察供试品的吸湿潮解性 能。若吸湿增重5%以上,则在相对湿度75%±5% 条 件下,同法进行试验;若吸湿增重5%以下,且其他 考察项目符合要求,则不再进行此项试验。
1、稳定性研究的目的与意义
考察原料药或药物制剂在温度、湿度、光线 的影响下随时间变化的规律,为药品的生产、 包装、储存、运输条件提供科学依据,同时通 过试验建立药品的有效期。为物料储存期和有 效期提供数据。
1、稳定性研究的目的与意义
制剂工艺研究
质量研究
稳定性研究
2、稳定性试验的基本要求
(1)稳定性试验包括影响因素试验、加速试验 和长期试验。
2、稳定性试验的基本要求
(3)供品质量标准一致。
(4)加速试验与长期试验所用供试品包装方式 应与上市产品一致。
2、稳定性试验的基本要求
(5)研究药物稳定性,要采用专属性强、准确、 精密、灵活的药物分析方法与有关物质(含降解 产物及其他变化所生成的产物)的检查方法,并 对方法进行验证,以保证药物稳定性试验结果的 可靠性。在稳定性试验中,应重视有关物质的检 查。
药物制剂留样制度与 稳定性研究
一、药物制剂留样制度
2023年执业药师之药事管理与法规模考预测题库(夺冠系列)

2023年执业药师之药事管理与法规模考预测题库(夺冠系列)单选题(共60题)1、某市食品药品监督管理局接到举报,反映该市甲兽药店销售人用药品。
市局调查发现甲兽药店药柜上摆放有多个品种的人用药品。
经查实,兽药店所经营的人用药品达30余种,货值金额5000元,主要是非处方药,部分药品已销售,销售金额已达到1000元。
当事的兽药店有《兽药经营许可证》,无《药品经营许可证》。
A.毒性药品的生产计划由国家药品监督管理部门批准B.生产企业按批准的计划生产C.由医药专业人员负责配制和质量检验D.每次配料必须2人以上复核无误【答案】 A2、关于处方正文部分的叙述,正确的是()。
A.处方编号,以Rp或R标示,临床诊断,分列药品名称、规格、用量B.以Rp或R标示,分列药品名称、剂型、规格、数量、用法用量C.以Rp或R标示,分列药品金额以及审核、药师签名D.临床诊断,以Rp或R标示,分列药品名称、数量、用法用量【答案】 B3、特殊情况需超剂量使用时A.要准确规范,不得使用“遵医嘱”“自用”等含糊不清字句B.应当清楚,不得涂改;如需修改,应当在修改处签名并注明修改日期C.一般按君、臣、佐、使的顺序排列D.应注明原因并再次签名【答案】 D4、2020年1月31日,某药品零售企业甲从药品批发企业乙购进药品上市许可持有人丙生产的中药注射剂Z。
在验收入库时,核对验明票、货、账三者一致后入库、销售。
中药注射制剂Z说明书标注标注“有效期24个月”,标签标注“生产日期为2019年7月1日,有效期至2021年6月”。
2020年6月,甲所在地突降暴雨,中药注射剂Z被雨水浸泡,导致药品标签剥落或字迹模糊。
2020年7月,甲将该批药品中的三盒销售给某患者,销售总价为200元。
该患者用药后病情加重。
A.Z说明书中标注的有效期格式“有效期至2021年6月”有误,应该退回B.采购时仅向配送药品的乙索要、核对验证发票即可C.作为药品零售企业,甲不能购进中药注射剂D.购进票据保存期不得少于5年,至少保存至2025年2月1日【答案】 A5、不得发布广告的是A.基本药物B.非处方药C.医疗机构配制的制剂D.处方药【答案】 C6、2014年8月,某省市场和质量监督管理委员会在全省启动中药材、中药饮片专项检查。
2022年-2023年执业药师之药事管理与法规能力检测试卷A卷附答案

2022年-2023年执业药师之药事管理与法规能力检测试卷A卷附答案单选题(共30题)1、《中华人民共和国药品管理法》和《中华人民共和国中医药法》对医疗机构中药制剂进行了一系列规定。
某医院有以下制剂配制行为:①自配中药制剂未经批准;②自配中药制剂不按批准的标准配制;③委托配制中药制剂未批准;④应用传统工艺配制中药制剂未按照备案材料载明的要求配制中药制剂。
A.自配中药制剂未经批准B.自配中药制剂不按批准的标准配制C.委托配制中药制剂未批准D.应用传统工艺配制中药制剂,未按照备案材料载明的要求配制中药制剂【答案】 D2、《进口药品注册证》《医药产品注册证》的有效期为A.1年B.2年C.3年D.5年【答案】 D3、仅化学药品非处方药说明书有此项,如“解热镇痛类”应列人非处方药说明书中的A.[作用类别]B.[注意事项]C.[不良反应]D.[药理毒理]【答案】 A4、根据《化学药品和治疗用生物制品说明书规范细则》了解合并用药的注意事项,可查阅A.【用法用量】B.【药物相互作用】C.【禁忌】D.【药物过量】【答案】 B5、2014年8月,某省市场和质量监督管理委员会在全省启动中药材、中药饮片专项检查。
中药材、中药饮片是药品的重要组成部分,为确保中药制剂源头的质量安全,从即日起至11月30日,集中查处中药材、中药饮片生产经营领域以次充好、以假充真、染色增重、掺杂使假等违法违规行为,规范本省中药产品生产经营秩序。
该省市场和质量监督管理委员会要求各药品生产企业及医疗机构制剂室,用于生产购入的中药材、中药饮片要严格按照规定进行入库验收、存放,每个购入批次必须按照法定标准进行检验合格后方可投产使用。
A.按生产假药给予处罚B.按生产劣药给予处罚C.按无证生产给予处罚D.按从无证企业购入药品给予处罚【答案】 A6、基本药物制度是医改的核心内容之一,也是推进医改的重要一环。
长春市结合实际,建立了以“721”资金保障、“同城同价”等政策为核心的一整套基本药物制度运行模式。
医疗机构制剂法规文件汇编

医疗机构制剂法规文件汇编《医疗机构制剂配制监督管理办法》(试行)于2005年3月22日经国家食品药品监督管理局局务会审议通过,现予公布,自2005年6月1日起施行。
局长:郑筱萸二00五年四月十四日医疗机构制剂配制监督管理办法(试行)第一章总则第一条为加强医疗机构制剂配制的监督管理,根据《中华人民共和国药品管理法》(以下简称《药品管理法》)、《中华人民共和国药品管理法实施条例》(以下简称《药品管理法实施条例》)的规定,制定本办法。
第二条医疗机构制剂的配制及其监督管理适用本办法。
第三条医疗机构制剂配制监督管理是指(食品)药品监督管理部门依法对医疗机构制剂配制条件和配制过程等进行审查、许可、检查的监督管理活动。
第四条国家食品药品监督管理局负责全国医疗机构制剂配制的监督管理工作。
省、自治区、直辖市(食品)药品监督管理部门负责本辖区医疗机构制剂配制的监督管理工作。
第五条医疗机构配制制剂应当遵守《医疗机构制剂配制质量管理规范》。
第二章医疗机构设立制剂室的许可第六条医疗机构配制制剂,必须具有能够保证制剂质量的人员、设施、检验仪器、卫生条件和管理制度。
第七条医疗机构设立制剂室,应当向所在地省、自治区、直辖市(食品)药品监督管理部门提交以下材料:(一)《医疗机构制剂许可证申请表》(见附件1);(二)实施《医疗机构制剂配制质量管理规范》自查报告;(三)医疗机构的基本情况及《医疗机构执业许可证》副本复印件;(四)所在地省、自治区、直辖市卫生行政部门的审核同意意见;(五)拟办制剂室的基本情况,包括制剂室的投资规模、占地面积、周围环境、基础设施等条件说明,并提供医疗机构总平面布局图、制剂室总平面布局图(标明空气洁净度等级);制剂室负责人、药检室负责人、制剂质量管理组织负责人简历(包括姓名、年龄、性别、学历、所学专业、职务、职称、原从事药学工作年限等)及专业技术人员占制剂室工作人员的比例;制剂室负责人、药检室负责人、制剂质量管理组织负责人应当为本单位在职专业人员,且制剂室负责人和药检室负责人不得互相兼任;(六)拟配制剂型、配制能力、品种、规格;(七)配制剂型的工艺流程图、质量标准(或草案);(八)主要配制设备、检测仪器目录;(九)制剂配制管理、质量管理文件目录。
医疗机构制剂配制监督管理办法

(2005年4月14日国家食品药品监督管理局令第18号公布自2005年6月1日起施行)第一章总则第一条为加强医疗机构制剂配制的监督管理,根据《中华人民共和国药品管理法》(以下简称《药品管理法》)、《中华人民共和国药品管理法实施条例》(以下简称《药品管理法实施条例》)的规定,制定本办法。
第二条医疗机构制剂的配制及其监督管理适用本办法。
第三条医疗机构制剂配制监督管理是指(食品)药品监督管理部门依法对医疗机构制剂配制条件和配制过程等进行审查、许可、检查的监督管理活动。
第四条国家食品药品监督管理局负责全国医疗机构制剂配制的监督管理工作。
省、自治区、直辖市(食品)药品监督管理部门负责本辖区医疗机构制剂配制的监督管理工作。
第五条医疗机构配制制剂应当遵守《医疗机构制剂配制质量管理规范》。
第二章医疗机构设立制剂室的许可第六条医疗机构配制制剂,必须具有能够保证制剂质量的人员、设施、检验仪器、卫生条件和管理制度。
第七条医疗机构设立制剂室,应当向所在地省、自治区、直辖市(食品)药品监督管理部门提交以下材料:(一)《医疗机构制剂许可证申请表》(见附件1);(二)实施《医疗机构制剂配制质量管理规范》自查报告;(三)医疗机构的基本情况及《医疗机构执业许可证》副本复印件;(四)所在地省、自治区、直辖市卫生行政部门的审核同意意见;(五)拟办制剂室的基本情况,包括制剂室的投资规模、占地面积、周围环境、基础设施等条件说明,并提供医疗机构总平面布局图、制剂室总平面布局图(标明空气洁净度等级);制剂室负责人、药检室负责人、制剂质量管理组织负责人简历(包括姓名、年龄、性别、学历、所学专业、职务、职称、原从事药学工作年限等)及专业技术人员占制剂室工作人员的比例;制剂室负责人、药检室负责人、制剂质量管理组织负责人应当为本单位在职专业人员,且制剂室负责人和药检室负责人不得互相兼任;(六)拟配制剂型、配制能力、品种、规格;(七)配制剂型的工艺流程图、质量标准(或草案);(八)主要配制设备、检测仪器目录;(九)制剂配制管理、质量管理文件目录。
四川省《医疗机构制剂许可证》换证验收细则

附件5:
四川省《医疗机构制剂许可证》
换证验收细则
四川省药品监督管理局
二OOO年八月
四川省《医疗机构制剂许可证》换证检查评定原则
一、考核依据:国家药品监督管理局制订的《医疗机构制剂许可证》验收标准。
二、评定规则:
1、本细则分人员与机构、厂房与设施、设备、物料、卫生、配制管理、质量管理、其它8个大项,共
设评定条款93条。
其中设否决条款5条(条款号前加“**”);重点条款17条(条款号前加“*”),每条满分为10分;一般条款71条,每条满分为5分。
总分为525分。
2、验收评定时,按医疗机构配制制剂类别确定具体检查条款。
3、否决条款应全部合格,且一般条款总得分率不低于60%为合格。
三、评分办法
1、各一般条款按评分系数评分,评分系数以达到该条款所要求的程度确定。
评分系数如下:
1.0达到要求
0.6基本达到要求
0达不到要求
2、否决条款以达到各有关条款要求为合格,未达到要求为不合格。
四川省《医疗机构制剂许可证》换证验收细则
注:否决条款评定结果以“合格”或“不合格”结论填在实得分栏内。
四川省《医疗机构制剂许可证》换证验收细则
四川省《医疗机构制剂许可证》换证验收细则
四川省《医疗机构制剂许可证》换证验收细则
四川省《医疗机构制剂许可证》换证验收细则附表1 制剂配制环境空气洁净度级别要求表
四川省《医疗机构制剂许可证》换证验收细则
附表2 洁净区空气洁净度级别表
注:1、沉降菌用Φ90mm培养皿取样,暴露时间不低于30分钟。
2、100级洁净室(区)的垂直层流0.3米/秒,水平层流0.4米/秒。
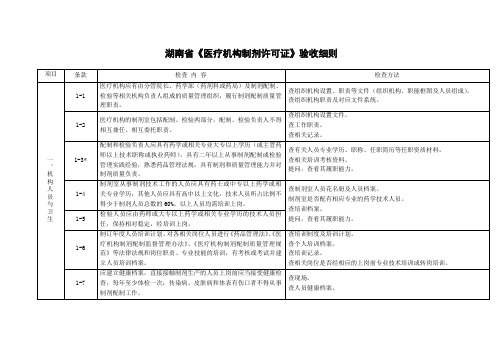
湖南省《医疗机构制剂许可证》验收细则
1-9
进入配制间(区)的人员应按照卫生操作规程更衣。工作服的选材、穿戴方式应与从事的工作和空气洁净室级别要求相适应。
查现场是否设置工作服专用洗衣设备
询问工作服管理有关规定并查看现场人员工作服穿着情况
1-10
进入配制间(区)人员不得化妆和佩带饰物,不得裸手直接接触药品及与药品直接接触的包装材料和设备表面。
查培训档案。
提问,查看其履职能力。
1-5
检验人员应由药师或大专以上药学或相关专业学历的技术人员担任,保持相对稳定,经培训上岗。
1-6
制订年度人员培训计划。对各相关岗位人员进行《药品管理法》、《医疗机构制剂配制监督管理办法》、《医疗机构制剂配制质量管理规范》等法律法规和岗位职责、专业技能的培训,有考核或考试并建立人员培训档案。
湖南省《医疗机构制剂许可证》验收细则
项目
条款
检查 内 容
检查方法
一、机构人员与卫生
1-1
医疗机构应有由分管院长、药学部(药剂科或药局)及制剂配制、检验等相关机构负责人组成的质量管理组织,履行制剂配制质量管理职责。
查组织机构设置、职责等文件(组织机构、职能框图及人员组成)。
查组织机构职责及对应文件系统。
1-2
医疗机构的制剂室包括配制、检验两部分,配制、检验负责人不得相互兼任、相互委托职责。
查组织机构设置文件。
查工作职责。
查相关记录。
1-3*
配制和检验负责人应具有药学或相关专业大专以上学历(或主管药师以上技术职称或执业药师),具有二年以上从事制剂配制或检验管理实践经验,熟悉药品管理法规,具有制剂和质量管理能力并对制剂质量负责。
2-6
制剂室洁净区内表面(墙壁、顶棚、地面)应平整、光滑,无裂缝、接口严密、地面无积水,无颗粒物脱落,便于有效清洁,必要时应进行消毒。
医疗机构制剂配制质量管理规范

《医疗机构制剂配制质量管理规范》(局令第27号)国家药品监督管理局令第27号《医疗机构制剂配制质量管理规范》(试行)于2000年12月5日经国家药品监督管理局局务会议通过,现予发布。
本规范自发布之日起施行。
二○○一年三月十三日医疗机构制剂配制质量管理规范( 试行)第一章总则第一条根据《中华人民共和国药品管理法》的规定,参照《药品生产质量管理规范》的基本原则,制定本规范。
第二条医疗机构制剂是指医疗机构根据本单位临床需要而常规配制、自用的固定处方制剂。
第三条医疗机构配制制剂应取得省、自治区、直辖市药品监督管理局颁发的《医疗机构制剂许可证》。
第四条国家药品监督管理局和省、自治区、直辖市药品监督管理局负责对医疗机构制剂进行质量监督,并发布质量公告。
第五条本规范是医疗机构制剂配制和质量管理的基本准则,适用于制剂配制的全过程。
第二章机构与人员第六条医疗机构制剂配制应在药剂部门设制剂室、药检室和质量管理组织。
机构与岗位人员的职责应明确,并配备具有相应素质及相应数量的专业技术人员。
第七条医疗机构负责人对本《规范》的实施及制剂质量负责。
第八条制剂室和药检室的负责人应具有大专以上药学或相关专业学历,具有相应管理的实践经验,有对工作中出现的问题作出正确判断和处理的能力。
制剂室和药检室的负责人不得互相兼任。
第九条从事制剂配制操作及药检人员,应经专业技术培训,具有基础理论知识和实际操作技能。
凡有特殊要求的制剂配制操作和药检人员还应经相应的专业技术培训。
第十条凡从事制剂配制工作的所有人员均应熟悉本规范,并应通过本规范的培训与考核。
第三章房屋与设施第十一条为保证制剂质量,制剂室要远离各种污染源。
周围的地面、路面、植被等不应对制剂配制过程造成污染。
第十二条制剂室应有防止污染、昆虫和其它动物进入的有效设施。
第十三条制剂室的房屋和面积必须与所配制的制剂剂型和规模相适应。
应设工作人员更衣室。
第十四条各工作间应按制剂工序和空气洁净度级别要求合理布局。
2023年执业药师之药事管理与法规过关检测试卷B卷附答案

2023年执业药师之药事管理与法规过关检测试卷B卷附答案单选题(共60题)1、国家基本医疗保险目录原则上每几年调整一次A.1年B.2年C.3年D.5年【答案】 B2、承担生物制品批签发相关工作的是A.国家药典委员会B.国家药品监督管理局总局药品评价中心C.国家药品监督管理部门药品审评中心D.中国食品药品检定研究院【答案】 D3、根据《药品注册管理办法》,下列药品批准文号格式符合规定的是A.国药证字H20160008B.国药准字S2*******C.国食药准字220163026D.国食药监字H20160085【答案】 B4、在人工作业的库房储存药品,按质量状态实行色标管理,已经超过药品有效期的应挂A.绿色标牌B.蓝色标牌C.红色标牌D.黄色标牌【答案】 C5、药品零售企业营业员A.应当具备执业药师资格B.应当具有药学或者医学、生物、化学等相关专业学历或者具有药学专业技术职称C.应当具有中药学中专以上学历或者具有中药学专业初级以上专业技术职称D.应当具有高中以上文化程度或者符合省级药品监督管理部门规定的条件【答案】 D6、(2020年真题)根据《麻醉药品和精神药品管理条例》邮寄时需要预先办理准予邮寄证明,托运时无需预先办理运输证明的精神药品是()A.阿托品B.咖啡因C.布桂嗪D.氯胺酮【答案】 B7、负责标定国家药品标准品的机构是A.中国食品药品检定研究院B.国家药典委员会C.省级药品监督管理部门D.国家中医药管理局E.国家药品监督管理部门【答案】 A8、根据《疫苗管理法》,关于疫苗上市许可和临床试验要求的说法,错误的是A.疫苗临床试验应当由符合国务院药品监督管理部门和国务院卫生健康主管部门规定条件的三级医疗机构或者省级以上疾病预防控制机构实施或者组织实施B.开展疫苗临床试验,应当取得受试者的书面知情同意,受试者为限制民事行为能力人的,只需要取得监护人的书面知情同意C.对疾病预防、控制急需的疫苗和创新疫苗,国务院药品监督管理部门应当予以优先审评审批D.国务院药品监督管理部门在批准疫苗注册申请时,对疫苗的生产工艺、质量控制标准和说明书、标签予以核准【答案】 B9、某药品批发企业经营范围中包括中药材、中药饮片和生物制品。
黑龙江省食品药品监督管理局关于印发《医疗机构制剂配制监督管理办法实施细则》的通知

黑龙江省食品药品监督管理局关于印发《医疗机构制剂配制监督管理办法实施细则》的通知文章属性•【制定机关】黑龙江省食品药品监督管理局•【公布日期】2010.06.03•【字号】黑食药监安发[2010]78号•【施行日期】2010.06.03•【效力等级】地方规范性文件•【时效性】现行有效•【主题分类】药政管理正文黑龙江省食品药品监督管理局关于印发《医疗机构制剂配制监督管理办法实施细则》的通知(黑食药监安发〔2010〕78号)各市(地)食品药品监督管理局:为了适应我省食品药品监管机构改革新形势,加强对医疗机构制剂配制质量的监督管理,依据《药品管理法》、《药品管理法实施条例》和《医疗机构制剂配制监督管理办法》等法律法规的相关规定,省局对省内医疗机构制剂配制监督管理的有关规范性文件和制度进行了重新梳理和调整,制定了《医疗机构制剂配制监督管理办法实施细则》,现予以发布,自发布之日起施行。
《关于部分调整开办药品生产企业或新增生产范围审批程序和〈药品生产许可证〉和〈医疗机构制剂许可证〉项目变更审批程序的通知》(黑食药监安发〔2004〕79号)、《关于调整医疗机构配制制剂审批、〈医疗机构制剂许可证〉核发及项目变更审批程序的通知》(黑食药监安发〔2004〕226号)和《关于印发〈黑龙江省医院类别医疗机构中药制剂委托配制管理办法(试行)〉的通知》(黑食药监安综〔2006〕181号)等文件同时废止。
黑龙江省食品药品监督管理局二〇一〇年六月三日医疗机构制剂配制监督管理办法实施细则第一章总则第一条为了适应我省机构改革新形势,明确办事程序,分清责权,加强对医疗机构制剂配制质量的监督管理,保证公众用药安全,依据《药品管理法》、《药品管理法实施条例》和《医疗机构制剂配制监督管理办法》等法律法规的相关规定,制定本细则。
第二条本细则适用于省内各级药品监督管理部门对辖区内各类医疗机构配制制剂的监督与管理。
第三条医疗机构制剂配制监督管理是指食品药品监督管理部门依法对医疗机构制剂配制条件和配制过程等进行审查、许可、检查的监督管理活动。
医疗机构制剂审批和调剂使用的规定

医疗机构制剂审批和调剂使用的规定
(1)《医疗机构制剂许可证》的审批:应当向所在地省、自治区、直辖市人民政府卫生行政部门提出申请,经审核同意后,报同级人民政府药品监督管理部门审批。
省、自治区、直辖市人民政府药品监督管理部门验收合格的,予以批准,发给《医疗机构制剂许可证》。
医疗机构终止配制制剂或者关闭的:《医疗机构制剂许可证》由原发证机关缴销。
(2)医疗机构配制制剂批准文号管理:必须经所在地省、自治区、直辖市人民政府药品监督管理部门批准,并发给制剂批准文号后,方可配制。
(3)医疗机构配制的制剂:不得在市场上销售或者变相销售,不得发布医疗机构制剂广告。
(4)医疗机构制剂的调剂规定:①发生灾情、疫情、突发事件或者临床急需而市场没有供应时;②经国务院或者省、自治区、直辖市人民政府的药品监督管理部门批准;③在规定期限内;④医疗机构配制的制剂可以在指定的医疗机构之间调剂使用;⑥国务院药品监督管理部门规定的特殊制剂的调剂使用以及省、自治区、直辖市之间医疗机构制剂的调剂使用,必须经国务院药品监督管理部门批准。
依照《中华人民共和国药品管理法实施条例》,医疗机构配制的制剂可以在指定的医疗机构之间调剂使用的是
a、发生灾情、疫情、突发事件
b、临床急需而市场没有供应
c、经国务院或省级药品监督管理部门批准
d、医疗机构之间协议调剂使用
e、在规定期限内。
《医疗机构制剂许可证》验收标准(1)

《医疗机构制剂许可证》验收标准
检查评定原则和方法
二、本标准设评定条款共93条。
其中设否决条款5条(条款号前加“** ”;重点条款17条(条款号前加“ * ”, 每条满
分为10分;一般条款71条,每条满分为5分。
三、各条款评分系数以达到该条款所要求的程度确定。
各条款评分系数规定如下:
①达到要求的系数为1;
②基本达到要求的系数为0.6 ;
③达不到要求的系数为0。
四、验收评定时,按配制制剂类别确定具体检查项目。
否决条款合格,且评分条款总得分率不低于60%为合格。
《医疗机构制剂许可证》验收标准实施细则
项。
医疗机构制剂许可证验收标准百度文库

《医疗机构制剂许可证》验收标准第一部分评定原则和方法1、根据《中华人民共和国药品管理法》及其实施办法制订本标准。
2、本标准设评定条款共 93条。
其中设否决条款 5条(条款号前加“**” ;重点条款 17条(条款号前加“*” ,每条满分为 10分;一般条款 71条,每条满分为 5分。
3、各条款评分系数以达到该条款所要求的程度确定。
各条款评分系数规定如下:①达到要求的系数为 1;②基本达到要求的系数为 0.6;③达不到要求的系数为 0。
4、验收评定时,按配制制剂类别确定具体检查项目。
否决条款合格,且评分条款总得分率不低于 60%为合格。
第二部分检查评定项目一、人员与机构:1、医疗机构应有由主管院长、药学部(药剂科、药局及制剂室、药检室等相关部门负责人组成的质量管理组织。
2、医疗机构的制剂室应直属药剂科领导,包括配制、检验两部分。
** 3、配制和药检负责人应具备大专以上药学学历 (或具有主管药师以上技术职称 , 熟悉药品管理法规,具有制剂和质量管理能力并对制剂质量负责。
* 4、医疗机构制剂室从事制剂技术工作的人员应具有药士或中专以上药学学历, 其他人员应具有高中以上文化程度并经培训合格持证上岗。
药学技术人员所占比例不得少于制剂人员总数的 50%。
5、灭菌制剂、普通制剂与中药制剂应配有相应专业的药学技术人员。
6、药检室检验人员应由药师或大专以上药学学历的技术人员担任并要保持相对稳定。
7、从事灯检工作的人员裸眼视力应在 0.9以上,无色盲。
8、制剂和药检负责人变更时应 30天内报所在地药品监督管理部门备案。
9、应制订年度人员培训计划,对各类人员进行《药品管理法》、及技术培训,每年至少考核一次,并有考核记录备存。
二、厂房与设施:10、制剂室周围环境必须保证制剂质量的要求,距制剂室 30米以内不得有公厕、锅炉房、太平间、传染病房、动物房以及其他污染源, 10米以内不得有露土地面,外部环境要保持清洁。
11、制剂室内墙壁、顶棚、地面应平整、光洁,不得有脱落物和缝隙,应耐受清洗和消毒。
2023年执业药师《药事管理与法规》考试全真模拟易错、难点汇编贰(答案参考)试卷号:43

2023年执业药师《药事管理与法规》考试全真模拟易错、难点汇编贰(答案参考)(图片大小可自由调整)一.全考点综合测验(共50题)1.【单选题】根据《化学药品和治疗用生物制品说明书规范细则》说明书【药品名称】项中所列顺序正确的是A.通用名称、汉语拼音、商品名称、英文名称B.通用名称、商品名称、英文名称、汉语拼音C.通用名称、商品名称、汉语拼音、英文名称D.通用名称、,英文名称、商品名称、汉语拼音E.商品名称、通用名称、英文名称、汉语拼音正确答案:B2.【单选题】外配处方必须由A.定点医疗机构医师开具B.定点零售药店执业药师开具C.定点医疗机构的临床药师开具D.个体诊所医师开具正确答案:A3.【单选题】在城乡集市贸易市场设点销售的药品超出批准经营的药品范围的A.按从无证企业购进药品处罚B.按无证经营处罚C.按经营假药处罚D.按经营劣药处罚正确答案:B4.【单选题】药品的特殊性之一体现在A.药品生产、销售、使用消费遵循市场规律B.属于经济性商品C.消费者低选择性D.属于竞争性商品E.需求平衡性正确答案:C5.【多选题】GMP的适用范围为A.无菌制剂生产的全过程B.注射液生产的全过程C.片剂生产的全过程D.胶囊剂生产的全过程E.外用药品生产的全过程正确答案:ABCDE6.【单选题】根据《医疗机构制剂配制质量管理规范( 试行)》,制剂使用过程中发现的不良反应,应按规定予以记录,且保留病历和有关镎验、检查报告单等原始记录备查,原始记录的最短保存期限为A.1年B.2年C. 3年D.4年E.5年正确答案:A7.【单选题】《中华人民共和国药品管理法实施条例》规定生产注射剂的药品生产企业的GMP认证A.国务院质量技术监督管理部门负责B.国务院卫生行政部门负责C.国务院药品监督管理部门负责D.省级人民政府药品监督管理部门负责E.省级人民政府卫生行政部门负责正确答案:C8.【单选题】根据《中华人民共和国药品管理法》,药品监督管理部门批准开办药品经营企业,除应具备规定的开办条件外,还应遵循的原则是A.市场调节、方便群众购药B.合理布局、保证质量C.合理布局、方便群众购药D.品种齐全、诚实信用E.公平合理、救死扶伤正确答案:C9.【单选题】根据《中华人民共和国药品管理法实施条例》,实行政府定价或政府指导价的药品是A.列入国家基本医疗保险药品目录的药品B.列入国家基本药物目录的药品C.列入中华人民共和国药典的药品D.刿入国家基本医疗保险药品目录以外生产和经营的常用药品E.列入国家基本药物目录以外生产和经营的具有垄断性药品正确答案:E10.【单选题】根据《药品经营质量管理规范》,关于药品批发企药品收货与验收的说法,错误的是A.实施批签发管理的生物制品,抽样验收时可不开箱检查B.对包装异常、零货、拼箱的药品,抽样验货时应当开箱检查至最小包装C.冷藏、冷冻药品如在阴凉库待验,应尽快进行收货验货,验收合格尽快送入冷库D.冷藏、冷冻药品到货时,应当查验运输方式及运输过程的温度记录、运输时间等质量控制状况,不符合温度要求的应当拒收正确答案:C11.【单选题】根据《进口药材管理办法(试行)》,《进口药材批件》分一次性有效批件和多次使用批件。
2022-2023年执业药师之药事管理与法规考前冲刺模拟试卷B卷含答案

2022-2023年执业药师之药事管理与法规考前冲刺模拟试卷B卷含答案单选题(共50题)1、急诊科医师开具的盐酸肾上腺素注射液处方,一般每张处方限量为A.3日常用量B.15日常用量C.一次常用量D.7日常用量【答案】 A2、药品标签使用注册商标的,应当A.不得分行书写B.不得同行书写C.印刷在边角D.印制在首页左上角【答案】 C3、行政机关对不履行行政决定的公民法人或者其他组织可采取的行政强制执行方式是()A.责令组织听证B.划拨存款、汇款C.责令停产停业D.查封场所、设施或者财物【答案】 B4、(2018年真题)某药厂生产的诺氟沙星胶囊所用原料被污染该诺氟沙星胶囊应()A.按假药论处B.认定为劣药C.按劣药论处D.认定为假药【答案】 B5、从事下列活动,无需取得行政许可的事项是A.种植中药材B.开办药品零售企业C.开办药品批发企业D.开办药品生产企业【答案】 A6、必须由具有蛋白同化制剂、肽类激素定点批发资质的药品批发企业从事批发业务的产品是()A.药品类易制毒化学品B.含麻黄碱类复方制剂C.第三类易制毒化学品D.含可待因复方口服液体制剂【答案】 B7、某医疗机构药师收到四张处方,逐一进行审核:第一张是为门诊患者开具的含有磷酸可待因片的处方,第二张是为门诊癌症疼痛患者开具的含有硫酸吗啡控释片的处方,第三张是为门诊患者开具的含有地西泮片的处方,第四张是为住院患者开具的含有盐酸二氢埃托啡的处方。
A.为门诊患者开具的含有磷酸可待因片的处方B.为门诊癌症疼痛患者开具的含有硫酸吗啡控释片的处方C.为门诊患者开具的含有地西泮片的处方D.为住院患者开具的含有盐酸二氢埃托啡的处方【答案】 C8、根据《医疗机构制剂配制监督管理办法(试行)》,属于《医疗机构制剂许可证》许可事项变更的是A.医疗机构名称变更B.医疗机构类别变更C.法定代表人变更D.制剂室负责人变更【答案】 D9、中药二级保护品种的最低保护年限是A.30年B.7年C.20年D.10年【答案】 B10、应当分柜摆放A.生产企业将药品的警示语或忠告语醒目地印制在B.非处方药警示语或忠告语为C.处方药和非处方药D.非处方药【答案】 C11、在药品经营企业执业的执业药师,去药品生产企业执业的应办理A.注销注册B.首次注册C.延续注册D.变更注册【答案】 D12、《处方管理办法》属于A.法律B.行政法规C.地方性法规D.部门规章【答案】 D13、(2021年真题)根据国务院办公厅《关于改革完善仿制药供应保障及使用政策的意见》,关于仿制药供应保障及使用配套支持政策的说法,错误的是A.促进“临床必需、疗效确切、价格合理”的仿制药研发,鼓励仿制重大传染病防治和罕见病治疗所需药品B.药品集中采购机构要按照药品通用名编制采购目录,及时将符合条件的仿制药纳入采购目录范围C.将与原研药质量和疗效一致的仿制药纳入与原研药可以相互替代的药品目录,在说明书、标签中予以标注D.加快制定医保药品支付标准,原研药、与原研药质量和疗效一致的仿制药按照相同标准支付【答案】 A14、列出需要慎用的情况(如肝、肾功能的问题)的说明书项目是A.【禁忌】B.【注意事项】C.【不良反应】D.【成分】【答案】 B15、某医疗机构拟从某药品批发企业购进一种以前从未购进过的抗菌药物。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
《医疗机构制剂许可证》验收标准
检查评定原则和方法
一、根据《中华人民共和国药品管理法》及其实施办法制订本标准。
二、本标准设评定条款共93条。
其中设否决条款5条(条款号前加“**”);重点条款17条(条款号前加“*”),
每条满分为10分;一般条款71条,每条满分为5分。
三、各条款评分系数以达到该条款所要求的程度确定。
各条款评分系数规定如下:
①达到要求的系数为1;
②基本达到要求的系数为0.6;
③达不到要求的系数为0。
四、验收评定时,按配制制剂类别确定具体检查项目。
否决条款合格,且评分条款总得分率不低于60%为合格。
《医疗机构制剂许可证》验收标准实施细则
(
项。
