土壤中全钾、全磷标准曲线
土壤中各种钾的测定

6.1概述土壤中全钾的含量(K,g·kg-1)一般在16.1g·kg-1左右,高的可达24.9~33.2g·kg-1,低的可低至0.83~3.3g·kg-1。
在不同地区、不同土壤类型和气候条件下,全钾量相差很大。
如华北平原除盐渍化土外,全钾为18.2~21.6g·kg-1,西北黄土性土壤为14.9~18.3 g·kg-1,到了淮河以南,土壤中钾的含量变化十分悬殊。
如安徽南部山地钾含量为9.9~33.2g·kg-1,广西为5.0~24.9g·kg-1,海南岛为0.83~32.4g·kg-1。
由此可以看出华北、西北地区钾的含量变幅较小,而淮河长江以南则较大。
这是因为华北、西北地区成土母质均一和气候干旱,而淮河长江以南成土母质不均一和气候多雨有关。
此外,土壤全钾量与粘土矿物类型有密切关系。
一般来说2:1型粘土矿物较1:1型粘土矿物为高,特别是伊利石(一系列水化云母)高的土壤钾的含量较高。
土壤中钾主要成无机形态存在。
按其对作物有效程度划分为速效钾(包括水溶性钾、交换性钾)、缓效性钾和相对无效钾三种。
它们之间存在着动态平衡,调节着钾对植物的供应。
按化学形态分:非交换性钾(层间钾)水溶性钾→非交换性钾Ⅰ→非交换性钾Ⅱ→非交换性钾Ⅲ……→矿物钾按植物有效性分[2]:速效钾→相对无效钾L-1热HNO3植物有效性降低土壤中钾主要成矿物的结合形态,速效性钾(包括水溶性钾和交换性钾)只占全钾的1%左右。
交换性钾(K)含量从小于一百m g·kg-1到几百m g·kg-1,而水溶性钾只有几个m g·kg-1。
通常交换性钾包括水溶性钾在内,这部分钾能很快地被植物吸收利用,故称为速效钾。
缓效钾或称非交换性钾(间层钾),主要是次生矿物如伊利石、蛭石、绿泥石等所固定的钾。
我国土壤缓效钾的含量,一般在40~1400m g·kg-1,它占全钾的1%~10%。
植株全氮、全磷、全钾的测定

植株全氮、全磷、全钾的测定一、待测液的制备(H2SO4—H2O2消煮法)二、植株全氮的测定(H2SO4—H2O2消煮,蒸馏法)三、植株全磷的测定(H2SO4—H2O2消煮,钒钼黄比色法)四、植株全钾的测定(H2SO4—H2O2消煮,火焰光度法一、待测液的制备(H2SO4—H2O2消煮法)1 H2SO4—H2O2消煮原理植物样品在浓H2SO4溶液中,经过脱水、碳化、氧化等一系列的作用后,易分解的有机物则分解,然后再加入H2O2,H2O2在热的浓H2SO4溶液中会分解出新生态氧,具有强烈的氧化作用,可继续分解没被H2SO4破坏的有机物,使有机态氮全部转化为无机铵盐。
同时,样品中的有机磷也转化为无机磷酸盐,故可用同一消煮液分别测定N、P、K(植株中K以离子态存在)。
2 主要仪器:万分之一电子天平、0.5 mm筛、三角瓶(50ml)或消煮管、移液管(5、10ml)+吸耳球、弯颈小漏斗、消煮炉、吸管、漏斗、无磷钾滤纸、容量瓶(100ml)2 试剂:浓硫酸(GB T625):化学纯、比重1.8430%H2O2(GB 6684):阴凉处存放3 操作步骤称取烘干、磨细的植物样品(过0.5 mm筛)0.19g,置于50ml三角瓶(或消煮管)底部(勿将样品粘附在瓶颈上),加浓硫酸5mL,摇匀(最好放置过夜),瓶口盖一弯颈小漏斗,在电炉上先缓缓加热,待浓硫酸分解冒大量白烟时再升高温度(在消煮炉上先250℃消煮—温度稳定后计时,时间约30min,待浓硫酸分解冒大量白烟时再升高温度至400℃)。
消煮至溶液呈均匀的棕黑色时,取下三角瓶,稍冷后提起弯颈漏斗,滴加30%H2O210滴,并不断摇动三角瓶。
再加热(微沸)约7-10 min,取下,稍冷后重复滴加30%H2O25~10滴,再消煮。
如此反复进行3-5次,每次添加的H2O2应逐次减少,消煮至溶液呈无色或清亮后,再加热5-10min(以赶尽剩余的H2O2),取下三角瓶冷却,用少量水冲洗漏斗,洗液流入三角瓶中。
土壤指标全氮全磷全钾有机质速效磷速效钾解性氮PH

土壤指标全氮全磷全钾有机质速效磷速效钾解性氮PH 土壤是一个复杂的生态系统中的重要组成部分,它对植物生长和健康有着重要的影响。
土壤指标是用来评估土壤质量和肥力的重要参数,其中包括全氮、全磷、全钾、有机质、速效磷、速效钾、解性氮以及pH值等。
全氮是指土壤中的总氮含量,包括有机氮和无机氮。
全氮是植物生长所需的重要营养元素之一,对植物的生长和发育起着重要的促进作用。
全氮含量过低会导致植物生长不良,而过高则可能引发环境问题。
全磷是土壤中的总磷含量,包括有机磷和无机磷。
磷是植物生长过程中必需的营养元素之一,对于植物的根系发育、开花和结果等方面起着重要的作用。
过低的全磷含量会限制植物的生长,而过高则可能造成环境污染。
全钾是土壤中的总钾含量,包括土壤固定态和交换态的钾。
钾是植物生长所需的重要营养元素之一,对植物生长和发育起着重要的调节作用。
适量的全钾含量可以促进植物的健康生长,但过低或过高的全钾含量都会影响植物的生长和产量。
有机质是指土壤中含有的易于分解的有机物质,包括植物残体、动物残体和微生物产物等。
有机质是土壤中的重要组分之一,对土壤水分保持、养分保持和微生物活动等方面起着重要的作用。
适量的有机质含量有助于改善土壤质地和肥力,提高土壤保水保肥的能力。
pH值是土壤的酸碱度指标,反映了土壤中水解离态阳离子和阴离子的活性。
适宜的pH值有助于提供植物生长所需的适宜环境条件,影响土壤中营养元素的有效性和植物对营养元素的吸收利用能力。
综上所述,全氮、全磷、全钾、有机质、速效磷、速效钾、解性氮以及pH值等土壤指标对土壤质量和植物生长有着重要的影响。
合理评估和管理这些土壤指标,有助于提高土壤肥力和植物生长的效果。
土壤基本指标检测

1 有机质的测定(重铬酸钾外加热法)试剂1、0.2mol/L的FeSO4溶液:称56.0g FeSO4(化学纯)溶于1L水,再ml浓硫酸。
2、重铬酸钾-浓硫酸混合液:称39.23g(通常可直接称40g),加1L水溶解,再加1L浓硫酸。
(为防止结晶,经验是400L水溶解重铬酸钾,用600ml水稀释浓硫酸,再混合)。
3、邻啡啰啉指示剂:1.485g邻啡啰啉+0.695gFeSO4溶于100mL水里,储存在棕色瓶中。
4、Ag2SO4防止氧化物(C-)的干扰,约加0.1g左右。
(石灰土壤一般不用)。
5、重铬酸钾标准液的配制:39.2245g重铬酸钾(分析纯)加400ml水,加热溶解,定容1L.设备:消煮炉、消煮管、万分之一天平、2L大烧杯、大储存瓶、瓶口分液器(10ml)、酸式滴定管、三角瓶、洗瓶实验步骤:1、称0.1000-0.5000g (0.25mm) 土样至消煮管,加入10ml重铬酸钾-浓硫酸混合液,摇匀。
2、放入消煮炉(190℃)沸5min。
3、完全转移至三角瓶中,加入邻啡罗啉指示剂3~4滴,用硫酸亚铁滴定。
注意:滴至快终点时用洗瓶洗壁,减少误差。
每批样3空白。
每天对FeSO4标定一次。
(标定方法:0.2000g重铬酸钾溶于50-70ml水+5ml浓硫酸+邻啡啰啉指示剂)计算公式:方法1: C FeSO4=(标准重铬酸钾质量/M重铬酸钾)*6*5/消耗FeSO4体积5:表示每次吸重铬酸钾标准液方法2: C FeS04=0.2000/ (消耗FeSO4体积*0.04904) ppm有机质(g/Kg) ={CFeSO4*(V0-V)*10-3*3*1.1*1.724*1000}/样重加Ag2SO4时,校正系数变为1.04。
(1.1为氧化校正系数)两次平行允许误差<0.5g/kg2有效磷(碳酸氢钠浸提一硫酸钼锑抗比色法)试剂:1、4mol/L NaOH:4g NaOH+25ml 水2、0.5mol/L NaHCO3浸提剂:42g NaHCO3+1L水,用4mol/L NaOH调pH≈8.53、稀硫酸溶液:153ml浓硫酸+400ml水,待其冷却4、5g/L酒石酸锑钾溶液: 0.5g酒石酸锑钾+100ml水5、6.5mol/L钼铁抗存储液:将硫酸溶液缓缓倒入700ml蒸馏水中+10g钼酸铵,冷却后,加入100ml 5g/L的酒石酸锑钾溶液,总体积定容1L,存储于棕色瓶中,可以长期保存。
土壤全钾的测定实验方法

土壤全钾的测定实验方法一、目的意义钾素是植物生长所需要的养分之一,近年来,随着复种指数的增加和单位面积产量的提高。
在我国某些地区,施用钾肥已成为夺取高产的措施之一。
钾在土壤中以各种矿物及盐类的状态存在,其中绝大部分不能被植物吸收利用。
植物只能吸收土壤中的水溶性钾。
为了判断土壤肥力,测定土壤钾素的含量是有重要意义的。
二、方法原理样品的分解有碳酸钠碱熔法,氢氟酸-高氯酸法,碳酸钙一氯化钱法,这些方法各有优缺点。
如碳酸钠碱法制备的待测液可用于全磷,全钾的测定和其它元素的测定,但需用柏钳锅,受到条件限制。
若单独测定全钾则无此必要,氢氟酸-高氯酸法亦需用铝钳锅,但目前已经可用塑料钳锅代替,所制备的待测液也可同时测定多种元素,而且溶液中杂质较少,有昨于各种元素的分析,但结果偏低,同时对钳锅的腐蚀性大。
氢氧化钠碱熔法提取完全,可采用银、银、铁钳锅,是适用于一般实验室的较好方法。
同时所制备的同一待测液可以测定全磷和全钾。
本实验着重介绍氢氧化钠碱熔-火焰光度计测定法。
用NaOH熔融土壤,增加盐基成分,促进硅铝酸盐的分解,以利于各种元素的溶解。
面成为含K+的碱性待测液。
将此待测液置于火焰光度计上,用压缩空气使火焰喷成雾状,与乙快或其它可燃气体混合燃烧,溶液中的钾离子则发射特定波长的光,用滤光片分离选择后,由光电流将火焰发出的光能变成光电流,再由检流计量出光电流的强度。
光电流的强度与溶液的含钾量成正相关。
再从同样条件下测定的标准液所作的曲线上查出相对应的浓度而计算出未知溶液含钾量。
三、操作步骤称取通过0.25mm孔筛的风干土样或烘干样品0.3000g,于银钳锅底部(切勿粘在壁上)。
用95%酒精稍湿润样品,加2g固体氢氧化钠于钳锅的土壤面上,铺平。
暂时放于大干燥器中,以防止吸水潮解。
同时做空白试验。
将钳锅加盖留一缝隙,放在高温电炉内,由低温升至720℃并保持15分钟,取出冷却。
加IonII左右蒸储水,在电炉上加热至80°C左右,熔块熔解后,再煮沸5分钟,然后将钳锅内的溶液用漏斗转入50ml容量瓶中,用5ml左右蒸储水,2ml9N硫酸和少量蒸储水依次洗涤钳锅并倒入容量瓶中。
土壤中磷的测定(全磷、速效磷)

1土壤全磷的测定(硫酸一高氯酸消煮法)方法原理在高温条件下,土壤中含磷矿物及有机磷化合物与高沸点的硫酸和强氧化剂高氯酸作用,使之完全分解,全部转化为正磷酸盐而进入溶液,然后用钼锑抗比色法测定。
操作步骤1.在分析天平上准确称取通过100目筛(孔径为0.25mm)的土壤样品1g(精确到0.0001)置于50ml三角瓶中,以少量水湿润,并加入浓H2SO48ml,摇动后(最好放置过夜)再加入70—72%的高氯酸(HClO4)10滴摇匀。
2.于瓶口上放一小漏斗,置于电炉上加热消煮至瓶内溶液开始转白后,继续消煮20分钟,全部消煮时间约为45—60分钟。
3.将冷却后的消煮液用水小心地洗入100ml容量瓶中,冲冼时用水应少量多次。
轻轻摇动容量瓶,待完全冷却后,用水定容,用干燥漏斗和无磷滤纸将溶液滤入干燥的100ml三角瓶中。
同时做空白试验。
4.吸取滤液2—10ml于50ml容量瓶中,用水稀释至30ml,加二硝基酚指示剂2滴,用稀氢氧化钠(NaOH)溶液和稀硫酸(H2SO4)溶液调节pH至溶液刚呈微黄色。
5.加入钼锑抗显色剂5ml,摇匀,用水定容至刻度。
6.在室温高于15℃的条件下放置30分钟后,在分光光度计上以700nm的波长比色,以空白试验溶液为参比液调零点,读取吸收值,在工作曲线上查出显色液的P—mg/L数。
7.工作曲线的绘制。
分别吸取5mg/L标准溶液0,1,2,3,4,5,6ml于50ml 容量瓶中,加水稀释至约30ml,加入钼锑抗显色剂5ml,摇匀定容。
即得0,0.1,0.2,0.3,0.4,0.5,0.6,mg/LP标准系列溶液,与待测溶液同时比色,读取吸收值。
在方格坐标纸上以吸收值为纵坐标,Pmg/L数为横坐标,绘制成工作曲线。
结果计算全P %=显色液mg/L×显色液体积×分取倍数/(W×106)×100式中:显色液Pmg/L—从工作曲线上查得的Pmg/L;显色液体积—本操作中为50ml;分取倍数—消煮溶液定容体积/吸取消煮溶液体积;106—将ug换算成gW—土样重(g)。
土壤全磷、速效磷、速效钾含量,植物组织全磷、全氮含量快速测试方法
离心替代过滤,酶标仪替代分光光度计的土壤全磷测试方法1.用万分之一天平,称取1g左右的风干土,记录下重量。
2.加入8ml浓硫酸,放置过夜后加入10滴高氯酸,消煮至白色。
3.在50ml消煮管中定容,可以先加水1/3,混匀后再加水至刻度线附近,放置过夜后再加水至刻度线,摇匀。
4.吸取1ml消煮液到1.5ml离心管中,10000rpm,离心1分钟。
5.吸取50ul上清液+750ul H2O+100ul NaOH(4mol/L,16g NaOH定容到100ml)+100ul钼锑抗试剂到1.5ml离心管中。
6.摇匀后,14000rcf离心一分钟,室温高于15℃情况下,30min后,吸取300ul至酶标板比色备注:5.中吸取的上清液的量可根据显色状况调整,相应地NaOH的量也要做出调整,保证比色体系体积为1ml,氢离子浓度为0.55mol/L左右,每个样品做三个重复,重复间允许误差<0.005%即50mg/kg。
磷酸二氢钾工作曲线制做方法1.先将100mg/L(0.4394g KH2PO4(烘干2小时)先加水300ml,再加5ml浓硫酸,再定容到1L)的磷标贮液(磷酸二氢钾溶液)稀释20倍,比如吸取5ml定容到100ml2.配制3.摇匀后,10000rpm离心一分钟,室温高于15℃情况下,30min后,吸取300ul至酶标板比色备注:利用散点图绘制曲线,添加趋势线和r值,r^2要大于0.999。
利用forecast.line函数计算比色液磷含量钼锑抗配制方法1.浓硫酸153ml加入500ml左右H2O(用1L的烧杯),用磁力搅拌器搅匀2. 1L烧杯中加入10g 钼酸铵,用磁力搅拌器融化3. 0.5g酒石酸锑钾加入100ml左右H2O(用100ml的烧杯),用磁力搅拌器溶化4. 步骤3所得溶液倒入1L烧杯,在磁力搅拌器上混合均匀,定容到1L备注:避光储存,使用时每10ml 加入0.15g抗坏血酸二硝基酚溶液:0.2g 二硝基酚溶于100ml水中离心替代过滤,酶标仪替代分光光度计的土壤有效磷(碳酸氢钠浸提)测定方法1. 42g碳酸氢钠定容到1L,用4mol/L NaOH溶液(4mol/L,16g NaOH定容到100ml)调节pH至8.5,得到浸提剂2. 1.00g风干土加入50ml塑料管中,再加入0.1g活性炭粉,再加入20ml碳酸氢钠溶液,20~25℃,180rpm,震荡30min3.吸取1ml浸提液到1.5ml离心管中,10000rpm,离心1分钟4.吸取200ul上清液+700ul H2O+100ul钼锑抗试剂到1.5ml离心管中5.摇匀后,14000rcf,离心一分钟,室温高于15℃情况下,30min后,吸取300ul至酶标板比色备注:吸取的上清液体积可以根据显色情况调整,保证比色体系1ml,每个样品做三个重复植物组织全磷含量快速测定1.将烘干后的植物组织样品磨碎,再将样品粉末继续烘干至恒重。
土壤基本指标测定方法

吸取消化液10mL于反应瓶中,加入2mL 300g/L的氯化亚锡溶液,立 即盖上瓶塞,接测汞仪,记下电流表上显示的最大峰值。
标准曲线的绘制:取0.1mL100μg/mL的汞标准溶液加入10mL的硝酸重铬酸钾溶液稀释成0.1μg/mL的汞标准溶液。再分别吸取0、2、 4、6、8、10此标准溶液于6个反应瓶中,用1mol/L硫酸溶液补足至 10mL,按试液测定步骤操作,与试液同条件测定,读取吸收值,绘 制标准曲线。 (2)试剂 50g/L高锰酸钾溶液:称取5g高锰酸钾,溶于1mol/L硫酸溶液中,稀 释至100mL; 300g/L氯化亚锡溶液:称取30g氯化亚锡加热溶于5mL浓盐酸中,用 去离子水稀释至100mL,临用时配制,放置半天后使用;
酸钾标液浓度,V为硫酸亚铁体积)
(2)试剂
K2Cr2O7溶液:称取重铬酸钾20g溶于水中,加入500mL浓硫酸,再加
水定容于1000mL容量瓶中。
0.2mol/L
FeSO4溶液:称取硫酸亚铁37.0g溶于水中,加浓硫酸
20mL,稀释至1L。
邻菲罗啉指示剂:称取邻菲罗啉1.5g和硫酸亚铁0.7g溶于100mL水
计算:硫酸根离子(mg/kg)=C*25/m C是样品中硫酸根离子在标准曲线上的浓度(ug/mL),m是称取土壤 的质量(g)。 7、 有效硼的测定(甲亚铵法)
(1)操作步骤 称取5g土壤(2mm筛土壤)于离心管中,加入20mL水,沸水浴
5min,然后过滤到 离心管中,再吸取4mL到离心管中,加入缓冲液10mL和5mL甲亚铵显
1、 pH测定方法(电位测定法) 称取通过2mm筛孔的风干土10g,放在50mL的烧杯中,加入25mL去 离子水,间歇搅拌或摇动30min,放置30min后用pH计测定,记录pH 计测定的pH值。 2、 全N、P、K测定方法 (1)操作步骤 取通过0.25mm筛孔的风干土0.5g,加入5mL的H2SO4和0.1mL的 HClO4,煮到白色为止,直接转移到50mL容量瓶后分别取样测定N、 P、K。同时还有两个空白实验。 全K:取0.5mL到25mL的容量瓶中,定容到25mL,用原子吸收测定, 全N:取25mL到凯氏瓶中,加40%NaOH15mL,用硼酸液吸收溜出液 约50mL,蒸馏完毕,用标准酸滴定, 全P:取1mL到25mL容量瓶,加二硝基酚指示剂2滴,用4mol/L的 NaOH调pH,至溶液微黄后加钼锑抗试剂2.5mL,定容,放置30min, 700nm比色。 绘制P的校准曲线:分别准确称取5mg/L的P标准溶液0、2、4、6、 8、10mL于25mL容量瓶中,其他操作如上述测P的步骤一样。 (2)试剂 40% NaOH:40gNaOH溶于100mL的水中; 硼酸液:20g的H2BO3溶于1L水中,每升H2BO3溶液中加入甲基红-溴 甲酚绿混合指示剂5mL并用稀酸或稀碱调节至微红色,此时溶液的 pH为4.8。 0.02mol/L(1/2H2SO4)标准溶液:量取H2SO4分析纯2.83mL,加水稀 释至5000mL,然后用硼砂标定。 0.01 mol/L(1/2H2SO4)标准溶液:用0.02mol/L(1/2H2SO4)标准溶 液准确稀释一倍。
土壤全磷——精选推荐
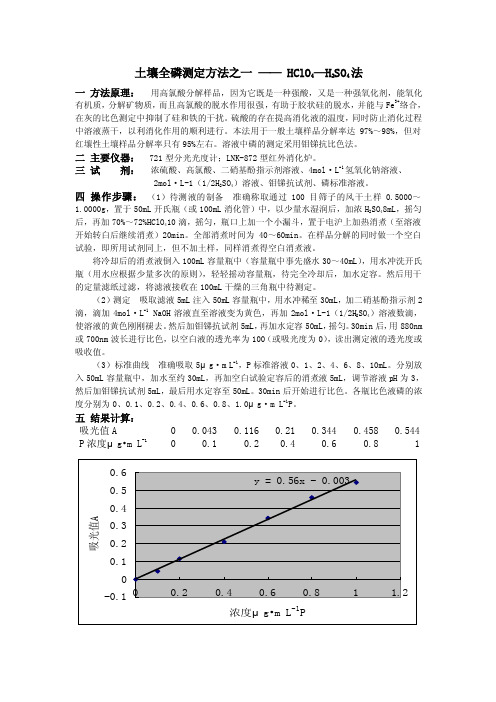
土壤全磷测定方法之一—— HClO4—H2SO4法一方法原理:用高氯酸分解样品,因为它既是一种强酸,又是一种强氧化剂,能氧化有机质,分解矿物质,而且高氯酸的脱水作用很强,有助于胶状硅的脱水,并能与Fe3+络合,在灰的比色测定中抑制了硅和铁的干扰。
硫酸的存在提高消化液的温度,同时防止消化过程中溶液蒸干,以利消化作用的顺利进行。
本法用于一般土壤样品分解率达97%~98%,但对红壤性土壤样品分解率只有95%左右。
溶液中磷的测定采用钼锑抗比色法。
二主要仪器: 721型分光光度计;LNK-872型红外消化炉。
三试剂:浓硫酸、高氯酸、二硝基酚指示剂溶液、4mol·L-1氢氧化钠溶液、2mol·L-1(1/2H2SO4)溶液、钼锑抗试剂、磷标准溶液。
四操作步骤:(1)待测液的制备准确称取通过100目筛子的风干土样0.5000~1.0000g,置于50mL开氏瓶(或100mL消化管)中,以少量水湿润后,加浓H2SO48mL,摇匀后,再加70%~72%HClO410滴,摇匀,瓶口上加一个小漏斗,置于电沪上加热消煮(至溶液开始转白后继续消煮)20min。
全部消煮时间为40~60min。
在样品分解的同时做一个空白试验,即所用试剂同上,但不加土样,同样消煮得空白消煮液。
将冷却后的消煮液倒入100mL容量瓶中(容量瓶中事先盛水30~40mL),用水冲洗开氏瓶(用水应根据少量多次的原则),轻轻摇动容量瓶,待完全冷却后,加水定容。
然后用干的定量滤纸过滤,将滤液接收在100mL干燥的三角瓶中待测定。
(2)测定吸取滤液5mL注入50mL容量瓶中,用水冲稀至30mL,加二硝基酚指示剂2滴,滴加4mol·L-1 NaOH溶液直至溶液变为黄色,再加2mol·L-1(1/2H2SO4)溶液数滴,使溶液的黄色刚刚褪去。
然后加钼锑抗试剂5mL,再加水定容50mL,摇匀。
30min后,用880nm 或700nm波长进行比色,以空白液的透光率为100(或吸光度为0),读出测定液的透光度或吸收值。
土壤农化分析常用化指标测定方法【精选】

土壤农化分析常用指标测定方法土壤有机质测定一、原理170~180℃条件下,用一定浓度的K2Cr2O7-H2SO4溶液(过量)氧化土壤有机质,剩余的K2Cr2O7用FeSO4滴定,由消耗的K2Cr2O7量计算出有机碳量,再乘以常数1.724,即为土壤有机质含量。
其反应式如下:K2Cr2O7与有机碳反应K2Cr2O7+8 H2SO4+3C→2Cr2(SO4)3+3CO2+8H2O过量的K2Cr2O7与FeSO4的滴定反应K2Cr2O7+4FeSO4+7 H2SO4→K2SO4+Cr2(SO4)3+3Fe2(SO4)3+7H2O二、试剂1、0.4mol/L(K2Cr2O7-浓H2SO4)标准溶液:称取经130℃烘干的K2Cr2O7(AR)39.2245g61溶于水中,加热溶解后加入1000mL浓H2SO4定容至2000mL。
2、0.2mol/L FeSO4溶液:称取FeSO4(AR)56g溶于水中,加浓硫酸5mL,稀释至1L。
3、石英砂:粉末状。
三、实验步骤称取<0.25mm风干土0.5×××~1.0×××g于干燥试管中。
加入少量水润湿样品,准确沿避缓慢加入10.0mL K2Cr2O7-H2SO4混合液,摇分散土样,加入小漏斗,放入铁丝笼中。
将铁丝笼放入已开启185~190℃油浴锅中(使温度在170~180℃)沸腾准确5分钟;取出稍冷,擦净试管外壁油污(同时做空白实验);冷却后把溶液全部转移到200~250mL三角瓶中(最后体积控制在60~70mL),加入指示剂3滴,用已知浓度的FeSO4滴定。
四、结果计算有机质()100724.11.1100.3%30⨯⨯⨯⨯⨯⨯-=-WcVV式中:V0——滴定空白所用的FeSO4溶液的体积(mL);V——滴定样品所用的FeSO4溶液的体积(mL);c——0.2mol/L FeSO4溶液准确浓度;3.0——1/4碳原子的摩尔质量(g/mol);10-3——将mL换算为L;1.1——氧化校正系数;1.724——土壤有机碳换算成土壤有机质的平均换算系数。
磷标准曲线的绘制

磷标准曲线的绘制磷是植物生长中必不可少的营养元素,对于土壤中的磷含量的准确测定对于农业生产和土壤环境保护都有着重要的意义。
而磷标准曲线的绘制则是进行磷含量测定的重要步骤之一。
下面将介绍如何绘制磷标准曲线。
首先,我们需要准备一定浓度的磷标准溶液。
通常情况下,我们会选择含有不同浓度磷的标准溶液,以便后续的测定。
接着,我们需要准备一定数量的试管或烧杯,将不同浓度的磷标准溶液分别加入试管或烧杯中。
然后,我们需要选择一种适合的磷检测方法。
常见的磷检测方法包括分光光度法、原子荧光光谱法等。
在选择检测方法的同时,我们需要根据实际情况确定合适的检测波长和仪器参数。
接下来,我们将分别对不同浓度的磷标准溶液进行检测,并记录下各自的吸光度值。
在进行吸光度测定时,我们需要注意保持仪器的稳定性,避免外界因素对测定结果的影响。
在完成吸光度测定后,我们将各个浓度点的吸光度值绘制成曲线图。
通常情况下,我们会选择将吸光度值作为纵坐标,浓度值作为横坐标,绘制出磷标准曲线。
在绘制曲线图时,我们需要保证曲线的平滑性和连续性,以便后续的测定和计算。
最后,我们需要对磷标准曲线进行验证和修正。
在验证曲线的过程中,我们可以选择一些已知浓度的磷溶液进行检测,以验证曲线的准确性和可靠性。
如果发现曲线存在偏差或不连续的情况,我们需要及时对曲线进行修正,以确保后续的磷含量测定能够得到准确的结果。
综上所述,磷标准曲线的绘制是进行磷含量测定的重要步骤之一。
通过准备标准溶液、选择合适的检测方法、进行吸光度测定和绘制曲线图,我们可以得到准确可靠的磷含量测定结果,为农业生产和土壤环境保护提供有力的支持。
土壤中全磷、全钾及氟化物的测定 氢氧化钠熔融法

土壤中全磷、全钾及氟化物的测定氢氧化钠熔融法1 范围本文件规定了氢氧化钠熔融法测定土壤中全磷、全钾及氟化物的方法。
本文件适用于土壤中全磷、全钾及氟化物的测定。
2 规范性引用文件下列文件中的内容通过文中的规范性引用而构成本文件必不可少的条款。
其中,注日期的引用文件,仅该日期对应的版本适用于本文件;不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
GB/T 603 化学试剂试验方法中所用制剂及制品的制备GB/T 6682 分析实验室用水规格和试验方法GB/T 22104 土壤质量氟化物的测定离子选择电极法NY/T 87 土壤全钾测定法NY/T 88 土壤全磷测定法HJ 873 土壤水溶性氟化物和总氟化物的测定离子选择电极法LY/T 1232 森林土壤磷的测定LY/T 1234 森林土壤钾的测定3 术语和定义本文件没有需要界定的术语和定义。
4 方法原理4.1 土壤样品与氢氧化钠高温熔融,使土壤中含磷矿物及有机磷化物全部转化为可溶性正磷酸盐,用水溶解熔块,在规定的条件下样品溶液与钼锑抗显色剂反应,生成磷钼蓝,用分光光度计测定全磷。
显色反应后其颜色深浅与磷含量成正比。
4.2 土壤样品与氢氧化钠高温熔融,使土壤中有机化合物和矿化态钾全部转化为钾离子,用水溶解熔块,火焰光度计或原子吸收分光光度计测定钾离子浓度,再换算成土壤全钾含量。
4.3 土壤样品与氢氧化钠高温熔融,用水溶解熔块,使有干扰作用的阳离子变为不溶的氢氧化物,经澄清后除去,用溴甲酚紫指示剂调节试液pH,用氟离子选择电极测定氟化物。
5 试剂与材料5.1本试验方法所用试剂和水,除特殊注明外,均指分析纯试剂和GB/T 6682中规定的二级水。
所述溶液如未指明溶剂,均系水溶液。
试验中所需制剂及制品在没有注明其他要求时均按GB/T 603的规定制备。
5.2氢氧化钠(NaOH)。
5.3氢氧化钠溶液(ρ=720 g/L):称取720 g氢氧化钠(5.2),快速溶于水中,冷却后,稀释至1 L。
-土壤中钾的测定

5)注意
① 加热时温度要求均匀,用火煮 10 min 时 间应严格控制。
② 一定趁热过滤,以防土壤颗粒再次对钾的 吸附。
1)原 理
用中性 1 mol/L NH4OAc浸提土壤时,NH4+与胶 体表面的k+进行交换,连同水溶液中的k+一起进 入溶液,用火焰光度法测定。
K+ → 蓝光 → 滤光片 → 光电池 → 电流检测计 用标准溶液测定值与浓度的函数关系(Y = aX + b)计算溶液中K+的浓度
2)步骤
称过 1 mm 筛风干土 2.50 g → 100 ml 带 盖塑料瓶(或三角瓶) → 加入 25.0 ml 1 mol/L 中性 NH4OAc →(盖紧盖子)→ 在 振荡机上振荡 30 min(200r/min,25℃) → 过滤于 50 ml 三角瓶中→ 与标准系列同 上火焰光度计。
火焰光度计构造主件
气 源:装可燃气体(石油醚、汽油等)
光 源
喷雾器:待测液被压缩空气分散成细雾
喷 灯:细雾和助燃气体混合燃烧 光电池(硒光或硅光电池)将光换成电 光度计 检流计:将光转成的电显示出来(以刻度表示)表示。
单色器:让被测的波长谱线通过(k滤光片) 附 件:空气压缩机(通常调制0.4 kg/cm2)
2、土壤缓效钾的测定
热 1 mol/L HNO3 浸提——火焰光度法 P109
1)原理:
用 1 mol/L 热 HNO3 浸提可将黑云母、伊 利石、含水云母分解的中间体以及粘土矿
物晶格所固定的钾离子浸提出来。
2)步骤
称 1 mm 风干土 2.500 g → 100 ml 三角瓶 或硬 质试管中 → 加 1 mol/L HNO3 20 ml → 用文火煮 或油浴中微沸 10 min → 热过滤于 100 ml 容量 瓶中 → 以水定容 → 稀释10倍 → 与标准系列一 同上火焰光度计测定
土壤全磷全钾与有效磷测定

二、全P含量: 土壤全P含量的高低决定于土壤性质、气候条件 以及耕作管理措施,特别是施磷肥量等因素。
我国一般土壤全P量变化的范围大致为0.05-0.48% P2O5,且通常是西北地区高于东南地区。 东北黑土 0.14-0.35% P2O5 华北黄土 0.1-0.22% P2O5 南方红壤 0.04-0.08% P2O5
H3PO4 + 12 H2MoO4 = H3P(Mo3O10)4 + 12 H2O P多时呈黄色,少时无色
在一定酸度下,加入还原剂后,杂多酸中的Mo被 还原,产生特殊兰色-钼兰,其中一部分Mo6+被还 原成Mo5+或Mo3+,或Mo3+、Mo5+都有。在钼兰的 吸收光谱曲线中有两个吸收峰(660nm或880nm)。 测定时可以根据分光光度计的性能选用。我国GB
Si4+:在酸度较低时(0.25mol/L以下)可生成SiMo 杂多酸,但在P的测定中,PMo杂多酸形成的酸度 较高(在0.45mol/L以上),此酸度抑制了SiMo杂 多酸的形成。另外,用H2SO4-HClO4消煮时,由于 HClO4的脱水作用很强,使胶状Si脱水成SiO2析出, 所以少量的Si可用控制酸度的方法消除。
60年代初创用了改进的抗坏血酸法---钼锑抗法,它 是在钼酸铵试剂中添加了催化剂酒石酸氧锑钾 (K(SbO)C4H4O4),此法既具有抗坏血酸的优点, 又增加了四大优点。
(1)能加速显色反应; (2)在常温下能迅速显色; (3)锑参与了“钼兰”配合物的组成(P:Sb:Mo=1:2:12),
使兰色加深,提高了反应的灵敏度; (4)钼锑抗试剂是由钼酸铵、H2SO4、酒石酸氧锑钾、
华中与华南地区
0.5-3.0%(K2O)
