有机化学期末复习重点及难点
高中有机化学学习难点及策略

高中有机化学学习难点及策略高中有机化学是化学的重要分支,是化学领域的重要知识点,也是考研、高考等的重点考察内容。
然而,学习有机化学往往是很多学生感到比较难的一门学科,那么,高中有机化学学习难点有哪些?怎样采取策略提升学习效果呢?接下来,本文将一一为你解答。
1.基础概念理解不够明确学习有机化学必须理解一些基础的概念,如“原子、分子、化学键、分子式、分子式简化、分子构型、同分异构体、立体异构体”等概念理解不到位,就会导致后续学习效果不够理想。
2.反应机理缺乏详细了解有机化学的反应机理需要较为细致的了解,学生如果不理解反应机理,不知反应中化学键的崩裂和形成等过程,就难以掌握有机反应的规律,而理解反应机理的前提是掌握基本的化学反应类型和机理。
3.化学键剖析不够。
有机化学本质是化学反应,很多反应过程需要对化学键进行剖析。
但学生在学习过程中,常会把化学键看成简单的关系,没有深刻思考化学键内部的特征。
4.光学异构体理解不足学习有机化学也需要了解光学异构体,光学观测剂、AOAC 理论、菁子盘游、实验方法等等。
光学异构体理解不够就可能导致对手性化合物的分离、分子结构的确认等问题的误解。
5.记忆化合物结构容易混淆有机化学要求掌握大量的分子式、分子的结构、命名等知识,而一些细节、命名等往往容易让学生记混。
1.强化基础概念首先要明确,高中有机化学相较于初中化学具有难度增加的特点,因此必须理解初中化学中的基本概念独立才能继续深入地学习有机化学。
学生需要抽时间回溯初中化学中关于化学基本概念、元素周期表等关键概念的理解,争取做到精细、深入掌握。
2. 利用网络学习资源提高化学反应机理的理解学习有机化学较为繁琐,容易让学生感到枯燥乏味,这就需要学生寻找多种方式的资源来辅助学习。
学生可以借助网络上的各种电子书、视频等学习资料来了解化学反应机理及相关的科学理论。
同时还可以选择一些有机化学的报刊杂志、学术期刊等集合实战优秀的案例让学生学习。
有机化学重、难点提示和辅导

有机化学重、难点提示和辅导一.用费歇尔投影式表示单糖的开链结构:主要是葡萄糖和果糖。
二.重要的化学性质1.单糖的化学性质差向异构化:在弱碱性条件下,差向异构体的互相转化过程。
氧化:醛糖可被溴水氧化,而酮糖不能。
可用来鉴别葡萄糖和果糖。
醛糖和酮糖都能被托伦斯试剂和斐林试剂氧化,称为还原糖。
还原:用催化氢化或硼氢化钠可将单糖还原为相应的多元醇。
成:糖与过量的苯肼作用可生成糖,醛糖、酮糖都能生成糖。
D-葡萄糖、D-果糖、D-甘露糖可生成相同的。
成苷:环状结构的糖,在干HCl催化下与醇作用可生成糖苷。
2.双糖的化学性质麦芽糖、纤维二糖、乳糖是还原糖;蔗糖是非还原糖,可用托伦斯试剂和斐林试剂进行鉴别。
3.油脂的性质皂化:即酯的碱性水解。
干化、酸败。
4.氨基酸的性质两性与等电点:氨基酸分子中既含有碱性的氨基,又含有酸性的羧基,在结晶状态以两性离子存在。
氨基酸在等电点时的溶解度最小。
受热失水;与水合茚三酮反应:α-氨基酸与水合茚三酮反应生成蓝紫色物质,可用来鉴别α-氨基酸。
5.蛋白质的性质两性与等电点:蛋白质也是两性物质,等电点时溶解度最小。
盐析:在蛋白质溶液中加入盐,蛋白质会沉淀析出。
变性:蛋白质受到物理和化学因素影响时,会导致理化和生物性质的改变。
用酒精或高温、高压消毒是使细菌蛋白质变性而被杀灭,将预防接踵的疫苗储存在冰箱中,是为了避免蛋白质因高温变性而失去生物活性。
三.重要的名词、概念、缩写、药名差向异构体、还原糖、非还原糖、糖、糖苷、两性、等电点、盐析、变性、油脂的酸败、DNA、 RNA、PE、PP、PVC、甘油、硝酸甘油、阿司匹林(乙酰水杨酸)、扑热息痛(对乙酰氨基酚)等。
有机化学2下学期期末复习要点

3、芳香族衍生物(酸、酯、酚)等的结构推测。
4
2014-6-12
1、重新复习要求完成的作业,并参考相关的答案,认真思考 和总结。 2、完成提供的复习资料,并归纳总结。
祝大家取得好的成绩!
5
2014-6-12
有机化学2 期末复习要点
一、回答问题
1、醛酮的亲核加成(HCN,NaHSO)反应活性顺序判断。 2、醛酮烯醇式含量高低的比较。 3、取代酚酸酸性强弱的比较。 4、取代酸酸性强以及酰卤、酸酐、酯和酰胺反应活性的比较。 5、芳香化合物亲电反应速率的比较。 6、杂环化合物发生一取代(亲电、亲核)反应的位置。 7、氨基酸的类型、性质及二肽、三肽结构的推断。 8、葡萄糖、果糖及其糖苷的结构式、构象式、变旋现象、鉴别 方法。
1
二、鉴别
1、醛、酮及羧酸的鉴别。
2、伯、仲、叔胺的鉴别。 3、单糖及其糖苷的鉴别。
2014-6-12
4、麦芽糖、蔗糖、淀粉及纤维素的鉴别。
5、-氨基的制备及-位的卤代。 2、烯胺反应及其应用。 3、伯胺及-氨基酸的合成法—Gabriel合成法。
4、胺的氧化及氧化叔胺的消去反应。
2
2014-6-12
5、芳香胺的重氮化反应及偶氮化合物的形成。 6、氨基的保护及二肽的合成。 7、乙酰乙酸乙酯、丙二酸二乙酯的反应。 8、Reformatsky反应—羟基酸酯的合成。 9、糖苷的生成及水解。
四、反应机理
1、羟醛缩合反应、克莱森酯缩合。 2、酸催化合成酯及酯的碱性水解机理。 3、酰胺的Hofmann降解机理。 4、伯胺的重氮化及重排反应机理。 5、复习上学期的亲电加成(C+离子)、自由基取代反应机理
3
2014-6-12
高中有机化学学习难点及策略

高中有机化学学习难点及策略一、难点分析1. 观念理解有机化学中的很多概念和观念对于学生来说是全新的,比如键合、同分异构体、共轭体系等,这些概念的理解需要学生具备较强的逻辑思维能力和学科知识储备。
而很多学生在初学阶段往往对这些概念的理解存在模糊和混淆,造成后续学习的困难。
2. 化学反应机理有机化学中的化学反应机理是学生学习的重要内容,其中包括亲电加成反应、亲核取代反应、醛酮反应等。
这些反应的理解需要学生具备较强的动手实践能力和化学反应机理的理解能力,但是很多学生对于反应机理的理解存在困难。
3. 化学方程式的书写有机化学中的化学方程式的书写是学习的重要内容之一,但是很多学生在书写化学方程式时往往存在错误,比如遗漏部分物质、错误标明反应条件或者错误标明化学反应机理等。
二、学习策略1. 夯实基础学习有机化学之前,学生需要夯实化学的基础知识,包括化学键、原子结构、化学键理论等基础知识。
只有充分掌握了这些基础知识,才能更好地理解有机化学的相关知识和技巧。
2. 多练多思学生在学习有机化学的过程中需要多做相关练习,尤其是对于化学方程式的书写和化学反应机理的理解,需要不断地进行实践和思考,这样才能更好地掌握相关知识和技巧。
3. 培养逻辑思维有机化学涉及了很多复杂的化学反应和结构,而这些内容的理解需要学生具备较强的逻辑思维能力。
学生在学习有机化学的过程中需要培养自己的逻辑思维能力,这样才能更好地理解和掌握相关知识。
4. 结合实际5. 合理安排学习时间学生在学习有机化学的过程中需要合理安排学习时间,不能一味地死记硬背,而是要通过多种方式进行学习,比如课堂学习、课外阅读、实验操作等,这样才能更好地提高学习效率。
6. 寻求帮助学生在学习有机化学的过程中遇到困难时,可以寻求老师和同学的帮助,也可以通过查阅相关资料和参加有机化学学习班进行学习,这样能更好地解决学习中的困难。
三、总结有机化学是高中化学学科中的重要内容,也是学生备战高考的关键内容之一。
最新大学有机化学期末复习总结

有机化学期末复习总结一、有机化合物的命名命名是学习有机化学的“语言”,因此,要求学习者必须掌握。
有机合物的命名包括俗名、习惯命名、系统命名等方法,要求能对常见有机化合物写出正确的名称或根据名称写出结构式或构型式。
1、俗名及缩写:要求掌握一些常用俗名所代表的化合物的结构式,如:木醇、甘醇、甘油、石炭酸、蚁酸、水杨醛、水杨酸、氯仿、草酸、苦味酸、肉桂酸、苯酐、甘氨酸、丙氨酸、谷氨酸、巴豆醛、葡萄糖、果糖等。
还应熟悉一些常见的缩写及商品名称所代表的化合物,如:RNA、DNA、阿司匹林、福尔马林、尼古丁等。
2、习惯命名法:要求掌握“正、异、新”、“伯、仲、叔、季”等字头的含义及用法,掌握常见烃基的结构,如:烯丙基、丙烯基、正丙基、异丙基、异丁基、叔丁基、苄基等。
3、系统命名法:系统命名法是有机化合物命名的重点,必须熟练掌握各类化合物的命名原则。
其中烃类的命名是基础,几何异构体、光学异构体和多官能团化合物的命名是难点,应引起重视。
要牢记命名中所遵循的“次序规则”。
4、次序规则:次序规则是各种取代基按照优先顺序排列的规则(1)原子:原子序数大的排在前面,同位素质量数大的优先。
几种常见原子的优先次序为:I>Br>Cl>S>P>O>N>C>H(2)饱和基团:如果第一个原子序数相同,则比较第二个原子的原子序数,依次类推。
常见的烃基优先次序为:(CH3)3C->(CH3)2CH->CH3CH2->CH3- (3)不饱和基团:可看作是与两个或三个相同的原子相连。
不饱和烃基的优先次序为: -C≡CH>-CH=CH2>(CH3)2CH-次序规则主要应用于烷烃的系统命名和烯烃中几何异构体的命名烷烃的系统命名:如果在主链上连有几个不同的取代基,则取代基按照“次序规则”一次列出,优先基团后列出。
按照次序规则,烷基的优先次序为:叔丁基>异丁基>异丙基 >丁基>丙基>乙基>甲基。
大学有机化学期末复习总结

有机化学期末复习总结一、有机化合物的命名命名是学习有机化学的“语言”,因此,要求学习者必须掌握.有机合物的命名包括俗名、习惯命名、系统命名等方法,要求能对常见有机化合物写出正确的名称或根据名称写出结构式或构型式.1、俗名及缩写:要求掌握一些常用俗名所代表的化合物的结构式,如:木醇、甘醇、甘油、石炭酸、蚁酸、水杨醛、水杨酸、氯仿、草酸、苦味酸、肉桂酸、苯酐、甘氨酸、丙氨酸、谷氨酸、巴豆醛、葡萄糖、果糖等.还应熟悉一些常见的缩写及商品名称所代表的化合物,如:RNA、DNA、阿司匹林、福尔马林、尼古丁等.2、习惯命名法:要求掌握“正、异、新”、“伯、仲、叔、季”等字头的含义及用法,掌握常见烃基的结构,如:烯丙基、丙烯基、正丙基、异丙基、异丁基、叔丁基、苄基等.3、系统命名法:系统命名法是有机化合物命名的重点,必须熟练掌握各类化合物的命名原则.其中烃类的命名是基础,几何异构体、光学异构体和多官能团化合物的命名是难点,应引起重视.要牢记命名中所遵循的“次序规则”.4、次序规则:次序规则是各种取代基按照优先顺序排列的规则1原子:原子序数大的排在前面,同位素质量数大的优先.几种常见原子的优先次序为:I>Br>Cl>S>P>O>N>C>H2饱和基团:如果第一个原子序数相同,则比较第二个原子的原子序数,依次类推.常见的烃基优先次序为:CH33C->CH32CH->CH3CH2->C H3-3不饱和基团:可看作是与两个或三个相同的原子相连.不饱和烃基的优先次序为: -C≡CH>-CH=CH2>CH32CH-次序规则主要应用于烷烃的系统命名和烯烃中几何异构体的命名烷烃的系统命名:如果在主链上连有几个不同的取代基,则取代基按照“次序规则”一次列出,优先基团后列出.按照次序规则,烷基的优先次序为:叔丁基>异丁基>异丙基 >丁基>丙基>乙基>甲基.(1)、几何异构体的命名:烯烃几何异构体的命名包括顺、反和Z、E两种方法.简单的化合物可以用顺反表示,也可以用Z、E表示.用顺反表示时,相同的原子或基团在双键碳原子同侧的为顺式,反之为反式.如果双键碳原子上所连四个基团都不相同时,不能用顺反表示,只能用Z、E表示.按照“次序规则”比较两对基团的优先顺序,较优基团在双键碳原子同侧的为Z型,反之为E型.必须注意,顺、反和Z、E是两种不同的表示方法,不存在必然的内在联系.有的化合物可以用顺反表示,也可以用Z、E表示,顺式的不一定是Z型,反式的不一定是E型.例如:CH3-CH2BrC=C 反式,Z型H CH2-CH3CH3-CH2CH3C=C 反式,E型H CH2-CH3脂环化合物也存在顺反异构体,两个取代基在环平面的同侧为顺式,反之为反式.双官能团化合物的命名:双官能团和多官能团化合物的命名关键是确定母体.常见的有以下几种情况:①当卤素和硝基与其它官能团并存时,把卤素和硝基作为取代基,其它官能团为母体.②当双键与羟基、羰基、羧基并存时,不以烯烃为母体,而是以醇、醛、酮、羧酸为母体.③当羟基与羰基并存时,以醛、酮为母体.④当羰基与羧基并存时,以羧酸为母体.⑤当双键与三键并存时,应选择既含有双键又含有三键的最长碳链为主链,编号时给双键或三键以尽可能低的数字,如果双键与三键的位次数相同,则应给双键以最低编号.官能团的优先顺序:-COOH羧基>-SO3H磺酸基 > -COOR酯基>-COX卤基甲酰基 > -CONH2氨基甲酰基 > -CN 氰基> -CHO醛基> -CO- 羰基> -OH醇羟基> -OH 酚羟基 >-SH 巯基> -NH2氨基 > -O- 醚基> 双键 > 叁键4、杂环化合物的命名由于大部分杂环母核是由外文名称音译而来,所以,一般采用音译法.要注意取代基的编号.二、有机化合物的基本反应1、加成反应:根据反应历程不同分为亲电加成、亲核加成和游离基加成.(1)、亲电加成:由亲电试剂的进攻而进行的加成反应.要求掌握不对称烯烃进行亲电加成反应时所遵循的马氏规则,即试剂中带正电核的部分加到含氢较多的双键碳原子上,而负性部分加到含氢较少的双键碳原子上.烯烃加卤素、卤化氢、硫酸、次卤酸、水,炔烃加卤素、卤化氢、水以及共轭双烯的1,2和1,4加成都是亲电加成反应.烯烃进行亲电加成反应时,双键上电子云密度越大,反应越容易进行.2、亲核加成:由亲核试剂进攻而进行的加成反应.要掌握亲核试剂的概念、亲核加成反应的历程简单加成及加成─消除、不同结构的羰基化合物进行亲核加成反应的活性顺序及影响反应活性的因素.羰基化合物与氰氢酸、亚硫酸氢钠、醇、格氏试剂、氨及氨衍生物的加成都是亲核加成反应. 羰基化合物进行亲核加成反应的活性顺序为:HCHO>CH3CHO>RCHO>C6H5CHO>CH3COCH3>RCOCH3>C6H5COCH3>C6H5COC6H53、自由基加成:由自由基引发而进行的加成反应.烯烃在过氧化物存在下与溴化氢进行的加成是自由基加成.不对称烯烃与溴化氢进行自由基加成时得到反马氏规则的产物,即氢加到含氢较少的双键碳原子上.加成反应除上述三种类型之外,还有不饱和烃的催化氢化,共轭二烯的双烯合成等.2、消除反应从一个化合物分子中脱去较小分子如H2O、HX、NH3而形成双键或三键的反应叫消除反应.卤代烃脱卤化氢和醇脱水是重要的消除反应.1、卤代烃脱卤化氢:卤代烃的消除反应是在强碱性条件下进行.不同结构的卤代烃进行消除反应的活性顺序为:三级>二级>一级.要掌握卤代烃进行消除反应时所遵循的查依采夫规则,当卤代烃中不只含有一个β碳时,消除时脱去含氢少的β碳上的氢原子,或者说总是生成双键碳上连有烃基较多的烯烃,亦即仲卤代烷和伯卤代烷发生消去反应时, 主要生成双键上连接烃基最多的烯烃.要注意,卤代烃的消除和水解是竞争反应.2、醇的消除:醇的消除反应在强酸性条件下进行,消除方向也遵循查依采夫规则.要掌握不同结构的醇进行消除反应的活性顺序:叔醇>仲醇>伯醇.3、取代反应根据反应历程的不同可分为亲电取代、亲核取代、游离基取代.⑴、亲电取代:由于亲电试剂的进攻而引发的取代反应称亲电取代反应.苯环上的卤化、硝化、磺化、付氏烷基化和酰基化以及重氮盐的偶合反应等,都是亲电取代反应,萘环和芳香杂环上也能发生亲电取代反应.要注意苯环上有致钝基团时不能进行付氏反应,苯环上进行烷基化时会发生异构化现象.掌握萘环上进行亲电取代反应的规律,第一个取代基主要进入α位,第二个取代基是进入同环还是异环由原取代基的定位效应决定.掌握五员、六员芳香杂环化合物的亲电取代反应以及它们与苯环比较进行亲电取代反应活性的差异,呋喃、噻吩、吡咯进行亲电取代反应的活性比苯大,而吡啶比苯小.⑵、亲核取代由亲核试剂的进攻而引起的取代反应称亲核取代反应.卤代烃的水解、醇解、氰解、氨解,醇与氢卤酸的反应,醚键的断裂,羧酸衍生物的水解、醇解、氨解等都是亲核取代反应.卤代烃的亲核取代反应可按两种历程进行,单分子历程SN 1和双分子历程SN2,伯卤代烃易按SN2历程反应,叔卤代烃一般按SN1历程反应,仲卤代烃则两者兼而有之.要在理解反应历程的基础上掌握不同卤代烃进行亲核取代反应的活性,SN1反应支链越多活性越强,反应速率越快,SN2反应支链越多,反应活性越弱,反应速率越慢.如:下列化合物按SN1历程反应的活性由大到小排序为:CH33CI > CH33CBr > CH32CHBr. 要注意,在碱性条件下卤代烃的取代和消除是互相竞争的反应,叔卤代烃容易发生消除,伯卤代烃易发生取代,强极性溶剂如水有利于取代,而弱极性溶剂如醇和强碱如醇钠有利于消除,高温有利于消除.⑶、自由基取代:由自由基的引发而进行的取代称自由基取代.烷烃的卤代,烯烃和烷基苯的α卤代是自由基取代反应.反应条件是高温、光照或过氧化物存在.自由基的稳定性和中心碳原子上所连的烷基数目有关,烷基越多,稳定性越大.自由基的稳定次序为:三级>二级>一级>·CH34、氧化还原反应包括氧化反应和还原反应两种类型.⑴、氧化反应烯、炔、芳烃侧链以及醇、酚、醛、酮等都易发生氧化反应要掌握几种常用的氧化剂,如高锰酸钾、重铬酸钾的硫酸溶液、氧气空气、臭氧以及托伦试剂、斐林试剂、次卤酸钠等.掌握氧化反应在实际中的应用,如臭氧氧化可用来推测烯烃的结构,托伦试剂和斐林试剂的氧化可用来鉴别醛和酮等.⑵、还原反应 不饱和烃的催化氢化、醛、酮、羧酸及酯还原为醇,硝基苯还原为苯胺等都是还原反应.要掌握几种常用的还原剂,如H 2/Ni 、 Na+C 2H 5OH 、Fe+HCl 、NaBH 4、、 、LiAlH 4、异丙醇/异丙醇铝等,注意后面三种是提供负氢离子的还原剂,只对羰基选择加氢,与双键、三键不发生作用.还要掌握羰基还原为亚甲基的两种方法,注意,进行克莱门森还原时反应物分子中不能存在对酸敏感的基团,如醇羟基、双键等,用伍尔夫─吉日聂尔还原及黄鸣龙改进法时,反应物分子中不能带有对碱敏感的基团,如卤素等.5、缩合反应 主要包括羟醛缩合和酯缩合.1羟醛缩合 含有α氢的醛在稀碱条件下生成β—羟基醛,此化合物不稳定受热容易脱水,生成α、β不饱和醛.因此,此反应常用来增长碳链制备α、β不饱和醛.要求掌握羟醛缩合的反应条件.2克莱森酯缩合 含有α氢的酯在强碱条件下发生克莱森酯缩合,两分子酯之间脱去一分子醇生成β酮酸酯.要掌握反应条件及在实际中的应用,有机合成中广泛应用的乙酰乙酸乙酯就是通过此反应制备的.除了上述五种类型的反应之外,还要求掌握重氮化反应、芳香重氮盐的取代反应、脱羧反应等,注意反应条件、产物及其在实际中的应用.三、有机化合物的转化及合成方法要求掌握有机化合物各类官能团之间的转化关系、增长和缩短碳的方法,在此基础上设计简单有机化合物的合成路线.熟练掌握苯进行付氏烷基化、酰基化、炔化物的烃化、羟醛缩合、格氏试剂法等都可以增长碳链;炔化物的烃化、格氏试剂法及芳香重氮盐等在有机合成中应用非常广泛.1、炔化物的烃化具有炔氢的炔烃与氨基钠作用得炔钠,炔钠与伯卤代烃反应得到烷基取代得炔烃.此反应可增长碳链,制备高级炔烃.2、格氏试剂法格氏试剂在有机合成中应用极为广泛,它与环氧乙烷、醛、酮、酯反应可用来制备不同结构的醇等.这些反应既可增长碳链,又可形成所需的官能团.3、重氮盐取代法芳香重氮盐的重氮基可被氢原子、卤素、羟基、氰基取代,由于苯环上原有取代基定位效应的影响而使某些基团不能直接引入苯环时,可采用重氮盐取代的方法.要注意被不同基团取代时的反应条件.四、有机化学的知识点1、两类定位基:邻对位定位基:使新进入的取代基主要进入它的邻位和对位邻位和对位异构体之和大于60%;同时一般使苯环活化卤素等例外.例如—O-,—NCH32,—NH2,—OH,OCH3,—NHCOCH3,—OCOCH3,—R,—XCl,Br ,I,—C6H5等.间位定位基:使新进入的取代基主要进入它的间位间位异构体大于40%;同时使苯环钝化.例如—NCH33,—NO2,—CN,—SO3H,—CHO,—COCH3,—COOH,—COOCH3,—CO NH2,—NH3等.2、两类电子基:吸电子基:使电子云密度减小的基团,如-COOH,-COOR,-NO2,-X,-HSO3,-CHO,-CO-R等.供电子基:使电子云密度增大的基团,如-R,-OH,-OR,-NH2,-NHCOR等.3、相同C原子有机物的熔沸点:支链越多沸点越低,对称性越高,熔点越高,如下列化合物沸点由低到高排列为:正戊烷 < 3,3-二甲基戊烷 < 2-甲基己烷 <正庚烷 < 2-甲基庚烷.五、有机化合物的鉴别烯烃、二烯、炔烃及三、四元的脂环烃:溴的四氯化碳溶液,溴腿色含有炔氢的炔烃:硝酸银或氯化亚铜的氨溶液,生成炔化银白色沉淀或炔化亚铜红色沉淀.卤代烃:硝酸银的醇溶液,生成卤化银沉淀;不同结构的卤代烃生成沉淀的速度不同,叔卤代烃和烯丙式卤代烃最快,仲卤代烃次之,伯卤代烃需加热才出现沉淀.醇:与金属钠反应放出氢气鉴别6个碳原子以下的醇;用卢卡斯试剂鉴别伯、仲、叔醇,叔醇立刻变浑浊,仲醇放置后变浑浊,伯醇放置后也无变化.酚或烯醇类化合物:用三氯化铁溶液产生颜色.苯酚与溴水生成三溴苯酚白色沉淀.羰基化合物:2,4-二硝基苯肼,产生黄色或橙红色沉淀;区别醛与酮用托伦试剂,醛能生成银镜,而酮不能;区别芳香醛与脂肪醛或酮与脂肪醛,用斐林试剂,脂肪醛生成砖红色沉淀,而酮和芳香醛不能;鉴别甲基酮和具—CH—结构的醇用碘的氢氧化钠溶液,有CH3OH生成黄色的碘仿沉淀.甲酸:用托伦试剂,甲酸能生成银镜,而其他酸不能.胺:区别伯、仲、叔胺有两仲方法1.用苯磺酰氯或对甲苯磺酰氯,在NaOH溶液中反应,伯胺生成的产物溶于NaOH;仲胺生成的产物不溶于NaOH溶液;叔胺不发生反应.2.用NaNO2+HCl:脂肪胺:伯胺放出氮气,仲胺生成黄色油状物,叔胺不反应.芳香胺:伯胺生成重氮盐,仲胺生成黄色油状物,叔胺生成绿色固体.糖:葡萄糖与果糖:用溴水,葡萄糖能使溴水腿色,而果糖不能.麦芽糖与蔗糖:用托伦试剂或斐林试剂,麦芽糖可生成银镜或砖红色沉淀,而蔗糖不能.。
大学有机化学期末复习1

第一章链烃一、命名1、烷烃的命名系统命名法要点:ⅰ选主链(C数最多的链)ⅱ编号(靠近取代基的一端)ⅲ命名(将复杂基团后列出)注:1、用汉字的数字表示取代基的个数,用阿拉伯数字表示取代基的位置(如2,3—二甲基)2、不要忘记短线连接2、烯烃的命名1、系统命名法同烷烃(离双键最近的位置开始编号)2、顺反命名分别连接在双键碳原子上的两个相同的原子和原子团位于双键的同一侧称为顺式(或cis-);在双键的两侧称为反式(或trans-)3、Z/E命名法1)取代基与双键碳直接连接的原子按其原子序数大小排列,大者为“较优”基团;如为同位素,则质量高的定为“较优”基团I > Br > Cl > S > O > C > D > H2)如果两个取代基团的第一个原子相同,则比较与第一个原子相连的几个原子。
比较时,按原子序数排列,先比较各组中最大者:若仍相同,再依次比较第二、第三个……3)含有双键和三键基团,可以认为连有两个或三个相同原子注:1、当两个优先基团位于双键的同一侧时,记为Z-构型(Zusammen);位于双键异侧,记为E-构型(Entgegen)2、写法(例如E-3-乙基-2-己烯),对于烯烃的命名,一定要首先看是否为Z/E构型3、炔烃的命名1、系统命名(同烷烃,靠近三键的一段开始编号)2、分子中同时含有双键和三键时(1)选同时含双键和三键的最长碳链为主链(2)编号从靠近三键或双键最近的一端开始,同等位置时选离双键最近端开始(3)名称均为某(位次加主链碳数)烯某(位次)炔(如1-庚烯-6-炔)二、化学性质烯烃1)加成反应1、加氢(空间位阻)2、加卤素(电子效应)3、加卤代烃(1)无氧化物时:遵循马氏规则(H 加在含H 较多的双键C 上) (2)有氧化物时:与HBr 反应遵循反马氏规则 4、加水(生成醇) 2)氧化1、高锰酸钾氧化 (区分酸碱性)RCH = CHR + KMnO4RCH = CH2 + KMnO4 RCOOH + CO2 + H2O + Mn2 + 注: 碳原子上连接一个氢,则氧化生成羧酸 连接两个氢则生成二氧化碳和水未连接氢则生成酮2、臭氧氧化炔烃1、加成同烯烃2、特征反应(必须一端有H)HC ≡C-R + Cu(NH3) 2+ —→ CuC ≡CCu ↓乙炔亚铜(红棕色) HC ≡C-R + Ag(NH3)2+ —→ AgC ≡CAg ↓乙炔银(白色)第二章 环烃3.1 环烷烃1环烷烃的命名 ①环的命名 ②顺反命名C(CH 3)3HCH 3H2化学反应+ Br 2 300℃Br+ HBrRCH CHROH OH+ MnO 2中性或碱性H RC CHR RO 3R R C C OOOR H RR C CO OR H+22) 加成反应Addition (1)加氢Hydrogenation (2)加卤素、卤化氢BrCH 2CH CH 2+ HBr CH 3CHCH 2 CH 3CH 3加热CH 3CH 2CH 2 + HBr CH 2CH 2CH 2BrCH 2CH 2CH 2 + Br 2 CH 2CH 2CH 2BrBrCH 2 CH 2 CH 2 CH 2+ H 2 CH 3CH 2CH 2CH 3Ni200℃CH 2CH 2 CH 2+ H 2 Ni80℃CH 3CH 2CH 3碳环开环发生在连接氢原子最多和最少的两个碳原子之间,氢原子加在连接氢原子较多的碳原子上.3.2 芳香烃(Aromatic hydrocarbon ) 重难点重点 命名、亲电取代、氧化反应 难点 亲电取代反应的机理具有“芳香性”的化合物称为芳香化合物 结构上:1.具有平面或接近平面的环状结构;2.键长平均化。
有机化学期末复习重点

第1 章 绪 论 1. 有机化合物与有机化学的定义2.有机化合物的特点(了解)3.共价键的特性和属性。
注意:分子的极性与键的极性和分子的对称性有关。
4.共价键的断裂和有机化学反应的基本类型(1) 共价键的断裂方式分为均裂和异裂,根据共价键的断裂和形成的方式不同,可把有机反应机理分为:游离基反应、离子型反应和协同反应等 3 大类。
5.有机反应中“离子型”反应根据反应试剂类型不同,分为亲电反应与亲核反应两类:(1) 亲电试剂与亲电反应:由缺电子的试剂进攻部分负电荷的碳原子而发生的,这类十分需要电子的试剂称为亲电试剂。
如含有 H +、Cl +、Br +、NO 2+、RN 2+、R 3C +等正离子的试剂。
由亲电试剂的进攻而引起的反应称为亲电反应。
(2) 亲核试剂和亲核反应:由能供给电子的试剂进攻具有部分正电荷的碳原子而发生的,这类能供给电子的试剂称亲核试剂,如 H 2O、ROH、OH -、RO -、Br -、NH 3、RNH 2、CN -等。
由亲核试剂的进攻而引起的反应称为亲核反应。
注意:有机反应中,加成反应分为亲电加成(烯烃与卤素的反应)、亲核加成(羰基与氰氢酸、水、醇、格氏试剂、氨的衍生物之间的反应)、自由基加成(如:不对称与 HBr 在过氧化物存在下的反应属于自由基加成,遵循反马氏规则)三类。
第 2 章 烷烃和环烷烃一、烷烃的命名:1.掌握有机化合物系统命名的基本原则2.碳原子的分类(伯、仲、叔、季)与常见烷基的结构和名称(P 48)3.顺序规则 —— 主要烷基的优先次序:甲基<乙基<丙基<异丙基二、烷烃的结构(了解)三、烷烃的构象异构(属于立体异构)乙烷中最典型的 2 种构象是交叉式(稳定构象)和重叠式,用 Newman 投影式和锯架式表示。
丁烷的 4 种典型构象及其稳定顺序:对位交叉式>邻位交叉式>部分重叠式>全重叠式。
四、烷烃的化学性质(掌握)烷烃卤代反应的机制——游离基(自由基)反应,分链引发、链增长与链终止是的 3 个阶段;烷烃卤代反应的取向主要由自由基稳定性次序来决定。
高中有机化学学习难点及策略

高中有机化学学习难点及策略高中有机化学是化学的重要分支之一,也是高中化学教学的难点之一。
本文将介绍高中有机化学的学习难点,并提出相应的学习策略,以帮助广大高中生更好地掌握有机化学知识。
一、学习难点1.理论知识广泛、抽象难懂有机化学理论极其丰富,体系庞大,具有很强的抽象性和逻辑思维。
学生需要耐心钻研其理论体系,了解分子结构、键合原理、反应机理等基本概念。
2.实验操作复杂、容易产生误差有机化学实验操作相对复杂,需要进行多次控制试验,有时需要使用一些特殊的设备和药剂。
学生在实验操作中要严格遵守实验操作要求,小心谨慎,杜绝偏差和误差。
3.知识点多、暗示性多、记忆要求高有机化学知识点繁多,暗示性多,很多化合物的结构特征和反应机理具有相似之处,需要学生进行理解和记忆,才能应对考试。
二、学习策略1.理论知识:(1)掌握基本概念:从分子结构、键合原理、反应机理等角度出发,在学习各种反应时,要注重理论知识的内在联系。
(2)反复训练:有机化学是一门反复练习琢磨的学科,只有通过大量的练习才能将理论概念转化为具体的实践操作方法。
(3)勤于总结:在复习阶段,要根据课本、笔记等资料进行总结,梳理有机化学的核心理论、重要概念和难点内容。
2.实验操作:(1)正确操作:对于不同的实验,学生应该详细了解所需的操作流程,在进行实验操作时保持警觉,确保每个步骤的正确性。
(2)模拟实验和观察实验:在学习有机化学实验操作时,可通过观察和模拟实验等方式加深对于实验原理和运作流程的理解。
(3)合理调整参数:在实验操作中遇到问题时,首先要找出原因,合理调整操作参数,并寻找其他解决方法尝试。
3.记忆要求:(1)利用丰富图解和历史:有机化学的发展历程丰富且具有历史性,可以采用图画、参照实验列表等方式增强记忆。
(2)多种方法记忆:记忆方法因人而异,可通过口诀、图表、结构公式、化学式等多种形式来辅助记忆。
(3)查漏补缺:及时归纳总结所学内容,检查是否存在知识盲区,对于漏学或是没有理解的知识点要及时补充。
高中有机化学学习难点及策略

高中有机化学学习难点及策略有机化学是高中化学的重要组成部分,也是学生们普遍认为比较难以掌握的一个领域。
有机化学涉及到众多的化合物、反应及结构,对学生的理解和记忆能力都提出了相当高的要求。
本文将就高中有机化学学习的难点进行分析,并提出一些相应的学习策略,帮助学生更好地掌握这一部分的知识。
高中有机化学学习的难点主要表现在以下几个方面:1. 多样的化合物和反应:有机化学中的化合物种类繁多,结构多样,而且其反应类型也很多,这给学生的记忆带来了很大的挑战。
学生很容易混淆各种化合物的命名、结构及性质,对这些内容的掌握需要大量的记忆和实际运用。
2. 反应机理的理解:有机化学的反应机理是学习的重点和难点,尤其是一些复杂的反应路线和重要的反应类型。
学生需要理解反应的机理、原因和影响,这需要学生具备较强的逻辑思维和理解能力。
3. 有机化合物的命名和结构的确定:有机化合物的命名方法繁多,学生需要掌握多种命名规则,并能根据化合物的结构确定其命名。
学生还需要理解有机化合物的结构特点,从结构中找出规律和特性,这是一个耗费大量时间和精力的过程。
在面对这些难点的情况下,学生们可以采取以下策略来更好地学习有机化学:1. 建立系统化的学习框架:对于那么多的化合物和反应,学生可以通过建立一个系统化的学习框架来整理和归纳所学知识。
可以制作思维导图或者总结表格,将不同的化合物和反应分类、归纳出规律,有助于学生更好地理解和记忆。
2. 多做练习,巩固知识点:有机化学是一个实践性很强的学科,学生可以通过大量的练习来巩固所学的知识。
可以做大量的习题和实验,通过实际操作来理解和掌握有机化学的知识和技能。
3. 培养逻辑思维和推理能力:有机化学中的反应机理需要学生具备很强的逻辑推理能力,因此学生可以通过学习逻辑思维的方法,提高自己的推理能力,更好地理解反应机理和规律。
4. 结合实际生活,增加学习的兴趣:有机化学的知识与我们的日常生活息息相关,学生可以通过结合实际生活中的例子和应用,增加学习的兴趣。
大学有机化学复习重点总结
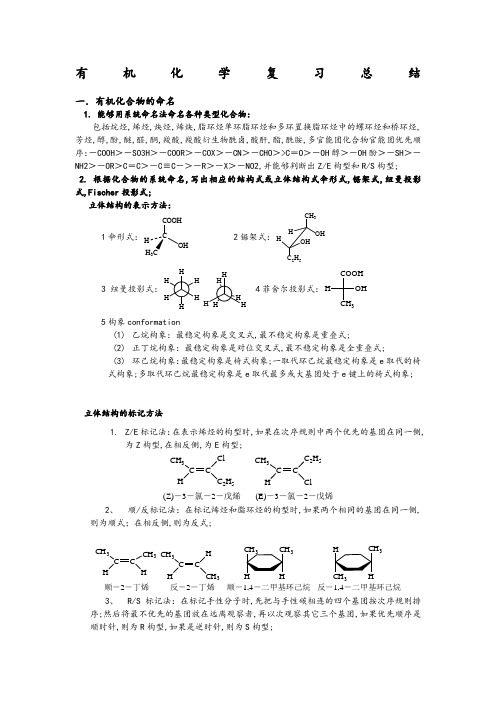
有机化学复习总结一.有机化合物的命名1. 能够用系统命名法命名各种类型化合物:包括烷烃,烯烃,炔烃,烯炔,脂环烃单环脂环烃和多环置换脂环烃中的螺环烃和桥环烃,芳烃,醇,酚,醚,醛,酮,羧酸,羧酸衍生物酰卤,酸酐,酯,酰胺,多官能团化合物官能团优先顺序:-COOH>-SO3H>-COOR>-COX>-CN>-CHO>>C=O>-OH醇>-OH酚>-SH>-NH2>-OR>C=C>-C≡C->-R>-X>-NO2,并能够判断出Z/E构型和R/S构型;2. 根据化合物的系统命名,写出相应的结构式或立体结构式伞形式,锯架式,纽曼投影式,Fischer投影式;立体结构的表示方法:1伞形式:CCOOH32锯架式:CH3HH OHC2H53纽曼投影式:4菲舍尔投影式:COOHCH3OHH5构象conformation(1)乙烷构象:最稳定构象是交叉式,最不稳定构象是重叠式;(2)正丁烷构象:最稳定构象是对位交叉式,最不稳定构象是全重叠式;(3)环己烷构象:最稳定构象是椅式构象;一取代环己烷最稳定构象是e取代的椅式构象;多取代环己烷最稳定构象是e取代最多或大基团处于e键上的椅式构象;立体结构的标记方法1.Z/E标记法:在表示烯烃的构型时,如果在次序规则中两个优先的基团在同一侧,为Z构型,在相反侧,为E构型;CH3CH C2H5CH3C CH2H5Cl(Z)-3-氯-2-戊烯(E)-3-氯-2-戊烯2、顺/反标记法:在标记烯烃和脂环烃的构型时,如果两个相同的基团在同一侧,则为顺式;在相反侧,则为反式;CH3C CHCH3HCH3C CHHCH3顺-2-丁烯反-2-丁烯333顺-1,4-二甲基环己烷反-1,4-二甲基环己烷3、R/S标记法:在标记手性分子时,先把与手性碳相连的四个基团按次序规则排序;然后将最不优先的基团放在远离观察者,再以次观察其它三个基团,如果优先顺序是顺时针,则为R构型,如果是逆时针,则为S构型;CaR型S型注:将伞状透视式与菲舍尔投影式互换的方法是:先按要求书写其透视式或投影式,然后分别标出其R/S构型,如果两者构型相同,则为同一化合物,否则为其对映体;二. 有机化学反应及特点1. 反应类型还原反应包括催化加氢:烯烃、炔烃、环烷烃、芳烃、卤代烃氧化反应:烯烃的氧化高锰酸钾氧化,臭氧氧化,环氧化;炔烃高锰酸钾氧化,臭氧氧化;醇的氧化;芳烃侧链氧化,芳环氧化2. 有关规律1)马氏规律:亲电加成反应的规律,亲电试剂总是加到连氢较多的双键碳上;2)过氧化效应:自由基加成反应的规律,卤素加到连氢较多的双键碳上;3)空间效应:体积较大的基团总是取代到空间位阻较小的位置;4)定位规律:芳烃亲电取代反应的规律,有邻、对位定位基,和间位定位基;5)查依切夫规律:卤代烃和醇消除反应的规律,主要产物是双键碳上取代基较多的烯烃; 6)休克尔规则:判断芳香性的规则;存在一个环状的大π键,成环原子必须共平面或接近共平面,π电子数符合4n+2规则;7)霍夫曼规则:季铵盐消除反应的规律,只有烃基时,主要产物是双键碳上取代基较少的烯烃动力学控制产物;当β-碳上连有吸电子基或不饱和键时,则消除的是酸性较强的氢,生成较稳定的产物热力学控制产物;8)基团的“顺序规则”3. 反应中的立体化学烷烃:反应类型(按历程分)自由基反应离子型反应协同反应:双烯合成自由基取代:烷烃卤代、芳烃侧链卤代、烯烃的α-H卤代自由基加成:烯,炔的过氧化效应亲电加成:烯、炔、二烯烃的加成,脂环烃小环的开环加成亲电取代:芳环上的亲电取代反应亲核取代:卤代烃、醇的反应,环氧乙烷的开环反应,醚键断裂反应,卤苯的取代反应消除反应:卤代烃和醇的反应亲核加成:炔烃的亲核加成烷烃的自由基取代:外消旋化烯烃:烯烃的亲电加成:溴,氯,HOBrHOCl,羟汞化-脱汞还原反应-----反式加成 其它亲电试剂:顺式+反式加成烯烃的环氧化,与单线态卡宾的反应:保持构型 烯烃的冷稀KMnO 4/H 2O 氧化:顺式邻二醇 烯烃的硼氢化-氧化:顺式加成 烯烃的加氢:顺式加氢环己烯的加成1-取代,3-取代,4-取代 炔烃:选择性加氢:Lindlar 催化剂-----顺式烯烃 Na/NH 3L-----反式加氢亲核取代:S N 1:外消旋化的同时构型翻转 S N 2:构型翻转Walden 翻转 消除反应:E2,E1cb: 反式共平面消除; 环氧乙烷的开环反应:反式产物四.概念、物理性质、结构稳定性、反应活性 一.概念 1. 同分异构体2. 试剂 亲电试剂:简单地说,对电子具有亲合力的试剂就叫亲电试剂electrophilic reagent;亲电试剂一般都是带正电荷的试剂或具有空的p 轨道或d 轨道,能够接受电子对的中性分子, 如:H +、Cl +、Br +、RCH 2+、CH 3CO +、NO 2+、+SO 3H 、SO 3、BF 3、AlCl 3等,都是亲电试剂;亲核试剂:对电子没有亲合力,但对带正电荷或部分正电荷的碳原子具有亲合力的试剂叫亲核试剂nucleophilic reagent;亲核试剂一般是带负电荷的试剂或是带有未共用电子对的中性分子,如:OH -、HS -、CN -、NH 2-、RCH 2-、RO -、RS -、PhO -、RCOO -、X -、H 2O 、ROH 、ROR 、NH 3、RNH 2等,都是亲核试剂;自由基试剂:构造异构立体异构位置异构碳架异构官能团异构互变异构构型异构构象异构H 2C C CH 3CH 3H 2C C HCH 2CH 2CH 3CH 2OH CH2CHOH3CHO顺反异构对映异构同分异构CH 2CHCH 2CH 3CH 3CH CHCH 3 CH 3OCH 3Cl 2、Br 2是自由基引发剂,此外,过氧化氢、过氧化苯甲酰、偶氮二异丁氰、过硫酸铵等也是常用的自由基引发剂;少量的自由基引发剂就可引发反应,使反应进行下去; 3. 酸碱的概念布朗斯特酸碱:质子的给体为酸,质子的受体为碱; Lewis 酸碱:电子的接受体为酸,电子的给与体为碱; 4. 共价键的属性键长、键角、键能、键矩、偶极矩; 5. 杂化轨道理论 sp 3、sp 2、sp 杂化; 6. 旋光性平面偏振光: 手性: 手性碳: 旋光性:旋光性物质光学活性物质,左旋体,右旋体: 内消旋体、外消旋体,两者的区别: 对映异构体,产生条件: 非对映异构体: 苏式,赤式:差向异构体: Walden 翻转: 7. 电子效应 1 诱导效应2 共轭效应π-π共轭,p-π共轭,σ-p 超2共轭,σ-π超共轭;3 空间效应8. 其它CHO CH 2OH H H OH OH 赤式CHOCH 2OH H H OH HO苏式2Clhv 或高温均裂hv 或高温Cl Br 立体效应(空间效应)范德华张力:扭转张力:两个原子或原子团距离太近,小于两者的范德华半径之和而产生的张力。
高中有机化学学习难点及策略

高中有机化学学习难点及策略高中有机化学是化学学科中的重要部分,也是学生们普遍认为较难的学习内容之一。
有机化学是研究有机化合物的结构、性质、合成及反应规律的一门学科,是化学中的一大难点,主要包括有机物的命名、结构、化学键、反应机理等内容。
本文将探讨高中有机化学学习的难点,并提出相应的解决策略,以帮助学生更好地掌握有机化学知识。
一、难点分析1. 有机物的命名有机物的命名是有机化学中的首要难点,因为有机物数量众多,很多有机物的名称较为复杂,常常需要记忆大量的规则和命名方法。
有机物的同分异构体命名也是一个学生较难掌握的内容。
2. 有机物的结构有机物的结构包括分子式、结构式、立体异构体等,学生需要理解有机物分子的空间构型、键角、键长,这往往需要较强的空间想象力和化学直觉。
3. 化学键有机物中存在不同种类的键,如共价键、极性键、π键等,学生需要理解这些不同类型的键的性质及在有机物中的应用。
4. 反应机理有机化合物的反应机理是学生们比较头疼的问题,有机化合物的反应机理种类繁多,而且有些反应机理比较复杂,学生需要理解反应的条件、速率、过渡态等内容。
二、解决策略1. 建立良好的基础有机化学是建立在化学基础知识的基础上的,学生需要首先巩固好化学的基本理论知识,包括化学键、化学式、构型等基础概念,在此基础上才能更好地学习有机化学知识。
2. 理清思路,逐步深入在学习有机化学知识时,学生应按照有机物的名称、结构、化学键、反应机理等顺序逐步深入,逐步扩展知识面。
在学习过程中,要理清思路,不懂的地方要及时请教老师或同学,及时解决问题,不要等到问题累积到一定程度才解决。
3. 多练习,多总结在学习有机化学知识时,学生要不断地进行练习,多解有机化学的例题和习题,通过练习巩固所学知识,提高解题能力。
要多总结归纳,理解有机化学知识的内在联系和规律。
4. 利用工具和资源学生可以利用各类学习资源,如教科书、教学视频、网络课程、学习app等,辅助自己学习有机化学知识,尤其是一些比较抽象的知识点可以通过多媒体的方式更形象地呈现出来。
有机化合物结构特点与研究方法--高二化学下学期期末重难点易错专题复习 学生版

有机化合物结构特点与研究方法复习专题微专题一:同分异构体的书写与判断1.同分异构体的异构类别(1)碳链异构:由于碳骨架不同产生的异构现象。
如C5H12有三种同分异构体:正戊烷、异戊烷和新戊烷。
(2)位置异构:由于官能团或取代基在碳链或碳环上的位置不同而产生的同分异构现象。
如氯丙烷有两种同分异构体:1-氯丙烷和2-氯丙烷。
(3)官能团异构(又称类别异构):有机物的官能团种类不同,但分子式相同。
如:①单烯烃与环烷烃;②单炔烃和二烯烃、环烯烃;③饱和一元醇和醚;④饱和一元醛和酮;⑤饱和一元羧酸和饱和一元酯;⑥芳香醇、芳香醚和酚;⑦葡萄糖和果糖;⑧蔗糖和麦芽糖;⑨硝基化合物与氨基酸等。
2.同分异构体的书写方法(1)有机物同分异构体的书写方法①烷烃(降碳对称法)主链由长到短支链由整到散位置由心到边(不到端)排布由邻、对到间②烯烃(插入法)先写出可能的碳链形式(碳骨架)再将官能团(双键)插入碳链中(此法也可适用于炔烃、酯等)③醇(取代法)先碳链异构:写出可能的碳链后位置异构:移动官能团(-OH)的位置3.同分异构体的判断方法(1)基元法:如丁基有四种结构,则丁醇有四种同分异构体。
(2)换元法:如二氯苯C6H4Cl2有三种同分异构体,四氯苯也有三种同分异构体(将H替代Cl、Cl替代H)。
(3)对称法(又称等效氢法):等效氢法的判断可按下列三点进行:①同一甲基上的氢原子是等效的;②同一碳原子上所连甲基上的氢原子是等效的;③处于对称位置上的氢原子是等效的。
(4)定一移一法:对于二元取代物的同分异构体的判定,可固定一个取代基位置,再移动另一取代基,以确定同分异构体数目。
1微专题测评1下列烷烃的一氯代物中没有同分异构体的是A.丙烷B.2-甲基丙烷C.丁烷D.新戊烷2下列各种烷烃进行一氯取代反应后,只能生成四种沸点不同的产物的是A.CH3CH2CH3B.CH32CHCH2CH3 C.CH3CH2CH2CH3 D.CH3CH24CH33下列有机物的一氯代物数目最多的是A.CH3CH2CH3B.C. D.4丙烷的二氯取代物的个数是A.3B.4C.5D.65分子式为C9H12的某烃,苯环上有一个取代基,其与足量氢气加成的产物的一氯代物共有A.6种B.11种C.12种D.13种6以下结构的三种烃分子,说法不正确的是A.1mol甲分子内含有10mol共价键B.甲、乙、丙三者互为同系物C.丙分子的二氯取代产物只有三种D.丙与苯乙烯()互为同分异构体7已知A为苯的同系物,且A的分子量为120,则A属于苯的同系物的可能结构有A.5种B.6种C.7种D.8种8某苯的同系物的分子式为C11H16,经分析分子式中除含苯环外(不含其它环状结构),还含有两个“-CH3”,两个“-CH2-”、一个“”它的可能结构式有A.2种B.3种C.4种D.5种9组成和结构可用表示的有机物(不考虑立体结构)共有种A.3种B.12种C.20种D.36种10分子式为C4H8的烯烃的二氯代物中,只含一个甲基的结构有(不考虑立体异构)A.9种B.10种C.11种D.12种微专题二:有机物的分离和提纯1.分离提纯的几种思路(1)杂转纯:如除去Na2CO3中的NaHCO3,将混合物加热使NaHCO3全部转化为Na2CO3。
高中有机化学学习难点及策略

高中有机化学学习难点及策略高中有机化学是化学学科中非常重要的一部分,涉及到许多有机物的结构、性质和反应等内容。
由于其知识点繁杂、有机物种类众多,许多同学在学习时容易感到困难。
下面是高中有机化学学习难点及相应的策略。
一、命名和结构式命名和结构式是有机化学的基础,影响到后续知识点的学习。
因此,正确理解和熟练掌握命名和结构式的规则是高中有机化学学习的第一步。
策略:1.掌握命名规则:通过反复阅读和练习,熟悉各类有机物的命名规则。
这里的练习可以包括在线测试、习题集、参考书等,建议多种方式结合使用。
2.勤画结构式:在学习过程中,关键时刻可以通过画结构式来确认化合物的结构。
在掌握之后,要多进行练习,以加深对结构和型态的理解。
3.相互关联:将命名和结构式的规则相互关联,便于理解和记忆。
例如,命名指导下的结构式;结构式核实下的命名等。
二、共轭体系共轭体系是指一系列相邻的双键或三键分别被单键分开的有机物分子。
由于特殊的电子结构,导致共轭体系在一些反应中表现出同样的特性,因此必须正确理解其性质。
策略:1.理解电子共轭:电子共轭是共轭体系的本质。
从宏观到微观,逐渐深化理解它的形成原因,这对于后面的细节学习、实践操作能够有很好的启示作用。
2.比较异质体不同之处:多比较不同的异构体之间共轭体系的性质和反应特征,对比可以发现共性和不同之处。
3.注意与自由基反应的区别:由于共轭体系的存在,使得共轭体系中的化合物具有自由基反应出现的一些特征,例如自由基链反应。
与此同时,又存在着一些性质上的区别,要特别注意。
三、重要反应有机化学是通过一系列反应学习有机物的性质以及化学反应过程。
其中一些反应比较重要且难点较多,如卤代烃的重排反应、醇酸碱反应、醛酮加成反应等。
策略:1.分类认识反应:对于学过的反应要进行分类,理解反应机制、特点和适用条件,同时要能够加快反应速率和选择一个低副反应的最佳条件。
2.掌握关键原理:对于反应机理和中间体的构成、环境条件和影响,以及重要性质和反应特殊体现也要十分了解。
有机化学重点难点

有机化学1-3章(绪论、烷烃、烯烃)重、难点提示和辅导一.命名1.烷烃的命名烷烃的命名是有机化合物命名的基础,主要有习惯命名和系统命名法,习惯命名法要求掌握“正、异、新”、“伯、仲、叔、季”等字头的含义及用法。
最常用的是系统命名法,要熟练掌握其命名原则和步骤。
(1).选主链选取结构式中最长的碳链为主链,按照主链碳原子数叫做某烷。
十个碳原子以下的数目用甲、乙、丙、丁、戊、己、庚、辛、壬、癸,十个以上碳原子则用十一、十二……等数目表示。
其它较短的链作为主链上的取代基或叫做支链。
注意最长碳链不一定是结构式中的直链。
例如:式中虚线框中的碳链为最长碳链。
(2).将主链碳原子编号从离取代基最近的一端开始用阿拉伯数字编号(从右边开始用1,2,3…表示),取代基所在位次由所连碳原子的号数表示。
注意使各取代基有尽可能小的编号,或取代基位次之和最小。
(3).书写名称取代基名称放在母体名称之前,取代基位次放在取代基名称之前,其间用半字线“-”隔开。
上面化合物被命名为3-甲基-5-乙基辛烷,而不是6-甲基-4-乙基辛烷(从左边编号)。
2.烯烃的命名烯烃中几何异构体的命名是难点,应引起重视。
要牢记命名中所遵循的“次序规则”。
烯烃几何异构体的命名包括顺、反和Z、E两种方法。
简单的化合物可以用顺反表示,也可以用Z、E表示。
用顺反表示时,相同的原子或基团在双键碳原子同侧的为顺式,反之为反式。
如果双键碳原子上所连四个基团都不相同时,不能用顺反表示,只能用Z、E表示。
按照“次序规则”比较两对基团的优先顺序,较优基团在双键碳原子同侧的为Z型,反之为E型。
必须注意,顺、反和Z 、E是两种不同的表示方法,不存在必然的内在联系。
有的化合物可以用顺反表示,也可以用Z、E表示,顺式的不一定是Z型,反式的不一定是E型。
例如:存在几何异构体的烯烃命名的步骤和原则:(1)确定构型:一般用Z、E表示。
例如:按照“次序规则”比较双键碳原子所连两对基团的优先顺序,-CH3 >-H ,-CH2CH2CH3 >-CH2CH3,两个较优基团在双键碳原子两侧,因此,为E型。
高中有机化学重点和难点总结

高中有机化学重点和难点总结
高中有机化学的重点和难点主要涉及以下几个方面:
1. 官能团:官能团是有机化学中的基础概念,每种官能团都有独特的化学性质。
学生需要理解并掌握常见官能团的性质以及它们之间的转化。
2. 反应类型:有机化学中存在多种反应类型,如加成反应、消去反应、氧化反应、还原反应、酯化反应、水解反应等。
学生需要理解每种反应类型的特征以及发生的条件。
3. 有机物的结构:有机物的结构决定了其性质,学生需要理解有机物的构造原理,如碳原子的四面体结构、共价键的形成等。
4. 有机物的合成与分离:有机物的合成与分离是有机化学中的重要实践内容,学生需要掌握常见的合成方法和分离技术。
5. 有机物的应用:了解常见有机物的应用领域和用途,如醇、醛、酸等有机物在日常生活和工业生产中的应用。
针对这些重点和难点,学生可以通过多做习题、参加课外辅导或网上课程等方式来加深理解和掌握。
同时,也要注重实验操作和实践能力的培养,通过实验来加深对有机化学的理解和掌握。
高中有机化学学习难点及策略

高中有机化学学习难点及策略有机化学是高中化学学科的重要组成部分,也是考研、读研乃至科研的基础。
然而,正因其泛化性和庞杂性,一些学生在学习有机化学时会出现难点。
本文旨在探讨有机化学学习中的难点及应对策略。
一、知识框架难点有机化学的知识框架错综复杂,建立在化学反应和分子结构之间。
学生需要运用电子排斥原理、杂化和分子轨道理论、极性和分子内氢键等概念来理解各种反应和分子结构的形成和特性。
个别学生对这些概念的掌握较为困难,从而对后续的学习产生了负面影响。
面对这样的难点,我们需要找到一种适合自己的学习方法。
首先,建议同学们先弄清楚各个概念的定义和本质。
其次,可以通过模型或模拟器来模拟不同的反应和分子间相互作用,用图表或流程图来理清学科知识的框架结构,增加自己的感性认识,深化自己的理论知识。
二、反应机理难点有机化学中的反应机理非常复杂,需要学生理解每个反应的各个步骤、剖析每个反应的反应条件和影响因素。
不过,只看书本知识是很难真正领会反应机理的,需要多看一些原始文献,了解不同思路的实验方法,实验执行过程及结果,才能更好掌握反应机理。
针对反应机理的难点,同学们可以通过模拟器来模拟不同反应的形成过程,学习物质转化的过程。
此外,建议同学多积累做实验的经验,亲身体验不同反应的实际操作,从而更好理解反应机理。
三、实战能力难点有机化学是一门实验型的科学,学生需要通过实验来发现化学规律和研究物质状态,这就要求有机化学的学习必须通过实验进行深度学习,培养科学实验和分析实验结果的实战能力。
然而,由于实验条件和实验操作技巧的限制,个别学生还会遭遇实验无法成功的情况,导致学习产生困难。
解决实验能力难点可以借鉴以下几点:一是多观察实验现象,积累实验规律;二是多进行实验操作,提高手工技能的熟练度,规避实验失误;三是多关注不同实验中的实验设备和材料,进一步理解实验原理,提升实验分析能力。
总之,学习有机化学不能仅仅通过看书来掌握,需要多进行实验、讨论和研究,灵活运用各种方法,提高自己的感性认识和综合分析能力,只有这样,才能在高中和大学学习过程中更好地掌握有机化学知识。
有机化学期末难点

(4)O CH=NNH 2(4)α-呋喃甲醛腙 (6)N NHCONH 2(6)环己酮缩氨脲CH 2=CH-CHO丙烯醛CH 3CH=CH-CHO 2-丁烯醛(巴豆醛)PhCH=CH-CHO 3-苯丙烯醛(肉桂醛)4、OOCH 34、2-甲基-1,4-萘醌(3)HClOHClOH注:由于苯环的特殊稳定性,此处为酮式重排成烯醇式(酚)。
OHK Cr O + H SO 4OOOHOHAg 2O对苯醌4、OZn--Hg5、CH=CHCHO1)NaBH 42)H 3O +6、HC CHH 2O HgSO 4, H 2SO 4稀 NaOH 0-5℃4、 5、CH=CHCH 2OH6、CH 3CHO CH 3CHCH 2CHO OH7、OH CHOCH 3HOAB7、A:B:O CH 3O+CH 3COONaCH 3CH 2OHCH 2=CH 2 + HBr CH 3CH 2BrMg 无水Et 2O CH 3CH 2MgBr(1)CH 3CH 2BrH 2OC 2H 5OH NaOH(2)CrO 吡啶3CHO(3)CH 3CHCH 2CH 3OHCH 3CH 2MgBr +3+CH 33CHCH 2CH OMgBr无水Et 2(注:乙醇氧化为乙醛也可经铜的催化脱氢而制得) CH 2CHCHO 2 EtOH干HClCH 2CH CH(OEt)2CH 2OH CH CH(OEt)2OH 42TM HC CCH 2CH 3H 2O H 3CCOCH 2CH 3244LiAlH 4H 3CCHCH 2CH 3OHHBr TM4、C 6H 6Ph C OHCH 3CH 3(习题6(2) )解:产物为增加碳原子的叔醇,考虑酮与格式试剂。
产物分割有两种方法:(一)Ph MgBr + CH 3COCH 3; (2) Ph C CH 3O+ CH 3MgBr合成一:C 6H 6Br 22)H 3O +TM3PhBrPhMgBr3合成二:C 6H 6CH 3COCl 3Ph CCH 3O 1)CH 3MgBr3+TM7、CH 3COCH 3(CH 3)3CCH 2COCH 3(习题6(1) )HBrMg/Et 2OCrO C 6H 5N(CH 3)2CO (CH 3)3CCH 2CH(OH)CH 31) CH 3CHO 1)CH 3MgBr 3TM(CH 3)3COH 1)HBr 2(CH 3)3CMgBr1)HCHO 3+(CH 3)3CCH 2OH (CH 3)3CCH 2Br(CH 3)3CCH 2MgBr3+6、A(C 5H 12O)[O]→B(C 5H 10O);B+斐林→⨯,可碘仿反应;A+热浓硫酸→C ;C 可使溴水褪色但无顺反异构。
有机化学复习要点

有机化学复习要点有机化学是研究有机物(含碳的化合物)的合成、结构、性质和反应的科学。
下面是有机化学复习的重点要点:1.有机化合物的分类:根据碳的连接方式,有机化合物可分为链状、环状和支链状化合物。
根据它们的官能团,化合物可以被进一步分类为醇、酮、酯、醛、酸、胺等等。
2.有机化合物的命名:有机化合物的命名是有机化学的基础。
在命名时,需要确定主链、编号碳原子、标记官能团和提供适当的前缀和后缀。
3.有机化合物的构造:有机化合物的构造表示确定其分子的原子结构,包括原子的类型、化学键的类型(单键、双键、三键)和宇称等。
4.共价键的极性:共价键是由两个原子之间共享电子形成的,极性共价键指电子不均匀地共享。
这导致一侧带有部分正电荷,而另一侧带有部分负电荷,形成极性分子。
5.引入官能团:官能团是有机化合物中特定原子或原子组合的集合,确定化合物的性质和反应。
常见官能团有羟基(-OH)、醛基(-CHO)、酮基(-C=O)、羧基(-COOH)、胺基(-NH2)等等。
6.有机反应的基本原理:有机反应是有机化学的核心,包括加成反应、消除反应和取代反应。
加成反应是指在化合物中添加一个原子或基团;消除反应是指分子中的两个基团消除,形成一个双键或三键;取代反应是指一个基团被替换成另一个基团。
7.重要的有机反应:有机化学有许多重要的反应,其中一些包括酯化、醇酸化、加氢、亲电取代、亲核取代、还原和氧化等等。
了解这些反应及其机理对于理解有机化学非常重要。
8.常见的有机化学术语:在有机化学中,有许多常见的术语和概念,例如:轴手性、对映体、立体异构体、环状化合物等等。
了解这些术语可以帮助理解和解决有机化学问题。
9.溶剂的选择:在有机化学实验中,溶剂的选择非常重要。
常见的有机溶剂包括乙醇、丙酮、乙醚、二甲基甲酰胺等等,选择合适的溶剂可以促进反应的进行。
10.立体化学:立体化学涉及分子和化合物的空间构型和对称性。
手性和立体异构体是立体化学的重要概念,影响分子的性质和化学反应。
高一必修2有机化学期末复习提纲

第三章有机化学知识点总结有机化合物:含有碳元素的化合物。
常有氢和氧,还含有氮、磷、硫、卤素等元素。
【注意】(碳的氧化物、碳酸及其盐、碳的金属化合物是无机化合物)。
烃:只含有碳和氢两种元素的有机物,甲烷是最简单的烃。
一、甲烷空间结构:正四面体结构(四个C-H键的长度和强度相同,夹角相等)2、物理性质:甲烷是一种没有颜色,没有气味的气体。
密度比空气小,极难溶于水。
(可以用排水法和向下排空气法收集甲烷)3、化学性质:通常情况下,甲烷比较稳定,与酸性高锰酸钾等强氧化剂不反应,与强酸、强碱也不反应。
但在一定条件下,甲烷也会发生某些反应。
1)燃烧反应:CH4+2O2CO2+2H2O 。
(纯净的甲烷在空气中安静地燃烧,火焰呈淡蓝色)2)取代反应:(有机化合物分子里的原子或原子团被其它原子或原子团所代替的反应)甲烷与氯气的反应方程式①。
②。
③。
④。
★(条件:光照)五种产物(两种气体:一氯甲烷和氯化氢,其他三种均为液体)甲烷与氯气取代反应实验现象:气体颜色逐渐变浅,试管壁有油状液滴出现,同时试管上方有白雾生成,试管内液面逐渐降低。
二、烷烃:(烃分子中碳原子之间都以碳碳单键结合成链状,剩余价键均与氢原子结合,使每个碳原子的化合价都达到“饱和”,这样的烃叫做饱和烃,也称为烷烃)。
分子通式为C n H2n+21、烷烃的命名:烷烃碳原子数在十以内时,以甲、乙、丙、丁、戊、己、庚、辛、壬、癸依次代表碳原子数,其后加“ 烷”字,碳原子数在十以上时,以“汉字数字”代表。
例如:十一烷。
2、烷烃的物理性质:常温下的状态(设碳原子数为n),当n ≤4 时为气态;随着碳原子数的增加,烷烃的熔沸点依次升高,烷烃的密度依次增大。
3. 烷烃的化学性质:1、稳定性:与甲烷类似,通常情况下,不与强酸、强碱、高锰酸钾等强氧化剂反应。
2、可燃性:都能燃烧,反应通式为C n H2n+2+213nO2nCO2+(n+1)H2O。
3、在光照条件下能与氯气发生取代反应。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
期末复习重点及难点一、有机化合物命名有机合物的命名包括俗名、习惯命名、系统命名等方法,要求能对常见有机化合物写出正确的名称或根据名称写出结构式或构型式。
1、俗名及缩写要求掌握一些常用俗名所代表的化合物的结构式,如:木醇、甘醇、甘油、石炭酸、蚁酸、水杨醛、水杨酸、氯仿、草酸、苦味酸、肉桂酸、苯酐、甘氨酸、丙氨酸、谷氨酸、巴豆醛、葡萄糖、果糖等。
还应熟悉一些常见的缩写及商品名称所代表的化合物,如:RNA、DNA、阿司匹林、福尔马林、扑热息痛、尼古丁等。
2、习惯命名法要求掌握“正、异、新”、“伯、仲、叔、季”等字头的含义及用法,掌握常见烃基的结构,如:烯丙基、丙烯基、正丙基、异丙基、异丁基、叔丁基、苄基等。
3、系统命名法系统命名法是有机化合物命名的重点,必须熟练掌握各类化合物的命名原则。
其中烃类的命名是基础,几何异构体、光学异构体、多官能团化合物和杂环化合物的命名是难点,应引起重视。
4、几何异构体的命名烯烃几何异构体的命名包括顺、反和Z、E两种方法。
重点掌握Z、E表示法。
要牢记命名中所遵循的“次序规则”。
必须注意,顺、反和Z、E是两种不同的表示方法,不存在必然的内在联系。
有的化合物可以用顺反表示,也可以用Z、E表示,顺式的不一定是Z型,反式的不一定是E型。
5、双官能团化合物命名双官能团化合物的命名双官能团和多官能团化合物的命名关键是确定母体。
常见的有以下几种情况:① 当卤素和硝基与其它官能团并存时,把卤素和硝基作为取代基,其它官能团为母体。
② 当双键与羟基、羰基、羧基并存时,不以烯烃为母体,而是以醇、醛、酮、羧酸为母体。
③ 当羟基与羰基并存时,以醛、酮为母体。
④ 当羰基与羧基并存时,以羧酸为母体。
⑤ 当双键与三键并存时,应选择既含有双键又含有三键的最长碳链为主链,编号时给双键或三键以尽可能低的数字,如果双键与三键的位次数相同,则应给双键以最低编号。
6、杂环化合物命名由于大部分杂环母核是由外文名称音译而来,所以,一般采用音译法,要注意取代基的编号。
二、有机化合物基本结构理论1、能判断有机化合物分子中各碳原子的杂化形式。
掌握σ键和π键的形成及它们的区别,共轭π键和芳香大π键的特性以及双键、叁键是由什么键组成的。
2、掌握各种类型的同分异构,要求能举出各种异构体的例子。
3、要求掌握诱导效应和共轭效应产生的原因及特点,用电子效应解释取代基对羧酸、酚酸性的影响及对胺碱性的影响;解释不对称烯烃进行亲电加成时所遵循的马氏规则、卤代烃和醇进行消除时所遵循的查依采夫规则、不同结构的卤代烃进行亲核取代反应的活性、羰基化合物进行亲核加成反应的活性等。
三、化学反应加成反应(1)要求掌握不对称烯烃进行亲电加成反应时所遵循的马氏规则,即试剂中带正电核的部分加到含氢较多的双键碳原子上,而负性部分加到含氢较少的双键碳原子上。
烯烃加卤素、卤化氢、硫酸、次卤酸、水,炔烃加卤素、卤化氢、水以及共轭双烯的1,2和1,4加成都是亲电加成反应。
烯烃进行亲电加成反应时,双键上电子云密度越大,反应越容易进行。
(2)要掌握亲核试剂的概念、亲核加成反应的历程(简单加成及加成─消除)、不同结构的羰基化合物进行亲核加成反应的活性顺序及影响反应活性的因素。
羰基化合物与氰氢酸、亚硫酸氢钠、醇、格氏试剂、氨及氨衍生物的加成都是亲核加成反应。
羰基化合物进行亲核加成反应的活性顺序为:HCHO>CH3CHO>RCHO>C6H5CHO>CH3COCH3>RCOCH3>C6H5COCH3>C6H5COC6H5(3)掌握烯烃在过氧化物存在下与溴化氢进行的加成是自由基加成。
不对称烯烃与溴化氢进行自由基加成时得到反马氏规则的产物,即氢加到含氢较少的双键碳原子上。
(4)不饱和烃的催化氢化。
(5)共轭二烯的双烯合成。
消除反应(1)卤代烃脱卤化氢:卤代烃的消除反应是在强碱性条件下进行。
不同结构的卤代烃进行消除反应的活性顺序为:三级>二级>一级。
要掌握卤代烃进行消除反应时所遵循的查依采夫规则,当卤代烃中不只含有一个β碳时,消除时脱去含氢少的β碳上的氢原子。
要注意,卤代烃的消除和水解是竞争反应。
(2)醇的消除:醇的消除反应在强酸性条件下进行,消除方向也遵循查依采夫规则。
要掌握不同结构的醇进行消除反应的活性顺序:叔醇>仲醇>伯醇。
取代反应(1)掌握苯环上的卤化、硝化、磺化、付氏烷基化和酰基化以及重氮盐的偶合反应等,它们都是亲电取代反应,萘环和芳香杂环上也能发生亲电取代反应。
要注意苯环上有致钝基团时不能进行付氏反应,苯环上进行烷基化时会发生异构化现象。
(2)掌握五员、六员芳香杂环化合物的亲电取代反应以及它们与苯环比较进行亲电取代反应活性的差异,呋喃、噻吩、吡咯进行亲电取代反应的活性比苯大,而吡啶比苯小。
(3)掌握卤代烃的水解、醇解、氰解、氨解,醇与氢卤酸的反应,醚键的断裂,羧酸衍生物的水解、醇解、氨解等,它们都是亲核取代反应。
要在理解反应历程的基础上掌握不同卤代烃进行亲核取代反应的活性。
要注意,在碱性条件下卤代烃的取代和消除是互相竞争的反应,三级卤代烃容易发生消除,一级卤代烃易发生取代,强极性溶剂(如水)有利于取代,而弱极性溶剂(如醇)和强碱(如醇钠)有利于消除,高温有利于消除。
(4)掌握烷烃的卤代,烯烃和烷基苯的α卤代,它们是自由基取代反应。
反应条件是高温、光照或过氧化物存在。
氧化还原反应(1)烯、炔、芳烃侧链以及醇、酚、醛、酮等易发生氧化反应,常用的氧化剂有高锰酸钾、重铬酸钾的硫酸溶液、氧气(空气)、臭氧以及托伦试剂、斐林试剂、次卤酸钠等。
(2)醛、酮、羧酸及酯还原为醇,硝基苯还原为苯胺等都是还原反应。
常用的还原剂有H2/Ni、 Na+C2H5OH、Fe+HCl、NaBH4、LiAlH4、异丙醇/异丙醇铝等。
还有羰基还原为亚甲基的两种方法,注意,进行克莱门森还原时反应物分子中不能存在对酸敏感的基团,如醇羟基、双键等,用伍尔夫─吉日聂尔还原及黄鸣龙改进法时,反应物分子中不能带有对碱敏感的基团,如卤素等。
缩合反应(1)羟醛缩合含有α氢的醛在稀碱条件下生成β—羟基醛,此化合物不稳定,受热容易脱水,生成α、β不饱和醛。
(2)克莱森酯缩合含有α氢的酯在强碱条件下发生克莱森酯缩合,两分子酯之间脱去一分子醇生成β酮酸酯。
重氮化及芳香重氮盐取代。
重氮化反应注意反应条件及产物。
芳香重氮盐的取代反应在有机合成中广泛应用。
四、有机化合物的转化及合成要求掌握有机化合物各类官能团之间的转化关系、增长和缩短碳的方法,在此基础上设计简单有机化合物的合成路线。
苯进行付氏烷基化、酰基化、炔化物的烃化、羟醛缩合、格氏试剂法等都可以增长碳链;炔化物的烃化、格氏试剂法及芳香重氮盐等在有机合成中应用非常广泛。
1、炔化物的烃化具有炔氢的炔烃与氨基钠作用得炔钠,炔钠与伯卤代烃反应得到烷基取代得炔烃。
此反应可增长碳链,制备高级炔烃。
2、格氏试剂法格氏试剂在有机合成中应用极为广泛,它与环氧乙烷、醛、酮、酯反应可用来制备不同结构的醇等。
这些反应既可增长碳链,又可形成所需的官能团。
3、重氮盐取代法芳香重氮盐的重氮基可被氢原子、卤素、羟基、氰基取代,由于苯环上原有取代基定位效应的影响而使某些基团不能直接引入苯环时,可采用重氮盐取代的方法。
要注意被不同基团取代时的反应条件。
五、有机化合物的鉴别1、烯烃、二烯、炔烃鉴别方法:溴的四氯化碳溶液,溴腿色2、含有炔氢的炔烃:硝酸银或氯化亚铜的氨溶液,生成炔化银白色沉淀或炔化亚铜红色沉淀。
3、卤代烃:硝酸银的醇溶液,生成卤化银沉淀;不同结构的卤代烃生成沉淀的速度不同,叔卤代烃和烯丙式卤代烃最快,仲卤代烃次之,伯卤代烃需加热才出现沉淀。
4、醇:与金属钠反应放出氢气(鉴别6个碳原子以下的醇);用卢卡斯试剂鉴别伯、仲、叔醇,叔醇立刻变浑浊,仲醇放置后变浑浊,伯醇放置后也无变化。
5、酚或烯醇类化合物:用三氯化铁溶液产生颜色。
苯酚与溴水生成三溴苯酚白色沉淀。
6、羰基化合物:2,4-二硝基苯肼,产生黄色或橙红色沉淀;区别醛与酮用托伦试剂,醛能生成银镜,而酮不能;区别芳香醛与脂肪醛或酮与脂肪醛,用斐林试剂,脂肪醛生成砖红色沉淀,而酮和芳香醛不能;鉴别甲基酮和具有CH3—CH—结构的醇用碘的氢氧化钠溶液,生成黄色的碘仿沉淀。
7、甲酸:用托伦试剂,甲酸能生成银镜,而其他酸不能。
8、胺:区别伯、仲、叔胺有两仲方法(1)用苯磺酰氯或对甲苯磺酰氯,在NaOH溶液中反应,伯胺生成的产物溶于NaOH;仲胺生成的产物不溶于NaOH溶液;叔胺不发生反应。
(2)用NaNO2+HCl:脂肪胺:伯胺放出氮气,仲胺生成黄色油状物,叔胺不反应。
芳香胺:伯胺生成重氮盐,仲胺生成黄色油状物,叔胺生成绿色固体。
9、糖:葡萄糖与果糖:用溴水,葡萄糖能使溴水腿色,而果糖不能。
麦芽糖与蔗糖:用托伦试剂或斐林试剂,麦芽糖可生成银镜或砖红色沉淀,而蔗糖不能。
六、排列化合物顺序(一)沸点高低:1、烷烃的沸点随分子量的增加而升高,在相同碳数的异构体中,支链越多的沸点越低。
2、低分子量的醇的沸点比相近分子量的烷烃高得多。
3、醛酮的沸点比相近分子量的烃高,但比醇低。
4、羧酸的沸点比分子量相近的醇还高。
(二)酸性强弱:在羧酸的分子中,带有吸电子取代基使羧酸的酸性增强,带有给电子取代基使羧酸的酸性减弱;取代基距离羧基越近对羧酸的酸性影响越大。
(三)碱性强弱:1、脂肪胺的碱性比氨强,芳香胺的碱性比氨弱;在脂肪胺中,二级胺的碱性最强。
2、吡啶的碱性比吡咯强,也比苯胺强,但比脂肪胺弱得多。
(四)反应活性的大小1、苯环上亲电取代反应活性。
2、卤代烃亲核取代反应的活性。
3、羰基化合物亲核加成反应活性。
