水总硬度的测定
实验 水的总硬度测定

实验水的总硬度测定水的总硬度是指水中包括钙和镁的盐类含量的总和。
硬度是水质的一个关键指标,因为高硬度的水可能导致很多问题,例如水垢、管道结垢和洗涤剂余留,影响生活和工业使用。
因此,测定水的总硬度对于监测和保护水资源至关重要。
本实验将介绍几种不同的测定水总硬度的方法,以及如何评估样品中的硬度级别。
材料:- 试剂:分别是0.01M EDTA(乙二胺四乙酸)试剂、Eriochrome Black T指示剂,硝酸钡、氯化铯标准溶液。
- 仪器:烧杯、容量瓶、移液管、分析天平。
实验步骤:第一种:滴定法(管理员/Expert建议使用)1. 取50毫升的水样,并进行过滤和清洁,以去除悬浮物和颗粒物。
2. 将50毫升的样品倒入250毫升锥形瓶中。
加入2毫升的Eriochrome Black T指示剂,并用0.01 N HCl调整pH为6.0±0.1。
3. 在滴定中添加0.01M EDTA试剂,反应至溶液颜色变红蓝色,表示钙离子和镁离子都与EDTA配位了,达到终点。
记录所需的体积,这是水样中总硬度的指标。
4. 重复上述步骤,进行三次滴定,确保获得可靠的结果。
5. 计算总硬度的浓度,单位通常为毫克/L(mg/L)。
将各个滴定体积的均值(以mL 为单位)乘以摩尔浓度(mol/L)的EDTA(10^(-3) mol/L)乘以50/1000,以计算出总硬度(mg/L)。
第二种:沉淀法2. 在样品中加入若干氯化铯试剂。
这会沉淀掉样品中的硫酸盐、碳酸盐和硬度离子。
3. 沉淀物稍加加热,分离清液和沉淀物。
4. 沉淀物用硝酸钡溶液滴定,测量其中硫酸盐的含量。
5. 通过查阅基准表格,将SO4^2-的浓度转换为硬度值,以获得样品的总硬度。
第三种:离子选择性电极法2. 将样品注入离子选择性电极测量室,并将电极移入其中。
该电极会测量水中钙和镁的离子浓度。
3. 根据测定结果,得出样品中钙和镁离子的总量,以计算样品硬度。
结果分析:1. 根据测定结果,确定水样中的硬度水平。
水中总硬度的测定

提高水质硬度测定准确性的建议
规范操作流程
01
制定并遵守标准化的操作流程,确保测定过程中的每一步都符
合规范要求。
使用高质量试剂和仪器
02
选用高质量的试剂和仪器,确保测定的准确性和稳定性。
加强人员培训
03
对操作人员进行专业培训,提高其技能水平,确保操作的规范
性和准确性。
THANKS
指示剂添加
在滴定过程中,加入铬黑T指 示剂,观察颜色变化。
数据记录
记录滴定过程中使用的EDTA 标准溶液体积、水样体积以及
实验温度等信息。
实验结果分析
数据处理
根据滴定数据计算水中总硬度含量,并进行误差分析。
结果判断
根据计算结果判断水样中总硬度是否符合标准要求。
结果报告
撰写实验报告,包括实验目的、实验原理、实验步骤、 数据分析和结论等内容。
EDTA标准溶液等。
准备好实验所需的仪器 设备,如滴定管、容量
瓶、烧杯等。
确保实验环境干净整洁, 避免外界因素干扰实验
结果。
实验操作步骤
01
02
03
04
水样预处理
对水样进行适当的预处理,如 过滤、稀释等,以便后续操作
。
滴定操作
使用滴定管加入适量EDTA标 准溶液,并使用缓冲液调节 pH值,然后进行滴定操作。
预防疾病
硬水中的矿物质元素如钙、 镁等对身体健康有益,适 量摄入有助于预防某些疾 病。
节约能源
硬水在加热过程中不易形 成水垢,可以减少热水器 等设备的能耗。
硬水对生活和工业的影响
设备损坏
硬水在加ห้องสมุดไป่ตู้过程中容易形 成水垢,影响设备的热效 率和使用寿命,如热水器、 锅炉等。
水中总硬度的测定
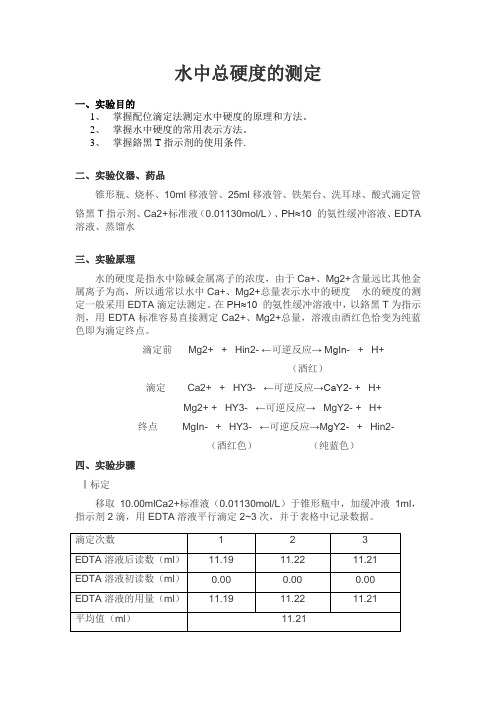
水中总硬度的测定一、实验目的1、掌握配位滴定法测定水中硬度的原理和方法。
2、掌握水中硬度的常用表示方法。
3、掌握鉻黑T指示剂的使用条件.二、实验仪器、药品锥形瓶、烧杯、10ml移液管、25ml移液管、铁架台、洗耳球、酸式滴定管铬黑T指示剂、Ca2+标准液(0.01130mol/L)、PH≈10 的氨性缓冲溶液、EDTA 溶液、蒸馏水三、实验原理水的硬度是指水中除碱金属离子的浓度,由于Ca+、Mg2+含量远比其他金属离子为高,所以通常以水中Ca+、Mg2+总量表示水中的硬度水的硬度的测定一般采用EDTA滴定法测定。
在PH≈10 的氨性缓冲溶液中,以鉻黑T为指示剂,用EDTA标准容易直接测定Ca2+、Mg2+总量,溶液由酒红色恰变为纯蓝色即为滴定终点。
滴定前Mg2+ + Hin2- ←可逆反应→ MgIn- + H+(酒红)滴定 Ca2+ + HY3- ←可逆反应→CaY2- + H+Mg2+ + HY3- ←可逆反应→MgY2- + H+终点MgIn- + HY3- ←可逆反应→MgY2- + Hin2-(酒红色)(纯蓝色)四、实验步骤Ⅰ标定移取10.00mlCa2+标准液(0.01130mol/L)于锥形瓶中,加缓冲液1ml,指示剂2滴,用EDTA溶液平行滴定2~3次,并于表格中记录数据。
Ⅱ测定移取25.00ml自来水于锥形瓶中,加缓冲液1ml,指示剂2滴,滴定至终点,平行滴定2~3次,并于表格中记录数据。
五、实验数据记录及处理实验数据已填于上述表格中实验数据计算:EDTA溶液浓度标定:由C(Ca2+)*V(Ca2+)=C(EDTA)*V(EDTA)得C(EDTA)= C(Ca2+)*V(Ca2+)/V(EDTA)= 0.01130mol/l*10.00ml/11.21ml =0.01008mol/l自来水硬度测定:由n(EDTA)=C(EDTA)V(EDTA)n(Caco3):n(EDTA)=1:1 n(Caco3)=m (Caco3)/ M(Caco3)自来水硬度ρ=m (Caco3)/ Vaq 所以计算可得ρ=0.135g/l=135mg/l六、注意事项:1.各个使用仪器用前需要润洗的注意润洗;2. 络合反应速度较慢,滴定时滴加速度不能太快,特别是临近终点时,要边滴边摇晃。
水的总硬度的测定

水的总硬度的测定水的总硬度的测定一、目的要求1.了解EDTA测定水的总硬度的基本原理。
2.把握水的总硬度的测定方法。
二、基本原理在pH=10时,EDTA能与钙、镁形成稳定的搭配物,其稳定性比铬黑T与镁形成的搭配物的稳定性强。
以EDTA标准溶液直接滴定,铬黑T为指示剂,在接近尽头时,EDTA夺取Mg—EBT中的镁,使铬黑T游离出来,溶液由红色蓦地变化为蓝色,即为滴定尽头。
滴定时,加入三乙醇胺和KCN来除去水中少量的Fe3+、Al3+、Cu2+、Pb2+等离子的干扰。
三、试剂1.铬黑T指示剂:0.5g铬黑T与50g氯化钠充分混合。
2.氨—氯化铵缓冲溶液(pH=10):称取5.4g氯化铵,加适量水溶解后,加入35ml氨水,再加水稀释至100ml。
3.1%KCN溶液4.1:1三乙醇胺5.1:1HCl溶液6.钙指示剂:0.5g钙指示剂与50g氯化钠充分混合7.0.01mol/L钙标准溶液: **称取干燥(110℃)至恒重的0.5g基准碳酸钙于250ml烧杯中,用1:1的HCl溶液加热完全溶解,冷却后转入500ml的容量瓶中,用水稀释至刻度,摇匀。
8.0.01mol/LEDTA标准溶液的配制与标定。
配制:称取3.7gEDTA二钠盐(分子量为372.2),用去离子水稀释至1000ml,摇匀,贮存于聚乙烯瓶中待标定。
标定:用移液管精准移取25.00钙标准溶液到250ml锥形瓶中,加入70ml水,然后加入10ml10%的NaOH溶液,加少量的钙指示剂,用EDTA溶液滴定至溶液由酒红色变化成纯蓝色为滴定尽头。
记录消耗EDTA的体积V(EDTA)。
平行测定三次。
计算公式:c(EDTA)=四、操作方法精准吸取水样100.00ml于锥形瓶中,加入三乙醇胺6ml、KCN 溶液1ml、氨—氯化铵缓冲溶液10ml、铬黑T指示剂少许,用EDTA 标准溶液滴定至溶液由红色变为蓝色即为尽头。
记录消耗EDTA标准溶液的体积。
平行测定三次。
水总硬度检测方法

水总硬度检测方法硬水是指含有较高浓度钙、镁离子的水,对于人体健康和家庭设备的使用都有一定程度的影响。
因此,准确测量水的硬度对于人们选择适当的水处理方法非常重要。
本文将介绍几种常见的水总硬度检测方法,帮助读者了解如何准确测量水的硬度。
一、滴定法滴定法是一种广泛应用于水质检测中的方法,也可用于测定水的总硬度。
这种方法需要使用到 EDTA(乙二胺四乙酸)指示剂和乙锭紫溶液。
具体步骤如下:1. 用取样瓶收集待测水样。
2. 取 100 mL 待测水样,加入少量乙锭紫溶液,并用准确称量的EDTA 标准溶液进行滴定。
3. 滴定过程中,EDTA 过量配比溶液将与水中的镁和钙离子反应生成络合物,溶液颜色由红变为蓝或紫。
4. 当颜色变为蓝色或紫色时,停止滴定,并记录所用的 EDTA 标准溶液的体积。
5. 用以下公式计算水样的总硬度:总硬度(mg/L)= EDTA 标准溶液的体积 ×溶液浓度 × 1000 / 取样体积。
二、离子选择电极法离子选择电极法是一种便捷、准确测定水样离子含量的方法。
通过离子选择电极(如钙离子选择电极或镁离子选择电极)与电位计配合使用,测量水样中钙离子或镁离子的浓度,并计算水的总硬度。
具体步骤如下:1. 根据离子选择电极的说明书调节电极,确保其工作在最佳状态。
2. 使用清洁的容器收集待测水样,避免污染。
3. 将离子选择电极浸入水样中,等待电位计稳定。
4. 读取电位计所示的电位值,并记录。
5. 根据离子选择电极的校准曲线,计算水样中钙离子或镁离子的浓度。
6. 根据水样中钙离子和镁离子的浓度,计算水的总硬度。
三、原子吸收光谱法原子吸收光谱法是一种高灵敏度的测定水样中金属离子含量的方法,也可以用于测定水的总硬度。
该方法使用特定金属离子(如钙和镁)的特征吸收光谱进行分析。
具体步骤如下:1. 准备标准溶液:根据不同硬度水样的需求,配制一系列不同浓度的标准溶液,范围覆盖待测水样的浓度范围。
水的总硬度的测定

水的总硬度的测定一、实验原理1 EDTA标准溶液的标定原理以CaCO3为基准物标定EDTA,选用铬黑T指示剂指示终点,用氨性缓冲溶液控制pH ≈10。
滴定前:MgY +EBT(蓝)+ Ca2+ =CaY + Mg—EBT(酒红色)滴定中:Ca2+ + Y= CaY终点时:Mg—EBT(酒红色)+ Y = MgY +EBT(蓝)2 水的总硬度测定原理水的总硬度是指水中Ca2+、Mg2+的总量。
在pH ≈10的氨性缓冲溶液中,以铬黑T(EBT)为指示剂,采用EDTA标准溶液直接测定Ca2+、Mg2+总量。
滴定前:Mg2+ +EBT(蓝)= Mg—EBT(酒红色)滴定中:Ca2+ + Y= CaY Mg2+ + Y= MgY终点时:Mg—EBT(酒红色)+ Y = MgY + EBT(蓝)二、实验步骤(一)EDTA标准溶液的配制与标定1.0.01mol·L-1EDTA标准溶液的配制称取EDTA二钠盐 1.1 g于500 mL烧杯中,在烧杯中加水300mL 、温热溶解、冷却后转移至试剂瓶,摇匀。
2.0.01 mol·L -1钙标准溶液的配制准确称取CaCO 3 0.21~0.22g 于100 mL 烧杯中。
先用少量水润湿,盖上表面皿,从烧杯嘴滴加5mL 6mol·L -1HCl 溶液使CaCO 3全部溶解(注意:5mLHCl 不用加完,溶解完后,再补加1~2滴即可)。
加水使溶液总量约50mL ,微沸几分钟以除去CO 2。
冷却后用少量水冲洗表面皿,定量地转移至250 mL 容量瓶中,用水稀释至刻度,定容、摇匀。
3.EDTA 溶液浓度的标定移取25.00 mL 钙标准溶液置于250mL 锥形瓶中,加1滴0.05%甲基红,用(1+2)NH 3·H 2O 溶液中和至溶液由红色变浅黄色。
加3mLMg-EDTA ,再加5mL 氨性缓冲溶液及4滴铬黑T 指示剂,摇匀后立即用0.01 mol·L -1EDTA 溶液滴定至溶液由酒红色变为纯蓝色即为终点。
水的总硬度测定

⽔的总硬度测定实验⼆、⽔的总硬度的测定⼀、实验⽬的1.学习EDTA标准溶液的配制及标定⽅法。
2.了解⽔的硬度的测定意义和常⽤的硬度表⽰⽅法。
3.掌握EDTA法测定⽔的硬度的原理和⽅法。
4.掌握铬⿊T等⾦属指⽰剂的应⽤,了解⾦属指⽰剂的特点。
⼆、实验原理1⼄⼆胺四⼄酸(简称EDTA)能和Ca2+Zn2+ Mg2+等许多⾦属离⼦按照1:1的⽐例络合,形成⽆⾊的EDTA⾦属络合物。
M n+代表⾦属离⼦,Y代表EDTA, 上述反应可⽤下式表⽰:M n++ Y----[MY]n+。
根据络合反应到达终点,即⾦属离⼦完全被络合时所消耗的EDTA的量,推算出⾦属离⼦的量。
反之,也可以根据⾦属离⼦的量推算EDTA的量如何判断⾦属离⼦完全被络合了呢?需要⽤⾦属指⽰剂来指⽰。
⾦属指⽰剂也能够和⾦属离⼦形成络合物,⽽且指⽰剂本⾝的颜⾊和指⽰剂与⾦属离⼦形成的络合物的颜⾊是不同的。
(⼆甲酚橙指⽰剂本⾝显黄⾊,与Zn2+等的络合物呈紫红⾊,铬⿊T 指⽰剂本⾝显蓝⾊,与Zn2+等的络合物呈紫红⾊)同时,指⽰剂和⾦属离⼦的络合能⼒要⽐EDTA络合能⼒弱。
⽤EDTA溶液滴定⾄近终点时,指⽰剂被游离了出来,溶液发⽣颜⾊改变。
2、⽔的硬度主要是⽔中含有Ca2+和Mg2+离⼦形成的,其他⾦属离⼦如Al3+、Fe3+、Mn2+、Zn2+、Cu2+等离⼦也形成硬度,但⼀般含量甚微,在测量硬度时可忽略不计。
硬度有暂时硬度和永久硬度,⽔中的Ca2+、Mg2+的酸式碳酸盐加热能被分解出沉淀⽽除去,这种盐形成的硬度叫暂时硬度,Ca、Mg的其他盐类(如硫酸盐、氯化物等),经加热不能分解,这种盐形成的硬度叫永久硬度,暂时硬度和永久硬度的总和就是总硬度。
测定⽔的总硬度⼀般采⽤络合滴定法,⽤EDTA标准溶液直接测定Ca、Mg总量,然后换算成相应的硬度单位。
测Ca、Mg总量时,⼀般是在pH=10的氨性缓冲溶液中进⾏,⽤铬⿊T做指⽰剂,等当点前,Ca、Mg和铬⿊T形成紫红⾊的络合物,当⽤EDTA标准溶液滴定⾄等当点时,游离出指⽰剂,溶液呈现铬⿊T的纯蓝⾊。
水的总硬度的测定

>水的总硬度的测定总硬度 (Total hardness)是指水中钙、镁离子的总浓度,并换算成氧化钙计算。
硬度对工业用水关系很大,尤其是锅炉用水。
各种工业对水的硬度都有一定的要求。
饮用水中硬度过高会影响肠胃的消化功能,我国生活饮用水卫生标准中规定总硬度(以CaCO<sub>3</sub>计)不得超 450mg/L。
总硬度的测定方法有:① EDTA 络合滴定法,此方法使用设备简单、快速,是一般常选用的方法。
②原子吸收法,该方法简单、快速、灵敏、准确,干扰易于消除。
当用 EDTA 法测定有干扰时,最好改用原子吸收法。
③等离子发射光谱法,此方法快速、灵敏度高、干扰少,且可同时测定多种元素。
(一)实验方法:EDTA 络合滴定法(二)实验原理在 PH10 的条件下,用 EDTA 溶液络合滴定钙和镁离子,用铬黑T 作指示剂。
铬黑T能与水中钙和镁离子形成紫色或紫红色络合物。
滴定中游离的钙、镁离子首先与 EDTA 反应,与指示剂络合的钙和镁离子随后与 EDTA反应,到达终点时,钙、镁离子全部与 EDTA 络合而使铬黑T 游离,溶液由紫红色变为天蓝色。
(三)仪器(1)50ml 酸式滴定管(2)100mL 量筒(3)250mL 三角瓶(四)药品(1)乙二胺四乙酸二钠(简称EDTA-2Na 或Na<sub>2</sub>H<sub>2</sub>Y·2H<sub>2</sub>O )(2)氯化铵(3)硫酸镁(4)铬黑T(5)硫化钠(6)盐酸羟胺(7)浓氨水(8)碳酸钙或锌粒(9)氯化钠(五)试剂(1)氯化铵-氨水溶液(试剂A):称取 16.9g 氯化铵,溶于 143mL 浓氨水中。
(2)EDTA-Mg 溶液(试剂B):称取0.78g 硫酸镁(MgSO<sub>4</sub>·7H<sub>2</sub>O)及 1.179g EDTA-2Na 二水合物,溶于50mL 蒸馏水中,加入 2mL 试剂A、5滴铬黑T 指示剂或 0.2g铬黑T干粉,用0.01mol/L EDTA 溶液滴定至溶液由紫红色变为天蓝色。
水中总硬度的测定

水中总硬度的测定水中总硬度测定的重要性及应用一、水中总硬度概述水中总硬度是指水中溶解的钙和镁离子浓度的总和。
钙和镁是构成硬水的主要金属离子,它们在水中溶解的量决定了水的硬度。
硬度是衡量水质的一个重要指标,对于生活用水、工业用水和环保领域都有着重大的影响。
二、水中总硬度测试方法1. 滴定法:滴定法是一种常用的水中总硬度测试方法。
其原理是利用钙离子和镁离子与某些指示剂反应,当达到一定浓度时,指示剂会发生颜色变化,从而可以确定水中钙镁离子的总量。
该方法具有操作简单、快速、准确度高等优点。
但需要注意的是,滴定法只能测定钙镁离子的总量,无法分别测定各自的数量。
2. 双试剂法:双试剂法是一种改进的滴定法,可以分别测定水中钙离子和镁离子的数量。
其原理是利用两种不同的试剂分别与钙离子和镁离子反应,通过滴定来确定各自的数量。
双试剂法的优点是可以获得水中钙离子和镁离子的具体含量,但操作相对复杂,耗时较长。
三、实验操作过程及注意事项以双试剂法为例,实验操作过程如下:1. 准备好实验用的仪器和试剂,如滴定管、三角瓶、电子天平等。
2. 配制好双试剂,分别用于测定钙离子和镁离子。
3. 取一定量的水样,用移液管或吸管加入三角瓶中。
4. 加入第一试剂,搅拌均匀,放置一段时间,观察颜色变化。
5. 加入第二试剂,继续搅拌均匀,放置一段时间,观察颜色变化。
6. 用滴定管滴定第一试剂和第二试剂,记录滴定量。
7. 根据滴定量计算水中钙离子和镁离子的含量。
注意事项:1. 实验操作过程中要保证试剂的纯度和精度,避免影响测定结果。
2. 实验操作过程中要严格遵守操作规程,避免出现误差。
3. 对于不同类型的水样,可能需要调整实验条件或方法,以获得更准确的测定结果。
四、影响水中总硬度测定准确性的因素及改进措施1. 试剂纯度:试剂的纯度对于水中总硬度测定的准确性有很大的影响。
如果试剂中含有杂质或其它干扰物质,会影响到指示剂的颜色变化,从而影响测定结果的准确性。
水的总硬度的测定

水的总硬度的测定一、实验背景:水的总硬度是指水中钙和镁离子的总含量。
各国对水的硬度的表示方法各有不同,我国“生活饮水卫生标准”规定总硬度(以碳酸钙计)不得超过450mg/L ,这是用物资的质量浓度(单位:mg/L )表示的。
我国目前使用较多的表示方法还有用物质的量浓度(单位:mol/L )表示的。
除了对饮用水的总硬度有一定的要求之外,各种工业用水对水总硬度也有不同的要求。
因此,测定水的总硬度有很重要的实际意义。
二、实验原理水的硬度是表示水质的一个重要指标,对工农业用水、饮用水关系很大。
所谓水的硬度是指水中各种可溶性钙盐和镁盐的含量,它包括暂时硬度和永久硬度。
暂时硬度主要是指水中含钙、镁的酸式碳酸盐,加热能析出沉淀而除去;永久硬度是指钙、镁的硫酸盐、硝酸盐和氯化物,它们在加热时不沉淀。
测定Ca2+、Mg2+总量时,用缓冲溶液调节溶液的pH 为10。
以铬黑T 为指示剂,用EDTA 标准溶液滴定。
铬黑T 和EDTA 都能与Ca2+、Mg2+形成配合物,其稳定性EBT C EBT M MgY Y C K K K K -->>>a g a 。
因此,加入铬黑T 后,它先与部分Mg2+配合生成MgIn-(紫红色)。
当滴加EDTA 标准溶液时,EDTA 首先与游离的Ca2+配位,其次与游离的Mg2+配位,最后夺取MgIn-中的Mg2+,使铬黑T 游离出来,溶液由紫红色变为纯蓝色,指示达到终点。
水的总硬度的测定,一般采用EDTA 配位滴定法。
在pH=10的氨性缓冲溶液中,以铬黑T为指示剂,用EDTA标准溶液直接测定水中Ca2+、Mg2+总量,终点由紫红色变为纯蓝色。
若有Fe3+、Al3+干扰,可用三乙醇胺掩蔽,Cu2+、Pb2+、Zn2+等重金属离子可用KCN、Na 2S予以掩蔽。
滴定前: EBT + Mg2+═ Mg-EBT(蓝色)(紫红色)化学计量点前:Ca2+ + H2Y2-═ CaY2- + 2H+Mg2+ + H2Y2-═ MgY2- + 2H+化学计量点: Mg-EBT + H2Y2-═ MgY2- + EBT + 2H+(紫红色)(蓝色)水的硬度有多种表示方法。
水的总硬度测定

水的总硬度测定摘要:水的硬度,是指沉淀肥皂的程度,主要指水中含有可溶性钙盐和镁盐的多少。
目前测定水质中的总硬度的最好方法,就是用配位滴定分析法(EDTA一2Na)滴定,标准规定硬度不超过450mg/1(以CaCO,)。
水的硬度的测定,是水的质量控制的重要指标之一。
一、实验目的1、掌握EDTA标准溶液的配制和标定方法。
23456升水中含.Y4-的形式与用EDTApH=10,通式为:M2++HIn2-MIn-+H+(蓝色)(酒红色)Ca2+,Mg2+离子与EDTA及铬黑T形成配合物的稳定性不同,其稳定性大小的顺序为:CaY2->MgY2->MgIn->CaIn-测定时,先用NH3·H2O-NH4Cl缓冲溶液调节溶液的pH=10左右.滴定前,当加入指示剂铬黑T时,它首先与水中少量的Mg2+配位形成酒红色的配合物,当用EDTA溶液滴定时,EDTA便分别与水中游离的Ca2+,Mg2+离子配位,接近终点时,因MgY2-的稳定性大于MgIn-,故EDTA夺取MgIn-中的Mg2+,使铬黑T 游离出来,这时溶液由酒红色变为蓝色,指示终点到达.根据等物质的量反应规则,根据EDTA 标准溶液的浓度和消耗的体积,可按下式计算水的总硬度.水的硬度=水样体积vC ×100.09(mg/L )式中C 为EDTA 的浓度,V 为EDTA 的体积,100.09为CaCO 3的质量三、仪器,药品仪器:50ml 碱式滴定管移液管(25ml,50ml)250ml 锥形瓶250ml 容量瓶500ml 试剂瓶铬黑T 指示剂,边震,再加入五、思考题1.滴定时为什么要加入NH3·H2O -NH4Cl 缓冲溶液2.在配位滴定中,指示剂应具备什么条件附注1.EDTA 固体含结晶水不稳定,故不能直接配制其标准溶液.2.以MgCO3作基准物质标定EDTA 溶液:准确称取MgCO3(于110℃干燥2小时至恒重)0.20-0.22g(称至小数点后第四位)置于烧杯中,加5滴蒸馏水润湿,缓慢滴入6mol·L-1HCl约3ml,搅拌溶解,移入250ml容量瓶中,稀释至刻度,摇匀待用.用移液管吸取上述标准溶液25.00ml于锥形瓶中,滴加3-4滴9mol·L-1NH3·H2O,再加入NH3·H2O-NH4Cl缓冲溶液10ml,3滴铬黑T指示剂,用EDTA溶液滴定,当溶液由酒红色刚好变为纯蓝色时,即达滴定终点.记录消耗EDTA溶液的体积.再重复滴定2次.计算EDTA溶液的准确浓度.六、注意:1、自来水样较纯、杂质少,可省去水样酸化、煮沸,加Na2S?掩蔽剂等步骤。
水的总硬度测定

一、实验目的:1. 了解络合滴定法的原理及其应用。
2. 掌握络合滴定法中的直接滴定法,学会用配位滴定法测定水的总硬度。
3. 掌握EDTA标准溶液的配制与标定的原理。
4. 了解标定EDTA所用指示剂的性质和使用的条件。
5. 掌握用CaCO3标定EDTA的方法。
二、实验原理:1、水的总硬度的测定:水的硬度主要由于水中含有钙盐和镁盐,其他金属离子如铁、铝、锰、锌等离子也形成硬度,但一般含量甚少,测定工业用水总硬度时可忽略不计。
测定水的硬度常采用配位滴定法,用乙二胺四乙酸二钠盐(EDTA)的标准溶液滴定水中Ca、Mg总量,然后换算为相应的硬度单位(我国采用mmol/L或mg/L(CaCO3)为单位表示水的硬度)。
按国际标准方法测定水的总硬度:在pH=10的NH3—NH4Cl缓冲溶液中(为什么?),以铬黑T(EBT)为指示剂,用EDTA标准溶液滴定至溶液由紫红色变为纯蓝色即为终点。
滴定过程反应如下:⑴指示剂:铬黑T(EBT)PH <6.3 (紫);PH 6.3~11.5 (蓝);PH >11.5 (橙)⑵滴定过程颜色变化:滴定前:EBT + Mg2+ = Mg-EBT(蓝色) (紫红色)滴定时:EDTA + Ca2+ = Ca-EDTA(无色)EDTA + Mg2+ = Mg-EDTA(无色)终点时: EDTA + Mg-EBT = Mg-EDTA + EBT(紫红色) (蓝色)到达计量点时,呈现游离指示剂的纯蓝色。
⑶终点颜色变化:(紫红色) → (蓝色)⑷干扰离子的掩蔽:若水样中存在Fe3+,Al3+等微量杂质时,可用三乙醇胺进行掩蔽,Cu2+、Pb2+、Zn2+等重金属离子可用Na2S或KCN掩蔽。
⑸水硬度的表示:各国对水硬度表示的方法尚未统一,我国生活饮用水卫生标准中规定硬度(以CaCO3计)不得超过450mg/L。
除了生活饮用水,我国目前水硬度表示方法还是用mmol/L(CaCO3)表示。
德国:CaO 10mg/L或0.178mmol/L英国:CaCO3格令/英仑,或0.143mmol/L法国:CaCO3 10mg/L或0.1mmol/L美国:CaCO3 1mg/L或0.01mmol/L⑹分测钙、镁硬度:可控制pH介于12~13之间(此时,氢氧化镁沉淀),选用钙指示剂进行测定。
水的总硬度测定

水的总硬度测定实验目的1、学习EDTA 标准溶液的配制与标定方法。
2、学习水的总硬度的测定方法。
3、了解金属指示剂的变色原理和使用方法。
实验原理由于EDTA 酸不易溶于水,通常采用EDTA 二钠盐配制标准溶液。
0.1mol/L EDTA 二钠盐溶液的PH ,按理论计算,应为4.42,一般不用市售的EDTA 试剂直接配制准确浓度的标准溶液,而需要用适当的基准物来标定。
用于标定EDTA 溶液的基准物很多,常用的有Zn 、ZnO 、CaCO 3、Mg 、Cu 等,本实验采用CaCO 3溶解并制成钙标准溶液。
吸取一定量此标准溶液,用 NH 3-NH 4Cl(pH=10)缓冲溶液,以K-B 为指示剂,用0.01mol ·L -1EDTA 溶液滴定至溶液由紫红色变为蓝绿色,即为终点。
水的硬度主要是由于水中含钙盐和镁盐所形成。
硬度对工业用水关系很大,如锅炉给水要经常进行硬度分析,为水的处理提供依据。
在水中以碳酸氢盐形式存在的钙、镁盐,加热能被分解,析出沉淀而除去,这类盐所形成的硬度称为暂时硬度。
例如O H CO CaCO HCO Ca 22323)(+↑+↓−→−∆Mg(HCO 3)3(沉淀不完全)+CO 2O+H 2OMg(OH)而钙、镁的硫酸盐、氯化物、硝酸盐等所形成的硬度称为永久硬度,暂时硬度和永久硬度之和为总硬度。
测定水的总硬度就是测定水中钙、镁的总量,一般采用EDTA 配位滴定法。
用EDTA 滴定水中Ca 2+、Mg 2+离子总量时,采用NH 3·H 2O -NH 4CL 缓冲溶液控制溶液的酸度为PH =10,以铬黑T 为指示剂,滴定至溶液由酒红色变为纯蓝色即为终点:+--=--++−−→−+H HIn MgY Y H MgI PH a 221022 式中H 2Y 2-表示EDTA ,Hi n 2-表示铬黑T 。
酒红色 蓝色水的硬度有多种表示方法,随各国的习惯而有所不同,目前我国通常是以度(°)计。
实验九天然水总硬度的测定

试剂及仪器
• 仪器:分析天平、台秤、细口瓶、干 燥器、称量瓶、电炉、烧杯、玻璃棒、 表面皿、酸式滴定管、容量瓶、移液 管、洗瓶。
25 。C 1000mL
四、实验步骤
天然水总硬度的测定
取适量的水样(一般取50~100mL)(用什么量 取?)置于250mL的锥形瓶中,加入1~2滴HCl (1+1)溶液使之酸化。煮沸数分钟,以除去CO2。 冷却后加入3mL三乙醇胺溶液,5mL氨性缓冲溶液, 1mLNa2S溶液及2~3滴铬黑T指示剂,用EDTA标 液滴定至溶液由酒红色变为蓝紫色,即为终点。平 行测定三份。计算水的总硬度,以度(o)和 mg/L(CaCO3)表示分析结果。
• 世界各国对水的硬度表示方法不同。德国硬度是水 硬度表示比较早的一种方法,它以度(o)为计,它 表示是十万份水中含有一份CaO,即1L水中含有 10mgCaO时为1o,我们采用此法。
三、试剂及仪器
• 试剂:0.02mol•L-1 EDTA溶液、碳 酸钙、盐酸(1+1)、20%氢氧化钠、 K-B指示剂、氨性缓冲溶液、2% Na2S溶液、20%三乙醇胺。
天然水总硬度的测定
一、实验目的 二、实验原理 三、试剂及仪器 四、实验步骤 五、注意事项 六、数据处理 七、思考题
一、实验目的
• 掌握络合滴定的原理与特点; • 巩固络合滴定法中金属指示剂的变色
二、实验原理
• 水的硬度的测定可分为水的总硬度的测定和钙、 镁硬度的测定两种。总硬度的测定是滴定Ca、Mg总 量,并以Ca进行计算。后一种是分别测定Ca和Mg 的含量。
五、注意事项
• 分析天平的正确使用; • 电炉的正确使用(注意安全); • 容量瓶与移液管的规范操作; • 溶液pH的调节; • 滴定管的正确使用; • 滴定接近终点时滴定速度要慢,
水质总硬度的测定gb7477-87

水质总硬度的测定gb7477-87
GB7477-87是用于水质总硬度测定的国家标准,也称为中华人民共和国水质总硬度的监测标准标准。
它通过碱度计的pH值的测定用于测定水的水质硬度。
总硬度指的是水含有的总污染物(元素或离子)的量,这些污染物对溶解在水中的某些有机物和金属元素有吸附作用,使其受到影响。
根据GB7477-87,水总硬度的大小取决于水中钙和镁元素的含量。
换言之,水质硬度越高,水中所含钙和镁元素就越多。
根据GB7477-87标准,水质总硬度的测定步骤如下:
1.将测试水以一定的浓度加入滤瓶中,待测水体积大约为20ml;
2.将碱度计的棒放入滤瓶,按照标准的测量步骤进行测量;
3.按表格计算测定的结果,计算水质总硬度;
4.最后,根据测得的硬度值将水质分类,分为:软水、中硬水、硬水和很硬水。
总硬度是水质影响最重要的一个因素,对水的综合污染有重要的指示作用,可以用碱度计的测试结果更准确的判断水质硬度。
因此,检测水质总硬度的最佳方法是按照GB7477-87标准来进行测定。
水的总硬度检测标准

水的总硬度检测标准水的总硬度是指水中钙和镁离子的总和,通常以mg/L(毫克/升)或者以ppm (百万分之一)来表示。
水的总硬度对于水质的影响非常重要,因此需要进行准确的检测。
下面将介绍水的总硬度检测标准及相关内容。
一、水的总硬度检测方法。
1. 直接滴定法,直接滴定法是通过加入EDTA(乙二胺四乙酸)试剂与水中的钙和镁离子发生螯合反应,从而测定水中的总硬度。
这种方法操作简便,结果准确可靠。
2. 分光光度法,分光光度法是通过分光光度计测定水中钙和镁离子的浓度,进而计算出水的总硬度。
这种方法灵敏度高,适用于各种类型的水样。
3. 离子选择电极法,离子选择电极法是通过离子选择电极检测水中的钙和镁离子浓度,从而计算出水的总硬度。
这种方法操作简单,适用于实验室和现场检测。
二、水的总硬度检测标准。
根据《水质分析方法》(GB/T 5750.5-2006)的规定,水的总硬度检测标准如下:1. 饮用水,水的总硬度不应超过100mg/L,超过此标准可能对人体健康产生不利影响。
2. 工业用水,根据不同的工业生产需求,水的总硬度标准会有所不同,一般在50-500mg/L范围内。
3. 农业灌溉水,水的总硬度对于农业灌溉水的影响较大,一般应控制在150-300mg/L范围内。
三、水的总硬度检测结果的解读。
根据水的总硬度检测结果,可以对水质进行合理的评估和处理:1. 如果水的总硬度超过了相关标准,可以采取适当的软化处理,如加入适量的软化剂或者进行离子交换处理。
2. 如果水的总硬度低于标准,可能会影响到水的饮用、工业生产或者农业灌溉等方面,需要根据具体情况进行调整和处理。
3. 对于不同用途的水,其总硬度标准和处理方法也会有所不同,需要根据实际情况进行科学合理的处理。
四、水的总硬度检测的意义。
水的总硬度检测对于保障饮用水安全、保护环境、促进工业生产和农业灌溉等方面都具有重要意义。
通过科学准确的检测,可以及时发现和解决水质问题,保障人民群众的健康和生产生活的需要。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
一、实验原理
总硬度、钙硬度、镁硬度的概念及表示方法;
水的硬度主要是指水中含可溶性的钙盐和镁盐。
总硬度通常以每L水中含的碳酸钙的mg数,即mg/L.
钙硬度即每1L水中含的钙离子的mg数,mg/L.
镁硬度即每1L水中含的镁离子的mg数,mg/L
测定条件:以NH
3-NH
4
Cl 缓冲溶液控制溶液pH=10,以铬黑T为指示剂,用EDTA
滴定水样。
原理:滴定前水样中的钙离子和镁离子与加入的铬黑T指示剂络合,溶液呈现酒红色,随着EDTA的滴入,配合物中的金属离子逐渐被EDTA夺出,释放出指示剂,使溶液颜色逐渐变蓝,至纯蓝色为终点,由滴定所用的EDTA的体积即可换算出水样的总硬度。
总硬度=(CV1)EDTA M CaCO3/0.1
实验步骤
总硬度的测定
用100mL吸管移取2份水样,分别加5mL NH
3-NH
4
Cl 缓冲溶液(PH=10),2~3
滴铬黑T指示剂,用EDTA标准溶液滴定,溶液由酒红色变为纯蓝色即为终点。
NH
3-NH
4
Cl 缓冲溶液(PH=10):取氯化铵5.4g,加水20ml溶解后,加浓氨溶液35ml,再
加水稀释至100ml,即得。
液态铬黑T的配制方法:称取0.50g铬黑T和2.0g盐酸羟胺溶于乙醇,用三乙醇胺稀释至100ml冰箱冷藏3个月。
选择工作基准试剂的原则是与测定对象尽量一致,因此在水硬度的测定中,标定EDTA溶液的工作基准试剂也可选用CaCO3。
<1> CaCO3基准试剂的干燥
将CaCO3放烘箱中于393K下干燥2h,稍冷后置于干燥器中冷至室温。
<2> CaCO3标准溶液配制
准确称取0.17~0.20gCaCO3,先用少量水湿润,盖上表面皿,缓慢加1:1 HCl 10mL,加热溶解。
溶解后将溶液转入250mL容量瓶中,用水稀释至刻度,摇匀。
<3> 0.01mol·L-1 EDTA标准溶液的标定
a. 用吸管吸取25.00mLCa2+试液,加入10mLpH=10的氨缓冲溶液,2~3滴K-B指示剂
(0.2g酸性铬蓝K和0.4g萘酚B,配制为1000mL水溶液),用EDTA溶液滴定至溶液由紫红色变为蓝绿色,即为终点。
我国通常以1×10-3g·L-1 CaCO
3
表示水的总硬度,德国以10×10-3g·L-1 CaO表
示水的硬度,因此,如以我国1×10-3g·L-1CaCO
3
表示的总硬度换算成德国度时,需乘以系数0.056。
德国度o DH(10×10-3g·L-1 CaO) = 总硬度(g·L-1
CaCO
3)×56.08/(100.09×10) = 总硬度(g·L-1 CaCO
3
)×0.056
为什么测定钙、镁总量时,要控制pH=10?。
⑴因稳定常数 CaY2-> MgY2-,滴定Ca2+的最低pH=8,滴定Mg2+的最低pH=10,指示剂铬黑T使用的最适宜pH范围为9~10.5,因此测定时pH=10。
测定总硬度时,溶液中发生了哪些反应,它们如何竞争
在pH=10的缓冲溶液中,加入铬黑T指示剂后,指示剂先与Mg2+配位(为什么?)为MgIn-,当滴加EDTA后,EDTA先与游离的Ca2+、Mg2+配位,最后夺取MgIn-中的Mg2+:
MgIn- + H
2
Y2-= MgY2- + HIn2- + H+
溶液的颜色由酒红色变为纯蓝色。
如果待测液中只含有Ca2+,能否用铬黑T为指示剂进行测定?
若按本实验条件用直接滴定法测定总硬度,则不能。
经计算可知,在pH=10的氨性溶液中,以铬黑T为指示剂,用0.02mol·L-1EDTA滴定0.02mol·L-1Ca2+溶液,终点误差为-1.5%;若滴定的是0.02mol·L-1Mg2+溶液,终点误差为0.11%。
此结果表明,采用铬黑T为指示剂时,尽管CaY比MgY稳定,但测定钙的终点误差较大,这是由于铬黑T与Ca2+显色不灵敏所致。
若按照置换滴定法进行实验,则可以。
只要在溶液中加入少量MgY,在pH=10的条件下,用铬黑T为指示剂就能进行测定
如水样中含有Al3+、Fe3+、Cu2+,能否用铬黑T为指示剂进行测定,如可以,实验应该如何做?
由于Al3+、Fe3+、Cu2+等对指示剂有封闭作用,如用铬黑T为指示剂测定此水样,应加掩蔽剂将它们掩蔽:Al3+、Fe3+用三乙醇胺,Cu2+用乙二胺或硫化钠掩蔽。
例:取适量体积的水样,加入3mL三乙醇胺(200g·L-1水溶液),5mL氨性缓冲
溶液,1mL 20g·L-1Na
2
S溶液,2~3滴铬黑T指示剂,用EDTA标准溶液滴定至溶液由紫红色变为纯蓝色即为终点。
选择工作基准试剂的原则是与测定对象尽量一致,因此在水硬度的测定中,标定EDTA溶液的工作基准试剂也可选用CaCO3。
⑴当水样中Mg2+的含量较低时(一般要求相对于Ca2+来说须有5% Mg2+存在),因用铬黑T指示剂往往得不到敏锐的终点,可在EDTA标准溶液中加入适量Mg2+(标定前加入Mg2+,对终点没有影响)或者在缓冲溶液中加入一定量的Mg-EDTA盐,利用置换滴定法的原理来提高终点变色的灵敏性,后者配法如下:
Mg-EDTA盐溶液的配制,称取0.25gMgCl2·6H2O于100mL烧杯中,加入少量水溶解后转入100mL容量瓶中,用水稀释至刻度,用干燥的吸管移取50.00mL溶液,加5mLpH=10的氨缓冲溶液,4~5滴铬黑T指示剂,用0.1mol·L-1 EDTA溶液滴定至溶液由紫红变为蓝色,即为终点。
取此同量的EDTA溶液加入容量瓶剩余的镁溶液中,即成Mg2+-EDTA盐,将此溶液全部倾入上述缓冲溶液中。
