对甲苯磺酸的制备
对甲苯磺酸制备和乙酰水杨酸的合成

对甲苯磺酸制备一.实验原理原先教材实验方法存在如下弊端:1.分水器的容积约有15~25mL,而加入的甲苯仅有25mL,大部分的甲苯在反应初期就被蒸发到分水器中。
留在反应器中的甲苯量少。
2.由于反应器中的甲苯量少,反应温度高,反应物料易炭化变黑。
3.原实验方案是反应物料预先一次性混合在一起的,慢慢加热的操作方式生成较多的邻位异构体,所形成的物料粘稠,抽滤困难所以对实验进行改进:温度高有利于对甲苯磺酸的生成以及对甲苯磺酸一水化合物能从稀硫酸中结晶出来的原理,采用浓硫酸过量,把甲苯滴加到90~100摄氏度的浓硫酸中反应二.改进实验药品用量和实验仪器甲苯15ml 、浓硫酸20ml、水5ml三口烧瓶一侧连接温度计,一侧接恒压漏斗,中间接分水器,分水器上再接冷凝管三.实验步骤四.实验结果产物性状:呈为微粉红色的晶体产量11.2g 产率=11.2/24.2=46.3%乙酰水杨酸的合成一.实验原理M=138.12 M=102.09 M=180.15二.实验试剂水杨酸3g、Na2CO3 0.15g、醋酸酐 3.2 ml 三.实验步骤四.实验结果产物性状:白色颗粒状晶体产量:2.3 g 产率=2.3/3.9=58%下面是赠送的团队管理名言学习,不需要的朋友可以编辑删除谢谢1、沟通是管理的浓缩。
2、管理被人们称之为是一门综合艺术--“综合”是因为管理涉及基本原理、自我认知、智慧和领导力;“艺术”是因为管理是实践和应用。
3、管理得好的工厂,总是单调乏味,没有任何激动人心的事件发生。
4、管理工作中最重要的是:人正确的事,而不是正确的做事。
5、管理就是沟通、沟通再沟通。
6、管理就是界定企业的使命,并激励和组织人力资源去实现这个使命。
界定使命是企业家的任务,而激励与组织人力资源是领导力的范畴,二者的结合就是管理。
7、管理是一种实践,其本质不在于“知”而在于“行”;其验证不在于逻辑,而在于成果;其唯一权威就是成就。
8、管理者的最基本能力:有效沟通。
ptsa 有机化学

ptsa 有机化学PTSA有机化学中文1000字磺酸对甲苯磺酸(PTSA)是一种重要的有机化学中间体,也是一种强酸催化剂。
PTSA 是一种固体物质,呈白色或类白色粉末状。
它是一种强酸催化剂,可用于许多有机合成反应。
在工业上,它通常用于酯化反应和糖化反应。
下面将介绍PTSA的制备、性质、用途等方面的知识。
一、PTSA的制备方法1.苯磺酰氯法苯磺酰氯和甲苯在三氯化铝的存在下反应,生成PTSA。
C6H5SO2Cl + C7H8 → C6H5SO3C7H7 + HCl2.硫三氧化氮法3.醇法在正庚醇中加入氯化磺酸,然后加入一个等摩尔的苯磺酸钠和甲苯混合物,反应生成PTSA。
4.C2H5COOH法在正丙酸中加入硫酸和C7H8,反应生成PTSA。
二、PTSA的性质1.化学性质PTSA是一种强酸催化剂,它可以将醇和酚转化为它们的甲基醚或甲基苯醚。
此外,PTSA还可用于通过羰基化合物制备酯类、部分酯化反应、甾体合成、脱水反应等。
2.物理性质PTSA是一种白色或类白色粉末状的固体,密度为1.428 g/cm³。
它不易挥发,在空气中也稳定。
它可以在水中或有机溶剂中溶解。
1.酯化反应催化剂PTSA是典型的酯化反应催化剂。
它可以将醇和酸转化为酯。
例如,用PTSA催化甲醇和乙酸反应可得到甲酸甲酯。
PTSA是糖化反应催化剂,可用于合成淀粉、果糖、蔗糖等。
3.有机合成反应中的催化剂PTSA可以用于部分酯化,甾体合成,脱水反应,烯丙基化反应等。
对于不同的有机化学反应,PTSA都可以提供不同的催化效果。
4.其它应用PTSA还可以用于染料工业、塑料工业、涂料工业和有机合成化学品工业等领域。
总之,PTSA是一种重要的有机化学中间体和催化剂,广泛应用于工业化学和有机合成反应中。
各种制备方法可根据需要选择。
在应用过程中,需要遵循安全操作规程,避免对人体造成危害。
对甲苯磺酸的制备及应用

对甲苯磺酸的制备及应用甲苯磺酸是一种重要的有机化学品,广泛应用于化学、药物和染料工业等领域。
下面将介绍甲苯磺酸的制备方法及其应用。
甲苯磺酸的制备方法主要有以下几种:1. 甲苯直接磺化法:该方法是使用浓硫酸对甲苯进行磺化反应得到甲苯磺酸。
首先将甲苯加入到反应釜中,加热至80-90,然后缓慢滴加浓硫酸,并保持温度。
反应完成后,冷却并加入稀硫酸使溶液中的甲苯磺酸析出,经过过滤、洗涤、干燥即可得到纯品。
2. 甲苯氯化后的磺化法:该方法首先对甲苯进行氯化得到对甲基苯基氯,然后再用浓硫酸对其进行磺化反应得到甲苯磺酸。
该方法的优点是可以避免甲苯与浓硫酸直接接触,减少环境污染。
甲苯磺酸主要用途如下:1. 化学工业中的合成试剂:甲苯磺酸可以作为有机合成中的重要试剂,例如作为催化剂、还原剂、酸化剂等。
在有机合成中,甲苯磺酸可用于酯化反应、醚化反应、羧化反应等,通过调整反应条件,可以得到不同的有机化合物。
2. 染料工业中的中间体:甲苯磺酸可以用作染料工业中的中间体,用于合成不同类型的染料。
例如,甲苯磺酸经过酰化反应后可以得到苯酰氯,再与苯胺反应可以得到二苯亚胺,进一步与不同的芳香醛类化合物反应可以合成不同颜色的染料。
3. 药物工业中的原料:甲苯磺酸可以作为药物合成中的重要原料,用于制备多种药物。
例如,它可以用于合成抗生素、体外诊断试剂盒中的荧光标记剂以及保健品中的某些成分。
4. 电子工业中的添加剂:甲苯磺酸可以用作电子工业中的添加剂。
例如,在锂离子电池的电解质中加入甲苯磺酸,可以提高电池的电导率和稳定性。
5. 其他应用领域:甲苯磺酸还可以用作催化剂、去污剂、通用溶剂、防腐剂等。
在化学研究中,甲苯磺酸也常常用作研究试剂。
综上所述,甲苯磺酸是一种重要的有机化学品,在化学、药物和染料工业等多个领域具有广泛的应用。
它的制备方法主要有甲苯直接磺化法和甲苯氯化后的磺化法。
甲苯磺酸的主要应用包括化学工业中的合成试剂、染料工业中的中间体、药物工业中的原料、电子工业中的添加剂等。
对甲苯磺酸的制备实验报告

对甲苯磺酸的制备实验报告甲苯磺酸的制备实验报告一、引言甲苯磺酸是一种重要的有机化合物,广泛用于医药、染料、涂料等行业。
本实验旨在通过甲苯的硝化和硝基甲苯的还原反应制备甲苯磺酸。
二、实验原理甲苯硝化反应是指将甲苯与浓硝酸在硫酸的催化下反应生成硝基甲苯。
硝基甲苯经还原反应后,得到甲苯磺酸。
三、实验步骤1. 准备实验器材和试剂:甲苯、浓硝酸、浓硫酸、氢氧化钠、无水乙醇。
2. 在通风橱内进行实验,佩戴防护眼镜和实验手套。
3. 将甲苯与浓硝酸按1:1的比例加入干净的烧杯中。
4. 加入适量的浓硫酸,用玻璃杯搅拌均匀。
5. 将混合液放入冰水浴中冷却,搅拌保持温度。
6. 在冷却的混合液中缓慢加入氢氧化钠溶液,反应产生的硝基甲苯沉淀出来。
7. 将硝基甲苯用无水乙醇洗涤,过滤并干燥。
8. 将干燥的硝基甲苯与浓硫酸混合,加热回流反应。
9. 过滤得到甲苯磺酸溶液,用无水乙醇洗涤并干燥。
四、实验结果与分析经过实验制备得到的甲苯磺酸呈白色结晶体,纯度较高。
通过对产物的红外光谱分析,发现在1700-1800 cm-1处有强烈的酰基伸缩振动吸收峰,证明甲苯磺酸的结构正确。
同时,通过对产物的元素分析,发现其中含有硫元素,进一步证明了甲苯磺酸的生成。
五、实验讨论在本实验中,我们采用了硝化和还原反应的方法制备甲苯磺酸。
硝化反应是一种常用的有机合成方法,通过硝酸与有机物反应,可以引入硝基基团。
而还原反应则是将硝基基团还原为氨基或烷基基团的过程。
通过这两个反应的组合,我们成功合成了甲苯磺酸。
然而,在实验过程中,我们也遇到了一些问题。
首先,硝化反应需要在低温下进行,以避免副反应的发生。
因此,在实验中需要严格控制温度,以确保反应的选择性和产率。
其次,还原反应需要使用浓硫酸作为催化剂,但硫酸对皮肤和眼睛有刺激性,需要注意安全操作。
六、结论通过本实验,我们成功制备了甲苯磺酸。
实验结果表明,制备的甲苯磺酸纯度较高,结构正确。
本实验不仅加深了我们对有机合成反应的理解,同时也提醒了我们在实验中要注意安全操作。
对甲苯磺酸制备

四、实验装置
分水反应装置
抽滤装置
五 实 验 流 程
1、加反应物:在100 mL的圆底烧瓶中加入25.0 mL甲苯,电磁
搅拌,缓慢加入5.5 mL浓硫酸,再依次安装好分水器,回流冷凝 管,开始加热至回流2个小时。
2.结晶抽滤:停止加热,静置冷却至不烫手后,转移至50 mL小 烧杯中,加入1.5 mL水,会有晶体析出,再用玻璃棒搅拌,晶体 完全析出后,减压抽滤。
使水面略低于回流支管(大约1 cm), 当水面接近支管处 时,打开活塞,适当放出部分水分,当反应所生成理论量 的水全部时,反应结束。
七 、思考题
1.利用什么性质除去对甲苯磺酸中的邻位 衍生物?
2. 在本实验条件下,会不会生成相当量的
甲苯二磺酸?为什么?
CH3 H2SO4
CH3 SO3H
主反应:
CH3 CH3 H2SO4
副反应:
SO3H
三、仪器与药品
• 仪器:100 ml圆底烧瓶、分水器、球形冷 凝管、250 ml烧杯、250 ml吸滤瓶、布氏 漏斗。 • 试剂:甲苯25.0 mL(0.24 mol);98 % 浓硫酸5.5 mL(0.1 mol)、浓盐酸
3、重结晶纯化:在50 mL烧杯(或大试管)里,将12.0 g粗产物溶于 约6 mL水中。往此溶液里通入氯化氢气体.直到有晶体析出。在 通氯化氢气体时,要采取措施,防止“倒吸”。析出的晶体用布氏
漏斗快速抽滤。晶体用少量浓盐酸洗涤。用玻璃瓶塞挤压去水分, 取出后保存在干燥器里。
六 注意事项
• 1. 趁热过滤时,吸滤瓶和布氏漏斗要充分预热。滤液要 自然冷却。 • 2. 滴加浓硫酸时一定要在振摇下用滴管慢慢加入。 • 3. 析出结晶时要慢慢搅拌。 • 4. 在实验开始前要在分水器的活塞立管中加入少量水,
对甲苯磺酸原材料

对甲苯磺酸原材料的介绍与应用一、甲苯磺酸原材料的概述甲苯磺酸,又称甲基苯磺酸,是一种有机化合物,化学式为C8H8O3S。
它是一种白色结晶性粉末,具有良好的水溶性和稳定性。
甲苯磺酸是一种重要的有机合成中间体,在医药、染料、涂料等领域有广泛应用。
二、甲苯磺酸原材料的制备方法1. 甲苯硫酰氯和氢氧化钠反应制备法:将甲苯硫酰氯加入到氢氧化钠水溶液中,并在搅拌下反应,得到沉淀后过滤并洗涤,即可得到甲苯磺酸。
2. 甲基丙烯腈和亚硫酸钠反应制备法:将甲基丙烯腈和亚硫酸钠混合并在加热下反应,得到产物后经过结晶分离纯化即可得到甲苯磺酸。
三、甲苯磺酸原材料的应用1. 医药领域:甲苯磺酸是一种重要的医药中间体,可以用于合成多种药物,如头孢菌素、氨基苄青霉素等。
2. 染料领域:甲苯磺酸可以用于合成多种染料,如偶氮染料、硫化染料等。
3. 涂料领域:甲苯磺酸可以用于合成多种涂料树脂,如酚醛树脂、环氧树脂等。
4. 其他领域:甲苯磺酸还可以用于合成橡胶助剂、表面活性剂等。
四、甲苯磺酸原材料的市场前景随着人们对生活品质的要求不断提高,医药、染料、涂料等行业的发展也越来越迅速。
而作为这些行业中重要的有机合成中间体之一,甲苯磺酸的市场需求也在不断增加。
据统计,未来几年内,全球甲苯磺酸市场将保持稳定增长态势,并有望达到数十亿美元的规模。
五、甲苯磺酸原材料的生产企业目前,国内外生产甲苯磺酸原材料的企业较多,其中国内主要有江苏昊华化工、山东临沂金诺化工、湖南天宇化工等企业。
这些企业在生产技术、产品质量等方面均有一定优势,在满足国内市场需求的同时,也在积极开拓海外市场。
对甲苯磺酸的制备与应用

摘要本文主要对对甲苯磺酸的制备工艺和应用前景进行了研究,分别采用了传统工艺和两种改进工艺制备对甲苯磺酸,并对此进行了比较。
改进工艺克服了传统工艺的弊端。
第一种改进方案是运用了部分结晶选择性原理制备对甲苯磺酸。
甲苯与浓硫酸在甲苯沸腾回流(110℃)的条件下反应5h后,在80℃下加一定量的水使对甲苯磺酸结晶水合物从磺化混合液中析出,而间位和邻位两种异构物留在体系中,补充原料后继续反应,体系重新达到化学平衡状态,再析出产品。
如此循环反应-结晶过程,即抑制了新的间位和邻位异构物进一步产生,又使较纯的对位产物分离出体系。
优化了工艺条件,结果表明,该生产工艺路线为硫酸定量反应,无废酸或甲苯排放,产品纯度大于85%,对于高选择性生产对甲苯磺酸和清洁磺化过程具有重要的意义。
第二种改进工艺是将甲苯缓慢滴加到热的浓硫酸中,此工艺减短了实验时间,使操作时间为平时的四分之一,不但节省了反应物的用量,而且还大大提高了产量,改进的方法制备收率高,反应操作简单。
本文以对甲苯磺酸做催化剂催化合成了邻苯二甲酸二丁酯,其产率为84.0%,用浓硫酸作催化剂的产率为82.8%,尽管两者间的产率相近,但对甲苯磺酸没有腐蚀性,且在反应过程中不能产生废酸,对环境无污染。
关键词:对甲苯磺酸;磺化;结晶;催化剂AbstractThis paper focuses on the p-toluene sulfonic acid preparation process and application prospects were studied, respectively using traditional technology and two kinds of improved preparation process of p-toluene sulfonic acid, and make a comparison. Improved technology overcomes the defects of the traditional process. The first improvement plan is the use of partially crystalline selective preparation principle of p-toluene sulfonic acid. Refluxing toluene with concentrated sulfuric acid in toluene (110 ℃) 5h reaction conditions, adding a certain quantity of water at 80 ℃for crystalline hydrate precipitated from the sulfonated toluene sulfonic acid in the mixture, and meta - and ortho two isomers in the system, supplementary materials after reaction, system to achieve chemical equilibrium, then precipitation products. So the cycle reaction crystallization process, which inhibits the new meta - and ortho isomer to produce, and the para product is pure isolated system. Process conditions, the optimization results show that, the production process for sulfuric acid quantitative reaction, no waste acid or toluene emissions, the purity of product is more than 85%, high selectivity for the production has the vital significance to the toluene sulfonic acid and clean the sulfonation process. Process improvement of second is concentrated sulfuric acid to toluene is slowly added into hot, this process to shorten the experimental period, the operation time is usually 1/4, not only to save the amount of reactants, but also greatly improve the yield, high yield improved method of operation is simple, reactiThe catalyst p-toluene sulfonic acid dibutyl phthalate was synthesized, its yield is 84%, with concentrated sulfuric acid as catalyst. The yield is 82.8%, although similar between the yield, but no corrosive p-toluene sulfonic acid, and can not waste acid produced in the reaction process, no pollution to the environment.Keywords: catalyst p-toluene sulfonic acid sulfonation crystallization目录第1章文献综述 (1)1.1 对甲苯磺酸的性质 (6)1.2对甲苯磺酸的制备方法 (6)1.2.1硫酸磺化法 (6)1.2.2三氧化硫磺化法 (7)1.2.3 氯磺酸磺化法 (8)1.3对甲苯磺酸的精制 (8)1.3.1真空精馏法 (8)1.3.2水稀释法 (8)1.3.3苯—乙醇法 (9)1.4对甲苯磺酸的应用 (9)1.4.1催化剂 (9)1.4.2有机合成 (9)1.4.3稳定剂 (9)1.5选题意义 (9)第2章实验部分 (11)表2.1实验药品 (11)表2.2实验仪器 (11)2.3制备对甲苯磺酸的传统工艺 (12)2.3.1原理 (12)2.3.2实验步骤 (12)2.3.3传统工艺存在的问题 (12)2.4工艺改进一 (13)2.4.1改进原理 (13)2.4.2 实验过程 (14)2.5工艺改进二 (14)2.5.1改进原理 (14)2.5.2实验步骤 (14)2.6实验改进的结果讨论 (14)表2.6.1工艺一实验结果讨论 (15)表2.6.2工艺二 (15)第3章对甲苯磺酸的应用 (16)3.1对甲苯磺酸的应用 (16)3.1.l催化剂 (16)3.1.2有机合成 (16)3.1.3稳定剂 (16)3.2对甲苯磺酸合成酯 (16)3.2.1对甲苯磺酸催化合成邻苯二甲酸二丁酯 (16)3.2.2 酯的合成 (17)3.3 结果与讨论 (17)第4章结论 (19)致谢 (21)第1章文献综述对甲苯磺酸是贾沃斯基(Jaworsky)于1865年用硫酸磺化而首先制得的,该产品是无色或白色片状或柱状结晶,易溶于醇,难溶于苯,对皮肤、眼睛、黏膜有刺激性。
1.5对甲苯磺酸的生产解析

• 泄漏应急处理 • 迅速撤离泄漏污染区人员至安全区,并进行隔离,严格限 制出入。切断火源。建议应急处理人员戴自给正压式呼吸 器,穿消防防护服。尽可能切断泄漏源,防止进入下水道、 排洪沟等限制性空间。小量泄漏:用活性炭或其它惰性材 料吸收。也可以用不燃性分散剂制成的乳液刷洗,洗液稀 释后放入废水系统。大量泄漏:构筑围堤或挖坑收容;用 泡沫覆盖,降低蒸气灾害。用防爆泵转达移至专用收集器 内,回收或运至废物处理场所处置。如有大量甲苯洒在地 面上,应立即用砂土、泥块阴断液体的蔓延;如倾倒在水 里,应立即筑坝切断受污染水体的流动,或用围栏阴断甲 苯的蔓延扩散;如甲苯洒在土壤里,应立即收集被污染土 壤,迅速转移到安全地带任其挥发。事故现场加强通风, 蒸发残液,排除蒸气。 • 防护措施 • 呼吸系统防护:空气中浓度超标时,应该佩戴自吸过滤式 防毒面罩(半面罩)。紧急事态抢救或撤离时,应该佩戴空 气呼吸器或氧气呼吸器。 • 眼睛防护:戴化学安全防护眼镜。 • 身体防护:穿防毒渗透工作服。
• 防护措施 • 呼吸系统防护:可能接触其粉尘时,佩戴自吸过滤式防尘口具。紧急事态抢 救或撤离时,应该佩戴空气呼吸器。 • 眼睛防护:戴化学安全防护眼镜。 • 身体防护:穿防毒物渗透工作服。 • 手防护:戴橡胶手套。 • 其它:工作毕,淋浴更衣。单独存放被毒物污染的衣服,洗后备用。保持良 好的卫生习惯。 • 急救措施 • 皮肤接触:立即脱去被污染的衣着,用肥皂水和清水彻底冲洗皮肤。就医。 • 眼睛接触:提起眼睑,用流动清水或生理盐水冲洗。就医。 • 吸入:迅速脱离现场至空气新鲜处。保持呼吸道通畅。如呼吸困难,给输氧。 如呼吸停止,立即进行人工呼吸。就医。 • 食入:饮足量温水,催吐,就医。 • 灭火方法:灭火剂:干粉、二氧化碳、砂土。禁止用水。
三、甲苯 • 健康危害 • 侵入途径:吸入、食入、经皮吸收。 • 健康危害:对皮肤、粘膜有刺激性,对中枢神经系统有麻醉作用。 • 急性中毒:短时间内吸入较高浓度本品可出现眼及上呼吸道明显的刺激症状、 眼结膜及咽部充血、头晕、头痛、 恶心、呕吐、胸闷、四肢无力、步态蹒 跚、意识模糊。重症者可有躁动、抽搐、昏迷。 • 慢性中毒:长期接触可发生神经衰弱综合征,肝肿大,女性月经异常等。皮 肤干燥、皲裂、皮炎。 • 毒理学资料 • 毒性:属低毒类。 • 急性毒性:LD505000mg/kg(大鼠经口);LC5012124mg/kg(兔经皮);人吸 入71.4g/m3,短时致死;人吸入3g/m3×1~8小时,急性中毒;人吸入0.2~ 0.3g/m3×8小时,中毒症状出现。 • 刺激性:人经眼:300ppm,引起刺激。家兔经皮:500mg,中度刺激。 • 慢性毒性:大鼠、豚鼠吸入390mg/m3,8小时/天,90~127天,引起造血系统 和实质性脏器改变。 • 致突变性:微核试验:小鼠经口200mg/kg。细胞遗传学分析:大鼠吸入 5400µg/m3,16周(间歇)。
对甲苯磺酸的制备
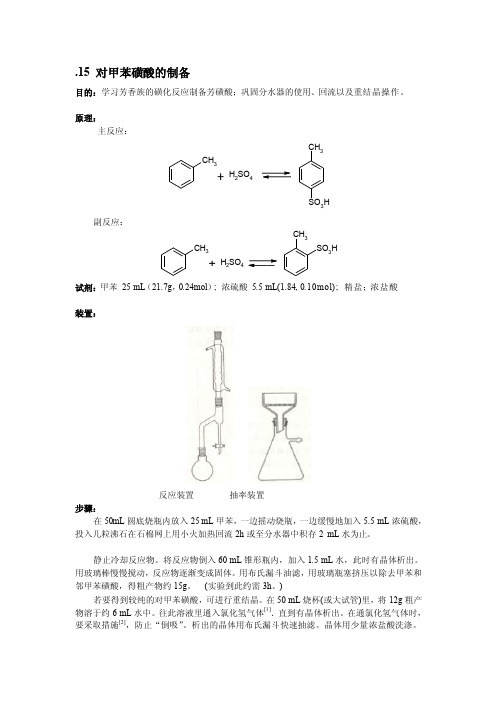
.15 对甲苯磺酸的制备目的:学习芳香族的磺化反应制备芳磺酸;巩固分水器的使用、回流以及重结晶操作。
原理:主反应:CHH 2SO 4CH 3SO 3H副反应:CHH 2SO 4CH 3SO 3H试剂:甲苯 25 mL (21.7g ,0.24mol ); 浓硫酸 5.5 mL(1.84, 0.10mol); 精盐;浓盐酸装置:反应装置 抽率装置步骤:在50mL 圆底烧瓶内放入25 mL 甲苯,一边摇动烧瓶,一边缓慢地加入5.5 mL 浓硫酸,投入几粒沸石在石棉网上用小火加热回流2h 或至分水器中积存2 mL 水为止。
静止冷却反应物。
将反应物倒入60 mL 锥形瓶内,加入1.5 mL 水,此时有晶体析出。
用玻璃棒慢慢搅动,反应物逐渐变成固体。
用布氏漏斗油滤,用玻璃瓶塞挤压以除去甲苯和邻甲苯磺酸,得粗产物约15g 。
(实验到此约需3h 。
)若要得到较纯的对甲苯磺酸,可进行重结晶。
在50 mL 烧杯(或大试管)里,将12g 粗产物溶于约6 mL 水中。
往此溶液里通入氯化氢气体[1].直到有晶体析出。
在通氯化氢气体时,要采取措施[2],防止“倒吸”。
析出的晶体用布氏漏斗快速抽滤。
晶体用少量浓盐酸洗涤。
用玻璃瓶塞挤压去水分,取出后保存在干燥器里。
纯对甲苯磺酸一水合物为无色单斜晶体,熔点96℃;对甲苯磺酸熔点104-105℃。
注释:[1] 此操作必须在通风橱内进行。
产生氯化氢气体最常用的方法是:在广口圆底烧瓶里放入精放,加入浓盐酸至浓盐酸的液面盖住食盐表面。
配一橡皮塞,钻三孔,一孔插滴液漏斗,一孔插压力平衡管,一孔插氯化氢气体导山管.滴液漏斗上口与玻璃平衡管通过橡皮塞紧密连接(不能漏气)。
在滴液漏斗中放入浓硫酸。
滴加浓硫酸,就产生氯化氢气体。
[2] 为防止“倒吸”,可不用插入溶液中的玻璃管来引入氯化氢气体,而是使气体通过一略微倾斜的倒悬漏斗让溶液吸收,漏斗的边缘有一半浸入溶液中,另一半在液面之上。
问题:1)利用什么性质除去对甲苯磺酸中的邻位衍生物?2)在本实验条件下,会不会生成相当量的甲苯二磺酸?为什么?。
第五组对甲苯磺酸的制备

5
小鼠经口)
硫酸
无色黏 稠油状 液体
98.08
易溶于水,
能以任意 比与水混
10.5
溶
330.0
0.834 2
1.83
2140mg/kg( 大鼠经口)
名称
间甲 苯磺 酸
外观
白色 结晶 性粉
末
分子 量
溶解性
熔点 /℃
沸点 /℃
折光 率 /20℃
相对 密度 /20 ℃/4 ℃
LD50/mg/kg
溶于水, 222 易溶于醇、 -
谢谢
灭火剂:泡沫、干粉、二氧化 碳、砂土。
合成路线选择的结果
合成路 线的选 择
对甲苯 磺酸的 制备
可行性 实用性 安全性 经济性 环保性
制备所需 生产环境 反应过程 产率高, 反应过程
的原料易 适中,反 稳定
得
应时间较
短
设备简单,简单,无 操作条件 副产物生 弹性大 成
产品用途
广泛用于合成医药、农药、聚合反应的稳定 剂及有机合成(酯类等)的催化剂。用作医药、 涂料的中间体和树脂固化剂,也用作电镀中间体。
②三氧化硫磺化法 理论上,三氧化硫是最有效的磺化剂,因为只是直接的
加成而不是脱除反应生产的水。在适宜的条件下,产品几 乎全部是对甲苯磺酸。
以气相三氧化硫磺化剂磺化甲苯,宜选择降膜吸收 反应器采用1%的有机酸作为定位剂温度控制在17℃~20℃ 之间,三氧化硫浓度6%~9%,反应得到的对甲苯磺酸纯度 高。
128.8 ℃
-
-
4000mg/kg( 大鼠经口)
【注意事项】
温度对反应的组成影响较大,必须进行控制。 根据对甲苯磺酸不溶于50-80%之间的硫酸溶液而 邻和对甲苯磺酸溶解的特性,选择在适当的温度下 ,加适量的水,使大部分的对甲苯磺酸以一水化合 物的结晶形式析出。
对甲苯磺酸的制备--有机实验

一、实验目的
1、学习芳香族的磺化反应制备芳磺酸。
2、巩固分水器的使用、回流、抽滤等操作。
二、实验原理
烷基苯在磺化剂作用下进行磺化是一个可逆反应。
甲苯在低温下磺化主要得到1:1的邻位和对位磺化产物的混合物,属于动力学控制;于较高温度进行磺化反应,由于空间效应,主要得到热力学稳定的对位产物。
本实验的化学反应式如下:
在制备对甲苯磺酸的时候会产生副反应,降低对甲苯磺酸的产率。
反应方程式如下:
实验装置图如下:
三、实验步骤
1、在50mL圆底烧瓶内放入25mL甲苯,一边摇动烧瓶,一边缓慢的加入5.5mL浓硫
酸,投入几粒沸石。
2、将烧瓶组装到回流分水装置上,加热回流2h或至分水器中积存2mL水为止。
3、反应结束,冷却反应物。
4、将反应物倒入烧杯中,加入1.5mL水,用玻璃棒慢慢搅动,反应物逐渐变成固
体。
用布氏漏斗抽滤,得粗产品。
5、在50mL烧杯里,将粗产品溶于约6mL水。
往此溶液里通入氯化氢气体,直到析出
结晶。
在通氯化氢气体时,要采取措施,防止“倒吸”。
析出的晶体用布氏漏斗快速抽滤。
抽滤完成的晶体保存在干燥器中。
注:实验报告的内容: 一、实验目的;二、实验原理;三、实验步骤;四、实验结果;五、讨论分析(完成指定的思考题和作业题);六、改进实验建议。
对甲苯磺酸性质及制作工艺

对甲苯磺酸性质及制作工艺甲苯磺酸是一种有机磺酸,化学式为C7H8O3S。
它是一种白色结晶粉末,可以溶解于水、醇和醚等有机溶剂中。
甲苯磺酸具有许多重要的化学性质,同时也有多种制作工艺。
首先,甲苯磺酸具有较强的酸性。
它可以与碱反应生成对应的甲苯磺酸盐,并释放出氢气。
由于甲苯磺酸的分子中含有磺酸基(-SO3H),因此具有较强的亲电性。
这使得甲苯磺酸可以作为一种重要的酸催化剂,在有机合成中起到催化反应的作用。
其次,甲苯磺酸还具有良好的溶解性。
它可以在水中溶解并离解成氢离子(H+)和苯磺酸根离子(C6H5SO3-)。
这使得甲苯磺酸可以作为一种重要的溶剂,在有机合成和催化反应中起到溶剂的作用。
甲苯磺酸的制备方法有多种,下面介绍其中两种常见的工艺:1.甲苯磺酸的合成工艺:以甲苯为原料,氯磺酸为反应试剂,通过磺化反应合成甲苯磺酸。
反应条件通常是在加热和搅拌的条件下进行。
首先将甲苯和氯磺酸按一定的摩尔比加入反应釜中,然后在适当的温度下进行反应。
反应进行一段时间后,产物会从反应混合物中析出。
最后通过过滤、洗涤、干燥等处理得到甲苯磺酸的纯品。
2.甲苯磺酸的氧化工艺:以甲苯为原料,通过氧化反应将其氧化为甲苯磺酸。
常用的氧化剂是过氧化氢(H2O2)。
反应条件通常是在较低的温度和中性条件下进行。
首先将甲苯和过氧化氢按一定的摩尔比加入反应釜中,然后在适当的温度下进行反应。
反应进行一段时间后,产物可以通过蒸馏等方式进行分离和纯化。
总的来说,甲苯磺酸是一种重要的有机磺酸,具有较强的酸性和良好的溶解性。
它可以作为酸催化剂和溶剂在许多有机合成中起到重要的作用。
甲苯磺酸可以通过磺化反应和氧化反应等工艺来制备。
制备过程中需要控制适当的反应条件和纯化步骤,以获得高纯度的甲苯磺酸产物。
对甲苯磺酸制备

对甲苯磺酸制备
甲苯磺酸,又称对甲苯磺酸,是一种常用的有机合成中间体,广泛应用于药物、染料、农药等领域。
本文将介绍如何通过对甲苯硫酸和苯腈合成甲苯磺酸的方法。
我们需要了解对甲苯硫酸和苯腈的化学性质。
对甲苯硫酸是一种白色晶体,可溶于水和乙醇等溶剂,具有较强的酸性。
苯腈则是一种无色液体,有苦杏仁味,可溶于乙醇和乙醚等溶剂,易挥发。
制备甲苯磺酸的方法是通过对甲苯硫酸与苯腈反应,得到产物甲苯磺酸。
反应方程式为:
对甲苯硫酸 + 苯腈→ 甲苯磺酸
在实验室中,可以采用以下步骤进行制备。
步骤一:将对甲苯硫酸和苯腈按照化学计量比例混合,并加入适量的溶剂,如甲醇、乙醇或二甲苯等,以增加反应的速率和效率。
步骤二:加热反应混合物,将其保持在一定的温度范围内,通常为100-120摄氏度。
反应过程中,需要不断搅拌反应液,以保证反应均匀。
步骤三:反应进行一定时间后,将反应液冷却至室温,然后过滤得到产物甲苯磺酸,再用适量的溶剂将其洗涤干净。
需要注意的是,在实验过程中,需要控制反应的温度和时间,以避免产生副反应和不必要的损失。
此外,也需要对反应液的pH值进行调节,以提高反应效率和产物纯度。
甲苯磺酸在医药、染料、农药等领域中具有广泛的应用前景。
例如,在医药领域中,甲苯磺酸可以用于合成抗肿瘤药物、抑制剂等;在染料领域中,甲苯磺酸可以用于合成各种颜料;在农药领域中,甲苯磺酸可以用于合成杀虫剂、除草剂等。
甲苯磺酸是一种重要的有机合成中间体,其制备方法简单,应用范围广泛。
未来,随着科技的不断发展和应用领域的扩大,甲苯磺酸的研究和开发将会得到更广泛的关注和应用。
对甲苯磺酸制备实验报告

对甲苯磺酸制备实验报告甲苯磺酸制备实验报告引言甲苯磺酸是一种重要的有机合成中间体,广泛应用于医药、染料、涂料等领域。
本实验旨在通过对甲苯磺酸的制备过程进行研究,探索最优的制备条件和方法。
实验原理甲苯磺酸的制备方法主要有两种:一种是通过甲苯与浓硫酸反应得到甲苯磺酸;另一种是通过甲苯与亚硝酸钠反应生成对甲基苯磺酸,再通过酸化反应得到甲苯磺酸。
实验步骤1. 实验前准备准备好所需的实验器材和试剂,包括甲苯、浓硫酸、亚硝酸钠等。
2. 反应条件选择根据实验要求和已有文献资料,选择适宜的反应条件。
如温度、反应时间、反应物的摩尔比等。
3. 反应操作将甲苯和浓硫酸按一定比例加入反应瓶中,加热搅拌,控制反应温度在适宜的范围内。
反应结束后,将反应混合物进行冷却。
4. 结晶分离将反应混合物转移到漏斗中,加入适量的冷水进行结晶分离。
通过过滤或离心等方式将结晶物分离出来。
5. 洗涤和干燥用冷水洗涤分离得到的结晶物,去除杂质。
然后将洗净的结晶物晾干或用低温烘干。
6. 验收对制备得到的甲苯磺酸进行质量验收,包括外观、纯度、溶解性等方面。
实验结果与讨论通过实验操作,成功合成了甲苯磺酸。
经过结晶分离、洗涤和干燥等步骤,得到了白色结晶状的甲苯磺酸产物。
对产物进行质量验收,外观无明显杂质,纯度较高,溶解性良好。
在实验过程中,我们发现反应温度对甲苯磺酸的产率和纯度有重要影响。
过高的温度可能导致副反应的发生,降低产率和纯度。
因此,在实验中应控制好反应温度,保证反应的高效进行。
此外,亚硝酸钠的用量也是影响甲苯磺酸产率的关键因素。
过量的亚硝酸钠可能导致副反应的发生,降低产率。
因此,在实验中应根据实际需要合理控制亚硝酸钠的用量。
结论通过本次甲苯磺酸制备实验,我们成功合成了高纯度的甲苯磺酸。
实验结果表明,反应温度和亚硝酸钠的用量是影响甲苯磺酸产率和纯度的重要因素。
在实际应用中,可以根据需要对反应条件进行调整,以获得更好的制备效果。
总结甲苯磺酸作为一种重要的有机合成中间体,在医药、染料、涂料等领域具有广泛的应用前景。
对甲苯磺酸的制备

CH3 + H2O SO3H
甲苯80.84%, 水19.16%, 共沸物:b.p. 84.1℃
+ H2SO4
副反应:
CH3
mp 67.5℃, bp128.8 ℃, 微溶于甲苯
CH3 SO3H + H2O
+ H2SO4
有机化学实验
Chem is try !
二、实 验 原 理:
实验设பைடு நூலகம்:
本实验反应可逆,通过加大反应物甲苯的浓度和 除去生成物水(与甲苯形成共沸物)来促使平衡移动。 本实验用过量的甲苯来除去邻位副产物。
化学化工学院
实验二十七
对甲苯磺酸的制备
(4学时) 主讲教师:林东恩
有机化学实验
Chem is try !
有机化学实验
Chem is try !
一、实 验 目 的:
了解芳烃的磺化反应过程; 掌握分水器的使用方法;
理解邻甲苯磺酸和对甲苯磺酸的性质区别
有机化学实验
Chem is try !
二、实 验 原 理:
实验步骤及现象记录格式:
时间
00:00
实验步骤
分布按顺序详细列出
现象
每位同学现象不尽相同,需仔细记 录,每步骤现象与左边步骤对齐。
备注
化学化工学院
请同学们先凭实验卡领取仪器, 然后各自进行实验操作! 请同学们下次实验前预习 “己二酸的制备” !
有机化学实验
Chem is try !
磺化反应:
SO3H + H2SO4 + H2O
CH3
43% 4%
CH3
32% 6%
CH3
13% 8%
对甲苯磺酸制备

对甲苯磺酸制备甲苯磺酸是一种重要的有机化合物,广泛应用于化学、医药、染料、涂料等领域。
对甲苯磺酸是一种甲苯磺酸的同分异构体,其制备方法有多种途径,本文将介绍其中的一种方法。
制备原料制备对甲苯磺酸的原料主要有甲苯、硫酸、硝酸、氧化剂等。
其中,甲苯是最主要的原料,质量的好坏直接影响到产品的质量和产率。
制备方法对甲苯磺酸的制备方法主要有两种:硝化法和氧化法。
硝化法是利用硝酸对甲苯进行硝化反应,生成对硝基甲苯,再通过还原反应制备对甲苯磺酸。
氧化法则是利用氧化剂将甲苯氧化成对甲苯磺酸。
本文将着重介绍氧化法的制备方法。
将甲苯和硫酸加入反应釜中,经过搅拌混合,加热至反应温度(约150℃)。
然后,加入氧化剂(如过氧化氢、过氧化苯甲酰、过氧化丙酮等)进行氧化反应,生成对甲苯磺酸。
反应过程中,需控制反应温度和氧化剂的用量,以避免产生不必要的副产物和降低产率。
反应结束后,将混合物进行冷却,加入适量的水进行稀释,并加入碱液进行中和。
然后,通过过滤和蒸发等工艺步骤,获得对甲苯磺酸的成品。
制备优化对甲苯磺酸的制备方法在实际应用中,还需要根据不同情况进行优化。
例如,在氧化反应中,氧化剂的种类和用量会影响到反应的结果,过量的氧化剂会产生大量的副产物,降低产率。
因此,需要选择合适的氧化剂和用量,以提高产率和产品的质量。
反应温度、反应时间、溶剂种类等因素也会对反应结果产生影响。
因此,在实际操作中,需要进行多次试验和优化,以获得最佳的反应条件和最高的产率。
总结对甲苯磺酸作为一种重要的有机化合物,在实际应用中具有广泛的用途。
其制备方法主要有硝化法和氧化法两种途径,本文重点介绍了氧化法的制备方法。
在实际操作中,需要根据具体情况进行优化,以获得最好的反应结果和最高的产率。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
对甲苯磺酸的设计实验指导书
实验目的:学习芳香族的磺化反应制备芳磺酸;巩固分水器的使用、回流以及重结晶操作反应原理:
主反应:
副反应:
原料与产物的物理常数Array
装置图
实验内容
仪器药品:烧杯(100ml)、布氏漏斗、抽滤瓶、圆底烧瓶、球形冷凝管、分水器、锥形瓶。
甲苯25ml(21.7g,0.24mol),浓硫酸(d=1.84)5.5ml(0.10mol),精盐,浓盐酸。
实验步骤:
①在50ml圆底烧瓶内放入25ml甲苯,一边摇动烧瓶,一边缓慢地加入5.5ml浓硫酸,投入几根上端封闭的毛细管,毛细管的长度的长度应能使其斜靠在烧瓶颈内壁。
在石棉网上用小火加热回流2h或至分水器中积存2ml水为止
②静置。
冷却反应物。
将反应物倒入60mL锥形瓶内,加入1.5mL水,此时有晶体析出。
用玻璃棒慢慢搅动,反应物逐渐变成固体。
用布式漏斗抽滤,用玻璃瓶塞挤压以除去甲苯和邻甲苯磺酸,得粗产品约15g。
(实验到此约3h)
③若欲获得较纯的对甲苯磺酸,可进行重结晶。
在50ml烧杯里,将12g粗产物溶于约6ml 水里。
往此溶液里通入氯化氢气体,直到有晶体析出。
在通氯化氢气体时,要采取措施,防止“倒吸”。
析出的晶体用布氏漏斗快速抽率。
晶体用少量浓盐酸洗涤。
用玻璃瓶塞挤压去水分,取出后保存在干燥器里。
注意事项
1)滴加浓硫酸时一定要在振摇下用滴管慢慢加入。
2)控制加热强度。
3)析晶时要慢慢搅拌。
问题:
1)利用什么性质除去对甲苯磺酸中的邻位衍生物?
2)在本实验条件下,会不会生成相当量的甲苯二磺酸?为什么?
八、设计要求:
从实验原理出发设计原料配比。
从实验反应条件出发设计实验装置
从原料的物理常数等条件设计实验步骤和反应温度、催化剂、溶剂、反应终点的确定。
设计出产物的纯化方法和纯度测定方法
设计出产物的结构测定方法,写出红外光谱分析此化合物的意义完成一份设计实验报告后经教师认可才能完成实验。
