胸腺肽α1
胸腺肽对我们人体的作用原来这么大!

胸腺肽对我们人体的作用原来这么大!2003年非典的时候,小汤山的军队医务人员是全体注射了胸腺肽的,最终0感染。
在新冠疫情确认后,军队派出的医疗队全部都有打胸腺肽。
除了军队医务人员外,当地支援医疗队也尽量打胸腺肽,最终支援的医务人员感染率非常低。
这东西有用么?没人能说出来到底有多大用,但是为什么医生和肿瘤患者都会选择胸腺肽呢?今天我们就来揭秘胸腺肽究竟是什么?01人体的免疫和胸腺胸腺为人体最重要的免疫器官,是人体的免疫中枢有事具有内分泌机能的器官,可分泌胸腺肽类物质,是人体第一道免疫防护城墙。
当一个人出生时,胸腺的重量约为10-15克,这是一个人一生中体重相对最大的时期。
随着年龄的增长,胸腺继续发育到青春期,大约30-40克。
从那时起,胸腺逐渐退化和萎缩,淋巴细胞减少,脂肪组织增加,老年时仅达到15克。
这意味着随着年龄的增长,免疫力会逐渐下降,因此才会有要补充胸腺肽的说法。
02胸腺肽到底是什么胸腺肽(又称胸腺素,Thymosin)是胸腺组织分泌的一类具有生理活性的肽。
含有多种激素,属于α、β、γ三种类型,共同诱导T细胞的成熟和分化。
胸腺肽是从小牛胸腺中发现并纯化的一种具有非特异性免疫作用的小分子多肽。
在疫情期间,医务人员注射胸腺肽以提高免疫力。
03胸腺肽起到的作用是什么?1.在体内不断诱导T细胞分化发育,最终形成大量具有杀伤能力的T细胞2.维持机体免疫平衡,增强T细胞对抗原的识别和杀伤能力3.提高身体抵抗疾病的能力04胸腺肽在各类癌症中的临床研究有哪些?011、胸腺肽α1与结直肠癌:胸腺肽 1对结直肠癌术后化疗患者免疫功能的影响在胸腺肽治疗结直肠癌的研究中,49例结直肠癌术后患者被随机分为单纯化疗组(20例)和胸腺肽A1组(化疗加胸腺肽)。
目的是比较胸腺肽A1是否对患者的免疫功能有积极影响。
结果非常振奋人心,数据显示:单独化疗组治疗8天后,所有患者细胞免疫功能皆降低;化疗+胸腺肽a1组治疗22天后,免疫功能显著高于单纯化疗组;总结:胸腺肽1作为一种免疫增强剂与化疗联合应用,可显著改善被化疗抑制的机体免疫功能,加速T淋巴细胞的恢复,减少化疗的毒副作用,增强患者对化疗的耐受性。
胸腺肽结构式

胸腺肽结构式
胸腺肽α1是一种由28个氨基酸组成的多肽,其结构式如下:
Ac-Ser-Asp-Ala-Ala-Val-Asp-Thr-Ser-Ser-Glu-Ile-Thr-Thr-Lys-Asp-Leu-Lys-Glu-Lys-Lys-Glu-Val-Val-Glu-Glu-Ala-Glu-Asn-OH
其中,Ac表示乙酰基,Ser、Asp、Ala、Val、Thr、Ile、Leu、Glu、Lys 等为氨基酸,OH表示羟基。
胸腺肽α1的分子式为C129H215N33O55,分子量为3108,等电点为。
分子中无半胱氨酸,所以不存在二硫键,唯一的修饰是N-乙酰化。
其构象变化可能与调节免疫应答时淋巴细胞的激活有关。
Ta1在体内稳定性高,但半衰期很短,易被降解。
以上信息仅供参考,如有需要,建议查阅相关文献或咨询专业人士。
α1胸腺肽辅助治疗肺结核疗效观察

收缩 ,这就 和 肾脏集 合管 内的加压素 受体共 同作 用 ,提 高了集合管 重
吸收的 能力 ,也提 高了 胃肠道 平滑肌 的兴奋性 ,因此可 表现为 头疼 、 心脏不 适、腹疼 、血压变 高、多便 、少尿等 异常症状 ,若患者有 心血 管性疾 病 及肺 心病 则 应禁 止其 服用 此类 药物 ,其 异 常反 应的 出现 率
1 . 察上 ,肺 内无 空洞 或缩 小 ,痰菌 转为 阴 /或
性 ;有效 :病 灶范 围减小 ,肺 内空洞 缩小 ,6 月 内痰 菌转 为阴性 。 个
无 效 :不能达到 上述 标准者 。
选择 在2 1年 1 00 月至2 1年5 来 自本院 的6 01 月 0例 肺结 核患 者 ,所
【 关键 词 】抗 结核 化 疗 ; 。 【 胸腺 肽 ;痰 茵转 阴率 ;恢 复效 果 中 图分类 号 :R 2 51 文 献标 识码 :B 文章 编 号 :17 - 14 (02 1- 50 0 6 1 89 21 ) 08 - 2 7
在 全球范 围内 ,当今肺结核 是威胁人体 健康 的主要传染病 ,结 核
50 ・临床 研 究 ・ 8
这 样便 有利 于血 栓 的形成 来堵 塞破 裂的血 管达 到止 血 的 目的[】 1。本 药 的半 衰期较 短 ,可在体 内持续3 mi 右 的效果 ,最 终在 肝脏处 灭 0 n 左 活 ,因此应连 续进行 药物治疗 。但一 般情 况下 ,伴 有 咯血的患者 也 】 会伴有紧 张 、害怕 、恐慌 等心理特 征 ,提高 了交感神经 的兴奋性 ,增 加 心排血量 和肺部血 流量 ,导 致体循环压 和肺动 脉压上升 ,使大 咯血 的症状 不断恶 化 ,治愈率 可在7 %左右 ;而且 可 以引起冠状 动脉 的 0 ]
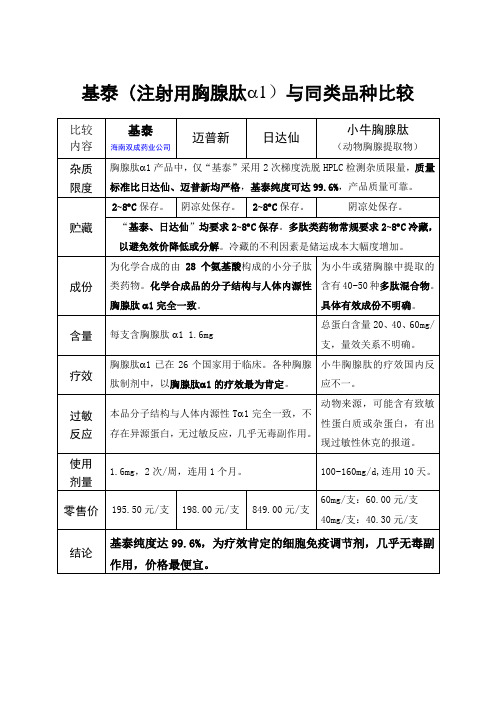
国产胸腺肽α1 基泰与胸腺肽类药品比较
比较
内容
基泰
海南双成药业公司
迈普新
日达仙
小牛胸腺肽
(动物胸腺提取物)
杂质
限度
胸腺肽1产品中,仅“基泰”采用2次梯度洗脱HPLC检测杂质限量,质量标准比日达仙、迈普新均严格,基泰纯度可达99.6%,产品质量可靠。
贮藏
2~8C保存。
阴凉处保存。
2~8C保存。
阴凉处保存。
每支含胸腺肽1 1.6mg
总蛋白含量20、40、60mg/支,量效关系不明确。
疗效
胸腺肽1已在26个国家用于临床。各种胸腺肽制剂中,以胸腺肽1的疗效最为肯定。
小牛胸腺肽的疗效国内反应不一。
过敏
反应
本品分子结构与人体内源性T1完全一致,不存在异源蛋白,无过敏反应,几杂蛋白,有出现过敏性休克的报道。
“基泰、日达仙”均要求2~8C保存。多肽类药物常规要求2~8C冷藏,以避免效价降低或分解。冷藏的不利因素是储运成本大幅度增加。
成份
为化学合成的由28个氨基酸构成的小分子肽类药物。化学合成品的分子结构与人体内源性胸腺肽1完全一致。
为小牛或猪胸腺中提取的含有40~50种多肽混合物。具体有效成份不明确。
含量
使用
剂量
1.6mg,2次/周,连用1个月。
100~160mg/d,连用10天。
零售价
195.50元/支
198.00元/支
849.00元/支
60mg/支:60.00元/支
40mg/支:40.30元/支
结论
基泰纯度达99.6%,为疗效肯定的细胞免疫调节剂,几乎无毒副作用,价格最便宜。
胸腺肽法新说明书

胸腺肽法新说明书摘要:1.胸腺肽法的概念和作用2.胸腺肽法的说明书内容3.胸腺肽法的使用方法和注意事项4.胸腺肽法的副作用和禁忌5.胸腺肽法的储存和有效期正文:胸腺肽法是一种利用重组人胸腺肽α1(rhTα1)刺激人体免疫系统,增强机体抗病毒、抗肿瘤能力的方法。
该方法广泛应用于治疗慢性乙型肝炎、肿瘤等疾病。
本文将详细介绍胸腺肽法的说明书内容。
一、胸腺肽法的概念和作用胸腺肽是一种由胸腺分泌的蛋白质激素,对T细胞的发育和功能具有重要的调节作用。
胸腺肽法通过补充患者体内缺乏的胸腺肽,从而增强机体免疫力,达到治疗疾病的目的。
二、胸腺肽法的说明书内容胸腺肽法的说明书主要包括以下几个方面:1.药品名称:胸腺肽注射液。
2.成分:重组人胸腺肽α1(rhTα1)。
3.性状:无色或微黄色澄明液体。
4.规格:1ml:10μg。
5.用法用量:根据病情和患者年龄,医生会给出具体的用药方案。
一般为皮下注射或肌肉注射,每周1-2次。
6.有效期:24个月。
7.批准文号:国药准字H20103265。
三、胸腺肽法的使用方法和注意事项1.使用方法:皮下注射或肌肉注射。
2.注射前:应摇匀药物。
3.注射后:局部可能有红肿、疼痛,一般无需特殊处理。
4.特殊人群:孕妇、哺乳期妇女和儿童需在医生指导下使用。
5.药物相互作用:与其他药物的相互作用尚不明确,使用时应咨询医生。
四、胸腺肽法的副作用和禁忌1.常见副作用:注射部位疼痛、红肿、硬结等。
2.罕见副作用:过敏反应、发热、头痛等。
3.禁忌:对该药物成分过敏者、活动性结核病患者、严重肝肾功能损害者禁用。
五、胸腺肽法的储存和有效期1.储存:遮光、密封,在阴凉处(不超过20℃)保存。
2.有效期:24个月。
基泰(注射用胸腺肽)说明书

数十位资深药师
实时免费解答用药难题
了解基泰
享受贴心的药学服务
历经十年,服务专业,提倡合理用药,提供 优质药品。
国内首家“全国连锁专科药房”,也是全国大 型的专科医药连锁企业之一。
坚持“专注于重大慢性疾病用药,持续改善患 者健康”的经营理念。
慎重。
【基泰适应症】 1.慢性乙型肝炎。 2.作为免疫损害病者的疫苗免疫应答增强剂。免疫 系统功能受到抑制者,包括接受慢性血液透析和老 年病患,基泰可增强病者对病毒性疫苗,例如流感 疫苗或乙肝疫苗的免疫应答。
【基泰用法用量】 用前每瓶胸腺肽α1(1.6mg)以1ml注射用水溶解后 立即皮下注射(不应作肌注或静注)。 治疗慢性乙型肝炎的推荐剂量:每次1.6mg,每周2 次,两次相隔3-4天。连续给药6个月(共52针), 其间不应间断。
【百济药师温馨提示】
对基泰成份过敏者禁用;正在接受免疫抑制治疗的患 者如器官移植者禁用。
【基泰不良反应】
胸腺肽α1的耐受性良好。部分患者可有注射部位不 适。慢性乙肝患者接受基泰治疗时,可能出现ALT水 平暂时波动至基础值两倍以上,此时通常应继续使用, 除非有肝衰竭的症状和预兆出现。
基泰价格、优惠
【基泰成分】 主要成份:每瓶含胸腺肽α1 1.6mg,甘露醇 14.4mg。
【基泰性状】 基泰为白色疏松块状物。
【基泰毒理研究】 遗传毒性:基泰遗传毒性试验结果阴性。
生殖毒性:基泰对动物胎仔无明显致畸作用。目前 尚不清楚妊娠妇女使用基泰后,是否会影响其生殖 能力或对胎儿造成损害。只有在确实需要时,妊娠 妇女才能使用基泰。同样,目前也不清楚基泰是否 能够经人乳汁分泌,因此哺乳期妇女使用基泰时应
基泰注射用胸腺肽说明书注射用胸腺肽注射用胸腺肽a1胸腺肽注射液胸腺肽注射液价格胸腺肽说明书慧基泰展陕西基泰基泰工程司诸城基泰
日达仙(注射用胸腺肽α1)

日达仙(注射用胸腺肽α1)【药品名称】商品名称:日达仙通用名称:注射用胸腺肽α1英文名称:Thymosin Alpha-1 for Injection【成份】主要成份:每瓶含胸腺肽α1 1.6mg,甘露醇14.4mg。
【适应症】1.慢性乙型肝炎。
2.作为免疫损害病者的疫苗免疫应答增强剂。
免疫系统功能受到抑制者,包括接受慢性血液透析和老年病患,本品可增强病者对病毒性疫苗,例如流感疫苗或乙肝疫苗的免疫应答。
【用法用量】用前每瓶胸腺肽α1(1.6mg)以1ml注射用水溶解后立即皮下注射(不应作肌注或静注)。
治疗慢性乙型肝炎的推荐剂量:每次1.6mg,每周2次,两次相隔3-4天。
连续给药6个月(共52针),其间不应间断。
临床试验提示胸腺肽α1与α干扰素联用可能比单用α干扰素或单用胸腺肽α1效果为好。
如联用α干扰素,应参考α干扰素处方资料内的剂量和注意事项。
一般胸腺肽α1在上午给药而α干扰素在晚上给药。
作为免疫损害病者的疫苗免疫应答增强剂:每次1.6mg,每周2次,两次相隔3-4天,连续4周(共8针),第一针应在给疫苗后立即皮下注射。
【不良反应】本品耐受性良好。
超过2000例不同年龄各种疾病的患者得到临床经验,没有任何关于使用本品发生不良事件的报导。
病毒性感染(慢性乙型肝炎、慢性丙型肝炎、人类免疫功能低下症);癌症(非小细胞肺癌、黑色素瘤);疫苗增强剂(乙型肝炎疫苗、流感疫苗);免疫异常(自身免疫性肝病、原发性免疫缺乏症)所有适应症的副反应发生率少于1%。
副作用都很轻微且并不常见。
主要是注射部位疼痛。
极少情况下有红肿、短暂性肌肉萎缩,多关节痛伴有水肿和皮疹。
慢乙肝病人接受本品治疗时,可能ALT水平有一过性上升到基础值的两倍(ALT波动)以上,当ALT波动发生时本品通常应继续使用,除非有肝衰竭的症状和预兆出现。
基泰注射用胸腺新

基泰注射用胸腺新关于《基泰注射用胸腺新》,是我们特意为大家整理的,希望对大家有所帮助。
基泰注射用胰腺新别名胸腺肽α1,适用漫性乙型肝炎及其做为免疫力危害病患的疫苗免疫应答改性剂。
针对免疫功能接到抑止的病人,可以协助其提高回复。
要在医师的具体指导下服药,切勿盲目跟风擅自应用药品,以防造成皮肤过敏,使用量还要严控,在应用全过程中若出現副作用应立即就诊。
基泰(注射用胸腺法新)聚瑞胸腺肽α1的优良安全系数归功于它的高纯,人造合成的胸腺肽α1纯净度达到99.6%上下,另外以碳水化合物为起止原材料的生产加工工艺,保证其肯定不带有高分子材料残渣,因此最大限度地减少了致敏性和模糊不清物质引起的模糊不清生理需要,这一优势是其他小动物原性(一般胸腺肽),绿色植物原性(猪苓含糖量、香姑含糖量),转基因水稻原性(干扰素栓、白介素)免疫制剂所无可比拟的,由于后几种药品全是带有活性物质的化合物,并非特异性分子结构单个。
血压主冶作用1.漫性乙型肝炎。
2.做为免疫力危害病患的疫苗免疫应答改性剂。
人体免疫系统作用遭受抑止者,包含接纳漫性血液分析和老年康复患,本产品可提高病患对病毒性感染疫苗,比如流感疫苗或乙肝疫苗的免疫应答。
血液副作用胸腺法新的耐受力优良。
一部分病人可能有注射位置不适感。
慢性乙肝病人接纳本产品医治时,可能出現ALT水准临时波动至基本值二倍以上,这时一般应再次应用,除非是有肝衰竭的病症和征兆出現。
补充忌讳对本产品成分过敏症状禁止使用;已经接纳免疫抑制医治的病人如肝脏移植者禁止使用。
负重常见问题1、当用于医治慢性乙肝时,肝功能检查实验,包含血细胞ALT、人体白蛋白和总胆红素应在医治期内作定期评定,医治结束后应检验乙肝e抗原(HBeAg)、表面抗原(HBsAg)、HBV-DNA 和ALT酶,亦应在医治结束后2、4和6月检验,由于患者可能在医治结束后随诊期限内出現回复。
2、本产品应在医生具体指导下运用。
如病人自主去医院外应用,应留意注射器材的消毒杀菌和解决。
胸腺肽α1的作用机制和临床应用

""""""""""""""""""""""""""""""""""""""""""""""""
[ 关键词] 胸腺肽 !! ;作用机制;临床应用 [ 中图分类号] D&,’- !’+ + + [ 文献标识码] E 功能而调节免疫系统的,概括起来大致有以下几个方面: ! - !" 免疫调节作用 " ( ! ) 诱导和促进胸腺细胞的分化和成 熟:<!! 可促进胸腺内的骨髓干细胞转化为 < 淋巴细胞,并 + + 胸腺肽 !! ( :;F@/264 8=3;8>! ,<!! ) 是 G/H 等
或不存在的条件下,<!! 可促进骨髓来源的树突状细胞 ( M. ) 成熟分化并增强其功能,而 M. 直接影响 < 细胞的成熟和分
[(] [#] 化 。研究表明 ,<!! 不但促进表达 .M) [ 的树突状细胞
!" #!! 的作用机制
<!! 是由 ’% 个 氨 基 酸 组 成 的 多 肽,其 组 成 为:EC>N10> E23>E=8>O8=>E23><;0>N10>N10>P=9>J=1><;0><;0>GF2>E23>G19>GF2> P=9>GF2>GF2>P=9>O8=>O8=>P=9>P=9>E=8>P=9>E24>QR。 相 对 分 子 质量 ( !0 ) 为 & !"% ,SJ 为 )- ’ 。美国 NC6.=/41 公司生产的药品 日达仙 ( T858U64 ) 是一种人工化学合成的 <!! ,每支产品含 <!! !- ( @7,供皮下注射。该产品的 3R 为 (- % ,血浆半衰期 约 ’ ;。每次注射后使外周血中 <!! 的浓度增加约 *" V !"" 倍, ’ ; 后可达 *" "7 W G。在慢性乙型肝炎 ( .RX ) 和慢性丙型 的治疗中,每周 ’ 次注射,在肿瘤患者化疗过程 肝炎 ( .R.)
国产胸腺肽α1配合化疗治疗中晚期肿瘤

国产胸腺肽α1配合化疗治疗中晚期肿瘤【关键词】胸腺肽α1;恶性肿瘤;免疫功能人工合成的胸腺肽α1 是一种较为有效的提高机体免疫功能的生物反应调节剂,国内外用于肝炎和恶性肿瘤的治疗已取得满意的疗效〔1,2〕。
本文对中晚期恶性肿瘤化疗患者应用胸腺肽α1(迈普新)治疗,观察生活质量的影响。
1 资料与方法1.1 一般资料经病理学确诊为恶性肿瘤患者30例,符合美国国立癌症综合网络(NCCN)的TNM分期标准Ⅲ~Ⅳ期,年龄36~68〔平均(52±14.8)〕岁,其中男19例,女11例,健康状况自我评分(KPS)>60分,预计生存期>3个月。
30例患者中胃癌5例,肠癌15例,非小细胞肺癌10例,其中20例患者出现远处转移。
患者随机分为治疗组和对照组两组,各15例。
1.2 治疗方法对照组采用单纯化疗,治疗组在化疗给药的第1天起使用国产胸腺肽α1(商品名:迈普新)1.6 mg皮下注射,每周2次,疗程为1个月,3个疗程后进行评估,全部病例均完成3个疗程,两组化疗均使用相同方案。
胃癌使用表柔比星、顺铂和5氟尿嘧啶(ECF)方案,肠癌使用奥沙利铂联合5氟尿嘧啶/甲酰四氢叶酸(FOLFOX4)方案,非小细胞肺癌使用健择/泰素/顺铂(GTP)方案。
1.3 观察指标(1)近期疗效按NCCN推荐的实体瘤疗效评价标准,完全缓解(CR),部分缓解(PR),稳定(SD),进展(PD),CR+PR为有效。
(2)免疫功能指标:比较治疗前后T细胞亚群(CD3,CD4,CD8细胞数及CD4/CD8比值),检测自然杀伤(NK)细胞活性。
1.4 统计学方法应用SPSS13.0统计软件进行处理,资料数据以x±s表示,组间比较采用χ2及配对的t检验。
2 结果2.1 近期疗效对照组CR 1例,DR 6例,总有效率47%;治疗组CR 2例,PR 7例,总有效率60%,两组无显著性差异。
2.2 免疫功能指标治疗前后细胞免疫指标变化,治疗组CD3,CD4,CD8,CD4/CD8,NK淋巴细胞活性明显高于对照组,差异有显著性(P<0.05)。
胸腺肽临床应用指引

注射用胸腺法新临床应用指引注射用胸腺肽α1作为免疫调节剂主要是通过增强T细胞功能而调节机体的免疫系统,其说明书中的适应症为:①慢性乙型肝炎患者;②作为免疫损害患者。
使用前每瓶胸腺肽α1(1.6mg)以1ml注射用水溶解后立即皮下注射(不应作肌注或静注)。
治疗慢性乙型肝炎的推荐剂量:每次1.6mg,每周2次,两次相隔3-4天。
连续给药6个月(共52针),其间不应间断。
作为免疫损害病者的疫苗免疫应答增强剂:每次1.6mg,每周2次,两次相隔3-4天,连续4周(共8针),第一针应在给疫苗后立即皮下注射。
《中国严重脓毒症/脓毒性休克治疗指南(2014)》、Me ta分析及数篇多中心随机对照研究指出对胸腺肽α1能降低严重脓毒症患者28天病死率;也有大量文献报道胸腺肽α1可提高重症肺炎、恶性肿瘤患者的免疫力。
该药耐受性良好。
部分患者可有注射部位不适。
慢性乙肝患者接受本品治疗时,可能出现ALT水平暂时波动至基础值两倍以上,此时通常应继续使用,除非有肝衰竭的症状和预兆出现。
我院现有两种注射用胸腺法新:商品名分别为日达仙(意大利赛生制药有限公司)及和日(海南中和药业有限公司)。
抽查使用该药的ICU病人11例,主要用于重症肺炎伴呼吸衰竭及感染性休克、脓毒症患者,均属于超说明书用药,也有循证数据支持,一般推荐的用法、用量及疗程为:1.6毫克,1次/天,连续7天,联合其他药物时也有用到1.6mg,2次/天,连续3天,后改为1.6毫克,1次/天,连续四天。
在我们的抽查病例中,胸腺法新的用法、用量均符合推荐,但疗程方面欠妥,使用时间最短的为2天,最长达36天。
对注射用胸腺肽α1的临床应用提出以下建议:1 禁用该药的患者:①对胸腺法新或注射液内任何成份有过敏历史的患者;②免疫抑制的病人例如器官移植受者;③年龄在18岁以下的患者;2 本品为怀孕C类,只能在真正需要时给予怀孕妇女使用;3 本品与其它免疫调节药物同时使用时,以避免与任何其它药物混合后注射;4 用于严重脓毒症,重症肺炎伴呼吸衰竭患者时,使用疗程不宜超过7天;5 用于恶性肿瘤患者,依据治疗方式的不同,推荐以下用法:①手术患者,术后使用,1.6毫克,1次/天,②放疗患者:900ug/m2,2次/周,③化疗患者,化疗前4天,1.6毫克,1次/天,化疗后,1.6毫克,3次/周,具体使用情况依据患者基本情况及病情等而定。
胸腺肽α1用于反复呼吸道感染老年患者的疗效观察和护理

摘要 : 目的 胸腺肤 a 用于反复呼吸道 感染老年患者疗效的临床观察和护理。 方法 l 将 4 例反复呼吸道感染老 年患者随机分 为两组. 0 治疗
组( =2 ) n 0 用胸腺肽 口 加常规 治疗. I 对照组( :2 ) 予常规治疗。两组患者均进行 1年的随访观察 。 4周随访 1次, 行临床病精评价。 结 n 0给 每 进 果 治疗组病人给予用药前 、 治疗中、 治疗后的宣教和护理, 所选病例均完成 1年时间的用药, 出现不 良反应 , 治疗后, 无 经 治疗组的上呼吸道 感
治疗 。
*与 治 疗 前 比较 。 P<0 0 .5
3 讨 论
妊 娠 期 妇 女 由于 血 容 量 的 增 加 和 胎 儿 生 长 发 育 的 需 要 , 对 铁 的 需 要 量 增 大 。 期 额 外 需 铁 较 多 ( 1虽然 此 时 孕 妇 对 铁 的 吸 收率 提 高 , 每 但
参考 文 献
(] ee M, e d i sMK. e r 1 P rzE H n r k c B a d儿 , t 1 Mo h r n a t n ea t n e . te . fn trci s a i i o
a d n a td v lp n r le e y ma e n r n d f in y a e a n i f n e e me ta e at r d b t r a i e i e c n mi o l o c
血清蛋 白铁 (F 恢复正常 ; s) 好转 : 内 H 8周 b较治疗 前至少上 升 2gL 1无效 : 不到上述标准。 0 ・ -; 达
17 数据统计方法 . 计 量 资 料 以均 值 ±标 准 差 表 示 。 组 间 计 量 资 料采 用 t 验 。 数 资 料 用 . 检 验 。P<0 0 检 计 ) c .5为 有 统
胸腺肽α1在肾病综合征中的应用及研究进展

胸腺肽α1在肾病综合征中的应用及研究进展黎汝婷综述刘华锋,姚翠微审校广东医科大学附属医院肾脏疾病研究所,广东湛江524001【摘要】肾病综合征是较常见的慢性肾脏病,其并发症或反复复发可导致疾病迁延进展,从而对患者造成更多的精神心理和经济负担。
目前认为免疫功能失衡与肾病综合征的发病密切相关。
胸腺肽α1作为免疫调节剂,具有改善机体免疫功能、抗氧化、抗炎等作用,在临床上越来越受重视并且在肿瘤及感染等疾病中已经广泛应用于临床,但在肾病综合征中的作用效果仍有待进一步探究。
胸腺肽α1的免疫调节疗法或可能成为新的治疗方法应用于肾病综合征。
因此,本文将对胸腺肽α1在肾病综合征中的潜在作用机制及临床价值进行综述。
【关键词】肾病综合征;胸腺肽α1;免疫调节治疗;临床应用;研究进展【中图分类号】R692【文献标识码】A【文章编号】1003—6350(2020)22—2975—04Application and research progress of thymosin α1in nephrotic syndrome.LI Ru-ting,LIU Hua-feng,YAO Cui-wei.Institute of Nephrology,the Affiliated Hospital of Guangdong Medical University,Zhanjiang 524001,Guangdong,CHINA【Abstract 】Nephrotic syndrome is a more common chronic kidney disease,and its complications or repeated re-currence can lead to the progression of the disease,thus causing more mental,psychological and economic burden to pa-tients.As an immunomodulator,thymosin α1has the effects of improving immune function,anti-oxidation,anti-inflam-mation and so on.It has been paid more and more attention in clinic and has been widely used in diseases such as tumor and infection.However,the effect of thymosin α1on nephrotic syndrome remains to be further explored.Thymosin α1im-munomodulatory therapy may become a new treatment for nephrotic syndrome.Therefore,this article will review the po-tential mechanism and clinical value of thymosin α1in nephrotic syndrome.【Key words 】Nephrotic syndrome;Thymosin α1;Immunomodulatory therapy;Clinical application;Research progress·综述·doi:10.3969/j.issn.1003-6350.2020.22.030基金项目:广东省湛江市科技攻关计划项目(编号:2014B01204);广东医科大学附属医院临床研究项目(编号:LCYJ2017A0002)通讯作者:姚翠微,主任医师,E-mail:********************肾病综合征(nephrotic syndrome ,NS)是一个主要表现为大量蛋白尿(≥3.5g/d)、低蛋白血症(血浆白蛋白≤30g/L)、高脂血症、水肿的临床症候群[1-2]。
胸腺肽α1对肝硬化并自发性细菌性腹膜炎的治疗价值

2 . 4 副反应
治疗 。
所 有患者 治疗 前 、 后对 比血 常规 、 尿 常规 、 电
解质和 肾功能等检查项 目, 均无异 常变化 。所有 患者均 完成
表 2 治疗前 、 后两组患者肝功能改善
情况 比较 ( 士5 , n =3 0 )
隔簪 理论 与 甄艘
2 0 1 3 年第 2 6 卷第 1 3 期
Vo 1 . 2 6 , No . 1 3 , J u l 2 0 1 3 J Me d T h eor &P r ac 囹 1 7 3 7 9 7 . 0 , 对照组 总有效 率 8 3 . 0 。两 组 比较有 显 著性 差 异
组织 委员会( C I O Ms ) 的推荐分为 : 肝细胞损伤类 型 : A I ≥2 倍正 常值上限或 R ̄5 ( R = 超过 正常 的最大倍数 的上 限/ A LP超 过正常值 上 限的倍 数 ) , 胆 汁淤 积 类型 : AL P ≥2 倍正 常值上限或 R ≤2 ; 混合型 : 6 和A I , I , 、 > 2 倍 的正常 的
积 的肝 损害 1 3 例, 肝功能损害 6例 。两组性别 、 年龄 和临床
注: 治疗前和治疗后 , 肝功能改善存 在显著性差异 。 P <0 . 0 1 , 治 疗后治疗组 和对照组仍存在显著性差异a P <0 . 0 5 。
3 讨 论
分型等均没 有显著性差异 ( P >0 . 0 5 ) , 顾具有可 比性 。
治疗后 5 1 . 1 士3 7 . 5 5 7 . 7 士4 3 . 2 3 2 . 6 - t - 2 5 . 9
汁淤积 性损害 1 1 例, 肝 功能损 害 7例 ; 对照组 3 O 例, 男 1 6 例, 女1 4 例 。平 均年龄 6 2 . 5 1 岁; 肝 细胞损 伤 1 1 例, 胆 汁淤
胸腺肽α1治疗严重脓毒症的疗效评估

胸腺肽α1治疗严重脓毒症的疗效评估欧阳骞【摘要】目的探讨胸腺肽α1治疗严重脓毒症的疗效.方法根据治疗方案将69例严重脓毒症患者分为对照组(32例)与观察组(39例),对照组接受常规治疗,观察组在常规治疗基础上再联合使用胸腺肽α1.现回顾分析上述研究对象的临床资料.结果治疗前,两组患者急性生理功能和慢性健康状况(APACHEⅡ)评分、序贯性器官衰竭(SOFA)评分相比差异无统计学意义(P>0.05);治疗7d后,观察组APACHEⅡ评分、SOFA评分均显著低于对照组(P<0.05).治疗前,两组患者外周血CD3+T细胞、CD4+T细胞、CD8+T细胞,血清α-肿瘤坏死因子(TNF-α)、C反应蛋白(CRP)、降钙素原(PCT),血浆内毒素相比差异无统计学意义(P>0.05);治疗7d后,观察组外周血CD3+T细胞、CD4+T细胞、CD8+T细胞均显著高于对照组(P<0.05),血清TNF-α、CRP、PCT,血浆内毒素均显著低于对照组(P<0.05).观察组呼吸机使用时间、ICU治疗时间均显著低于对照组(P<0. 05),两组患者28d病死率相比差异无统计学意义(P>0.05).结论胸腺肽α1治疗严重脓毒症的疗效良好,在改善患者免疫功能的同时还可以调节其炎症反应状态.【期刊名称】《江西医药》【年(卷),期】2017(052)010【总页数】3页(P1004-1006)【关键词】胸腺肽α1;严重脓毒症;免疫功能;炎症反应【作者】欧阳骞【作者单位】江西省肿瘤医院重症医学科,南昌330029【正文语种】中文【中图分类】R459.7脓毒症是指感染引起的全身炎症反应综合征(SIRS),当脓毒症患者伴随有由其导致的器官功能障碍和/或组织灌注不足时即称之为严重脓毒症[1]。
严重脓毒症是重症医学面临的重要临床问题之一,随着人口老龄化的加重、恶性肿瘤发病率的升高、侵入性医疗手段的增加,脓毒症以及严重脓毒症在临床上愈来愈常见,因此探讨治疗严重脓毒症的有效方案一直以来都是重症医学研究的热点[2,3]。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
胸腺肽α1
胸腺肽α1是一种化学合成药物,是一个乙酰化的多酞,有如下的氨基酸组合:
Ac-Ser-Asp-Ala-Ala-Val-Asp-Thr-Ser-Ser-Glu-Ile-Thr-Thr-Lys-Asp-Leu-Lys-Glu-Lys-Lys-Glu-Val-Val-Glu-Val-Val-Glu-Glu-Ala-Glu-Asn-OH,其分子量是3108,PI是3.8。
注射用胸腺肽α1是胸腺肽α1的消毒冻干粉制剂,每一瓶含1.6 mg胸腺肽α1。
【申请类别】6类
【剂型规格】原料、冻干粉针(1.6mg)
【适应症】1.慢性乙型肝炎。
2.作为免疫损害病者的疫苗免疫应答增强剂。
免疫系统功能受到抑制者,包括接受慢性血液透析和老年病患,本品可增强病者对病毒性疫苗,例如流感疫苗或乙肝疫苗的免疫应答。
【用法用量】
本药不应作肌注或静注。
应使用随盒的1.0 mL注射用水溶解后马上皮注。
慢性乙型肝炎本药治疗慢性乙肝的推荐量是每针1.6 mg,皮下注射,每周二次,两剂量大约相隔3-4日。
治疗应连续6个月(52针)期间不得中断。
假如本药是与α干扰素联合使用,应参考α干扰素处方资料内的剂量和注意事项,在联合应用的临床经验上,当两药物在同一日使用时,一般上在早上给予本药而在晚上给予干扰素。
作为免疫损害病者的疫苗增强剂本药作为病毒性疫苗增强剂使用,推荐剂量是1.6 mg 皮下注射,每周二次,每次相隔3-4日,疗程应持续4周(共8针),第一针应在疫苗后马上给予。
【专利及行政保护情况】
开发申报胸腺肽α1及粉针不涉及专利或行政保护情况,现有几个制剂制备方法专利在申请,不影响本品开发。
【生产申报情况】
胸腺肽α1早在1999年国内即有开发申报,2002年成都地奥九泓制药厂首家获得批准生产,保护期6年;同期亦有意大利进口品获批准,商品名“日达仙”。
国内生产企业如下:注射用胸腺肽α1 (国药准字H20103322 上海实业联合集团长城药业有限公司
注射用胸腺肽α1 (国药准字H20103201 苏州天马医药集团天吉生物制药有限公司
注射用胸腺肽α1 (国药准字H20051916 海南中和药业有限公司和日
注射用胸腺肽α1 (国药准字H20020545 成都地奥九泓制药厂迈普新
下表为标准转正后,自2006年底以来申报的企业(其中2家已批准,见上表)受理号药品名称申请类型注册类型CYHS0901066 注射用胸腺肽α1 成都圣诺生物制药有限公司2010-5-24在审评CYHS0901065 胸腺肽α1 成都圣诺生物制药有限公司2010-5-24在审评CXHS0900130 胸腺肽α1注射液海南中和药业有限公司2010-6-24发批件CYHB0812580 注射用胸腺肽α1 北京凯因科技股份有限公司2009-7-21发批件CYHB0812581 胸腺肽α1 北京凯因科技股份有限公司2009-7-21发批件CYHR0800077 胸腺肽α1 成都圣诺生物制药有限公司2009-10-22发批件CYHS0800821 注射用胸腺肽α1 哈药集团生物工程有限公司在审评
CYHS0800820 胸腺肽α1 哈药集团生物工程有限公司在审评
CYHS0700638 注射用胸腺肽α1 扬子江药业集团四川海蓉药业有限公司2009-4-27发批件CXHS0700167 胸腺肽α1注射液北京双鹭立生医药科技有限公司2009-7-21发批件CYHS0700329 胸腺肽α1 北京凯因生物技术有限公司2009-7-17发批件CYHS0700330 注射用胸腺肽α1 北京凯因生物技术有限公司2009-4-27发批件CYHS0604626 注射用胸腺肽α1 成都圣诺生物制药有限公司2009-4-27发批件CYHS0604625 胸腺肽α1 成都圣诺生物制药有限公司2008-10-31发批件
从上表可以看出,除已获批准2家外,还有4家在申报注射用胸腺肽α1,其中有的企业经退审后,多次申报。
实际上,现在药审中心还在审评的只有“成都圣诺生物制药有限公司”、“哈药集团生物工程有限公司”2家。
上表中还显示有2家企业申报了改剂型5类新药胸腺肽α1注射液,从审评结果来看,并未获得批准。
【药理作用】
本品治疗慢性乙型肝炎和增强免疫系统反应性的作用机制尚未完全阐明。
多项体外试验显示,本品通过刺激外周血液淋巴细胞丝裂原来促进T淋巴细胞的成熟,增加抗原或丝裂原激活后T细胞分泌的干扰素α、干扰素γ以及白介素2、白介素3等淋巴因子水平,同时增加T细胞表面淋巴因子受体水平。
本品还可通过对CD4细胞的激活,增强异体和自体的人类混合淋巴细胞反应。
本品可能增加前NK细胞的聚集,而干扰素可使其细胞毒性增强。
体内试验显示,本品可以提高经刀豆蛋白A激活后小鼠淋巴细胞白介素2受体的表达水平,同时提高白介素2的分泌水平。
【临床评价】
本药用来治疗那些18岁以上的慢性乙型肝炎患者,且患者的肝病有代偿性和有乙肝病毒复制(血清HBV-DNA阳性),在那些血清乙肝表面抗原阳性最少6个月,且有血清转氨酶升高的患者所做的研究显示,本药治疗后可产生病毒性缓解并使转氨酶水平恢复正常。
在一些作出应答的患者,本药治疗可除去血清表面抗原。
临床试验提示当本药与α干扰素联用时可能比单用本药或单用干扰素具有更高的应答率。
作为免疫损害病者的免疫增强剂免疫系统功能受到抑制者,包括接受慢性血液透析者和老年病患,本药可增强病者对病毒性疫苗,例如流感疫苗或乙肝疫苗的免疫应答。
对血液透析患者所作研究显示,在接种流感疫苗后,应用本药作为佐剂者有65%病人产生抗流感病毒抗体滴度水平增高4倍以上,安慰剂组只有24%患者作出此反应。
【市场评估】
胸腺肽α-1有广泛临床应用的非特异性免疫调节剂,具有高活性,无副作用,无毒性和适应症广泛等诸多优点,同时产品本身具有低生产成本,高附加值的经济学特性。
1.用于治疗慢性乙型肝炎、丙型肝炎、重症肝炎
我国为肝炎大国,人群中乙肝病毒携带者占10%,约1.2亿人,其中20%会发展成需要接受治疗的乙肝患者,加上丙型肝炎患者,临床意义上的肝炎患者在2500万人以上,而且此数量每年仍在递增。
慢性肝炎不同于普通炎症,是与自体免疫状态密切相关的疾病,因此在肝炎治疗方案中运用免疫调节剂已成为广大肝病医师的共识。
2.用于治疗恶性肿瘤,自体免疫病(风湿,类风湿,红斑狼症等)及其它免疫相关性疾病,可明显降低放化疗副反应,改善患者生存品质,延长患者生存期。
我国恶性肿瘤发病率按最保守估计约为0.1%,则每年新增患者120万例。
3.此外,风湿、类风湿及老年性免疫功能退化患者为数众多,其中任一适应症的应用前景都是广阔的。
随着市场深度和广度的不断扩展,仍将有新的适应症被发掘。
自2002年以来,国产与进口2个产品对市场不断开拓,已使胸腺肽α1的应用有了雄厚的市场基础。
算上2005年才获准上市的海南中和,实际到到2010年为止,市场上仅有3家企业,因此本品尚有较大的市场容量待开发。
附:注射用胸腺肽α1零售参考价格
【开发事项】
原料及粉针现申报均可,注射液不建议申报。
PS:
查询可见,现国内常见胸腺肽产品有胸腺五肽、胸腺肽、胸腺肽α1三种,区别简述如下:
1、胸腺五肽由5种氨基酸组成,胸腺肽α1由28种氨基酸组成,均是采用化学工程固相方法合成,纯度高,用药前不需做皮试;而胸腺肽采用从动物胸腺提取(从小猪、小牛胸腺中冷冻提取),可能会产生过敏等不良反应,有时用药前需做皮试。
2、胸腺五肽与胸腺肽α1有明确的生物化学分子式,而胸腺肽成分不稳定,内含不明确,缺乏标准化(现在尚无胸腺肽原料标准)。
3、胸腺五肽与胸腺肽α1含量稳定,保质期较长;而胸腺肽含量不稳定,缺乏质控标准,随原料不同,厂家工艺不同,质量和含有效治疗量,每批不一样。
