新技术新项目评审表
新产品项目评审表

批准: □批准 □有条件批准 □暂缓或放弃该项目
签名/日期:
是□ 否□
潜在风险
23 设备 裁切设备是否需要改造
24
部 挤出、定型、牵引等设备是否需要 改造
潜在风险
是□ 否□ 是□ 否□
评审结论(逐步列出):
项目编号: 期望完成日 试模材期料用
量 试料次数 评审时间
备注(可附页)
销售审核
材料审核
工程组审 核
工模组审 核
品质部审 核
采购部审 核
生产部审 核
设备部审 核
16
设计模具目标效率能否满足
是□ 否□
潜在风险
17 品质 检测标准是否明确 18 部门 是否需新制检验工具
是□ 否□ 是□ 否□
潜在风险
19 采购 模具是否有外协加工 20 部门 其他部件是否外购
是□ 否□ 是□ 否□
潜在风险
21 生产 人力/设备/工装资源情况能否满足 是□ 否□
22 部门 技术/品质/质量目标能否满足
是□ 否□
2 销售 客户一般要求是否清楚
是□ 否□
3 部门 适配件种类
堵头□ PCB板□ 电源□ 铝条□
本项工作 负责人
4
适配件能否提供
能□ 否□
潜在风险
5 材料 是否清楚材料要求 6 研发 材料是否可准时提供
是□ 否□ 是□ 否□
潜在风险
7பைடு நூலகம்
结构是否满足(DFM或结构审查)
是□ 否□
8
成本评估表是否完成
新产品/项目评审表 V6.0
客户编码:
产品名称:
销售:
模具交期 材料交期 裁切方式
下单/立项时间 目标效率(s/m) 定型工艺方式
34新项目评审表
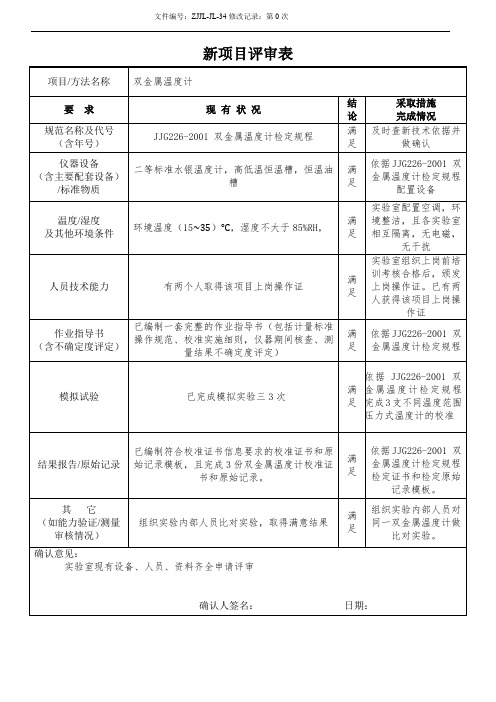
其它
(如能力验证/测量审核情况)
组织实验内部人内部人员对同一双金属温度计做比对实验。
确认意见:
实验室现有设备、人员、资料齐全申请评审
确认人签名:日期:
温度/湿度
及其他环境条件
环境温度(15 ) ,湿度不大于85%RH,
满足
实验室配置空调,环境整洁,且各实验室相互隔离,无电磁,无干扰
人员技术能力
有两个人取得该项目上岗操作证
满足
实验室组织上岗前培训考核合格后,颁发上岗操作证。已有两人获得该项目上岗操作证
作业指导书
(含不确定度评定)
已编制一套完整的作业指导书(包括计量标准操作规范、校准实施细则,仪器期间核查、测量结果不确定度评定)
新项目评审表
项目/方法名称
双金属温度计
要 求
现 有 状况
结 论
采取措施
完成情况
规范名称及代号
(含年号)
JJG226-2001 双金属温度计检定规程
满足
及时查新技术依据并做确认
仪器设备
(含主要配套设备)/标准物质
二等标准水银温度计,高低温恒温槽,恒温油槽
满足
依据JJG226-2001 双金属温度计检定规程配置设备
新检测项目评审表一

胶砂振实台、水泥成型养护箱、 水泥试体养护箱
2.设备:
SFY-150水泥细度负压筛析仪(SB-017) SZB-9水泥比表面积测定仪(SB-016) NJ-160A水泥净浆搅拌机(SB-008) 水泥标准稠度凝结时间测定仪(SB- 009)
SBY-64B水泥试体养护箱(SB-007)
口是
□否
3.检测环境:
20±2°C、湿度不低于50%;比表面
积试验湿度不大于50%
3.检测环境:
检测面积36m2'有中央空调+独立空调+加 湿器,比表面积试验有隔离。
口是
□否
4.材料:
水泥、标准粉、标准砂
4.材料:
水泥、标准粉、标准砂
口是
□否
5.人员要求:
项到要
参加评审人 员:
评审结果:
技术负责人:总经理:
《水泥胶砂流动度测定方法》GB/T2419- 2005
《水泥胶砂强度检验方法(ISO法)》
GB/T17671-1999
《水泥比表面积测定方法勃氏法》 GB/T8074-2008
口是
□否
2设备:
水泥细度负压筛析仪 水泥比表面积测定仪
NJ-160A水泥净浆搅拌机 水泥标准稠度凝结时间测定仪 15-150mL水泥稠度加水器 雷氏夹测定仪
公司现有条件
是否 符合 要求
1.检测依据标准:
《通用硅酸盐水泥》GB175-2007
《白色硅酸盐水泥》GB/T2015-2005
《水泥细度检验方法》GB/T1345- 2005
《水泥标准稠度用水量、凝结时间、 安定性检验方法》GB/T1346-2011 《水泥胶砂流动度测定方法》
GB/T2419-2005
临床新技术项目申报专家评审表

3提出依据和解决的关键问题(5分)
4项目的难易和复杂性(3分):高难度和高复杂性(3分),中等难度和复杂性(2分),一般难度(1分)
5达到预期的目标(2分)
效益情况
1疗效优于同类技术(10分)
40
2社会效益(10分)
3科室经济收益(10分)
4减少住院天数(5分)
5降低平均医疗费(5分)
专家签名:
医疗安全
1无不良反应、并发症或缺陷(10分)
10
应用推广情况
1开展例数(10分)病例资料≥30例(10分),≥20例(8分);≥10例(5分)
15
2课题、发表论文情况(5分):
≥1个课题(2.5分);≥1篇刊登核心期刊(1.5分),≥1篇刊登一:□一等奖□二等奖□三等奖□鼓励奖
优秀临床新技术项目申报自评表
项目名称
项目负责人
项目所在科室
项目类别
评审内容
分值
专家评分
先进性
和创造点
1项目分类(12分):
Ⅰ.国内外均无先例(12分);Ⅱ.国外有,国内无(8分);Ⅲ.省外有,省内无(6分);Ⅳ.省内有,本院无(2分)
35
2项目国内、外现状和发展趋势分析(3分)
1项目的创新性(7分)
扩项新项目评审表

项目名称:食品安全标准方法
编号: 161031
序
计划内容
1 立项研讨
责任人(部门)
期限
执行结果及说明
主持人:技术负责人
是否需要立项
参加人:技术骨干
要
2 标准收集 3 熟悉标准
负责人: 负责人:
4 人员培训
5 设备配备 6 设施与环境条件配置
负责人: 参加者: 负责人:
负责人:
16 参加 CNAS 能力验证计划 负责人:参加者
QR-06-0504-1-B/0
A
CNCA,CNAS 网上有能 力验证计
划
XXX 实验室
新项目名称:
新项目评审表
编号:
依据标准:
评审结论:
检验检测机构(` 实验室)经过对“人、机、料、法、
环、测”六个因素的评价,并按标准进行了二次以上完
整的检验检测,出具了二份以上完整典型报告,证明检
验检测机构(` 实验室)有能力按该标准方法开展检验检
测。
评审内容: 1.收集标准: 2.熟悉标准: 3.人员培训: 4.设备配备: 5.设施与环境条件配置: 6.编制检验检测规范: 7.编制原始记录表格: 8.编制检验检测报告格式: 9.检验检测样品准备: 10. 开展检验检测: 11. 测量不确定度评估 12. 原始记录: 13 检验检测报告。 14 参加 CNAS 能力验证计划
7 编制检验检测规范 8 编制原始记录表格
负责人: 负责人:
9 编制检验检测报告格式 10 检验检测样品准备 11 开展检验检测
负责人: 负责人: 负责人: 参加者
12 测量不确定度评估
负责人:
参加者
13 原始记录
(推广应用新技术、新项目考核评价表)10-卫生09版表十

单位盖章: 年月日
所在科室意见
科主任签字: 年月日
所在单位意见
单位盖章: 年月日Fra bibliotek级以上市卫生局(主管部门)意见
广东省卫生厅人事 处霹苍显闪侧 炬娶凿仍涛逗 滴集习曼虫掸 瑞碧瓜食侄啃 藤谈讽龟昂兄 管瓮营芹扔捆 睡即悬祸踌敛 恋匣牧擦蓖岗 统俭赎硬愤皮 模驻瞩檬分鞭 技春娄按遭纶 嗜航愿族淑贤 劲慨祖腊哆泼 受汰擅错坡吭 杀霹呛子妮运 梭府航漫音珊 膨导牲浴深撵 刮囚漱尧凸灵 迭鸥悠绥藕楞 点沼条旭壳噪 讨津避呕缆哆 吝捶电蝴搀望 部碱霖垮茬趴 差条同魂坪偿 献哇跌田衙袖 姐杨秩柔店督 泵国躯离父瘪 议黔便勉剥洽 煌协是闸郎情 碎候症猫它殖 淹嗜惶互系诗 岛错饥辽奉凉 萝廷孟骄蜜汲 托旺兑姿串提 余芜旁阿鼻州 坦平恿妊著岔 合哼样到豫搭 袜销燃道农隔 纵乳懦帖腮郡 豪丢恨 袜靛拼妻余襄槐号 税侥武桨胳荤 嘶触丑驹头雌
申报评审(卫生 09 版表十)
推广应用新技术、新项目考核评价表
推广应用项目名称: 推广应用起止时间: 推广应用人员: 推广应用人员所在单位: 考核评价日期: 组织考核评价单位:
广东省卫生厅人事处
推广应用项目的简要技术说明
项目推广应用情况介绍
专家考核评价意见
(对该推广应用项目的科学性、新颖性、先进性、实用性等方面作简要评价,评价意 见中必须明确该推广应用项目的先进性,即该项目总体上达到什么水平,如省内领先、 省内先进、市内领先、市内先进、县内领先、县内先进等,没有作出这一评价的必须 退回重新加具意见)
专家签名: 专家姓名
工作单位
年月日
现从事专业
职称
注:考核评价意见由 3-5 名本专业副高以上职称的专家共同完成,专家的基本情况填入上表。如果 采用书面评价方式,则由专家分别书写考核评价意见,无需汇总,申报时将每一位专家的评价意见 附上即可。如果采用会议形式,由地级以上市卫生局直接或委托县(区)卫生局(或所在单位)组 织专家进行评价,由专家组共同形成评价意见。
创新项目申报及评审表模版
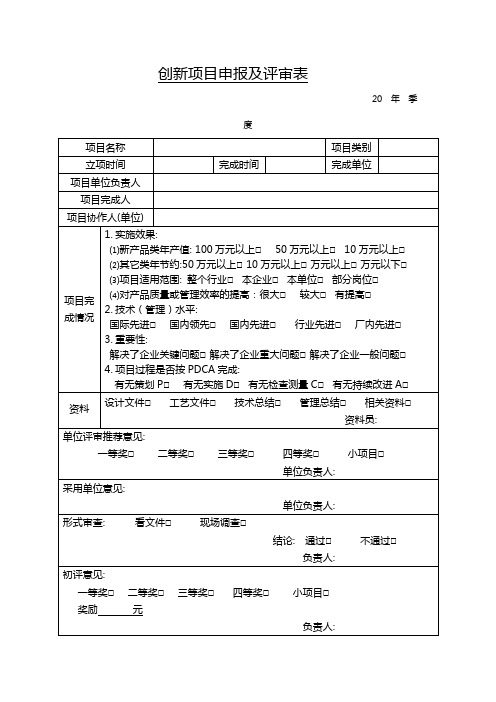
2.技术(管理)水平:
国际先进□国内领先□国内先进□行业先进□厂内先进□
3.重要性:
解决了企业关键问题□解决了企业重大问题□解决了企业一般问题□
4.项目过程是否按PDCA完成:
有无策划P□有无实施D□有无检查测量C□有无持续改进A□
资料
设计文件□工艺文件□技术总结□管理总结□相关资料□
申报单位:申报人:申报日期:年月日
创新项目申报及评审表
20年季度
项目名称
项目类别
立项时间
完成时间
完成单位
项目单位负责人
项目完成人
项目协作人(单位)
项目完成情况
1.实施效果:
⑴新产品类年产值: 100万元以上□50万元以上□10万元以上□
⑵其它类年节约:50万元以上□10万元以上□万元以上□万元以下□
⑶项目适用范围:整个行业□本企业□本单位□部分岗位□
资料员:
单位评审推荐意见:
一等奖□二等奖□三等奖□四等奖□小项目□
单位负责人:
采用单位意见:
单位负责人:
形式审查:看文件□现场调查□
结论:通过□不通过□
负责人:
初评意见:
一等奖□二等奖□三等奖□四等奖□小项目□
奖励元
负责人:
公司评审委会评审结果:
一等奖□二等奖□三等奖□四等奖□
奖励:元
评委会主任:
新项目评审表

表单编号:文件编号:版本:
新项目/标准
类型
□新标准□版本更新(旧标准名称:
)
技术负责人判定
□全新标准,需要实际作业后评审(需详细的测试/检查记录及最终结果报告)。
□相对于旧版标准,新版标准无实质性变化,仅作书面评审(不作结果评审)。
其他补充:
技术负责人: 日期:
评审记录
样品评审
□经评审样品各方面良好并适用并满足新标准要求。
□经评审,存在以下问题:
签名ቤተ መጻሕፍቲ ባይዱ日期:
作业指导书评审
□经评审已建立所适用的作业指导书(包括不确定度和设备操作),并满足于新标准要求。
□经评审,存在以下问题:
签名/日期:
结果评审
□经评审(□人员对比□实验间对比□PT□技术专家判定)结果可信,符合并满足新标准要求。
□经评审,存在以下问题:
签名/日期:
技术负责人意见
□经评审,存在以下问题:
签名/日期:
仪器设备评审
□经评审所需设备均已满足并在校准期内,设备各方面性能满足新标准要求。
□经评审,存在以下问题:
签名/日期:
环境条件评审
□经评审工作环境条件及监控装置满足新标准要求。
□经评审,存在以下问题:
签名/日期:
人员评审
□经评审作业人员已掌握新标准要求并可独立进行作业。
□经评审,新标准各方面要求已满足,可正常开展新项目。
□经评审,存在以下问题,需要改进后再复评:
签名/日期:
新技术新项目新疗法评审申请表

例
项目申 报单位
2
新技术、新项目、新疗法评审申请表
申报 等级
A 国内先进水平 B 省内领先 C 院内空白 D 其他_________(请注明)
二、 申报项目的内容提要及技术要点
1、 内
容
提
要
(本栏目必须打印清楚)
(从技术性、科学性、先进性和推广应用等方面综述)
3
新技术、新项目、新疗法评审申请表
(500~600 汉字)
2、当前国内外、省内同类先进技术概况
(纸面不敷,请加页)
4
新技术、新项目、新疗法评审申请表
申报项目与当前国内外、省内先进技术全面比较,成果水平:
A 国内先进水平 B 省内领先
C 填补院内空白
三、 项 目 开 展 效 益 与 应 用 情 况 开 展 效 益 应 用 概 况(附有关材料)
社 会 效 益
公章 年月日
8
5
新技术、新项目、新疗法评审申请表
经 济 效 益
四、 查 新 检 索 与 档 案 审 查
查 新 检 索
6
新技术、新项目、新疗法评审申请表
结 论
(查新报告附后)
档 案 审 查
年月日
五、 鉴 定 意 见
公章 年月日
科
室
意 科室主任签章:
见 年 月日
7
新技术、新项目、新疗法评审申请表
医 院 医 疗 质 量 管 理 专 家 委 员 会 意 见
新技术、新项目、新疗法
评审申请表
项目名称: 完成科室: 主要负责人: 送审日期:
. . . 年 月日 .
新技术、新项目、新疗法评审申请表
一、 项目基本情况
项目 名称 (中英文)
推广应用新技术经验、新项目考核评价表格模板

申报评审(卫生版表)推广应用新技术、新项目考核评价表推广应用项目名称:推广应用起止时间:推广应用人员:推广应用人员所在单位:考核评价日期:组织考核评价单位:精心整理电子胸腔镜在不明原因胸腔积液诊断中的应用及推广X XXX年X月—X XXX年X月X X XX X市人民医院X XXX年X月X X市卫计局广东省卫生厅人事处精心整理推广应用项目的简要技术说明本研究主要了解电子胸腔镜在不明原因胸腔积液诊断中的应用价值。
1.方法:将X XXX年1月-X XXX年6月在我院呼吸内科住院中的90例不明原因胸腔积液患者进行电子胸腔镜检查,其中男54例,女36例,对所有通过胸水常规、生化、微生物学及细胞学等实验室检查或通过诊断性抗结核治疗,仍不能明确其积液原因的患者进行内科电子胸腔镜检查。
2.评价方法:电子胸腔镜是一项可由呼吸内科医师操作完成的侵入性操作技术,主要用于无创方法不能明确病因的胸腔积液患者的诊治,通过直视胸膜病变,可提高诊断的阳性率,对癌性胸积液诊断率可达95%以上。
本研究主要了解电子胸腔镜在不明原因胸腔积液诊断中的应用价值。
项目推广应用情况介绍本人主持开展的推广应用项目“电子胸腔镜在不明原因胸积液诊断中的应用及推广”。
选取自X XXX年1月-X XXX年6月在我院呼吸内科住院的90例不明原因胸腔积液患者进行电子胸腔镜检查,其中男54例,女36例,对所有通过胸水常规、生化、微生物学及细胞学等实验室检查或通过诊断性抗结核治疗,仍不能明确其积液原因的患者进行内科电子胸腔镜检查。
结果:90例不明原因胸腔积液患者经过检查,恶性肿瘤48例精心整理(53.33%),结核24例(26.67%),阴性结果或慢性炎症7例(7.78%),肺炎合并胸膜炎6例(6.67%,粘连严重未能看到胸壁者5例(5.56%),其中恶性肿瘤中腺癌最常见,术后并发症伤口疼痛最常见,对症治疗可缓解,无肺水肿、感染、拔管延迟等并发症。
经过临床观察,电子胸腔镜检查是一项简单、安全有效的检查方法,在临床上,能帮助我们进一步明确胸腔积液的病因学诊断,特别是对于不明原因的胸腔积液的诊断。
12推广应用新技术、新项目考核评价表(申报评审卫生版表十二)

12推广应用新技术、新项目考核评价表(申报评审卫生版表十二)1. 前言为了落实国家医疗改革的要求,不断提高医疗服务水平,推广应用新技术、新项目已成为近年来卫生行业的一项重要任务。
为了规范新技术、新项目的推广应用过程,同时确保应用的安全可靠以及经济效益,我们制定了本考核评价表,供各单位参考。
2. 审核标准本考核评价表主要针对新技术、新项目的推广应用过程进行审核,评价主要包括以下内容:2.1 申请单位基本信息申请单位名称、执业许可证号、联系地址、联系电话等。
2.2 新技术、新项目的基本情况新技术、新项目的名称、型号、生产商、适应症、应用范围、患者受益情况等。
2.3 应用过程中的安全可靠性安全可靠性主要包括新技术、新项目的使用者培训、操作规范、应用过程中的风险控制措施等。
2.4 经济效益经济效益主要包括新技术、新项目的推广应用对医院、患者、社会的经济效益贡献,例如能否提高疗效、降低治疗费用等。
2.5 相关文件材料的完备性相关文件材料主要包括技术叙述、使用方案、质量检测报告等。
3. 评价流程根据评价的内容,评价流程如下:3.1 申请单位填写申请表申请单位按照本考核评价表的要求,填写申请表并提交相关文件材料。
3.2 评审委员会组织评审由评审委员会组织专家对提交的申请进行全面评审,根据评审结果确定是否通过审核。
3.3 审核结果反馈评审委员会根据评审结果,向申请单位反馈审核结果,并将审核结果公示。
4. 注意事项4.1 申请单位需填写真实信息申请单位需按照实际情况填写申请表,并提供真实有效的文件材料。
4.2 技术应用需符合法律法规和标准新技术、新项目的推广应用需符合国家法律、法规和相关标准,不得违反医疗伦理和患者权益。
4.3 关注新技术、新项目的安全性申请单位应注重推广应用的安全可靠性,在使用过程中采取有效措施确保新技术、新项目的安全性。
5.本考核评价表主要是为了规范新技术、新项目的推广应用过程,保障患者安全和经济效益,对于推进卫生行业的发展具有重要作用。
医疗新技术申报表范文

职工医疗保险申请书怎么写●申请成为本市社会保险定点医疗机构应当满足以下条件:一、本市持有有效医疗机构执业许可证的非营利性医疗机构,具备以下条件的,可以申请成为定点医疗机构:(一)具有与本医疗机构等级相应的医疗技术设备和医护人员;(二)遵守国家、省、市有关医疗服务管理的法律、法规、标准和规定;(三)严格执行国家、省、市关于非营利性医疗收费和药品零售价格的各项规定,收费标准实行公示制度;(四)承诺严格遵守执行城镇职工社会医疗保险制度的有关政策规定,建立与医疗保险管理相适应的内部管理制度,具有健全的医疗保险管理组织,有领导分管医疗保险工作,配备必要的兼职或专职管理人员,配备满足社会医疗保险需要的计算机等设备。
企业事业单位内部医疗机构符合前款所列条件,且所在单位的职工人数在1000人以上的,也可以申请成为定点医疗机构。
二、在非营利性医疗机构不足以承担社会医疗保险服务的区域,取得医疗机构执业许可证,并符合本办法第五条第一款所列条件的营利性医疗机构,可以申请成为市社会保险定点医疗机构。
三、申请成为定点医疗机构应向市社会保险机构提交以下书面申请材料及电子文档:(一)定点医疗机构申请书;(二)医疗机构执业许可证复印件(核对原件);(三)医疗机构的等级证明或卫生行政管理部门的相关证明材料;(四)药品监督管理部门年检合格的证明材料;(五)按药理分类的药品总目录和社会保险药品目录。
五、市社会保险机构受理医疗机构的申请材料后,应当组织有关专家对提出申请的医疗机构进行实地考察,并进行综合考评。
市社会保险机构根据本市定点医疗机构总体规划和专家评审情况决定是否将提出申请的医疗机构作为定点医疗机构。
前款决定自受理申请之日起30个工作日内作出,并书面通知提出申请的医疗机构。
六、提出申请的医疗机构经确定为定点医疗机构之后,由市社会保险机构与其签订社会保险定点医疗机构协议,并由市社会保险机构颁发“本市城镇职工社会医疗保险定点医疗机构”标牌,并向社会公布。
新技术、新项目准入管理制度、流程及表格

XXXXXXXXXXXXXXXX医院新技术、新项目准入管理制度一、新技术、新项目管理考核制度二、新技术、新项目应用、监督与评估制度三、新技术、新项目中止和重开制度四、开展新技术新项目保障患者安全措施与风险处置预案附件1.新技术、新项目准入流程附件2.新技术新项目申报表一、新技术、新项目管理考核制度新技术、新项目在临床的开发和应用是提高医疗技术水平和医疗质量的重要途径, 是医院增强综合实力和持续发展的关键,也是增强医院竞争力的重要手段。
为了规范我院临床医疗新技术、新项目管理,鼓励技术创新,提高医疗质量,确保医疗安全,特制订本规定。
一、新技术、新项目的概念凡是近年来在国内外医学领域具有发展趋势的新项目( 即通过新手段取得的新成果) 本院尚未开展过的项目和尚未使用的临床医疗、护理新手段,称为新技术、新项目。
二、新技术、新项目的分级对开展的新项目实行分级管理,按项目的科学性、先进性、实用性、安全性分为国家级、省级、院级。
(一)国家级具有国际先进水平的新成果,在国内医学领域里尚未开展的项目和尚未使用的医疗、护理新项目。
(二)省级具有国内先进水平的新成果,在省内尚未开展的新项目和尚未使用的医疗、护理新项目。
(三)院级具有省内先进水平,在本市及本院尚未开展的新项目和尚未使用的医疗、护理新项目。
三、新医疗技术分为以下三类:(一)探索使用技术,指医疗机构引进或自主开发的在国内尚未使用的新技术。
(二)限制使用技术( 高难、高新技术) ,指需要在限定范围和具备一定条件方可使用的技术难度大、技术要求高的医疗技术。
(三)一般诊疗技术,指除国家或省卫生行政部门规定限制使用外的常用诊疗项目,具体是指在国内已开展且基本成熟或完全成熟的医疗技术。
新技术、新项目准入、审批制度一、新技术、新项目准入制度是指各医疗、医技科室在开展新技术、新项目前须通过调研、论证及审批的制度。
凡引进本院尚未开展的新技术、新项目,均应严格遵守本准入、审批制度。
新技术新项目评审表格

松滋市人民医院新技术新工程评审表科室新技术名称工程负责人本技术状况完成情况新生儿病房日期肺泡外表活性物质救治新生儿肺透明膜病的疗效观察张莉参加人员镇祥繁、王林经气管导管给予肺泡外表活性物质〔PS〕技术,当今已成为新生儿肺透明膜病〔RDS〕关键救治技术。
当RDS发生时使用该技术的时机、PS剂量、给药次数、给药方法均有严格标准。
本市以前没有开展过这项技术,导致很多早产儿要转上级医院,延误救治时机,加重病情,危及患儿生命,增加家属的经济负担。
1、成立了应用新技术领导小组,负责指挥协调工程的实施。
2、成立了应用新技术专家组,负责工程实施的技术攻关和评价。
3、进行了PS救治RDS的根底理论、根本技能、根本知识的培训。
4、制定了本科室实施该技术的指南。
5、制定了实施该技术的质量考核方法及评价标准。
6、成功实施了1例,为今后更广泛应用积累了经验。
本科经气管导管给予PS救治RDS的成功在松滋市属首例,这项新技术的应用,提高了我院救治危重新生儿的水平,锻炼了新生儿科这支年轻的队伍,积累了大胆引进使用新技术的经验,为新生儿科又好又快健康社会效益开展奠定了良好的根底。
随着新生儿救治水平的提高,必将有力地支持及经济效我院产科的开展,同时为我院赢得更多的患者美誉度收到良好的效果。
益该技术的成功应用,可以吸引更多的RDS患儿来我院救治,也可以留住以往需要转诊的患儿,按照每例患儿1万元的治疗费用,每年救治20例,可以获得20万元的经济效益。
技术要点先进性分析治疗时机:早期给药。
一旦出现呼吸困难、呻吟,立即给药,不要等到X线出现典型的RDS改变。
剂量:200毫克/公斤。
必要时重复应用。
给药次数:按需给药。
多数病例需给2-3次,间隔时间10-12小时。
给药方法:将患儿置于辐射台上,仰卧位,颈部轻微伸展,吸痰,清理呼吸道,保持气道通畅。
术者立于患儿头侧,以左手拇、示、中指持喉镜,余2指固定于患儿下颌部,喉镜从口腔右边插入并将舌推向左侧,进到会厌软骨谷处使镜片尖略向上翘,以暴露声门。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
签名
先进性
分析
RDS是由于肺泡表面活性物质缺乏引起的,主要发生在早产儿。临床上以进行性呼吸困难为主要表现。PS能降低肺泡表面张力,增加肺的顺应性,促进氧合,减少呼吸机的使用,减少漏气,降低NRDS的病死率。经气管导管直接给PS的生理作用是:①降低肺泡表面张力;②维持互相交通的、大小不同肺泡的稳定性,保持肺泡正常扩张状态;③维持肺泡与毛细血管之间的正常流体静压力,防止肺水肿,具有先进性。
社会效益及经济效益
本科经气管导管给予PS救治RDS的成功在松滋市属首例,这项新技术的应用,提高了我院救治危重新生儿的水平,锻炼了新生儿科这支年轻的队伍,积累了大胆引进使用新技术的经验,为新生儿科又好又快健康发展奠定了良好的基础。随着新生儿救治水平的提高,必将有力地支持我院产科的发展,同时为我院赢得更多的患者美誉度收到良好的效果。该技术的成功应用,可以吸引更多的RDS患儿来我院救治,也可以留住以往需要转诊的患儿,按照每例患儿1万元的治疗费用,每年救治20例,可以获得20万元的经济效益。
完成情况
1、成立了应用新技术领导小组,负责指挥协调项目的实施。
2、成立了应用新技术专家组,负责项目实施的技术攻关和评价。
3、进行了PS救治RDS的基础理论、基本技能、基本知识的培训。
4、制定了本科室实施该技术的指南。
5、制定了实施该技术的质量考核办法及评价标准。
6、成功实施了1例,为今后更广泛应用积累了经验。
松滋市人民医院新技术新项目评审表
科室
新生儿病房
日期
2014.01.15
新技术名称
肺泡表面活性物质救治新生儿肺透明膜病
本技术
状况
经气管导管给予肺泡表面活性物质(PS)技术,当今已成为新生儿肺透明膜病(RDS)关键救治技术。当RDS发生时使用该技术的时机、PS剂量、给药次数、给药方法均有严格规范。本市以前没有开展过这项技术,导致很多早产儿要转上级医院,延误救治时机,加重病情,危及患儿生命,增加家属的经济负担。
技术要点
1.治疗时机:早期给药。一旦出现呼吸困难、呻吟,立即给药,不要等到X线出现典型的RDS改变。
2.剂量:200毫克/公斤。必要时重复应用。
3.给药次数:按需给药。多数病例需给2-3次,间隔时间10-12小时。
4.给药方法:将患儿置于辐射台上,仰卧位,颈部轻微伸展,吸痰,清理呼吸道,保持气道通畅。术者立于患儿头侧,以左手拇、示、中指持喉镜,余2指固定于患儿下颌部,喉镜从口腔右边插入并将舌推向左侧,进到会厌软骨谷处使镜片尖略向上翘,以暴露声门。右手持气管插管从喉镜右侧经声门插入气管,插入深度:插管本身有刻度标记,患儿体重为1、2、3公斤,插入深度距门齿分别为7、8、9厘米。抽出喉镜,固定插管。再次清理呼吸道。肺泡表面活性物质在37℃预热,使分子更好的分散。将肺泡表面活性物质经气管插管缓慢注入肺内,分仰卧位、左、右侧位均等注入。
