氢原子光谱 课件
物理选修3-518.3《氢原子光谱》ppt课件

续的
D.该公式包含了氢原子的所有光谱线 解析:巴耳末公式是分析氢原子的谱线得到的一个公式,
它只反映氢原子谱线的一个线系,故 A 对 D 错;公式中的
n 只能取不小于 3 的正整数,B 错 C 对。 答案:AC
3.氢原子光谱的巴耳末系中波长最长的光波的光子能量为 ε1,其
次为 ε2,则εε12为 A.2207
小灯泡(灯座)2个,电压表,电源,导线,电键
用电压表测量串联电路的电压
[步骤] 设计电路图并连接实 物图,使两个小灯泡 连接成串联电路。
用电压表测量串联电路的电压
[步骤]
按电路图连接实物图,
U1
使电压表测量小灯泡
L1两端的电压U1
L1
L2
L1
L2
V
S
用电压表测量串联电路的电压
[步骤]
U2
按电路图连接实物图, 使电压表测量小灯泡L2 两端的电压U2
和大人一起读
想一想,说一说:唐僧师徒一行四 人都有谁?各有什么特点?
想想练练
如下图所示,电源由三节新干电池串联组成, 开关闭合后,已知 的示V1 数为1.5V,则 的 示数V为 4.5V, 的示V2 数为 3V。
V
L1
V2
V1
L2
不能用 于光谱 分析
用分光镜观察时,见到 连续光谱背景上出现一 些暗线(与特征谱线相对 应)
可用于 光谱分 析
1.关于光谱,下列说法正确的是 A.一切光源发出的光谱都是连续谱 B.一切光源发出的光谱都是线状谱
()
C. 稀薄气体发出的光谱是线状谱
D.做光谱分析时,利用连续谱和线状谱都可以鉴别物质和
确定物质的组成成分 解析:物体发光的发射光谱分为连续谱和线状谱,A、B 错;
18.3 氢原子光谱(45张PPT)

分布。
C 在研究太阳光谱时发现太阳光谱中有许多暗线, 这说明了太阳内部缺少对应的元素。
D 在研究太阳光谱时发现太阳光谱中有许多暗线, 这些暗线与某些元素的特征谱线相对应,这说明 了太阳大气层内存在对应的元素。
随堂练习
1. 对原子光谱,下列说法正确 的是(ACD).
A.原子光谱是不连续的
B.由于原子都是由原子核 和电子组成的,所以各种原 子的原子光谱是相同的
X射线照射激发荧光, 通过分析荧光判断越王 勾践宝剑的成分.
(5)意义:原子光谱的不连续性反映出原子结构的不 连续性,所以光谱分析也可以用于探索原子的结构。
------光谱分析还为深入原子世界打开了道路。近代原 子物理学正式从原子光谱的研究中开始的。
研究原子结构规律有两条途径:
1.利用高能粒子轰击原子—轰出未知粒子来 研究(高能物理);
σ其它谱系
三、经典理论的困难
三、经典理论的困难
卢瑟福的原子核式模型正确地指出了原子核的存在,很好地解释了α粒子散射实验。
卢瑟福原子核式模型无法解释原子光谱的分立特征
原子核式结构模型与经典电磁理论的矛盾
核外电子绕核运动
辐射电磁波
电子轨道半径连续变小
原子不稳定 辐射电磁波频率连续变化 事实上:原子是稳定的 原子光谱是线状谱,频率不变
《波尔的原子模型》预习问题:
【问题1】什么是轨道量子化?什么是能量量子化? 【问题2】什么是能级?什么是基态?什么是激发态? 【问题3】什么是跃迁?什么是频率条件? 【问题4】画出氢原子n=1、2、3、4的能级图。
谱是线状谱
太阳光谱是吸收光谱,不连续 稀薄的氢气和钠蒸汽产生 的是原子光谱为线状谱
白光通过钠蒸汽产生的光谱是
氢原子光谱优秀课件
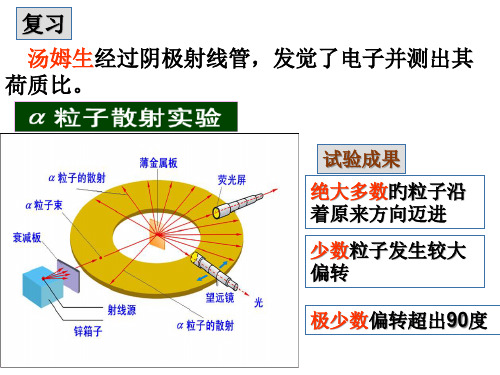
令
T
(m)
R m2
,
T
(n)
R n2
1 T (m) T (n)
T (m),T (n) 称为光谱项。
三、经典理论旳困难
卢瑟福原子核式模型正确地指出了原子核旳存 在,很好地解释了α粒子散射试验。但是。经 典物理学既无法解释原子旳稳定性,又无法解 释原子光谱旳分立特征。
按经典物理学电子绕核旋转,作加速运动,电子 将不断向四面辐射电磁波,它旳能量不断减小, 从而将逐渐接近原子核,最终落入原子核中。但 实际上原子是个稳定旳系统。
还 有 三
布喇开系
1
R
1 42
1 n2
n 5,6,7,
个 线 系
普丰特系
1
R
1 52
1 n2
n 6,7,8,
氢原子光谱不是不相关旳,而是有内在联络旳。体现在 其波数可用一普遍公式来表达:1 NhomakorabeaR
1
m
2
1 n2
其 中
m 1,2,3
n m 1, m 2, m 3,
相应一种m构成一种谱线系 每一谱线旳波数都等于两项旳差数
二、光谱分类:
1.发射光谱:物体发光直接产生旳光谱叫做发射光谱。
发射光谱可分为两类:连续谱和线状谱。
2.吸收光谱:
特点:在连续谱上 缺失了某些成份旳光
此光谱图有何特点?
成因:高温物体发出旳白光(其中包括连续分布旳一切 波长旳光)经过物质时,某些波长旳光被物质吸收后产 生旳光谱,叫做吸收光谱。
3.发射光谱与吸收光谱旳相应关系:
轨道及转动频率不断变化,辐射电磁波频率 也是连续旳, 原子光谱应是连续旳光谱。而 实际上看到旳是分立旳线状谱。
这些矛盾阐明尽管经典物理学理论能够很好地 应用宏观物休,但它不能解释原子世界旳现象, 引入新观念是必要旳。
氢原子光谱课件

氢原子光谱课件引言氢原子光谱是量子力学和原子物理学领域的基础内容,对于理解原子结构、光谱现象以及化学键的形成具有重要意义。
本课件旨在介绍氢原子光谱的基本原理、实验观测和理论解释,帮助读者深入理解氢原子的能级结构和光谱特性。
一、氢原子的基本结构1.1电子轨道和量子数氢原子由一个质子和一个电子组成,电子围绕质子旋转。
根据量子力学的原理,电子在氢原子中只能存在于特定的轨道上,这些轨道被称为能级。
每个能级由主量子数n来描述,n的取值为正整数。
1.2能级和能级跃迁氢原子的能级可以用公式E_n=-13.6eV/n^2来表示,其中E_n 是第n能级的能量,单位为电子伏特(eV)。
当电子从一个能级跃迁到另一个能级时,会吸收或发射一定频率的光子,这个频率与能级之间的能量差有关。
二、氢原子光谱的实验观测2.1光谱仪和光谱图氢原子光谱可以通过光谱仪进行观测。
光谱仪将入射光分解成不同频率的光谱线,并将这些光谱线投射到感光材料上,形成光谱图。
通过观察光谱图,可以得知氢原子的能级结构和光谱特性。
2.2巴尔末公式实验观测到的氢原子光谱线可以通过巴尔末公式来描述,公式为1/λ=R_H(1/n1^21/n2^2),其中λ是光谱线的波长,R_H是里德伯常数,n1和n2是两个能级的主量子数。
巴尔末公式可以准确地预测氢原子光谱线的位置。
三、氢原子光谱的理论解释3.1玻尔模型1913年,尼尔斯·玻尔提出了氢原子的量子理论模型,即玻尔模型。
该模型假设电子在氢原子中只能存在于特定的轨道上,每个轨道对应一个能级。
当电子从一个能级跃迁到另一个能级时,会吸收或发射一定频率的光子。
3.2量子力学解释1925年,海森堡、薛定谔和狄拉克等人发展了量子力学理论,为氢原子光谱提供了更为精确的解释。
量子力学认为,电子在氢原子中的状态可以用波函数来描述,波函数的平方表示电子在空间中的概率分布。
通过解薛定谔方程,可以得到氢原子的能级和波函数。
四、结论氢原子光谱是量子力学和原子物理学的基础内容,对于理解原子结构、光谱现象以及化学键的形成具有重要意义。
氢原子光谱和玻尔的原子模型课件-高二物理人教版(2019)选择性必修第三册

3. n=1定态(基态),原子能 量最小,电子轨道半径最小;
4.能级为n 的原子,电子
轨道半径为 rn n2r1
能级越高,电子轨道半径越大
1 2
3
5.原子从高能级向低能级跃迁时_辐__射_光子,
轨道半径_减__小_,库仑力_做__正__功__,电势能_减__小_, 电子动能_增__加___,原子能量_减__小_。
氢原子光谱的其他线系
紫
外 线
莱曼线系
区
1
R
1
12
1 n2
n 2,3,4,
红
外 线
帕邢系
区
1
R
1
32
1 n2
n 4,5,6,
三、经典理论的困难
核外电子绕核运动
辐射电磁波
电子轨道半径连续变小
原子不稳定
原子是稳定的
辐射电磁波频率连续变化
原子光谱是线状谱 —— 分立
经 电子绕核运动将不断 典 向外辐射电磁波,电 理 子损失了能量,其轨 论 道半径不断缩小,最 认 终落在原子核上,而使 为 原子变得不稳定。
实物粒子:电子、质子、中子等 原子能吸收实物粒子的部分动能。
例1 对于基态氢原子,下列说法中正确的是 A.它能吸收10.2 eV的光子 B.它能吸收11 eV的光子 C.它能吸收14 eV的光子 D.它能吸收具有11 eV动能的电子的部分动能
答案:ACD
2.如图所示为氢原子的能级图,若用能量为10.5 eV 的光子去照射一群处于基态的氢原子,则氢原子
答案:D
六、玻尔模型的局限性
玻尔理论成功的解释并预言了氢原子辐射 的电磁波的问题,但是也有它的局限性.
在解决核外电子的运动时 成功引入了量子化的观念
氢原子光谱PPT教学课件

代入: PV PoVo M PoVmol
T
To
M mol To
理想气体物态方程: PV M RT M mol
阿伏伽德罗常数: N A 6.022 1023 mol 1
玻耳兹曼常数: k R 1.38 1023 (J K 1) NA
设:分子质量为 m,气体分子数为N,分子数密度 n。
单个分子速率不可预知,大量分子的速率分布是遵 循统计规律,是确定的,这个规律也叫麦克斯韦速 率分布律。
氢原子光谱
引言
每种原子、分子都有其特征光谱。因此分析其特征 光谱,对研究不同原子、分子及其结构有着重大的意义。 光谱学已成为光学的一个重要分支,并被广泛用于科研 和生产中。
氢原子是最简单的原子,其光谱线在按波长(或波 数)大小的排列次序上显示出简单的规律性。研究原子 结构,很自然氢原子首先被关注。
热现象
热学的研究方法:
1.宏观法. 最基本的实验规律逻辑推理(运用数学) ------称为热力学。
优点:可靠、普遍。 缺点:未揭示微观本质。 2.微观法.
物质的微观结构 + 统计方法 ------称为统计力学 其初级理论称为气体分子运动论(气体动理论) 优点:揭示了热现象的微观本质。 缺点:可靠性、普遍性差。
宏观法与微观法相辅相成。
气体动理论 §1 分子运动的基本概念
一.热力学系统 热力学研究的对象----热力学系统. 热力学系统以外的物体称为外界。 孤立系统:系统和外界完全隔绝的系统
例:若汽缸内气体为系统,其它为外界
二.系统状态的描述 微观量:分子的质量、速度、动量、能量等。
在宏观上不能直接进行测量和观察。 宏观量: 温度、压强、体积等。
2
高中物理课件第2章 第4节 氢原子光谱与能级结构

[后思考]
被测电阻值越大,流过电流表表头的电流越小,电流的大小与被测电阻的阻
值成反比,这种说法对吗?为什么?
【提示】
电流I=
E Rx+R+Rg+r
,Rx越大,电流越小,但二者不是反比关
系.
[合作探讨]
甲
乙
丙
图2-8-2
如图2-8-2所示,甲、乙、丙分别为欧姆表红黑表笔短接、红黑表笔断开、被
测电阻为Rx所对应的电路图.
[再判断] 1.氢原子光谱是不连续的,是由若干频率的光组成的.( √ ) 2.由于原子都是由原子核和核外电子组成的,所以各种原子的原子光谱是相 同的.( × ) 3.由于不同元素的原子结构不同,所以不同元素的原子光谱也不相同.(√ )
[后思考] 氢原子光谱有什么特征,不同区域的特征光谱满足的规律是否相同? 【提示】 氢原子光谱是分立的线状谱.它在可见光区的谱线满足巴耳末公 式,在红外和紫外光区的其他谱线也都满足与巴耳末公式类似的关系式.
[后思考] 玻尔理论的成功和局限是什么?
【提示】 成功之处在于引入了量子化的观念,局限之处在于保留了经典粒 子的观念,把电子的运动看做是经典力作用下的轨道运动.
[核心点击] 1.成功方面 (1)运用经典理论和量子化观念确定了氢原子的各个定态的能量并由此画出能 级图. (2)处于激发态的氢原子向低能级跃迁辐射出光子,辐射光子的能量与实际符 合的很好,由于能级是分立的,辐射光子的波长也是不连续的. (3)不仅成功地解释了氢光谱的巴尔末系,计算出了里德伯常数,而且,玻尔 理论还预言了当时尚未发现的氢原子的其他光谱线系,这些线系后来相继被发 现,也都跟玻尔理论的预言相符.
[先填空]
1.理论推导
按照玻尔原子理论,氢原子的电子从能量较高的能级跃迁到n=2的能级上
人教版高中物理选修3-5课件第十八章第3节氢原子光谱

灿若寒星整理制作
第第 十3 八节 章
新知预 习·巧设计
名师课 堂·一点通
创新演 练·大冲关
要点一 要点二
随堂检测 归纳小结 课下作业 综合提升
1.知道光谱、线状谱、连续谱、吸收 光谱、光谱分析等概念。 2.知道氢原子光谱的实验规律。 3.知道经典物理的困难在于无法解释 原子的稳定性和光谱分立特征。
特征谱
的不,同说明不同原子的发光频率是的,光不谱一中样的亮
线
线称为原子的
特征谱线
光谱分析:利用原子的来特鉴征别谱物线质和确定物质的
应用 优点:高,组样成本成中分一种元素的含量达到10-就可 被检测到灵敏度
[关键一点] 连续谱含有可见光的一切波长,不具有原子
的特征谱线,不能用来进行光谱分析。
2.氢原子光谱的实验规律 (1)许多情况下光是由原子内部电子的运动产生的,因此光 谱研究是探索 原子结构 的重要途径。 (2)巴耳末公式:1λ= R(212-n12) (n=3,4,5…),式中 R 叫 里德伯常量,其值为 R=1.10×107 m-1。 (3)巴耳末公式的意义:以简洁的形式反映了氢原子的线状 光谱,即辐射波长的 分立 特征。
成,由此知A、C、D说法正确。故选B。
答案:B
3.关于巴耳末公式1λ=R(212-n12)的理解,正确的是(
)
A.此公式是巴耳末在研究氢原子光谱特征时发现的
B.公式中 n 可取任意值,故氢原子光谱是连续谱
C.公式中 n 只能取大于或等于 3 的整数值,故氢原子光
谱是线状谱
D.公式不但适用于氢原子光谱的分析,也适用于其他原
5.计算巴耳末系中,当 n=5 时氢原子光谱线的波长。 解析:当 n=5 时,由巴耳末公式有1λ=R(212-512),则 λ= 0.211R=0.21×11.10×107 m=4.33×10-7 m。 答案:4.33×10-7 m
物理新课标教科版 氢原子光谱 课件课件PPT

16、明确的目标和执著的精神几乎可以让你实现任何理想,达成任何目标! 28. 一切能激发生机的思想都是美好的。敌人只有一个,那就是自私,它能使生命的泉水变得浑浊而枯竭,它能使心灵的天空变得狭窄而阴暗 ,它能使理想的星辰变得昏暗而模糊。努力激发你心中的光明和力量,激发那无私的爱和奉献的喜悦。
26、我允许你走进我的世界,但不允许在我的世界走来走去。 31、出门走好路,出口说好话,出手做好事。 21. 辛苦一年,收益一生。 25. 哪天你的处境非常困难,请你在心中默想:一切都会过去的,明天会好起来的。 15. 人格的完善是本,财富的确立是末。 11. 不要问别人为你做了什么,而要问你为别人做了什么。 5、知识就是力量。 33. 没有天生的信心,只有不断培养的信心。 5. 再长的路,一步步也能走完,再短的路,不迈开双脚也无法到达。 31. 学会在交流时,看着对方的眼睛,真诚而用心地注视。 9、知道自己要干什么,夜深人静,问问自己,将来的打算,并朝着那个方向去实现。而不是无所事事和做一些无谓的事。 30. 学会赞美,赞美可以拉近你和对方的距离。 15、人生难得几回搏,此时不搏更待何时? 2、希望是厄运的忠实的姐妹。
60. 再长的路,一步步也能走完,再短的路,不迈开双脚也无法到达。 25. 哪天你的处境非常困难,请你在心中默想:一切都会过去的,明天会好起来的。 3、有了成绩要马上忘掉,这样才不会自寻烦恼;有了错误要时刻记住,这样才不会重蹈覆辙;有了机遇要马上抓住,这样才不会失去机会; 有了困难要寻找对策,这样才能迎刃而解。
氢原子光谱和波尔的原子模型ppt课件
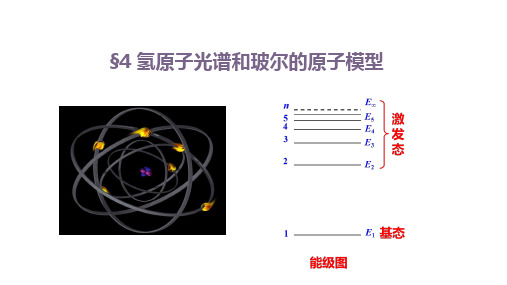
Na原子的发射光谱(明线)
H原子的吸收光谱(暗线)
H原子的发射光谱(明线)
吸收光谱和线状谱(发射光谱)的关系:
各种原子的吸收光谱中的每一条暗线都跟该种原子的发射光谱(线状光谱)中的
一条明线相对应。
3.光谱分析
既然每种原子都有自己的特征谱线,我们就可以利用它来鉴别物质和确定物质的组
成成分。这种方法称为光谱分析。
4.由于不同的原子具有不同的结构,能级各不
相同,因此辐射(或吸收)的光子频率也不相
同。这就是不同元素的原子具有不同的特征谱
线的原因。
六、玻尔理论的局限性
1.玻尔理论的不足之处在于保留了
经典粒子的观念,仍然把电子的运
动看作经典力学描述下的轨道运动。
2.玻尔理论成功地解释了氢原子光
谱的实验规律。但对于稍微复杂一
1
E1
激
发
态
h E n E m
基态
原子从低能级向高能级跃迁(电子从低轨道向高轨道跃迁): 吸收光子,原子能量增大
电子从低轨道向高轨道跃迁,电子克服库仑引力做
功,电势能增大,原子的能量增加,要吸收能量。
吸收光子能量:
h E n E m
原子从高能级向低能级跃迁(电子从高轨道向低轨道跃迁): 辐射光子,原子能量减小
优点:灵敏度高
样本中一种元素的含量达到10-13kg时就可
以被检测到。
利用白炽灯的光谱,能否检测出灯丝的成分?
不能,白炽灯的光谱是连续谱,不是原子
的特征谱线,因而无法检测出灯丝的成分
原子的特征光谱
二、氢原子光谱(发射光谱)的实验规律
氢原子是最简单的原子,其光谱也最简单。
n=6
n=5
人教版高中物理选择性必修三 第4章第3节氢原子光谱和玻尔的原子模型 课件

四、玻尔原子理论的基本假设
假说3:频率条件(跃迁
假说)
吸
收
基光
子
态
针对原子光谱是线状
谱提出
电子克服库仑力做功增大电
势能,
激
n
E∞
5
4
3
E
5E
4
E
原子的能量增加
跃
发
辐
电子所受库仑力做正功减小电
迁
射
势能,
原子的能量减少
光
子
3
2
E
2
态
= − (
> )
激
发
态
1
E
1
基
态
新知讲解
五、玻尔理论对氢光谱的解释
光谱研究是探索原子结构的一条重要途径。
氢气光
谱管
分光
镜
高压电
源
新知讲解
二、氢原子光谱的实验规律
许多情况下光是由原子内部电子的运动产生的,因此
光谱研究是探索原子结构的一条重要途径。
新知讲解
二、氢原子光谱的实验规律
新知讲解
二、氢原子光谱的实验规律
氢原子是最简单的原子,其光谱也最简单。
7 m−1
4
N=
5
N=
6
帕邢系(红
外线)
布喇开系
逢德
系
成功解释了
氢光谱的所
有谱线
新知讲解
五、玻尔理论对氢光谱的解释
新知讲解
五、玻尔理论对氢光谱的解释 Nhomakorabea新知讲解
五、玻尔理论对氢光谱的解释
新知讲解
五、玻尔理论对氢光谱的解释
1.从高能级向低能级跃迁
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
氢原子光谱
1
11
λ = R( 2 2 - n 2 )
巴尔末公式R=1.10.107m-1
n ∈ (3 .4 .5 ......)
里德伯常量
n有两层含义:
一,n取一个值,可求出氢光谱中一条谱线的波长,说明每一个n值分别对应一条谱线 二,n只能取正整数值3,4,5……,不能取连续值,说明了原子光谱波长的分立特性。
光谱中国展将世界先进的测试测量产品、先进 的检测手段和理念与国内实际检测需求融合, 并能得以完美体现;希望能尽情展现中国测试 测量与检测企业的风采,搭建测试测量行业 “产、学、研、用”的互动交流平台,同时 “十三五”规划中重点发展的环境监测、冶金、 化工、钢铁、矿山、水泥、电力,水利、石油 化工、石化煤气层监测、城市管网建设等众多 领域都将为其应用带来无限的拓展空间。
原子中电子的轨道是 不是可以用它发出的 光来分析呢
早在17世纪,牛顿就发现了 日光通过三棱镜后的色散现 象,并把试验中得到的彩色 光带叫做光谱。光谱是电磁 辐射(不论是在可见光区域 还是在不可见光区域)的波 长(频率)成分和强度分布 的记录。光栅也可以得到一 样的光谱。
一、发射光谱 物体发光直接产生的光谱
其他谱系:
卢瑟福模型的困难:
卢瑟福原子核式模型无法解释氢原子光谱的规律
原子核式结构模型与经典电磁理论的矛盾
核外电子绕核运动 辐射电磁波
电子轨道半径连续变小
原子不稳定 事实上 原子是稳定的
辐射电磁波频率连续变化 原子光谱是线状谱
课堂小结:
一、光谱
发射光谱 连续光谱和线状光谱(原子光谱) 吸收光谱 用分光镜观察时,见到连续光谱背景上出现
定义:连续光谱中某些波长的光被物质吸收后产生的 吸 光谱 收 光 产生条件:炽热的白光通过温度较白光低的气体后, 谱 再色散形成的
光谱形式:用分光镜观察时,见到连续光谱背景上 出现一些暗线(与特征谱线相对应)
用途:光谱分析
由于每种原子都有自己的特征谱线,因此可以根据光谱来签别物质和确定化学组成, 这种方法叫做光谱分析。原子光谱的不连续性反映出原子结构的不连续性,所以光谱 分析可以探索原子的内部结构。
各种光谱的特点及成因:
{ 发
射
定义:由发光体直接产生的光谱 产生条件:炽热的固体、液体和高压气体发
光 连续光谱 光形成的
谱
光谱的形式:连续分布,一切波长的光都有
光 谱
{ 线状光谱 产生条件:稀薄气体发光形成的光谱
(原子光谱) 光谱形式:一些不连续的明线组成,不同 元素的明线光谱不同(又叫特征光谱)
第十八章 原子结构
第三节 氢原子光谱
学情回顾:
α 粒子的散射的实验使我们知道原子具有核式
结构,但是电子在核的周围怎样运动?它的能量 怎样变化?这些还要通过其他事实才能认识。
把一根蘸了食盐溶液的金属丝放到 酒精灯的火焰上,火焰的颜色会被 黄色主导.食盐的主要成分是氯化钠 。放铜丝的时候,火焰会变成绿色。 说明每种元素的光都是不一样。
研 究 太 阳 高 层 大 气 所 含 元 素
其基本原理:
是将人体置于特殊的磁场中,用无线 电射频脉冲激发人体内氢原子核,在 外磁场作用下自旋能级发生分裂,共 振吸收某一定频率的射频辐射的物理 过程。核磁共振波谱学是光谱学的一 个分支,其共振频率在射频波段,相 应的跃迁是核自旋在能级上的跃迁。
光谱中国主题展
吸收光谱
光谱中产生的一组暗线,每条暗线的波 长都跟那种气体原子的特征谱线相对应。
二、吸收光谱
高温物体发出的白光(其中包含连续分布的一切波长的 光)通过物质时,某些波长的光被物质吸收后产生的光 谱,叫做吸收光谱。各原子的吸收光谱中每一条暗线都 跟该种原子的发射光谱中的一条明线相对应。这表明, 低温气体原子吸收的光,恰好就是这种原子在高温时发 出的光。因此吸收光谱中的暗谱线,也就是原子的特征 谱线。太阳的光谱是吸收光谱
(1)连续光谱
连续分布的包含有从红光到紫光各种色光的光带叫做连续光谱。
例如:炽热的固体,液体和高压气体的发射光谱是连续光谱。
a 一束白光通过三棱镜折射后,可以分解成赤橙黄绿蓝靛紫等不同 波长的光谱,称之为连续光谱。 b 自然界中,雨后天空的彩虹是连续光谱。 c 炽热的固体,液体和高压气体的发射光谱是连续光谱。
暗线(与特征谱线相对应)
二、氢原子光谱的实验规律
在可见光区域的谱线的波长可以用巴尔末公式表示
在红外和紫外光区的其他谱线都满足与巴尔末公式类似的关系式
三、经典理论的困难
经典物理学无法解释原子的稳定性,也关氢原子光谱的说法中正确的是: A 氢原子的发射光谱是连续谱。 B 氢原子的光谱说明氢原子只能发出特定频率的光。 C 氢原子的光谱说明氢原子能级是分立的。 D 氢原子光谱线的频率与氢原子能级的能量差无关。
白炽灯丝发出的光,烛焰,炽热的钢水发出的光都形成连续光谱。
一、发射光谱 物体发光直接产生的光谱
(2)线状谱(明线光谱)
只含不连续的亮线的光谱叫做线状谱。线 状谱中的亮线叫做谱线,各条谱线对应不 同波长的光。
稀薄气体或金属的蒸汽的发射光谱是明线光谱。
明线光谱是由游离状态的原子发射的,也 叫原子光谱
各种原子的发射光谱都是线状谱,说明原子只能发出几种特定频率 的光。不同原子的亮线位置不同,说明不同原子的发光频率是不一 样的,因此这些亮线称为原子的特征谱线。
二、氢原子光谱的实验规律
许多情况下光是由原子内部电子的运动产生的,因此光谱研究是探索原子结构的一条 重要途径。 氢原子是宇宙中最基本,最简单的原子。
什么是气体放电管?
玻璃管中的稀薄的气体分 子在强电场的作用下电离 成为自由移动的正负电荷 于是气体变导体,导电时 会发光。
二、氢原子光谱的实验规律
在真空管中充入少量氢气,通过高压放电,氢气可以产生可见光、紫外光和红外光,这些 光经过三棱镜分成一系列按波长大小排列的线状光谱。从氢气放电管可以获得氢原子光谱 原子光谱的不连续性反映出原子结构的不连续性,所以光谱分析也可以用于探索原子的结 构。
(B C)
二、在实际生活中,我们可以通过光谱分析来签 别物质和分析物质的组成成分。例如某样本中一 种元素的含量达到10-10g时就可以被检测到。那么 我们是通过分析下列那种谱线来签别物质和分析 物质的组成部分的?
