丙二酸酐结构
高三化学第二次模拟试题(实验班,含解析) 人教新目标版

——————————教育资源共享步入知识海洋————————2019高三第二次模拟(实验班)化学试题1. 设N A为阿伏加德罗常数值。
下列叙述正确的是A. 28gC2H4和CO的混合气体中含有的分子数为N AB. 28gN2和6gH2充分反应,生成NH3的分子数为2N AC. 标准状况下,11.2LO2参加反应转移的电子数一定为2N AD. 0.1molFeCl3完全水解转化为氢氧化铁胶体,生成0.1N A个胶粒【答案】A【解析】A、C2H4和CO的摩尔质量都为28g/mol,28gC2H4和CO的混合气体为1mol,则其中含有的分子数为N A,选项A正确;B、合成氨是可逆反应,反应不可能完全转化,28gN2和6gH2充分反应,生成NH3的分子数小于2N A,选项B错误;C、标准状况下,11.2LO2参加反应转移的电子数可能为N A,如氧气与金属钠反应生成过氧化钠,选项C错误;D、l个氢氧化铁胶体中含有多个Fe(OH)3,1molFeCl3完全水解生成的氢氧化铁胶体胶粒数没有N A个,选项D错误。
答案选A。
2. 三氯甲烷(CHCl3)又称氯仿,可用作麻醉剂,但在光照下易被氧化成剧毒的光气(COCl2)。
其反应式为2CHCl3+O22COCl2+2HCl,为了防止事故发生,在使用三氯甲烷前要先检验一下其是否变质,检验用的最佳试剂是A. NaOH溶液B. AgNO3溶液C. 溴水D. 淀粉碘化钾溶液【答案】B【解析】A、加入NaOH溶液,没有明显的现象,不能用来检验,故A错误;B、氯仿被氧化时生成HCl,加入硝酸酸化的硝酸银溶液生成AgCl白色沉淀,可检验,故B正确;C、溴水与氯化氢不反应,不能用来检验,故C错误;D、淀粉KI试剂与氯化氢不反应,不能用来检验,故D错误;故选B。
点睛:本题考查氯仿是否变质的实验设计,题目难度不大,本题注意根据氯仿变质的方程式结合有关物质的性质进行判断,解题关键:根据方程式2CHCl3+O22COCl2+2HCl,可知,如果氯仿变质会生成HCl,可以通过检验是否有氯化氢生成判断氯仿是否变质,如加入AgNO3溶液生成AgCl白色沉淀。
有机化学羧酸及其衍生物
Organic Chemistry
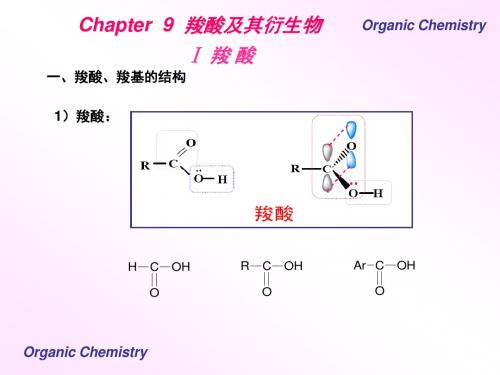
Ⅰ羧酸
一、羧酸、羧基的结构 1)羧酸:
H
C O
OH
R
C O
OH
Ar C O
OH
Organic Chemistry
Chapter 9 羧酸及其衍生物
2)羧基的结构:
C O
R
Organic Chemistry
OH
O
..
R C O H
形式上看,羧基由羰基和羟基组成。羟基氧原子的未共用电子对所 占据的 p轨道和羰基的 π键形成 p-π共轭。羟基氧上电子云密度有所 降低,羰基碳上电子云密度有所升高。因此,羧酸中羰基对亲核试 剂的活性降低,不利于HCN等亲核试剂反应。 Organic Chemistry
对于含不饱和键的不饱和羧酸则取包括羧基和不饱和键的最长碳链为主链称某烯酸并注明不饱和键的位置命名含脂碳环羧酸和芳香羧酸时则把脂碳环和芳环当作取代基choh3乙基己酸3丙基4戊烯酸coohchcoohchcoohcoohcooh乙基丙二酸邻苯二甲酸环戊基甲酸四物理性质羧酸的沸点比相近分子质量的其它有机物要高
3—丙基—4—戊烯酸
COOH
COOH
乙基丙二酸
环戊基甲酸
邻苯二甲酸
Organic Chemistry
Chapter 9 羧酸及其衍生物
四、物理性质
羧酸的沸点比相近分子质量的其它有机物要高: 乙 丙 酸(60):117.9℃ 醛(58): 48.8℃ 8 ℃
Organic Chemistry
正丙醇(60): 97.4℃ 甲乙醚(60):
味道 沸点
酰氯和酸酐都对粘膜有刺激性,酯有香味。 酰氯、酸酐和酯由于不能形成氢键,熔沸点与分子量相近
分析化学3胺

胺的命名普通命名
简单的胺,把他所含烃基的名称和数目
写在前面,按简单到复杂先后列出后面加
上胺字:
CH3CH2NCH2CH2CH3
CH3CH2NH2NH2Βιβλιοθήκη CH3乙胺苯胺
甲乙丙胺
胺的命名-系统命名法
选最复杂的烃基作母体,称某胺,氮上 其它的烃基作为取代基,并用N定其位。
遇到比较复杂的胺则以烃为母体, 把氨基作取代基。
R N R X-
R 季铵碱: 季铵盐分子[R4N]+X-中的X-被 OH- 取
代的化合物。显碱性,NaOH相近
[R4N]+OH-
R
+
R N R OH-
R
胺的命名 氨?胺?铵?
氨:作为取代基时称氨基,如-NH2
CH3NH-甲氨基
胺:作为官能团时称胺,CH3NH2甲胺 铵:氮上带有正电荷时称铵如 CH3N+H3Cl 氯化甲基铵
有机合成中用来保护氨基。 例:由苯合成对氨基苯甲酸(退热药)
(二)酰化反应 磺酰化反应
伯胺和仲胺都能与酰氯或 酸酐反应而生成酰胺。
不溶于酸和碱
R兴S斯O2堡N+反R3应Cl-
分离提纯和鉴别: 伯胺 仲胺 叔胺
(三)与亚硝酸反应 区别伯仲叔胺
1. 伯胺与亚硝酸反应 ( N2↑ )
(1).脂肪伯胺在强酸存在下与亚 硝酸反应,生成醇并定量放出氮气↑。
结构:
.. 107º ..
108º ..
N H HH
N H3C H H
N H3C CH3CH3
氨的结构 甲胺的结构 三甲胺的结构
(一)碱性与成盐反应
氨及胺的碱性强弱比较:
(CH3)2NH > CH3 NH2 > (CH3)3N > NH3 >
高中化学选择性必修三 第1章第1节 有机化合物的同分异构体数目的判断方法

2020—2021学年人教版(2019)选择性必修三章节自我强化训练1.1.6 有机化合物的同分异构体数目的判断方法1.已知有机物A 、B 之间存在转化关系:61222A C H O +H O B+H ()HCOO (已配平)。
则符合条件的A 的同分异构体有(不考虑立体异构)( ) A.5种B.6种C.7种D.8种2.某烷烃主链上有4个碳原子的同分异构体有2种,含有相同碳原子数且主链上也有4个碳原子的单烯烃的同分异构体有( ) A.2种B.4种C.5种D.7种3.分子式为512C H O 且可与金属钠反应放出氢气的有机物有(不考虑立体异构)( ) A.5种B.6种C.7种D.8种4.丁烷(410C H )失去1个氢原子后得到丁基(—49C H ),丁基的结构共有( ) A. 2种B. 3种C. 4种D. 5种5.分子式为C 9H 11Cl 且含有苯环的同分异构体有( ) A.30种B.36种C.39种D.42种6.并六苯的某衍生物结构简式为,其苯环上的氢原子再被1个Cl 原子 取代的产物有( ) A.3种B.6种C.7种D.8种7.相对分子质量为100的有机物 A 能与钠反应,且完全燃烧只生成2CO 和2H O 。
若 A 含一个六碳环,则环上一氯代物的数目为( ) A.4B.5C.3D.28.分子式为511C H Br 且含有两个甲基的同分异构体共有(不考虑立体异构)( )A. 3种B. 4种C. 5种D. 6种9.分子式为5102C H O 并能与饱和3NaHCO 溶液反应放出气体的有机物有( ) A.3种B.4种C.5种D.6种10.分子式为512C H O 的有机物,能与Na 反应的同分异构体的种数: ( ) A .6B .7C .8D .911.分子式为482C H Cl 的有机物共有(不含立体异构)( ) A. 7种B. 8种C. 9 种D. 10 种12.分子式为5102C H O 且可与碳酸氢钠溶液反应放出气体的有机化合物有() A. 3种 B. 4种 C. 5种 D. 6种13.下列物质在给定条件下的同分异构体数目(不包括立体异构)正确的是( ) A.乙苯的一氯代物有4种B.分子式为512C H O 且属于醇的有机物有6种C.分子式为482C H O 且属于酯的有机物有4种D.分子式为48C H 且属于烯烃的有机物有4种14.对羟基桂皮酸()的同分异构体中满足下列条件的有(不考虑立体异构)( )①能与3NaHCO 溶液发生反应产生2CO②能发生银镜反应的芳香族化合物 A.15种B.16种C.17种D.18种15.网络趣味图片“一脸辛酸”,是在熊猫脸上重复画满了辛酸的键线式结构。
032二烯烃

O
+
R N O-
O-
+
RN O
O
RN O
(b) 同一化合物的不同极限结构只是电子排布的变化,原
子核位置不变。
CH3CH CH CH2+
+
CH3CH CH CH2
CH2 CH O
CH3 CH O
H
(c)同一化合物的不同极限结构的成对电子数目必须相同。
CH2 CH CH2
H2C CH CH2
H2C CH CH2
n
丁苯橡胶
n CH2 CH C CH2 Cl
聚合
CH2 CH C CH2 Cl
n
氯丁橡胶
四. 离域体系的共振论表述法 (1)共振论的基本概念
共振论:即离域体系可以用几个经典结构的叠加来描述。
CH2 CH CH CH2
+CH2 CH CH2 CH2-
-CH2 CH CH2 CH2+
1,3-丁二烯的共振杂化体
一. 二烯烃的分类
二烯烃是指含有两个碳碳双键的烃类化合物。二烯烃的 通式都是CnH2n-2,都含有两个不饱和度。根据分子中两个双 键的相对位置,又可以分成下面三种:
(1)累积二烯烃 是指分子中两个双键合用一个碳原 子,即含有>C=C=C<结构的二烯烃。例如:
CH2 C CH2
丙二烯
CH3 CH C CH2
1,4- 制产物:利用平衡
1,2-加成反应进程 1,4-加成
达到控制的主要产 物。
2. 狄尔斯(O.Diels)-阿德耳(K.Alder)反应
共轭二烯烃与含活化烯键或炔键(烯键或炔键碳原子上有
的化合物(称为亲二烯体)反应,生成含六元环的化合物。例 如:1,3-丁二烯与丙烯醛反应,生成环己烯-4-甲醛:
有机化学II-13羧酸及其衍生物
羧酸和芳香族羧酸都是固体。
水溶性:
C1~C4羧酸可以和水混溶。芳香族羧酸分子量大,
难溶于水。 4-11碳部分溶解;羧酸盐水中溶 解性好
(长链羧酸盐为好的表面活性剂)。
实 例
O O H H
COOH OH
COOH
O
OH
邻位
诱导吸电子作用大、 共轭给电子作用大、 氢键效应吸电子作用大。 pka 2.98 苯甲酸的pka 4.20
间位
诱导吸电子作用中、 共轭给电子作用小。
对位
诱导吸电子作用小、
共轭给电子作用大。
pka 4.08
pka 4.57
二元酸: 有两个解离常数 举例:
十八酸 硬脂酸
CH2 COOH CH2 COOH
乙二酸(草酸) 丙二酸(胡萝卜酸) 丁二酸(琥珀酸)
HOOC
COOH
顺丁烯二酸 (马来酸)
反丁烯二酸 (富马酸)
苯甲酸(安息香酸)
(乙)系统命名法
(A)脂肪族羧酸
母体: 选含羧基的最长连续碳链,不饱和羧酸选含羧 基和不饱和键在内的最长连续碳链为主链.
内酐
COOH 230oC COOH
CO O + H2O CO
二元酸酐
邻苯二甲酸酐
混合酸酐
O
O
CH3CH2 C Cl + Na OCCH3
△
O O CH3CH2C OCCH3
3. 酯的生成
RCOOH + R'OH H+
RCOOR' + H2O
酸酐反应特性实验报告(3篇)

第1篇一、实验目的1. 研究酸酐的基本性质和反应活性。
2. 探讨酸酐在有机合成中的应用,特别是与醇、酚、酰胺等化合物的反应。
3. 通过实验,加深对酸酐反应机理的理解。
二、实验原理酸酐是一类含有两个羰基的化合物,具有强烈的亲电性,能够与多种化合物发生反应。
常见的酸酐包括乙二酸酐、丙二酸酐、丁二酸酐等。
酸酐与醇、酚、酰胺等化合物反应时,可以生成酯、酐、酰胺等化合物。
三、实验材料与仪器材料:- 酸酐(如乙二酸酐)- 醇(如甲醇、乙醇)- 酚(如苯酚)- 酰胺(如乙酰胺)- 碱性催化剂(如NaOH)- 醋酸(用于中和)仪器:- 圆底烧瓶- 冷凝管- 热水浴- 抽滤装置- 旋转蒸发仪- 紫外-可见光谱仪四、实验步骤1. 酸酐与醇的反应- 将一定量的醇加入圆底烧瓶中,加热至回流温度。
- 缓慢滴加酸酐,同时不断搅拌。
- 反应结束后,冷却至室温,加入适量的醋酸中和,然后进行抽滤。
- 将滤液旋蒸浓缩,得到产物。
2. 酸酐与酚的反应- 将一定量的酚加入圆底烧瓶中,加热至回流温度。
- 缓慢滴加酸酐,同时不断搅拌。
- 反应结束后,冷却至室温,加入适量的醋酸中和,然后进行抽滤。
- 将滤液旋蒸浓缩,得到产物。
3. 酸酐与酰胺的反应- 将一定量的酰胺加入圆底烧瓶中,加热至回流温度。
- 缓慢滴加酸酐,同时不断搅拌。
- 反应结束后,冷却至室温,加入适量的醋酸中和,然后进行抽滤。
- 将滤液旋蒸浓缩,得到产物。
五、实验结果与分析1. 酸酐与醇的反应- 反应产物为酯,通过紫外-可见光谱仪检测,发现产物在特定波长下有吸收峰,与理论预测一致。
2. 酸酐与酚的反应- 反应产物为酐,通过紫外-可见光谱仪检测,发现产物在特定波长下有吸收峰,与理论预测一致。
3. 酸酐与酰胺的反应- 反应产物为酰胺,通过紫外-可见光谱仪检测,发现产物在特定波长下有吸收峰,与理论预测一致。
六、实验结论1. 酸酐与醇、酚、酰胺等化合物反应,可以生成相应的酯、酐、酰胺等化合物。
有机化学 第十三章 羧酸衍生物

羧酸衍生物
O
OO
O
O
R CXR CO C RR CO RR ' CN 2H ( RCN)
O
上述化合物中均含有 R C 因此它们的化学性质相似:
① 均可以核亲核试剂发生亲核加成消去反应; ② 均可由羧酸制备; ③ 水解均可以得到羧酸。 一、羧酸衍生物结构的比较:
1、酰胺:
O
CN O
H C NH 2 CH 3 NH 2
1.376
1.474 Oδ -
H C NH 2
C
δ+
NH 2
① 羰基碳正电荷降低,亲核加成困难;
② N原子电荷降低,碱性减弱,显弱酸性。
2、酯:
O
H C O CH 3 CH 3 OH
CO
1.334
1.430
OC O
由于O的电负性大于N,因此,酯中羰基碳 的正电荷应大于酰胺中羰基碳的正电荷。
酯 +酯
β -酮 酸 酯
酯 + 甲酸酯
α -甲 酰 酯
酯 + 苯甲酸酯
α -苯 甲 酰 酯
酯 + O C( OE t) 2 酯 + 草酸酯
取代丙二酸酯 β -环 二 酮 酯
酯+ 酮
β -二 酮
二元酸酯
β -环 酮 酯
七、达参缩合:
O
α-卤代酸酯+ C O
α ,β -环氧酯 O E tO -
O + C Cl2HC Ot E
取代基—I效应:
O
X2>R C O >RO> N2 H
羰基的正电荷:
O
OO
O
O
第十三章 羧酸衍生物

酮与格氏试剂的反应比酯与格氏试剂的反应快,因此,仅位阻较大的 酯才能停留在酮的阶段。内酯也能发生相同的反应,产物为二醇。
O
O
1, C2H5MgBr 2, H3O
OH HOCH2CH2CH2CH2C C2H5 C2H5
(3)还原反应 )
催化氢化
RCOOR' + H2
氢化铝锂
CuO-CrO3 20-30MPa
(COOC2H5)2 170℃
C6H5CHCOOC2H5 COCOOC2H5
C6H5CHCOOC2H5 COOC2H5
C6H5CH2COOC2H5 +
HCOOC2H5
C2H5ONa
C6H5CHCOOC2H5 CHO
利用甲酸酯和草酸酯是在酯的α-位引入醛基和酯基的重要方法。
酮的α-氢比酯的α-氢更活泼,因此当酮与酯进行缩合时就可以得到β-羰基酮。
*
O * + OH R C OCH3
2、酸性条件下的机理
O R C L + H OH R C L
H2 O 慢
R
OH C L OH2
-H
R
OH C L OH
H
R
OH C LH OH
OH R C OH
-H
O R C OH + HL
3o醇的羧酸酯水解:SN1机制 醇的羧酸酯水解: 机制
O RCOC(CH3)3
O NH O
邻苯二甲酰亚胺
二、物理性质与光谱性质
酰卤、酸酐有刺激性气味,强腐蚀作用。酯有香味。 IR光谱:C=O的特征吸收峰 酰卤:1800~1750 cm-1 酸酐:1850~1800 cm-1 ,1790~1740 cm-1两个 酯: 1750~1745 cm-1,没有OH的吸收峰 酰胺:1690~1630 cm-1,3550~3050 cm-1有N-H吸收
第三章 酰化反应

O C O CH2CH2N(C2H5)2 + C2H5OH
(3)反应条件
水容易使酯水解,因此反应需要在无水条件下进 行,还要防止其他酯类在乙醇中重结晶。例:抗胆碱 药溴美喷酯(宁胃适)的合成
HO C OH CH3 COOCH2CH3 + N CH3CH2ONa 60-80℃,45min
C OH
COO N CH3
攻,而且使中间体稳定;若是给电子的作用相反。
根据上述的反应机理可以看出,作为被酰化物质 ( 醇 ) ,
其亲核性越强越容易被酰化。具有不同结构的被酰化物的 亲核能力一般规律为; RCH2 - > R-NH- > R-O - > R-NH2 >R-OH。(难酯化的醇需AlCl3催化)
在消除阶段
反应是否易于进行主要取决于 L的离去倾向。L—碱性 越强,越不容易离去, Cl— 是很弱的碱,—OCOR的碱性 较强些,OH— 、OR—是相当强的碱,NH2—是更强的碱。
O ROH + R' C L R' O C OR + HL
醇的结构对酰化反应的影响 伯醇(苄醇、烯丙醇除外)>仲醇>叔醇
一 、醇的氧酰化 (一) 酰氯为酰化剂
RCOCl + R'OH
RCOOR' + HCl
酰氯常用于空间位阻大的醇,如叔醇的酰化:
(CH3)3COH + C6H5CH=CHCOCl (CH3)3COOCHCH=CHC6H5
醇的结构对酰化反应的影响 立体影响因素:伯醇>仲醇>叔醇、烯丙醇 叔碳正离子倾向与水反应而逆转
电子效应的影响
羟基a位吸电子基团通过诱导效应降低O上电子云
密度,使亲核能力降低
苄醇、烯丙醇由于p-p共轭,使活性降低
材料化学

一碳化学氧化碳摘要:化学反应过程中反应物只含一个碳原子的反应统称为一碳化学。
一碳化学的主要目的是节约煤炭和石油资源,用少的碳原料生成多的燃料,提供给人类。
碳氧化物是指只由碳与氧组成的化合物。
最简单常见的碳氧化物包括一氧化碳(CO)和二氧化碳(CO2)。
除了这两种为人熟知的无机物,碳与氧其实还能构成许多稳定或不稳定的碳氧化物,但在现实生活中很难接触到其他碳氧化物(例如二氧化三碳(C3O2)等)。
关键词:氧化碳;一氧化碳;二氧化碳;三氧化四碳;九氧化十二碳所谓一碳化学从广义上说是由含一个碳的化合物合成碳-碳键化合物的化学。
这里所指的一个碳的化合物是一氧化碳(CO)、二氧化碳(CO2)、甲烷(CH4)、甲醇(CH2OH)、甲醛(HCHO)、甲酸(HCOOH)等。
它们的相互关系如图所示,这些C1化合物是很普遍的化合物,而其利用反应,早就有研究。
但是一碳化学或C1化学这个名称是在1980年左右才出现的这是为什么呢?这是和1980年前发生的所谓“石油危机”有密切的关系上午,那时的有机化工产品的原料大部分是依靠石油。
但是,石油是有限的天然资源,在那时,由于工业的高速度发展,石油的消耗量非常大,隐藏量一年比一年少,价额越来越高为此,人们不得不考虑代替石油的资源,而所考虑到的一些资源都是属于含一个碳的化合物。
因此,出现了“一碳化学”这个名称。
1.前沿1.1一氧化碳在古代用来处决希腊人和罗马人,在11世纪一个西班牙医生第一次描述了这种气体。
最早制备一氧化碳的是法国化学家de Lassone(在1776年)。
他通过加热氧化锌和碳制得了一氧化碳。
但由于一氧化碳燃烧时产生了与氢气类似的蓝色火焰,de Lassone错误地认为他制得的是氢气。
在1800年英国化学家William Cruikshank才证明一氧化碳是由碳元素和氧元素组成的化合物。
最早对一氧化碳的毒性进行彻底研究的是法国的生理学家Claude Bernard。
丙酸酐安全技术说明书(msds)
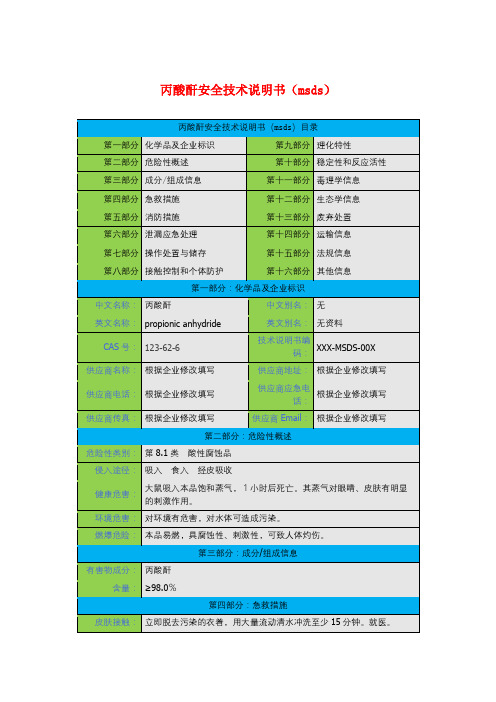
包装标志:
20
包装类别:
O53
包装方法:
无资料
运输注意事项:
起运时包装要完整,装载应稳妥。运输过程中要确保容器不泄漏、不倒塌、不坠落、不损坏。严禁与氧化剂、碱类、食用化学品等混装混运。运输时运输车辆应配备相应品种和数量的消防器材及泄漏应急处理设备。运输途中应防曝晒、雨淋,防高温。公路运输时要按规定路线行驶,勿在居民区和人口稠密区停留。
第十六部分:其他信息
参考文献:
[1~25]参考书:危险化学品安全技术全书.第一卷/张海峰主编.—2版.北京;化学工业出版社,2007.6 ISBN 978-7-122-00165-8
修改说明:
第一版
其他信息:
MDL号:MFCD00009303PubChem号:暂无BRN号507066
填表部门:
审核部门:
食入:
用水漱口,给饮牛奶或蛋清。就医。
第五部分:消防措施
危险特性:
其蒸气与空气可形成爆炸性混合物,遇明火、高热易引起燃烧爆炸。与强氧化剂接触可发生化学反应。具有腐蚀性。
建规火险分级:
丙
有害燃烧产物:
一氧化碳、二氧化碳。
灭火方法:
消防人员须戴好防毒面具,在安全距离以外,在上风向灭火。用水喷射逸出液体,使其稀释成不燃性混合物,并用雾状水保护消防人员。灭火剂:抗溶性泡沫、干粉、砂土。
丙酸酐
丙酸酐安全技术说明书(msds)目录
第一部分
化学品及企业标识
第九部分
理化特性
第二部分
危险性概述
第十部分
稳定性和反应活性
第三部分
成分/组成信息
第十一部分
毒理学信息
第四部分
急救措施
1,3-丙二磺酸酐结构式

1,3-丙二磺酸酐结构式1,3-丙二磺酸酐是一种有机化合物,其结构式为C3H6O6S2。
它是一种无色结晶固体,在常温下稳定性较好。
本文将从其物理性质、化学性质和应用领域等方面进行探讨。
我们来了解一下1,3-丙二磺酸酐的物理性质。
该化合物的密度为1.79 g/cm³,熔点为130-135℃,沸点为355℃。
它在水中溶解度较高,可溶于醇、酮等有机溶剂。
接下来,我们将重点关注1,3-丙二磺酸酐的化学性质。
它是一种酸酐化合物,可以与一些亲核试剂发生反应。
例如,它可以与胺类化合物反应生成相应的酰胺。
此外,它还可以与亲电试剂如卤代烃反应,生成烷基化产物。
这些反应都可以通过酐中的酰氧与试剂中的亲核或亲电中心发生反应来实现。
1,3-丙二磺酸酐在有机合成中有着广泛的应用。
首先,它可以作为一种试剂用于合成其他化合物。
例如,它可以与氨基酸反应生成相应的酰胺,这在肽合成中有着重要的应用。
此外,它还可以用于制备含磺酸酯基团的有机化合物,这些化合物在医药和农药领域具有一定的应用潜力。
1,3-丙二磺酸酐还可以作为一种表面活性剂。
表面活性剂是一类能够改变溶液表面张力的化合物,常用于洗涤剂、乳化剂等领域。
由于1,3-丙二磺酸酐具有含有磺酸基团的特点,使其在表面活性剂中具有一定的应用潜力。
总结一下,1,3-丙二磺酸酐是一种重要的有机化合物,具有较好的物理稳定性和化学反应性。
它在有机合成和表面活性剂领域有着广泛的应用前景。
通过进一步研究和开发,相信1,3-丙二磺酸酐在更多领域中将发挥重要作用,为人们的生活带来更多便利和创新。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
丙二酸酐结构
丙二酸酐,也称为马来酸二乙酯,是一种有机化合物,化学式为C5H6O3。
其分子式中含有两个羧酸基和一个双键。
丙二酸酐的结构是一个五元环,由两个羧酸基和一个双键构成。
它的分子中有一个碳-碳双键和一个羧酸基,这意味着它具有反式立体构型。
在分子中,双键的两侧分别连接着一个羧酸基和一个乙基基团。
丙二酸酐是一种重要的化学品,广泛用于制造塑料、树脂、涂料、染料等化工产品。
它还可用作有机合成的重要中间体,包括用于制造药品、香料和食品添加剂等。
