丹参内控质量标准
丹参中国药典标准

丹参中国药典标准丹参是一种中草药,也被称为红参、血栓通。
在中国药典中,丹参有着详细的标准和规定,下面将对丹参的药典标准进行详细介绍。
丹参的药材是丹参的根茎,成熟的根茎连同主根一起采收,除去根冠和须根,晒干备用。
药材应具有鲜红色或紫红色,表面有皱纹和纵裂的根茎。
根茎应具有较大的长度和直径,有的根茎还带有分枝。
根茎应无虫蛀、腐朽、生霉及糟粕者。
二、【性状特征】丹参的根茎一般呈圆柱形或近圆柱形,多弯曲,长10-20厘米,直径0.3-2厘米。
表面紫红色或紫褐色,有皱纹和纵裂。
质坚韧,断面呈淡红色或鲜红色,有凹陷的纵隔和弦纹。
气香,味微苦。
三、【理化性质】丹参含有丹参酮、丹参酮ⅡA、丹参酮ⅢA等活性成分。
研究发现,丹参具有舒张血管、增加血流量、抗心肌缺血、抗炎、抗氧化、抗凝血等药理作用。
四、【有效成分】丹参中的有效成分主要是丹参酮类化合物,其中包括丹参酮、丹参酮ⅡA、丹参酮ⅢA等。
这些成分具有改善血液循环、抗炎、抗氧化、抗凝血等作用,对心脑血管疾病具有疗效。
五、【药理作用】丹参具有扩张血管、增加血流量、抗血小板凝聚、抗炎、抗氧化等药理作用。
丹参还可以改善微循环,增加红细胞变形能力,减少黏滞度,抑制血小板凝聚,降低血小板粘附,增加纤溶活性,防止和抑制血栓形成。
六、【临床应用】丹参主要用于治疗心脑血管疾病,如心绞痛、心肌梗死、冠心病等。
丹参还可以用于治疗糖尿病、高血脂、高血压等疾病。
丹参具有很高的药用价值,成为许多中药方剂中的重要组成部分。
它不仅具有显著的疗效,而且具有较低的毒副作用。
丹参的药典标准的制定和实施,使得丹参的质量得到保证,从而更好地发挥其药理作用,为人们的健康提供了有效的保障。
丹参检验标准操作规程
原药材检验标准操作规程目的:建立一个中药饮片原药材检验标准操作程序,确保检验结果准确可靠。
适用范围:中药原药材。
责任人:质量保证部主任、质量控制部主任、化验员。
标准来源:《中华人民共和国药典》2010年版一部、《安徽省中药饮片炮制规范》。
内容:1、性状取本品适量,放入白瓷盘中,用眼观察,可见以下性状特征:本品根茎短粗,顶端有时残留茎基。
根数条,长圆柱形,略弯曲,有的分枝并具须状细根,长10~20cm,直径0.3~1cm。
表面棕红色或暗棕红色,粗糙,具纵皱纹。
老根外皮疏松,多显紫棕色,常呈鳞片状剥落。
质硬而脆,断面疏松,有裂隙或略平整而致密,皮部棕红色,木部灰黄色或紫褐色,导管束黄白色,呈放射状排列。
气微,味微苦涩。
栽培品较粗壮,直径0.5~1.5cm。
表面红棕色,具纵皱,外皮紧贴不易剥落。
质坚实,断面较平整,略呈角质样。
2、鉴别主要使用仪器:电子分析天平、电子显微镜、紫外光灯等。
2.1显微鉴别:2.1.1 试液配制2.1.1.1 水合氯醛试液:取水合氯醛50克,加水15毫升与甘油10毫升使溶解,即得。
2.1.1.2 甘油醋酸试液:取甘油、醋酸及水各等份混匀,即得。
2.1.1.3 稀甘油:取甘油33毫升,加水稀释至100毫升,再加樟脑一小块或液化苯酚1滴,即得。
2.1.2 供试品制备2.1.2.1 取本品10g,研细后取少量粉末,置载玻片上,滴加水合氯醛搅拌均匀,置酒精灯上加热透化;加稀甘油数滴,搅拌均匀,分装2~3片,加盖玻片,即得。
2.1.2.2 取研细的粉末少量置载玻片上,加甘油醋酸试液,搅拌均匀,加盖玻片,即得。
2.1.2.3取研细后取少量粉末,置载玻片上,滴加水搅拌均匀,同时滴加少许稀甘油,加盖玻片,即得。
2.1.3 置显微镜下观察可见本品粉末红棕色。
石细胞类圆形、类三角形、类长方形或不规则形,也有延长呈纤维状,边缘不平整,直径14~70 μm,长可达257 μm,孔沟明显,有的胞腔内含黄棕色物。
丹参及其制剂的质量标准研究_杨宇宏

激活纤溶酶原为纤溶酶,从而间接溶解纤维蛋白;3)在体内、体外能够促进组织型纤溶酶原激活物表达;4)与水蛭素样物质共同作用可以直接抑制血管损伤后局部的血液凝固及附壁血栓的形成。
疏血通具有抑制血小板、红细胞聚集性,促进脑组织及脑组织微血管内皮细胞分泌组织型纤溶酶原激活物,增强纤溶活性,降解纤维蛋白原,有效降低血液黏稠度,对抗凝血,从而抑制、对抗血栓形成;还能促进血管内皮生长因子表达,并促进微血管生成,高效、迅速地改善脑部血液循环,增加脑血流量,一定程度上恢复脑梗死区及梗死周边缺血半暗带区脑细胞的功能。
本组研究结果表明:疏血通与血塞通注射液均为治疗急性脑梗死的有效静制剂,但两者的总有效率差异有显著性。
本研究结果表明,治疗后两组全血高切黏度,血浆黏度,红细胞压积,纤维蛋白原血液流变学指标都下降,但疏血通注射液降低血液粘稠度的作用强于血塞通注射液,提示该药通过改善血液微循环降低脑水肿有关,而起到治疗作用。
疏血通作用机制可能为:一方面可通过促纤溶、抗凝作用,促进血栓溶解使血管再通而恢复血液灌注,并防止血栓再次形成,阻止疾病的进展和复发,另一方面可通过其神经保护作用减轻脑组织缺血再灌注损伤。
应用疏血通注射液治疗急性脑梗死,使病灶的血流量增加,避免梗死区向外蔓延和扩大,显著地降低全血粘度、红细胞比容、血浆粘度、还原比粘度以及纤维蛋白原的含量,使红细胞均匀地分布在血浆中,有利于血浆在血管中流动,有利于防止血栓的再发生。
临床应用,安全有效,副作用较小,可参考文献[1] 中华医学会第四届全国脑血管病学术会议.各类脑血管病诊断要点[J].中华神经科杂志,1996,29(6):379-380.[2] 江承平,吴碧华,刘福等.疏血通对脑梗塞患者血清IL-6和TNF 的影响[J]. 脑与神经疾病杂志,2007,l5(6):445-446.[3] 吴祖舜,高俊冈,冯美江,等.急性脑梗血栓形成不同治疗时间窗的溶栓 (尿激酶治疗疗效分析.附738例报告)[J].中华常见病临床研究,2002,2(3):1-4.[4] 丛乃旺.疏血通注射液治疗急性脑梗死的疗效观察[J].实用全科医学,2006,4(1):8-9.[5] 李支援,张东君,徐龙君,等.疏血通对沙士鼠脑缺血再灌注损伤的保护作用及其对NO、NOS含量的影响[J].卒中与神经疾病,2003,l0(4):207-211.表3 两组治疗前后血液流变学指标比较组别 全血高切黏度 血浆黏度 红细胞压积( ) 纤维蛋白原(mpa.s) (mpa.s)( ) (g/l)对照组 治疗前 6.3±1.2 1.95±0.2550±4.6 4.32±0.26 治疗后 5.6±1.5* 1.84±0.23 46±4.1 3.56±0.19*治疗组 治疗前 6.3±1.3 1.95±0.25 50±4.6 4.32±0.26 治疗后 5.1±0.9*※1.66±0.21*※43±3.9*※3.28±0.18*※注:和治疗前比较,*P <0.05,和对照组比较,※P <0.05表2 两组治疗前后神经功能缺损程度评分比较组别 例数 治疗前积分 治疗后积分对照组 50 27.08±3.52 19.02±8.45*治疗组5027.09±3.6914.99±8.66*※注:和治疗前比较,*P <0.05,和对照组比较,※P <0.05表1 两组有效率的比较组别例数 基本痊愈 显著进展进展无变化恶化 总有效率对照组 50 (7)14% (10)20% (19)38% (7)14% (7)14% (36)72%治疗组 50 (13)26% (20)40%(8)16% (6)12% (3)6% (41)82%*注:和对照组比较,*P <0.05丹参为唇形科植物丹参(salvia miltiorrhiza Bga)的干燥根及根茎。
延丹

4、防伪标签ZB/SOP/NK/BC/
5、中盒ZB/SOP/NK/BC/
6、大箱
7、PVC硬片
成品JB/ZB/CP/00801 ZB/SOP/NK/CP/00801
四、留样观察情况
见留样观察台帐中延丹益心胶囊部分
留样观察记录中延丹益心胶囊部分
三、质量标准、内控质量标准及检验操作ห้องสมุดไป่ตู้程
原料
1、丹参JB/ZB/YF/07901 ZB/SOP/NK/YF/00101
2、乳香JB/ZB/YF/08501 ZB/SOP/NK/YF/08602
3、五灵脂JB/ZB/YF/08201 ZB/SOP/NK/YF/09701
4、白芍JB/ZB/YF/08701 ZB/SOP/NK/YF/08801
5、枳壳JB/ZB/YF/04001 ZB/SOP/NK/YF/09801
6、瓜蒌JB/ZB/YF/08301 ZB/SOP/NK/YF/09602
7、延胡索JB/ZB/YF/09201 ZB/SOP/NK/YF/09401
8、延丹益心胶囊醇提粉ZB/SOP/NK/YF/10702
9、延丹益心胶囊水提粉ZB/SOP/NK/YF/10601
10、延丹益心胶囊生粉ZB/SOP/NK/YF/10801
中间体
1、延丹益心胶囊烘干粉ZB/SOP/NK/ZC/01101
2、延丹益心胶囊胶囊粒ZB/SOP/NK/ZC/01201
包装材料
1、铝箔ZB/SOP/NK/BC/025001 ZB/SOP/NK/BC/120000
2、小盒ZB/SOP/NK/BC/
丹参质量标准

XXXXXXXXX有限公司
一、目的:建立丹参药材、饮片的质量标准,确保投用药材、饮片的质量。
二、范围:本规定适用于丹参药材、饮片的质量控制。
三、责任:
四、内容:
1.标准来源
《中国药典》2015年版一部
2.技术要求
2.1丹参药材:
2.2丹参饮片:
3.贮存条件:置干燥处。
4.相关标准操作规程:丹参检验操作规程(SOP-ZL-JG(YL)-041)、物料取样标准操作规程(SOP-ZL-QA-001)。
5.企业统一指定的物料名称:与2015年版《中国药典》一部一致。
6.内部使用的物料代码:1101250。
7.经批准的供应商:见合格供应商目录。
8.印刷包装材料的实样或样稿:无此项内容。
9.注意事项:无此项内容。
10.复验期:执行“物料有效期及复验期管理规程(SMP-WL-008)”相关规定。
11.文件附件:共0份。
12.修订及变更历史:。
丹参片生产工艺质量标准及检验方法2
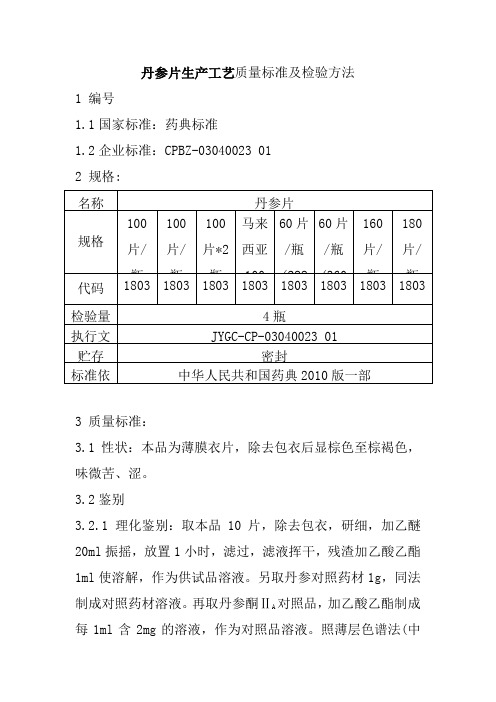
丹参片生产工艺质量标准及检验方法1 编号1.1国家标准:药典标准1.2企业标准:CPBZ-03040023 012 规格:名称丹参片规格100片/瓶100片/瓶100片*2瓶马来西亚10060片/瓶(28860片/瓶(360160片/瓶180片/瓶代码1803040018030400180304001803040018030400180304001803040018030400检验量4瓶执行文JYGC-CP-03040023 01贮存密封标准依中华人民共和国药典2010版一部3 质量标准:3.1性状:本品为薄膜衣片,除去包衣后显棕色至棕褐色,味微苦、涩。
3.2鉴别3.2.1 理化鉴别:取本品10片,除去包衣,研细,加乙醚20ml振摇,放置1小时,滤过,滤液挥干,残渣加乙酸乙酯1ml使溶解,作为供试品溶液。
另取丹参对照药材1g,同法制成对照药材溶液。
再取丹参酮ⅡA对照品,加乙酸乙酯制成每1ml含2mg的溶液,作为对照品溶液。
照薄层色谱法(中国药典一部附录Ⅵ B)试验,吸取上述三种溶液各5μl,分别点于同一硅胶G薄层板上,以环己烷-乙酸乙酯(6:1)为展开剂,展开,取出,晾干。
供试品色谱中,在与对照药材色谱相应的位置上,至少显3个相同颜色的主斑点;在与对照品色谱相应的位置上,显相同的暗红色斑点。
3.3检查3.3.1 外观:完整光洁,色泽均匀.3.3.2重量差异:平均片重±5%。
按中国药典一部附录Ⅰ D 片剂重量差异。
3.3.3崩解时限:按中国药典一部附录ⅫA崩解时限检查法。
3.3.3.1国家标准:应在1小时内全部崩解。
3.3.3.2企业标准:应在50分钟内全部崩解。
3.3.4 水分:按中国药典一部附录Ⅸ H水分测定法第一法。
3.3.4.1企业标准:不得过7.5%。
3.3.5 微生物限度:按中国药典附录XIII C微生物限度检查法。
3.3.5.1国家标准:细菌每1g不得过1000 cfu,霉菌和酵母菌每1g不得过100 cfu,大肠埃希菌每1g不得检出,活螨不得检出。
关于丹参药材质量控制的几点建议_邓乔华

为 此 我 们 建议 对 不 同 产 区
,
一
4 % 1
,
。
丹 参药材 水分偏
, ,
丹参药 材 质 量 进行 评 价 在 此 基 础 上 建 立 丹 参 道 地
高 不 利 于 贮 藏 保 养 易发霉 生 虫变 质 甚 至 霉烂 发
臭 而 不 能人 药
。
药材生产 基 地
2
。
贮 藏 时 间亦 不 宜 过 久 以
革等革羊 革 羊 羊羊 革 苹 羊 等 苹 羊 羊 羊 羊 羊 羊 羊 羊 等 爷苹 苹 羊 羊 羊 羊 等 羊 等 羊 苹 苹 羊 苹 等 苹 苹 羊 羊 革 爷 苹 革 *
中药材第 解 卷第
7
期 2X ) (
1
年
7
月
,
易受 贮藏 环 境 中 的 温 度 湿 度及 贮 藏 时 间 的 影 响 丹
广 栽培 地 区 多 使 得 药 材 质 量 参差 不 齐 严 重 影 响
丹参药材 的 质 量 控 制
。
参药 材 本 身含 水 分 的 高低亦 影 响 贮藏 期 长 短 及 内 在
质量 水 分 宜 控 制 在 1
, , ,
“
。
,
,
2 月 青 前挖根 收 获 但 以 当 年 收 获 为 好 ; 且 以 n 至 1 采 收 的丹 参 丹 参 酮 n A 含 量 最 高 图 其 他 季 节 尤
,
,
诸草木 昆虫 产 之 有 地
失 其 地则 性 味 少 异 若 不
。 ”
,
其 夏 天 丹 参 根 所 含 丹 参 酮 有效 成 分低 不 宜 采 收
, , 。
、
中药材验收 工 作 十 几 年 对 丹 参 药材 的 检 验 积 累 了
原药材丹参质量标准

【浸出物】水溶性浸出物照水溶性浸出物测定法(附录Ⅹ A)项下的冷浸法测定,不得少于40.0%。
醇溶性浸出物照醇溶性浸出物测定法(附录Ⅹ A项下的热浸法)测定,用乙醇作溶剂,不得少于15.0%。
【含量测定】丹参酮IIA照高效液相色谱法(附录Ⅵ D)测定。
色谱条件与系统适用性试验以十八烷基硅烷键合硅胶为填充剂;以甲醇-水(75:25)为流动相;检测波长为270nm。理论板数按丹参酮IIA峰计算应不低于2000。
【检查】水分不得过13.0%(附录Ⅸ H第一法)。
总灰分不得过10.0%(附录Ⅸ K)。
酸不溶性灰分不得过3.0%(附录Ⅸ K)。
重金属及有害元素照铅、镉、砷、汞、铜测定法(附录Ⅸ B原子吸收分光光度法或电感耦合等离子体质谱法)测定,铅不得过百万分之五,镉不得过千万分之三,砷不得过百万分之二,汞不得过千万分之二,铜不得过百万分之二十。
(3)取本品粉末0.2g,加75%甲醇25ml,加热回流1小时,滤过,滤液浓缩至1ml,作为供试品溶液。另取丹酚酸B对照品,加75%甲醇制成每1ml含2mg的溶液,作为对照品溶液。照薄层色谱法(附录Ⅵ B)试验,吸取上述两种溶液各5μl,分别点于同一硅胶GF254薄层板上,以甲苯-三氯甲烷-乙酸乙酯-甲醇-甲酸(2:3:4:0.5:2)为展开剂,展开,取出,晾干。置紫外灯(254nm)下检视,供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的斑点。
对照品溶液的制备取丹参酮IIA对照品适量, 精密称定,置棕色量瓶中,加甲醇制成每1ml中含丹参酮IIA16μg的溶液。
供试品溶液的制备取本品粉末(过三号筛)0.3g,精密称定,置具塞锥形瓶中,精密加入甲醇50ml,称定重量,加热回流1小时,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。
135酒丹参

酒丹参质量标准1.目的:建立酒丹参的质量标准,保证其质量。
2.范围:本公司生产的酒丹参。
3.责任:质量管理部负责人、QC负责人、检验员。
4.内容:4.1 品名:酒丹参汉语拼音名称:JiuDanshen拉丁名称:ZINGIBERIS RHIZOMA4.2 物料代码:C1354.3 产品规格:饮片4.4 包装规格:1.0kg/袋×5袋4.5 标准依据:《中国药典》(2010年版)一部4.6 取样和检验方法4.6.1 取样方法:中药饮片取样标准操作规程。
4.6.2 检验方法:酒丹参检验标准操作规程。
4.7 贮存期:暂定24个月4.8 质量控制项目与限度:4.8.1炮制方法:取丹参片,照酒炙法(附录ⅡD)炒干。
4.8.2 性状:本品呈类圆形或椭圆形的厚片,表面红褐色,略具酒香气。
4.8.3 鉴别(1)本品粉末红棕色。
石细胞类圆形、类三角形、类长方形或不规则形,也有延长呈纤维状,边缘不平整,直径14~70μm,长可达257μm,孔沟明显,有的胞腔内含黄棕色物。
木纤维多为纤维管胞,长梭形,末端斜尖或钝圆,直径12~27μm,具缘纹孔点状,纹孔斜裂缝状或十字形,孔沟稀疏。
网纹导管和具缘纹孔导管直径11~60μm。
(2)取本品粉末1g,加乙醚5ml,振摇,放置1小时,滤过,滤液挥干,残渣加乙酸乙酯1ml使溶解,作为供试品溶液。
另取丹参对照药材1g,同法制成对照药材溶液。
再取丹参酮ⅡA对照品,加乙酸乙酯制成每1ml含2mg的溶液,作为对照品溶液。
照薄层色谱法(附录ⅥB)试验,吸取上述三种溶液各5μl,分别点于同一硅胶G薄层板上,以石油醚(60~90℃)-乙酸乙酯(4:1)为展开剂,展开,取出,晾干。
供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的斑点;在与对照品色谱相应的位置上,显相同的暗红色斑点。
(3)取本品粉末0.2g,加75%甲醇25ml,加热回流1小时,滤过,滤液浓缩至1ml,作为供试品溶液。
国家药品标准中丹参的质量控制情况

国家药品标准中丹参的质量控制情况
丹参是一种具有多种生物活性成分的中草药,被广泛应用于中医药领域。
国家药品标准对丹参的质量控制主要包括以下方面:
1.外观特征:应为呈红棕色或红色的细粉末,无明显气味,味
甜微苦。
2.理化性质:丹参的含水量不应超过13%;挥发油含量不应低
于0.2%;总酚含量不应低于1.5%;丹参酮B1的含量不应低
于1.0%。
3.微生物限度:应符合国家药典中规定的微生物限度标准。
4.重金属、农药残留等细节质量指标。
综上,国家药品标准对丹参的质量控制非常严格,以保证丹参的品质和疗效。
SP-RM-003-01丹参质量标准

题目:丹参质量标准起草:日期:年月日审核:日期:年月日编码: SP-RM-003-01 日期:年月日替代: SP-RM-003-00 批准:日期:年月日编订部门:技术品管部生效日期:年月日本质量标准印发至:各分公司、供应部门────────────────────────────────标准依据:中国药典适用范围:中药制剂责任:供应部门、QA、QC、仓库、生产车间。
质量标准:1 原料编号:010032 原料名称2.1 名称中文名:丹参汉语拼音:Danshen拉丁文名:RADIX SALVIAE MILTIORRHIZAE2.2 来源本品为唇形科植物丹参Salvia miltiorrhiza Bge.的干燥根及根茎。
春、秋二季采挖,除去泥沙,干燥。
3 法定标准(中国药典一部“丹参”)3.1 性状本品根茎短粗,顶端有时残留茎基。
根数条,长圆柱形,略弯曲,有的分枝并具须状细根,长10~20cm,直径0.3~1cm。
表面棕红色或暗棕红色,粗糙,具纵皱纹。
老根外皮疏松,多显紫棕色,常呈鳞片状剥落。
质硬而脆,断面疏松,有裂隙或略平整而致密,皮部棕红色,木部灰黄色或紫褐色,导管束黄白色,呈放射状排列。
气微,味微苦涩。
栽培品较粗壮,直径0.5~1.5cm。
表面红棕色,具纵皱,外皮紧贴不易剥落。
质坚实,断面较平整,略呈角质样。
3.2 鉴别3.2.1 取本品粉末5g,加水50ml,煎煮15~20分钟,放冷,滤过,滤液置编码:SP-RM-003-01 页号:2/3水浴上浓缩至黏稠状,放冷后,加乙醇3~5ml使溶解,滤过,取滤液数滴,点于滤纸条上,干后,置紫外光灯(365nm)下观察,显亮蓝灰色荧光。
将此滤纸条悬挂在浓氨溶液瓶中(不接触液面),20分钟后取出,置紫外光灯(365nm)下观察,显淡亮蓝绿色荧光。
3.2.2 取鉴别3.2.1项下的滤液0.5ml,加三氯化铁试液1~2滴,显污绿色。
3.2.3 取本品粉末1g,加乙醚5ml,置具塞试管中,振摇,放置1小时,滤过,滤液挥干,残渣加醋酸乙酯1ml使溶解,作为供试品溶液。
丹参片生产工艺质量标准及检验方法1

丹参片生产工艺质量标准及检验方法1 编号:ZJBZ-040023 022 规格:名称丹参片规格浸膏喷雾粉颗粒素片包衣品内包装品代码见4检验量50g 50g 50g 50g 50g 5瓶执行文件JYGC-ZJ-040023 01贮存置遮光容器内密闭,阴凉密闭密封,干燥,防止受潮密封密封密封标准依据中国药典2010年版一部3 质量标准:3.1 浸膏3.1.1 外观:应乌润细腻,无杂质。
3.1.2 相对密度:按《相对密度测定法标准操作程序》中比重瓶法检查,应为1.10-1.16(65-75℃)。
3.2 喷雾粉3.2.1 外观:应色泽一致,均匀,无粗粒。
3.2.2 水分:按《水分测定法(快速水分测定仪)标准操作程序》检查,不得过7.5%。
3.2.3 含量测定:数据积累。
3.3 颗粒3.3.1 外观:应粒度均匀,色泽一致,无异物。
3.3.2 水分:按《水分测定法(快速水分测定仪)标准操作程序》检查,应为4.0%~8.0%。
3.3.3 粒度:能全部通过12目筛,95%以上能通过14目筛。
3.3.4 含量测定3.3.4.1 方法:按《高效液相色谱法标准操作程序》检查。
3.3.4.2 色谱条件与系统适用性检验:以十八烷基硅烷键合硅胶为填充剂;以甲醇-乙腈-甲酸-水(30:10:1:59)为流动相;检测波长为286nm。
理论板数按丹酚酸B峰计算应不低于2000。
3.3.4.3 对照品溶液的制备:精密称取丹酚酸B对照品适量,加水制成每1ml含10µg的溶液,即得。
3.3.4.4 供试品溶液的制备:取本品5g,研细,取约0.2g,精密称定,置50ml量瓶中,加水适量,超声处理(功率250W,频率33kHz)20分钟,放冷,加水至刻度,摇匀,滤过,精密量取续滤液1ml,置25ml量瓶中,加水至刻度,摇匀,滤过,取续滤液,即得。
3.3.4.5 测定法:分别精密吸取对照品溶液与供试品溶液各20µl,注入液相色谱仪,测定,即得。
丹参药材质量标准草案

丹参药材质量标准草案丹参拼音:Danshen拉丁文:Radix Salviae Miltiorrhizae本品为唇形科植物丹参Salvia miltiorrhiza Bge.的干燥根及根茎。
春、秋季采挖,以秋季采挖质量较好。
栽培品于种植第二、三年秋季采挖,除去地上部分及须根,将根摊开曝晒,晒至五、六成干时,集中堆放2~3天,经发热出汗、内变紫红色后,再摊晒干透为止。
【性状】根1至数条,圆柱形或圆锥形,常稍弯曲,并有分枝,长10~20cm,直径0.2~lcm。
表面砖红色或棕红色,粗糙,有不规则纵沟或纵皱纹及须根痕;老根栓皮灰褐色或棕褐色,多呈鳞片状剥落,露出棕红色新栓皮,有时皮部开裂,露出白色木部;根头部粗大,有时残留茎基。
质硬脆,易折断,折断面角质样或纤维性,皮部暗红棕色,木部导管束黄白色,放射状排列。
气微香,味淡、微苦涩。
饮片;呈不规则圆形的横切片,直径4~10mm,厚1~2mm,边缘呈波状凸凹,切断面皮部暗红棕色,木部的导管束呈黄白色,呈放射状排列,有多数裂隙。
【显微鉴别】根横切面:木栓层为数列木栓细胞,大多含橙色或淡紫棕色物;有时可见落皮层。
皮层窄。
韧皮部宽广,筛管群明显,颓废筛管群呈横条状。
形成层成环。
木质部射线甚宽;导管束作2~3歧状径向排列,近中心导管较少,向外渐多,常单个或2~12个径向或切向相接,后者与木薄壁组织间隔排成层状;木纤维发达,多分布于导管周围。
少数根的皮层及韧皮部有厚壁组织(纤维或石细胞);栽培品(四川)皮层和韧皮部一般无纤维或石细胞,导管束多,导管稀疏,木纤维少。
丹参粉末1. 石细胞类圆形、类长方形、类梭形或不规则形,边缘不平整,壁较厚,有的胞腔含棕色物。
2. 韧皮纤维梭形,壁略厚,孔沟明显,有的可见纹孔。
3. 网纹导管分子长梭形,末端斜尖,壁增厚不均匀,网孔狭细,穿孔多位于侧壁。
【理化鉴别】(1)取本品粉末5g,加水50ml,煎煮15~20分钟,放冷,滤过,滤液置水浴上浓缩至黏稠状,放冷后,加乙醇3~5ml使溶解,滤过,取滤液数滴,点于滤纸条上,干后,置紫外光灯(365nm)下观察,显亮蓝灰色荧光。
丹参注射液标准

丹参注射液标准
丹参注射液是一种中药注射剂,主要成分为丹参素和丹参酮,具有活血化瘀、抗氧化、抗炎等功效。
为确保丹参注射液的质量和安全性,制定了以下标准:
1. 质量标准:丹参注射液的外观应为棕红色透明液体,不得有沉淀和异物。
药液的pH值应在5.5 ~ 7.5之间,密度应在1.06 ~
1.08g/mL之间。
丹参酮含量应在0.3 ~ 0.8mg/mL之间。
2. 检测方法:采用高效液相色谱法(HPLC)测定丹参酮的含量。
药液的pH值可以使用酸碱滴定法或pH计进行测定。
3. 生产要求:生产丹参注射液应符合药品生产质量管理规范要求,采用先进的生产工艺和设备,严格执行生产工艺流程和质量控制标准。
4. 储存要求:丹参注射液应存放在阴凉、干燥、通风的地方,避免阳光直射和高温、高湿环境。
药液的储存温度应在2 ~ 8℃之间,避免冻结。
以上标准为保证丹参注射液的质量和安全性提供了依据,同时也为医护人员在使用丹参注射液时提供了参考。
- 1 -。
中药丹参及其制剂的质量控制方法初探

中药丹参及其制剂的质量控制方法初探作者:赵小民来源:《中国实用医药》2010年第34期【摘要】丹参及其制剂对许多疾病如心脑血管疾病、癌症、抗衰老、中风、肝炎等有良好治疗效果。
中药丹参及其制剂的质量控制方法也多种多样。
【关键词】中药丹参;制剂;质量控制方法丹参为常用中药,来源于唇形科植物丹参的干燥根及根茎[1],丹参制剂约有100多种,有些制剂的有效成份是丹参的水溶性成分,有些制剂的有效成分是丹参的脂溶性成分。
测定方法多样化,主要包括:比色法、紫外分光光度法、薄层扫描法、HPLC法、气相色谱法、可见分光光度法、薄层层析-紫外分光光度法等,现就其几种研究方法介绍如下。
1 比色法此方法多用于丹参及其制剂中水溶性总酚酸类和脂溶性总丹参酮类的测定,具有快速、准确等优点。
袁璐等[1]采用比色-可见分光光度法对丹参及复方丹参注射液中有效成分进行测定、薄层扫描测定,并建立了儿茶酚类物质总量测定法,发现市售产品有效成分含量差异很大。
注射液中鞣质对红细胞及血浆蛋白的相关性研究证实,市售产品均含大量鞣质,能使人红细胞及血浆蛋白变性,会导致毒副作用。
李广胜等[2]采用比色法对丹参口服液中总酚酸性成分进行含量测定,此方法回收率为(98.84±0.86)%,RSD为0.87%。
该方法简便快速,准确度高,重现性好,可作为丹参口服液的质量控制标准。
2 紫外分光光度法主要利用丹参中的水溶性酚酸类在紫外区(281±3)nm波长处有最大吸收,脂溶性隐丹参酮在442~452 nm波长处有最大吸收的特性,通过测定丹参药材和制剂的吸收值来控制质量。
多用于丹参液体制剂有效成分的含量测定,具有操作简便,结果准确,重现性好等优点。
何建国[3]等采用一阶导数光谱法测定复方丹参注射液中原儿茶醛的含量,测定波长为268 nm。
结果平均回收率为98.1%,RSD为1.23%。
该法操作简便,易行,具有实用性。
许腊英[4]等采用紫外分光光度法测定参芪胶囊中丹参素含量。
丹参质量标准

1.目的:通过制定丹参质量标准,为采购和检验提供依据,以确保丹参的质量。
2.范围:适用于丹参的质量控制。
3.责任:质量管理部、生产技术部、储运部、采购部。
4.内容:4.1基本信息4.1.1物料名称品名:丹参汉语拼音:Danshen拉丁名:SALVIAE MILTIORRHIZAE RADIX ET RHIZOMA4.1.2物料代码:Z334.1.3质量标准依据:《中国药典》2015年版一部(第76~77页)、四部通则0502、2301、0832、2302、2331、2321、05124.1.4批准供应商:见质量管理部批准的供应商清单4.2取样及检验操作规程编号物料、中间产品(待包装产品)、成品取样标准操作程序 2S-307703 丹参检验标准操作规程 2S-3375054.3定性和定量的限度要求4.3.1法定质量标准【来源】本品为唇形科植物丹参salvia miltiorrhiza Bge.的干燥根和根茎。
春、秋二季采挖,除去泥沙,干燥。
【性状】本品根茎短粗,顶端有时残留茎基。
根数条,长圆柱形,略弯曲,有的分枝并具须状细根,长10~20cm,直径0.3~1cm。
表面棕红色或暗棕红色,粗糙,具纵皱纹。
老根外皮疏松,多显紫棕色,常呈鳞片状剥落。
质硬而脆,断面疏松,有裂隙或略平整而致密,皮部棕红色,木部灰黄色或紫褐色,导管束黄白色,呈放射状排列。
气微,味微苦涩。
【鉴别】(1)本品粉末红棕色。
石细胞类圆形、类三角形、类长方形或不规则形,也有延长呈纤维状,边缘不平整,直径14~70μm,长可达257μm,孔沟明显,有的胞腔内含黄棕色物。
木纤维多为纤维管胞,长梭形,末端斜尖或钝圆,直径12~27μm,具缘纹孔点状,纹孔斜裂缝状或十字形,孔沟稀疏。
网纹导管和具缘纹孔导管直径11~60μm。
(2)取本品粉末1g,加乙醇5ml,超声处理15分钟,离心,取上清液作为供试品溶液。
另取丹参对照药材1g,同法制成对照药材溶液。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
制药GMP管理文件
一、目的:制定薄丹参的内控标准,规范公司丹参的采购与使用
二、适用范围:适用于丹参的采购与验收
三、责任者:生产部、检验员、仓库保管员
四、正文:
丹参
本品为唇形科植物丹参的干燥根及根茎。
春秋二季采挖,出去泥沙,干燥。
【性状】本品根茎短粗,顶端有时残留茎基。
根数条,长圆柱形,略弯曲,有的分枝并具须状细根,长10~20cm,直径O.3~lcm。
表面棕红色或暗棕红色,粗糙,具纵皱纹。
老根外皮疏松,多显紫棕色,常呈鳞片状剥落;质硬而脆,断面疏松,有裂隙或略平整而致密,皮部棕红色,木部灰黄色或紫褐色,导管束黄白色,呈放射状排列。
气微,味微苦涩。
栽培品较粗壮,直径O.5~1.5cm。
表面红棕色,具纵皱,外皮紧贴不易剥落。
质坚实,断面较平整,略呈角质样。
【鉴别】(1)取本品粉末lg,加乙醚5ml,振摇,放置1小时,滤过,滤液挥干,残渣加乙酸乙酯lml使溶解,作为供试品溶液。
另取丹参对照药材1g,同法制成对照药材溶液。
再取丹参酮IA对照品,加醋酸乙酯制
成每1ml含2mg的溶液,作为对照品溶液。
照薄层色谱法试验,吸取上述三种溶液各5μl,分别点于同一硅胶G薄层板上,以苯-乙酸乙酯(19:1)为展开剂,展开,取出,晾干。
供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的斑点;在与对照品色谱相应的位置上,显相同的暗红色斑点。
(2)取本品粉末0、2克,加75%甲醇25 ml,加热回流1小时,滤过,滤液浓缩至1 ml作为供试品溶液。
另取丹酚酸B对照品,加75%甲醇醇制成每1 ml含2毫克的溶液,作为对照品溶液。
照薄层色谱法试验,吸取上述两种溶液各5微升,分别点于同一硅胶GF254薄层板上,以甲苯-三氯甲烷-乙酸乙酯-甲醇-甲酸(2:3:4:0、5:2)为展开剂,展开,取出,晾干,置紫外光灯(254纳米)下检视。
供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的斑点。
【检查】水分照水分测定法测定,不得过13.0%。
总灰分不得过10.0%
酸不溶性灰分不得过3.0%。
【浸出物】水溶性浸出物照水溶性浸出物测定法项下的冷浸法测定,不得少于35.0%。
醇溶性浸出物照醇溶性浸出物测定法项下的热浸法测定,用乙
醇作溶剂,不得少于15.0%。
【含量测定】丹参酮ⅡA 照高校液相色谱法测定。
色谱条件与系统适用性试验用十八烷基硅烷键合硅胶为填充剂,甲醇-水(75:25)
为流动相;检测波长为270nm.理论板数按丹参酮ⅡA峰计算应不低于2000.
对照品溶液的制备精密称取丹参酮ⅡA对照品10mg,置50ml棕色量瓶中,加甲1ml中含丹参酮ⅡA16ug)。
供试品溶液的制备取本品粉末0.3g,精密称定,置具塞锥形瓶中,精密加入甲醇50ml,称定重量,加热回流1小时,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。
测定法分别精密吸取对照品溶液与供试品溶液各5ul,注入液相色谱仪,测定,即得。
本品含丹参酮ⅡA不得少于0.20%。
丹酚酸B 照高校液相色谱法测定。
色谱条件与系统适用性试验以十八烷基硅烷键合硅胶为填充剂;以甲醇-乙腈-甲酸-水(30:10:1:59)为流动相;检测波长为286nm。
理论板数按丹酚酸B峰计算应不低于2000.
对照品溶液的制备精密称取丹酚酸B对照品适量,加75%甲醇制成每1ml含0.14mg的溶液,即得。
供试品溶液的制备取本品粉末约0.2g,精密称定,置具塞锥形瓶中,精密加入75%甲醇50ml,称定重量,加热回流1小时,取出,放冷,再称定重量,用75%甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。
测定法分别精密吸取对照品溶液与供试品溶液各10ul,注入液相色谱仪,测定,即得。
本品按干燥品计算,含丹酚酸B不得少于3.0%。
