苯甲醇,苯甲酸,水杨酸的毛细管电泳分离
毛细管电泳仪分离测定雪碧 化学实验教学中心

饮料中各组分的分离测定色谱科学自从1903年俄国的茨维特发明了液固柱色谱之后,已有近100年的历史。
但是在20世纪末的20年间,以前所未有的速度发展,特别是进人生命科学。
材料科学和信息科学时代,对分离分析提出越来越高的要求。
常见的色谱可分为气相色谱、液相色谱、毛细管电泳。
气相色谱法(GC)分离效率、选择性、灵敏度都很高,但是它只适用于热稳定性好、易挥发的物质。
高效液相色谱法(HPLC)不受热稳定性及挥发性的限制,可以分析热稳定性差。
难挥发的物质,但是和GC相比,缺乏灵敏的通用型检测器,实验中需消耗大量的有机溶剂,特别是对于大分子物质因其分子扩散系数小、传质阻力大,使柱效率大大降低,以至于难以分离分子量大于2000的物质。
经典电泳技术和色谱理论相结合,利用毛细管电泳的分离模式多样化,毛细管内壁的修饰方法及流动的缓冲液中的添加剂的不同,以及新检测技术的发展,使毛细管电泳的应用非常广泛。
可分离多种阴阳离子、生物大分子等,利用多种手性选择剂,具有高分离能力的毛细管电泳在手性分离中极为重要。
饮料中的成份相对比较复杂,其中各种不同的物质选择不同的色谱分离检测方法至关重要。
本实验选取饮料中不同物质分别采用气相色谱、液相色谱、毛细管电泳等方法分离检测。
通过实验对比,对各类色谱进行较深入了解。
气相色谱仪分离测定奶茶中胆固醇1 实验目的(1)了解外标法定量的基本原理及操作步骤,掌握其计算方法及注意事项。
(2)了解奶茶的前处理过程,掌握仪器的基本操作。
2 实验原理外标法也叫标准曲线法,适用于在成分很复杂的样品中对某一种或几种组分定量,常用于常规分析。
外标法首先要配置一系列浓度的标准溶液,分别测定峰面积,以峰面积对浓度作图(下图):A i~c i 关系曲线A i=fC i+a(a是常数),用线性回归法求出f 和a,代入未知样的峰面积求出未知样的组分含量。
在用外标法定量时,要注意进样量一定要标准不能有误差,否则会导致标准曲线上的点偏高或偏低,影响结果的准确性。
1掌握毛细管电泳法的基本原理

毛细管电泳法测定水杨酸 的含量
实验目的 1.掌握毛细管电泳法的基本原理、结构与使用方 .掌握毛细管电泳法的基本原理、 法。 2.掌握紫外吸收光谱检测方法。 .掌握紫外吸收光谱检测方法。 3.测定阿司匹林与水杨酸。 .测定阿司匹林与毛细管电泳又称高效毛细管电泳 High Performance Capillary Electrophoresis, HPCE) 是一种仪器分析方法。通 是一种仪器分析方法。 过施加10-40kV的高电压于充有缓冲液的极细毛细管 的高电压于充有缓冲液的极细毛细管, 过施加10-40kV的高电压于充有缓冲液的极细毛细管,对液 体中离子或荷电粒子进行高效、快速的分离。现在, HPCE已广泛应用于氨基酸 、 蛋白质 、 多肽 、 低聚核苷酸 、 已广泛应用于氨基酸、 已广泛应用于氨基酸 蛋白质、 多肽、 低聚核苷酸、 DNA等生物分子分离分析, 药物分析, 临床分析, 无机离 等生物分子分离分析, 等生物分子分离分析 药物分析,临床分析, 子分析,有机分子分析, 子分析 , 有机分子分析 , 糖和低聚糖分析及高聚物和粒子 的分离分析。人类基因组工程中DNA的分离是用毛细管电 的分离分析 。人类基因组工程中 的分离是用毛细管电 泳仪进行的。 泳仪进行的。
数据处理
从色谱工作站打开保存的文件,通过调节参数表里的满屏量程和满屏 时间,把谱图调到最佳。当需要改动起始峰宽水平时,还要按在处理 这个图标。把谱图调到最佳后,点击定量组分,出现一张表格。选中 套峰时间下的一个空格,再用鼠标右键点击需要研究的峰的内部,弹 出一个菜单,点击自动填写“定量组分”表中套峰时间。然后输进样 品的浓度,点击定量方法,点击计算校正因子,点击屏幕上的定量计 算图标,点击定量结果表,出现校正因子和峰面积,记录校正因子和 峰面积。点击定量结果,在定量结果表格里输入组分名称、浓度、平 均校正因子、平均峰面积。点击当前表存档,重复上述操作,存入七 档数据。然后点击定量方法,点击工作曲线中的计算,再点击显示。 显示出峰面积—浓度的线性关系图和峰面积—浓度的方程。然后把标 准曲线复制到word文档里。 将样品中水杨酸峰面积的平均值代入峰面积—浓度方程,求得水杨酸 的浓度。
高效毛细管电泳实验

高效毛细管电泳实验一、实验目的1. 进一步理解毛细管电泳的基本原理;2. 熟悉毛细管电泳仪器的构成;3. 了解影响毛细管电泳分离的主要操作参数。
二、实验原理1.电泳淌度毛细管电泳(CE )是以电渗流 (EOF)为驱动力,以毛细管为分离通道,依据样品中组分之间淌度和分配行为上的差异而实现分离的一种液相微分离技术。
离子在自由溶液中的迁移速率可以表示为:ν = μE (1)r 6q πημ= (2)式中ν是离子迁移速率,μ为电泳淌度,E 为电场强度。
η为介质粘度,r 为离子的流体动力学半径,q 为荷电量。
因此,离子的电泳淌度与其荷电量呈正比,与其半径及介质粘度呈反比。
2.电渗流和电渗淌度电渗流(EOF )指毛细管内壁表面电荷所引起的管内液体的整体流动,来源于外加电场对管壁溶液双电层的作用。
在水溶液中多数固体表面根据材料性质的不同带有过剩的负电荷或正电荷。
就石英毛细管而言,表面的硅羟基在pH 大于3以后就发生明显的解离,使表面带有负电荷。
为了达到电荷平衡,溶液中的正离子就会聚集在表面附近,从而形成所谓双电层,如图1所示。
这样,双电层与管壁之间就会产生一个电位差,叫做Zeta 电势。
但毛细管两端施加一个电压时,组成扩散层的阳离子被吸引而向负极移动。
由于这些离子是溶剂化的,故将拖动毛细管中的体相溶液一起向负极运动,这便形成了电渗流。
电渗流的大小可用速率和淌度来表示:()E EOF ηεξν/=(3) 或者 ηεξμ/=EOF (4)式中νEOF 为电渗流速率,μEOF 为电渗淌度,ξ为Zeta 电势,ε为介电常数。
3.毛细管电泳的分离模式CE 有6种常用的分离模式,其中毛细管区带电泳(CZE )、胶束电动毛细管色谱(MEKC )和毛细管电色谱(CEC )最为常用。
本实验的内容为CZE 。
4.毛细管电泳的基本参数CE 中的分析参数可以用色谱中类似的参数来描述,比如与色谱保留时间相对应的有迁移时间,定义为一种物质从进样口迁移到检测点所用的时间,迁移速率(ν)则是迁移距离(l ,即被分析物质从进样口迁移到检测点所经过的距离,又称毛细管的有效长度)与迁移时间(t )之比:t l=ν (5)因为电场强度等于施加电压(V)与毛细管长度(L)之比:L VE = (6)就CE 的最简单的模式—毛细管区带电泳(CZE )而言,结合式(1),可得:tV lL tE l a ==μ (7)在毛细管区带电泳(CZE )条件下测得的淌度是电泳淌度与电渗流淌度的矢量和,我们称之为表观淌度μa ,即:EOF e a μμμ+= (8)实验中可以采用一种中性化合物,如二甲亚砜或丙酮等,来单独测定电渗流淌度,然后求得被分析物的有效淌度。
毛细管电泳法的原理和应用

毛细管电泳法的原理和应用1. 原理毛细管电泳法(Capillary Electrophoresis,CE)是一种基于电场作用下离子在毛细管中迁移的分离技术。
其原理基于离子在电场中带电迁移速度与其电荷量、电场强度以及溶液介质的性质相关的事实。
毛细管电泳法通过在毛细管中施加电场,利用分子的电荷差异和大小来实现分离物质的目的。
1.1 分离机制毛细管电泳法的分离机制主要包括以下几个步骤:1.进样:待测样品经过电泳柱,在毛细管中形成等电流聚焦带。
2.分离:应用电场,待测物质开始在毛细管内移动,根据分子的电荷和尺寸差异,分离成不同的带电物质。
3.检测:通过检测器对不同迁移距离的带电物质进行监测和记录。
1.2 主要影响因素影响毛细管电泳分离效果的主要因素包括:•电场强度:电场强度越高,迁移速度越快,但也容易产生电泳柱壁的热效应。
•pH 值:溶液的pH 值会影响离子的电荷状态,从而影响其迁移速度。
•温度:温度的变化会影响毛细管电泳的分离效果,通常需要控制温度来确保数据的可靠性。
2. 应用领域毛细管电泳法在许多领域中得到了广泛的应用,下面列举了其中的几个主要应用领域:2.1 生物医药领域•药物分析:毛细管电泳法可以用于药物代谢产物分析、毒性物质筛选和药物质量分析等。
•蛋白质分析:毛细管电泳法对于蛋白质的分析具有高分辨率和高灵敏度的特点,被广泛应用于蛋白质药物的质量控制和结构研究等方面。
2.2 环境监测领域•水质监测:毛细管电泳法可以用于水质中有机和无机物质的分析,可用于环境污染监测和水质安全评价等。
•大气污染物监测:毛细管电泳法可以用于大气中挥发性有机物质(VOCs)和颗粒物的分析,对于大气污染物的来源和分布有重要作用。
2.3 食品安全领域•农药残留分析:毛细管电泳法可以用于食品中农药残留的检测,对于保证食品安全和农产品质量具有重要意义。
•食品添加剂分析:毛细管电泳法可用于食品添加剂的定性和定量分析,用于食品质量控制和标签声明的验证等。
非水体系毛细管电泳_紫外检测法测定苯甲酸和苯甲醛_李利军

非水体系毛细管电泳-紫外检测法测定苯甲酸和苯甲醛李利军X1,黄文艺2,程昊2,孔红星1,吴健玲2(1.广西工学院生物与化学工程系,柳州545006; 2.广西大学化学与化学工程学院,南宁530005)摘要:建立了用非水相体系高效毛细管电泳-紫外检测法同时测定苯甲酸和苯甲醛的新方法,考察了运行电压、非水相介质和电解质等因素的影响,在25e下,以V(乙腈)B V(碳酸丙烯酯)=1B1的混合液为溶剂,缓冲体系中含15mmol P L十六烷基三甲基溴化铵体积分数1%乙酸,重力进样30s,运行电压20kV,毛细管总长45cm有效长度30c m,<75L m,检测波长285nm。
苯甲酸线性范围为5~40L g P mL,线性方程为:y=13.473Q+13.336,相关系数r=0.9985,检出限为0.92L g P mL,RSD为318%。
苯甲醛的线性范围75~1125L g P mL线性方程为:y=512449Q+564101,相关系数r=019997,检出限为15160L g P m L,RSD为315%。
已用于经空气氧化后的苯甲醛中苯甲酸和苯甲醛的测定。
关键词:苯甲酸;苯甲醛;非水相体系;毛细管电泳;紫外检测中图分类号:O657.8文献标识码:A文章编号:1000-0720(2006)07-056-04苯甲醛是一种广泛应用于合成染料、香料和药物等精细化学品的中间体。
在合成中发挥着越来越重要的作用。
在苯甲醛的合成过程中,通常会有少量的副产物苯甲酸生成。
测定合成过程中苯甲酸和苯甲醛的量,据此来选择适当的投料比,尽量避免副产物苯甲酸的生成,以获得满意的苯甲醛产率。
因此,建立能同时快速、准确、简便测定苯甲醛和苯甲酸的方法具有一定实际意义。
测定苯甲醛的方法主要有气相色谱法[1]、分光光度法[2]、极谱法[3]和荧光光度法[4]等。
这些方法大多数采用将苯甲醛衍生后间接进行测定,因此样品处理较繁琐。
而且由于苯甲醛不溶于水而苯甲酸溶于水,能同时对苯甲醛和苯甲酸进行测定的方法较少。
毛细管电泳法分离测定食品中山梨酸、苯甲酸、糖精

毛细管电泳法分离测定食品中山梨酸、苯甲酸、糖精胡美珍;王文铮;张燕琴【摘要】采用毛细管电泳-紫外检测法,考察了波长,电压,缓冲试剂、浓度、pH对山梨酸、苯甲酸、糖精分离的影响,得到了优化的实验条件.以硼砂20mmol/L(pH=7.5)为运行缓冲溶液,20kV为分离电压,检测波长为230nm的电泳条件下,进样时间为10s,山梨酸、苯甲酸、糖精可在12min内实现分离.山梨酸在5mg/L~50mg/L,苯甲酸在5mg/L~50mg/L,糖精在15mg/L~150mg/L范围内呈良好线性关系,迁移速度、峰面积相对标准偏差均小于4.5%,(n=5).用上述方法对实际样品进行测定,回收率在95%以上.【期刊名称】《上海师范大学学报(自然科学版)》【年(卷),期】2004(033)003【总页数】4页(P63-66)【关键词】毛细管电泳-紫外检测法;添加剂;山梨酸;苯甲酸;糖精【作者】胡美珍;王文铮;张燕琴【作者单位】上海师范大学,生命与环境科学学院,上海,200234;上海师范大学,生命与环境科学学院,上海,200234;上海师范大学,生命与环境科学学院,上海,200234【正文语种】中文【中图分类】O6570 引言毛细管电泳(简称CE),是80年代初发展起来的一种新型高效的分离技术[1].它具有高效、快速、样品用量少、测定成本低等优点,自其产生以来,迅速渗透到与分析化学相关的各个学科.如:医药、环境、食品等各个领域.苯甲酸、山梨酸、糖精是常用的食品添加剂.国家规定限量使用.所以测定食品中苯甲酸、山梨酸、糖精的含量十分重要.目前上述三种添加剂,大都采用紫外分光光度法、薄层层析法、气相色谱法和高效液相色谱法等[2~4].本文用CE法分离测定上述三种添加剂,方法简便,灵敏度和重现性均符合食品分析的要求,样品前处理测定步骤较紫外光度法、薄层层析法简单,测定成本较HPLC低,有很好的实用价值.1 实验部分1.1 主要仪器与试剂仪器高效毛细管电泳仪、ACS2000紫外检测器(北京彩陆科学仪器有限公司)(中科院研究生院应用化学研究所); 毛细管总长度:60cm, 有效长度:54cm, 直径:50μm; CQ50超声波清洗器(上海超声波仪器厂);pHs-3C 型酸度计(上海华侨仪表厂);过滤器Ø25(上海市医工院);0.22μm 滤膜(上海兴亚净化材料厂);注射器5mL试剂硼砂(优级纯)、磷酸二氢钠、磷酸氢二钠、三(羟甲基)氨基甲烷(简称Tris)、山梨酸、苯甲酸、糖精均为分析纯,样品为汽水、番茄沙司,蜜饯,水为二次蒸馏水.1.2 实验方法1.2.1 标准样品的制备参照国标法,准确称取山梨酸、苯甲酸、糖精.分别溶解、定容,使其质量浓度均为1.0mg/mL.以0.22μm滤膜过滤备用.1.2.2 样品的制备汽水,经超声波超声,除去二氧化碳,0.22μm滤膜过滤,待用.番茄沙司、蜜饯:准确称取2g左右样品置于具塞小量筒中,加H3PO4数滴,准确加入乙醚10mL,连同量筒称其总量,猛烈振摇2min,再次称重,如重量减少,加入乙醚补充至原有重量,混匀.取乙醚5mL,置于烧杯中,经40℃水浴加热,将乙醚挥发后,用硼砂缓冲液定容至10 mL.经0.22μm滤膜过滤,待用.1.2.3 电泳条件以硼砂20mmol/L(pH=7.5)为电泳缓冲液,在20kV恒压下进行电泳分离,在230nm波长处检测,电动进样,进样时间10s.毛细管使用前用0.10mol/L的NaOH,水和电泳缓冲液分别冲洗30min.每次电泳后,用上述溶液各冲洗2min.2 结果与讨论2.1 测定波长的选择据有关资料[3,4]报道苯甲酸的最大吸收波长为227nm,山梨酸为250nm,糖精为207nm,综合考虑以230nm为测定波长.2.2 分离电压的选择分别配制山梨酸、苯甲酸、糖精浓度均为10mg/L的混合标准溶液.在波长为230nm,进样时间为10s,缓冲液为硼砂30mmol/L(pH=7.5)的电泳条件下,改变电压(10~25kV),并观察分离情况.结果表明,电压在10~20kV范围内各组分的迁移时间随着分离电压增高,迁移时间减小,峰高增大,但分离度有所降低.电压增高,电流增大,产生焦耳热,使谱线变宽.综合考虑,实验选用20kV作为分离电压.2.3 缓冲试剂的选择分别配制浓度均为30mmol/L的硼砂、磷酸体系(磷酸二氢钠和磷酸氢二钠混合液)、Tris的缓冲体系,调节pH到7.5,进行试验.用山梨酸、苯甲酸、糖精浓度均为10mg/L的混合标准溶液试验.电泳条件:波长为230nm,进样时间为10s,电压20kV.结果表明,山梨酸、苯甲酸、糖精在在硼砂体系中分离情况最好,选择硼砂体系作为缓冲体系.2.4 缓冲液浓度选择以硼砂为缓冲液,分别配制20,30,40mmol/L硼砂溶液,pH均调节为7.5,按上述电泳条件进行.结果表明,硼砂浓度为20mmol/L时,山梨酸、苯甲酸、糖精可在12min内得到很好的分离,峰面积、峰高和峰形较30 mmol/L,40 mmol/L好,故选择20 mmol/L硼砂作为运行缓冲溶液.2.5 缓冲液pH的选择以20mmol/L硼砂溶液为缓冲介质,分别调节溶液的pH为7.5,8.0,8.5,9.0.在上述试验确定的条件下,观察上述3种组分的迁移行为,实验结果表明在pH为7.5时山梨酸、苯甲酸、糖精迁移时间差别最大,而且其中糖精的峰高较其他pH值时高,故缓冲液pH选择7.5.2.6 优化条件下的电泳图配制30 mg/L的山梨酸、30 mg/L的苯甲酸和90 mg/L的糖精混合标准溶液,按上述确定的分离条件进行,分离情况,见图1.2.7 工作曲线及检测限在上述优化条件下,对一系列山梨酸、苯甲酸、糖精的标准混合样品进行分析测定,测定其峰面积与浓度的关系,所得山梨酸、苯甲酸、糖精的线性范围相关系数及检测限.结果见表1.1-山梨酸;2-苯甲酸;3-糖精图1 混合标准液电泳图表 1 山梨酸、苯甲酸、糖精的线性范围及检测限被测物线性范围mg/L相关系数γ检测限mg/L山梨酸5.0^500. 99583.0苯甲酸5.0^500.99504.0糖精15^1500.99535.0*检测限按3倍噪声计算2.8 精密度试验配制浓度分别为30 mg/L的山梨酸、苯甲酸和90 mg/L的糖精的标准混合液平行进样5次,测得山梨酸迁移时间的RSD为1.9%,峰面积的RSD为4.5%;苯甲酸的迁移时间的RSD为2.2%,峰面积的RSD为4.2%;糖精的迁移时间的RSD 为3.8%,峰面积的RSD为3.3%.2.9 实际样品的测定取汽水、番茄沙司、蜜饯,经预处理后,按上述确定的电泳条件进行分离测定,结果见表2:表 2 实际样品测定结果(n=3)样品名称组分实际含量 (mg/L)添加量(mg/L)测得量(mg/L)回收率(%)汽水苯甲酸81.4440119.495.0番茄沙司苯甲酸82.2080169.4109山梨酸68.3580149.2101蜜饯苯甲酸107.080183.295.0糖精104.040145.11032.10 结论本法选用20mmol/L(pH=7.5)的硼砂作为缓冲溶液,20kV为采样和分离电压,10s进样,检测波长为230nm的电泳条件下,,山梨酸、苯甲酸、糖精可在12min内得到分离.本法线性关系良好(R>0.995),迁移时间和峰面积相对标准偏差均小于4.5%,实际样品测定的回收率在95%以上,方法简单、快速,相对于其他分析方法,具有预处理简便,检测成本低等特点.由此可见,毛细管电泳法在食品分析领域有良好的应用前景.参考文献:[1] 陈义. 毛细管电泳技术及应用[M]. 北京:化学工业出版社,2000.[2] 胡慰望,谢笔钧.食品化学[M].北京:科学出版社,1992.[3] 国家技术监督局. 中华人民共和国国家标准[S].1996.[4] 黄伟坤.食品检验与分析[M]. 北京:中国轻工业出版社,1993.。
应用毛细管气相色谱技术测定化妆品中防腐剂苯甲醇含量

应用毛细管气相色谱技术测定化妆品中防腐剂苯甲醇含量周耀斌;彭亚锋;雷涛;严罗美
【期刊名称】《香料香精化妆品》
【年(卷),期】2009(000)004
【摘要】采用超声抽提法对化妆品中的苯甲醇进行了气相色谱测定的研究,建立了一种简单、快速、准确测定化妆品中苯甲醇的测定方法.结果表明,该方法能够有效地提取化妆品中的苯甲醇,并可对其进行测定.苯甲醇加标回收率为99.08%~104.47%(n=15),相对标准偏差0.971%~3.53%(n=15),检出限为0.005%.
【总页数】3页(P9-10,13)
【作者】周耀斌;彭亚锋;雷涛;严罗美
【作者单位】上海市质量监督检验技术研究院/国家食品质量监督检验中心上海上海 200233;上海市质量监督检验技术研究院/国家食品质量监督检验中心上海上海 200233;上海市质量监督检验技术研究院/国家食品质量监督检验中心上海上海 200233;上海出入境检验检疫局上海 200123
【正文语种】中文
【中图分类】TQ65
【相关文献】
1.毛细管气相色谱法快速测定化妆品中4种对羟基苯甲酸酯防腐剂 [J], 迪丽努尔·马立克;龙萍;李琛琛;刘虎威
2.GC 法测定盐酸特比萘芬乳膏中防腐剂苯甲醇的含量 [J], 钟莉银;刘红宁;朱卫丰;
王森;沈冬冬
3.胶束电动毛细管色谱快速测定化妆品中的防腐剂 [J], 王萍;丁晓静
4.气相色谱法测定化妆品中的防腐剂苯甲醇和苯氧基乙醇 [J], 刘青;陈文锐;吴宏中;林晓棠
5.高效毛细管电泳法同时分离测定化妆品中7种防腐剂 [J], 张帅; 高立娣; 梁辉; 秦世丽; 蒋春红; 段圣村; 徐蕾; 林肖同; 王媛媛
因版权原因,仅展示原文概要,查看原文内容请购买。
毛细管电泳法

毛细管电泳法分离水杨酸、苯甲酸及阿司匹林中的含量测定毛细管电泳法分离水杨酸、苯甲酸及阿司匹林中的含量测定毛细管电泳又称高效毛细管电泳( High Performance Capillary Electrophoresis, HPCE) 是一种仪器分析方法。
通过施加10-40kV 的高电压于充有缓冲液的极细毛细管,对液体中离子或荷电粒子进行高效、快速的分离。
现在,HPCE 已广泛应用于氨基酸、蛋白质、多肽、低聚核苷酸、DNA 等生物分子分离分析,药物分析,临床分析,无机离子分析,有机分子分析,糖和低聚糖分析及高聚物和粒子的分离分析。
人类基因组工程中DNA 的分离是用毛细管电泳仪进行的。
毛细管电泳较高效液相色谱有较多的优点。
其中之一是仪器结构 简单(见图1)。
它包括一个高电压源,一根毛细管,紫外检测器及计算机处理数据装置。
另有两个供毛细管两端插入而又可和电源相连的缓冲液池。
high-v oltagepower supply BufferV ialBuffer V ial Detector Recording dev icecapillaryElectrode Electrode图1 CE 仪器组成示意图毛细管中的带电粒子在电场的作用下,一方面发生定向移动的电泳迁移,另一方面,由于电泳过程伴随电渗现象,粒子的运动速度还明显受到溶液电渗流速度的影响。
粒子的实际流速 V 是电泳流速度 Vep 和渗流速度 Veo 的矢量和。
即:V = Vep + Veo (1)电渗流是一种液体相对于带电的管壁移动的现象。
溶液的这一运动是由硅/水表面的Zeta 势引起的。
CE 通常采用的石英毛细管柱表面一般情况下(pH>3)带负电。
当它和溶液接触时,双电层中产生了过剩的阳离子。
高电压下这些水合阳离子向阴极迁移形成一个扁平的塞子流,如图2。
毛细管管壁的带电状态可以进行修饰,管壁吸附阴离子表面活性剂增加电渗流, 管壁吸附阳离子表面活性剂减少电渗流甚至改变电渗流的方向。
毛细管电泳法分离检测饮料中的防腐剂

毛细管电泳法分离检测饮料中的防腐剂王钰;杨思文;代语林;邓宁;王燕;何建波;朱燕舞【摘要】采用高效毛细管电泳法,同时在线分离检测对羟基苯甲酸甲酯、山梨酸钾和苯甲酸3种防腐剂.考察了运行缓冲液的浓度、pH值、分离电压、进样时间等因素对电泳分离的影响.在检测波长为230nm时,获得了3种防腐剂分离检测的最优化实验条件为:20mmol/L pH 9.2的硼砂缓冲溶液,分离电压为22kV,进样时间15s.在最优化实验条件下,3种防腐剂检测的线性相关系数均大于0.98,检出限为1.0×10-2g/kg.利用此方法检测了市售3种饮料中所含防腐剂的种类和含量,各种防腐剂的回收率在88%~102%之间.【期刊名称】《中国酿造》【年(卷),期】2014(033)004【总页数】5页(P124-128)【关键词】毛细管电泳;防腐剂;分离;检测【作者】王钰;杨思文;代语林;邓宁;王燕;何建波;朱燕舞【作者单位】合肥工业大学化学工程学院,安徽合肥230009;合肥工业大学化学工程学院,安徽合肥230009;合肥工业大学化学工程学院,安徽合肥230009;合肥工业大学化学工程学院,安徽合肥230009;合肥工业大学化学工程学院,安徽合肥230009;合肥工业大学化学工程学院,安徽合肥230009;合肥工业大学化学工程学院,安徽合肥230009【正文语种】中文【中图分类】O657.8食品是人类生存的基本物质保障,现代化的食品生产要求食品能够方便贮存和运输,防腐剂既能使食品保存期延长,也能防止食品腐败变质,因此被广泛应用于食品生产中。
但是食品防腐剂的过量使用会对人体健康造成较大的危害,伤害人体正常机能,降低人体免疫力。
我国明确规定了防腐剂使用标准,但仍然有一些商家没有按照标准合理使用防腐剂。
2007年国家质检总局对北京等13个省、直辖市96家企业生产的117种产品进行抽查,抽查中发现部分碳酸饮料中防腐剂的含量超标[1]。
毛细管电泳

2. 药物分析 analysis of pharmaceutics
3. 氨基酸分析 analysis of amino acids 4. 核酸分析及DNA测序 analysis of nucleic acids and sequence of DNA 5. 新进展及热点问题 advances and special topics
2 DL
ap ELef
2D
tR ; 色谱 : n 5.54 Y 1/ 2
2
D—扩散系数;Y1/2--半峰宽
扩散系数小的溶质分离效率高,分离生物大分子的依据。
3.分离度
R 0.177
apVLef
DL
平均
平均
ap1 ap 2
2
影响分离度的主要因素;工作电压V;毛细管有效长度与总 长度比;有效淌度差。分离度可按谱图直接由下式计算:
苯甲醇、苯甲酸、水杨酸 的毛细管电泳分离
肖艳玲、陶海升
安徽师范大学化学与材料科学学院
一、实验目的
1、掌握毛细管电泳的基本概念; 2、通过实验熟悉毛细管电泳仪的基本原理和操作; 3、了解影响毛细管电泳分离的主要操作参数。
二、基本概念
电泳:在电解质溶液中,位于电场中的带电粒子在电场力的 作用下,以不同的速度向其所带电荷相反的电极方向迁移的 现象,称为电泳。 由于不同粒子所带电荷及性质的不同,迁移速率不同,可实 现分离。利用电泳现象对某些化学或生物物质进行分离分析 的方法(技术)叫电泳法(技术)。 电泳 毛细管电泳
电渗流的速度约等于一般离子电泳速度的5~7倍; (1)可一次完成带正电粒子、带负电粒子以及中性粒子的分离; (2)改变电渗流的大小和方向可改变分离效率和选择性, 如同改变LC中的流速;在CE中,控制电渗流非常重要。
毛细管电泳法测定PTA中苯甲酸含量

2 .0
2 .0 0
2 . 5
2 .0 5
用 0 4 u 滤 膜 过滤 后 装 入 样 杯 。放 在 仪器 样 品 盘 上 , .5 m
出参 比系数 ( 积 / g K ) 和 曲线 相 关 系数 。 面 m /g
选择好仪器条件 后进 行测定 。以峰面 积为纵坐标 ,对 应 的
作者简介 : 常毓巍 (9 3 , , 1 6 一)男 山西平遥人 , 合作 民族师范高等专科学校化学 系副教授 。
表 1 标 准 曲线 制 作 序 号 1 2 3 4 5 6
加入 B A、标准溶液量 ( ) m1
相 当 于 lP A 中 B gT A含 量 ( g K ) m / g
0
0
0 .5
5 .0
1 .0
1 .0 0
1 . 5
1 .0 5
目前 。还 未见 有测 定 P A 中 的 B 含 量 的 报 道 。本 文 研 究 T A
少量稀 氨水溶解 ,并定 量转移入 1 0 ml 量瓶 中。再用 稀 00 容
氨水 稀 释 至 刻 度 。 3 5 仪器 条 件 设 置 . 毛 细管 :10 m ( 0u 内径 ) *7 mm ( 0 L) ( 长度 为 有 效 该
摘 要 : 甲酸 ( A 是 精 对 苯 二 甲酸 ( T 产 品 的 一 个 质 量 控 制 指 标 , 确 地 测 定 其 含 量 十 分 重 要 。本 文 介 苯 B ) P A) 正
绍 了用 毛 细 管 电泳 仪 测 定 P A 中 B T A含 量 的 方 法 , 标 回 收 率 为 9 —1 6 , 方 法操 作 简便 、 速 、 确 。 加 6 0% 该 快 准
将 该 溶 液 用 1 u 的过 滤膜 过 滤 入 试 剂瓶 中 ,再将 该 .2 m 试 剂瓶 放 在 超 声 波 清 洗 器 中 振荡 脱 气 。
实验8 毛细管电泳仪分离测定苯甲酸、山梨酸

正因子分别为:1.000、0.262、0.224,苯甲酸通过归一化公式可以计算出:
未知样中苯甲酸的百分含量:
0.262 22 .2364
100 % 8.40 %
1.000 59 .4683 0.262 22 .2364 0.224 18 .2952
未知样中山梨酸的百分含量:
测器上都能产生信号的样品,可用归一化法定量,其中组分 i 的质量分数按如下公式计算:
Wi
fi Ai
fi Ai
100%
式中 Ai 为组分 i 的峰面积,fi 为组分 i 的质量(或摩尔、体积)校正因子。
优点:简便、准确,特别是在进样量不容易控制时,进样量以及流速、柱温等测定条件对定量结果影响很小。
过.45μm 的滤膜过滤后,转移至进样瓶中备用。 称量 0.1g 的苯甲酸样品,用超纯水加热溶解于 100ml 的容量瓶中,再从中移取 5mL 溶液至 50ml 容量
管中定容。 称量 0.1g 的山梨酸样品,用超纯水加热溶解于 100ml 的容量瓶中,再从中移取 5mL 溶液至 50ml 容量
管中定容。
• 粒子的运动速度:由于同时存在着泳流和渗流,粒子在毛细管电介质中的运动速度应当是这两种速度的矢量 和,其迁移速率是电泳和电渗力的函数:
正离子:运动方向和电渗一致,应当最先流出;中性离子:泳流速度为 0,将随电渗而行; 负离子:因其运动方向和电渗相反,在电渗速度大于电泳速度时,它将在中性离子之后流出;
3、归一化定量的优缺点是什么?
答:优点:简便、准确,特别是在进样量不容易准确控制时,进样两的变化对定量结果的影响很小。其他操作条 件,如流速、柱温等变化对定量结果的影响也很小。
缺点:校正因子测定很麻烦。
仪器分析实验 毛细管电泳仪分离测定雪碧中的苯甲酸钠

毛细管电泳仪分离测定雪碧中的苯甲酸钠开课实验室:环境资源楼310【实验目的】1、了解毛细管电泳分离的基本原理;2、了解毛细管电泳仪(以安捷伦7100为例)的结构及基本操作;3、掌握毛细管电泳的基本定性、外标法、标准曲线定量方法。
【基本原理】•原理概述:本实验通过使用毛细管电泳法,通过外标法绘制工作曲线,对饮料中苯甲酸钠含量进行定性定量测量,得出饮料中苯甲酸钠的含量。
•电泳:定义:带电粒子在电场作用下在缓冲溶液中作定向运动的现象;分类:自由电泳、区带电泳(将样品加于载体上,并加一个电场,在电场作用下,得到良好的分离)。
•电渗:液体相对于带电的管壁移动的现象。
由于毛细管材料通常为熔融硅胶,其中的硅醇基团,是构成氢键吸附并使毛细管内电介质产生电渗流的重要原因。
在常用缓冲液pH值下,毛细管壁带负电,于是在贴近管壁的液体表面形成了一个和管壁电荷异号的偶电层。
在毛细管电泳中,电渗是指高电场作用下,偶电层中水和阳离子或质子引起流体朝负极方向运动。
电渗是毛细管电泳中最重要和最有趣的性质之一。
•粒子的运动速度:由于同时存在着泳流和渗流,粒子在毛细管电介质中的运动速度应当是这两种速度的矢量和,其迁移速率是电泳和电渗力的函数:正离子:运动方向和电渗一致,应当最先流出;中性离子:泳流速度为0,将随电渗而行;负离子:因其运动方向和电渗相反,在电渗速度大于电泳速度时,它将在中性离子之后流出;图1 不同粒子在毛细管电介质中的运动•毛细管电泳:特点:它的电泳过程在散热效率极高的毛细管内进行,故能够引入高的电场强度,从而全面改善分离质量。
优点:使用细柱子,一是减小电流,因此减少自热;二是增大散热面积(侧面积与截面积之比),加快散热;缺点:进样和检测等技术方面的麻烦与困难;检测:电泳毛细管的直径极小,产生的溶质谱带体积也极小。
通常采用的检测方法是电泳的柱上检测。
此时峰宽对迁移时间将有一定的依赖性。
移动较快的组分通过检测窗所需的时间较短,反之则较长。
毛细管电泳法测定饮料中苯甲酸和山梨酸的含量(1)

实验毛细管电泳法测定饮料中苯甲酸和山梨酸的含量一、实验目的1、掌握毛细管电泳法的基本原理2、熟悉Beckman P/ACE™ MDQ 毛细管电泳仪以及其32Karat工作站的使用方法。
3、掌握毛细管电泳法测定苯甲酸和山梨酸含量的方法。
二、实验原理苯甲酸和山梨酸是广泛使用在饮料、调味品中的防腐剂,由于此类防腐剂带有一定的负效应,甚至还有微量毒素,使用不当会给人体带来危害,应严格限制其在食品中的添加量,所以其检测工作也变得极其重要。
毛细管电泳(CE)技术是以高电场为驱动力,在细内径毛细管内荷电粒子按其淌度或(和)分配系数的不同而进行分离的一种新技术。
毛细管电泳具有高效快速、进样体积小、溶剂消耗少和样品预处理简单等优点,现已广泛地用于分离分析领域。
传统的食品添加剂的测定一般采用气相色谱(GC)和高效液相色谱(HPLC)方法,当采用GC与HPLC分析时一般都必须对样品进行复杂的前处理。
而CE与之相比,实验成本低,分析时间短,适用范围宽,可同时分离和检测多个组分。
本实验使用的毛细管区带电泳法(CZE),在毛细管中仅填充缓冲液,基于溶质组分的迁移时间或淌度的不同而分离,除了溶质组分本身的结构特点和缓冲溶液组成,不存在其他因素如聚合物网络、pH梯度的影响。
实验采用硼砂为缓冲液,待测饮料只需用缓冲液稀释,在特定的条件下,以峰高为定量依据,测定3种待测饮料中苯甲酸的含量。
三、仪器和试剂仪器:Beckman P/ACE™ MDQ 毛细管电泳仪试剂:硼砂缓冲溶液(45mmol/L)、NaOH溶液(0.1mol/L)、苯甲酸钠和山梨酸钠的混标1mg/ml。
市售3种果汁饮料四、实验步骤1、制作标准曲线分别吸取上述苯甲酸钠储备液0.5ml、1ml、2ml、3ml、4ml于50ml容量瓶中,加去离子水稀释至刻度,配置成折合苯甲酸、山梨酸浓度为10、20、40、60、80μg/ml的标准液,在上述实验条件下,测各苯甲酸的峰值,和山梨酸的峰值,绘制各标准曲线。
毛细管电泳

毛细管电泳分离混合样品
摘要:区带电泳
1、试药与仪器:苯甲酸钠、吡啶、苯酚及三者的混合样品
2、方法和结果:
2.1原理
在电场作用下,毛细管柱中出现电泳现象和电渗流现象。
毛细管壁带负电,靠外层带正电,加高压电场下形成向负极移动的电渗流,电泳是正、负电粒子自身的差速迁移,因此:
正离子:本身迁移速度+电渗流速度,最快,在负极最先流出。
中性离子:本身无电泳现象,受电渗流影响,在正离子后流出。
阴离子:电渗流速度-本身迁移速度,最慢,在负极最后流出。
在PH=5.8时,吡啶为正离子,苯酚为中性,苯甲酸钠为负离子。
本实验主要看分离电压对迁移时间、分离度的影响。
采用PH=5.8的缓冲盐,估计出峰顺序为吡啶、苯酚、苯甲酸钠。
2.2方法:254nm下分离混合样品
先采用20KV的电压分离,迁移时间太长。
改用30KV的电压分离,分离效果较好,记录出峰时间t R分别为吡啶
7.218min,苯酚10.237min,苯甲酸钠21.597min。
3、讨论:
毛细管电泳时,分离电压小会使分析时间长,进样前需用水冲洗后用缓冲液冲洗,冲洗2~3min,使毛细管柱充满缓冲溶液;设定方法时,将工作站INI 下进行初始化。
高效毛细管电泳法同时分离测定化妆品中7种防腐剂

base/naesepaeainoawnihna5mna.Theha/nbeainoahaeeesweee/naeaenaihehoaheaieainoaeaageoo5200mgZL, wnihhoee/ainoahoeonhneais( 2) o o0 0990 7 - 0 09989.The de ie hino a /nm niswe ee na ihe eaageoo1023-4030mgZL, aadiheee/aineesiaadaeddeenainoas( RSD) ooemngeainoainmeweeeaoi
张 帅4,高立娣4**,梁 辉0,秦世丽4,蒋春红9,段圣村9, 徐蕾4,林肖同4,王媛媛4
(1.齐齐哈尔大学 化学与化学工程学院,黑龙江 齐齐哈尔161006 ; 5.生工生物工程(上海)
l
,
5201611;3.
P *l
,
5200040)
摘 要:建立了毛细管电泳(CE)法同时分离测定化妆品中7种防腐剂(对轻基苯甲酸甲酯、对轻基苯甲酸乙
were idvestiqaten. The ophmg conCitiocs were fohows : aPditive : 5 mmol/Z solfonutyl-d-cyclonext iena, baoee: pH80020mmo/ZLpoospoaiebaoee, sepaeaieeo/iage: 20kV, deiehinoawaee/eagio: 280 am.Resa/isshowed ihai, aadeeiheopinma/hoadninoas, seeeapeeseeeaineeshoa/deeahhihe
Abstract: A capilla/ emetropporesis ( CE) metaoh was /tam0/ for tUo simultadeons s/ggion
毛细管电泳溶解样品所用试剂的选择解读
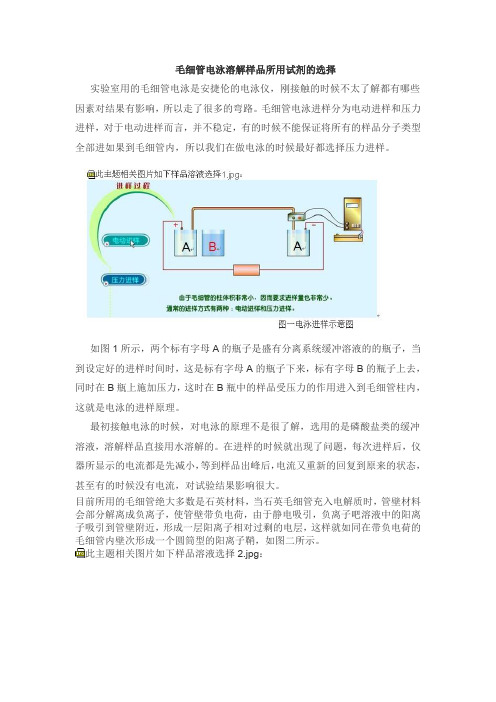
毛细管电泳溶解样品所用试剂的选择实验室用的毛细管电泳是安捷伦的电泳仪,刚接触的时候不太了解都有哪些因素对结果有影响,所以走了很多的弯路。
毛细管电泳进样分为电动进样和压力进样,对于电动进样而言,并不稳定,有的时候不能保证将所有的样品分子类型全部进如果到毛细管内,所以我们在做电泳的时候最好都选择压力进样。
如图1所示,两个标有字母A的瓶子是盛有分离系统缓冲溶液的的瓶子,当到设定好的进样时间时,这是标有字母A的瓶子下来,标有字母B的瓶子上去,同时在B瓶上施加压力,这时在B瓶中的样品受压力的作用进入到毛细管柱内,这就是电泳的进样原理。
最初接触电泳的时候,对电泳的原理不是很了解,选用的是磷酸盐类的缓冲溶液,溶解样品直接用水溶解的。
在进样的时候就出现了问题,每次进样后,仪器所显示的电流都是先减小,等到样品出峰后,电流又重新的回复到原来的状态,甚至有的时候没有电流,对试验结果影响很大。
目前所用的毛细管绝大多数是石英材料,当石英毛细管充入电解质时,管壁材料会部分解离成负离子,使管壁带负电荷,由于静电吸引,负离子吧溶液中的阳离子吸引到管壁附近,形成一层阳离子相对过剩的电层,这样就如同在带负电荷的毛细管内壁次形成一个圆筒型的阳离子鞘,如图二所示。
此主题相关图片如下样品溶液选择2.jpg:从图2中看以看出,在缓冲溶液冲洗柱子的过程中,毛细管柱内离子已经达到了一个相对平衡的状态,而当把用水溶解的样品以压力进样的方式压进毛细管柱内后,这段样品所在的溶液相对缓冲溶液而言,离子强度非常的小,甚至会出现电泳零的状态,这个时候也就相当于断流,如图3所示,仪器不再工作,因为电泳现象发生的首要条件就是能够成一个回路。
同样的道理,只用有机试剂溶解样品也存在这类似的问题,不过选择有机试剂溶解样品,有些试剂在电泳中也能解离,但效果仍然不如用缓冲溶液溶解样品。
水杨酸及其氯代物的毛细管电泳分析研究

【关键词】水杨酸;分析;药物;毛细管电泳;氯代水杨酸
【作 者】苏萍;张新祥;孙玲;李元宗;常文保
【作者单位】北京大学化学与分子工程学院
【正文语种】中 文
【中图分类】TQ463.25;O625.511
【相关文献】
1.铁(Ⅲ)催化氯代炔烃水化反应合成α-氯代甲基酮类化合物 [J], 易卫国;鄢东;吴超;兰立新
因版权原因,仅展示原文概要,查看原文内容请购买
2.高效毛细管电泳分离测定水中的乙酸和氯代乙酸 [J], 朱金花;陈兴国;刘绣华
3.高效液相色谱法同时测定反应物中的单氯代苯酐及单氯代邻苯二甲酸 [J], 袁秀伶
4.两亲性聚氯代乙醇酸-聚乙二醇-聚氯代乙醇酸三嵌段共聚晓璇;刘兴胜
5.氯代苯及氯代酚类优先污染物好氧生物降解动力学的研究 [J], 瞿福平;张晓健;何苗;顾夏声
水杨酸及其氯代物的毛细管电泳分析研究
苏萍;张新祥;孙玲;李元宗;常文保
【期刊名称】《分析科学学报》
【年(卷),期】2000(16)4
【摘 要】建立了分析水杨酸、5-氯代水杨酸、三氯水杨酸等水杨酸类化合物的毛细管区带电泳法 ( CZE)。讨论了电压、缓冲溶液的浓度和 p H值对分析结果的影响。其中缓冲溶液的 p H值对分析结果的影响最为显著。 p H<7.40时 ,三种化合物的出峰顺序为 :三氯水杨酸、5-氯代水杨酸、水杨酸 ;当 p H>7.40时 ,三种化合物的出峰顺序为 :5-氯代水杨酸、水杨酸、三氯水杨酸。水杨酸、5-氯代水杨酸、三氯水杨酸的检出限分别为 0 .1、0 .2和 0 .1μg/m L。
毛细管电泳法检测化妆品中对羟基苯甲酸酯类防腐剂

毛细管电泳法检测化妆品中对羟基苯甲酸酯类防腐剂田莉;叶能胜;谷学新;纪晓慧【期刊名称】《现代仪器与医疗》【年(卷),期】2009(015)006【摘要】采用毛细管区带电泳法同时测定化妆品中4种对羟基苯甲酸酯类防腐剂.色谱条件是:75μm×57 cm(有效长度50 cm)毛细管,电解质为25 mmol/L硼砂(pH 10.0)缓冲溶液,分离电压20 kV,温度25℃,0.5 psi进样5 s,检测波长200 nm.对羟基苯甲酸甲酯、对羟基苯甲酸乙酯、对羟基苯甲酸丙酯、对羟基苯甲酸丁酯在10 min内基线分离,10~500μg/mL范围内线性关系良好(r>0.9949),检出限为0.60~1.20μg/mL,样品加标回收率为75.5%~112.0%.【总页数】3页(P32-34)【作者】田莉;叶能胜;谷学新;纪晓慧【作者单位】首都师范大学化学系,北京,100048;首都师范大学化学系,北京,100048;首都师范大学化学系,北京,100048;首都师范大学化学系,北京,100048【正文语种】中文【相关文献】1.高效液相色谱-串联质谱法测定多种食品中7种酚类抗氧化剂和对羟基苯甲酸酯类防腐剂 [J], 张勋;刘韬;吴连鹏;高杰;康明芹;熊龙;仲文严;付瑶;邢燕燕2.毛细管电泳法检测化妆品中对羟基苯甲酸酯类防腐剂 [J], 谷学新;田莉;叶能胜;纪晓慧3.高效液相色谱法测定化妆品中对羟基苯甲酸酯类防腐剂 [J], 王晓强;胡文炬;张军4.高效液相色谱-串联质谱法同时测定酒中6种对羟基苯甲酸酯类防腐剂 [J], 赵灵芝;黄笑晨;花中霞;秦江芬;杨莉丽;王可5.化妆品中七种对羟基苯甲酸酯类防腐剂的定量测定法 [J], 王鹏;李洁;朱杰因版权原因,仅展示原文概要,查看原文内容请购买。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
苯甲醇、苯甲酸、水杨酸的毛细管电泳分离一、实验目的1.进一步理解毛细管电泳的基本原理;2.熟悉毛细管电泳仪器的构成;3.了解影响毛细管电泳分离的主要操作参数。
二、实验原理1.电泳淌度毛细管电泳(CE )是以电渗流 (EOF)为驱动力,以毛细管为分离通道,依据样品中组分之间淌度和分配行为上的差异而实现分离的一种液相微分离技术。
离子在自由溶液中的迁移速率可以表示为:ν = µE (1)式中ν是离子迁移速率,µ为电泳淌度,E 为电场强度。
对于给定的荷电量为q 的离子,淌度是其特征常数,它由离子所受到的电场力(F E )和通过介质所受到的摩擦力(F F )的平衡所决定。
F E = qE (2)对于球形离子:F F = -6πηr ν (3)式中η为介质粘度,r 为离子的流体动力学半径。
在电泳过程达到平衡时,上述两种力方向相反,大小相等:qE = -6πηr ν (4)将式(4)代入式(1),得:r 6q πηµ= (5)因此,离子的电泳淌度与其荷电量呈正比,与其半径及介质粘度呈反比。
带相反电荷的离子其电泳淌度的方向也相反。
需要指出,我们在物理化学手册中可以查到的离子淌度常数是绝对淌度,即离子带最大电量时测定并外推至无限稀释条件下所得到的数值。
在电泳实验中测定的值往往与此不同,故我们将实验值称为有效淌度(µe )。
有些物质因为绝对淌度相同而难以分离,但我们可以通过改变介质的pH 值,使离子的荷电量发生改变。
这样就可以使不同离子具有不同有效淌度,从而实现分离。
下文中所提到的电泳淌度除特别说明外,均指有效淌度。
2.电渗流和电渗淌度电渗流(EOF )是CE 中最重要的概念,指毛细管内壁表面电荷所引起的管内液体的整体流动,来源于外加电场对管壁溶液双电层的作用。
在水溶液中多数固体表面根据材料性质的不同带有过剩的负电荷或正电荷。
就石英毛细管而言,表面的硅羟基在pH 大于3以后就发生明显的解离,使表面带有负电荷。
为了达到电荷平衡,溶液中的正离子就会聚集在表面附近,从而形成所谓双电层,如图1所示。
这样,双电层与管壁之间就会产生一个电位差,叫做Zeta 电势。
但毛细管两端施加一个电压时,组成扩散层的阳离子被吸引而向负极移动。
由于这些离子是溶剂化的,故将拖动毛细管中的体相溶液一起向负极运动,这便形成了电渗流。
需要指出,很多非离子型材料如聚四氟乙烯和聚丙烯等材料表面也可以产生电渗流,原因可能是其表面对阴离子的吸附。
电渗流的大小可用速率和淌度来表示:()E EOF ηεξν/=(6) 或者 ηεξµ/=EOF (7)式中νEOF 为电渗流速率,µEOF 为电渗淌度,ξ为Zeta 电势,ε为介电常数。
Zeta 电势主要取决于毛细管表面电荷的多寡。
一般来说,pH 越高,表面硅羟基的解离程度越大,电荷密度越大,电渗流速率就越大。
除了受pH 的影响外,电渗流还与表面性质(硅羟基的数量、是否有涂层等)、溶液离子强度有关,双电层理论认为,增加离子强度可以使双电层压缩,从而降低Zeta 电势,减小电渗流。
此外,温度升高可以降低介质粘度,增大电渗流。
电场强度虽然不影响电渗淌度,但却可改变电渗流速率。
显然,电场强度越大,电渗流速率越大。
由上可知,电渗流的方向一般是从正极到负极,然而,在溶液中加入阳离子表面活性剂后,由于毛细管表面强力吸附阳离子表面活性剂的亲水端,而阳离子表面活性剂的疏水端又会紧密结合一层表面活性剂分子,结果就形成了带负电的表面,双电层Zeta 电势的极性发生了反转,最后使电渗流的方向发生了变化。
在分析小分子有机酸时,这是常用的电渗流控制技术。
电渗流的一个重要特性是具有平面流型。
由于引起流动的推动力在毛细管的径向上均匀分布,所以管内各处流速接近相等。
其优点是径向扩散对谱带扩展的影响非常小,如图2所示。
与此形成鲜明对照的是高压泵驱动的抛物线流型(如在HPLC 中),由于管内径向上各处的流速不同,使得谱带峰形变宽。
这也是与HPLC 相比,CE 具有更高分离效率的一个重要原因。
电渗流的另一个重要优点是可以使几乎所有被分析物向同一方向运动,而不管其电荷性质如何。
这是因为电渗淌度一般比离子的电泳淌度大一个数量级,故当离子的电泳淌度方向与电渗流方向相反时,仍然可以使其沿电渗流方向迁移。
这样,就可在一次进样分析中,同时分离阳离子和阴离子。
中性分子由于不带电荷,故随电渗流一起运动。
如果对毛细管内壁进行修饰可以降低电渗流,而被分析物的淌度则不受影响。
在此情况下,阴阳离子有可能向不同的方向迁移。
3.毛细管电泳的仪器及操作图3所示为CE 仪器示意图。
其组成部分主要是高压电源、缓冲液瓶(包括样品瓶)、毛细管和检测器。
下面分别简要讨论之。
高压电源是为分离提供动力的,商品化仪器的输出直流电压一般为0~30kV,也有文献报道采用60kV以至90kV电压的。
大部分直流电源都配有输出极性转换装置,可以根据分离需要选择正电压或负电压。
缓冲液瓶多采用塑料(如聚丙烯)或玻璃等绝缘材料研制成,容积为1~3mL。
考虑到分析过程中正负电极上发生的电解反应,体积大一些的缓冲液瓶有利于pH的稳定。
进样时毛细管的一端伸入样品瓶,采用压力或电动方式将样品加载到毛细管入口,然后将样品瓶换为缓冲液瓶,接通高压电源开始分析。
4.毛细管电泳的分离模式CE有6种常用的分离模式,其分离依据及应用范围如表1 所示。
其中毛细管区带电泳(CZE)、胶束电动毛细管色谱(MEKC)和毛细管电色谱(CEC)最为常用。
本实验的内容为CZE。
表1 6种CE分离模式的分离依据及应用范围分离模式 分离依据 应用范围毛细管区带电泳(CZE) 溶质在自由溶液中的淌度差异 可解离的或离子化合物、手性化合物及蛋白质、多肽等毛细管胶束电动色谱(MECC) 溶质在胶束与水相间分配系数的差异中性或强疏水性化合物、核酸、多环芳烃、结构相似的肽段毛细管凝胶电泳(CGE) 溶质分子大小与电荷/质量比差异蛋白质和核酸等生物大分子毛细管等电聚焦(CIEF) 等电点差异 蛋白质、多肽毛细管等速电泳(CITP) 溶质在电场梯度下的分布差异(移动界面)同CZE,电泳分离的预浓缩毛细管电色谱(CEC) 电渗流驱动的色谱分离机制 同HPLC毛细管区带电泳(CZE)是最简单的CE模式,因为毛细管中的分离介质只是缓冲液。
在电场的作用下,样品组分以不同的速率在分立的区带内进行迁移而被分离。
由于电渗流的作用,正负离子均可以实现分离。
在正极进样的情况下,正离子首先流出毛细管,负离子最后流出。
中性物质在电场中不迁移,只是随电渗流一起流出毛细管,故得不到分离。
在CZE中,影响分离的因素主要有缓冲液的种类、浓度和pH值、添加剂、分析电压、温度、毛细管的尺寸和内壁改性等。
缓冲液种类的选择主要考虑其pKa值要与分析所用pH匹配,另外,有的缓冲液与样品组分之间有特殊的相互作用,可提高分析选择性。
比如,分析多羟基化合物时,多用硼酸缓冲液,因为硼酸根可与羟基形成络合物,有利于提高分离效率。
增大缓冲液的浓度一般可以改善分离,但电渗流会降低,因而延长了分析时间,过高的盐浓度还会增加焦耳热。
缓冲液的pH 主要影响电渗流的大小和被分析物的解离情况,进而影响被分析物的淌度,是CZE 分析中最重要的操作参数之一。
缓冲液添加剂多为有机试剂,如甲醇、乙腈、尿素、三乙胺等,其作用主要是增加样品在缓冲液中的溶解度,抑制样品组分在毛细管壁的吸附,改善峰形。
提高分析电压有利于提高分离效率和缩短分析时间,但可能造成过大的焦耳热。
温度的变化可以改变缓冲液的粘度,从而影响电渗流。
毛细管内径越小,分离效率越高,但样品容量越低;增加毛细管长度可提高分离效率,但延长了分析时间。
有时为了改善分离,要对毛细管内壁进行改性,比如采用涂层技术。
5.毛细管电泳的基本参数CE 中的分析参数可以用色谱中类似的参数来描述,比如与色谱保留时间相对应的有迁移时间,定义为一种物质从进样口迁移到检测点所用的时间,迁移速率(ν)则是迁移距离(l ,即被分析物质从进样口迁移到检测点所经过的距离,又称毛细管的有效长度)与迁移时间(t )之比:t l=ν (8)因为电场强度等于施加电压(V)与毛细管长度(L)之比:L V E = (9)就CE 的最简单的模式—毛细管区带电泳(CZE )而言,结合式(1),可得:tV lL tE l a ==µ (10)在毛细管区带电泳(CZE )条件下测得的淌度是电泳淌度与电渗流淌度的矢量和,我们称之为表观淌度µa ,即:EOF e a µµµ+= (11)实验中可以采用一种中性化合物,如二甲亚砜或丙酮等,来单独测定电渗流淌度,然后求得被分析物的有效淌度。
例如,图4是一个混合物的分离结果,其中三个峰分别为阳离子(t = 39.5s )、中性化合物(t = 66.4s )和阴离子(t = 132.3s )。
实验用毛细管总长度为48.5cm ,有效长度(从进样口到检测点的距离)为40cm ,施加电压为20kV 。
根据上述公式,我们便可以计算出电渗淌度以及不同离子的表观淌度和有效淌度。
电渗淌度:11231046.14.66200005.4840−−−⋅×=××=s V cm EOF µ阳离子:11246.25.39200005.4840−−⋅=××=s V cm a µ 1123101−−−⋅×=−=s V cm EOF a e µµµ阴离子:11241033.73.132200005.4840−−−⋅×=××=s V cm a µ11241087.5−−−⋅×−=−=s V cm EOF a e µµµ注意,阴离子的有效淌度为负值,因为其电泳淌度与电渗淌度的方向相反。
三、实验设备每四人一组共用一台Capel-103RT 电泳仪。
四、实验仪器及试剂5 mL 移液管2只,1mL 移液管共2支,分别标上四种标样的标签,两组公用。
每组10 mL 容量瓶2个,滴管2支,分别标上标准、未知的标签。
塑料样品管共16个,每组8个,分别用于标准样品、未知样品、三种缓冲溶液、NaOH 、水和废液,做好标号。
滴瓶一共5个,分别装三种缓冲液(buffer)、1mol/L 的NaOH 和乙醇。
镊子、洗瓶、吸耳球、试管架、塑料样品管架、废液烧杯每组一个。
剪刀一把,记号笔一支,滤纸。
标样:苯甲醇、苯甲酸、水杨酸、对氨基水杨酸,均溶于二次水中,浓度1.00 mg/mL ,作为标准品,混合稀释作为标样。
