电化学基础和氧化还原平衡
第七章-氧化还原反应与电化学基础

§7.2 电化学电池
5. 正负极
• 电子的流出极叫负极:Zn极 • 电子的流入极叫正极:Cu极
6. 阴阳极
• 阳极(Positive Electrode): 凡是进行氧化反应的电极叫阳极。
• 阴极(Negative Electrode): 凡是进行还原反应的电极叫阴极。
第七章 氧化还原反应与电化学基础
在超氧化物中(KO2),氧的氧化数 为 1 ;
2
在氧的氟化物(OF2,O2F2)中,氧的 氧化数分别为+2和+1。
❖ 在所有的氟化物中氟的氧化数为-1。
第七章 氧化还原反应与电化学基础
§7.1 基本概念
例:
SiO2: Si的氧化数为+4; Cr2O72-:Cr的氧化数为+6; Fe3O4: Fe的氧化数为 8 ;
Mz+(aq)+ze-
–
离子电极
2OH-(aq) Pt | O2(p)|OH-(c)
金属-难 溶盐电极
AgCl(s) +e-
Ag(s) +Cl-(aq) Ag|AgCl|Cl-
§7.3 电极电势
(Electrode Potential)
7.3.1 电极电势的产生 7.3.2 电极电势的意义 7.3.3 电池电动势 7.3.4 标准电极电势 7.3.5 标准电极电势表 7.3.6 Nernst方程式 7.3.7 Nernst 方程式的应用
MgCl2(s)
第七章 氧化还原反应与电化学基础
§7.1 基本概念
2. 失去电子的过程叫氧化,得到电子的
过程叫还原
Zn(s) Zn2+(aq)+2eCu2+(aq)+2e- Cu(s) 局限性:形成共价分子的氧化过程不
氧化还原反应和电化学反应

氧化还原反应和电化学反应氧化还原反应是化学反应中最为重要和常见的反应之一。
它涉及到物质中的电子转移过程。
在氧化还原反应中,物质可以同时发生氧化和还原。
与之相伴随的是电化学反应,电化学反应是指在化学反应中涉及电子的转移和电流的流动的反应。
一、氧化还原反应氧化还原反应中,氧化和还原是同时进行的。
氧化是指物质失去电子;还原则是指物质获得电子。
这一过程中,电子从一个物质转移到另一个物质。
氧化和还原总是同时发生,因为电子不能独立存在。
例如,当铁和氧气发生反应时,铁原子(Fe)失去两个电子,被氧(O2)接受,生成氧化铁(Fe2O3)。
这里,铁原子发生了氧化,而氧气发生了还原。
氧化还原反应在日常生活中非常常见。
例如,金属的生锈、水的电解、电池的工作原理等都是氧化还原反应的例子。
二、电化学反应电化学反应是指在化学反应中涉及电子的转移和电流的流动的反应。
它是由氧化还原反应导致的。
电化学反应可以分为两种类型:电解反应和电池反应。
1. 电解反应电解反应是指在电解池中,通过外加电压使化学反应发生。
在电解过程中,正极(阳极)接受电子,发生氧化反应;负极(阴极)释放电子,发生还原反应。
电解反应在工业生产和实验室中广泛应用。
例如,电解盐水时,氯离子(Cl-)在阳极上接受电子,发生氧化反应生成氯气(Cl2),而阳离子(Na+)在阴极上释放电子,发生还原反应生成氢气(H2)。
2. 电池反应电池反应是指在电化学电池内,将化学能转化为电能的反应。
电池由两个半电池组成,每个半电池都有一个氧化反应和一个还原反应。
半电池之间通过电子流进行电荷平衡。
常见的电池包括干电池、蓄电池和燃料电池等。
干电池是通过将氧化剂和还原剂隔离,以阻止反应直接进行,并通过电子在电路中流动来提供电能。
蓄电池是通过可逆的氧化还原反应来存储和释放电能。
燃料电池是通过将燃料和氧气直接反应生成电能。
总结:氧化还原反应和电化学反应密切相关,涉及到电子转移和电流的流动。
氧化还原反应是物质中的电子转移过程,分为氧化和还原。
氧化还原反应和电化学基础

8
⑷ 离子型化合物中,元素的氧化数等于该 ⑸ 离共子价所型带化的合电物荷中数,,共如用:电N子aC对I。偏向于电负性大 的原子 ,两原子的形式电荷数即为它们的氧化数, 如:HCI。 ⑹ 中性分子中,各元素原子氧化数的代数和为9 零。
S4O62- 4x+(-2)×6=-2 x=2.5 H5IO6 I:+7 ; S2O32- S:+2 例:求MnO4-中Mn的氧化值
2×3
0
+5
Zn+ HNO3
+2
+2
Zn(NO3)2+ NO + H2O
3 ×2
56
配系数
先配变价元素,再用观察法配平其 它元素原子的系数。
15
用氧化数表示氧化还原的状态 对于离子化合物的氧化还原反应来说,电 子是完全失去或完全得到的。但是,对于共价化 合物来说,在氧化还原反应中,有电子的偏移, 但还没有完全的失去或得到,因此用氧化数来表 示就更为合理。
16
例如:
H2+Cl2=2HCl 这个反应的生成物是共价化合物,氢原子的电子 没有完全失去,氯原子也没有完全得到电子,只是形成 的电子对偏离氢,偏向氯罢了。用氧化数的升降来表示 就是氯从0到-1,氢从0到+1。这样,氧化数的升高就是 氧化,氧化数的降低就是还原。在氧化还原反应里,一 种元素氧化数升高的数值总是跟另一种元素氧化数降低 的数值相等的。
11
一、氧化值的定义
在氧化还原反应中,电子转移引起某些原子的价 电子层结构发生变化,从而改变了这些原子的带电状 态。为了描述原子带电状态的改变,表明元素被氧化 的程度,提出了氧化态的概念。表示元素氧化态的的 数值称为元素的氧化值,又称氧化数。
无机化学:第九章 氧化还原反应与电化学基础解析

第九章氧化还原反应和电化学基础一、氧化还原反应方程式的配平1、元素的氧化数(氧化值)(中学:化合价)❖定义:氧化数是某一个元素的荷电数,这种荷电数由假设把每个键中的电子数指定给电负性更大的原子而求得。
❖本质:a、离子化合物中,即正、负离子所带的电荷数;b、极性化合物中,即元素的一个原子提供参与共价键的电子数,其中电负性小,共用电子对离得较远的元素为正氧化数,电负性大、共用电子以离得较近的元素为负氧化数。
『①单质的氧化数为0-1;②在配合物中,当自由基或原子团作为配体时,其氧化数均看作 1;2❖定义:凡有电子得失或共用电子对偏移发生的反应。
氧化——失去电子或共用电子对偏离的变化,相应的物质称为“还原剂”;还原——得到电子或共用电子对接近的变化,相应的物质称为“氧化剂”。
❖氧化剂还原剂——氧化还原反应中,失去电子、氧化数升高的物质(发生氧化反应)因此,凡元素氧化数发生变化的过程,就是氧化还原反应!3、氧化还原反应方程式的配平方法与应用(一)氧化数法:适用于任何氧化还原反应❖依据:还原剂氧化数的升高总值 = 氧化剂氧化数降低总值例1:KMnO4 + FeSO4 + H2SO4 ==①根据反应事实,写出反应产物,注意介质酸碱性:KMnO4 + FeSO4 + H2SO4==MnSO4 +Fe2(SO4)3 + K2SO4 + H2O②调整计量系数,使氧化数升高值 = 降低值:+7 +2 +2 +3KMnO4 + 5 FeSO4 + H2SO4==MnSO4 + 5/2 Fe2(SO4)3 + K2SO4 + H2O③若出现分数,可调整为最小正整数:2 KMnO4 +10 FeSO4 + H2SO4==2 MnSO4 + 5 Fe2(SO4)3 + K2SO4 + H2O法2:配平各元素原子数(观察法)——先配平非H、O原子,后配平H、O原子。
①配平K+、SO42-数目 SO42-:左11,应+7;右182 KMnO4 + 10 FeSO4 + 8 H2SO4 ==2 MnSO4 + 5 Fe2(SO4)3 + K2SO4 + H2O②配平H+数目 H+:左2,应 8 H2O2 KMnO4 +10 FeSO4 + 8 H2SO4==2 MnSO4 +5 Fe2(SO4)3 + K2SO4 + 8 H2O③配平(或核对)O原子数目:已平衡。
《无机化学》第五章 氧化还原反应和电化学基础

二、氧化还原反应方程式的配平
1. 氧化值法
配平原则:氧化剂中元素氧化值降低的总数等 于还原剂中元素氧化值升高的总数。
配平步骤: (1)写出反应方程式,标出氧化值有变化 的元素,求元素氧化值的变化值。
(2)根据元素氧化值升高总数和降低总数相等 的原则,调整系数,使氧化值变化数相等。
(3)用观察法使方程式两边的各种原子总数相 等。
酸表。
(4)E是电极处于平衡状态时表现出来的特
征,与反应速率无关。
(5)E仅适用于水溶液。
5.饱和甘汞电极:
Hg | Hg2Cl2(s) |KCl (饱和)
Hg2Cl2 (s) + 2e
2Hg(l) +2Cl-
E (Hg2Cl2/Hg)=0.245V
三、 影响电极电势的因素
1.影响 因素
(1)电极的本性:即电对中氧化型或还 原型物质的本性。
还原型:在电极反应中同一元素低氧化值的物质。)
电对:氧化型/还原型
例:MnO2 +4H+ + 2e
Mn2+ +2H2O
电对:MnO2 / Mn2+
(2)E与电极反应中的化学计量系数无关。
例:Cl2 + 2e 1/2Cl2 + e
2Cl- E(Cl2/Cl-)=1.358V Cl-
(3)电极反应中有OH- 时查碱表,其余状况查
(3)分别配平两个半反应,使等号两边的原子 数和电荷数相等。
(4)根据得失电子数相等的原则,给两个半 反应乘以相应的系数,然后合并成配平的离子 方程式。
(5)将离子方程式写成分子方程式。
离子电子法配平时涉及氧原子数的增加和减 少的法则:
氧化还原平衡电化学基础

拓展电化学技术的应用领 域
将电化学技术应用于其他领域 ,如生物医学、传感器、电子 器件等,可以开拓新的应用领 域并促进相关领域的发展。
THANKS
感谢观看
保持实验室通风良好
注意电源安全
在实验过程中,可能会产生有毒或刺激性 气体,因此应保持实验室通风良好,及时 排出有害气体。
在接通电源进行实验时,应注意电源安全 ,避免电极短路或过载,以免发生意外事 故。
实验结果分析
记录实验数据
在实验过程中,应认真观察并 记录电极反应的现象、电流的
变化情况等数据。
整理数据
电解过程
电解池
电解过程是在外加电源的作用下,在电解池中发生的氧化还 原反应。
电解产物
电解过程中,根据电解质的性质和电解条件的不同,会产生 不同的电解产物。
电镀过程
电镀原理
电镀过程是通过电解方法,在金属表 面沉积金属或合金的过程。
电镀应用
电镀广泛应用于工业、电子、航空航 天、汽车、建筑等领域,用于提高材 料表面的耐磨性、耐腐蚀性和美观度 等。
深入研究反应机理和动力 学过程
通过理论计算和实验手段,深 入揭示氧化还原反应的微观机 制和动力学过程,有助于优化 电化学反应过程和提高能源转 换效率。
发展新型电化学储能技术
针对可再生能源的间歇性特点 ,发展高效、长寿命、低成本 的新型电化学储能技术,如锂 硫电池、钠离子电池等,对于 实现可再生能源的高效利用具 有重要意义。
还原态
表示某元素被还原的状态,通常用负 号“-”表示,例如Fe0的还原态为0。
氧化还原反应的方向
氧化反应
物质失去电子的反应,通常需要外界提供能量。
还原反应
物质得到电子的反应,通常释放能量。
第六章氧化还原平衡和电化学基础习题

第六章 氧化还原平衡和电化学基础练习:1、已知: ϕ(Fe 3+/Fe 2+) = 0.77 V , ϕ(Br 2/Br -) = 1.07 V , ϕ(H 2O 2/H 2O) = 1.78 V ,ϕ(Cu 2+/Cu) = 0.34 V , ϕ(Sn 4+/Sn 2+) = 0.15V 则下列各组物质在标准态下能够共存的是:A 、Fe 3+,CuB 、Fe 3+,Br 2C 、Sn 2+,Fe 3+D 、H 2O 2,Fe 2+2、Pt│Fe 3+(1 mol·L -1),Fe 2+(1 mol·L -1)‖C e 4+(1 mol·L -1),Ce 3+(1 mol·L -1)│Pt 的电池反应是: A 、Ce 3+ + Fe 3+ = Ce 4+ + Fe 2+ B 、Ce 4+ + Fe 2+ = Ce 3+ + Fe 3+C 、Ce 3+ + Fe 2+ = Ce 4+ + FeD 、Ce 4+ + Fe 3+ = Ce 3+ + Fe 2+3、已知:Fe 3+ + e - = Fe 2+ ϕ= 0.77 V Cu 2+ + 2e - = Cu ϕ= 0.34 VFe 2+ + 2e - = Fe ϕ= -0.44 V Al 3+ + 3e - = Al ϕ= -1.66 V则最强的还原剂是: A 、Al 3+ B 、Fe 2+ C 、Fe D 、 Al4、 ϕ(MnO -4/Mn 2+) = 1.51 V , ϕ(MnO -4/MnO 2)= 1.68 V , ϕ(MnO -4/MnO -24) = 0.56 V ,则还原型物质的还原性由强到弱排列的次序是:A 、 MnO -24> MnO 2 > Mn 2+ B 、 Mn 2+ > MnO -24> MnO 2C 、 MnO -24> Mn 2+ > MnO 2 D 、 MnO 2 > MnO -24> Mn 2+5、对于下面两个反应方程式,说法完全正确的是:2Fe 3+ + Sn 2+ = Sn 4+ + 2Fe 2+, Fe 3+ + 21Sn 2+ = 21Sn 4+ + Fe 2+A 、两式的 E , m r G ∆,K 都相等B 、两式的 E , m r G ∆,K 不等C 、两式的 m r G ∆相等, E ,K 不等D 、两式的E 相等, m r G ∆,K 不等6、原电池Zn + 2Ag + = Zn 2+ + 2Ag 在标准状态下的电动势为:A 、ε= 2φθ(Ag +/Ag )-φθ(Zn 2+/Zn );B 、ε= {φθ(Ag +/Ag )}2 -φθ(Zn 2+/Zn );C 、ε= φθ(Ag +/Ag )-φθ(Zn 2+/Zn );D 、ε= φθ(Zn 2+/Zn )- φθ(Ag +/Ag )7、已知 ϕ(Fe 3+/Fe 2+) = +0.77 V , ϕ(Fe 2+/Fe) = -0.44 V ,则 ϕ(Fe 3+/Fe)的值为: -0.037V8、根据铬在酸性溶液中的元素电势图可知, ϕ(Cr 2+/Cr)为:-0.905V9、某氧化还原反应的标准吉布斯自由能变为 Δr G θ m 、平衡常比数为K θ 、标准电极电势为E θ 。
氧化还原反应电化学基础N
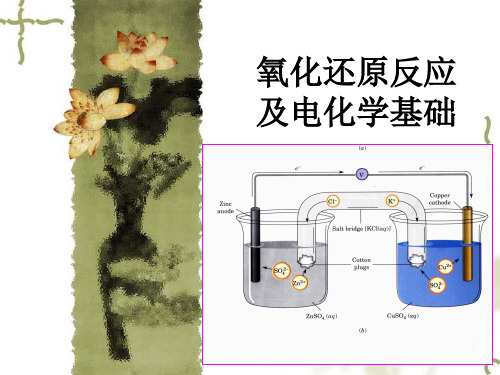
这一反应可在下列装置中分开进行
盐桥:在U型管中装 满用饱和KCl溶液和 琼胶作成的冻胶。 盐桥的作用:使Cl向锌盐方向移动, K+向铜盐方向移动, 使Zn盐和Cu盐溶液 一直保持电中性, 从而使电子不断从 Zn极流向Cu极。
这种装置能将化学能转变为电能,称为原电池。
正极(铜电极): Cu2+ + 2eCu 负极(锌电极): Zn Zn2+ + 2e正、负两极分别发生的 反应,称为电极反应。 电池反应:Zn + Cu2+ = Cu + Zn2+(总反应)
例:
H5I O6 S2 O S4 O
2 3 2 6
I的氧化值为 7 S的氧化值为 2 S的氧化值为 2.5 8 Fe的氧化值为 3
Fe3O 4
2、氧化还原半反应和氧化还原电对
氧化还原反应的方程式可分解成两个“半反应”。 反应中,氧化剂(氧化型)在反应过程中氧化数降 低生成氧化数较低的还原型; 还原剂(还原型)在反应 过程中氧化数升高转化为氧化数较高的氧化型。 由一对氧化型和还原型构成的共轭体系称为氧化还 原电对,可用“氧化型/还原型”表示。
Fe3+
溶液中,另一铂片插入到含有MnO4- 、Mn2+ 及H+ 的溶液
正极反应: MnO4- + 8H+ + 5e- = Mn2+ + 4H2O 电池反应: MnO4- + 8H+ + 5Fe2+ = Mn2+ + 5Fe3+ + 4H2O
电池符号:
(-)Pt|Fe2+(c1),Fe3+(c2)||MnO4-(c3),H+(c4),Mn2+(c5)|Pt (+)
华东理工大学现代基础化学课后习题解答第10章

2
= -0.700 V 9、求下列电极在 25℃时的电极反应的电势。
(1) 101.3 kPa 的 H2(g)通入 0.10 mol⋅L −1的 HCl 溶液中;
(2) 在 1L 上述(1)的溶液中加入 0.1 mol 固体 NaOH; (3) 在 1L 上述(1)的溶液中加入 0.1 mol 固体 NaAc。(忽略加入固体引起的溶液体积变化)。
− 3
+
H
+
→Zn
2+
+
NH
+ 4
+ H2O
(4) Ag +
+
NO
− 3
+
H
+
→Ag
+
+
NO
+
H2O
(5) Cl2 + OH − →Cl − + ClO − + H2O
(6)
Al
+
NO
− 3
+
OH
−
+
H2O→[Al(OH)4]
−
+
NH3
解: (1) 2KMnO4 + 5K2SO3 + 3H2SO4 = 6K2SO4 + 2MnSO4 + 3H2O (2) 5NaBiO3(s) + 2MnSO4 + 16HNO3 = 2HMnO4 + 5Bi(NO3)3 + 2Na2SO4 + NaNO3 + 7H2O
7、根据电对 Cu 2+ /Cu、Fe 3+ /Fe 2+ 、Fe 2+ /Fe 的电极反应的标准电势值,指出下列各 组物质中哪些可以共存,哪些不能共存,并说明理由。
(完整版)08电化学基础与氧化还原平衡习题解答

10. 已知下列反应的原电池电动势为0.46V,且Zn2+/Zn 的Eθ=-0.76V,则氢电极溶液中的pH为( D ) Zn(s)+2H+(x mol·L–1)Zn2+(1 mol·L–1)+H2(101.3kPa) (A)10.2 (B)2.5 (C)3 (D)5.1
11.下列氧化还原电对中,Eθ值最大的是(D)
……( D )
(A) O2(g)+4H+(aq)+4e =2H2O(l) (B) Fe3+(aq)+e-=Fe2+(aq)
(C)Fe(s)+2Fe3+(aq)= Fe2+(aq)
(D) 2 Fe3+(aq)+3e = Fe(s)
15.使下列电极反应中有关离子浓度减小一半,
而E值增加的是
(B)
(A)Cu2+ +2e = Cu
电化学基础 与氧化还原平衡
习题解答
一、选择题
1.根据反应式: 2MnO4-+10Fe2+ +16H+=2Mn 2+ +10Fe3+ +8H2O 设计成原电池,其原电池的表示式是…… ( C ) (A) Fe | Fe2+ ,Fe3+ || Mn2+ ,MnO4-, H+ | Mn (B) Pt | MnO4-,Mn2+ ,H+ || Fe2+ ,Fe3+| Pt (C) Pt | Fe2+ ,Fe3+ || Mn2+ ,MnO4-,H+ | Pt (D) Mn | MnO4-,Mn2+ ,H+ || Fe2+,Fe3+ | Mn
08电化学基础与氧化还原平衡习题解答

< >
Eθ (Ag2CrO4/Ag) Eθ (AgCl/Ag)
三、计算题 1.将下面的电池反应用电池符号表示之, 将下面的电池反应用电池符号表示之, 将下面的电池反应用电池符号表示之
Cu(s)+2H+(0.01mol·L-1) = Cu2+ (0.1mol·L-1)+H2(0.9×1.013×105Pa) × ×
15.使下列电极反应中有关离子浓度减小一半, 使下列电极反应中有关离子浓度减小一半, 使下列电极反应中有关离子浓度减小一半 而E值增加的是 值增加的是 (A)Cu2+ +2e = Cu ) (B)I2+2e = 2I) (C)2H+ +2e = H2 ) (D)Fe3+ +e = Fe2+ ) ( B )
(-)Cu(s)|Cu2+(1mol·L-1)||H+(1mol·L-1)|H2(1.013×105Pa)|Pt(+) ×
E池θ=EθH /H - EθCu2+/Cu =-0.34 v < 0 。
2 +
nE池 lg K = = −11.5, K ө=2.98×10-12 × 0.059
θ
θ
θ × ∆rGmθ = -nFE池 = 6.56×104J·mol-1>0。
-
2.将下列反应设计成原电池时,不用惰性电 将下列反应设计成原电池时, 将下列反应设计成原电池时 极的是 (A)H2+Cl2 = 2HCl ) (B)2Fe3+ +Cu = 2Fe2+ +Cu2+ ) (C)Ag+ +Cl- = AgCl ) (D)2Hg2+ +Sn2+ = Hg22+ +Sn4+ ) (C)
氧化还原反应与电化学基础

碱性介质中,不能出现 H+ 2、难溶或弱电解质应写成分子形式 3.注明沉淀、气体等
第六页, 共37页。
二、电池电动势(E)与电极电势()
1 原电池: Cu-Zn原电池
负极
正极
第七页, 共37页。
原电池(Galvanic cells): ------化学能转化成电能的装置 (区别于电解池 electrolytic cells)
0 .0 n 5 9 1lg ( (氧 还 化 原 型 型 )) m q (2 5C )
影响存在三种类型: (1)一边型: 如 Zn2+/Zn:
Zn2+ + 2e = Zn(s)
0 .0 5 9 1 7lg (Z n 2 ) (2 5C )
(2)二边型: 如 Fe3+/ Fe2+2 : Fe3+ + e = Fe2+
将 E=正-负和 E=正-负代入上面电池反应的 Nernst方程式,可得到 电极反应的 Nernst方程式 :
电极反应的 Nernst方程式:
0 .0 n 5 9 1lg ( (氧 还 化 原 型 型 )) m q (2 5C )
电极反应式一般写为: m 氧化型 + n e = q 还原型
第二十页, 共37页。
0.82 (V)
0.05917
(C l)2
E0.82 n lg(P C l2/P )(I)2
例2 试求下列电池的电动势E池
(–) Zn | Zn2+(0.1 mol/dm3) || Cu2+(0.001 mol/dm3) | Cu (+)
第十九页, 共37页。
2) 电极反应的 Nernst 方程式
第六章 氧化还原反应及电化学基础_6

如:标准锌电极与标准氢电极组成原电池,锌为负极, 标准锌电极与标准氢电极组成原电池,锌为负极, 氢为正极, 氢为正极,测得 εθ = 0.7618 (V) , 则 Eθ(Zn2+/Zn) = 0.0000 – 0.7618 = -0.7618(V)
标准电极电势表
标准电极电势表
Eθ(Li+/Li)值最小的原因:(严宣申,王长富《普通无机化学》(第二版)p10) (Li+/Li)值最小的原因 值最小的原因: 严宣申,王长富《普通无机化学》 第二版) 热 sGmθ(Μ) hGmθ(Μ+) 化 学 M(s) + H+(aq) M+(aq) + 1 H2(g) 2 循 1 G θ(Η ) hGmθ(Η+) 2 2 d m 环 iGmθ(Η) H(g) H+(g)
“形式电荷” +1 -2 形式电荷” 形式电荷 称为“氧化数” 称为“氧化数”
经验规则: 各元素氧化数的代数和为零。 经验规则: 各元素氧化数的代数和为零。 1)单质中,元素的氧化数等于零。(N2 、H2 、O2 等) 单质中,元素的氧化数等于零。(N 。( 2)二元离子化合物中,与元素的电荷数相一致。 NaCl 二元离子化合物中,与元素的电荷数相一致。 CaF2 +1,- +2,+1,-1 +2,-1 共价化合物中,成键电子对偏向电负性大的元素。 3) 共价化合物中,成键电子对偏向电负性大的元素。 超氧化钾) O: -2 (H2O 等); -1 (H2O2); -0.5 (KO2 超氧化钾) 一般情况; H: +1, 一般情况; -1, CaH2 、NaH
思考题: 确定氧化数 思考题:
Na2S4O6 (1)Na2S2O3 ) +2 +2.5 (2)K2Cr2O7 ) CrO5 +6 +10 KO3 (3)KO2 ) -0.5 -1/3 注意:1) 同种元素可有不同的氧化数; 注意: 同种元素可有不同的氧化数; 氧化数可为正、负和分数等; 2) 氧化数可为正、负和分数等;
化学教案:氧化还原反应与电化学反应

化学教案:氧化还原反应与电化学反应氧化还原反应与电化学反应一、引言氧化还原反应和电化学反应是化学领域中的重要概念。
它们在日常生活中广泛应用于许多领域,例如电池技术、电解过程和腐蚀现象等。
本文将详细介绍氧化还原反应和电化学反应的概念、原理和应用。
二、氧化还原反应的概念氧化还原反应是指物质中的电子在反应中的转移过程。
在氧化还原反应中,氧化剂接受电子,发生氧化反应,而还原剂失去电子,发生还原反应。
反应过程中电子的转移导致物质的氧化和还原,因此称为氧化还原反应。
氧化还原反应可以表征为以下反应方程式:一般反应方程式:氧化剂 + 还原剂→ 氧化物 + 还原物其中,氧化剂是接受电子的物质,还原剂是失去电子的物质。
氧化物是被氧化剂形成的物质,还原物是被还原剂形成的物质。
三、电化学反应的概念电化学反应是指在电解质溶液中,通过外加电压使物质发生氧化还原反应的过程。
电化学反应包括两个部分:电解质溶液中的离子在电极上发生氧化还原反应的过程称为半反应;两种半反应相互结合并与外电路相连,使电荷得以平衡的过程称为全反应。
电化学反应可以分为两类:在电解池内,正极发生氧化反应,负极发生还原反应,称为电解反应;在电池内,正极发生还原反应,负极发生氧化反应,称为电池反应。
四、氧化还原反应和电化学反应的联系氧化还原反应和电化学反应之间存在着紧密的联系。
在电化学反应中,电流的产生和流动涉及到电子的转移,即氧化还原反应的发生。
电化学反应可以通过外加电压来驱动氧化还原反应,因此可以将电化学反应看作是氧化还原反应在电解质溶液中发生的过程。
五、氧化还原反应和电化学反应的应用1. 电池技术电池是将化学能转化为电能的设备。
其中,氧化还原反应是电池技术的基础。
例如,常见的干电池就是通过氧化还原反应产生电能的。
在干电池中,锌电极发生氧化反应,放出电子,而二氧化锌是氧化产物;而在负极的电解质中,二氧化锰接受电子,发生还原反应,产生锰酸锌。
这种氧化还原反应使得电池能够持续地产生电能。
电化学基础与氧化还原平衡习题解答

11.下列氧化还原电对中,Eθ值最大的是(D)
(A) AgCl/Ag (B) AgBr/Ag
(C)AgI/Ag
(D) Ag+/Ag
.
12. 298K时,在标准Ag-Cu原电池正极半电池中
加入氨水,则
……( D )
(已知EθAg+/Ag = 0.80V, EθCu2+/Cu = 0.34V)
(A) 原电池电动势减小;
.
2.将Ag-AgCl电极[Eθ(AgCl/Ag)=0.2222V,与标准 氢电极[Eθ(H+/H2)=0.000V]组成原电池,该原电池的 电池符号为 1 ;正级反应 2 ;负极反应 3 ;电 池反应 4 ;电池反应的平衡常数为 5 。
.
1.
(-) Pt H2 (1.013×105 Pa) H+ (1mol L-1) ||Cl-1 (1mol L-1)|AgCl (s),Ag (s) (+)
.
9.将氢电极[p(H2)=100kPa]插入纯水中与标准 氢电极组成原电池,则E为 ……( A ) (A)0.414V (B)-0.414V (C)0V (D)0.828V
.
10. 已知下列反应的原电池电动势为0.46V,且Zn2+/Zn 的Eθ=-0.76V,则氢电极溶液中的pH为( D ) Zn(s)+2H+(x mol·L–1)Zn2+(1 mol·L–1)+H2(101.3kPa) (A)10.2 (B)2.5 (C)3 (D)5.1
7. 某氧化还原反应的电动势Eθ是正值,这是指……( B ) (A)G θ是正值,K>1 (B)G θ是负值,K>1 (C)G θ是正值,K<0 (D)G θ是负值,K<1
氧化还原反应和电化学

氧化还原反应和电化学氧化还原反应(Redox)是化学反应中的一种重要类型,涉及物质间的电子的转移。
它在许多行业中都有广泛应用,尤其在电化学领域中占有重要地位。
一、氧化还原反应基础氧化还原反应是指在化学反应中,原子、离子或分子中的电子由一个物质转移给另一个物质的过程。
其中,电子的转移发生在氧化剂和还原剂之间。
氧化剂是指能够接受电子的物质,而还原剂则是能够捐赠电子的物质。
氧化还原反应常常伴随着物质的氧化与还原状态的改变。
二、氧化还原反应的重要性1. 电池和蓄电池:氧化还原反应是电池工作的基础。
电池中的正极发生氧化反应,负极发生还原反应,通过外部电路,电子从负极流向正极,从而产生电流供应给外部设备。
蓄电池则将反应进行逆转,将电流用于电解还原,实现电能转化和储存。
2. 腐蚀和防腐:许多金属材料在氧化还原环境中容易发生腐蚀现象,因此了解氧化还原反应规律可以帮助我们有效地进行防腐措施,延长材料的使用寿命。
3. 化学分析:氧化还原反应在化学分析中发挥着重要的作用。
比如电位滴定、氧化还原指示剂的应用等,使得化学分析的方法更加全面和准确。
4. 电解和电镀:电解过程是利用外加电流使物质发生化学反应,氧化还原反应是其中关键环节。
电化学反应在电镀工艺中广泛运用,可使金属表面得到保护或改变其性质。
三、电化学基础电化学是研究电能与化学能之间相互转化关系的学科。
它与氧化还原反应有着密切的联系,通过电化学实验可以研究电流与氧化还原反应之间的关系。
电化学反应包括两种基本类型:非自发反应(电解反应)和自发反应(电池反应)。
电解反应是指在外界电源的作用下,使非自发的氧化还原反应发生。
而电池反应则是在没有外界电源的情况下,使自发的氧化还原反应发生,从而产生电能。
电化学反应中的重要参数包括电位和电解质浓度。
电位是物质发生氧化还原反应时与标准氢电极之间电势差的度量。
而电解质浓度的改变会影响电解反应的速率和方向。
电化学反应在电池、电解、电镀、电解分析等领域都有广泛应用。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
E = 1.36V
E = 1.36V
1 Cl2 (g) e 2
Cl (aq)
④ 一些电对的 E 与介质的酸碱性有关
酸性介质: EA ;碱性介质: B E
标准电极电势 (298K, 在酸性溶液中)
标准电极电势 (298K, 在碱性溶液中)
第十一章
氧化还原反应
§11.1 基本概念 §11.2 电极电势和电池电动势
特征:反应中氧化过程和还原过程同时发生。
0 +2 Cu2+ + Zn = Cu + Zn2+ +2 0
自氧化–还原反应:反应过程中氧化数的升高
和降低发生在同一化合物(又称歧化反应) +5 +7 –1 4KClO3 = 3KClO4 + KCl
+5 +5 +7 –1
3KClO3 + KClO3
3KClO4 + KCl
Cl 2.0mol L ‖
2Cl (aq ) 3 Fe (aq )
) Pt Fe2 1.0mol L1 , Fe3 0.1mol L1 (
·
1
Cl 101325Pa︱Pt ()
2Leabharlann 二、 电极的类型(a) 金属–金属离子电极
如: Zn2+/Zn电对所组成的电极 电极反应: 电极符号: Zn2+ + 2e– Zn(s) | Zn2+ Zn
半反应的原子数及电荷数。
③根据电荷守恒,以适当系数分别乘以两
个 半反应式,然后合并,整理,即得配平的 离子方程式;有时根据需要可将其改为分子 方程式。
例: 配平MnO4– + SO32– Mn2+ + SO42–(酸性介质) 解: 2) MnO4– + 5e– + 8H+ Mn2+ + 4H2O 5) SO32– + H2O SO42– + 2e– + 2H+ +) 2MnO4– + 6H+ + 5SO32– = 2Mn2+ + 5SO42– + 3H2O
在氧化还原反应中, 反应一般按较强的氧化
剂和较强的还原剂相互作用的方向进行
氧化还原半反应式
Cu2+ / Cu Zn2+ / Zn
MnO4– / Mn2+
SO42– / SO32–
Cu2+ + 2e–
Zn
Cu
Zn2+ + 2e–
Mn2+ + 4H2O SO32– + H2O
MnO4– + 8H+ + 5e– SO42– + 2H+ 2e–
固体导体: Pt, 石墨
(c) 金属–金属难溶盐或氧化物–阴离子电极 氯化银电极: 涂有AgCl的银丝插入HCl溶液 电极反应: AgCl + e– Ag + Cl– 电极符号: Ag–AgCl(s) | Cl
–
甘汞电极: 金属汞的表面覆盖Hg2Cl2, 然后 注入KCl溶液 1 Hg Cl + e– 电极反应: 2 2 2 Hg(l) + Cl– 电极符号: Hg–Hg2Cl2(s) | Cl–
§11.3 氧化还原平衡 §11.4 影响电极电势的因素 §11.5 元素电势图及其应用 §11.6 氧化还原滴定法
一、原电池
工作状态的化学电池同时发生三个过程: 1.两个电极表面分别发生氧化反应和还原反应; 2.电子流过外电路; 3.离子流过电解质溶液。
盐桥:通常内盛饱和KCl溶液(以琼胶做成冻胶) 作用:1.让溶液始终保持电中性使电极反应得以
解: 3)
+)
ClO–+ 2e– + H2O Cl– + 2OH–
2) Cr(OH)4– + 4OH– CrO42– + 3e– + 4H2O
3ClO– + 2OH– + 2 Cr(OH)4– = 3Cl– + 2CrO42– + 5H2O
第十一章
氧化还原反应
§11.1 基本概念
§11.2 电极电势和电池电动势
例:
H5I O6 I的氧化值 7
2 3 2 6
S2 O
S的氧化数 2
S的氧化值为 2.5
8 Fe的氧化值为 3
S4 O
Fe3O 4
(3) 氢在化合物中的氧化数一般为+1, 但在活 泼金属的氢化物中为–1。
(4) 氧在化合物中的氧化数一般为–2; 在过氧
化物中为–1; 在超氧化物中为–1/2 (KO2) ;
= ECu /Cu EH /H 0.34 = ECu /Cu 0
2+ + 2+
2
= ECu
2+/Cu
EZn
2+/Zn
ECu
2+/Cu
= 0.34V
= 0.34 – (–0.76) = 1.1V
3.标准电极电势表
① 采用还原电势;
② E 小的电对对应的还原型物质还原性强; E 大的电对对应的氧化型物质氧化性强。 ③ E 无加和性(强度性质) 2e Cl2 (g) 2Cl (aq)
氧化数定义:化合物中某元素所带形式电荷
的数目。
由于化合物中组成元素的电负性不同,原子结合 时电子对总要移向电负性大的原子一方,从而化合物 中组成元素的原子必须带正或负电荷(形式电荷)。
确定元素氧化数的规则
(1) 单质的氧化数为零。
(2) 在多原子分子中所有元素氧化数的代数和
等于零; 在多原子离子中所有元素氧化数 的代数和等于离子所带的电荷数。
§11.3 氧化还原平衡
§11.4 影响电极电势的因素 §11.5 元素电势图及其应用 §11.6 氧化还原滴定法
1.电池的电动势和化学反应吉布斯自由能的关系
DrG = –W非体积 = –W电池 W电池 = E Q E = E正极 E负极 1e = 1.60210–19C
1mol e = 1F = 9.65104C
将电池反应分解为两个半反应:
负极反应: Zn 2e = Zn EZn2 / Zn = 0.7628v
溶解 > 沉积
沉积 > 溶解
金属的电极电势:产生在金属和它的盐溶液之间的电势。
两个电极的电势差(电池电动势)是
电池反应的推动力。
E 池 = E(+) – E(-)
2.标准H电极和标准电极电势
标准电极电势 是指标准电极的电势。凡是符
合标准条件的电极都是标准电极。
标准态
● ● ●
所有的气体分压均为标准压强 Pθ(101325P)。 溶液中所有物质的活度均为1mol•L-1。 所有纯液体和固体均为Pθ条件下最稳定的单质。
第十一章
氧化还原反应及其应用
第十一章
氧化还原反应
§11.1 基本概念
§11.2 电极电势和电池电动势 §11.3 氧化还原平衡 §11.4 影响电极电势的因素 §11.5 元素电势图及其应用 §11.6 氧化还原滴定法
氧化数
基 本 概 念
氧化还原反应的特征
氧化还原反应的配平
一、氧化数 (Oxidation mumber)
Q = nF W电池 = nFE
DrG = –nFE
DrG = –nFE
例:试根据下列电池写出反应式并计算在298K
时电池的E 值和ΔrG 值.
(–)Zn|ZnSO4(1mol· –1)||CuSO4(1mol· –1)|Cu(+) L L
解: 电池的氧化–还原反应式:
Zn + Cu2+ Zn2+ + Cu
(d) ―氧化还原”电极 组成: 惰性导电材料 (Pt或石墨) 插入含有同 一元素不同氧化数的两种离子的溶液 Fe2+/Fe3+电极 电极反应: Fe3+ + e– 电极符号: Pt | Fe3+, Fe2+ Fe2+
三、电极电势
1.电极电势的产生
双电层
M(s)
溶解 沉淀
Mn+(aq) + ne
0 2Cl2 + H2O
+0 +0
+1 –1 HClO + HCl
2HClO + 2HCl
+1 –1
Cl2 + Cl2 + 2H2O
从电子的角度:
反应中失去电子(氧化数升高)的物质为还原 剂。还原剂能给出电子促使另一物质获得电子而还
原,自身则失去电子而氧化。
反应中得到电子(氧化数降低)的物质为氧化剂。
Cu2+ + Zn Zn2+ + Cu Zn2+ Zn
共轭的 氧化还 原体系
Cu2+
Cu
(氧化剂) (还原剂) 氧化型物质
电对共同作用的结果
(氧化剂) (还原剂) 还原型物质
氧化还原反应是两个 (或两个以上) 氧化还原
氧化剂降低氧化数的趋势越强, 其氧化能力
越强, 则其共轭还原剂升高氧化数的趋势就 越弱, 还原能力越弱。MnO4– / Mn2+ 还原剂的还原能力越强, 则其共轭氧化剂的 氧化能力越弱Sn4+/Sn2+
配平中的经验处理方法:
酸性介质: O原子多的一边加H+ ,O原子少的一边加 H2O; 碱性介质: O原子多的一边加H2O ,O原子少的一边加 OH ; 中性介质: 左边一律加H2O,右边根据O原子的多少确定加H+或加OH 。
