二茂铁制备过程中的分离与提纯(台州市公开课)
高效液相色谱法手性分离二茂铁衍生物

高效液相色谱法手性分离二茂铁衍生物徐峰;万晓龙;王军锋;康经武【摘要】The method for the enantioseparation of ferroence derivatives,four derivatives with single chirality and three derivatives with double chiralities containing centre and face chirality , on chiral stationary phases,namely Chiralpak IC( cellulose-tris( 3,5-dichlorobenzene carba-mate))and Chiralpak IE3(amylose-tris(3,5-dichlorobenzene carbamate)),was investigated. We found that the three derivatives of the four chiral ferroence derivatives with single chirality can be baseline separated on Chiralpak IE3;another one can be baseline separated on Chiral-pak IC. Meanwhile,the three chiral ferroence derivatives with double chiralities can be baseline separated on Chiralpak IC. The research shows that the both kinds of chiral stationary phases exhibited high enantiomeric recognition capability to the enantiomers of the chiral ferroence derivatives. This two chiral stationary phases exhibited complementary selectivities in the enan-tioseparation of chiral ferroence derivatives. This study provides a reference method for the enantioseparation of chiral ferroence derivatives.%建立了4个单手性和3个双手性(含有手性中心和面手性)的二茂铁衍生物在Chiralpak IC(纤维素-三(3,5-二氯苯基氨基甲酸酯))和 Chiralpak IE3(直链淀粉-三(3,5-二氯苯基氨基甲酸酯))手性固定相上的高效液相色谱分离方法。
光度滴定法测定二茂铁

光度滴定法测定二茂铁
二茂铁的光度滴定法测定
二茂铁(ferrocene)是一种五元杂环化合物,以二茂烯(ferrocene)命名,其
分子内部有两个连接起来的茂环,并且它是一种均相金属有机物,通常需要有特殊的分析方法来测定其中的成分。
而光度滴定法就是常见的测定二茂铁的方法之一。
光度滴定法的测定过程一般是:首先将样品进行稀释,水加入缓冲液,在pH
范围内定量前处理后滴定;然后,将反应管中加入含有苯甲醛(PCC)和甲酸(用于滴定)等溶液,使用适当吸光度计去测量反应后溶液的光谱;最后,根据吸光度读数结果,计算出样品中的二茂铁含量。
光度滴定法测定二茂铁的优点有很多,其中最重要的是操作简便,效率高,而且精确度、准确度很高,因此被广泛用于二茂铁的测定中。
此外,光度滴定法的定性测试也能够鉴别出样品中的其它有机组分或者金属元素,比较适合高精度高效率的实验要求。
另外,在光度滴定法中,采用pH值缓冲及滴定,需要使用相应的试剂,此时
质量及纯度要高,这对光度滴定的准确度有着至关重要的影响。
同时,也需要注意一定的安全措施,确保实验过程中的安全。
由此可见,光度滴定法是一种比较简单、高效的测定二茂铁的分析方法,它的准确度高,应用价值大,可满足高精度实验的要求,因此在分析实验中被广泛使用。
二茂铁制备实验报告

华南师范大学实验报告学生姓名吴健华学号20102401046专业化学(师范) 班级10化学五班课程名称化学综合实验实验类型:□验证□设计√综合实验时间2014 年 3 月27 日指导老师郑盛润老师预习码:54074 实验评分二茂铁的绿色合成一、前言1.1.实验目的(1)了解一些易对环境造成污染的化合物的绿色合成方法,力求把对环境的影响降到最低限度,培养学生在从事科研与生产活动中绿色、环保理念。
(2)掌握用微型合成装置合成、提取二茂铁的操作技术。
(3)学会通过熔点的测定、红外光谱等手段来分析鉴定二茂铁。
1.2.背景知识二茂铁又叫双环戊二烯基铁,学名二环戊二烯基铁,是由两个环戊二烯基阴离子和一个二价铁阳离子组成的夹心型化合物。
其分子式为(C5H5)2Fe,分子量为186,外观为橙黄色针状或粉末状结晶,具有类似樟脑的气味,不溶于水,溶于甲醇、乙醇、乙醚、石油醚、汽油、煤油、柴油、二氯甲烷、苯等有机溶剂。
其分子呈极性,具有高度热稳定性、化学稳定性和耐辐射性,溶于浓硫酸中,在沸腾的烧碱溶液和盐酸中不溶解,不分解。
在化学性质上,二茂铁与芳香族化合物相似,不容易发生加成反应,容易发生亲电取代反应,可进行金属化、酰基化、烷基化、磺化、甲酰化以及配合体交换等反应,从而可制备一系列用途广泛的衍生物。
目前,二茂铁的制备方法主要可分化学合成法和电解合成法两大类。
化学合成法:化学合成法主要有环戊二烯钠法、二乙胺法、相转移催化法、二甲基亚砜法等。
电解合成法:在直流电的作用下,用恒电流法或恒电压法,以铁板和镍板作电极。
随着各种合成技术的出现,其衍生物也多达数百种,因此其用途越来也越来越广。
二茂铁及其衍生物在生活的应用非常广泛,概括的来讲,主要有以下几个方面:作燃料的添加剂,将二茂铁加到燃料中可能起到助燃、消烟以及抗震的作用;作催化剂,二茂铁可作为合成氨以及高分子过氧化物分解的催化剂;在生化和分析上的应用,二茂铁可用于银、钒、汞、铅、金等元素的安培滴定法分析中;作塑料、橡胶等高分子聚合物的添加剂,将二茂铁加到聚乙烯中可以改善聚乙烯电稳定器涂层的效果;此外, 二茂铁还可用于农业、机械等。
_二茂铁烷基碳正离子与硫代乙酸钾的反应研究

2011年第31卷有机化学V ol. 31, 2011第2期, 239~241 Chinese Journal of Organic Chemistry No. 2, 239~241* E-mail: baoguol @Received June 20, 2010; revised August 12, 2010; accepted September 27, 2010.内蒙古自然科学基金(Nos. 200308020103, 2009BS0204)资助项目.240有机化学V ol. 31, 2011Scheme 11.2 α-二茂铁烷基碳正离子的制备在100 mL三口瓶中, 加入4.35 mmol α-二茂铁烷基醇和40 mL二氯甲烷使之溶解, 冰水冷却并搅拌, 滴加26.10 mmol三氟化硼乙醚溶液, 溶液立即变为深红褐色, 继续搅拌5 min, 即可形成碳正离子, 不需提纯直接用于下步反应.1.3 α-二茂铁烷基碳正离子与硫代乙酸钾的反应在250 mL三口瓶中, 加入43.50 mmol硫代乙酸钾, 用30 mL二甲亚砜溶解, 再加入少量二氯甲烷, 然后把制得的碳正离子溶液滴加到三口瓶中, 溶液由深红褐色立刻变为桔黄色, 滴加完毕, 继续搅拌30 min (TLC监测反应完全), 反应混合物依次用等体积水、饱和食盐水、水洗, 无水Na2SO4干燥, 过滤, 减压除去溶剂, 残余物于碱性氧化铝柱层析(100~200目)分离纯化(石油醚作洗脱剂), 得产物α-二茂铁基硫代乙酸酯3a~3h.3a: 黄色液体, 产率80%. 1H NMR (500 MHz, CDCl3) δ: 1.64 (d, J=6.5 Hz, 3H), 2.33 (s, 3H), 4.13~4.38 (m, 9H), 4.59 (q, J=6.5 Hz, 1H); IR (KBr) ν: 3093, 2972, 2929, 1687, 1107, 1001, 819, 632 cm-1. Anal. calcd for C14H16FeSO: C 58.34, H 5.59; found C 58.47, H 5.64.3b: 黄色固体, 产率82%. m.p. 70~71 ℃; 1H NMR (500 MHz, CDCl3) δ: 1.04 (t, J=7.0 Hz, 3H), 1.80 (q, J=7.0 Hz, 2H), 2.38 (s, 3H), 4.14~4.21 (m, 9H), 4.46 (m, 1H); IR (KBr) ν: 3100, 2970, 2929, 1683, 1103, 1000, 823, 631 cm-1. Anal. calcd for C15H18FeSO: C 59.61, H 6.00; found C 59.73, H 6.02.3c: 黄色液体, 产率80%. 1H NMR (500 MHz, CDCl3) δ: 2.34 (s, 3H), 4.07~4.23 (m, 9H), 5.70 (s, 1H), 7.27~7.42 (m, 5H); IR (KBr) ν: 3091, 2954, 2924, 1689, 1105, 1001, 819, 631 cm-1. Anal. calcd for C19H18FeSO: C 65.15, H 5.18; found C 64.42, H 5.18.3d: 黄色液体, 产率88%. 1H NMR (500 MHz, CDCl3) δ: 2.37 (s, 3H), 3.91 (s, 3H), 4.11~4.25 (m, 9H), 6.12 (s, 1H), 7.26~7.29 (m, 2H), 7.36~7.38 (m, 2H); IR (KBr) ν: 3092, 2994, 2958, 2925, 1696, 1130, 1002, 818, 622 cm-1. Anal. calcd for C20H20FeSO2: C 63.17, H 5.30; found C 62.74, H 5.34.3e: 黄色液体, 产率89%. 1H NMR (500 MHz, CDCl3) δ: 2.34 (s, 3H), 2.38 (s, 3H), 4.15~4.33 (m, 9H), 5.68 (s, 1H), 7.15~7.16 (m, 2H), 7.28~7.32 (m, 2H); IR (KBr) ν: 3093, 2994, 2922, 1694, 1512, 1131, 1105, 1002, 958, 822, 746, 624 cm-1. Anal. calcd for C20H20FeSO: C 65.94, H 5.53; found C 65.67, H 5.58.3f: 黄色液体, 产率85%. 1H NMR (500 MHz, CDCl3) δ: 2.35 (s, 3H), 4.14~4.35 (m, 9H), 5.65 (s, 1H), 7.29~7.37 (m, 4H); IR (KBr) ν: 3093, 2958, 2924, 1688, 140, 1133, 1099, 1008, 823, 752, 630 cm-1. Anal. calcd for C19H17FeSOCl: C 59.32, H 4.45; found C 59.02, H 4.46.3g: 黄色液体, 产率86%. 1H NMR (500 MHz, CDCl3) δ: 2.35 (s, 3H), 4.14~4.19 (m, 9H), 5.63 (s, 1H), 7.29~7.31 (m, 2H), 7.45~7.47 (m, 2H); IR (KBr) ν: 3092, 2992, 2923, 1670, 1486, 1133, 1106, 1006, 823, 749, 628 cm-1. Anal. calcd for C19H17FeSOBr: C 53.18, H 3.99; found C 52.95, H 4.01.3h: 黄色固体, 产率80%. m.p. 149~150 ℃; 1H NMR (500 MHz, CDCl3) δ: 2.42 (s, 3H), 4.12~4.15 (m, 18H), 5.51 (s, 1H); IR (KBr) ν: 3083, 2923, 2887, 1684, 1137, 1104, 1000, 818 cm-1. Anal. calcd for C23H22Fe2SO: C 60.29, H 4.84; found C 60.06, H 4.87.2 结果与讨论2.1 溶剂的选择由于硫代乙酸钾的溶解性问题, 实验中首先选则极性较大、溶解性较好的甲醇, DMSO, DMF作溶剂. 研究发现, 使用甲醇作溶剂, 双二茂铁甲基碳正离子能与硫代乙酸钾较好地作用, 生成的双二茂铁甲基硫代乙酸酯的产率较高, 分离提纯容易; 而另外7种α-二茂铁烷基碳正离子与硫代乙酸钾反应得到的产物分离提纯较困难, 这是由于甲醇作亲核试剂也参与了反应, 与硫代乙酸钾形成竞争, 无法达到预期目标. 而以DMF作溶剂, 同样和活性较高的碳正离子发生亲核反应. 选用亲核性较小的DMSO作溶剂, 避免了溶剂参与竞争反应, 反应效率和产率均大幅度提高, 产率由53%提高到80%. 另外, 由于二茂铁烷基碳正离子在二氯甲烷中制备得到, 综合考虑, 最终选择DMSO/CH2Cl2混合溶剂.2.2 反应投料比的选择二茂铁烷基碳正离子和双二茂铁甲基碳正离子的稳定性差异, 决定了投料比的不同. 因为前者稳定性较后者差, 则前者形成消耗的BF3的量也就相应的有所提No. 2陈树峰等:α-二茂铁烷基碳正离子与硫代乙酸钾的反应研究241高, 结果列于表1中. 研究结果表明, 醇、BF 3• Et 2O 、硫代乙酸钾的适宜物质的量比选择分为两种情况: 其一, 前七种醇生成碳正离子消耗的BF 3•Et 2O 较多, 采取物质的量比为1∶6∶10 (表1, Entry 3)即可; 其二, 由于双二茂铁甲基碳正离子较稳定, 其生成需消耗较少的BF 3, 实验结果表明1∶2∶4的物质的量比为最佳比例(表1, Entry 6).表1 投料比对反应产率的影响Table 1 Effect of molar ratio of raw materials on the yields Entry Product n 醇∶n BF 3∶n KSAc Yield/%1 3a 1∶6∶6 532 3a 1∶6∶8 653 3a 1∶6∶10 804 3a 1∶6∶12 79 53h1∶2∶2 496 3h 1∶2∶4 807 3h 1∶2∶6 802.3 反应温度的控制一方面, 鉴于碳正离子的反应活性较高, 本文首先采取冰水冷却; 另一方面, 由于碳正离子与硫代乙酸钾反应时存在明显的放热现象, 为了避免副反应,实验需要低温冷却, 但DMSO 的凝固点较低, 低温条件下, 反应体系有结块现象. 综合考虑, 最终选取适宜的反应条件是先低温冷却片刻, 然后室温反应. 2.4 取代基对反应的影响不同α-二茂铁烷基碳正离子与硫代乙酸钾的反应结果见表2. 表2 α-二茂铁烷基碳正离子与硫代乙酸钾的反应Table 2 The reaction of α-ferrocenylalkyl carbocations withpotassium thioacetateEntry Compd. R Yield a /%1 3a CH 3 802 3b CH 2CH3 823 3c Ph 804 3d p -CH 3OC 6H 4 885 3e p -CH 3C 6H 4 896 3f p -ClC 6H 4 857 3g p -BrC 6H 4 868 3h Fc 80a 分离纯化后的产率.从表2可以看出, 当R 基为烷基和苯基时, 所得产物产率相当(80%~82%); 而当苯环上有供电子基或邻对位定位基时, 反应的产率稍稍增加; 对于双二茂铁甲基碳正离子而言, 虽然其空间位阻有所增加, 但反应产率仍可达80%.3 结论本文以二茂铁甲醇衍生物为底物, 在BF 3•Et 2O 作用下形成相应的碳正离子, 不需从溶液中提纯, 即可与硫代乙酸钾反应得到取代产物α-二茂铁基硫代乙酸酯. 合成方法操作简便, 处理方便, 为α-二茂铁基硫代乙酸酯的合成提供了一条可行的途径. References1 Tverdoklebov, V. P.; Polyakova, N. Y.; Tselinski, I. V. Zh . Org . Khim . 1986, 22, 1393.2 Bove, V. I.; Lyubich, M. S.; Larina, S. M. Zh . Org . Khim .1985, 21, 2195. 3 Li, B.-G.; Zhao, W.; Cao, L.-Z. Chin . J . Appl . Chem . 2002,19, 1142 (in Chinese). (李保国, 赵蔚, 曹立志, 应用化学, 2002, 19, 1142.)4 Edelmann, F.; Behrens, P.; Behrens, S.; Behrens, U. J . Organomet . Chem . 1986, 310, 333.5 Dahard, R.; Misterkiewicz, B.; Patin, H.; Wasielewski, J. J .Organomet . Chem . 1987, 328, 185.6 Bove, V. I. Zh . Org . Khim . 1985, 21, 636.7 Zou, C.; Wrighton, M. S. J . Chem . Soc . 1990, 112, 7579. 8 Abram, T. S.; Watts, W. E. J . Chem . Soc ., Perkin Trans . 11975, 113.9 Temerov, S. A.; Sachivkoa, A. V. Zh . Org . Khim . 1988, 24,2268. 10 Bildstein, B.; Denifl, P.; Wurst, K. J . Organomet . Chem . 1995, 496, 175. 11 Li, B.-G.; Bian, Z.-X.; Cao, L.-Z.; Zhao, W. Chin . J . Appl . Chem . 2001, 18, 877 (in Chinese).(李保国, 边占喜, 曹立志, 赵蔚, 应用化学, 2001, 18,877.)12 Li, B.-G.; Gao, D.-W.; Cao, L.-Z.; Zhao, W. Chin . J . Org .Chem . 2002, 22, 56 (in Chinese). (李保国, 高岱巍, 曹立志, 赵蔚, 有机化学, 2002, 22, 56.) 13 Hu, R.-J.; Li, B.-G.; Cao, L.-Z. Li, S.-C. Chin . J . Org .Chem . 2006, 26, 368 (in Chinese). (胡瑞珏, 李保国, 曹立志, 李树臣, 有机化学, 2006, 26, 368.)14 Pauson, P. L.; Watts, W. E. J . Chem . Soc . 1962, 764, 3880.(Y1006203 Lu, Y .; Dong, H.)。
乙酰二茂铁的制备与初分离

乙酰二茂铁的制备与初分离摘要:本实验先用升华法纯化二茂铁,再用Friendel-Crafts酰基化反应来制备乙酰二茂铁;在分离提纯的时候采用柱色谱分离的方法得到产品后用显微熔点仪测定产品的熔点。
关键字:乙酰二茂铁、Friendel-Crafts酰基化反应、柱色谱分离、显微熔点仪背景:1、乙酰二茂铁介绍分子式:C12H12FeO 分子量:228.072、物化性质:性状:橙黄色固体熔点:81-86℃纯净物熔点为85℃相对密度:1.014g/cm3溶解性:insoluble3、用途:二茂铁是一种金属有机化合物,它是火箭固体燃烧过程的加速剂、柴油的消烟节能添加剂、汽油抗爆助燃剂;各类重质燃料、煤、原油、聚合物等的消烟促然剂。
目前约90%的二茂铁是作为燃烧添加剂消耗的。
实验过程一、实验原理1、二茂铁又名双环戊二烯基铁,是由2个环戊二烯负离子和一个二价铁离子键合而成。
二茂铁具有类似苯的一些芳香性,比苯更容易发生亲电取代反应。
以乙酸酐为酰化剂,三氟化硼,氢氟酸或磷酸为催化剂,二茂铁可以发生Friendel-Crafts酰基化反应,主要生成一元取代物及少量1,1,-二元取代物。
2、本实验通过柱色谱“湿法装柱,干法上样”分离来提纯产品,主要是根据二茂铁、乙酰二茂铁和1,1,-二乙酰二茂铁对硅胶的吸附能力的差异而进行分离提纯。
二、仪器与试剂仪器:柱色谱管、量筒、漏斗、旋转蒸发仪、锥形瓶、圆底烧瓶、载玻片、镊子、显微熔点仪、直形冷凝管、沙芯漏斗、干燥管试剂:硅胶、二茂铁、石英砂、石油醚、无水乙醚、乙酸酐、磷酸三、实验步骤1、二茂铁的纯化将3g 二茂铁置于坩埚中,在坩埚上方放上一张已经扎好孔的滤纸,再盖上普通漏斗,并在漏斗下方塞上一团棉花。
用酒精灯加热坩埚,待坩埚内无固体后即可。
2、乙酰二茂铁的合成在50ml圆底烧瓶中,加入1.5g二茂铁和5ml乙酸酐,在振荡下用滴管慢慢加入1ml 85%的磷酸。
投料毕,用装有无水氯化钙干燥管的球形冷凝管塞住瓶口,70~80℃水浴上加热20min,并时加振荡。
乙酰基二茂铁的制备

一乙酰基二茂铁的制备与纯化摘要以磷酸为催化剂,乙酸酐作酰化剂,以二茂铁为原料合成一乙酰基二茂铁,并利用柱层析法别离提纯一乙酰基二茂铁。
通过红外光谱对一乙酰基二茂铁进行表征,测定合成的一乙酰基二茂铁的熔点。
关键词二茂铁、一乙酰基二茂铁、酰化、合成引言二茂铁又称双环茂二烯基铁, 它是一种具有夹心结构的金属有机化合物, 在常温下呈橙色结晶状,二茂铁及其衍生物有很高的辛烷值及抗爆性, 在催化、电化学、功能材料、医药、添加剂等方面具有重要作用【1】, 对研究和开发具有节能、高效、环保型产品具有深远的经济意义和社会意义。
乙酰基二茂铁是合成二茂铁衍生物的重要中间体,其合成方法代表性的有: 在磷酸催化下用乙酐酰化二茂铁【2】【3】;有三氟化硼催化下在二氯甲烷中用乙酐酰化二茂铁〔乙酰化产率高,但原料不易得〕; 在活性氧化铝存在下,用三氟乙酸-醋酸对二茂铁进行酰化;在二氯甲烷中以三氯化铝为催化剂,乙酰氯为酰化剂对二茂铁进行酰化【4】,但产物中二乙酰基二茂铁所占比例较高,不易提纯。
本实验以磷酸为催化剂,乙酰酐为酰化剂,利用二茂铁的酰化反应原理合成一乙酰基二茂铁,原料易得且操作方便,得到的产品经表征纯度较高,比较满意。
实验部分1.实验原理二茂铁容易发生亲电取代反应,如Friedel-Crafts反应,但对氧化的敏感性限制了它在合成中的应用,二茂铁的反应通常在隔绝空气下进行。
本实验由二茂铁与乙酐发生酰基化反应制备一乙酰基二茂铁,反应原理如下:并通过柱层析法别离提纯一乙酰基二茂铁,主要是根据二茂铁、一乙酰基二茂铁以及1,1'-二乙酰基二茂铁在硅胶上被吸附的牢靠程度的差异来实现的。
2.主要仪器及试剂仪器:提纯〔蒸发皿、滤纸、漏斗〕合成〔圆底烧瓶、干燥管、电热套、铁架台〕柱色谱别离〔外表皿、锥形瓶、圆底烧瓶、层析柱〕试剂:提纯〔二茂铁粗产品3g〕合成〔1.5g(0.0054mol)二茂铁、5.25g(5.0mL,0.10mol)乙酸酐、1ml85%磷酸、碳酸氢钠固体〕柱色谱别离〔石油醚、乙醚、石英砂、硅胶100~200目〕3.实验步骤3.1提纯二茂铁取粗制二茂铁(橙红色)3g置于干燥蒸发皿中间,蒸发皿上覆盖一张刺有小孔的滤纸,使小孔朝上,再在滤纸上罩一个大小合适的三角漏斗,漏斗颈部塞一小团蓬松的棉花〔如下图〕,用酒精灯隔着石棉网小心加热,实现空气浴,使二茂铁升华。
二茂铁的合成,分离与鉴定

二茂铁的合成1、环戊二烯的解聚:原因:环戊二烯久存后会聚合为二聚体,使用前应重新蒸馏使其解聚为单体。
组装好仪器,在烧瓶中加入25ml环戊二烯,在接收瓶中加入少量的无水氯化钙;电热套加热,收集40---44℃的馏分。
反应方程式:2、氯化亚铁的制备在250ml烧杯中加入25ml36﹪盐酸和18ml蒸馏水,在通风橱中加热至70℃,缓慢分批加入4g还原铁粉,待反应基本停止后(不再有氢气放出),过滤,滤液中加入用浓盐酸洗去铁锈的小铁钉几枚。
滤液放在蒸发皿中用酒精灯加热蒸发,然后冷却结晶,迅速抽滤,称5g加入100ml乙醚中供合成二茂铁使用。
注:FeCl2·4H2O为浅蓝色透明晶体总结:氯化亚铁制备时小铁钉应直到加热蒸发后,冷却结晶了才取出。
3.二茂铁的合成在装有搅拌器,滴液漏斗的干燥的150ml三颈烧瓶中加入17g片状氢氧化钾和40ml无水乙醚,搅拌10min,使KOH尽可能溶解,在加入4ml环状二烯,继续搅拌20min,使其生成环戊二烯钾:C5H6+KOH→C5H5K+H2O反应中生成的水应用过量的氢氧化钾除去。
在烧杯中加入17ml二甲亚砜和2ml无水乙醚,再加入5g新制的氯化亚铁,在40℃水浴上温热片刻,搅拌使其溶解。
然后将此液移入事先加有2ml无水乙醚的滴液漏斗中,在搅拌下滴加入反应瓶中,控制滴加速度,约15—20min 内加完;继续搅拌1h后分出乙醚层,水相用20ml无水乙醚分两次萃取,合并乙醚层,用2mol/L HCl洗涤醚液两次,然后用水洗涤两次,最后用无水硫酸钠干燥。
在旋转蒸发器上蒸去乙醚后倒入蒸发皿中升华的纯二茂铁。
总结:升华过程应在20—30分钟完成,不宜过快,否则不纯,用空气浴加热升华是若是出现黑烟或是滤纸变黑即是升华过快,要得到较纯的二茂铁应重新升华,最后蒸发皿中剩下色物质。
二茂铁的分离二、二茂铁的柱层析分离1.拌样称取上述粗产品20mg置于干燥小烧杯中,滴加乙酸乙酯使溶解,加入约200mg硅胶,搅拌均匀得浆状物,红外灯下干燥得到松散的颗粒状物。
二茂铁的电化学制备原理

二茂铁的电化学制备原理二茂铁是一种重要的过渡金属有机配合物,具有良好的电化学性质,因此在电化学制备中得到了广泛的应用。
本文将探讨二茂铁的电化学制备原理及其应用。
二茂铁的电化学制备是通过在电解质中施加电流,使得二茂铁发生氧化还原反应而得到的。
在电解质溶液中,二茂铁可以在电极表面发生氧化还原反应。
当施加正电位时,二茂铁会被氧化为二茂铁阳离子,反应如下:Fe(C5H5)2 + e- -> Fe(C5H5)2+而当施加负电位时,二茂铁阳离子会被还原为二茂铁,反应如下:Fe(C5H5)2+ + e- -> Fe(C5H5)2通过控制电位和电流密度,可以实现二茂铁的氧化和还原反应,从而使得二茂铁在电极表面进行电化学反应,得到所需的产物。
二茂铁的电化学制备原理可以归结为以下几个方面:1. 氧化还原反应:二茂铁的电化学制备过程中,氧化还原反应是关键的步骤。
通过在电解质溶液中施加适当的电位,可以使得二茂铁发生氧化还原反应。
2. 电极材料选择:在电化学制备中,电极材料的选择对反应过程具有重要影响。
通常情况下,以铂、金、碳等为电极材料,能够提供良好的电化学活性表面,促进反应的进行。
3. 电解质选择:电解质溶液的选择也是电化学制备中必不可少的要素。
电解质溶液应具有适当的离子浓度和稳定性,以保证反应的进行和产物的纯度。
4. 反应条件控制:在电化学制备中,反应条件的控制非常重要。
包括施加的电位、电流密度、反应时间和温度等因素。
合理控制这些条件,能够调控反应速率和产物的选择性。
二茂铁的电化学制备具有许多优点,如反应过程可控性强、产物纯度高、反应效率高等。
因此,二茂铁的电化学制备在有机合成、电化学储能等领域具有广泛的应用前景。
在有机合成中,二茂铁的电化学制备可以用于合成具有特殊结构和性质的有机分子。
通过控制反应条件和电化学环境,可以实现对反应过程的精确控制,从而得到所需的产物。
在电化学储能中,二茂铁被广泛应用于电池和超级电容器等能量储存器件中。
乙酰二茂铁的合成与分离实验-学生用

有机合成与制备实验实验一 乙酰二茂铁的合成一、实验目的:1. 通过乙酰二茂铁的合成,了解用Friendel-Crafts 酰基化反应制备非苯芳酮的原理和方法。
2. 学习用薄层色谱跟踪反应进程和检测产品纯度的方法。
二、实验原理:二茂铁,又称二环戊二烯合铁、环戊二烯基铁,是一种具有芳香族性质的有机过渡金属化合物。
二茂铁是最重要的金属茂基配合物,也是最早被发现的夹心配合物,包含两个环戊二烯环与铁原子成键。
常温下为橙黄色粉末,有樟脑气味。
熔点172°C-174°C ,沸点249°C ,100°C 以上能升华;不溶于水,易溶于苯、乙醚、汽油、柴油等有机溶剂。
与酸、碱、紫外线不发生作用,化学性质稳定,400°C 以内不分解。
其分子呈现极性,具有高度热稳定性、化学稳定性和耐辐射性,其在工业、农业、医药、航天、节能、环保等行业具有广泛的应用。
二茂铁是火箭固体燃烧过程的加速剂、柴油的消烟节能添加剂、汽油抗爆助燃剂等。
目前约90%的二茂铁是作为燃烧添加剂消耗的。
二茂铁具有类似苯的一些芳香性,比苯更容易发生亲电取代反应,例如Fridel-Crafts 反应:由于二茂铁分子中存在亚铁离子,对氧化的敏感限制了它在合成中的应用,如不能用混酸对其硝化。
一般认为,如用无水三氯化铝为催化剂,酰氯或酸酐为酰化剂,当酰化剂与二茂铁的摩尔比为2:1时,反应物以1,1’-二元取代物为主。
以乙酸酐为酰化剂,三氟化硼、氢氟酸或磷酸为催化剂,主要生成一元取代物。
在此反应条件下,主要生成单乙酰二茂铁,双乙酰二茂铁很少,但同时有未反应的二茂铁,利用层析分离法可以在混合物中分离这几种配合物,先使用薄层层析探索分离这些配合物的层析条件,然后利用这些条件在柱层析中分离而得到纯的配合物。
薄层层析是将吸附剂均匀地铺在一块玻璃板表面形成薄层(其厚度一般为33H 3二茂铁乙酰二茂铁1,1'-二乙酰基二茂铁32(CH 3CO)2O 磷酸0.1~2mm),在此薄层上进行色谱分离的方法。
乙酰二茂铁的制备及柱色谱分离

乙酰二茂铁的制备及柱色谱分离【摘要】通过本实验将了解半微量实验的操作方法,掌握柱色谱分离和提纯化合物的原理和技术,通过乙酰二茂铁的制备理解Friedel-Crafts酰基化反应原理。
本实验还将对之前实验所得的部分产品运用毛细管法进行熔点测定。
【关键词】乙酰二茂铁、Friedel-Crafts酰基化反应、柱色谱分离、毛细管法熔点测定。
【引言】(一)实验原理二茂铁又名双环戊二烯基铁,是由两个环戊二烯负离子和一个二价铁离子键合而成。
二茂铁具有类似苯的一些芳香性,比苯更容易发生亲电取代反应。
以乙酸酐为酰化剂,三氟化硼、氢氟酸或磷酸为催化剂,二茂铁可以发生Friedel-Crafts酰基化反应,主要生成一元取代物及少量1,1’-二元取代物。
本实验通过柱层析分离提纯产品,主要是根据二茂铁、乙酰二茂铁和1,1’-二乙酰二茂铁对硅胶的吸附能力的差异而进行分离提纯。
常用的柱层析色谱和薄层层析色谱均属于吸附色谱,因此用薄层层析可以筛选出适宜的柱层析洗脱剂。
本次实验对熔点的测定主要根据原理:熔点是1atm条件下,固体化合物从固态变为液态时的温度。
(二)反应式【实验部分】(一)实验仪器1.层析柱图1 层析柱示意图2.毛细管法测熔点图2 提勒管(b形管),浓硫酸作热浴(二)试剂及产物(三)实验步骤一. 乙酰二茂铁的制备称取150mg(0.81mmol)二茂铁,放入25ml茄形瓶中,加入1.0mL(1.08g,10mmol)醋酸酐。
安装装有无水氯化钙干燥管的空气冷凝管。
沸水浴加热并搅拌使二茂铁溶解。
稍冷,打开塞子迅速加入0.5mL 85% H3PO4,反应液变成红黑色。
由于第一次实验将水漏入,故重新合成。
于沸水中加热搅拌8--10min。
趁热用滴管将反应液滴入盛有约2g碎冰的烧杯中,搅拌下用Na2CO3饱和水溶液小心中和至无气泡产生,得到大量黄色固体和墨绿色溶液。
充分冷却后抽滤,用冷水充分洗涤沉淀至中性,抽干。
在红外灯下烘干。
实验一_华南师范大学实验报告

华南师范大学实验报告【前言】1、实验目的①了解一些易对环境造成污染的化合物的绿色合成方法,力求把对环境的影响降到最低限度,培养学生在从事科研与生产活动中绿色、环保理念。
②掌握用微型合成装置合成、提纯二茂铁的操作技术。
③学会通过熔点的测定、红外光谱等手段来分析鉴定二茂铁。
2、意义由于二茂铁及其衍生物具有广泛的用途,特别是在航天及军事工业上的应用,因而发达国家发展迅速。
我国从20世纪60年代开始研制二茂铁,但生产和衍生物的开发应用方面均较落后,年产量约2kt,而国内年需求量约为7.5kt,产不足需。
随着二茂铁在石油、石油切割气、汽油、柴油等方面的应用,二茂铁的特殊作用逐渐被国人所认识,其应用范围将越来越广。
另外,随着我国石油化工的不断发展,C5来源也不断增加,以环戊二烯为原料制备二茂铁,进而开发二茂铁及其衍生物的利用途径,对于合理利用石油化工的C5资源具有一定的现实意义,同时也将推动金属有机化工产品在我国的开发和利用。
因此二茂铁及其衍生物的生产和应用开发在国内将会有一个突破性进展,开发利用前景广阔。
3、文献综述与总结二茂铁(FcH)又名双环戊二烯基铁,学名二环戊二烯基铁,属于金属有机化合物,它是由两个环戊二烯基阴离子和一个二价铁阳离子组成的具有夹心形状的化合物(见图),其分子式为(C5H5)2Fe。
二茂铁易溶于甲醇、乙醇、乙醚、石油醚、汽油、二氯甲烷、苯等常用有机溶剂,溶于浓硫酸,在沸腾的烧碱和盐酸溶液中不溶解、不分解;二茂铁具有高度热稳定性、化学稳定性和耐辐射性;二茂铁具有芳香性,100℃以上能升华,不容易发生加成反应,易发生取代反应;此外二茂铁还有低毒性,在溶液中两个环可以自由旋转等特点。
正是基于二茂铁的这种稳定性、芳香性、低毒、亲油性、富电性、氧化还原性和易取代等特点,使得自二茂铁出现以来就引起了广大科研工作者极大的兴趣,对于二茂铁及其衍生物的合成、结构及性质和应用的研究一直以来都是大家所关注的热点。
二茂铁及其衍生物的合成、应用及展望

二茂铁及其衍生物的合成、应用及展望摘要:二茂铁及其衍生物以其独特的结构和性质而广受关注,作为合成和应用则一直是金属有机化学等学科研究的热点。
本文简要的介绍了二茂铁(η5-C5H5)2Fe)的发现结构和性质,重点介绍了二茂铁的电解合成方法和化学合成方法,以及二茂铁用作燃油添加剂、四乙基铅((C2H5)4Pb)替代剂和作为催化剂等方面的应用,并介绍了几种二茂铁衍生物以及二茂铁衍生物在电化学、医药、液晶材料和功能材料等方面的应用。
同时,本文对二茂铁的研究也做了展望。
关键词:二茂铁;二茂铁衍生物;合成;应用.一、二茂铁的结构与性质1、二茂铁的发现1951年Kealy和Pauson[1]利用格氏试剂C5H5MgBr与催化剂FeCl3合成富瓦烯却意外地获得了一种橙黄色晶体(式1-1),并用重量分析法确定了该化合物分子式:C10H10Fe,并初步测定了该化合物的熔点、沸点等基本物理和化学性质。
与此同时,Miller[2]等人用环戊二烯和铁在300℃,N2氛及常压下也制得了该物质(式1-2)。
反应式如下:Kealy和Pauson初步推断该化合物可能结构:2、二茂铁的结构及性质1952年,Wilkinson[3]等人对该化合物通过红外光谱(IR)、磁化率(cm)及偶极距(μ)等的测定,判定该物质应具有夹心型结构(如图1.1)。
Fischer[4]等人通过X射线衍射的研究,提出该物质具有五角反棱柱的结构。
通过这些研究确定了该物质结构为:上下为两个带负电荷的环戊二烯基芳环,中间为带二价正电荷的亚铁离子,类似于三明治的夹心型结构,并正式命名为“Ferrocene(二茂铁)”。
在该结构中,亚铁离子处于激发态,这使得二茂铁具有多种催化性能[5]。
(图1.1)二茂铁(Ferrocene,(η5-C5H5)2Fe),一种典型的过渡金属与茂环生成的具有芳香族性的有机金属化合物,分子式为:(C5H5)2Fe,遵循有效原子序数(EAN)规则,具有18电子稳定结构;常温下为橙黄色粉末或晶体,有樟脑气味,熔点172℃-174℃,沸点249℃,100℃以上能升华;不溶于水,易溶于甲醇、乙醇、乙醚、二氯甲烷和苯等有机溶剂,可溶于浓硫酸,在沸腾的烧碱和盐酸溶液中不溶解、不分解;具有高度热稳定性,400℃下不分解;化学性质稳定、耐辐射性,与酸、碱、紫外线等均不发生作用;具有芳香性,不易发生加成反应,易发生亲电取代反应、可发生氧化反应、还原反应和亲核取代反应;可进行金属化、酰基化、烷基化、磺化、甲酰化以及配合体交换等反应;此外二茂铁还有低毒性,在溶液中两个环可以自由旋转等特点[6-8]。
化学离子方程式

二茂铁及其衍生物的合成和色谱分离一.实验目的1. 了解二茂铁及其衍生物的合成方法和有关性质:2. 熟悉并掌握色谱分离的实验技术.二. 实验原理二茂铁又名环戊二烯合铁,是环状多烯烃和过渡金属形成的配合物中最有代表性的一种化合物。
在二茂铁分子中,二价铁离子被夹在两个平面环之间,二价铁离子与环戊二烯环形成牢固的配位键。
在固态时,两个环戊二烯互为交错构型.在溶液中,两个环可以自由旋转。
二茂铁还具有芳香性,在环上能形成多种取代基的衍生物。
二茂铁在常温下为橙色晶体,有樟脑气味,熔点为173~174`C,沸点为249`C,高于100`C就容易升华,加热至400`C也不分解;对碱和非氧化性酸稳定,能溶于苯、乙醚、石油醚等大多数有机溶剂中,基本上不溶于水。
在乙醇或己烷中的紫外光谱于250nm和440nm处有极大吸收值,在225nm处也有吸收峰。
本实验采用环戊二烯、氢氧化钾和氯化亚铁为原料合成二茂铁。
然后在磷酸催化下与乙酰发生Fridle-Crafts酰基化反应生成二茂铁的衍生物乙酰二茂铁。
由于产物含有一定量未反应的二茂铁,可用色谱法进行分离。
2FeCl3+Fe->3FeCl2C5H6+FeCl2->Fe(C5H5)2乙二胺在反应中作为碱,促使环戊二烯转变为环戊二烯阴离子C5H6+NH(C2H5)2->C5H5-N+H2(C2H5)2三.实验仪器与试剂三颈烧瓶(150mL)、滴液漏斗、直型冷凝管、砂芯漏斗、梨形具刺分馏烧瓶、烧瓶(50mL)、接受瓶、烧杯(250mL)、蒸发皿、布氏漏斗、搅拌器、高型烧杯、干燥管、旋转蒸发仪、恒压漏斗、柱色谱管,小抽滤瓶、电热套、温度计。
环戊二烯、二甲亚砜(DMSO)、氢氧化钾、氯化亚铁(FeCl2.4H2O)、乙酐、磷酸、无水乙醚、GF硅胶、苯、丙酮、乙酸乙酯、石油醚、无水氯化钙、36%盐酸、蒸馏水、铁粉、小铁钉、片状氢氧化钾、无水硫酸钠、85%磷酸、固体碳酸氢钠、石英砂。
四.实验步骤1.环戊二烯的解聚按如图安装仪器,在烧瓶中加入环戊二烯,接受瓶中加入少量无水氯化钙,收集40`C-44`C左右馏分。
实验八:乙酰二茂铁的制备

实验八 乙酰二茂铁的制备(4学时)一、实验目的1、通过乙酰化二茂铁的制备,了解利用傅列德尔-克拉夫茨( Friedel-Crafts )酰基化反应制备芳酮的原理和方法。
2、进一步巩固重结晶提纯的操作。
二、实验原理二茂铁及其衍生物是一类很稳定而且具有芳香性的有机过渡金属络合物。
二茂铁是橙色的固体,又名双环戊二烯基铁,是由两个环戊二烯基负离子和一个二价铁离子键合而成,具有夹心型结构。
二茂铁及其衍生物可作为火箭燃料的添加剂、汽油的抗爆剂、硅树脂和橡胶的防老剂及紫外线吸收剂等。
二茂铁具有类似于苯的芳香性,其茂基环上能发生多种取代反应,特别是亲电取代反应(例如 Fridel-Crafts 反应)比苯更容易。
因而,二茂铁与乙酸酐反应可制得乙酰二茂铁,但根据反应条件的不同形成的产物可以是单乙酰基取代物或双乙酰基取代物。
由于二茂铁分子中存在亚铁离子,对氧化的敏感限制了它在合成中的应用,如不能用混酸对其硝化。
三、试剂1g (0.0054mol )二茂铁,10.8g (10ml , 0.1mol )乙酸酐,磷酸,碳酸氢钠,石油醚(60—900C )四、步骤1、乙酰二茂铁的制备在100ml 圆底烧瓶中,加入1g 二茂铁和10ml 乙酸酐,在振荡下用滴管慢慢加入2ml 85%的磷酸。
投料毕,用装有无水氯化钙的干燥管塞住瓶口,沸水浴上加热15min ,并时加振荡。
将反应化合物倾入盛有40g 碎冰的400ml 烧杯中,并用10ml 冷水涮洗烧瓶,将涮洗液并入烧杯。
在搅拌下,分批加入固体碳酸氢钠(约需20—25g ),到溶液呈中性为止(要避免溶液溢出和碳酸氢钠过量)。
将中和后的反应化合物置于冰浴中冷却15min ,抽滤收集析出的橙黄色固体,每次用40ml 冰水洗两次,压干后在空气中干燥,用石油醚(60—900C )重结晶,产物约0.3g ,熔点84—850C 。
2、乙酰二茂铁的薄层层析取少许干燥后的粗产物溶于苯,在硅胶G 板上点样,用30:1的苯—乙醇(体积比)作展开剂,层析板上从上到下出现黄色、橙色和红色三个点,分别代表二茂铁、乙酰二茂铁和1,1—二乙酰基二茂铁,测定Rf 值。
二茂铁的电化学制备原理

二茂铁的电化学制备原理二茂铁(ferrocene)是一种具有重要应用价值的有机金属化合物,其电化学制备原理是通过电化学反应将铁离子还原并与环己二烯配体发生配位反应,生成二茂铁。
二茂铁的制备通常使用电解池来实现。
电解池中有两个电极,即阳极和阴极。
电解质溶液通过电解质媒介与两个电极相连。
在制备二茂铁时,阳极通常选择铂电极,而阴极则是钢电极。
电解质溶液中一般含有二茂铁的前体化合物、溶剂和电解质。
制备过程中的关键步骤是在电解质溶液中施加电压。
施加的电压使得阳极上发生氧化反应,阴极上发生还原反应。
具体而言,铁离子在阳极释放电子进入电解质溶液中,并与阴极上产生的电子发生反应。
这些电子首先与配体环己二烯形成配合物,然后与其他铁离子进一步反应,最终形成二茂铁。
同时,在阳极上生成的电子与阳极上的氧气反应,从而维持电解质溶液中的电中和。
二茂铁的电化学制备具有许多优点。
首先,该方法操作简单,所需的设备和试剂也相对简单易得。
其次,制备过程中可以通过调整电解质溶液的成分和反应条件来控制生成物的纯度和产率。
此外,除了生成二茂铁,该方法还能制备其他金属茂配合物。
二茂铁在各个领域有广泛的应用。
在有机合成中,它可用作不同反应的催化剂,如氢化反应、羰基反应等。
此外,二茂铁还可以用作电子传输物质、液晶显示器的彩色染料、防锈剂等。
由于其独特的结构和性质,二茂铁在材料科学、能源储存和转化等领域也具有重要作用。
总之,电化学制备二茂铁是一种简单可行的方法,通过施加电压,将铁离子还原并与配体反应,最终生成二茂铁。
这种方法具有操作简单、可控性强等优势,并且二茂铁在各个领域有广泛应用,给科研工作者提供了丰富的研究方向和应用前景。
二茂铁(Ferrocene)分子模型构建步骤
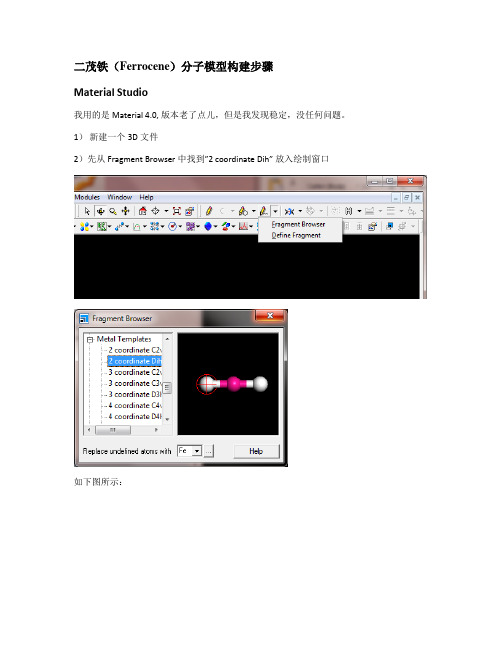
二茂铁(Ferrocene)分子模型构建步骤Material Studio我用的是Material 4.0, 版本老了点儿,但是我发现稳定,没任何问题。
1)新建一个3D文件2)先从Fragment Browser中找到”2 coordinate Dih”放入绘制窗口如下图所示:3)再从”Fragment Browser”中选择Ligand下面的Cyclopentadienyl,添加连接到Fe的两端完成后如果所示:4)下面的一步非常关键,选择“Measure/change”下的“Torsion”然后连接H、第一个五元环的中心、Fe和另外一个环上的H,如下图所示。
5)选择左侧“Property”下Filter的Torsion,然后双击,改角度为36度。
不要跨过Fe而选择两边的两个H和两个中心原子,不然不能修改角度(我也不知道为什么,但是我摸索了很久才发现这个)6)然后再Build下选择Symmetry,Find Symmetry,结果如下:Gaussian View 1)选择五元环:删除C上的两个H然后再添加一个H,结果如图:显示坐标:3)选择Edit菜单中的Point Group,选择Very loose(0.3),然后选择左边的D5h,点击Symmetrize得到结果如下:4)然后在坐标原点(也就是五元环的中心)加入X原子5)现在用Edit->PBC加入第二个五元环:修改C为3.3,修改Cell Replication的c为2添加完第二个五元环后,取消勾选Show Reference Cell Edges和Show Replicate Cell Edges。
6)用二面角编辑工具,选择C2,X11,X22和C13然后修改二面角为36度。
7)再次应用Point Group Symmetry,点击Symmetrize,把坐标原点移到两个五元环中间,在原点处加入Fe原子删除两个X原子和与他们相连的冗余键。
2500吨年二茂铁、3000吨年三聚环戊二烯项目

第一章总论项目名称:****化学工业股份有限公司2500吨/年二茂铁、3000吨/年三聚环戊二烯项目建设单位:****化学工业股份有限公司建设单位负责人:***项目负责人:***第一节编制项目可行性研究报告的依据和原则一、编制依据1、参考《中国石油化工总公司石油化工项目可行性研究报告编制规定》(1997年版)。
2、参考《建设项目经济评价方法与参数》。
3、按鸿飞集团与鸿瑞化工有限公司合作协商会议精神。
二、编制原则1、深入研究科学论证与方案比较,选择出技术先进、经济合理的方案,为投资决策提供可靠依据。
2、坚持走国产化道路,工艺技术立足国内、设备、材料均国内生产制造。
3、本项目的建设用地采取新征土地方式。
4、贯彻执行国家有关环保、消防、安全及工业卫生等方面的法规、政策,使开车后的装臵达到国家劳动安全,环境保护和节约能源的文明工厂。
第二节项目背景、经营体制类别投资意义一、项目背景和经营体制类别二、投资意义和有利条件二茂铁是用途广泛,出口潜力大的精细化工产品。
三聚环戊二烯我国尚无工业化产品,属于补国内空白的高新技术产品。
1、以上两个产品都是以粗双环戊二烯(80%纯度)为原料。
其原料来源十分丰富。
2、国内外有广泛的市场,出口潜力很大。
3、生产工艺技术成熟可靠,不需国外引进可实现清洁文明低碳生产。
4、投资少经济效益显著。
5、本公司技术力量比较雄厚,可确保安全平稳生产。
第三节项目研究范围精双环戊二烯、二茂铁、三聚环戊二烯项目主生产装臵及相关的公用工程及辅助设施。
1、二茂铁装臵1)原料贮运工序2)双环解聚工序3)环戊二烯钠合成工序4)活性氯化亚铁制备工序5)二茂铁合成工序6)产品干燥与粉碎工序7)回收与精制工序8)成品包装工序9)铁泥废渣处理工序2、三聚环戊二烯装臵1)原料贮运工序2)双环解聚与聚合工序3)双环精馏精制工序4)聚合反应工序5)精制精馏工序6)产品包装工序3、配套公用工程及辅助工程1)界区内供配电2)循环水系统3)热水系统4)冷冻水系统5)导热油系统6)冷油循环系统7)界区内消防系统8)采暖、通风系统9)分析化验10) 技术开发中心11)办公及生活设施12)检修维护系统第四节研究结果1、二茂铁产品、三聚环戊二烯产品均有较好的市场需求,产品出口潜力很大,投产后可迅速抢占市场,具有良好前景。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
KOH + C5H6
2 C5H5K + FeCl2
C5H5K+ H2O
(C5H5)2 Fe + 2KCl
C5H6 久存后会聚合为二聚பைடு நூலகம்。
实验步骤一
从环戊二烯二聚体制备环戊二烯单体
如何从环戊二烯二聚体制备环戊二烯单体? 得到的产物如何分离?
实验步骤一
温 度 计 分 馏 柱 a
分馏法制备环戊二烯单体 接收瓶中放入
b
固体干燥剂: 少量CaCl2 , 加 Na2SO4、 热,收集 MgSO4 41℃ ~ 42 ℃ CaCl2 · 2O 6H 馏分约50 mL, Na2SO4 · 2O 10H 备用 MgSO4 · 2O 7H 冷凝水应由 b 口流入
水冷凝管
圆底烧瓶
实验步骤二
氯化亚铁晶体(FeCl2· 2O)的制备 4H
2、已知(NH4)2SO4在水中可溶,在乙醇中难溶。 [C u(NH3)4]SO4· 2O在乙醇· H 水混合溶剂中的溶解 度随乙醇体积分数的变化曲线示意图如下:
下列选项中,最适合作为[C u(NH3)4]SO4· 2O H (含少量(NH4)2SO4 )的洗涤液是 C 。 A.乙醇 B. 蒸馏水 C. 乙醇和水的混合液 D. 饱和硫酸钠溶液
二茂铁制备过程中的 分离与提纯
2012.3.30
二茂铁是最重要的金属茂基配合物,也是最早 被发现的夹心配合物,它掀开了有机金属化学新 的帷幕,1973年慕尼黑大学的恩斯特· 奥托· 菲 舍尔及伦敦帝国学院的杰弗里· 威尔金森爵士因 此被授予诺贝尔化学奖
Fe
二茂铁及其衍生物已广泛地被用 作火箭燃料添加剂、汽油的抗震 剂、硅树脂和橡胶的热化剂、紫 外光的吸收剂等。
实验步骤三
恒 压 滴 液 漏 斗
二茂铁的制备 思考4、每次洗涤后 乙醚层在哪层?如何 从中分离出乙醚层? 如何从乙醚层中分离 出产品?
接液封装置
N2
答:上层、分液操作。
将分液漏斗中的乙醚层转入到 蒸发皿 中 蒸发结晶 (或采用 冷却 结晶的方法)。
实验步骤四
二茂铁的提纯
思考:二茂铁的进一步提纯方法有哪些?
4、正丁醛经催化剂加氢得到含少量正丁醛的 1—丁醇粗品,为纯化1—丁醇,该小组查阅文献 得知:①R—CHO+NaHSO3(饱和) →RCH(OH)SO3Na↓;②沸点:乙醚34℃,1—丁 醇118℃,并设计出如下提纯路线:
饱和NaHSO3溶液 过滤 试剂1为_________,操作1为________,操作2为 萃取 蒸馏 _______,操作3为_______。
升华法提纯二茂铁
或重结晶法提纯二茂铁
3、某混合溶液中NH4ClO4和NaCl的质量分数分 别为0.30和0.l5(相关物质的溶解度曲线见图9)。 从混合溶液中获得较多NH4ClO4晶体的实验操作依 次为(填操作名称) 、干燥。 蒸发浓缩、冷却结晶、抽滤、洗涤
变式、某混合溶液中NH4ClO4和NaCl的质量分数 分别为0.30和0.40(相关物质的溶解度曲线见图 9)。从混合溶液中获得较多NH4ClO4晶体的实验 操作依次为(填操作名称) 、 干燥。 蒸发浓缩、趁热过滤、冷却结晶、抽滤、洗涤
实验步骤三
恒 压 滴 液 漏 斗
二茂铁的制备
接液封装置
N2
思考2、制备环戊二 烯钾的过程中通氮气 与接液封装置的作用 是什么?
答:是为了防止环戊二烯钾被空气中的氧 气氧化而变质。
实验步骤三
恒 压 滴 液 漏 斗
二茂铁的制备
接液封装置
N2
思考3、洗涤的目的 是什么?如何判断产 品已用水洗涤干净?
答:除去二茂铁中易溶于水的杂质。 取最后一次洗涤液,向其中滴入硝酸酸化 的硝酸银溶液,若无沉淀产生,则说明产品 已洗涤干净。
回归课本
《有机化学基础》第50页
思考:已知实验室制得的粗溴苯中含有 少量的杂质溴化氢、溴化铁、溴、苯, 试设计分离和提纯溴苯的实验方案?
试剂 粗溴苯 操作
回归课本
思考:已知实验室制得的粗溴苯中含有 少量的杂质溴化氢、溴化铁、溴、苯, 试设计分离和提纯溴苯的实验方案? 水 NaOH溶液 粗溴苯 下层液体 萃取、分液 萃取、分液 下层液体 水 萃取、分液 蒸馏 溴苯
知识预备
熔点 173~174 ℃, 沸点 249℃,当 温度高于100℃时容易升华, 不溶于水,能溶于乙醚等大多数有 机溶剂,对碱和非氧化性酸稳定 。 乙醚不溶于水,沸点 34.6℃, 液体密度(20℃)为0. 7135g/mL
Fe
实验原理
• 二茂铁的制备方法较多,本实验采用非水 溶剂法,是实验室合成二茂铁的一种较为 简单易行的方法。其制备反应如下
1、取一只小烧杯,放入约4g铁屑,向其中注入 15mL1mol· -1 Na2CO3溶液,浸泡数分钟后, L 用 倾析 法分离并洗涤铁屑,晾干。
2、在小烧杯中放入上述铁屑,并注入15mL浓盐 酸和15mL水,加热至70℃,数分钟后过滤, 将滤液转入蒸发皿中蒸发浓缩至溶液表面出现 晶膜 为止, 冷却结晶 、 抽滤 ,并用少量 酒精 洗涤晶体,取出晶体用干净的滤纸 吸干。 HCl 3、FeCl2· 2O 4H FeCl2 △?
下层液体
无水CaCl2 滤液 过滤
1、已知NaOH 能溶于乙醇,K2FeO4难溶于乙醇, 在水溶液中易水解: 4FeO42- +10H2O 4Fe(OH)3 + 8OH- +3O2↑
提纯K2FeO4 (含少量NaOH)时最好选用的洗涤剂 是 D
A、水 B、KOH溶液、乙醇
C、氯化铵溶液、乙醇
D、乙醇
实验步骤三
恒 压 滴 液 漏 斗
二茂铁的制备
接液封装置
N2
思考1、与普通漏斗 相比从恒压滴液漏斗 中滴加液体的好处有 哪些?
思考1、与普通漏斗相比从恒压滴液漏斗中滴 加液体的好处有哪些?
恒 压 滴 液 漏 斗 普 通 漏 斗 分 液 漏 斗
旋塞 使内外气体相通
旋塞
支管
答:可以控制液体的流速,平衡气压有利 于液体顺利下滴。
晶体洗涤方法小结:
原则:除杂效果好、晶体损失少
1、难溶物的洗涤:用较多水浸没沉淀洗涤2-3次 2、可溶物的洗涤:用少量水(或冰水、酒精) 洗涤2-3次。 用酒精洗涤的好处是:除去晶体表面少量的水, 同时可减少晶体的损失
倾析法过滤 过滤
抽滤
实验步骤二
氯化亚铁晶体(FeCl2· 2O)的制备 4H
1、取一只小烧杯,放入约4g铁屑,向其中注入 15mL1mol· -1 Na2CO3溶液,浸泡数分钟后, L 用 倾析 法分离并洗涤铁屑,晾干。
2、在小烧杯中放入上述铁屑,并注入15mL浓盐 酸和15mL水,加热至70℃,数分钟后趁热过 蒸发皿 中蒸发浓缩至溶液表面出现 滤,将滤液转入 晶膜 为止, 冷却结晶 、 抽滤 ,并用少量 酒精 洗涤晶体,取出晶体用干净的滤纸 吸干。 HCl 3、FeCl2· 2O 4H FeCl2 △?
