当代给水与废水处理原理(第二版)第3章
【2019年整理】当代给水与废水处理原理

绪论
1. 水源、水处理与用水——三位一体
二、
给 水 与 废 水 处 理
20世纪50年代以前,给水处理与废水处理涵义的 划分是很清楚的。
给水处理:从天然水源取水,为供生活或工业的 使用(特别是生活使用)而进行的处理,称为给水处理。
废水处理:为了排除的目的,对于使用过的水所进 行的处理,称为废水处理。
绪论
(1)悬浮培养体:以活性污泥法为典型代表,它的特 征是起水处理作用的细菌培养体处于悬浮状态的絮体;
(2)生物膜法以滴滤池为典型代表,它的特征是起水 处理作用的细菌培养体呈一层膜固定在填料表面上。
20世纪60年代以后, 为了满足废水再用的水质要求或排放的标 准,出现了对于常规废水处理后的出水进一步处理的过程,称为废 水的高级处理
单元操作往往带有物理变化,但也有不产生物理变化的单元操作, 如:食盐的生产过程。
一、 食盐的生产过程只包括下列几种单元操作:
水
处
理 的
固 体 和
学 送液
科 方
体 的 输
热传
蒸
结
发
晶
干 燥 及 筛 选
法
学
一、
2.水处理中单元操作与单元过程
水
处
理
的 学
合混
沉 淀
浮 升
浓过 缩滤
单 元 操
科
作
方
法
属
于
当代给水与废水处理原理
高良敏 博士、教授 安徽理工大学地球与环境学院
绪论
1.单元操作与单元过程
一、 水 处 理 的 学 科 方 法 学
20世纪50年代起,引用了化学工程中单元操作(unit operation )及单元过程(unit process)的概念,目的是为了 建立各种水处理方法间的理论联系,提高学科的理论水平
清华当代给水与废水处理原理课件第2章 反应器

第五节 多空丸模型
2.有效系数E的概念
E Md Mr
E为衡量扩散系数D在整个过程中所起的作用的指标。E=1时, 说明扩散阻力不起作用;E值越小,说明扩散阻力越大。
第六节 活塞流反应器
1.反应器内浓度及出口浓度
c ci exp k co ci exp k
适用于垂直于液体的流动方向上可能有混合现象,而在液体流 动的方向上完全不存在混合现象。
DAB
均相反应模型
第五节 多空丸模型
1.多空丸数学模型
球的半径为Z,比表面为a; 边界条件:当Z=0时反应物的浓度c=0; z=Z时,c=cb ; 球内反应速率r=-k''c; 有效扩散系数为D。 依据模型得到c的表达式
Zcb sinh k''a DZ c
z sinh k ''a DZ
第五节 多空丸模型
稳态时可简化为
cA
cAi 1 k
第七节 连续搅拌反应器(CSTR)
4.平行反应解的稳态解
(1)CSTR的平行反应
A k1 B A k2 B
rA (k1 k2 )cA
(2)稳态解
cA
1
cAi (k1
k2 )
cB
k1cAi 1 (k1 k2 )
cC
k2cAi
1 (k1 k2 )
第七节 连续搅拌反应器(CSTR)
本章难点:
多空丸模型、停留时间函数与反应器、液龄分布函数 混合与动力学过程、分散模型与反应器
反应器简介
1.反应器设计影响因素 反应器的设计涉及了流体力学、传热、传质、化学动
力学的知识 2.反应器的类型
按反应特点分为: 均相反应器与多相反应器 按运行方式分为:间歇式反应器与连续流式反应器
生物化学工程基础当代给水与废水处理原理优选演示

§6-2 真核细胞微生物
• 真菌、单细胞藻类及原生动物等均属于真核细胞微生物。真核细 胞的结构如图6-2所示。真核细胞微生物的细胞核分化程度较高, 有核膜和核仁。细胞质内有完整的细胞器,包括中心粒、线粒体、 叶绿体、核糖体和内质网等。
§6-2 真核细胞微生物
• 原生动物是单细胞动物。原生动物具有核,核的数目有时不止一 个,这与细菌不同;原生动物均有发育完善的运动器官或运动方 法;原生动物通常按二分裂法繁殖,但有时也采取接合或自体受 精等复杂的有性生殖。另外还有通过孢子增殖的方法
生物。放线菌中的诺卡氏菌属有分解氧化无机氰化物和烃类化合 物的能力,在处理含烃类和无机氰化物的废水中起着重要作用。 4. 蓝细菌 • 蓝细菌有时列入藻类,也称蓝藻。因其细胞结构为原核,故归入 细菌类。蓝细菌是光合型微生物。多数蓝细菌生存于淡水中,是 水生系统食物链中的重要一环。当恶性增殖时,可形成“水华”, 造成水质恶化。海洋中的“赤潮”有时也系蓝细菌大量繁殖所致。
2. 丝状菌 • 丝状茵在废水处理中的作用重要而独特。废水处理中常见的丝状
细菌主要有球衣菌属、铁细菌属、贝日阿托氏菌属和发硫菌属。 • 但丝状细菌过度繁殖,特别是游离于菌胶团之外的非结构性丝状
细菌的大量繁殖.会引起废水处理系统的污泥膨胀。
§6-1 原核细胞微生物
3. 放线菌 • 放线菌为具有分枝的丝状菌,介于细菌与真菌之间,是单细胞微
生物化学工程基础当代给水与废水处理原理
优选生物化学工程基础当代给 水与废水处理原理
水处理中的微生物
给水与废水处所涉及的微生物种类很多,根据 其细胞结构、功能和组分差异,主要分三类:原核
细胞微生物、真核细胞微生物和病毒(噬菌体)。
§6-1 原核细胞微生物
当代给水与废水处理

1 x K f e n ★Freundlich公式为: m
• 改性活性炭(表面官能团性质及数量发生变化) 以去除 有机污染物为目的的改性方向应为:减少表面内酯基及羧 基等含氧官能团的含量,增加活性炭表面的疏水性。 • 活性炭工艺与其它手段的结合 活性炭起的是辅助性的作用,主体是生物法、催化剂的应 用等。活性炭与膜联用能解决单独使用膜过滤引起的膜阻 塞和膜污染问题。利用活性炭对进水进行必要的前处理, 以减少水中的有机物、无机物、微生物等在膜表面和膜内 孔积累,极大延长了膜的使用寿命;而膜的存在又可以克 服单独使用活性炭出水中细菌数偏高的问题。
2.混凝现象的四种机理 • 压缩双电层作用 向溶液中投入电解质,离子浓度增高,扩散层的厚度将 减小,ζ 电位降低,胶粒得以迅速凝聚。 • 吸附和电荷中和作用 胶粒表面对带异号电荷有强烈的吸附作用,中和了它的 部分电荷,减少了静电斥力,易与其他颗粒接近而互相 吸附。
•
吸附架桥作用 高分子物质与胶粒相互吸附,而使胶粒凝聚为大的絮凝 体。 • 沉淀物网捕作用 混凝剂金属盐投加量大,迅速形成金属沉淀物,水中的 胶粒可被这些沉淀物网捕。
当代给水与废水处理原理
第三章 活性炭吸附 第四章 传质及曝气
• 气一液传质模型
• 凝聚与絮凝 沉淀试验 • 膜分离
3-1 活性炭的性能 3-3 Langmuir公式的推导 3-5 吸附柱的设计
3-2 吸附等温线 3-4 吸附公式的应用
曝气设备的充氧能力
第五章 常规分离过程与膜分离
浓缩池 滤床过滤
1
活性炭吸附
2
凝聚与絮凝
3
膜分离
一、活性炭吸附
1.活性炭是一种多孔碳,堆积密度低,炭粒中有更细小 的孔——毛细管,比表面积大,能与气体(杂质)充分 接触,具有很强的吸附能力,起净化作用。 2.活性炭的制造 活性炭的制作分碳化及活化两步。 •碳化也称热解,是在隔绝空气的条件下对原材料加热, 一般温度在600℃以下。 •活化是在有氧化剂的作用下,对碳化后的材料加热。
当代给水与废水处理原理高良敏厌氧生物处理法

当代给水与废水处理原理:高良敏厌氧生物处理法引言水是生命的源泉,给水与废水处理是保护水资源、维护生态环境的重要环节。
在当代社会中,给水与废水处理技术得到了广泛的关注和应用。
在给水与废水处理领域,高良敏厌氧生物处理法作为一种高效、经济的处理技术,受到了越来越多的重视。
高良敏厌氧生物处理法概述高良敏厌氧生物处理法是一种利用厌氧微生物对有机物进行降解的处理技术。
该技术通过在无氧条件下引入厌氧微生物,使其降解废水中的有机物,从而达到净化水质的目的。
高良敏厌氧生物处理法的原理高良敏厌氧生物处理法的主要原理可以概括为以下几个方面:1. 厌氧环境的建立在高良敏厌氧生物处理法中,首先需要建立一个无氧环境。
通常使用密闭的反应器来实现无氧条件,可以通过调节反应器内的氧气供应,阻止氧气进入反应器内部。
2. 引入厌氧微生物经过厌氧环境建立后,需要引入适宜的厌氧微生物。
这些微生物具有降解有机物的能力,可以在无氧环境下快速生长和繁殖。
3. 有机物降解过程引入厌氧微生物后,有机物降解过程开始进行。
厌氧微生物通过代谢活动分解有机物,产生二氧化碳、水和甲烷等产物。
这些产物相对无害,并不增加废水的污染负荷。
4. 处理效果与影响因素高良敏厌氧生物处理法的处理效果受多种因素的影响。
例如,水质的初始特性、厌氧微生物的菌群结构、温度等都会对处理效果产生影响。
因此,在实际应用中,需要根据具体情况进行合理调整和控制。
高良敏厌氧生物处理法的优势相比传统的废水处理方法,高良敏厌氧生物处理法具有以下几个优势:1. 处理效率高高良敏厌氧生物处理法能够在无氧环境下有效降解有机物,处理效率高。
在相同处理时间内,相对于传统的氧化法,高良敏厌氧生物处理法能够达到更好的处理效果。
2. 能耗低由于在无氧条件下进行处理,高良敏厌氧生物处理法的能耗低。
相对于需要供氧的氧化法,高良敏厌氧生物处理法可以节约能源。
3. 处理成本较低除了低能耗外,高良敏厌氧生物处理法的处理成本也较低。
当代给水与废水处理原理 读书报告
当代给水废水处理原理第一章化学反应动力学化学动力学定义,从动态的角度研究化学反应产生、发展及消亡全过程。
化学动力学具体内容(1)比较化学反应的快慢及外部因素的影响;(2)揭示化学历程,即反应物按何种途径转化为最终产物;(3)呈现物质结构与反应性能之间的关系。
化学动力学研究层次(1)唯象动力学:研究总反应的速率及影响因素,“唯象”,即: 只以化反的宏观现象为依据。
(2)基元反应动力学:关于基反的动力学规律与理论,并探讨总反应的动力学行为。
(3)分子反应动态学:从分子、原子的量力角度研究分子间一次具体碰撞行为。
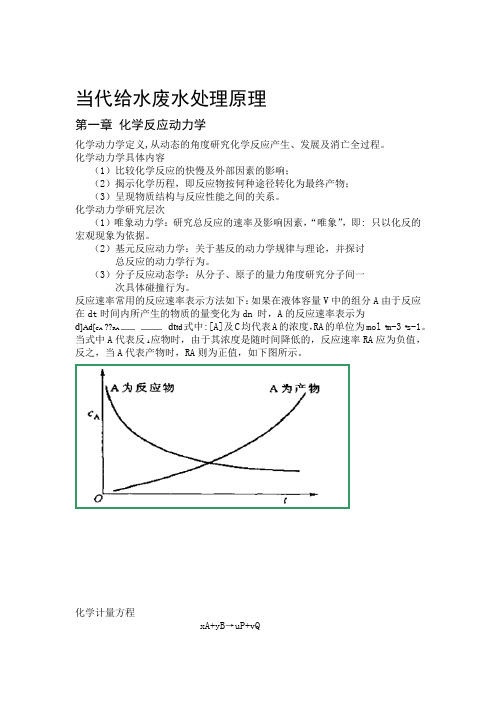
反应速率常用的反应速率表示方法如下:如果在液体容量V中的组分A由于反应在dt时间内所产生的物质的量变化为dn 时,A的反应速率表示为d]Ad[CA RA dt t d式中:[A]及C均代表A的浓度,RA的单位为mol·m-3·s-1。
当式中A代表反A应物时,由于其浓度是随时间降低的,反应速率RA应为负值,反之,当A代表产物时,RA则为正值,如下图所示。
化学计量方程xA+yB→uP+vQ这个方程式主要是表示一个质量守恒的关系,只是说明反应物A的x个分子与B的y个分子的质量与产物P的u个分子及Q的v个分子的质量相等,这种关系称为化学计量方程式。
令 N,N , N 和 N分别为相应物种在时刻t的物质的量,则Q??????d xxuvv i dζ称为反应进ABP?dn?dndndndn iAPQB度,为物种v的化学计量方程系数,反应物取负号,产物取i正号。
反应级数如果通过试验数据的数学处理,得出产物P的反应速率可以表示为:d[p]dc P=ab CKC r??P B A dtd t那末,产物P的反应称为:反应物A的a 级反应;反应物B的b级反应;总称为(a+b)级反应。
K称为反应的速率常数(rate constant).第二章反应器1.反应器设计影响因素:反应器的设计涉及了流体力学、传热、传质、化学动力学的知识2.反应器的类型按反应特点分为:均相反应器与多相反应器按运行方式分为:间歇式反应器与连续流式反应器3、反应器设计面临的新课题反应器体系的设计:如何传热、传质的问题;反应动力学研究;反应器参数优化,反应机理的研究。
【2018-2019】当代给水与废水处理,读书报告-精选word文档 (10页)

本文部分内容来自网络整理,本司不为其真实性负责,如有异议或侵权请及时联系,本司将立即删除!== 本文为word格式,下载后可方便编辑和修改! ==当代给水与废水处理,读书报告篇一:当代给水与废水处理原理课后习题答案许保玖篇二:水处理吸附理论与技术简析活性炭吸附技术在水处理方面应用摘要: 现代工业的迅猛发展给环境带来的污染日益严重,尤为严重的是水体污染,已经引起了全世界的普遍关注。
同时,随着人们生活水平的不断提高和环保意识的不断增强,使得人们对引用水水质的要求愈来愈严格。
活性炭是最常用的优良的吸附剂,深刻了解活性炭的特性,正确选择活性炭,充分发挥其在水处理的作用,达到深度处理的效果,成为近来研究的重点。
本文概述活性炭的特性及其吸附机理,介绍活性炭吸附技术及其组合工艺在国内外水处理中的应用和发展,总结它在应用中的优缺点并预测其前景和发展方向。
关键词: 活性炭、吸附、水处理、组合工艺引言传统的饮用水处理主要通过絮凝、沉淀、过滤和加氯消毒来去除水中的悬浮物和细菌,而对各种溶解性化学物质的脱除作用很低。
吸附法是采用多孔性的固体吸附剂,利用同一液相界面上的物质传递,使废水中的污染物转移到固体吸附剂上,从而使之从废水中分离去除的方法。
具有吸附能力的多孔固体物质称为吸附剂。
根据吸附剂表面吸附力的不同,可分为物理吸附、化学吸附和离子交换性吸附。
在废水处理中所发生的吸附过程往往是几种吸附作用的综合表现。
废水中常用的吸附剂有活性炭、磺化煤、沸石等。
1. 活性炭的特性及其吸附机理1.1活性炭的特性1活性炭是一种由煤、沥青、石油焦、果壳等含碳原料制成的外观呈黑色的粉末状或颗粒状的无定形碳。
活性炭内部孔隙结构发达、比表面积大、吸附能力强。
普通活性炭的比表面积为500-1500m2。
超级活性炭比表面积则高达3500 m/g活性炭所含主要元素是碳,含量为90-95%。
氧和氢大部分是以化学键的形式与碳原子相结合形成有机官能团,氧含量4%-5%左右,氢含量一般是1%-2%。
当代给水与废水处理原理(第二版)第5章

④ 离子型晶体Schottky缺陷(某种粒子可在晶体内自由运动 ):如粘土或其他铝硅酸盐矿物颗粒,其晶体内碱金属或 碱土金属离子取代了表面晶格中的铝离子,引起表面带负 电荷。这类胶体的表面电荷、电势不受溶液pH值或电位决 定离子影响,不存在电荷零点。
对式(5-12)积分得:
0 exp( x)
(5-13)
式中,κ为Debye-Huckel常数:
1
e2
ni0 zi2 kT
2
(5-14)
式(5-13)表明,扩散双电层中电势随距离x呈指数函数降
低,如图5-1(c)。κ-1代表了扩散双电层厚度,即界面静电场
影响范围。
8
2. Gouy-Ghapman扩散双电层理论(续3)
3
胶体的稳定性
胶体颗粒在水中继续保持分散状态的性质称为胶体的稳 定性。
憎水胶体,稳定性可以通过它的双电层结构来说明。亲水 胶体,虽然也具有双电层结构,但其稳定性主要由吸附的大量 水分子所构成的水壳来说明。亲水胶体保待分散的能力,即它 的稳定性比憎水胶体高。
双电层结构的产生原因:
颗粒巨大的 比表面积
只有一种Z-Z电解质时,式(5-11)可简化为:
d 2 dx2
2n0
ze
sinh
ze kT
(5-15)
式中:n0 n0 n0; z z z;
n0、z、n0、z —正负离子在主体溶液中的浓度和价数
7
2. Gouy-Ghapman扩散双电层理论(续2)
d 2
dx2
1
i
ni0zie exp(zie / kT )
清华当代给水与废水处理原理课件第1章 化学动力学

案例1:吸附动力学(基础研究) 案例2:降解动力学(工程应用)
第一节 反应速率和反应级数
1.1 反应速率
rA
1 V
dnA dt
dA
dt
dcA dt
式中:[A]及 c A均代表A的浓度, 的单位为molm-3s-1。当式(1.1)中 A代表反应物时,由于其浓度是
随时间降低的,反应速率 rA 应为 负值,反之,当A代表产物时,rA
k'cA
(1.16)
第二节 简单的基元反应
2.5 图解法求反应的级数
由已经给出的一级反应及二级反应的半衰期公式。同样,可以
推理得出基元反应的反应物A的反应级数n与半衰期t1 2 的关系如下:
1 t1 2 (cA0 )n1
(1.17)
第三节 较复杂的反应
较复杂的反应指的是由几个简单的基元反应所组合成一种反应.
则为正值,如图1-1所示。
(1.1)
图1-1 反应物及产物的历时曲线
第一章 化学动力学
1.2化学计量方程
xA+yB→uP+υQ
(1.2)
这个方程式主要是表示一个质量守恒的关系,只是说明反应物A的x个分
子与B的y个分子的质量与产物P的u个分子及Q的υ个分子的质量相等,这种关
系称为化学计量方程式。
d dnA dnB dnP dnQ dn1
单一组分的 零级反应
三级和更高级 的反应
基元反应
单一组分的 一级反应
两种反应物的 伪一级反应
两种反应物的 二级反应
第二节 简单的基元反应
2.级反应,A
的初始浓度为 cA0 ,k为反应的速率常数,则在
反应时刻t浓度cA的表达式为:
当代给水与废水处理原理第二版

这种反应器的特点是:一、上部设置的三相分离器 可使厌氧生物污泥自动回沉到下部反应区,因而反应器 可维持较高的生物量和较长的污泥停留时间。二、枯死 的厌氧器上升水流的微混合作用下形成粒状,为新生微 生物提供了附着生长的表面,形成所谓的粒状污泥这更 进一步延长了污泥的停留时间,因为颗粒污泥的形成使 UASB反应器部分地成为生物膜反应器了。实质上可认为, 具有颗粒污泥的UASB反应器是一个颗粒污泥处于流化状 态的流化床反应器。
(1)两相厌氧法:这种工艺也称两段厌氧法,是根据
产甲烷细菌的增殖率低,增代时间长,适宜的最佳pH
值范围窄,要求严格;而其它非产甲烷的细菌,例如
产酸细菌则增殖率高,增代时间短,对pH值和厌氧条
件的要求都不甚严格。
两相厌氧法把非产甲烷细菌和产甲烷细菌分开在 两个串联的反应器里培养,分别各自完成厌氧反应中 的水解、产甲烷反应,前者称产酸相(或产酸段), 后者称产甲烷相(或产甲烷段)。这样做的结果是, 消化池的总体积减小了,有机物容积负荷和处理效率 提高了。为了进一步提高产甲烷的厌氧生物污泥停留 时间,产甲烷相常采用厌氧生物膜反应器,如图10-4 (a)所示。
1. 基本原理
可将有机物在厌氧条件下 的降解过程分三个反应阶段。 第一阶段是水解阶段;第二阶 段是产酸和脱氢阶段;第三阶 段为产甲烷阶段。
这三个反应阶段右图所示。 在厌氧生物处理过程中,尽管 反应是按三个阶段进行的,但 在厌氧反应器中,它们应该是 瞬时连续发生的。在有些文献 中,将水解和产酸、脱氢阶段 合并统称为酸性发酵阶段,将 产甲烷称为甲烷发酵阶段。
厌氧生物处理法的主要优点有:能耗低;可回收生物能 源(沼气);每去除单位质量底物产生的微生物(污泥)量 少;而且由于处理过程不需要氧,所以不受传氧能力的限制, 因而具有较高的有机物负荷的潜力。其缺点是处理后出水的 COD、BOD值较高,水力停留时间较长并产生恶臭等。
当代给水与废水处理原理

非极性的 链烷化合 物在活性 炭表面的
吸附。
有关极性 分子氨基 酸及蛋白 质的吸附 资料极少
活性炭对于 吸附无机物 也有一定的 潜力
活性炭的吸 附性能是由 于它的表面 基团类型、 比表面积和 孔径的分布 决定的。
第5页,共19页。
第三章 活性炭吸附
§3-2 吸附等温线
吸附 等温 线的 类型
第一种类型的等温线, 没e 有极限值,但 却x 有m 一极限
ka代表单位体积活性炭在单位时间内所吸收的杂质量。
活性炭的容量传质系数可以通过实验得出。 当这个系数已知后,就能够确定吸附柱所需要的活性炭总体积。但这需要知 道吸附柱的吸附容量、吸附柱的吸附过程曲线与容积传质系数三者间的关系。
第15页,共19页。
第三章 活性炭吸附
求活性炭的容量传质系数
活性炭的容量传质系数ka,一般通过用初始有机物浓度ρ1的水样,每 升加活性炭mg做吸附试验,由吸附试验可以得出下列物料衡算关系:
值 ,(这x m种)0类型的吸附试验资料可用Langmuir公式处 理。
第二类型的等温线, 有e 一个极限值 ,称s 为饱和浓
度,但x/m却没有极限值。这种类型的等温线可用 Branauer和Emmett及Teller(简称BET)公式处理。
第三类型的等温线, 和e x都m没有极限值,可用
Freundlich公式处理。
活化的定义
活化是在有氧化剂的作用下,对碳化后的材料加热,以生产活性炭产品。当氧化过程的 温度在800-900℃时,一般用蒸汽或二氧化碳为氧化剂;当氧化温度在600℃以下时,一 般用空气做氧化剂。
第2页,共19页。
第三章 活性炭吸附
碳
①使原材料分解放出水气、一氧化碳、二氧化碳及氢等
当代给水与废水处理原理(第一章)

BOD5的含义:
生化需氧量的反应速度在很大程度上取决于微生物 的种类、数目及温度,而在测定过程中溶解氧又是逐渐 消耗的。所以测定生化需氧量就须保持一定的温度,同 时也需要规定一定的时间。通常是在20℃温度下培养 5d检查溶解氧的损失,用BOD5表示,单位以O2mg/L计。 测定温度用20℃是因为这个温度比较接近温带地区一般 河水的平均温度。
当代给水与废水处理原理
xxx大学 Xx教授
1
授课主要内容
相关基本概念介绍 生物化学工程基础 废水生物化学处理基础 活性污泥法 生物膜法
厌氧生物处理法 生物脱氮除磷 常规分离与膜分离 活性碳吸附 传质与曝气
2
第一部分:相关基本概念介绍
一、理论需氧量
理论需氧量(ThOD)是根据化学方程式计算求得的有 机物被全部氧化所需的氧量。例如,含有300mg/L葡萄 糖溶液的理论需氧量可计算如下:
推流系统示意图
在理想的推流式反应器中.进口处各层水流依次流到出口处,互不干扰,各层
水流中微生物的工作情况,如用微生物增长曲线来表示,将是一段线段,废水生物 处理的数学模式可直接采用下式(1)或式(2)。如二次沉淀池出水基质浓度为Se。上 两式可改写成:
3
氨基乙酸的理论需氧量,可利用下列化学方程式: (a) (b) (c)
4
由方程式a计算得氨基乙酸的碳化需氧量为: b c
5
二、化学需氧量
化学需氧量或耗氧量是指在一定严格条件下水中有机物与强氧 化剂(如重铬酸钾、高锰酸钾)作用所消耗的氧量。当用重铬酸钾作为 氧化剂,硫酸银作为催化剂时,水中有机物几乎可以全部(约90%95%左右)被氧化。这时所测得的耗氧量称为重铬酸钾耗氧量或称化 学需氧量,以CODCr或COD表示。在测定过程中无机性还原物质也 会被氧化。所以一般测得的COD包括可生物降解和不可生物降解两 部分,即化学需氧量区别不出可生物降解和不可生物降解的物质。
当代给水与废水处理原理(第二版)第3章

3. 活性炭性能及影响因素及吸附作用 (1)表面的氧化物复体(complex)的性能。一般把活性炭的 表面氧化物分成酸性的和碱性的两大类。酸性官能团有:羧基,酚 羟基,醌型羰基,正内酯基,荧光型内酯基,羧酸酐基及环式过氧 基等, 其中羧酸基,内酯基及酚羧基被多次报导为主要酸性氧化物, 对于碱性氧化物的说法有分歧。有的认为是如氧萘的结构,为苯并 恶英的衍生物,另一种说法认为碱性氧化物最好用类似吡喃酮的结 构来代表。 (2)酸性氧化物使活性炭具有极性的性质,因之倾向于吸附极 性较强的化合物。这些带极性的基团易于吸附带极性的水,因而阻 碍了在水浴液中吸附非极性物质的过程。为了避免形成更多的类似 羧基的基团,妨碍吸附非极性物质的过程,活化的温度必须在900OC 附近,再生的温度也同样注意。 (3)活性炭表面的金属离子部位带有正电荷,对那些有过剩电 子的部位的分子有吸引力,可以增加活性炭吸附的速率。活性炭表 面带有金属的是有利的。
第三章 活性炭吸附
第三章
活性炭吸附
第一节 活性炭的性能 1. 活性炭的制造——分为炭化及活化两步。炭化也称热解,是在隔 热空气的条件下对原材料加热,一般温度在600 OC以下。炭化有多 种作用: 一是使原材料分解放出H2O, CO, CO2 及H2等气体。第二个作用 是易使原材料分解成碎片,并重新集合成稳定的结构。活化是在有 氧化剂的作用下,对炭化后的材料加热。当氧化过程的温度在800— 900OC时,一般用蒸汽或CO2为氧化剂;当氧化过程的温度在600OC 以下时,一般用空气做氧化剂。在活化的过程中,烧掉了炭化时吸 附的碳氢化合物,起了扩大孔隙的作用,并把孔隙与孔隙之间烧穿, 活化使活性炭变成一种良好的多孔结构。 2.活性炭的吸附性能 活性炭分成粉末状和粒状两种类型。每克活性炭的表面积可高达 1000 m2 。 但99.9%以上的面积都在多孔结构颗粒的内部。活性炭的 极大地吸附能力即在于此。粒状以吸附柱的形式来应用,当吸附能 力饱和后,通过再生以恢复其吸附能力。粉末活性炭系直接投加于 水中,经混合吸附后分离出来,由于再生技术尚未完善的关系,过 去往往作为废物排掉。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
活性炭的吸附作用: (1)首先是对芳族化合物的吸附。例如农药、除草剂、表面活 化剂、天然色及酚类等。这类化合物与活性炭间形成给受复体。活 性炭中的羧基氧为电子给体,溶质中的芳环中有NO2一类取代基时, 给受作用还要加强。 (2)非极性的链烷化合物在活性炭表面的吸附过程同样也受酸 性氧化物的阻碍,这类化合物只是在无酸性氧化物的活性炭表面上 才能很好地被吸附。但在特殊情形下,当活性炭表面上的金属能起 加强吸附作用时,非极性的链烷化合物也能很好地被含有酸性氧化 物的活性炭吸附。突出的例子为活性炭吸附二丁基二硫(C4H9)2S2 的研究结果。(C4H9)2S2 是水中产生臭及味的原因。由于S—S键 是一个过剩电子的定位点,受活性炭表面的正电荷金属离子诱发了 (C4H9)2S2 分子的感应极化,加强了吸附能量,可以不受酸性氧化 物的影响。 (3)活性炭对于吸附无机物也有一定的潜力。粒状活性炭对于 Ag+,Cd2+,及Cr042- 等离子的吸附去除率可达85%以上。对于水中大多 数的金属如锑,砷,铋,锡,汞,钴,铅,镍,铁等均有很好的吸 附潜力。活性炭对水中卤族分子Cl2,Br2,及I2的吸附能力顺序为良 好,强及很强,Cl2及Br2 并被还原。 总之,活性炭的吸附性能是由它的表面基团类型,比表angmuir和BET公式都是理论公式,Freundlich公式则属于经验 公式。Langmuir公式是根据吸附的物质只有一层分子厚的假定出 来的。由于吸附剂的表面积是一定的,Langmuir公式中必然要出 现一个吸附量的极限值来。BET公式则从许多层物质的假定推导出 来的,故吸附量没有极限值,平衡浓度则以被吸附物质的饱和浓 度为极限。Freundlich公式则能适应介乎上述两者间的吸附情况。 最后要强调的是,究竟应选择哪一个公式来处理吸附数据, 必须以实验数据按照不同的吸附公式运用数学的方法进行比较得 出。
x 0.13 0.345 20 0.249 (mg / mg ) m 1 0.13 20
因此,物料衡算方程将变成 100(20—1)=M(0.249—0.0397) 每秒钟补充的新鲜活性炭M=9.1克,比47.9克小多了。
上面的计算提出了一个逆流吸附的概念。实践中需要两 个串联起来的CSTR才能体现。如下图与例题2相比,例题1 的操作方式称为顺流吸附。
M/g· s1
M/g· s-1
图2 二级逆流吸附
例题2 原始资料同例1,但按照图2所示的二级逆流吸附操作, 求每秒补充的新鲜活性炭量。 解:CSTR2的平衡浓度ρ2即出水浓度1mg/L,因此(x/m)2值 也和上题一样,为0.0397 mg/ mg,但CSTR1的ρ1和(x/m)1则必须重 新计算.补充的活性炭量仍以M代替。 在CSTR2中,M mg活性炭所吸附的有机物总量为0.0397M mg, 折合为从每升水中吸附了(0.0397M/100)mg,吸附后的平衡浓度 ρ2为1 mg/L,因此得CSTR的进水有机物质量浓度为
每克炭只起吸附0.0397克有机物的作用,但是,每克这种活性炭 实际具有吸附0.345克有机物的极限潜力(在平衡浓度相当高的条 件下).由于废水的有机物浓度为20 mg/L,这个极限潜力是无法发挥 的.如果把每克已经吸附了0.0397克有机物的活性炭再用来处理含 有20 mg/L有机物的废水,那么,活性炭的吸附能力为
3. 活性炭性能及影响因素及吸附作用 (1)表面的氧化物复体(complex)的性能。一般把活性炭的 表面氧化物分成酸性的和碱性的两大类。酸性官能团有:羧基,酚 羟基,醌型羰基,正内酯基,荧光型内酯基,羧酸酐基及环式过氧 基等, 其中羧酸基,内酯基及酚羧基被多次报导为主要酸性氧化物, 对于碱性氧化物的说法有分歧。有的认为是如氧萘的结构,为苯并 恶英的衍生物,另一种说法认为碱性氧化物最好用类似吡喃酮的结 构来代表。 (2)酸性氧化物使活性炭具有极性的性质,因之倾向于吸附极 性较强的化合物。这些带极性的基团易于吸附带极性的水,因而阻 碍了在水浴液中吸附非极性物质的过程。为了避免形成更多的类似 羧基的基团,妨碍吸附非极性物质的过程,活化的温度必须在900OC 附近,再生的温度也同样注意。 (3)活性炭表面的金属离子部位带有正电荷,对那些有过剩电 子的部位的分子有吸引力,可以增加活性炭吸附的速率。活性炭表 面带有金属的是有利的。
假
第三节 Langmuir公式的推导
设 !
推导假定有如下四条: (1)被吸附的物质只有一层分子厚; (2)被吸附物质的颗粒和水分子一样大; (3)每个吸附颗粒占面积σ o ; (4)只考虑在单层内的平衡关系。
如果用○及 ◎ 分别代表未被吸附的水分子及物质颗粒,●及⊙ 分别代表被吸附的水分子及物质颗粒,它们都是一般大,固定在吸 附表面上形成一层均匀的厚度。 假设被吸附的水分子和物质颗粒的粒目分别为n1s及n2s个;则未 被吸附的粒目分别为n1及n2个。由于两者颗粒大小相等,1克吸附剂 表面所具有的吸附部位数量是一定的(即n1s+n2s=n,即1克吸附剂表 面共有n个σo面积),在吸附部位以外能容纳水分子或者物质颗粒的 个数必然是一定的,也就是说,1克吸附剂表面积上能容纳的颗粒 总数量是一定的。
x f ( e ,T ) m
当T不变时
x f '(e ) m
按上述试验过程所得的 x/m对ρe所画出的曲线称为吸附等温线。 常见的吸附等温线有三种类型,每种类型相应于一种吸附公式, 如下页图所示:
x m
x ( )0 m
x m
x m
e
e
s
e
Ⅰ型
Ⅱ型
Ⅲ型
Ⅰ型:ρe没有极限值,但是x/m却有一极限值(x/m)0 。这 类吸附实验资料可以用Langmuir公式处理。 Ⅱ型: ρe有一个极限值ρs ,称为饱和浓度,但是x/m却没有 极限值,这种类型等温线可以用BET(brannauer 、Emmett 、 Teller)公式处理。 Ⅲ型: ρe与x/m都没有极限值,可以用Freundlich公式处理。 具体处理过程见下页
第三章 活性炭吸附
第三章
活性炭吸附
第一节 活性炭的性能 1. 活性炭的制造——分为炭化及活化两步。炭化也称热解,是在隔 热空气的条件下对原材料加热,一般温度在600 OC以下。炭化有多 种作用: 一是使原材料分解放出H2O, CO, CO2 及H2等气体。第二个作用 是易使原材料分解成碎片,并重新集合成稳定的结构。活化是在有 氧化剂的作用下,对炭化后的材料加热。当氧化过程的温度在800— 900OC时,一般用蒸汽或CO2为氧化剂;当氧化过程的温度在600OC 以下时,一般用空气做氧化剂。在活化的过程中,烧掉了炭化时吸 附的碳氢化合物,起了扩大孔隙的作用,并把孔隙与孔隙之间烧穿, 活化使活性炭变成一种良好的多孔结构。 2.活性炭的吸附性能 活性炭分成粉末状和粒状两种类型。每克活性炭的表面积可高达 1000 m2 。 但99.9%以上的面积都在多孔结构颗粒的内部。活性炭的 极大地吸附能力即在于此。粒状以吸附柱的形式来应用,当吸附能 力饱和后,通过再生以恢复其吸附能力。粉末活性炭系直接投加于 水中,经混合吸附后分离出来,由于再生技术尚未完善的关系,过 去往往作为废物排掉。
以(x/m)1和(x/m)2带入得
0.0397M 1) 100 100(20 1 ) [ 0.0397]M 0.0397M 1 0.13( 1) 100 0.13 0.345(
以ρ1=(0.0397M/100)+1代入并整理成下列形式
19 0.0397( M / 100) [ 0.00178 ( M / 100) 0.045 0.0397](M / 100) 0.00517 ( M / 100) 1.13
1 (
0.0397 M 1)mg / L 100
ρ1也就是CSTR1的平衡浓度,由ρ1可得CSTR的吸附量为
x ( ) m 0.13 0.345 ( 0.0397M 1) 100 0.0397M 1 0.13( 1) 100
仿照例题1对CSTR1写物料衡算方程得
x x 100 (20 1 ) [( )1 ( ) 2 ]M m m
第二节 吸附等温线 当达到平衡浓度ρe时,可知m mg活性炭所吸附的杂质量为 V(ρi-ρe) mg,因为每mg活性炭所吸附的杂质量为
V (i e ) x m m
其中x 代表被吸附的杂质质量。 当然,对同样的原水用不同种类的活性炭进行吸附试验,所得到 的平衡浓度ρe是不相同的,因而x/m值也不相同。但对同一种活性炭 来说,实验证明:
x b( x / m) 0 e 0.13 0.3451 0.0397(mg / mg) m 1 b e 1 0.131
令每秒种投加的补充活性炭为M mg,因投加的是新鲜活性炭, 未吸附任何有机物,即初始吸附量(x/m)0值为0,由物料平衡关 系有 100(20—1)=M(0.0397—0) M=1900/0.0397=47858 mg/S=47.9 g/S
Q=100L/S ρi=20mg/L
CSTR
100L/S ρ0=1mg/L
M/g· s-1 图1 顺流吸附
ρ/mg·L-1 100L/s (x/m) M/g· s-1
ρ1
活性炭 M/g· s-1
ρ1/mg· L-1
ρ2 CSTR2 (x/m)2
1mg/L 100L/s
CSTR1 ( x/m )
1
(x/m)2
K s s n 2 ( n n2 ) n2 n1
b' n2 n (1 b' n2 )n2
n2
s
s
b' n2 n
b=b’L n2/L代表未 被吸附物质 的摩尔数, 相当于平衡 浓度ρe 得到Langmuir公式
1 b' n2
n2 L
两边同时除以Avogadro常数L,得到
x m b ( x / m) 0 1 b n2 L
