土壤酸碱性和氧化还原反应森林土壤
合集下载
第五章2土壤酸碱性和氧化还原反应
我国则以碱化层的碱化度>30%,表层含盐量<0.5%和pH
值>9.0定为碱土(alkaline soil) 。而将土壤碱化度为5
-10Байду номын сангаас定为轻度碱化土壤,10-15%为中度碱化土壤, 15-20%为强碱化土壤。
三、影响土壤pH值的因素
(一)土壤胶体类型和性质对pH值的影响 1.土壤胶体的极限pH值
第五章 土壤酸碱性和氧化还原反应(二)
教学目标
•理解土壤酸碱性的内涵、类型 •了解土壤酸碱性的分级、成因 •学习土壤酸碱性的定量测定与表示 •掌握酸性土壤、碱性土壤壤的改良与治理方法 •了解土壤氧化还原的机理 •明白土壤氧化还原作用对土壤肥力的影响。
土壤酸碱性和氧化还原性的重要性
1. 土壤溶液的两项极为重要的化学性质 2. 既与土壤溶液的组成密切相关,又与土壤固相和 气相紧紧相连 3. 随着自然条件的变化(季节性的温度、湿度等的 变化)、人为耕作措施和植物生长的变化而变化 4.对土壤肥力和植物营养有重要影响
碱化度是指土壤胶体吸附的交换性Na+占阳离子 交换量的百分率。土壤碱化度常被用来作为碱土分 类及碱化土壤改良利用的指标和依据。
碱 化 度 = 阳 交 离 换 子 性 交 钠 换 量 1 0 0
当土壤碱化度达到一定程度,可溶盐含量较低时, 土壤就呈极强的碱性反应,土壤理化性质上发生恶劣
变化,称为土壤的“碱化作用”(alkalinization)。
(四)土壤氧化还原条件对pH的影响
酸性土淹水后pH升高的原因主要是由于在嫌气条件下形成 的还原性碳酸铁、锰呈碱性,溶解度较大,因之pH值升高。
硫化物(在硫化细菌的作用下)可氧化为硫酸,使土壤 pH值急剧下降
土壤酸碱性对作物生长的影响
值>9.0定为碱土(alkaline soil) 。而将土壤碱化度为5
-10Байду номын сангаас定为轻度碱化土壤,10-15%为中度碱化土壤, 15-20%为强碱化土壤。
三、影响土壤pH值的因素
(一)土壤胶体类型和性质对pH值的影响 1.土壤胶体的极限pH值
第五章 土壤酸碱性和氧化还原反应(二)
教学目标
•理解土壤酸碱性的内涵、类型 •了解土壤酸碱性的分级、成因 •学习土壤酸碱性的定量测定与表示 •掌握酸性土壤、碱性土壤壤的改良与治理方法 •了解土壤氧化还原的机理 •明白土壤氧化还原作用对土壤肥力的影响。
土壤酸碱性和氧化还原性的重要性
1. 土壤溶液的两项极为重要的化学性质 2. 既与土壤溶液的组成密切相关,又与土壤固相和 气相紧紧相连 3. 随着自然条件的变化(季节性的温度、湿度等的 变化)、人为耕作措施和植物生长的变化而变化 4.对土壤肥力和植物营养有重要影响
碱化度是指土壤胶体吸附的交换性Na+占阳离子 交换量的百分率。土壤碱化度常被用来作为碱土分 类及碱化土壤改良利用的指标和依据。
碱 化 度 = 阳 交 离 换 子 性 交 钠 换 量 1 0 0
当土壤碱化度达到一定程度,可溶盐含量较低时, 土壤就呈极强的碱性反应,土壤理化性质上发生恶劣
变化,称为土壤的“碱化作用”(alkalinization)。
(四)土壤氧化还原条件对pH的影响
酸性土淹水后pH升高的原因主要是由于在嫌气条件下形成 的还原性碳酸铁、锰呈碱性,溶解度较大,因之pH值升高。
硫化物(在硫化细菌的作用下)可氧化为硫酸,使土壤 pH值急剧下降
土壤酸碱性对作物生长的影响
第七章 土壤酸碱性和氧化还原反应

第七章 土壤酸碱性和氧化还原反应
第一节 土壤的酸碱性 四、土壤的缓冲性能
1、土壤缓冲性的概念 2、土壤具有缓冲性的原因 1)土壤溶液中弱酸及其盐类的存在; 2)土壤胶体的阳离子交换作用; 3)土壤中两性物质的存在。
第七章 土壤酸碱性和氧化还原反应
第一节 土壤的酸碱性 四、土壤的缓冲性能
1、土壤缓冲性的概念 2、土壤具有缓冲性的原因 3、缓冲容量 缓冲容量:表示缓冲作用的大小。指土壤溶液改变一
2250000×20%×10-7=0.045mol H+/公顷
所以需要中和活性酸量为 4.5-0.045=4.455mol H+/公顷 若以CaO中和:其需要量124.74 克 中和潜性酸: 2250000×(10 /100)×(1- 60/100)=90000 mol H+/公顷 90000×56/2=2520000克=2520公斤/公顷
水田土壤:
排水种植旱作期间:> 500 mv
淹水期间: < 150 mv
水稻适宜生长条件: 200 - 400 mv
影响土壤氧化还原的因素 1.微生物的活动
2.易分解有机的含量
在一定的通气条件下,土壤中的易分解的有机愈 多,耗氧也愈多,其氧化还原电位就较低。
3.土壤中易氧化和还原的无机物的含量 土壤的氧化体和硝酸盐含量高时,可使Eh值下降 得较慢。
潜 性 酸 (1)交换性酸度(soil exchangeable acidity) (2)水解性酸度(soil hydrolytic acidity)
几种土壤中的交换性酸量和水解性酸量的比较
3. 活性酸和潜性酸的关系
活性酸和潜酸的总和,称为土壤总酸度。由于 它通常是用滴定法测定的,故又称之为土壤的滴定酸 度。它是土壤的酸度的容量指标。它与pH值在意义 上是不同的。
土壤酸碱反应和氧化还原反应

过度施用石灰的负面影响
土壤板结,结构变劣; 部分微量元素有效性降低;磷的有效性
也下降。 因此,施用石灰要适量。 影响石灰施用量的因素有:
土壤潜性酸和pH;盐基饱和度;质地; 有机质含量;石灰的种类和施用方法; 作物的要求等;
石灰需要量的估算
石灰需要量= 土壤体积*容重*CEC*(1-盐基饱和度) 单位:千克/公顷
不同作物对土壤酸碱性都有一定的要求, 这是植物长期的自然选择的结果。常见 植物对土壤pH的要求见下表:
植物适宜的pH范围
适应偏碱 性pH7-8
紫苜蓿
适应中到微 碱性pH6.57.5
苹果
适应中到微 适应偏酸性 适应酸性 酸性的pH6-7 的pH5.5-6.5 的pH5-6
蚕豆
水稻
小麦
金花菜 黄花苜蓿 碗豆
包权
人书友圈7.三端同步
土壤酸碱性的分级
强酸性 酸性 中性 碱性 强碱性
pH<5.0 pH5.0-6.5 pH6.5-7.5 pH7.5-8.5 pH>8.5
2、潜性酸
(1)概念与成因 土壤胶粒上吸附的氢离子和铝离子进
入土壤溶液后表现出来的酸度,称为潜 性酸。
在一般矿质土壤中, 由交换性铝离子产 生的酸度, 比由交换性氢离子产生的酸度 重要。红壤的交换性酸度,90%以上是 由交换性铝所引起。
档消耗一个共享文档下载特权。
年VIP
月VIP
连续包月VIP
享受100次共享文档下载特权,一次 发放,全年内有效
赠每的送次VI的发P类共放型的享决特文定权档。有下效载期特为权1自个V月IP,生发效放起数每量月由发您放购一买次,赠 V不 我I送 清 的P生每 零 设效月 。 置起1自 随5每动 时次月续 取共发费 消享放, 。文一前档次往下,我载持的特续账权有号,效-自
土壤(第九章)土壤酸碱性和氧化还原反应..

土壤碱化度分级:
ESP 5%~10% 10%~15%
>15%
轻度碱化土 中度碱化土 强碱化土
盐土——土壤表层可溶性盐(以NaCl、Na2SO4等 中性盐为主)超过一定含量(6~20g/kg)。
我国碱土定义:碱化层碱化度>30%, 表层含盐量<5g/kg,pH>9.0
土壤学
资源环境学院土地资源与农业化学系
(2)生物因素 Na、K 、Ca、Mg等盐基的生物积累。 一些植物适应在较干旱条件下生长,而且有
富集碱性物质的作用:海蓬子含Na2CO3 3.75%, 碱蒿含2.76%。盐蒿含2.14%。
土壤学
资源环境学院土地资源与农业化学系
(3)母质 碱性物质的基本来源。基性岩、超基性岩富含
碱性物质。含盐基物质多,形成的土壤为碱性。 (4)施肥和灌溉
碱性土还原pH下降,主要由于在嫌气条件 下有机酸和CO2的积累过程及其综合作用。
土壤学
资源环境学院土地资源与农业化学系
第三节 土壤氧化还原反应
一、土壤氧化还原体系
土壤中同一物质可区分为氧化态(剂)和还原态 (剂),构成相应的氧化还原体系 。
土壤学
资源环境学院土地资源与农业化学系
1.土壤空气中O2是主要氧化剂 通气良好的土壤中,氧体系控制氧化还原反应,使 多种物质呈氧化态,如NO3-、Fe3+、Mn4+、SO42-等。 2.土壤有机质特别是新鲜有机物是主要还原剂,在 土壤缺O2条件下,将氧化物转化为还原态。 3.土壤中氧化还原体系可分为无机体系和有机体系。
6.土壤氧化还原状况随栽培管理措施特别是灌水、 排水而变化
土壤学
资源环境学院土地资源与农业化学系
二、土壤氧化还原指标
1. 强度指标 (1)氧化还原电位(Eh)
【土壤学】 第8章 土壤酸碱性和氧化还原性【精】

二、土壤碱度
碱性反应是土壤溶液OH-超过H+时反映出来,pH越高,碱性越强。
1、土壤总碱度
液相指标
石灰性土壤:具有石灰性反应的土壤。稀HCl检验。 2、土壤碱化度(钠饱和度) 固相指标
交换性钠离子占阳离子交换量的百分数,即钠饱和度。ESP 胶粒– Na + HOH =胶粒– H + NaOH 2 NaOH + H2CO3 = Na2CO3 + H2O 或 NaOH +CO2= Na2HCO3
石灰需要量 = 土壤体积 x 容重 x CEC x(1 -盐基饱和度) 石灰常数:石灰需用量理论值要乘以一经验常数,得出实际需用量。
石灰石粉: 1.3; 生石灰: 0.5
3、 改良土壤碱性
➢ 施用有机肥:CO2,有机酸 ➢ S及含S化合物 ➢ 生理酸性肥料 ➢ 石膏,硅酸钙,以钙换钠
第二节 土壤氧化还原性
3、与植物生长的关系
植物生长对土壤反应的要求 一般pH 6.5左右,各种养分有效性较高,大多数作物比较适宜。
五、土壤酸碱性的调节
1、土壤酸度的调节
1)施用石灰,调节土壤酸度,防Al, Mn危害
2)中和潜性酸 3)增加Ca,改良土壤结构 2、酸性土壤石灰需要量
方法
✓中和交换性酸或水解性酸 ✓依CEC和盐基饱和度计算
二、土壤氧化还原状况与土壤肥力的关系
1、指示土壤通气和排水情况
旱地一般 300-600; 若低于200,排水不良; 水田一般低于200-300,适宜180—200,若低于100,强还原,长期 -1 80以下,水稻死亡。
2、土壤养分形态和供应情况 高价—低价
3、 强还原状况下有毒物质产生和积累 有机酸, Fe2+ Mn2+ H2S CH4 H2
土壤酸碱性和氧化还原反应

活性酸 吸附 解吸 潜性酸
强酸性土壤 Soils with strong acidity
交换性Al3+与溶液Al3+处于平衡:
Soil colloid Al3+
Al3+
溶液中Al3+水解显示酸性:
Al3++3H2O
Al(OH)3+3H+
强酸性土中,Al3+大大多于交换性 H+,是活性酸(溶液 H+离子)的主要来源。 如:pH<4.8的红壤,交换性Al3+占总酸度的95%以上
M H
Soil colloid
M
+ 2H+
Soil colloid
H
+
2M+
土壤中H+的来源 Origin of H+ in soils
水的解离 Dissociation of H2O
HOH H OH
碳酸解离 Dissociation of H2CO3 有机酸的解离 Dissociation of organic acid
土壤酸碱性和氧化还原反应
第一节 土壤酸、碱性的形成
Formation of soil acidity and alkalinity
Importance
The soil reaction is a term used to indicate soil acidity/alkalinity or acid-base reactions in soils. Many soil chemical and biochemical reactions can occur only at specific soil acidity/alkalinity. The rate of decomposition of soil minerals and organic matter is influenced by soil acidity/alkalinity. Formation of clay minerals depends on soil pH. Plant growth is also affected either directly or indirectly by soil pH. H+ ions are reported to have a toxic effect on plants when present in high concentration.
强酸性土壤 Soils with strong acidity
交换性Al3+与溶液Al3+处于平衡:
Soil colloid Al3+
Al3+
溶液中Al3+水解显示酸性:
Al3++3H2O
Al(OH)3+3H+
强酸性土中,Al3+大大多于交换性 H+,是活性酸(溶液 H+离子)的主要来源。 如:pH<4.8的红壤,交换性Al3+占总酸度的95%以上
M H
Soil colloid
M
+ 2H+
Soil colloid
H
+
2M+
土壤中H+的来源 Origin of H+ in soils
水的解离 Dissociation of H2O
HOH H OH
碳酸解离 Dissociation of H2CO3 有机酸的解离 Dissociation of organic acid
土壤酸碱性和氧化还原反应
第一节 土壤酸、碱性的形成
Formation of soil acidity and alkalinity
Importance
The soil reaction is a term used to indicate soil acidity/alkalinity or acid-base reactions in soils. Many soil chemical and biochemical reactions can occur only at specific soil acidity/alkalinity. The rate of decomposition of soil minerals and organic matter is influenced by soil acidity/alkalinity. Formation of clay minerals depends on soil pH. Plant growth is also affected either directly or indirectly by soil pH. H+ ions are reported to have a toxic effect on plants when present in high concentration.
第9章 土壤酸碱性和氧化还原反应

6/60
(二)母质因素
母岩母质的组成性质对土壤酸碱度具有深刻的影响。
石灰岩、基性岩、超基性岩的盐基含量较高。当土壤的淋溶程 度较弱时,土壤pH会比附近其它母质上发育的土壤高。
滨海盐土含有丰富的易溶盐类及碳酸钙,加之地下水矿化度较 高。因此,发育的土壤的pH一般较高,土壤常呈碱性。
(四)施肥和灌溉的影响
1 土壤中的氧化还原体系 soil redox system
33/60
氧化剂:电子供体;被氧化; 还原剂:电子受体;被还原。
土壤中有多种氧化还原物质共存。
Oxidation: A reaction in which atoms or molecules gain oxygen, and lose hydrogen or electrons Fe2+=Fe3++eReduction: A reaction in which atoms or molecules lose oxygen, or gain hydrogen or electrons: N2+H2=NH3
high CEC = high buffering
29/60
3、 酸性土壤铝离子聚合对碱的缓冲作用
在 pH<5 的土壤中, Al3+ 被 6 个水分子所环绕, 形成水合铝离子。当土壤中 OH- 增多时,水合铝 离子聚合成更大的离子团,释放出H+:
2Al(H2O)63+ + 2OH[Al2(OH)2(H2O)8]4+ + 4H2O
我国土壤的酸碱性南北差异很大,由南向北土壤pH相差7个数量级。
2011_09土壤酸碱性和氧化还原反应

2. )潜性酸 土壤胶体上吸附的H 土壤胶体上吸附的 +和Al3+进入土壤溶液后表现出来的 酸度所引起的酸度。 酸度所引起的酸度。
表现形式 当它们从胶体上解离或被其它阳离子所交换 而转移到溶液中以后才显示酸性。 而转移到溶液中以后才显示酸性。
测定方法
交换性酸 水解性酸
3.) 活性酸与潜性酸的关系 )
M+ Al3+
H+ + 4KCl M+
K+ M+ K+ K+ K+ M+
+ Al3 + + H+
Al3++ 3H2O
Al(OH)3
+ 3H+
(2)水解性酸
用过量强碱弱酸盐( COONa)浸提土壤, 用过量强碱弱酸盐(CH3COONa)浸提土壤,胶体上的 氢离子或铝离子释放到溶液中所表现出来的酸性。 氢离子或铝离子释放到溶液中所表现出来的酸性。 COONa水解产生NaOH,pH值可达8.5, 水解产生NaOH 值可达8.5 CH3COONa水解产生NaOH,pH值可达8.5,Na+可以把绝 大部分的代换性氢离子和铝离子代换下来, 大部分的代换性氢离子和铝离子代换下来,从而形成醋 滴定溶液中醋酸的总量即得水解性酸度。 酸,滴定溶液中醋酸的总量即得水解性酸度。 Na+ M+ Al3+ H+ M+ + 4CH3COONa M+ Na+ Na+ Na+ + 4CH3COOH M+ + Al(OH)3
强酸性 酸性 微酸性 中性 微碱性 碱性 强碱性 pH值 值 <4.5 pH值 pH值 值 值 4.5~ 5.6~ ~ ~ 5.5 6.5 pH 值 pH 值 pH 值 pH值> 值 6.6 ~ 7.5 ~ 8.1~ 9.0 ~ . 7.4 8.0 9.0
第九章土壤酸碱性和氧化还原反应

水 解 酸
活性酸
Na+交换出的氢和铝离子产生的酸度
羟基化表面解离的H+
土壤活性酸与潜性酸的关系
活性酸与潜性酸具有动态平衡关系,是一个平衡体系中的 两种存在状态,他们同时存在且相互转化。
土壤活性酸(活性H+或Al3+)增多,可被土壤胶粒吸附成为潜性酸,促使潜性增多 潜性酸增多,胶体上的H+或Al3+又通过交换作用转移到土壤溶液中,促使活性酸增多
pH=pKa+lg[盐]/[酸]
pH=pKa+lg[盐基]/[H+、Al3+]
当土壤BS=50%时,对酸碱的缓冲能力最大。缓冲能力随 弱酸及其盐的总浓度或土壤CEC增加而增大。
(二)土壤酸碱缓冲体系(soil acid-base buffer system)
(1)碳酸盐体系:石灰性土壤的缓冲作用主要决定于
2、生物
主要是指具有富集碱性物质的植物,如海蓬子含Na2CO3 3.75%,碱蒿 2.76%,盐蒿2.14%,芦苇0.49%,这些植物死亡后,就将Na2CO3累积在土壤 中,从而导致土壤变碱。
3、施肥和灌溉
施用碱性肥料或用碱性水灌溉会使土壤碱化。如都江堰水质偏碱,长 期灌溉则会使稻田土壤pH升高。
4、母质
(2)土壤活性酸的测定
水浸酸:用水浸提得到的土壤酸度(pH水), 反应土壤活性酸
的强弱;
与盐浸酸:用KCl浸提获到的土壤酸度(pH盐),除反映土壤溶
液中的氢离子外,还反映由K+交换出的土壤胶体表面氢和铝 离子表现出的酸性。pH水通常大于pH盐
水土比对土壤pH值的影响:测定土壤pH值时的水土比一般用
4、植物根系的代谢作用:植物根系汾泌物可直接或间接影响根
土壤学第四章-土壤酸碱性和氧化还原反应

第二节 土壤氧化还原反应
一.土壤中的氧化还原体系
1、主要的体系:
Mn2+
Mn4+
锰
Fe3+
Fe2+
铁
O-2
O0
氧
S-2
S+6
硫
N-3
N+4
N+6 氮
H0
H+
氢
C-4
C+4
(有机)碳
2、主要的氧化剂和还原剂:
主要的氧化剂是土壤空气中的氧气当土壤中
的氧被消耗完后,依次NO-3、Mn4+、Fe3+、 SO42-作为电子受体被还原,这种依次被还原的 现象叫顺序还原作用.
三、土壤酸碱性和氧化还原状况与有毒物质的积 累:
1.强酸性土壤中Al3+、Mn2+的胁迫与毒害:
Al:PH<5.5 Al3+被活化, [Al3+]≥0.2 cmol/kg农作物受害,特别是幼苗。 PH5.5~6.3 可消除Al3+的毒害。
Mn:PH<5.5 [Mn2+]≥2~9cmol/kg、或植株干重 中含量为1000mg/kg时产生锰毒。
二、土壤碱性的形成: 1. 碱性形成机理: 土壤中碱性盐的水解是形成碱性反应的主要
机理 Ca Mg Na的CO32-和HCO3-以及吸附交换 性Na+
①CaCO3的水解: 石灰性土壤上交换性Ca2+占优势的土壤
CaCO3、CO2、H2O处于同一平衡体系中
CaCO3+H2O
Ca2++HCO3-+OH-
1>各种养分有效度较高的PH范围在6.5~7.5
第九章 土壤酸碱性和氧化还原反应

二.土壤酸度
1、 交换性酸 用中性盐溶液如1mol.L-1 KCL浸提土壤,土壤胶体表 面吸附的铝离子与氢离子进入溶液产生的酸。 2、水解性酸 用弱酸强碱盐溶液,如pH8.2的1mol.L-1 NaOAc溶 液浸提而产生的酸。
二.土壤酸度
(三)土壤酸化
是指在自然和人为条件下土壤pH下降的过程。 1、土壤酸化过程实质 2、土壤酸化的成因 (1)自然土壤发生过程 (2)生物地球化学过程 (3)施肥和土壤管理 (4)酸沉降 3、土壤酸化的环境效应 4、土壤酸化防治
土壤酸化过程
Al3+ Ca2+ 土壤 K+ 胶体 Na+ Mg2+ H+ + H+ Na Ca2+
Al3+
K+
Mg2+
H+
H+ 增加,土壤酸化 盐基离子淋溶
离子交换
二.土壤碱度
土壤碱性指标 1、pH 2、碱化度(钠碱化度;ESP-exchangeable sodium percentage) 是指土壤胶体吸附的交换性钠离子占阳离子交换量的百分率。
二.土壤酸度
(一)土壤活性酸 土壤溶液中的氢离子引起的酸,用pH表示。 土壤酸碱性划分 ﹤5.0 强酸性 5.0-6.5 酸性 6.5-7.5 中性 7.5-8.5 碱性 ﹥8.5 强碱性
二.土壤酸度
(二)土壤潜性酸 指土壤胶体上吸附的氢离子、铝离子等所产生 的酸,单位cmol.L-1/kg。 Al3++H2O⇋Al(OH)2++H+ Al(OH)2++ H2O⇋Al(OH)2++H+ Al(OH)2++H2O ⇋Al(OH)3+H+ 土壤中交换性铝离子是土壤潜性酸的主要贡献 者。在南方红壤土壤中占到90%以上。
土壤学课件第8章土壤酸碱性和氧化还原性

3、碱性土的成因
➢干旱气候;降水量低于蒸发量 ➢母质; 基性、超基性岩 ➢过量施用石灰; ➢引灌碱性污水; ➢海水pH7.5-8浸渍。
三、土壤缓冲作用
1、定义 ① 狭义:把少量的酸或碱加入到到土壤里,其pH值的变化却不大,这
种对酸碱变化的抵抗能力,叫做土壤的缓冲性能或缓冲作用。 ② 广义:土壤是一个巨大的缓冲体系,对营养元素、污染物质、氧化还
2、氧化还原电位 氧化还原反应的通式:氧化态 + ne- = 还原态
( 铂电极—甘汞电极,毫伏计) Nernst 公式
✓ E0为标准氧化还原电位(化学手册中可查到),氧化态和还原态浓度 相等时产生的电位
✓ n为反应中电子转移数 ✓ 用0.059时,单位为v,用59时为mv
Eh可作为土壤通气性的指标。
土壤酸、碱缓冲容量和滴定曲线
在土壤悬液中连续加入标准酸或碱液,测定pH的变化,以纵座 标表示pH,横座标表示加的酸或碱量,绘制滴定曲线,又称缓冲 曲线。
砖红壤、红壤和黄棕壤胶体的中和曲线(于天仁,1987)
四Байду номын сангаас土壤反应与肥力的关系
1、影响土壤微生物的活动
土壤细菌和放线菌,如硝化细菌,固N菌,纤维分解菌等,均 适宜于中性和微碱性环境;在酸性条件,活动急剧降低;真菌对酸 碱性要求不严格。
2、潜性酸:是土壤酸度的潜在来源。数量指标
表现:1、土壤胶体活性功能团解离H+离子 R-COOH = R-COO- + H+
2、土壤胶体上吸附的H+离子其它阳离子代换 3、土壤胶体上吸附的Al3+离子的作用
交换性Al3+离子进入溶液, Al3+离子水解,产生H+
9土壤酸碱性和氧化还原反应
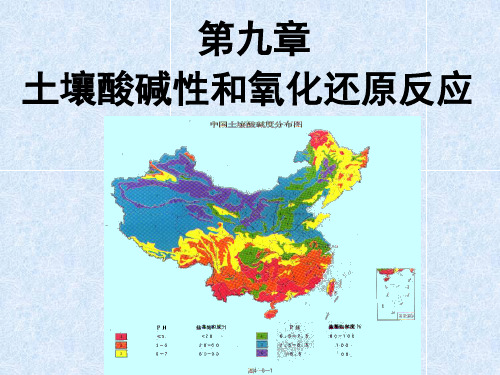
交换性酸量在进行调节土壤酸度,估算石灰用量时,有重要 参考价值。
(2)水解性酸度(soil hydrolytic acidity)
用弱酸强碱的盐类溶液(常用的为pH8.2的1mol NaOAc溶 液)浸提, 再以NaOH标准液滴定浸出液,根据所消耗的NaOH的 用量换算为土壤酸量。这样测得的潜性酸的量称之为土壤的水 解性酸。
***碱化度是指土壤胶体吸附的交换性钠离子
占阳离子交换量的百分率。
碱化度= 交换性钠 100 阳离子交换量
当土壤碱化度达到一定程度,可溶盐含量较低时, 土壤就呈极强的碱性反应,土壤理化性质上发生恶劣 变化,称为土壤的“碱化作用”(alkalinization)。
我国则以碱化层的碱化度>30%,表层含盐量<0.5%和 pH值>9.0定为碱土(alkaline soil) 。而将土壤碱化 度为5-10%定为轻度碱化土壤,10-15%为中度碱化 土壤,15-20%为强碱化土壤。
3
3
Al2 (OH) 2 ( H2 O) 8 4H2 O
[ Al4 (OH) 6 (OH2 )12 ]6 12H 2O
4
当土壤pH>5.0时,铝离子形成Al(OH)3沉淀, 失去它的缓冲能力。
5、有机酸体系 土壤腐殖酸,胡敏酸和富啡酸是一种大分 子有机酸,含有羧基、羟基、酚羟基、醇羟 基等功能团,此外,土壤中还存在多种低分 子有机酸,在土壤溶液中构成一个良好的缓 冲体系。对酸、碱具有缓冲作用。
石灰位= pH-0.5pCa
土壤酸度是土壤酸、碱性的简称
二、土壤酸度的数量指标
土壤胶体上吸附的氢、铝离子所反映的潜性酸量, 可用交换性酸度和水解酸度表示。 (1)交换性酸度(soil exchangeable acidity)
(2)水解性酸度(soil hydrolytic acidity)
用弱酸强碱的盐类溶液(常用的为pH8.2的1mol NaOAc溶 液)浸提, 再以NaOH标准液滴定浸出液,根据所消耗的NaOH的 用量换算为土壤酸量。这样测得的潜性酸的量称之为土壤的水 解性酸。
***碱化度是指土壤胶体吸附的交换性钠离子
占阳离子交换量的百分率。
碱化度= 交换性钠 100 阳离子交换量
当土壤碱化度达到一定程度,可溶盐含量较低时, 土壤就呈极强的碱性反应,土壤理化性质上发生恶劣 变化,称为土壤的“碱化作用”(alkalinization)。
我国则以碱化层的碱化度>30%,表层含盐量<0.5%和 pH值>9.0定为碱土(alkaline soil) 。而将土壤碱化 度为5-10%定为轻度碱化土壤,10-15%为中度碱化 土壤,15-20%为强碱化土壤。
3
3
Al2 (OH) 2 ( H2 O) 8 4H2 O
[ Al4 (OH) 6 (OH2 )12 ]6 12H 2O
4
当土壤pH>5.0时,铝离子形成Al(OH)3沉淀, 失去它的缓冲能力。
5、有机酸体系 土壤腐殖酸,胡敏酸和富啡酸是一种大分 子有机酸,含有羧基、羟基、酚羟基、醇羟 基等功能团,此外,土壤中还存在多种低分 子有机酸,在土壤溶液中构成一个良好的缓 冲体系。对酸、碱具有缓冲作用。
石灰位= pH-0.5pCa
土壤酸度是土壤酸、碱性的简称
二、土壤酸度的数量指标
土壤胶体上吸附的氢、铝离子所反映的潜性酸量, 可用交换性酸度和水解酸度表示。 (1)交换性酸度(soil exchangeable acidity)
医学课件第八章土壤酸碱性和氧化还原反应

白杨 洋槐 松树 栋树 泡桐
6.0—8.0 6.0—8.0 5.0—6.0 5.0—6.0 6.0—8.0
马铃薯 4.8——5.4
杏
6.0—8.0 油 桐 6.0—8.0
向日葵 6.0——8.0 苹 果 6.0—8.0 榆 树 6.0—8.0
甘 蔗 6.0—7.0 桃、梨 6.0—8.0 掸 树 5.0—6.0
(一)气候因素 它决定成土过程的淋溶强度。气温高、降雨量大
的气候条件,母质、土壤中的盐基成分易于遭受淋失,使土壤逐渐
酸化。反之,干旱气候,降雨量远远低于蒸发量,盐基成分积累于
土壤及地下水,使土壤向碱化方向演化。即“南酸北碱”。
(二)母质因素 母岩母质的组成性质对土壤酸碱度具有深刻的影
响。如酸性岩上发育的土壤容易向酸性发展,而基性岩相反。
碱性() 8.北方石灰性土壤的潜(性)在酸比南方酸性土壤高,是因为石灰
性土壤的CEC比酸性土高所致() 9.盐基饱和度大的土壤,缓冲酸的能力强,盐基饱和度小的缓冲碱
的能力强() 10.旱地通气条件良好,则Eh比水田要高()
氧化态 + ne ==== 还原态
氧化还原反应中的氧化态和还原态同时在电极上达到平 衡,其平衡电位,称为氧化还原电位,通常以Eh表示。
Eh E 0 RT ln a氧化剂
nF
a 还原剂
E0
0.059 n
log
[氧化态 ] [还原态 ]
☻(二)土壤间Eh的变化范围
➢ 旱地土壤Eh变动在200—750mv之间,如果大于 750mv,标志着土壤完全处于好气状态。如果Eh低 于200mv,则表明土壤水分过多,通气不良。土壤 的Eh在400—700mv之间,多数作物可以正常发育, 过高过低均对植物不利。
土壤酸碱性和氧化还原反应森林土壤

石灰位=
是Ca(OH)2的化学位的简单函数。上式中为Ca(OH)2 在标准状况下的化学位
3、土壤碱性指标
(一)总碱度 总碱度是指土壤溶液或灌溉水中碳酸根、重碳酸根的
总量。我国碱化土壤的总碱度占阴离子总量的50%以上, 高的可达90%,故可用总碱度作为土壤碱化程度分级的 指标之一。即
总 碱 度 = C O 3 2 H C O 3 ( 厘 摩 尔 ( ) / 升 )
一、土壤酸碱形成的原因
1、土壤酸性形成的机理 (1)土壤中氢离子的来源: ★水的解离 ★碳酸解离 ★有机酸的解离 ★酸雨 ★其它无机酸 (2)土壤中铝离子的活化(形成酸性土壤的重要原因)
土壤酸化过程 Al3+
A土l3+壤CKa2++ 胶体 Na+
Mg2+
Ca2+ K+
Mg2+
H+ H+ H+ Na+
交换性酸量在进行调节土壤酸度,估算石灰用量时,有重要 参考价值。
(2)水解性酸度(soil hydrolytic acidity)
用弱酸强碱的盐类溶液(如的1mol NaOAc溶液)浸提, 再以 NaOH标准液滴定浸出液,根据所消耗的NaOH的用量换算为土壤 酸量。这样测得的潜性酸的量称之为土壤的水解性酸。
土壤的pH值随土壤含水量增加有上升的趋势。 因此,在测定土壤pH值时,应注意土水比。土水比 愈大,所测得的pH值愈大。
(四)土壤氧化还原条件对pH的影响
淹水或施有机肥促进土壤还原的发展,对土壤pH有明 显的影响。酸性土淹水后pH升高的原因主要是由于在嫌 气条件下形成的还原性碳酸铁、锰呈碱性,溶解度较大, 因之pH值升高。
二、土壤酸碱性和氧化还原状况与养分的生物有效性
是Ca(OH)2的化学位的简单函数。上式中为Ca(OH)2 在标准状况下的化学位
3、土壤碱性指标
(一)总碱度 总碱度是指土壤溶液或灌溉水中碳酸根、重碳酸根的
总量。我国碱化土壤的总碱度占阴离子总量的50%以上, 高的可达90%,故可用总碱度作为土壤碱化程度分级的 指标之一。即
总 碱 度 = C O 3 2 H C O 3 ( 厘 摩 尔 ( ) / 升 )
一、土壤酸碱形成的原因
1、土壤酸性形成的机理 (1)土壤中氢离子的来源: ★水的解离 ★碳酸解离 ★有机酸的解离 ★酸雨 ★其它无机酸 (2)土壤中铝离子的活化(形成酸性土壤的重要原因)
土壤酸化过程 Al3+
A土l3+壤CKa2++ 胶体 Na+
Mg2+
Ca2+ K+
Mg2+
H+ H+ H+ Na+
交换性酸量在进行调节土壤酸度,估算石灰用量时,有重要 参考价值。
(2)水解性酸度(soil hydrolytic acidity)
用弱酸强碱的盐类溶液(如的1mol NaOAc溶液)浸提, 再以 NaOH标准液滴定浸出液,根据所消耗的NaOH的用量换算为土壤 酸量。这样测得的潜性酸的量称之为土壤的水解性酸。
土壤的pH值随土壤含水量增加有上升的趋势。 因此,在测定土壤pH值时,应注意土水比。土水比 愈大,所测得的pH值愈大。
(四)土壤氧化还原条件对pH的影响
淹水或施有机肥促进土壤还原的发展,对土壤pH有明 显的影响。酸性土淹水后pH升高的原因主要是由于在嫌 气条件下形成的还原性碳酸铁、锰呈碱性,溶解度较大, 因之pH值升高。
二、土壤酸碱性和氧化还原状况与养分的生物有效性
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
Mg2+
H+ H+ H+ Na+
离子交换
H+ 增加,土壤酸化 盐基离子淋溶
可编辑版
6
2、土壤碱性形成的机理
形成碱性反应的主要机理 是碱性物质的水解反应。
土壤中的碱性物质主要是钙、镁、 钠的碳酸盐和重碳酸盐,以及胶体表 面吸附的交换性钠。
可编辑版
7
▲碳酸钙水解
从上式可知:石灰性土壤的pH值主要受土壤空气中CO2分压控制 (1) 石灰性土壤的pH值,因CO2的偏压大小而变,所以在测定石灰 性土壤pH值时,应在固定的CO2偏压下进行,并必须注意在充分达到 平衡后测读。
交换性酸量在进行调节土壤酸度,估算石灰用量时,有重要
参考价值。
可编辑版
11
(2)水解性酸度(soil hydrolytic acidity)
用弱酸强碱的盐类溶液(如pH8.2的1mol NaOAc溶液)浸提, 再以NaOH标准液滴定浸出液,根据所消耗的NaOH的用量换算为 土壤酸量。这样测得的潜性酸的量称之为土壤的水解性酸。
当土壤胶体上吸附的阳离子全部是致酸离子,称为 盐基完全不饱和态。此时土壤的pH值,称为土壤的极限 pH值。
土壤总酸度=活性酸度+潜在酸度
活性酸是土壤酸度的起源,代表土壤酸度的强度; 潜在酸是土壤酸度的主体,代表土壤酸度的容量。
可编辑版
14
2、土壤酸度的强度指标
★土壤pH
土壤pH代表与土壤固相处于平衡的溶液中的H+离 子浓度的负对数, ★石灰位(lime potential)
在土壤胶体表面吸附的盐基离子中总是以钙离子 为主的,在酸性土壤的盐基离子中,钙离子约占总量 65-80%。因此,提出了表示土壤酸强度的另一指标 -石灰位。它将氢离子数量与钙离子数量联系起来,以 数学式pH-0.5PCa表示之,即
第九章
土壤酸碱性及氧化还原反应
可编辑版
1
第一节 土壤酸碱反应
土壤酸碱性反应
土壤酸碱反应是指土壤酸性或碱 性的程度,常以pH值表示。
土壤酸碱反应是气候、植被、成土 母质等及人为因素共同作用的结果
可编辑版
2
我国土壤的酸碱性反应,大多 数在pH4.5~8.5之间。在地理分布 上有“东南酸西北碱”的规律性。 大致可以长江为界(北纬33),长 江以南的土壤多为酸性或强酸性, 长江以北的土壤多为中性或碱性。 我国土壤的酸碱性南北差异很大
生
可编辑版
9
二、土壤酸碱性度类型和指标 1、土壤酸度类型
★ 活性酸度(soil active acidity)
土壤活性酸是自由扩散于土壤溶液中的氢离 子浓度直接反应出来的酸度。
可编辑版
10
★潜性酸 (soil potential acidity)土壤潜性酸是由于土 壤胶粒上吸附着氢离子和铝离子所造成的显出酸性,所 以它是土壤酸的潜在来源,故称为潜性酸。
结果:①交换程度比之用中性盐类溶液更为完全,土壤吸附性氢、 铝离子的绝大部分可被Na+离子交换。②水化氧化物表面的羟基 和腐殖质的某些功能团(如羟基、羧基)上部分H+解离而进入 浸提液被中和。
可编辑版
12
可编辑版
13
★活性酸和潜性酸的关系
活性酸和潜性酸的总和,称为土壤总酸度。由 于它通常是用滴定法测定的,故又称之为土壤的滴定 酸度。它是土壤的酸度的容量指标。它与pH值在意义 上是不同的。
总 碱 度 = C O 3 2 H C O 3 ( 厘 摩 尔 ( ) / 升 )
石灰性物质所引起的弱碱性反应(pH7.5-8.5)称为石灰性反应,
土壤称之为石灰性土壤。石灰性土壤的耕层因受大气或土壤中
CO2分压的控制,pH值常在8.0-8.5范围内,而在其深层,因植物 根系及土壤微生物活动都很弱,CO2分压很小,其pH值可升至 10.0以上。
可编辑版
17
(二)碱化度(钠碱化度:ESP)
碱化度是指土壤胶体吸附的交换性钠离子占 阳离子交换量的百分率。
碱 化 度 = 阳 交 离 换 子 性 交 钠 换 量 1 0 0
当土壤碱化度达到一定程度,可溶盐含量较低时, 土壤就呈极强的碱性反应,土壤理化性质上发生恶劣变
化,称为土壤的“碱化作用”(alkalinization)。
可编辑版
3
可编辑版
4
一、土壤酸碱形成的原因
1、土壤酸性形成的机理 (1)土壤中氢离子的来源: ★水的解离 ★碳酸解离 ★有机酸的解离 ★酸雨 ★其它无机酸 (2)土壤中铝离子的活化(形成酸性土壤的重要原因)
可编辑版
5
土壤酸化过程 Al3+
A土l3+壤CKa2++ 胶体 Na+
Mg2+
Ca2+ K+
可用交换性酸度和水解酸度表示。
(1)交换性酸度(soil exchangeable acidity)
用中性盐溶液如1mol KCl或0.06mol BaCl溶液(pH=7)浸提土壤时 土壤胶体表面吸附的铝离子与氢离子的大部分被浸提剂的阳离子 交换而进入溶液,浸出液中的氢离子及由铝离子水解产生的氢离 子,用标准碱液滴定,根据消耗的碱量换算,为交换性氢与交换性 铝的总量,即为交换性酸量(包括活性酸)。以厘摩尔(+)/千克) 为单位,它是土壤酸度的数量指标。
பைடு நூலகம்
我国则以碱化层的碱化度>30%,表层含盐量<0.5%和pH值>9.0
定为碱土(alkaline soil) 。而将土壤碱化度为5-10%定为轻
度碱化土壤,10-15%为中度碱化土壤,15-20%为强碱化土
壤。
可编辑版
18
三、影响土壤pH值的因素
(一)土壤胶体类型和性质对pH值的影响
1.土壤胶体的极限pH值
(2)土壤空气中CO2含量虽然高于大气,但很少高于10%,因此石灰
性土壤的pH总是在6.8~8.5之间,施用石灰中和土壤酸度是比较安
全的,不会使土壤过碱。
可编辑版
8
▲碳酸钠的水解
▲交换性钠的水解
土壤碱化与盐化有着发生学上的联系。
盐土和碱土并非一物“盐碱土”,盐土的pH值一般小于
8.5, 盐土脱盐才可能 形成碱土。积盐和脱盐交替发
石灰位= pH-0.5pCa
可编辑版
15
pH-0.5pCa是Ca(OH)2的化学位的简单函数。上式中 为Ca(OH)2在标准状况下的化学位
可编辑版
16
3、土壤碱性指标
(一)总碱度
总碱度是指土壤溶液或灌溉水中碳酸根、重碳酸根的 总量。我国碱化土壤的总碱度占阴离子总量的50%以上, 高的可达90%,故可用总碱度作为土壤碱化程度分级的 指标之一。即
H+ H+ H+ Na+
离子交换
H+ 增加,土壤酸化 盐基离子淋溶
可编辑版
6
2、土壤碱性形成的机理
形成碱性反应的主要机理 是碱性物质的水解反应。
土壤中的碱性物质主要是钙、镁、 钠的碳酸盐和重碳酸盐,以及胶体表 面吸附的交换性钠。
可编辑版
7
▲碳酸钙水解
从上式可知:石灰性土壤的pH值主要受土壤空气中CO2分压控制 (1) 石灰性土壤的pH值,因CO2的偏压大小而变,所以在测定石灰 性土壤pH值时,应在固定的CO2偏压下进行,并必须注意在充分达到 平衡后测读。
交换性酸量在进行调节土壤酸度,估算石灰用量时,有重要
参考价值。
可编辑版
11
(2)水解性酸度(soil hydrolytic acidity)
用弱酸强碱的盐类溶液(如pH8.2的1mol NaOAc溶液)浸提, 再以NaOH标准液滴定浸出液,根据所消耗的NaOH的用量换算为 土壤酸量。这样测得的潜性酸的量称之为土壤的水解性酸。
当土壤胶体上吸附的阳离子全部是致酸离子,称为 盐基完全不饱和态。此时土壤的pH值,称为土壤的极限 pH值。
土壤总酸度=活性酸度+潜在酸度
活性酸是土壤酸度的起源,代表土壤酸度的强度; 潜在酸是土壤酸度的主体,代表土壤酸度的容量。
可编辑版
14
2、土壤酸度的强度指标
★土壤pH
土壤pH代表与土壤固相处于平衡的溶液中的H+离 子浓度的负对数, ★石灰位(lime potential)
在土壤胶体表面吸附的盐基离子中总是以钙离子 为主的,在酸性土壤的盐基离子中,钙离子约占总量 65-80%。因此,提出了表示土壤酸强度的另一指标 -石灰位。它将氢离子数量与钙离子数量联系起来,以 数学式pH-0.5PCa表示之,即
第九章
土壤酸碱性及氧化还原反应
可编辑版
1
第一节 土壤酸碱反应
土壤酸碱性反应
土壤酸碱反应是指土壤酸性或碱 性的程度,常以pH值表示。
土壤酸碱反应是气候、植被、成土 母质等及人为因素共同作用的结果
可编辑版
2
我国土壤的酸碱性反应,大多 数在pH4.5~8.5之间。在地理分布 上有“东南酸西北碱”的规律性。 大致可以长江为界(北纬33),长 江以南的土壤多为酸性或强酸性, 长江以北的土壤多为中性或碱性。 我国土壤的酸碱性南北差异很大
生
可编辑版
9
二、土壤酸碱性度类型和指标 1、土壤酸度类型
★ 活性酸度(soil active acidity)
土壤活性酸是自由扩散于土壤溶液中的氢离 子浓度直接反应出来的酸度。
可编辑版
10
★潜性酸 (soil potential acidity)土壤潜性酸是由于土 壤胶粒上吸附着氢离子和铝离子所造成的显出酸性,所 以它是土壤酸的潜在来源,故称为潜性酸。
结果:①交换程度比之用中性盐类溶液更为完全,土壤吸附性氢、 铝离子的绝大部分可被Na+离子交换。②水化氧化物表面的羟基 和腐殖质的某些功能团(如羟基、羧基)上部分H+解离而进入 浸提液被中和。
可编辑版
12
可编辑版
13
★活性酸和潜性酸的关系
活性酸和潜性酸的总和,称为土壤总酸度。由 于它通常是用滴定法测定的,故又称之为土壤的滴定 酸度。它是土壤的酸度的容量指标。它与pH值在意义 上是不同的。
总 碱 度 = C O 3 2 H C O 3 ( 厘 摩 尔 ( ) / 升 )
石灰性物质所引起的弱碱性反应(pH7.5-8.5)称为石灰性反应,
土壤称之为石灰性土壤。石灰性土壤的耕层因受大气或土壤中
CO2分压的控制,pH值常在8.0-8.5范围内,而在其深层,因植物 根系及土壤微生物活动都很弱,CO2分压很小,其pH值可升至 10.0以上。
可编辑版
17
(二)碱化度(钠碱化度:ESP)
碱化度是指土壤胶体吸附的交换性钠离子占 阳离子交换量的百分率。
碱 化 度 = 阳 交 离 换 子 性 交 钠 换 量 1 0 0
当土壤碱化度达到一定程度,可溶盐含量较低时, 土壤就呈极强的碱性反应,土壤理化性质上发生恶劣变
化,称为土壤的“碱化作用”(alkalinization)。
可编辑版
3
可编辑版
4
一、土壤酸碱形成的原因
1、土壤酸性形成的机理 (1)土壤中氢离子的来源: ★水的解离 ★碳酸解离 ★有机酸的解离 ★酸雨 ★其它无机酸 (2)土壤中铝离子的活化(形成酸性土壤的重要原因)
可编辑版
5
土壤酸化过程 Al3+
A土l3+壤CKa2++ 胶体 Na+
Mg2+
Ca2+ K+
可用交换性酸度和水解酸度表示。
(1)交换性酸度(soil exchangeable acidity)
用中性盐溶液如1mol KCl或0.06mol BaCl溶液(pH=7)浸提土壤时 土壤胶体表面吸附的铝离子与氢离子的大部分被浸提剂的阳离子 交换而进入溶液,浸出液中的氢离子及由铝离子水解产生的氢离 子,用标准碱液滴定,根据消耗的碱量换算,为交换性氢与交换性 铝的总量,即为交换性酸量(包括活性酸)。以厘摩尔(+)/千克) 为单位,它是土壤酸度的数量指标。
பைடு நூலகம்
我国则以碱化层的碱化度>30%,表层含盐量<0.5%和pH值>9.0
定为碱土(alkaline soil) 。而将土壤碱化度为5-10%定为轻
度碱化土壤,10-15%为中度碱化土壤,15-20%为强碱化土
壤。
可编辑版
18
三、影响土壤pH值的因素
(一)土壤胶体类型和性质对pH值的影响
1.土壤胶体的极限pH值
(2)土壤空气中CO2含量虽然高于大气,但很少高于10%,因此石灰
性土壤的pH总是在6.8~8.5之间,施用石灰中和土壤酸度是比较安
全的,不会使土壤过碱。
可编辑版
8
▲碳酸钠的水解
▲交换性钠的水解
土壤碱化与盐化有着发生学上的联系。
盐土和碱土并非一物“盐碱土”,盐土的pH值一般小于
8.5, 盐土脱盐才可能 形成碱土。积盐和脱盐交替发
石灰位= pH-0.5pCa
可编辑版
15
pH-0.5pCa是Ca(OH)2的化学位的简单函数。上式中 为Ca(OH)2在标准状况下的化学位
可编辑版
16
3、土壤碱性指标
(一)总碱度
总碱度是指土壤溶液或灌溉水中碳酸根、重碳酸根的 总量。我国碱化土壤的总碱度占阴离子总量的50%以上, 高的可达90%,故可用总碱度作为土壤碱化程度分级的 指标之一。即
