二点速率法在比色分析中的应用
化学反应速率的实验测定方法

化学反应速率的实验测定方法化学反应速率是指反应物转化为生成物的速度,可以通过实验测定来确定。
本文将介绍几种常用的化学反应速率的实验测定方法。
一、初始速率法初始速率法是指在反应初期,当反应物的浓度变化很小,可以忽略不计时,测量单位时间内生成物的质量或体积变化。
它适用于反应速率在整个反应过程中变化不大的反应。
初始速率法的实验步骤如下:1. 准备好所需的实验器材和试剂,确保实验条件的准确性和稳定性。
2. 测量反应物初始浓度,并将反应物混合,开始反应。
3. 在一定的时间间隔内,取样并测量反应物浓度的减少或生成物浓度的增加。
4. 计算出单位时间内反应物的质量或体积变化,即可得到初始速率。
二、比色法比色法适用于颜色较深或有明显的吸光峰的反应。
通过比色计或分光光度计测量反应物或生成物的吸光度,从而确定反应速率。
比色法的实验步骤如下:1. 准备好所需的实验器材和试剂,确保实验条件的准确性和稳定性。
2. 反应开始后,定时取样,并将样品转移到比色皿中。
3. 使用比色计或分光光度计测量样品的吸光度。
4. 根据吸光度和时间的关系曲线,计算出反应速率。
三、体积法体积法适用于生成气体的反应。
通过测量气体的体积变化,确定反应速率。
体积法的实验步骤如下:1. 准备好所需的实验器材和试剂,确保实验条件的准确性和稳定性。
2. 在一定的时间间隔内,测量产生的气体体积的变化。
3. 根据体积变化与时间的关系,计算出反应速率。
四、导电法导电法适用于涉及电解质的反应。
通过测量反应液电导率的变化,确定反应速率。
导电法的实验步骤如下:1. 准备好所需的实验器材和试剂,确保实验条件的准确性和稳定性。
2. 反应开始后,定时测量反应液的电导率。
3. 根据电导率和时间的关系,计算出反应速率。
总结:化学反应速率的实验测定方法有初始速率法、比色法、体积法和导电法等。
在选择合适的方法时,需要根据反应类型、反应物的特性和实验条件等因素综合考虑。
通过实验测定反应速率,可以深入了解反应机理,并为控制和优化化学过程提供依据。
肌酐酶法测定的两点法

肌酐酶法测定的两点法摘要】建立了实用的肌酐酶法测定方法,通过实验将比色测定终点法改为两点法,使其适合自动分析,并节省工具酶。
本法的线性为0~2749 Μmmol/L,精密度:手工操作,批内CV<3%,总CV<5%。
三种分析仪的批内CV在0.34%~1.44%间,回收率99.66%~100.9%。
本法(Y)和BM的试剂(X)比较:Y=0.973X+10.33Μmol/L,r=0.9995。
【关键词】肌酐酶法两点法【中图分类号】R446 【文献标识码】B 【文章编号】2095-1752(2013)35-0355-02酶法测定肌酐目前已报告的有四条途径[1~5],其中三种为紫外测定,一种为比色测定。
相比之下比色测定具有更多优越性,商品试剂盒多采用此法。
但Fossati原法[1,2]的反应时间较长,且要做一血清空白以除去血清中肌酸的干扰,因此不适合自动分析。
自动分析一般总反应时间为10分钟,为了除去肌酸的干扰必须采用两步法,反应要求5分钟内达到终点。
据我们实验,必须将几种工具酶的用量增加到Fossati原法的5~10倍。
在实验过程中我们还发现几种工具酶的水解速率均较缓慢,反应的线性时间较长,因此将其改成两点法或速率法测定,取得很好的结果。
1 原理第一步反应:排除肌酸干扰;第二步反应:测定肌酐;肌酸反应同第一步。
2 材料和方法2.1仪器自动分析仪HITACHI 7170,Beckman Synchron △CX5和Ciba Coring Express Plus。
分光光度计Beckman DU-640。
2.2原料试剂肌酐酰氨基水解酶(Cretininase,CRNase);肌酸脒基水解酶(Creatininase,CRTase);肌氨酸氧化酶(SO);棘根过氧化物酶(POD),抗坏血酸氧化酶(ASO),均为Boehringer Mannheim公司产品。
3,5-二氯-2-羟-苯磺酸(DHBA),4-氨基安替比林(4-AAP)和肌酐为Sigma公司产品。
两点法、终点法、速率法

什么叫两点法、终点法、速率法?两点法:测定酶反应开始后某一时间内(t1到t2)产物或底物浓度的总变化量以求取酶反应初速度的方法。
终点法:通过测定酶反应开始到反应达到平衡时产物或底物浓度总变化量,以求出酶活力的方法,亦称平衡法。
速率法:是指连续测定(每15秒~1分钟监测一次)酶反应过程中某一反应产物或底物的浓度随时间的变化来求出酶反应的初速度的方法,即连续监测法。
一、常用生化检测项目分析方法举例1.终点法检测常用的有总胆红素(氧化法或重氮法)、结合胆红素(氧化法或重氮法)、血清总蛋白(双缩脲法)、血清白蛋白(溴甲酚氯法)、总胆汁酸(酶法)、葡萄糖(葡萄糖氧化酶法)、尿酸(尿酸酶法)、总胆固醇(胆固醇氧化酶法)、甘油三酯(磷酸甘油氧化酶酶法)、高密度脂蛋白胆固醇(直接测定法)、钙(偶氮砷Ⅲ法)、磷(紫外法)、镁(二甲苯胺蓝法)等。
以上项目中,除钙、磷和镁基本上还使用单试剂方式分析因而采用一点终点法外,其它测定项目都可使用双试剂故能选用两点终点法,包括总蛋白、白蛋白测定均已有双试剂可用。
2.固定时间法苦味酸法测定肌酐采用此法。
(两点法)3.连续监测法对于酶活性测定一般应选用连续监测法,如丙氨酸氨基转移酶、天冬氨酸氨基转移酶、乳酸脱氢酶、碱性磷酸酶、γ谷氨氨酰基转移酶、淀粉酶和肌酸激酶等。
一些代谢物酶法测定的项目如己糖激酶法测定葡萄糖、脲酶偶联法测定尿素等,也可用连续监测法。
4.透射比浊法透射比浊法可用于测定产生浊度反应的项目,多数属免疫比浊法,载脂蛋白、免疫球蛋白、补体、抗"O"、类风湿因子,以及血清中的其他蛋白质如前白蛋白、结合珠蛋白、转铁蛋白等均可用此法。
二、分析参数设置分析仪的一些通用操作步骤如取样、冲洗、吸光度检测、数据处理等,其程序均已经固化在存储器里,用户不能修改。
各种测定项目的分析参数(analysis paramete)大部分也已设计好,存于磁盘中,供用户使用;目前大多数生化分析仪为开放式,用户可以更改这些参数。
全自动生化分析仪的常用检测方法

A
( 吸 光 度 )
速率法
A/min=[(A2-A1 )-(Leabharlann 白)]/(t2-t1) Al A2
R2 S+R1
T
(时间)
1/13/2019
58
1.连续监测法特点
• 与固定时间法相比,属于即时观测,无需 停止酶促反应、不需添加其他呈色试剂, 且可将多点的测定结果绘图连线,快速、 直观查看酶促反应进程,很容易找到呈直 线的线性期,检查到是否偏离零级反应。
• 不同浓度的同一种物质,在某一定波长下 吸光度 A 不同,在λmax处吸光度A 的差异 最大。此特性可作为物质定量分析的依据 。
在分光光度法中, 以吸光度 ______为纵坐标, 以 波长 为横坐标作图可得光吸收曲线。 ____ 浓度不同的同种溶液, 在该种曲线中其最 相同 大吸收波长_______ ,相应的吸光度大小 不同 ,同一波长下摩尔吸数 相同 。 则_______
(一)光学因素
3.反射光和散色光的影响: 反射光和散色光均是入射光谱带宽度内 的光直接对T产生影响。 散射和反射使T↓,A↑,吸收光谱变形 注:一般可用空白对比校正消除 4.非平行光的影响: 使光程↑,A↑,吸收光谱变形
(二)化学因素
• 溶液中的溶质可因 c 的改变而有离解、 缔合、配位以及与溶剂间的作用等原因而 发生偏离 L-B 定律的现象 。
讨论
入射光的谱带宽度严重影响吸光系数和吸收光谱形状
E1=E2 E1≠E2 (E2-E1)↑
结论: ● ●
A=E1C·L A与C不成线性关系,偏离Beer定律 A与C偏离线性关系越严重
选择较纯单色光(Δ λ ↓,单色性↑) 选λ max作为测定波长
肌酐酶法测定的两点法分析

肌酐酶法测定的两点法分析摘要:目的:肌酐酶酶测定的两点分析。
方法:通过两种试剂进行比较。
反应温度为37℃,波长为500~520 纳米(主)/650 纳米(次);标准为15毫升;样品也为15 毫升;试剂Ⅰ:200 毫升,孵育时间为300秒;试剂Ⅱ:50 毫升,第一点读数时间为120秒,第二点读数时间为300秒。
结果:酶法具有去除肌酸的干扰能力,有线性范围宽,精度高等特点。
结论:两点法对肌酐酶法测点有良好的作用。
关键字:肌酐酶法两点法对于酶法测定肌酐,目前已报告的有四种方式,其中三种均为紫外测定,一种为比色测定。
然而,在相比之下比色测定在除去肌酸的干扰能力、线性范围、精度等具有更高的优越性;市场上出售的商品试剂盒大多采用此法。
但fossati 原法的反应时间比较长,且要做一血清空白以除去血清中肌酸的干扰,这样不适合进行自动分析。
自动分析的一般反应时间为十分钟,为了除去肌酸的干扰必须采用两步法,反应时间要求在五分钟内达到。
根据实验。
必须将几种工具酶的用量增加到fossati原法的五到十倍。
然而,在实验过程中发现几种工具酶的水解速率均比较缓慢,反应的线性时间比较长;所以,将其改成两点法或是速率法测定,会取得很好的实验结果。
这也体现出两点法的优势。
1原理第一步反应:排除肌酸干扰第二步反应:测定肌酐2材料与方法2.1仪器:自动分析仪HITACHI7170,Beckman Synchron △CX5和Ciba Coring Express Plus。
分光光度计Beckman DU-640。
2.2原料试剂:原料试剂采用的工具酶比较多,如:肌酐酰氨基水解酶,肌酸脒基水解酶,肌氨酸氧化酶,棘根过氧化物酶,抗坏血酸氧化酶,这些工具酶均为Boehringer Mannheim公司产品。
3,5-二氯-2-羟-苯磺酸(DHBA),4-氨基安替比林(4-AAP)和肌酐,均选用适量的剂量。
2.3应用试剂:试剂Ⅰ:每升磷酸盐缓冲液(150 Mmol/L,pH为7.5)中含CRTase 20 kU,SO 6 kU,POD 1 kU,ASO 1 kU,DHBA 3 Mmol,K4Fe(CN)6 20 Mmol,和4-AAP 4 Mmol。
化学反应的反应速率常数测定

化学反应的反应速率常数测定化学反应的反应速率常数是描述化学反应快慢程度的重要指标,它可以帮助我们了解反应机理和反应条件对反应速率的影响。
本文将介绍几种测定化学反应速率常数的常用方法。
一、初始速率法测定反应速率常数初始速率法是测定反应速率常数的一种简单有效的方法。
它要求在反应初期,反应物浓度变化不大,从而可以通过测定一段短时间内反应产物生成的变化来确定反应速率常数。
以一阶反应为例,反应速率方程可以表示为:r=k[A],其中r为反应速率,k为反应速率常数,[A]为反应物A的浓度。
1. 准备工作:将反应物A溶液和催化剂(如果有)分别置于两个烧杯中。
使用试剂枪将两个烧杯内的溶液喷射到反应器中,立即开启计时器。
2. 反应过程观察:记录在不同时间间隔内反应产物的浓度变化。
由于反应物浓度变化不大,可以通过测定较短时间内的产物生成量的变化来确定反应速率常数。
3. 数据处理:根据实验所得数据,使用对数函数来求解反应速率常数k的值。
对于一阶反应来说,可以使用公式ln[A]=-kt+ln[A]0,其中[A]0为反应开始时反应物A的浓度。
二、比色法测定反应速率常数比色法是一种利用反应物或产物与某种化学试剂生成有色化合物的方法。
这种方法对于那些反应产物能够呈现颜色的反应来说十分有效。
下面以酸碱反应为例进行说明。
1. 准备工作:将酸溶液和碱溶液分别注入两个比色皿中。
2. 反应前后比色:在反应开始后,定时抽取一定体积的混合溶液,与一种酸碱指示剂混合,并根据颜色的变化来判断反应的进程。
3. 比色定量:将反应过程中颜色的变化与已知浓度的标准溶液进行比较,通过比色定量来确定反应速率常数k的值。
三、热学法测定反应速率常数热学法是通过测定反应过程中释放或吸收的热量来确定反应速率常数的方法。
1. 准备工作:将反应物A和B溶液分别注入两个容量相同的容器中。
2. 测定温度变化:通过比较两个容器内温度的变化,可以判断出反应是否发生以及反应速率的大小。
生化分析仪常用分析方法共有三大类,分别为终点法固定时间法和动力学法

生化分析仪常用分析方法共有三大类,分别为终点法固定时间法和动力学法终点法:指通过一段时刻的反应,反应达到平稳,由于反应的平稳常数专门大,可认为全部底物(被测物)转变成产物,反应液的吸光度不再变化,只与被测物的浓度有关。
这类方法通常称为〝终点〞法,更确切地说应称〝平稳〞法。
单试剂单波长终点法:t1时刻加入试剂〔体积为V〕,t2刻加入样本〔体积为S〕,然后搅拌并反应,之后开始测量反应液的吸光度,在t3时刻反应达到终点,t3-t2为测定时刻。
反应度R=At3-At2-1×V/(V+S),或R=At3-ARBLK。
其中:Ati为i时刻的吸光度,ARBLK为试剂空白吸光度。
单试剂双波长终点法:差不多上同〝单试剂单波长终点法〞,只是关于每一个测定周期,事实上际吸光度等于Aλ1-Aλ2。
双试剂单波长终点法:t1时刻加入第一试剂(体积为V1),t2时刻加入样本(体积为S)之后赶忙搅拌,t3时刻加入第二试剂(体积为V2) 并赶忙搅拌,t4时刻反应达到终点。
t3-t2为孵育时刻,t4-t3为测定时刻。
在项目参数中,假如反应起始时刻设为0,那么反应度R=A时刻吸光度-双试剂空白吸光度。
假如反应起始时刻小于0,那么反应度R=At4 -双试剂空白吸光度-t3到t2间设定点的吸光度×〔V1+S〕/(V1+S+V2)。
双试剂双波长终点法:差不多上同〝双试剂单波长终点法〞,只是关于每一个测定周期,事实上际吸光度等于Aλ1-Aλ2。
固定时刻法:又称为一级动力学法、二点动力学法等,指在一定的反应时刻内,反应速度与底物浓度的一次方成正比,即v=k[S]。
由于底物在不断的消耗,因此整个反应速度在不断的减小,表现为吸光度的变化越来越小。
这类反应达到平稳的时刻专门长,理论上能够在任意时刻段进行监测,但由于血清成份复杂,反应刚启动时反应较复杂,杂反应较多,必需通过一段延迟时刻才能进入稳固反应期。
t1时刻加入试剂(体积为V),之后测量试剂空白的吸光度,t2时刻加入样本(体积为S),t3时刻反应稳固,t4时刻停止对反应进行监测;t2-t3为延迟时刻,t3-t4为测定时刻。
化学反应动力学的实验及其应用

化学反应动力学的实验及其应用化学反应动力学研究的是化学反应速率与反应机理等问题,是化学研究的一个重要分支。
本文将介绍化学反应动力学的实验方法及其应用。
一、实验方法1. 比色法比色法主要用于测定反应液的浓度变化,从而推算出反应速率。
比如,通过测量碘化物在二甲醚中的吸收光谱来判断反应过程中浓度的变化,从而得出反应速率。
2. 定量反应法定量反应法即测量反应物与生成物的摩尔浓度变化,进而计算反应速率。
其中比较常用的方法是“消耗物法”,即将一种反应物完全消耗后停止反应,并测量消耗掉的反应物和产物的浓度变化,以此计算反应速率。
3. 漏斗法漏斗法是一种间接测量反应速率的方法。
可以将一定量的反应物注入漏斗中,随着时间的推移,反应物变成产物,在漏斗底部集中的产物可以根据颜色、质量等特征测量其产生速率。
二、应用1. 工业应用反应动力学研究对于工业生产中的催化剂设计、反应器性能改进、生产过程优化等方面有着重要的意义。
例如,通过研究反应机理,可以设计出具有高效率、稳定性的催化剂,提高催化反应的产率和选择性。
2. 生物应用反应动力学研究对生物领域有着非常重要的应用。
例如,通过测量酶催化反应的速率来研究生物体的代谢过程,探究生命体系的运行机理。
3. 医学应用医学界也可以通过化学反应动力学研究来探索一些疾病的病理机制,例如利用化学反应动力学分析血液中各种物质的变化,进一步了解生理、病理等信息,为现代医学的发展提供了理论依据。
总之,化学反应动力学研究的实验方法和应用非常广泛,涵盖了许多不同领域。
通过对反应动力学的研究,我们能够更好地理解和掌握化学反应的规律,推动人类社会的发展。
化学反应动力学中的速率常数测定方法探究

化学反应动力学中的速率常数测定方法探究引言:化学反应的速率常数是描述反应速率快慢的重要参数,掌握速率常数测定方法对于研究和应用化学反应动力学具有重要意义。
本文将介绍几种常用的速率常数测定方法,并对其原理和应用进行探究。
一、测定方法一:初始速率法初始速率法是最常用的一种测定速率常数的方法,其基本原理是根据反应物质的浓度变化来计算反应速率。
具体步骤如下:1. 将一定量的反应物质加入反应容器中;2. 瞬时观察反应物质的浓度变化,确定初始速率值;3. 改变反应物质浓度,重新测定初始速率值。
初始速率法适用于反应物质浓度较低的情况,可以有效地测定反应的速率常数。
二、测定方法二:比色法比色法是基于反应中物质颜色的变化来测定速率常数的方法。
该方法适用于具有明显颜色变化的反应。
具体操作如下:1. 将反应物质与适当的试剂混合,引发反应;2. 在一定时间间隔内,取样并测量样品的吸光度;3. 根据吸光度与时间之间的关系,计算出反应速率常数。
比色法的优点是操作简单,适用于大多数颜色变化明显的反应体系。
三、测定方法三:电化学法电化学法是利用电化学技术来测定速率常数的方法,适用于电化学反应和电化学动力学研究。
具体步骤如下:1. 将反应物质溶解在适当的电解质中,形成电化学反应体系;2. 通过控制电极电位或电流密度,观察反应的速率变化;3. 根据电位-时间或电流密度-时间关系,计算出反应速率常数。
电化学法具有灵敏度高、精确度好的优点,是研究电化学反应动力学的重要手段之一。
四、测定方法四:示踪剂法示踪剂法是基于反应体系中可追踪的物质来测定速率常数的方法。
具体操作如下:1. 在反应体系中加入一个可追踪的示踪剂物质;2. 通过检测示踪剂物质浓度的变化,计算出反应速率常数。
示踪剂法适用于不同种类的反应,可以方便地测定反应的速率常数。
结论:速率常数的测定方法多种多样,根据不同反应体系和实验要求选择适当的方法进行测定。
初始速率法适用于浓度较低的反应物质;比色法适用于颜色明显变化的反应;电化学法适用于电化学反应的研究;示踪剂法则适用于不同种类的反应。
2点比色法

2点比色法
2点比色法理论上是通过比较样品颜色与已知颜色的标准样品或标准色卡的颜色深浅来确定样品中某种成分的含量。
其基本步骤如下:
1. 准备标准比色卡:标准比色卡是一种预先标定好颜色的样品卡片,通常包含多种颜色,可以用于比较和确定样品的颜色。
2. 样品制备和测量:将样品制备成适当的颜色样品,然后使用比色计(如色差仪)进行测量。
测量时,通常选择两个或更多的点(如两点或四点)来进行颜色比较,这就是所谓的“2点比色”。
3. 数据处理:根据测量的颜色数据,选择合适的色差仪进行数据处理,得出样品的色差值。
然后,根据标准比色卡或色差值,可以确定样品中某种颜色成分的含量。
需要注意的是,2点比色方法虽然简单、快速,但其结果受到许多因素的影响,如光源、观察者的主观判断、比色计的精度等。
因此,在实际操作中,需要严格控制实验条件,确保测量的准确性和可靠性。
测定酶活性浓度的两大类方法
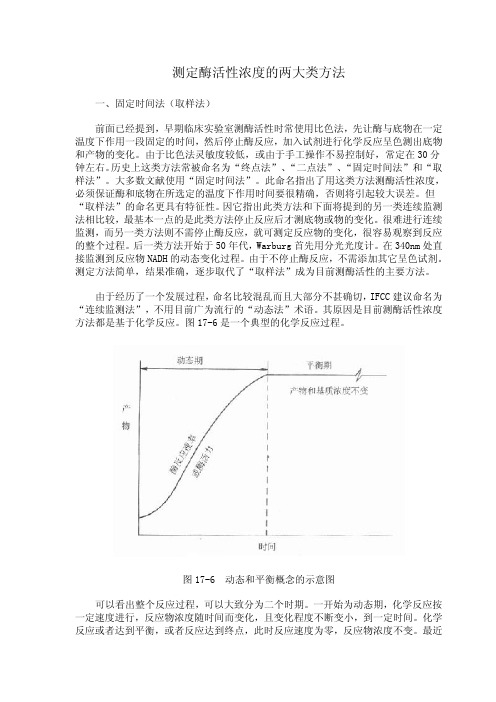
理论上的 V0 在实际工作中是不存在的,必须让酶和底物作用一段时间,消耗掉一 定量的底物,才能测出反应速度,一般说,如消耗底物在 5%内所测到的反应速度都 可认为是初速度,如底物浓度很高时,底物消耗在 20%以内的反应往往还在线性反应 期。
是不是所有类型的酶偶联反应都可用来测酶活性浓度?回答是否定的。因为测酶 的活性浓度是依据测定酶反应速度——△A/△t 或△B/△t 求出。在酶偶联法,此值 无法直接求出,而是通过测定指示酶反应△C/△t 间接求出,要使酶偶联法测得的酶 活性浓度准确可靠,则 Vind=Vx。换言之,指示酶的最大反应速度必须等于或接近测 定酶的最大反应速度。
只有当反应如曲线 A 时,用“固定时间法”才能测出真实的酶活性,实际工作中 是很少见的,图中曲线 B 代表了最常见的反应情况,在一个很短的线性反应期后在大 部分测定期间内主要为非线性反应期。曲线 C 说明在测定期间包括了延滞期,曲线 D 则不仅包括了延滞期,还包括非线性期,在这些反应中如用固定时间法来测定,结果 是不够准确的,一般是偏低的,而且酶浓度愈高,偏离程度愈大。
从理论上说,用酶偶联反应测酶活性浓度时,最好条件应是测定酶反应为限速反 应。动力学上为零级反应,而指示酶为一级反应,酶反应速度与指示酶底物浓度相关。
(二)指示酶、辅助酶的种类和浓度
指示酶、辅助酶的种类:常规化验中常用的酶偶联法中,多以脱氢酶为指示酶, 在常规化验中的自动分析仪几乎无一例外都有 340nm 波长,通过 NAD(P)H 系统可以很 方便地监测到指示酶反应。但从理论上说,往往可以有不止一种偶联方法,只要设法 使偶联反应中最后一个是指示酶反应,前面已提到测 CK 可以正向逆向二个方向建立 二种不同酶偶联的反应。又如在丙氨酸转氨基酶(ALT)测定法中,正向反应后产生 丙酮酸和谷氨酶,目前最常用的是用乳酸脱氢酶与丙酮酸偶联反应,伴有 NADH 下降。 但也可以用谷氨酸脱氢酶与谷氨酸作用,伴有 NADH 生成。
医院招标产品明细及参数要求

附件1:招标产品明细及参数要求:一、便携式彩超仪一台设备用途说明:用于腹部、心脏、妇产科、泌尿科、新生儿、血管、浅表组织与小器官等超声检查。
为方便隔离重症患者诊断,需便携式彩超仪,方便提取携带,避免患者移动,病毒扩散。
1、彩色多普勒超声波诊断仪包括:1.1彩色多普勒超声波诊断仪包括:*1.1.1≥15英寸高清晰度彩色液晶显示器;1.1.2数字化二维灰阶成像单元;1.1.3数字化彩色及能量多普勒单元;1.1.4数字化频谱多普勒显示和分析单元;1.1.5数字化波束形成器;1.1.6多角度空间复合成像技术,可分多级调节并与基础图像同屏双幅显示;1.1.7智能化斑点噪声抑制技术,可分多级调节并与基础图像同屏双幅显示;1.1.8自动优化功能,包括:二维自动优化、频谱自动优化、彩色血流自动优化;1.1.9实时同屏教学软件:系统内置实时操作切面指导工具;1.1.10自适应彩色增强技术,可自动滤除运动伪影;1.1.11编码脉冲反相二次谐波成像,用于所有探头;1.1.12原始数据技术:可对已存储的图像进行增益、动态范围、多普勒基线、多普勒角度、扫描速度等调节以及测量和分析;1.1.13解剖M型:实时及已存储图像M型扫描线可以以任意点为轴心360°旋转;*1.1.14整机重量≤5.5公斤;1.1.15数字化通道≥1024通道;1.1.16可视可调系统动态范围≥120db;*1.1.17超声系统最大探查深度≥33CM;1.1.18实时三同步成像;1.1.19方向性能量图(DCA);*1.1.20凸型扩展技术:支持线阵、相控阵探头,相控阵探头最大扫描角度≥100度;*1.1.21穿刺针增强显影技术:提高穿刺针显影;穿刺针增益可独立调节;1.1.22颈动脉中内膜自动测量技术;1.1.23轨迹球操作;1.1.24内置锂电池操作;1.1.25配备具有三探头接口的原厂台车,可升降调节;1.2测量和分析:(B型、M型、彩色M型、频谱多普勒、彩色模式);1.2.1一般测量;1.2.2妇产科测量;1.2.3多普勒血流测量与分析;1.2.4实时多普勒自动包络、测量和计算;1.2.5心脏功能测量以及各瓣膜功能的测量、分析及报告;1.2.6外周血管测量与分析;1.2.7泌尿科测量与分析;1.3一体化图像存储与(电影)回放重现及病案管理单元;1.4输入/输出信号:1.4.1输入:DVI,HDMI,USB,Lan;1.4.2输出:HDMI,DVI,USB,DVD,Lan;1.5连通性:配备医学数字图像和通信DICOM3.0版接口部件;1.6图像管理与记录装置:1.6.1超声图像存档与病案管理系统;*1.6.2内置固态硬盘≥128GB;2、彩超仪技术参数及要求:2.1探头规格2.1.1频率:宽频带或变频探头;2.1.2类型:支持凸阵,线阵,相控阵,微凸阵;2.1.3阵元:线阵探头及凸阵探头有效阵元数≥192阵元;2.1.4B/D兼用:线阵:B/PWD,凸阵:B/PWD;2.1.5穿刺导向:探头可选配穿刺导向装置;2.2二维灰阶显像主要参数:2.2.1电子凸阵:超声频率2.0-5.0MHz;2.2.2电子线阵:超声频率5.0-10.0MHz;2.2.3电子相控阵:超声频率2.0-4.0MHz;2.2.4系统支持超高频电子线阵:超声频率10.0-22.0MHz;2.2.5扫描速率:凸阵探头全视野,18cm深度时,帧速率≥50帧/秒;2.2.6发射声束聚焦:≥8段;2.2.7回放重现:灰阶图像回放≥1000幅、回放时间≥60秒;2.2.8增益调节:B/M/CF/D可独立调节;2.3频谱多普勒2.3.1方式:PWD,CWD,TVD;2.3.2多普勒发射频率:线阵≥2段;凸阵≥2段;2.3.3最大测量速度:PWD血流速度≥8.0 m/s;CWD:血流速度≥14.0 m/s2.3.4最低测量速度:≤5.0mm/s(非噪声信号);2.3.5显示方式:B、M、B/M、B/M/CFI、B/D、D、B/CFI/D;2.3.6电影回放:≥60秒;2.4彩色多普勒2.4.1显示方式:速度分散显示、能量显示、速度显示;2.4.2彩色帧频:相控阵探头90度角、18cm深、全视野,彩色帧频≥7 帧/秒;2.4.3显示控制:零位移动、黑白与彩色比较、彩色对比;2.4.4彩色增强功能:彩色多普勒能量图(CDE)(包括方向性能量图);2.4.5双幅实时显示、包括双幅不同模式实时显示(B/B;B/CFM);2.5超声功率输出调节:B/M、PWD、Color Doppler输出功率可调;二、高流量氧疗机(呼吸湿化治疗仪)六台参数要求:1.适用范围:儿童,成人;2.病人界面连接管具有透水不透气性能,不产生液态冷凝水;3流量设置范围:3 -50升/分;4.流量调节方式:3-25升/分,每次调节1升/分(儿童模式);10-60升/分,每次调节5升/分(成人模式);5.氧浓度监测/设置范围:21%,25--95%;6.内置涡轮技术:无需空压机,无气源也可独立工作;7.气体温湿度设置:在31℃目标温度时>10mg/L;在34℃目标温度时>10mg/L;在37℃目标温度时>33mg/L;8.管路具有加热和监测功能;9.主机可实时监测参数:气体流速,气体温度,气体氧浓度;10.主机具有一体式超声氧浓度监测系统,无需氧电池耗材;11.主机具有报警功能:呼吸管路连接异常,漏气,堵塞,氧浓度过高或过低,无法达到目标流量,水罐水量,无法达到目标温度,工作条件不合适,断电报警;*12.主机内置消毒功能并有实时消毒状态监测和显示;*13.主机具有气体过滤功能(细菌过滤效率>99.99999%,病毒过滤效率99.99%);14.提供与主机配套使用的原厂耗材,包括管路、湿化水罐、病人界面。
化学反应中反应动力学测量的使用方法

化学反应中反应动力学测量的使用方法引言:反应动力学研究是化学领域中重要的实验手段之一。
它可以帮助我们深入了解化学反应的速率、反应机理以及影响反应速率的因素。
在化学实验中,我们需要准确测量和分析反应的动力学参数,以便更好地理解和控制反应过程。
本文将介绍一些常用的化学反应动力学测量方法及其使用方法。
一、初始速率法(Initial Rate Method)初始速率法是一种简单直接的反应动力学测量方法。
它通过测量反应在初始时刻的速率来确定反应的速率定律。
下面是具体的操作步骤:1. 准备反应物质:确定反应物质的浓度和体积。
2. 操作步骤:将反应物质按照适当比例混合,并在反应容器中搅拌均匀。
3. 反应时间:将反应容器放置在适当的温度下,开始计时。
4. 反应停止:在不同时间点,取出一定量的反应液,迅速将其停止反应(如加入酸或碱以改变反应的pH值)。
5. 产物分析:使用合适的分析方法(如比色法、滴定法等)测量反应液中产生的物质的浓度。
二、方法比较:比色法、滴定法和电化学方法1. 比色法:比色法是一种常用的反应动力学测量方法。
它通过测量反应液中产生的物质的颜色变化来推断反应速率。
具体步骤包括:a) 准备反应物质:确定反应物质的浓度和体积。
匀。
c) 反应时间:将反应容器放置在适当的温度下,开始计时。
d) 反应停止:在反应一定时间后,取出一定量的反应液,立即对其进行颜色测量。
e) 数据处理:根据标准曲线或吸光度和时间关系计算反应速率。
2. 滴定法:滴定法是一种基于滴定的反应动力学测量方法。
它通过滴定试剂与反应物质的反应来推断反应速率。
具体步骤包括:a) 准备反应物质:确定反应物质的浓度和体积。
b) 操作步骤:将反应物质按照适当比例混合,并在反应容器中搅拌均匀。
c) 反应时间:将反应容器放置在适当的温度下,开始计时。
d) 滴定操作:在反应一定时间后,取出一定量的反应液,并加入滴定试剂进行滴定。
e) 反应停止:滴定至终点指示剂颜色发生明显变化时停止滴定。
化学反应中的反应速率及其测定方法

化学反应中的反应速率及其测定方法化学反应是指原子或化合物之间的结构和分子的重组,其中包括分子的拆分和合并,以及电子的共享和转移。
在化学反应中,反应速率是一个十分重要的概念,代表着单位时间内反应物的消耗量或产物的生成量。
本文将介绍化学反应中的反应速率及其测定方法。
一、反应速率的概念反应速率指单位时间内反应物消耗量或产物生成量的变化率,常用单位是mol/L∙s。
在化学反应中,反应速率与反应物浓度的关系十分密切。
众所周知,化学反应中反应物浓度越高,反应速率也就越快;反之,反应速率越慢。
反应速率还受到温度、压力、催化剂等因素的影响。
二、反应速率的测定方法1.容积法容积法是化学实验中常用的一种测定反应速率的方法。
该方法通常需要两个容器,一个容纳反应物,另一个容納產物。
例如,将稀盐酸和铜粉混合,可以观察到氢气的释放。
在做这个实验时,可以把稀盐酸倒进一个试管中,再加入铜粉,然后用橡皮塞堵住试管口。
预先准备好一个气球,将其套在试管口上。
当反应开始时,氢气会逐渐逸出,并逐渐占满气球。
通过观察气球的膨胀情况,我们就可以大约推算出反应速率。
2.比色法比色法可以用于测定反应物或产物在反应中的浓度变化。
该方法可以通过比较同一反应物在不同时间的吸光度,来测量反应速率。
例如,观察蛋白质酶酵素在水中的活性变化,就可以通过比色法来进行。
该实验中,可以将酶酵素与受体结合,形成一个颜色明显的化学物质。
当酶酵素活性较高时,受体与酶酵素的结合会减弱,反之则会加强。
通过测量这个化学物质的吸光度变化,我们就可以推算出酶酵素的活性变化及反应速率。
3.电势法电势法是一种基于电流变化来测定反应速率的方法。
例如,考虑在电解池中的化学反应。
在这种情况下,行到反应物的浓度变化会影响电池电势的变化,从而被转化为电流的变化。
总的来说,化学反应中的反应速率是十分重要的,其测量方法也是多种多样的。
在实验室里,通过选择合适的测量方法和工具,我们可以有效地测定反应速率,对化学反应的研究和应用提供有效的数据支持。
基础知识和7180的应用

18秒转动一圈, 秒转动 圈 10分钟转34圈。 圈 R1:加完样品后直接加入。 R2:1.5 1 5分钟左右加入,在 分钟左右加入 在5、6圈之间加入。 圈之间加入 R3:5分钟左右加入,在16、17圈之间加入。 R4:10分钟左右加入,在33、34点间加入
测光点选择
速率法公式
IF : S+R1<90s 第一测光点 第 测光点6+3T1 第二测光点6+3(T1+T2) IF:90s<S+R1<300s 第一测光点18+3T1 第二测光点18+3(T1+T2) Note: T1和T2分别是加入R2 后的延迟时间和检测时间 后的 迟时间和检测时间 下面举例说明
生化仪原理
郎伯一比尔 郎伯 比尔( Lambert-Beer) Lambert Beer) 定律
I0:入射光强度 I:透过光强度 K:摩尔吸收系数: :摩尔吸收系数: 表示物质对某一波长的辐射的吸收 特性。e 愈大,表示物质对某波长辐 射的吸收力愈强,因而分光光度法测 定的灵敏度就愈高。 定的灵敏度就愈高 C:溶液浓度 b:溶液的厚度
②
常用 具酶 例 常用工具酶(例一)
一、MDH偶联NADH
L-天门冬氨酸 + a-酮戊二酸 AST --------- L-谷氨酸 + 草酰乙酸
草酰乙酸
+ NADH + H+
MDH -----------
L-苹果酸 + NAD+
MDH偶联NADH
常用 具酶 例 常用工具酶(例二)
NADH偶联的LDH ALT
常用 具酶 表 常用工具酶(表一)
工具酶 甘油脱氢酶 3-磷酸甘油脱氢酶 L-乳酸脱氢酶 苹果酸脱氢酶 葡萄糖脱氢酶 6-磷酸葡萄糖脱氢酶 葡萄糖氧化酶 胆固醇氧化酶 3-磷酸甘油醛脱氢酶 谷氨酸脱氢酶 尿酸酶 过氧化氢酶(触媒) 过氧化物酶 Cat POD 英文缩写 ADH GLyDH LDH MDH GLuDH G6PD GOD CHOD GAPDH GLDH 用途(被测定的化合物) 甘油 3-磷酸甘油 丙酮酸、乳酸 草酰乙酸、苹果酸 葡萄糖 6-磷酸葡萄 葡萄糖 胆固醇 3-磷酸甘油醛 谷氨酸、氨 尿酸 过氧化氢 过氧化氢
化学反应速率的实验测定方法

化学反应速率的实验测定方法在化学反应中,反应速率是指单位时间内反应物消失或生成物增加的数量。
了解反应速率对于研究化学反应机理以及控制反应过程至关重要。
本文将介绍一些常用的化学反应速率的实验测定方法。
1. 初始速率法初始速率法是最常用的实验测定方法之一。
它利用反应在初始阶段快速进行的特点,通过测定初始时间段内反应物浓度的变化来确定反应速率。
实验中,可以调节反应物浓度、温度等条件,进行多组实验测定,从而求得反应速率和反应物浓度之间的关系,得到反应速率方程式。
2. 比色法比色法是一种基于溶液颜色变化的反应速率测定方法。
通过在反应过程中测量溶液的吸光度或透过率,可以确定反应物浓度随时间的变化,进而计算反应速率。
这种方法适用于含有有色物质的反应体系,如氧化还原反应、络合反应等。
需要注意的是,在进行比色法实验时,应选择适当的波长进行测量,并对实验过程中的各种因素进行正确的考虑和修正。
3. 电化学法电化学法利用反应溶液中的电荷转移过程来测定反应速率。
其中,电解法是一种常用的电化学测定方法。
通过在反应过程中测量电流或电位的变化,可以反映反应速率的变化。
电化学法适用于许多电化学反应,如金属在溶液中的腐蚀反应、电解制氢等。
在实验中,需要选择适当的电极和电解液,并控制好反应条件和测量参数。
4. 浊度法浊度法是一种基于溶液中悬浮固体颗粒的光散射现象来测定反应速率的方法。
在反应过程中,由于产物生成的微小颗粒,溶液的浊度会发生变化。
通过测量溶液的光散射强度或浊度的变化,可以确定反应速率。
这种方法适用于涉及胶体或悬浮颗粒的反应,如沉淀反应、凝胶反应等。
5. 发光法发光法是一种利用反应物或产物的发光特性来测定反应速率的方法。
在某些反应中,反应物或产物具有发光性质,通过测量发光强度随时间的变化,可以确定反应速率。
这种方法适用于分析荧光、化学发光、光化学等反应。
在实验中,需要选择适当的波长进行测量,并排除可能的干扰。
总结:通过初始速率法、比色法、电化学法、浊度法和发光法等实验测定方法,我们能够准确地测定化学反应速率。
比色分析的基本原理

第一节比色分析的基本原理比色分析是基于溶液对光的选择性吸收而建立起来的一种分析方法,又称吸光光度法。
有色物质溶液的颜色与其浓度有关。
溶液的浓度越人,颜色越深。
利用光学比较溶液颜色的深度,可以测定溶液的浓度。
根据吸收光的波长范闱不同以及所使用的仪器精密程度,可分为光电比色法和分光光度法等。
比色分析具有简单、快速、灵敏度高等特点,广泛应用于微量组分的测定。
通常中测定含量在i(r〜lO-'mg/L的痕量组分。
比色分析如同其他仪器分析一样,也具有相对误差较人(一般为1%〜5%)的缺点。
但对于微量组分测定来说,由于绝对误差很小,测定结果也是令人满意的。
在现代仪器分析中,有60%左右采用或部分采用了这种分析方法。
在医学学科中,比色分析也被广泛应用于药物分析、卫生分析、生化分析等方面。
一、物质的颜色和光的关系光是一种电磁波。
自然是由不同波长(400〜700nm)的电磁波按一定比例组成的混合光,通过棱镜可分解成红、橙、黄、绿、青、蓝、紫等各种颜色相连续的可见光谱。
如把两种光以适当比例混合而产生白光感觉时,则这两种光的颜色互为补色。
例如绿与紫、黄与蓝互为补色。
当白光通过溶液时,如果溶液对各种波长的光都不吸收,溶液就没有颜色。
如果溶液吸收了其中一部分波长的光,则溶液就呈现透过溶液后剩余部分光的颜色。
例如,我们看到KMnO4溶液在白光卞呈紫红色, 就是因为白光透过溶液时,绿色光大部分被吸收,而其他各色都能透过。
在透过的光中除紫红色外都能两两互补成白色,所以KMnOl溶液呈现紫红色。
同理,CuS04溶液能吸收黄色光,所以溶液呈蓝色。
由此可见,有色溶液的颜色是被吸收光颜色的补色。
吸收越多,则补色的颜色越深。
比较溶液颜色的深度,实质上就是比较溶液对它所吸收光的吸收程度。
表1-1列出了溶液的颜色与吸收光颜色的关系。
表1-1溶液的颜色与吸收光颜色的关系溶液颜色绿黄橙红紫红紫蓝青蓝青吸颜色紫蓝青蓝青青绿绿黄橙红收光波长/ nin400〜450450〜480480〜490490〜500500〜560560〜580580〜600600〜650650〜760二、朗伯-比尔(Lambert"Beer)定律当一束平行单色光(只有一种波长的光)照射有色溶液时,光的一部分被吸收,一部分透过溶液(图1-1) °图1-1光吸收示意图设入射光的强度为I。
确定化学反应速率的方法

确定化学反应速率的方法确定化学反应速率是研究化学反应动力学的重要内容之一。
化学反应速率描述了单位时间内反应物消耗或产物生成的数量。
本文将介绍几种常用的确定化学反应速率的方法。
一、初始斜率法初始斜率法是确定化学反应速率最常用的方法之一。
该方法通过观察反应物浓度随时间变化的曲线,计算出初始时刻反应物浓度变化的斜率,即可得到反应速率。
二、比色法比色法适用于反应物或产物可以形成有明显色彩的产物的反应。
该方法通过比较反应开始时和一段时间后反应体系的颜色变化程度,计算出单位时间内颜色变化的程度,即可得到反应速率。
三、浊度法浊度法适用于反应物或产物可以形成浊溶液的反应。
该方法通过测量反应混合液浊度的变化,计算出单位时间内浊度的变化程度,即可得到反应速率。
四、导电度法导电度法适用于反应物或产物的电导率与反应进程相关的反应。
该方法通过测量反应混合液的导电度随时间的变化,计算出单位时间内导电度的变化程度,即可得到反应速率。
五、质谱法质谱法适用于反应物或产物可以通过质谱仪进行定性和定量分析的反应。
该方法利用质谱仪对反应体系中气体或溶液的成分进行分析和检测,计算出反应物浓度随时间的变化,从而得到反应速率。
六、红外光谱法红外光谱法适用于反应物或产物可以通过红外光谱仪进行定性和定量分析的反应。
该方法通过红外光谱分析反应体系中的物质吸收光谱,计算出反应物浓度随时间的变化,从而得到反应速率。
七、瞬态法瞬态法适用于反应过程中存在中间物的反应。
该方法通过瞬态方法,即在反应体系中引入短暂但明显的扰动,观察扰动引起的反应体系的响应,从而推断出反应速率。
以上是常见的几种确定化学反应速率的方法,每种方法都有其适用的反应类型和优缺点。
根据实际情况选择合适的方法可以更准确地确定化学反应速率。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
较二者间显色差异情况并以 Ch 为例分析评
价见图 2。
经试验, Ig、GL U、Cr、Fs 标准液和血清
样本间曲 线差异不明 显。Ch 和 T g 标准液
与实际样本间显色速率有一定区别。图 2 所
示的三条曲线显色峰值时间相似, 但国产异
丙醇作溶剂的标准液显色 A 上升和下降均
快于血清标本。进口标准液和血清显色曲线
50
解放军医学 高等专科学校学报
第 25 卷
物的显色速率换算确定标本浓度的, 故标准 液和样本 显色曲线是否 一致直接影 响准确 性。由于市售标准液和血样间溶剂不同, 反 应中即使总升降幅度不变, 但可能产生启动 时间, 峰值时间上的差别。必然使在同一时 间内量取不同的速率导致误差。如前述 Ch 和 T g 标准和样本 间就存在 速度差。Ch 的 二种标准液也不尽相同。混合标准液比实际 样本显色启动快, 下降亦快。进口标准液则 和标本在 30 s90 s 间有同步变化区比较有利 于编程。总之, 二点动态法的标准液选择应 重于实验, 观察动态显色情况。最理想的应 采用定值血清作参照, 以保证溶剂背景的一 致性。 3 3 甘油三酯速率测定误差分析 T g 动态 法重复性可行, 但和终点法测值比较有显著 性差异。据观察二者配对测定差异呈无规律 性。有些标本二法结果吻合, 有些则相差甚 远, 差者为动态法偏低, 可达 70% 。考虑可 能为标本产生的游离甘油浓度不同而使酶反 应速度变化: 甘油酯 脂肪酶 甘油一步反应量
LPL
减少, 而甘油直接和显色剂反应增快, 导致
显色峰值时间移位使结果偏低。因终点法是 量取总变化量, 不能区别显色速度的细微差 异, 由此 产生了 二法符 合程 度呈不 规律变 化。目前已有双试剂出售, 即先加入甘油反 应试剂, 使甘油反应殆尽后, 再加脂肪酶作 为启动试剂用动态法测定, 从而可排除游离 甘油影响。综上所述, 通过对六种常用终点 法比色项目改二点速率法测定初步研究, 认 为除 T g 有待于进一步研究外, 其余各项均 可以原终点法试剂, 改用二点速率法测定。 这对于充 分利用现代生 化仪器的 自动化能 力, 发挥速率测定方法学的优点, 将不无裨 益。 参考文献
- 甘油酯血清标本 1 58 mmol/ L 延迟时间 10 s 间隔时间 15 s
- 肌酐血清标本
290 mol/ L 延迟时间 10 s 间隔时间 15 s
- 糖血清标本
5 83 mmol/ L 延迟时间 10 s 间隔时间 15 s
- 果糖胺血清标本 6 4 mmol/ L 延迟时间 5 s 间隔时间 30 s
作者单位: 116041 大连市解放军第 215 医院 116041 大连市旅顺中医医院
收稿日期: 1996-03-18
线性区作为编程依据, 并在此基础上做初步 方法学评价。现将结果报告如下: 1 试剂与仪器 1 1 试剂 Ch、T g 采用一步终点酶试剂[ 1] ( 渤嘉公司) 。标准液分为二种, 一种为 Ch、 T g 混合异丙醇溶剂标准, Ch 5 17 mmol/ L 、 T g 1 13 mmol/ L ( 上海医化所) 。另一种为 活性剂蛋白水溶剂标准 Ch 6 5 mmol/ L 、T g
关键词 比色分析 终点法 速率法 中图法分类号 R446
随着检验仪器自动化水平的普及提高及 方法学不断完善, 很多操作繁杂的生化项目 都试剂盒化, 上机编程测定。尤其速率法应 用于酶活力测定, 充分显示出其快速准确的 优越性。但临床常用的一些比色分析项目, 大多仍沿用终点法定量, 这种将被测物和试 剂混合, 作用一定时间后测总变化量的方法 存在一些不可避免的缺点。如: 反应时间较 长, 不利于仪器编程自动测定, 使生化自动 分析仪只起到一台高级比色计的作用; 为使 显色时间一致常须加入终止剂, 因而增加了 操作误差; 由于通常只设一个试剂空白调仪 器零点测定一批标本的总产色( 浊) 量, 故不 宜控制或排除样本间不同色泽干扰及动态干 扰引入的误差。如将某些比色反应改为速率 法定量就能较好地克服上述缺点, 使整个过 程更为迅速、准确。因此, 作者选出胆固醇 ( Ch) 、甘油三 酯( T g ) 、葡 萄糖 ( GLU ) 、肌酐 ( Cr) 、果糖胺( F s) 、免疫球蛋白( Ig ) 等六项比 色( 比浊) 终点法项目, 仍采用终点法原来的 试剂, 改用二点速率方式编程, 观察其从 5 s5 min 内的显色吸光度动态曲线, 选择最佳
海生物制品研究所) 。 1 2 仪器 SP- 501 全息光栅半自动生化 分析仪( 美国 M IL T ON ROY 公司) 。 2 方法与结果
48
解放军医学 高等专科学校学报
第 25 卷
2 1 显色 动态曲线 观察 根据所测 项目, 取各自试剂预温待用。另取临床混合血清一 份按表 1 加样并设置 501 仪动态法程序。
15
13 37
15
13 37
30
13 37
30
13 37
15
13 37
按项目设定顺序, 分别将血清加入试剂 后立即混匀在 5 s 内上机监测其显色动态曲 线, 结果见图 1。
图 1 可见, FS 和 GL U 显色曲线相似, 在 40 s60 s 达到峰值, 其后有一段平缓显色 区。GLU 在 3 min 内 F S 在 5 min 内 A 呈 弱下 降线性发展。延长监测时间, 则 GLU 迅速下降, 而 F S 无明显终点[ 4] A 继续缓慢 下降。根据 A 只随浓度变化而在一定时间 内与测定呈同步变化区应当是最佳监测阶段 的原则, 上述二项可供选择区较宽, 较适合 于动态测定编程。其余 4 项曲线类似, 显色 峰值均在 25 s40 s 间, 其后 A 下降快, 几 乎无平台区。其中 Ig 下降尤为明显, Ch 峰 值略后移, 肌酐变化稍缓为其各自特点。根 据这类反应的显色动态情况, 注意因可监测 区短, 在改为二点动态测定编程时, 延迟时 间和测定时间设置不当易引起较大误差, 应 当兼顾灵敏度和准确性。一般取峰值类半宽 度区间。同时标本和试剂混合上机时间和温 度要严格把关, 否则易造成监测时间差 ( 全 自动生化仪无此误差) 。根据上图结果和我 们实践选出上机参数见表 2。
0 28 0 36 0 03 0 23 0 12
0 23 3 22 0 94 0 10 0 69
> 0 05 < 0 02 > 0 05 > 0 05 > 0 05
* 以 IgM 为例, 单位是 g/ L。
第1期
二点速率法在比色分析中的应用 陈胜洪, 等
49
图 1 呈色速率动态图
- 胆固醇血清标本 3 1 mmol/ L 延迟时间 10 s 间隔时间 15 s
A/ m in 迅速下降, 故为获得足够的灵敏度 读取时 间取 2 min 内 为好, 但 过短正 处于
A 峰值区, 引起的误差就可能增加。Ch 读 数时间选 1 min 误差率可达 8% , 1 5 min2 min 则< 3% 。所以应根据反应类型、仪器和 试剂状况、遵循有利于抗干扰, 有足够灵敏 度以致准确度的原则适当调配延迟时间和读 数时间的长短。 3 2 标准液和血样本显色一致性影响 二 点速率法是通过记录和标本同样处理的标准
标本每个项目均按二点速率法编程, 连续测
定 10 次20 次, 观察该法批内重复性结果见
表 4。
表3
终点法与速率法比较
测定均值 mmol/ L
项目 例数
S
t
P
终点法 动态法
Ch 10
Tg 9
Ig*
8
Fs 10
GLU 10
3 91 2 14 1 66 5 36 6 49
3 88 1 75 1 63 5 37 6 53
第 25 卷第 1 期
解放军医学高等专科学校学报
1997 年 3 月
技术与方法
二点速率法在比色分析中的应用
陈胜洪 王雅范 刘静华
摘要 通过对胆固醇、甘油三酯、葡 萄糖、肌酐、果糖 胺、免疫球 蛋白等 常用
比色( 比浊) 终点法项目 试改 二点 速率法 测定, 观 察各自 动态 显色曲 线, 选 择出最佳同步 反应区, 并做 初步 方法 学评价, 为 该类 显色反 应向 速率测 定 转化 提供参考数据。
- Ig 类血清标本 正常法合血清值 延迟时间 10 s 间隔时间 30 s
图 2 Ch 标准与样本显色曲线比较
- 胆固醇进口标准液( 带活性济水溶济) 6 5 mmo l/ L - 胆固醇国产标准液( 异丙醇溶剂) 5 2 mmo l/ L - 血清标本
表4
速率法批内重复性
项目 GLU
Cr Fs Tg Ch Ig
较相近, 至少 40 s80 s 间有同步斜率变化区。
T g 情况类似 于 Ch。因此, 要注意选择和实
际样本显色曲线相近的标准作为参照, 以免
引入因显色动态过程不同导致的分析误差。
2 3 准确性和重复性观察 取临床实际样
本数份分别用终点法和二点速率法测定, 比
较二组间差异结果见表 3。另对一混合血清
例数 10 10 20 10 10 10
x ( mmol/ L) 19 83
190 30 3 39 3 27 7 60 1 63
S 0 32 3 98 0 04 0 11 0 19 0 06
CV % 16 21 12 33 25 39
表 3 结果表明, 5 个项目( Cr 因已有该 法应用故免做) 中除 T g 外 其它和终点法比 较均无显 著性差异其准确性 是可靠的。T g 二点速率法明显低于终点法, 可能与游离甘 油含量的多寡在二种方法中干扰不同所致。 表 4 中 6 个项目的批内重复性波动在 1 2%3 9% 之间, 从方法学上讲符合目前临床和 质量控制的要求。 3 讨论 3 1 关于延迟时间与测定时间选择 动态 测定是以监测显色速率定量的, 延迟时间选 择应根据显色反应快慢, 温度平衡状态及反 应启动时间确定。同时对某些初期有非特异 性显色的反应通过延迟时间的适当延长来排 除。如 Fs 初期 V c 的干扰[ 5] 、肌酐测定中假 性肌酐的干扰等。一般 Fs 和 GL U 反应曲线 较平坦, 监测期较长的项目延迟时间可长至 1 m in3 m in。Ch、T g 等显色( 浊) 迅速的反应 延迟时间在 10 s30 s 为宜。读数时间最理想 应选择在反应中 A 同步变化区。上述五项 显色反应( Fs 除外) 在 2 m in 时已完成过半,
