医疗设备更新流程图
医院设施设备更新与维护管理制度

医院设施设备更新与维护管理制度第一章总则第一条为了保障医院设施设备的正常运行和使用,提高服务质量,保障患者和医护人员的安全,订立本管理制度。
第二条本制度适用于本医院内的全部设施设备的更新和维护管理工作,包含但不限于医疗设备、电力设备、供水设备、空调设备等。
第三条设施设备更新和维护工作应遵从科学规划、合理布局、安全高效、经济节能的原则。
第二章设备更新管理第四条设备更新应依据医院的发展需求、患者的需求以及设备的技术更新情况进行决策,并经过医疗质量管理部门和经济管理部门的审核。
第五条设备更新项目需提前做好项目立项,包含设备摘牌、采购计划、资金预算等,经过医院领导的审批后方可实施。
第六条设备更新采购时应严格遵从采购法律法规,采取公开招标的方式进行,确保公平、公正、公开。
采购合同应明确设备的规格、性能、保修期等要求。
第七条设备更新项目应有专人负责,全程跟踪,并及时与供应商、施工单位等沟通,确保项目定时、按质、按量完成。
设备更新后,需进行设备验收,验收合格后方可投入使用。
验收人员应由医疗质量管理部门、设备科技部门等构成,验收结果应有书面记录。
第九条设备更新后,应加强设备使用培训,确保医护人员熟识操作方法,正常使用设备,并做好设备的保养、维护和修理和管理工作。
第三章设备维护管理第十条设施设备的维护管理工作应由设备维护和修理科负责,依据设备使用、维护、保养手册进行管理。
第十一条设备维护管理包含计划性维护和故障维护和修理两部分。
计划性维护应依照设备维护手册中规定的维护周期和内容进行,故障维护和修理应及时响应、快速处理。
第十二条设备维护人员应具备相应的维护和修理技能和专业知识,定期参加相关培训,保证维护和修理工作的质量和安全。
第十三条设备维护工作应建立台账,对每台设备的维护和修理记录、维护和修理费用、维护和修理人员、维护和修理时间等进行认真记录。
对于维护和修理费用较高或维护和修理时间较长的设备,应另行编制维护和修理报告。
医疗设备的维护保养计划和流程

故障处理流程
发现设备故障: 操作人员发现 设备异常,立 即停止使用并
报告
故障确认:维 修人员对故障 进行确认,判 断故障类型和
严重程度
故障处理:根 据故障类型和 严重程度,采 取相应的处理 措施,如维修、 更换零部件等
故障记录:记 录故障情况、 处理过程和结 果,以便后续 分析和改进
故障分析:对 故障原因进行 分析,找出问 题根源,制定
0 设 维修保养 规范
维修保养内容
01
定期检查设备:检查设备的运行状态,及时发 现问题
02
清洁设备:保持设备的清洁,防止灰尘和污垢 影响设备的性能
03
更换易损件:定期更换易损件,确保设备的正 常运行
04
设备校准:定期对设备进行校准,确保设备的 准确性和可靠性
05
培训操作人员:对操作人员进行培训,提高操 作人员的技能和意识
05
操作结果:填写本次操 作的结果,如成功、失 败等
06
备注:填写其他需要说 明的情况,如设备故障、 操作建议等
06 设 维护保养 管理制度
01
依据法律法规和行业 标准制定
管理制度制定要求
02
结合医院实际情况和 设备特点制定
03
明确设备维护保养的 责任部门和责任人
04
制定详细的维护保养 计划和流程
归档记录:记录设备 维护保养的历史记录
和归档情况
THANK YOU
汇报人:XXX
预防措施
反馈与改进: 将故障处理结 果反馈给相关 部门,持续改 进设备维护保 养计划和流程
故障处理注意事项
01 保持冷静,判断故障原因 02 遵循设备操作手册,避免误操作 03 及时报告故障,寻求专业支持 04 记录故障情况,便于后续分析与改进
黑龙江省卫生健康委员会关于印发《黑龙江省乙类大型医用设备配置许可管理实施细则》的通知

黑龙江省卫生健康委员会关于印发《黑龙江省乙类大型医用设备配置许可管理实施细则》的通知文章属性•【制定机关】黑龙江省卫生健康委员会•【公布日期】2024.01.31•【字号】•【施行日期】2024.01.31•【效力等级】地方规范性文件•【时效性】现行有效•【主题分类】卫生医药、计划生育其他规定正文黑龙江省卫生健康委员会关于印发《黑龙江省乙类大型医用设备配置许可管理实施细则》的通知各市(地)、县(市、区)卫生健康委(局),各有关医疗卫生机构:现将《黑龙江省乙类大型医用设备配置许可管理实施细则》印发给你们,请遵照执行。
黑龙江省卫生健康委员会2024年1月31日目录第一章总则第二章配置许可申请与受理第三章配置许可审查与决定第四章配置许可证管理第五章设备使用与监督管理第六章附则黑龙江省乙类大型医用设备配置许可管理实施细则第一章总则第一条为深入推进简政放权、放管结合、优化服务改革,进一步规范我省乙类大型医用设备配置许可管理,根据《中华人民共和国行政许可法》《医疗器械监督管理条例》《大型医用设备配置与使用管理办法(试行)》及《甲类大型医用设备配置许可管理实施细则》等相关规定,结合我省实际,制定本细则。
第二条全省乙类大型医用设备配置许可的申请、受理、审查审核、决定及其监督管理,适用本细则。
第三条全省乙类大型医用设备配置许可应当遵循依法合规、公开透明、廉洁高效的原则。
第四条黑龙江省卫生健康委员会依据本省乙类大型医用设备配置规划,组织实施全省乙类大型医用设备配置行政许可事项管理,许可范围按照国家卫生健康委员会《大型医用设备配置许可管理目录(2023年)》执行,并随国家目录适时调整。
第五条引导、支持社会办医疗机构和医疗健康服务新业态、新模式发展,配置适宜的大型医用设备。
第二章配置许可申请与受理第六条申请乙类大型医用设备配置许可,应当具备下列条件:(一)符合我省乙类大型医用设备配置规划;(二)医疗器械使用单位具有执业许可证或医疗器械使用单位设置批准书;或具备符合相关规定要求的从事医疗服务的其他法人资质;(三)与功能定位、临床服务需求相适应,具有与申请的大型医用设备相适应的技术条件、配套设施和具备相应资质、能力的专业技术人员;(四)医疗质量安全保障制度健全。
医疗设备更新及报废制度

医疗设备更新及报废制度第一章总则第一条目的与依据为规范医院内的医疗设备使用和管理,确保医疗设备的安全性和有效性,提高医疗服务质量,依据相关法律法规和行业标准,订立本规章制度。
第二条适用范围本规章制度适用于医院内全部的医疗设备的更新与报废事务,包含但不限于医疗器械、医用仪器、检验设备等。
第三条定义1.医疗设备:指在医疗机构中用于医学诊断、防备、治疗、护理或病人生命维持和其它相关用途的设备。
2.设备更新:指医疗设备因技术、性能等原因需要进行更新替换的行为。
3.设备报废:指医疗设备因技术、性能等原因无法连续使用,需要予以废弃或处理的行为。
第二章设备更新第四条更新周期1.医院管理负责人应依据医疗设备的使用寿命、技术更新的需求以及相关法律法规的要求,订立医疗设备的更新周期。
2.不同类型的医疗设备可能存在不同的更新周期,具体周期应依据设备的具体情况进行调整。
第五条更新流程1.医院管理负责人应委托技术人员或设立特地的设备更新小组负责设备更新工作。
2.设备更新小组应依据医院的需求和预算订立设备更新计划,并报经医院管理负责人批准后执行。
3.设备更新计划应包含设备的具体型号、更新内容、预算、时间等方面的信息,并依据实际情况进行调整。
第六条设备更新评估1.在设备更新计划中,设备更新小组应对待更新的设备进行评估,包含设备的技术情形、故障率、维护和修理费用、使用效果等方面的考量。
2.评估结果应作为设备更新决策的紧要依据,以保证医院设备的质量和安全。
第七条设备更新采购1.设备更新小组应依据设备更新计划,采购具备相应技术和质量要求的医疗设备。
2.设备采购应遵从公开、公平、公正的原则,采购程序应符合相关法律法规和医院内部规定。
3.在选择供应商时,设备采购小组应综合考虑价格、服务质量、维护和修理支持等因素,选择合适的供应商。
第八条设备更新验收1.医院管理负责人应委托技术人员或设立特地的设备验收小组负责设备更新后的验收工作。
2.设备验收小组应对更新后的设备进行全面检查和测试,确保设备符合技术要求、性能稳定。
人民医院医疗设备管理工作流程图

医疗设备管理工作流程图
医用器材管理流程图
网络管理工作流程图
计量管理工作流程图
固定资产及物资购置工作流程图
物资供应管理工作流程图
至账务处理工作流程
物品领取工作流程图
报废工作流程图
固定资产管理工作流程图
工勤维修工作流程图
电梯检修保养工作流程图
供汽锅炉运气操作工作流程图
供氧工作流程图
供暖锅炉运行操作工作流程图
发电工作流程图
中央空调运行工作流程图
洗衣房工作流程图
电梯驾驶员操作工作流程图
安全检查工作流程图
应急突发事件管理工作流程图
安全保卫工作流程图
卫生管理工作流程图
门诊咨询工作流程图
门诊挂号工作流程图
住院病人住院流程图
住院病人出院流程图
门诊部医师工作流程图
门诊部护士工作流程图
门诊手术工作流程图。
医疗器械项目开发设计流程图详图

医疗器械项目开发设计流程图详图精品文档-可编辑
阶段划分
策划阶段
市场调研及项目论证
产品性能指标
采用的标准
类似产品的设计
安全性分析
流程图
XXX
项目建议书审批
XXX
设计输入
相关质量记录
市场调研报告
同类产品对比情况表项目可行性研究报告立项报告
设计开发输入清单设计开发任务书
设计开发计划书
作业文件
记录操作规程
工艺流程
产品质量标准
使用说明书
安全防护规定
输入阶段
设计开发任务书
具体实施阶段和步骤
可行性研究
XXX
会签/输入评审
XXX
评审记录、报告
初始过程流程图
项目进度跟踪表
设计开发输出清单
输出评审报告
设计开发计划书
输出阶段
设计方案
产品格量尺度说明书
产品图纸
原材料清单设备仪器清单工艺流程图初始包装方案灭菌方案
采购要求
合格证、
装箱单
工艺流程图
产品质量标准产品使用说明书产品设计图
初始包装方案设备、仪器清单原材料清单XXX
方案/输出评审XXX
小试阶段
尝试原始记录
精品文档-可编辑小样研制
加速老化测试包装运输测试性能检测
内毒素测定
重要性能测试
小试评审
XXX
中试阶段
软件:试产方案
岗位操作规程
包装、灭菌工艺
硬件:人员
原辅料
生产、检验设备
灭菌记录尝试室管理制度
尝试室生物平安规章制度
尝试室样品管理制度
配液等实验标准操作规程不合格品管理规程
不合格品销毁管理规定。
医疗器械项目开发设计流程图详图
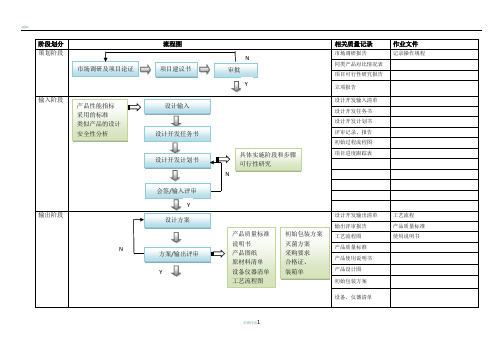
确认记录、报告 评审记录、报告 临床试验方案
wjkz
注册资料 准备阶段
总结评审 Y
技术文件定稿
会签批准 产品注册
备注: 评审报总经理批准,评审小组成员:总经理、研发、销售
临床试验合同 临床试验报告 产品技术报告 风险分析报告 产品说明书 临床试验报告
页脚内容3
小试验证:试生产
设计验证:型式检验 Y
更改、完善 N
设计确认:临床试验
确定临床医院 入组病人选择 实验过程跟踪 页结脚内果容统2 计
原材料清单
实验原始记录 灭菌记录 性能测试报告 评审记录、报告 设计更改申请表 采购合同 供应商评估
安全防护规定 实验室管理制度 实验室生物安全规章制度 实验室样品管理制度 液等实验标准操作规程 不合格品管理规程 不合格品销毁管理规定
设备、仪器清单
工艺流程 产品质量标准 使用说明书
页脚内容1
wjkz
小试阶段
加速老化测试 包装运输测试 内毒素测定 重要性能测试
中试阶段
软件:试产方案 岗位操作规程 包装、灭菌工艺 硬件:人员 原辅料 生产、检验设备
定型阶段 N
小样研制 性能检测
更改、完善
原辅料准备 工艺优化 包装确定
小试评审 N
Y
立项报告
设计开发输入清单 设计开发任务书 设计开发计划书 评审记录、报告 初始过程流程图 项目进度跟踪表
作业文件
记录操作规程
产品质量标准 说明书 产品图纸 原材料清单 设备仪器清单 工艺流程图
初始包装方案 灭菌方案 采购要求 合格证、 装箱单
设计开发输出清单 输出评审报告 工艺流程图 产品质量标准 产品使用说明书 产品设计图 初始包装方案
医疗器械项目开发设计流程图详图
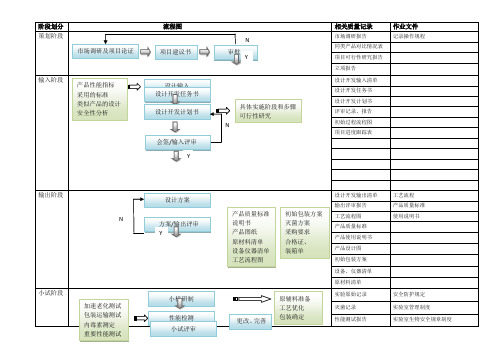
设计开发输出清单 输出评审报告 工艺流程图 产品质量标准 产品使用说明书 产品设计图 初始包装方案 设备、仪器清单 原材料清单 实验原始记录 灭菌记录 性能测试报告
工艺流程 产品质量标准 使用说明书
安全防护规定 实验室管理制度 实验室生物安全规章制度
N Y
中试阶段
软件:试产方案 岗位操作规程 包装、灭菌工艺 硬件:人员 原辅料 生产、检验设备
阶段划分 策划阶段
市场调研及项目论证
流程图 项目建议书
输入阶段
产品性能指标 采用的标准 类似产品的设计 安全性分析
设计输入 设计开发任务书
设计开发计划书
会签/输入评审 Y
N 审批
Y
具体实施阶段和步骤 可行性研究 N
相关质量记录
市场调研报告 同类产品对比情况表 项目可行性研究报告 立项报告 设计开发输入清单 设计开发任务书 设计开发计划书 评审记录、报告 初始过程流程图 项目进度跟踪表
作业文件
记录操作规程
输出阶段 N
小试阶段
加速老化测试 包装运输测试 内毒素测定 重要性能测试
设计方案 方案/输出评审 Y
小样研制 性能检测 小试评审
产品质量标准 说明书 产品图纸 原材料清单 设备仪器清单 工艺流程图
初始包装方案 灭菌方案 采购要求 合格证、 装箱单
更改、完善
原辅料准备 工艺优化 包装确定
确认记录、报告 评审记录、报告 临床试验方案 临床试验合同 临床试验报告
产品技术报告
风险分析报告
产品说明书
临床试验报告
备注: 评审报总经理批准,评审小组成员:总经理、研发、销售
试产方案、报告 自测报告 型式检验报告 验证记录、报告 批生产记录 批检验记录 留样记录 进货验证记录、报告
医院医疗设备的更新及报废报损制度

医院医疗设备的更新及报废报损制度**医院医疗设备的更新及报废报损制度**1. 引言医院作为一个重要的医疗机构,需要时刻保持其医疗设备的先进性与完好性。
本制度旨在规范医院医疗设备的更新、报废和报损过程,以确保医疗设备的有效利用和安全性。
2. 设备更新2.1 设备更新的定义设备更新是指对医院现有设备进行更换或者升级,以提高医疗服务质量和效率。
2.2 设备更新的流程2.2.1 确定更新需求:医院管理部门根据医疗部门的需求和医疗技术的发展趋势,确定设备更新的需求。
2.2.2 制定更新计划:医院管理部门与医疗部门共同制定设备更新计划,包括更新目标、预算、采购方式等。
2.2.3 查找供应商:医院管理部门通过招投标、谈判等方式查找合适的供应商,对设备进行比较评估。
2.2.4 采购设备:医院管理部门与供应商签订设备采购合同,并按照合同约定完成设备采购。
2.2.5 设备验收:医院管理部门按照设备验收标准对采购设备进行验收,确保设备满足医疗要求。
2.2.6 设备更新记录:医院管理部门对设备更新的过程进行记录,包括更新日期、设备型号、采购金额等。
3. 设备报废报损3.1 设备报废报损的定义设备报废报损是指医院对再也不使用或者无法修复的设备进行报废或者报损处理。
3.2 设备报废报损的流程3.2.1 设备评估:医院管理部门委派相关人员对待报废报损设备进行评估,确定设备是否可以修复或者继续使用。
3.2.2 制定报废报损方案:根据设备的实际情况,医院管理部门制定报废报损方案,包括报废报损时间、处理方式等。
3.2.3 设备报废报损记录:医院管理部门对设备报废报损的过程进行记录,包括设备名称、报废报损原因、报废报损日期等。
3.2.4 设备处理:根据报废报损方案,医院管理部门组织人员对设备进行处理,包括销毁、出售、捐赠等。
3.2.5 设备更新规划:根据报废报损的设备情况,医院管理部门及时进行设备更新规划,确保医疗服务的连续性。
4. 附件本所涉及的附件如下:- 设备更新流程图- 设备更新计划模板- 设备采购合同范本- 设备验收标准- 设备报废报损评估表5. 法律名词及注释本所涉及的法律名词及其注释如下:- 设备更新:根据法律法规和医疗技术的发展趋势对医院现有设备进行更换或者升级的行为。
医用诊疗设备保养工作流程

医用诊疗设备保养工作流程在医疗机构中,医用诊疗设备是医生诊断和治疗疾病的重要工具,准确、可靠的设备运行对患者的健康至关重要。
为了确保医用设备的正常运行和延长使用寿命,科学合理的保养工作流程必不可少。
本文将介绍医用诊疗设备的保养工作流程,并详细阐述各个环节的操作方法和注意事项。
一、设备保养前的准备工作保养工作的开展需要有一定的准备工作,下面是准备工作的内容:1. 确定保养计划:根据设备的使用情况和制造商的建议,制定设备保养的时间安排和频率。
2. 培训保养人员:医疗机构应组织相关人员进行设备保养的培训,确保保养人员具备相关的知识和技能。
3. 准备设备保养手册:整理和编制设备的使用说明书、维修手册等相关文档,供保养人员参考。
4. 确认保养工具和材料:根据设备保养手册的要求,准备好所需的保养工具和材料。
二、设备保养工作流程设备保养工作流程主要包括以下几个环节:设备清洁、设备检查、设备维护和设备记录。
下面将详细介绍每个环节的操作方法和注意事项。
1. 设备清洁设备清洁是设备保养工作中的重要环节,它直接关系到设备的卫生和使用寿命。
(1) 清洁前的准备:工作人员应先检查并关闭设备的电源,拆除易脱落的零部件。
(2) 清洁方法:根据设备保养手册的要求,选择合适的清洁方式。
一般情况下,可以使用软布擦拭表面,使用清洁剂清洗污渍。
(3) 清洁注意事项:避免使用含酸性或碱性成分的清洁剂,以免损坏设备表面。
清洁后,应彻底擦干设备,避免残留水分导致设备损坏。
2. 设备检查设备检查是保养工作的关键环节,通过对设备的检查,可以及时发现问题并解决。
(1) 外部检查:检查设备外部是否有明显的损坏或变形,如有则需记录并及时修复。
(2) 内部检查:根据设备保养手册的要求,检查设备内部的关键部件是否正常运转,如有异常,应记录并报修。
(3) 测试运行:按照设备保养手册的要求,进行设备的测试运行,确保设备各项功能正常。
3. 设备维护设备维护是保养工作的核心环节,通过对设备进行维护,可以延长设备的使用寿命。
医疗器械公司流程图

医疗器械公司流程图医疗器械公司流程图是公司运营的重要部分,它涵盖了公司的各个运营环节,从产品研发到生产、销售及售后服务。
一个标准的医疗器械公司流程图包括研发流程、生产流程、销售流程和售后服务流程等。
一、研发流程1、需求分析:了解市场需求,明确产品目标用户和需求。
2、概念开发:基于需求分析,进行产品概念设计。
3、详细设计:进行产品详细设计,包括功能设计、结构设计、材料选择等。
4、原型制造与测试:制造产品原型,进行各项性能测试,确保产品满足设计要求。
5、改进与优化:根据测试结果进行产品改进和优化。
6、准备生产:完成产品定型,准备进入批量生产。
二、生产流程1、采购:根据产品需求,采购所需原材料和零部件。
2、生产计划:制定生产计划,安排生产顺序。
3、生产制造:按照产品设计和工艺要求,进行产品制造。
4、质量检测:对成品进行质量检测,确保产品符合相关标准和设计要求。
5、包装与运输:对合格产品进行包装,安排运输,确保产品按时交付。
三、销售流程1、市场调研:了解市场需求,分析竞争对手,明确自身优势。
2、产品定价:根据产品成本、市场需求和竞争状况,制定合理的产品价格。
3、销售策略:制定销售策略,包括促销活动、渠道选择等。
4、客户沟通:与客户进行沟通,了解客户需求,提供解决方案。
5、订单处理:处理客户订单,包括订单确认、发货等。
6、售后服务:提供售后服务,解决客户问题,提高客户满意度。
四、售后服务流程1、问题接收:接收客户反馈的问题和需求。
2、问题处理:对问题进行分类处理,安排相应部门解决。
3、问题反馈:及时向客户反馈处理结果,确保客户满意度。
4、产品维修:对出现故障的产品进行维修或更换。
5、定期回访:定期对客户进行回访,了解产品使用情况,收集反馈意见。
6、产品升级:根据市场需求和客户反馈,对产品进行升级改进。
医疗器械公司流程图的制定需要考虑多方面因素,包括市场需求、产品质量、生产成本、客户需求等。
通过对流程图的梳理和优化,可以提高公司的运营效率和市场竞争力。
新版医疗设备GSP流程图

新版医疗设备GSP流程图
概述:
该文档旨在提供关于新版医疗设备GSP(Good Supply Practice)流程的详细信息。
GSP是一种确保医疗设备供应链的良好管理实践,旨在保证设备的安全性和合规性。
流程图说明:
以下是新版医疗设备GSP的流程图:
1.开始
2.确定设备供应链的所有参与方,包括制造商、分销商和终端
用户。
3.对参与方进行背景调查,包括查看其资质和合规性。
4.确定所需的医疗设备规范和标准。
5.制定供应链管理方案,包括质量控制、库存管理和记录保留。
6.对供应链参与方进行培训,以确保他们了解并遵守GSP要求。
7.建立合同和协议,确保所有参与方遵守规定。
8.设定设备交付和接收的标准操作流程。
9.确定GSP合规性的审计和监督程序。
10.周期性地进行供应链的内部审核。
11.对供应链中的不合规行为进行整改和改进。
12.定期评估设备供应链的绩效和效果。
13.结束
该流程图展示了新版医疗设备GSP的关键步骤和环节。
通过
严格遵循该流程,可以确保医疗设备供应链的安全性和质量合规性,从而提高医疗服务的可靠性和可用性。
请注意,本文档的内容可能随时进行更新和修改,以适应不断
变化的法规和行业要求。
最新版本的文档应始终被视为权威和具有
参考价值的信息源。
感谢您的阅读,如有任何疑问,请随时与我们联系。
医疗设备、耗材申购、审批、采购流程图
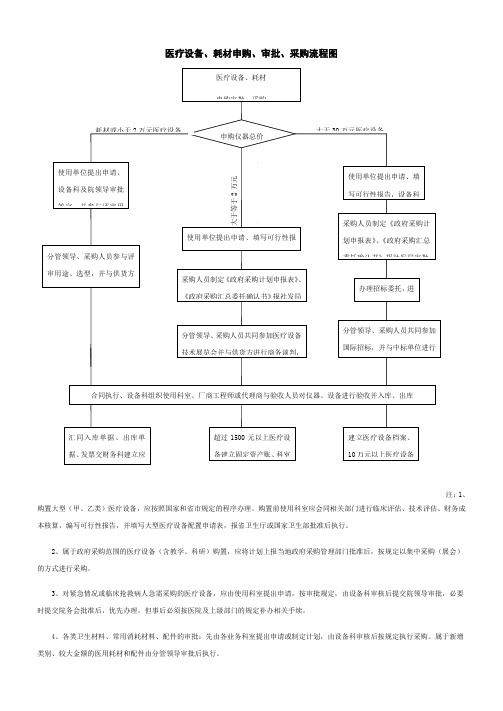
医疗设备、耗材申购、审批、采购流程图注:1、购置大型(甲、乙类)医疗设备,应按照国家和省市规定的程序办理。
购置前使用科室应会同相关部门进行临床评估、技术评估、财务成本核算,编写可行性报告,并填写大型医疗设备配置申请表,报省卫生厅或国家卫生部批准后执行。
2、属于政府采购范围的医疗设备(含教学、科研)购置,应将计划上报当地政府采购管理部门批准后,按规定以集中采购(展会)的方式进行采购。
3、对紧急情况或临床抢救病人急需采购的医疗设备,应由使用科室提出申请,按审批规定,由设备科审核后提交院领导审批,必要时提交院务会批准后,优先办理,但事后必须按医院及上级部门的规定补办相关手续。
4、各类卫生材料、常用消耗材料、配件的审批:先由各业务科室提出申请或制定计划,由设备科审核后按规定执行采购。
属于新增类别、较大金额的医用耗材和配件由分管领导审批后执行。
申购仪器总价耗材或小于2万元医疗设备大于30万元医疗设备大于等于2万元小于30万元医疗设备使用单位提出申请、设备科及院领导审批签字,并参与评审用分管领导、采购人员参与评审用途、选型,并与供货方使用单位提出申请、填写可行性报采购人员制定《政府采购计划申报表》、《政府采购汇总委托确认书》报社发局分管领导、采购人员共同参加医疗设备技术展览会并与供货方进行商务谈判,合同执行、设备科组织使用科室、厂商工程师或代理商与验收人员对仪器、设备进行验收并入库、出库使用单位提出申请、填写可行性报告,设备科采购人员制定《政府采购计划申报表》、《政府采购汇总委托确认书》报社发局审批办理招标委托,进分管领导、采购人员共同参加国际招标,并与中标单位进行建立医疗设备档案、10万元以上医疗设备汇同入库单据、出库单据、发票交财务科建立应超过1500元以上医疗设备建立固定资产账、科室医疗设备、耗材 申购审批、采购5、以上采购金额限度仅供参考。
医疗器械使用管理制度及流程图

医疗器械使用管理制度及流程图英文回答:Medical Device Use Management Policy and Process Flow.I. Purpose.The purpose of this policy is to establish a comprehensive system for the safe and effective use of medical devices within the organization. By implementing this policy, the organization aims to minimize risks associated with medical device use, ensure patient safety, and comply with applicable regulations.II. Scope.This policy applies to all medical devices used within the organization, including but not limited to:Implantable devices.Surgical instruments.Diagnostic equipment.Therapeutic devices.Monitoring devices.III. Responsibilities.Management:Establish and communicate the policy.Provide resources for implementation and adherence. Monitor compliance and make necessary improvements. Healthcare Professionals:Follow the policy and procedures for safe medicaldevice use.Report any incidents or adverse events related to medical device use.Medical Device Technicians:Maintain and calibrate medical devices.Provide training on device use.Troubleshoot and resolve device issues.Purchasing Department:Procure medical devices from approved suppliers.Verify compliance with safety standards.Quality Assurance Department:Conduct audits and inspections to ensurecompliance with the policy.Review and approve new medical devices before use.IV. Procedures.A. Device Selection and Acquisition.Medical devices must be selected and acquired based on an assessment of clinical need, safety, and effectiveness.Devices must be procured from reputable suppliers who meet industry standards.Documentation should be maintained for all medical devices acquired.B. Device Maintenance and Calibration.Medical devices must be maintained and calibrated according to manufacturer's specifications.A schedule for maintenance and calibration should be established and followed.Maintenance and calibration records should be kept for each device.C. Device Training and Competency.Healthcare professionals must receive training on the safe use and handling of all medical devices they use.Training must be documented and updated as needed.Healthcare professionals must demonstrate competency in using medical devices before using them on patients.D. Device Use.Medical devices must be used in accordance with the manufacturer's instructions for use.Devices must be used by trained and competenthealthcare professionals.Any incidents or adverse events related to medical device use must be reported immediately.E. Device Disposal.Medical devices must be disposed of in accordance with applicable regulations and industry standards.Disposal methods must minimize environmental impact and prevent unauthorized use.Records of device disposal should be maintained.V. Documentation.All aspects of medical device use must be documented, including:Device selection and acquisition.Device maintenance and calibration.Device training and competency.Device use.Device disposal.VI. Monitoring and Evaluation.The effectiveness of this policy will be monitored and evaluated regularly.Audits and inspections will be conducted to ensure compliance.Feedback from healthcare professionals, patients, and other stakeholders will be used to make improvements as needed.VII. Definitions.Medical Device: Any instrument, apparatus, implement, machine, reagent, or other similar or related article intended for use in the diagnosis of disease or other conditions, or in the cure, mitigation, treatment, or prevention of disease, in man or other animals.中文回答:医疗器械使用管理制度及流程图。
