JB+T+20091-2007制药机械(设备)验证导则
国家标准批准发布公告2009年第9号(总第149号)--关于批准197项国家标准的公告

国家标准批准发布公告2009年第9号(总第149号)--关于批准197项国家标准的公告
文章属性
•【制定机关】国家质量监督检验检疫总局(已撤销),国家标准化管理委员会•【公布日期】2009.08.27
•【文号】国家标准批准发布公告2009年第9号[总第149号]
•【施行日期】2009.08.27
•【效力等级】部门规范性文件
•【时效性】现行有效
•【主题分类】标准化
正文
国家标准批准发布公告
(2009年第9号总第149号)
国家质量监督检验检疫总局、国家标准化管理委员会批准以下197项国家标准,现予以公布(见附件)。
2009年8月27日
备注:1.GB/T 5953-1999已被代替完
2.从即日起,废止GB/T 21783-2008塑料毛细管法和偏光显微镜法测定部分结晶聚合物的熔融行为(熔融温度或熔融范围)。
制药机械设备验证导则DOC

制药机械设备验证导则1. 前言制药机械设备是药品生产过程中不可或缺的部分,设备验证是药品质量保证体系中的重要环节。
本文将从设备验证的基本概念、验证程序、验证报告以及验证结果评估等方面进行阐述,以便于制药企业进行设备验证时遵照本文进行,提高产品质量和生产效率。
2. 设备验证基本概念设备验证是指通过实验验证设备是否符合其预期用途和设计要求的过程,主要包括“设备安装确认、设备运行确认、性能验收确认三个阶段”。
2.1 设备安装确认安装确认是指确认设备在安装后是否与设计和规范相符,并符合生产要求的工程过程。
安装确认应包括以下内容:•设备是否与设计、规范及制造商提供的说明书一致;•设备的安装位置及设备间距是否符合设备要求和生产需求;•设备的供、排水系统是否符合设计规范;•设备是否符合安全、卫生要求。
2.2 设备运行确认设备运行确认是指在正式运行前进行的验证过程,主要包括以下内容:•设备预验收,包括设备外观检查、设备线路检查;•设备调试,包括机械调试、控制系统调试、安全检测等;•设备试运行,包括设备各项指标测试及性能参数测试。
2.3 性能验收确认性能验收确认是指通过过程验证、性能测试和运行记录等方式对设备的性能进行确认。
主要包括以下内容:•设备运行效果验收,包括产量、质量效果验收;•设备重要参数确认,包括设备注药量、控制精度、循环量等;•设备稳定性验收,包括设备长期运行时的稳定性、可靠性验收。
3. 设备验证程序设备验证程序包括预验证、执行验证、验证报告等过程。
3.1 预验证预验证是指在正式进行设备验证之前进行的过程,在此过程中,应对设备进行充分检查,主要包括以下两个步骤:•制定验证计划,明确验证范围、验证方法以及验证人员;•准备验证设备,包括设备运行前的清洁、检查等工作。
3.2 执行验证执行验证是指对预验证计划进行执行,主要包括以下几个步骤:•设备安装确认;•设备运行确认;•性能验收确认。
3.3 验证报告验证报告是验证人员根据设备验证结果编写的文档,其目的在于验证结果、评估验证内容,并作为设备合格性的标准依据。
制药机械(设备)验证导则(DOC)

制药机械(设备)验证导则1. 范围本标准规定了制药机械(设备)按照药品生产质量管理规范(GMP)进行制药机械(设备)验证的术语和定义、验证的原则、目的、范围、程序、验证方案、验证内容与实施及制造方应提供的技术文件资料。
本标准适用于制药机械(设备)按照药品生产质量管理规范(GMP)所涉及产品验证的设计确认(DQ)、安装确认(IQ)、运行确认(0Q)和性能确认(PQ)工作的指导。
2. 规范性引用文件下列文件中的条款,通过在本标准中引用而成为本标准的条款。
凡是注日期的引用文件,其随后所有的修改单(不包括勘误的内容)或修订版均不适用本标准,然而,鼓励根据本标准达成协议的各方研究是否可使用这些文件的最新版本。
凡是不注日期的引用文件,其最新版本适用于本标准。
GB9969.1 工业产品使用说明书总则JB20067-2005 制药机械符合药品生产质量管理规范的通则药品生产质量管理规范(1998 修订)国家药品监督管理局压力容器安全技术监察规程国家质量技术监督管理局3. 术语和定义3.1 制药机械(设备)验证Pharmaceuticals equipment Validation 制药机械(设备)验证是药品生产企业证明设备的任何程序、生产过程、物料、活动或系统确实能导致预期结果的有文件证明的一系列确认的活动。
3.2 用户需求标准(URS )User Requirement Specification用户对产品功能、使用、服务等提出的特殊要求,并在购销合同中经双方确认。
3.3 设计确认(DQ) Design Qualification设计确认(预确认)指使用方对所选制药机械(设备)满足药品生产质量管理规范(GMP)、用户需求标准(URS)及制造商的确认。
3.4 制药机械(设备)新产品设计确认Pharmaceuticals Equipment Design Qualification制药机械(设备)新产品的设计符合产品标准、药品生产质量管理规范(GMP),满足用户需求标准(URS)要求等方面的核实及文件化工作。
国家发展和改革委员会公告2007年第45号--127项机械、石化、稀土、

国家发展和改革委员会公告2007年第45号--127项机械、石化、稀土、制药装备行业标准编号、名称及起始实施日期
【法规类别】行业标准管理
【发文字号】国家发展和改革委员会公告2007年第45号
【发布部门】国家发展和改革委员会(含原国家发展计划委员会、原国家计划委员会) 【发布日期】2007.08.01
【实施日期】2008.01.01
【时效性】现行有效
【效力级别】XE0303
国家发展和改革委员会公告
(2007年第45号)
国家发展改革委批准《牧草种子清选机技术条件》等127项行业标准(标准编号、名称及起始实施日期见附件),其中机械行业标准88项、石化行业标准26项、稀土行业标准12项、制药装备行业标准1项,现予公布。
以上机械行业标准由机械工业出版社出版、石化行业标准由中国石化出版社出版、稀土行业标准由中国标准出版社出版、制药装备行业标准由中国计划出版社出版。
附件:127项机械、石化、稀土、制药装备行业标准编号、名称及起始实施日期
国家发展和改革委员会
二○○七年八月一日
附件:
127项机械、石化、稀土、制药装备行业标准编号、名称及起始实施日期。
制药机械(设备)验证导则标准介绍

制药机械(设备)验证导则标准介绍1. 引言制药机械验证导则是为了确保制药设备在安全有效的状态下运行而制定的一套标准。
此导则旨在提供对制药机械验证的一般要求和准则,以确保药品的生产符合法规和业界的标准。
2. 背景药品的生产过程需要依赖多种设备和机械来完成,如乳化机、负压灭菌器、混合搅拌机等。
这些设备必须满足一定的性能要求和验证标准,以确保其在生产过程中的稳定性、可靠性和有效性。
3. 制药机械验证的目的制药机械验证的主要目的是确保设备在设计、安装和操作过程中达到预期的性能和要求。
通过验证,可以确认设备是否符合相关法规、法律要求以及业界标准。
此外,验证也有助于保障生产过程的质量和药品的安全性。
4. 制药机械验证的内容制药机械验证通常包括以下内容:4.1 设计验证设计验证是指对药品生产设备的设计进行评估和确认的过程。
在设计验证中,应考虑设备的功能、工艺要求、材料选择等因素,并确保设计符合相关标准和规范。
此外,还应对设备进行风险评估,以预防可能发生的意外和事故。
4.2 安装验证安装验证是指在设备安装过程中对设备进行检查、测试和确认的过程。
验证的内容包括设备的地基、布局、管道连接、电气接线等方面的合规性和适用性。
同时,还需要对设备进行校准、校验和调试,确保设备在正常运行状态下。
4.3 运行验证运行验证是指对设备在正常运行状态下的性能和操作进行检验和验证的过程。
验证的目的是确保设备在生产过程中能够达到预期的性能要求,并满足相关法规和标准的要求。
运行验证需要对设备进行各项功能和性能的测试,以确保设备稳定、可靠、高效运行。
4.4 性能验证性能验证是指对设备的关键性能指标进行测量、测试和验证的过程。
验证的内容包括设备的温度控制、湿度控制、压力控制、流量控制等性能参数的测试,以确保设备在生产过程中能够满足要求。
4.5 清洁验证清洁验证是指对设备清洁性能和清洁过程进行评估和确认的过程。
验证的内容包括设备的清洁程序、清洁剂的选择和使用、清洁效果的检测等方面。
制药机械设备验证导则标准介绍doc 13页

制药机械(设备)验证导则标准介绍(doc 13页)JB/T20091-2007《制药机械(设备)验证导则》标准介绍《制药机械(设备)验证导则》是制药装备行业一项急需的指导性标准,急需制定的原因,在于《药品生产质量管理规范》(GMP)规定对制药设备要进行产品和工艺验证(未经过及未通过验证的不能投入使用);二是制药机械设备的验证正在成为药品生产企业(简称使用方)衡量和评价制药机械产品质量、订货以及对制药装备制造企业(简称制造方)产品的市场认可方式。
故急迫需要在行业内规范指导制药设备的验证活动,配合GMP的有效实施。
关于制药设备验证问题GMP在第七章专门进行了规定,GMP认为制药设备在作为药品生产手段的同时,又是不可忽视的污染因素之一,产生这种认识是源于美国食品药品管理局(FDA)就曾发生在60年代污染输液所至触目惊心的药难事件,针对一度频频爆发的败血症案展开的调查,得出的结论出乎意料,并非是企业没做无菌检查或违反药事法规,而是在于无菌检查本身的局限性、设备或系统设计的缺陷以及生产过程的偏差,导致了如:设备上的压力表及温度显示与实际部位的需要并不一致而未达到灭菌要求;设备密封缺陷导致药品再次受污染;操作方法以至设备排放(散尘、散热、废气、废水)等等,由于制药加工设备的设计、制造、使用环节的很多方面都可能存在引发污染和交叉污染的潜在危险,FDA将其原因归结为“过程失控”,故提出对药品生产环节进行管理和对生产设备进行验证的规定,这就是为什么要对制药用设备验证的主要原因,也是区别于一般用途机械而处在受监控的理由。
制药机械及设备的验证虽然是使用方按照GMP而展开的关于制药设备购置及投用前的例行工作,但它已成为用户选择和评价制药机械产品性能和质量的手段,也引发了制造方相互间产品的潜在竞争,设备的验证让企业感觉到了产品生产与市场的接轨和ISO所提出的社会责任标准的直接内涵,这一动态驱使制造方自觉或不自觉地开始关注自己产品的性能和服务水平,为指导和规范企业开展和参与验证活动适时提出了该验证导则的制定。
制药机械(设备)验证导则标准介绍

制药机械(设备)验证导则标准介绍
制药机械(设备)验证是确保药品生产设备符合规定标准的过程。
验证的目的是确保设备能够稳定可靠地生产高质量的药品,并且符合相关的法规和规定。
下面是一些制药机械验证的导则标准介绍:
1. 验证计划:在验证设备之前,首先应该编制一份验证计划。
验证计划包括验证的目标、范围、方法、资源、时间表和责任人。
验证计划应该经过管理部门批准,并且在验证过程中严格执行。
2. 设备确认:验证过程中应该确认设备的设计规格和功能特性是否符合制药生产的要求。
这包括对设备的功能、性能、控制系统、安全系统和清洁程序的确认。
3. 设备安装/调试确认:在设备安装/调试完成后,需要进行确
认验证,确保设备安装符合规定,设备的性能和功能符合规定要求。
4. 操作确认:操作员需要接受培训,保证其能够熟练、安全地操作设备。
操作确认验证是为了确保操作员按照规定的程序和标准要求进行操作。
5. 清洁确认:设备的清洁程序是保证药品生产质量的重要环节。
清洁确认验证需要确保设备清洁程序的有效性,以避免对产品质量和生产流程的影响。
6. 性能确认:设备的性能确认验证需要对设备进行性能测试,包括设备的稳定性、可靠性、精确性、灵敏度和可重复性等方面进行验证。
制药机械(设备)验证导则标准的目的是为了确保设备能够稳定可靠地生产高质量的药品,符合相关的法规和规定。
验证过程需要按照严格的程序和标准进行,以保证验证结果的有效性和可靠性。
这些导则标准对于确保药品生产设备的安全性和可靠性,保障药品生产质量具有重要意义。
制药机械(设备)验证导则(自校word版)

制药机械(设备)验证导则前言本标准按照《药品生产质量管理规范(2010年修订)》的有关要求和GB/T1.1—2009给出的规则起草。
本标准由全国制药装备标准化技术委员会(SAC/TC356)提出并归口。
本标准负责起草单位:上海天祥健台制药机械有限公司、中国制药装备行业协会。
本标准参加起草单位:上海新先锋药业有限公司、上海远东制药机械有限公司、上海理工大学。
本标准主要起草人:陈露真、田耀华、高云维、陈岚、李华强。
1范围本标准规定了制药机械(设备)(以下简称制药设备)验证的术语和定义、验证目的、原则、程序和方案。
本标准适用于指导制药设备的设计确认、安装确认、运行确认和性能确认等验证工作。
2规范性引用文件下列文件对于本文件的应用是必不可少的。
凡是注日期的引用文件,仅注日期的版本适用于本文件。
凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
GB28670-2012制药机械(设备)实施药品生产质量管理规范的通则TSGR0004—2009固定式压力容器安全技术监察规程(国家质量监督检验检疫总局2009年第83号公告)药品生产质量管理规范(2010年修订)(中华人民共和国卫生部2011年1月第79号令)3术语和定义下列术语和定义适用于本文件。
3.1制药设备验证pharmaceutical equipment validation对制药设备进行设计确认、安装确认、运行确认和性能确认,证明制药设备能够达到预期结果的一系列活动。
3.2用户需求标准user requirement specification在满足相关法规、标准的前提下,使用方要求设备达到生产、检验和管理的目标所需要条件的文件。
3.3验证方案validation protocol阐述如何进行验证并确定验证合格标准的书面计划,它包括验证的目标、内容、方法和合格标准。
3.4设计确认design qualification对制药设备的预审查,证明制药设备的设计符合预定用途、《药品生产质量管理规范(2010年修订)》及附录、用户需求标准和制药设备产品标准。
制药机械设备的验证方案(IQ、PQ、OQ与FAT、SAT测试)

制药机械设备的验证方案(IQ、PQ、OQ与FAT、SAT测试)1.验证的概念药品在生产制造的过程中需透过层层严密的确认,来证实药品的安全性及其品质是否确实有效、可靠,而要达到这样的目的,就必须对各种生产有关的事项,做一连串符合科学性的评价,包括各种生产设备、环境、生产工艺、计量仪器、分析方法的验证等,而我们将这些过程统称为确认(Validation)。
验证是建立一个书面的证据,保证用一个特殊的过程来始终如一地生产产品,是保证符合客户预先确定规格的质量特性。
(FDA 1987)那验证和确认这两个概念有什么区别呢?我们可以先看看在ISO9000中对这两个术语的解释:验证(3.8.4)通过提供客观证据对规定要求已得到满足的认定。
确认(3.8.5)通过提供客观证据对特定的预期用途或应用要求已得到满足的认定。
“规定要求"由组织从顾客/过程的“特定的预期用途或应用要求"“规定要求"中转化而来。
在转化的过程中是可能有偏差的,两者不能等同。
因此,确认比验证更注重实际结果的符合性。
制药机械设备的验证是药品生产工艺流程确认的一环,而设计确认、安装确认、运行确认和性能确认分别是设备验证中的一环。
2.验证的实施我们要对设备进行验证,就必须设计出一套审慎周密的验证(Qualification)计划及有效的测试(Test)方法;但首先我们要强调的是,验证与测试并不相同,验证是着重于评价系统是否按预期的功能运行,它的重点在于核对文件是否完整正确,而测试则是指对系统中误差的鉴定,重点在于评估预测值与实际结果的差异。
因此我们可以说验证包含测试。
一套完整的设备验证计划书(即验证方案)通常包含三个部分:安装验证IQ、操作验证OQ及性能验证PQ。
设计确认DQ不放入方案中,因为这一部分是一个设备选型、供应商选择等设备采购的前期工作。
这些工作完成后才能制订该设备的验证方案,当然也可以把设计确认的指标性参数和具体要求写入验证方案中,并对之前的工作进行确认。
医疗器械注册产品标准编写知识

单击此处添加正文,文字是您思想的提炼,为了演示发布的良好效果,请言简意赅地阐述您的观点。您的内容已经简明扼要,字字珠玑,但信息却千丝万缕、错综复杂,需要用更多的文字来表述;但请您尽可能提炼思想的精髓,否则容易造成观者的阅读压力,适得其反。正如我们都希望改变世界,希望给别人带去光明,但更多时候我们只需要播下一颗种子,自然有微风吹拂,雨露滋养。恰如其分地表达观点,往往事半功倍。当您的内容到达这个限度时,或许已经不纯粹作用于演示,极大可能运用于阅读领域;无论是传播观点、知识分享还是汇报工作,内容的详尽固然重要,但请一定注意信息框架的清晰,这样才能使内容层次分明,页面简洁易读。如果您的内容确实非常重要又难以精简,也请使用分段处理,对内容进行简单的梳理和提炼,这样会使逻辑框架相对清晰。
点击此处添加正文,请言简意赅的阐述观点。
标准的编写格式
点击此处添加正文,请言简意赅的阐述观点。
一、概述
2 标准的分类
按标准的层级分(中国): ——国家标准 ——行业标准 ——地方标准 ——企业标准/医疗器械注册产品标准*
1 标准的作用
用来规范产品、过程和服务,以利于贸易和交流。对医疗器械产品而言,要保证医疗器械产品的安全性和有效性。
《标准化法》第六条规定“企业生产的产品没有国家标准和行业标准的,应当制定企业标准。企业的产品标准须报当地政府标准化行政主管部门和有关行政主管部门备案。”
《医疗器械标准化管理办法》第三条规定“医疗器械标准分为国家标准、行业标准和注册产品标准。注册产品标准是指由制造商制定,应能保证产品安全有效,并经设区的市级以上药品监督管理部门依据国家标准和行业标准相关要求复核的产品标准。” 从而,在医疗器械行业,“企业标准”被“医疗器械产品注册标准”所代替。
制药装备行业标准目
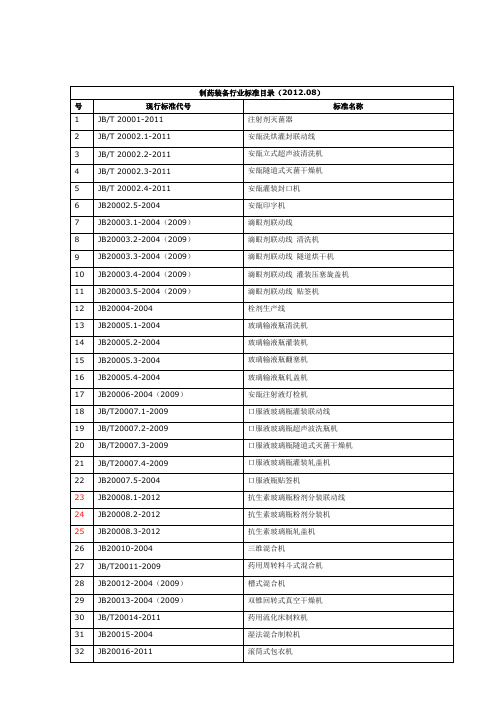
JB/T20056-2005
药用袋成型-充填-封口机
76
JB/T20057-2005
小丸瓶装机
77
JB/T20058-2005
药瓶塞纸机
78
JB/T20059
转鼓贴标签机
80
JB/T20061-2005
整粒机
81
JB/T20062-2005
擦瓶机
165
JB/T 20137-2011
机械搅拌式动物细胞培养反应器
166
JB/T 20138-2011
药用高纯度制氮机
167
JB/T 20139-2011
药用离心分离机械要求
168
JB/T 20140-2011
电加热多效蒸馏水机
169
JB/T 20141-2011
电加热纯蒸汽发生器
170
JB/T 20142-2011
42
JB20026-2004
空心胶囊自动生产线
43
JB/T 20027-2009
滚模式软胶囊压制机
44
JB20028-2004(2009)
胶囊药片印字机
45
JB20029-2004(2009)
热压式蒸馏水机
46
JB20030-2004
多效蒸馏水机
47
JB20031-2004
制药机械纯蒸汽发生器
48
JB20032-2004
94
JB/T20071-2005
立式安瓿机
95
JB/T 20072-2011
离心制粒包衣机
96
JB/T20073-2005
流化床包衣机
97
JB/T20074-2005
国食药监械【2007】597号

国食药监械【2007】597号2007年09月26日发布各省、自治区、直辖市食品药品监督管理局(药品监督管理局):为适应医疗器械监督管理工作的需要,国家局组织有关专家对一次性可注射针刀等61种产品进行了分类界定。
现通知如下:一、一次性可注射针刀(不含药):由气囊、手柄、针刀体三部分组成。
气囊采用一次性输液管材料,可吸取和储存少量利多卡因麻醉液;手柄采用一次性注射器材料;针刀体采用不锈钢材料。
气囊中吸取少量的利多卡因麻醉药液做患处皮内或皮下的麻醉,然后再做针刀治疗。
作为Ⅲ类医疗器械管理。
分类编码6815。
二、同种异体材料(不含活细胞):由从健康遗体捐赠者身体上取得的组织,经过清理、系统加工及灭菌后制成。
用于患者的骨质、关节、肌腱等损伤部位的外科修复。
作为Ⅲ类医疗器械管理。
分类编码6846。
三、异种脱细胞基质敷料:主要成分为去细胞动物(不包括人)的皮肤,用于创面的覆盖、维持创面正常的微环境。
作为Ⅲ类医疗器械管理。
分类编码6864。
四、胶原蛋白海绵:主要成分为胶原蛋白,用于伤口止血、创面的覆盖。
作为Ⅲ类医疗器械管理。
分类编码6864。
五、胃肠动力标记物胶囊:为口服含银环标记物的胶囊,进入胃后在胃液条件下融化,标记物分散于胃内,随蠕动进入胃肠道内。
根据标记物不透X线原理,通过透视或摄片,在一定时间内观察残留在胃肠道内的标记物分布情况并计数,从而对胃肠功能性紊乱等疾病进行诊断或疗效评估。
作为Ⅲ类医疗器械管理。
分类编码6831。
六、测痛仪:由主机、治疗床、针灸针组成。
根据氧自由基致痛原理,测出疼痛阈值后进行治疗。
作为Ⅲ类医疗器械管理。
分类编码6821。
七、脑卒中治疗仪:利用中频电脉冲刺激小脑顶核部位,治疗脑卒中。
作为Ⅲ类医疗器械管理。
分类编码6826。
八、一次性使用鞘组:由筋膜扩张器和可剥开鞘组成,为一次性使用高分子产品,不包含导丝及穿刺器械。
用于经皮肾穿刺进行尿道上端或肾结石取石,或通过该产品进行肾造瘘,在腹膜外穿刺和扩张建立一个到达结石部位的通道,配合输尿管镜进行取石或碎石。
国家食品药品监督管理局办公室关于印发生化分析仪等三个医疗器械产品注册技术审查指导原则的通知

国家食品药品监督管理局办公室关于印发生化分析仪等三个医疗器械产品注册技术审查指导原则的通知文章属性•【制定机关】国家食品药品监督管理局(已撤销)•【公布日期】2009.12.24•【文号】食药监办械函[2009]514号•【施行日期】2009.12.24•【效力等级】部门规范性文件•【时效性】现行有效•【主题分类】药政管理正文国家食品药品监督管理局办公室关于印发生化分析仪等三个医疗器械产品注册技术审查指导原则的通知(食药监办械函[2009]514号)各省、自治区、直辖市食品药品监督管理局(药品监督管理局):为加强对全国医疗器械产品注册工作的监督和指导,全面提高注册工作水平和审查质量,国家局组织制定了生化分析仪、电动手术台、外科纱布敷料(第二类)等三个产品注册技术审查指导原则。
现印发给你们,请参照执行。
国家食品药品监督管理局办公室二○○九年十二月二十四日生化分析仪产品注册技术审查指导原则本指导原则旨在指导和规范生化分析仪产品的技术审评工作,帮助审评人员理解和掌握该类产品原理/机理、结构、性能、预期用途等内容,把握技术审评工作基本要求和尺度,对产品安全性、有效性作出系统评价。
本指导原则所确定的核心内容是在目前的科技认识水平和现有产品技术基础上形成的,因此,审评人员应注意其适宜性,密切关注适用标准及相关技术的最新进展,考虑产品的更新和变化。
本指导原则不作为法规强制执行,不包括行政审批要求。
但是,审评人员需密切关注相关法规的变化,以确认申报产品是否符合法规要求。
一、适用范围本指导原则适用于《医疗器械分类目录》中以紫外-可见光分光光度法对液体样品进行定量分析的生化分析仪,类代号为6840。
本指导原则不包括具有诊断、统计功能软件的生化分析仪。
二、技术审查要点(一)产品名称的要求生化分析仪产品的命名应参考《医疗器械分类目录》或国家标准、行业标准上的通用名称,一般分为半自动生化分析仪和全自动生化分析仪。
命名原则如下:通道数(必要时)+自动化程度+生化分析仪(二)产品的结构和组成半自动生化分析仪的结构一般为固定式或流动式;单色装置分为滤光片式、光栅式、固定发光器件或其他等效方式。
制药机械设备的验证方案(IQ、PQ、OQ与FAT、SAT测试)

制药机械设备的验证方案(IQ、PQ、OQ与FAT、SAT测试)制药机械设备的验证方案(IQ、PQ、OQ与FAT、SAT测试)1. 验证的概念药品在生产制造的过程中需透过层层严密的确认,来证实药品的安全性及其品质是否确实有效、可靠,而要达到这样的目的,就必须对各种生产有关的事项,做一连串符合科学性的评价,包括各种生产设备、环境、生产工艺、计量仪器、分析方法的验证等,而我们将这些过程统称为确认(Validation)。
验证是建立一个书面的证据,保证用一个特殊的过程来始终如一地生产产品,是保证符合客户预先确定规格的质量特性。
(FDA 1987)那验证和确认这两个概念有什么区别呢?我们可以先看看在ISO9000中对这两个术语的解释:验证(3.8.4)通过提供客观证据对规定要求已得到满足的认定。
确认(3.8.5)通过提供客观证据对特定的预期用途或应用要求已得到满足的认定。
“规定要求"由组织从顾客/过程的“特定的预期用途或应用要求"“规定要求"中转化而来。
在转化的过程中是可能有偏差的,两者不能等同。
因此,确认比验证更注重实际结果的符合性。
制药机械设备的验证是药品生产工艺流程确认的一环,而设计确认、安装确认、运行确认和性能确认分别是设备验证中的一环。
2. 验证的实施我们要对设备进行验证,就必须设计出一套审慎周密的验证(Qualification)计划及有效的测试(Test)方法;但首先我们要强调的是,验证与测试并不相同,验证是着重于评价系统是否按预期的功能运行,它的重点在于核对文件是否完整正确,而测试则是指对系统中误差的鉴定,重点在于评估预测值与实际结果的差异。
因此我们可以说验证包含测试。
一套完整的设备验证计划书(即验证方案)通常包含三个部分:安装验证IQ、操作验证OQ及性能验证PQ。
设计确认DQ不放入方案中,因为这一部分是一个设备选型、供应商选择等设备采购的前期工作。
这些工作完成后才能制订该设备的验证方案,当然也可以把设计确认的指标性参数和具体要求写入验证方案中,并对之前的工作进行确认。
制药机械、医疗器械行业标准(GB、JB)

定价 16 16 16 16 18 18 16 16 16 18 16 16 16 16 18 16 16 16 16 16 16 16 16 16 16 18 16 16 16 16 16 16 16 16
JB20004—2004 JB20034—2004
起始实施日期 2017/10/1 2017/10/1 2017/10/1 2017/10/1 2017/10/1 2017/10/1 2017/10/1 2017/10/1 2016/9/1 2016/9/1 2016/9/1 2016/9/1 2016/9/1 2016/9/1 2016/9/1 2016/9/1 2016/9/1 2016/9/1 2016/9/1 2016/9/1 2016/9/1 2016/9/1 2016/9/1 2016/9/1 2017/7/1 2017/7/1 2017/7/1 2017/7/1 2017/7/1 2017/7/1 2017/7/1 2017/7/1 2017/7/1 2017/7/1
标准名称 细菌内毒素测定仪 热原检测仪 可见异物灯检仪 溶出度测定装置 中药大蜜丸蜡壳印字机 ZP系列压片机药片冲模 热泵外加热式双效浓缩器 小型动态提取浓缩机组 注射剂电子检漏机 药用纯蒸汽灭菌器 药用器具清洗干燥机 辊压干法制粒机 胶囊抛光机 玻璃瓶小容量液体制剂灯检机 药品泡罩包装机 热压式蒸馏水机 纯蒸汽发生器 提取浓缩罐 真空浓缩罐 提取罐 真空润药机 中药材热风穿流式烘干箱 可倾式蒸煮锅 中药材颚式破碎机 无菌隔离器 汽化过氧化氢灭菌传递舱 汽化过氧化氢发生器 制药用水 总有机碳分析仪 微生物限度检验仪 隔离装置用手套检漏仪 中药大蜜丸扣壳机 中药大蜜丸蜡封机 栓剂生产线 药用旋涡式振动筛
制药机械行业标准
原料药厂设备首次验证

部门 工程部
QA
部门 工程部 生产部
QA QC
部门 质量副总
原料药生产用设备验证方案
验证方案起草 起草人签名
验证方案审核 审核人签名
版本号 起草日期
审核日期
验证方案批准 批准人签名
批准日期
目录 1 设备概况 2 验证目的 3 验证范围 4.验证小组成员和职责 4.1 验证小组成员 4.2 职责 5.验证内容 5.1 风险分析 5.2 设计确认(DQ) 5.3 安装确认(IQ) 5.4 运行确认(OQ)及性能确认(PQ) 5.5 验证总结 6.偏差分析和处理 6.1 偏差分析和处理要求 6.2 偏差分析和处理内容 7.验证结论 7.1 评价与建议 7.2 再验证周期 8.附件
---培训设备操作人员;
4.2.4 生产部:
---负责配合协助工程部完成验证工作。
---负责验证过程中的生产操作。
4.2.5 QC:
---负责起草验证项目中产品质量标准、检验规程及取样程序;
---负责有关验证项目的检验,并根据检验结果出具检验报告单;
4.2.6 QA:
---负责验证方案和验证报告的审核
合格标准: 中间品、成品的相关法定标准。测试结果见附件 11。 5.5 验证总结 6.偏差分析和处理 6.1 偏差分析和处理要求 6.1.1 如果在验证过程中出现偏差,应做出合理解释或针对相应的偏差项目进行 整改,并进行再验证。 6.1.2 如果在验证过程中出现漏项,应及时对遗漏项目进行补验证。
6.2.偏差分析和处理内容 7 验证结果评定与结论 7.1 工程部负责收集各项验证、试验结果、记录,根据验证、试验结果起草验证 报告,报验证委员会审批。 7.2 验证委员会负责对验证结果进行综合评审,做出验证结论。对验证结果的评 审应包括: ●验证试验是否有遗漏? ●验证实施过程中对验证方案有无修改?修改原因、依据以及是否经过批准? ●验证记录是否完整? ●验证试验结果是否符合标准要求? ●偏差及对偏差的说明是否合理? ●是否需要进一步补充试验? 7.3 再验证周期: 7.3.1 验证小组根据设备的特性及验证的结果,拟定设备的验证周期,报验证小 组组长审批。 7.3.2 对已验证过的设备,若需进行重大结构改装、主要零部件进行检修或更换、 设备用途或工艺条件发生改变时,必须进行再验证。再验证的项目包括运行确认、 性能确认和结果分析及评价。 8.附件
设备验证(IQ、OQ、PQ)

设备验证(IQ、OQ、PQ)设备验证(IQ、OQ、PQ)《药品生产质量管理规范》(98修订版)就对设备的验证提出了专门的要求。
(第三十六条:生产设备应有明显的状态标志,并定期维修、保养和验证。
第五十七条:药品生产验证应包括厂房、设施及设备安装确认、运行确认、性能确认和产品验证。
)☆现阶段设备验证内容:(一)对设备在选型、设计、制造、安装、运行及性能等各个环节进行检查和评估,以证实设备是否符合药品生产的要求,是否满足设备安全有效的功能保证。
(二)设备验证的每一环节均有记录,并有验证的计划、方案、报告、建议和评价。
验证文件归档保存,便于追溯。
(验证概念指出验证应是有文件证明的系统活动)(三)设备验证的主要程序:预确认(DQ)、安装确认(IQ)、运行确认(OQ)、性能确认(PQ)。
1、预确认:预确认即设计确认:审查技术指标适用性及GMP要求,收集供应商资料,优选供应商。
(部分厂家在制定验证方案的时候并未有把设计确认这一部分放入方案中,因为这一部分是一个设备选型、供应商选择等设备购入的前期工作。
这些工作完成后才能制订该设备的验证方案,也可以把预确认的指标性参数和具体要求写入验证方案中,并对之前的工作进行确认。
)1)设计选型:具有符合国家政策法规,满足药品生产、保证药品生产质量的能力,安全、可靠,易于操作、维修和清洗。
(GMP对设备的要求:)2)性能参数设定:符合国家、行业或企业标准,接近并超过国际先进水平或与国内同类型产品相比具有明显的技术优势,而不是重复开发。
(国家计委下发的淘汰设备目录:无净化的热风干燥箱、安瓿拉丝灌封机不允许新上)(制药机械国家标准、制药机械行业标准)3)技术文件制定:具有完整的,符合国家标准的,能指导生产制造的技术文件。
(说明书、标准操作规程)4)采购:依据技术文件采购符合质量要求的,有质量保证书或合格证的原材料及各类物资。
5)制造:依据技术文件、工艺文件和相关标准进行零件制造、装配和调试。
JB-T 20091-2007 制药机械(设备)验证导则

JB-T 20091-2007 制药机械(设备)验证导则制药机械(设备)验证导则(征求意见稿)1.范畴本标准规定了制药机械(设备)按照药品生产质量治理规范(GM P)进行制药机械(设备)验证的术语和定义、验证的原则、目的、范畴、程序、验证方案、验证内容与实施及制造方应提供的技术文件资料。
本标准适用于制药机械(设备)按照药品生产质量治理规范(GMP)所涉及产品验证的设计确认(DQ)、安装确认(IQ)、运行确认(OQ)和性能确认(P Q)工作的指导。
2.规范性引用文件下列文件中的条款,通过在本标准中引用而成为本标准的条款。
凡是注日期的引用文件,其随后所有的修改单(不包括勘误的内容)或修订版均不适用本标准,然而,鼓舞按照本标准达成协议的各方研究是否可使用这些文件的最新版本。
凡是不注日期的引用文件,其最新版本适用于本标准。
GB9969.1工业产品使用讲明书总则JB20067-2005制药机械符合药品生产质量治理规范的通则药品生产质量治理规范(1998修订)国家药品监督治理局压力容器安全技术监察规程国家质量技术监督治理局3.术语和定义3.1制药机械(设备)验证Pharmaceuticals equipment Validation制药机械(设备)验证是药品生产企业证明设备的任何程序、生产过程、物料、活动或系统确实能导致预期结果的有文件证明的一系列确认的活动。
3.2 用户需求标准(URS)User Requirement Specification用户对产品功能、使用、服务等提出的专门要求,并在购销合同中经双方确认。
3.3设计确认(DQ) Design Qualification设计确认(预确认)指使用方对所选制药机械(设备)满足药品生产质量治理规范(GMP)、用户需求标准(URS)及制造商的确认。
3.4制药机械(设备)新产品设计确认Pharmaceuticals equipment D esign Qualification制药机械(设备)新产品的设计符合产品标准、药品生产质量治理规范(GMP),满足用户需求标准(URS)要求等方面的核实及文件化工作。
gbt制药机械(设备)清洗、灭菌验证导则

GBT 制药机械(设备)清洗、灭菌验证导则欢迎各位朋友留言讨论。
以下是全文内容,欢迎访问北京齐力佳网站获取本文和更多制药行业相关资讯及文档。
GB/T 36036-2018全文如下:制药机械(设备)清洗、灭菌验证导则1 范围本标准规定了制药机械( 设备)清洗与灭菌验证的术语和定义、验证目的、验证原则、验证范围、验证程序、验证方案和验证文件。
本标准适用于制药机械( 设备)清洗与灭菌验证。
2 规范性引用文件下列文件对于本文件的应用是必不可少的。
凡是注日期的引用文件,仅注日期的版本适用于本文件。
凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
GB/T 36030-2018 制药机械(设备)在位清洗、灭菌通用技术要求药品生产质量管理规范(2010年修订)(中华人民共和国卫生部)中华人民共和国药典(2015年版)(国家药典委员会) 3术语和定义GB/T36030-2018界定的以及下列术讲和定义适应于本文件。
3.1 验证文件validation document验证总计划、验证计划、验证方案、验证报告和验证总结及验证过程中形成的其他相关文档或资料。
[GB/T 28671-2012,定义3.8] 3.2 验证报告validation report对验证方案及已完成验证试验的结果、漏项及发生的偏差等进行回顾、审核并作出评估的文件。
[GB/T 28671-2012,定义3.9] 3.3挑战性试验challenge test旨在确定某一个工艺过程或一个系统的某一组件(如一个设备或一个设施)在设定的苛刻条件下能否达到预定质量要求的试验。
[GB/T 28671-2012,定义3.10] 4 清洗与灭菌验证4.1验证目的4.1.1 验证制药机械(设备)清洗与灭菌符合《药品生产质量管理规范(2010年修订)》、GB/ T 36030-2018 和用户需求标准,达到规定的清洗与灭菌效果。
4.1.2 验证制药机械(设备)清洗与灭菌系统结构符合药品生产工艺要求。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
制药机械(设备)验证导则1. 范围本标准规定了制药机械(设备)按照药品生产质量管理规范(GMP)进行制药机械(设备)验证的术语和定义、验证的原则、目的、范围、程序、验证方案、验证内容与实施及制造方应提供的技术文件资料。
本标准适用于制药机械(设备)按照药品生产质量管理规范(GMP)所涉及产品验证的设计确认(DQ)、安装确认(IQ)、运行确认(OQ)和性能确认(PQ)工作的指导。
2.规范性引用文件下列文件中的条款,通过在本标准中引用而成为本标准的条款。
凡是注日期的引用文件,其随后所有的修改单(不包括勘误的内容)或修订版均不适用本标准,然而,鼓励根据本标准达成协议的各方研究是否可使用这些文件的最新版本。
凡是不注日期的引用文件,其最新版本适用于本标准。
GB9969.1 工业产品使用说明书总则JB20067-2005 制药机械符合药品生产质量管理规范的通则药品生产质量管理规范(1998修订) 国家药品监督管理局压力容器安全技术监察规程国家质量技术监督管理局3.术语和定义3.1制药机械(设备)验证 Pharmaceuticals equipment Validation制药机械(设备)验证是药品生产企业证明设备的任何程序、生产过程、物料、活动或系统确实能导致预期结果的有文件证明的一系列确认的活动。
3.2 用户需求标准(URS)User Requirement Specification用户对产品功能、使用、服务等提出的特殊要求,并在购销合同中经双方确认。
3.3设计确认(DQ) Design Qualification设计确认(预确认)指使用方对所选制药机械(设备)满足药品生产质量管理规范(GMP)、用户需求标准(URS)及制造商的确认。
3.4制药机械(设备)新产品设计确认Pharmaceuticals Equipment Design Qualification制药机械(设备)新产品的设计符合产品标准、药品生产质量管理规范(GMP),满足用户需求标准(URS)要求等方面的核实及文件化工作。
3.4安装确认(IQ) Installation Qualification设备安装后进行设备的各种系统检查及技术资料的文件化工作。
3.5运行确认(OQ) Operational Qualification设备或系统达到设定要求而进行的各种运行试验及文件化工作。
3.6性能确认(PQ) Performance Qualification证明设备或系统达到设计性能的试生产试验及文件化工作,就生产工艺而言也可指模拟生产试验。
3.7验证方案Validation Protocol验证方案指一个阐述如何进行验证并确定验证合格标准的书面计划。
3.8验证文件Validation Document验证文件系指验证实施过程中形成系统的资料类文件的总称。
4.验证4.1 验证原则4.1.1药品生产企业(简称使用方)是制药机械(设备)验证工作的实施主体,制药机械制造企业(简称制造方)应积极配合使用方的设备验证工作。
4.1.2验证工作由使用方组织并完成。
验证工作的方案应根据制药机械产品标准、用户需求标准(URS)、JB20067、药品生产质量管理规范(GMP)和制药工艺等要求制定,验证方案应经使用方技术负责人审核批准后实施。
4.1.3制药机械(设备)验证应严格按照验证方案规定的内容和步骤进行。
4.1.4 制药机械(设备)验证的各阶段工作完成后,均应形成确认的相关文件。
4.2 验证目的1)确认制药机械(设备)设计与制造工艺符合产品标准,满足用户需求标准(URS)和药品生产管理规范(GMP)要求。
2)确认制药机械(设备)安装符合安装规范,产品相关资料和文件的归档管理符合要求。
3)确认制药机械(设备)在运行情况下的使用功能和控制功能符合规定。
4)确认制药机械(设备)在实际使用条件下的生产适用性和符合制药工艺与质量要求。
4.3验证范围制药机械(设备)验证范围的确定原则应依据制药工艺要求而定。
直接或间接影响药品质量的,与制药工艺过程、质量控制、清洗、消毒或灭菌等方面相关的制药机械设备,属于必须验证的范围,其它辅助作用或不对药品质量产生影响的制药机械设备可不列为验证的范围。
4.4验证程序4.4.1制药机械(设备)的验证程序依次是设计确认、安装确认、运行确认和性能确认。
在各确认阶段均应形成阶段性确认的结论性文件,达不到确认要求的应不进行下阶段的确认工作,整改复验达到要求后方可进行下阶段的确认工作。
4.4.2制造方在制药机械(设备)交付使用方前应完成制药机械新产品的设计确认和文件化工作。
设备到达使用方后,制药机械(设备)的安装确认、运行确认和性能确认由使用方完成。
必要时可由双方协议共同完成。
4.5验证方案4.5.1验证方案须有编制人、审核人、批准人的签署。
当使用方与制造方共同参与设备验证时,其验证方案应经双方认可确立。
4.5.2验证方案的编制参见附录A,验证方案的编写内容应包括:1)验证方案名称、编号;2)产品基本情况(包括设备名称、型号、用途、结构、工作原理、工艺流程、规格、产量、使用介质、主要参数、设备编号、制造单位、供货商等);3)验证人员(人员、资格、分工);4)验证目的;5)验证内容(确认项目、确认方法、试验器具和确认评估时参数的依据及检测数据等);6)验证结论(结果分析、结论,检验、审核及验证负责人员签字等)。
4.6验证内容与实施4.6.1设计确认(DQ)设计确认包括对制药机械(设备)的设计确认或对制药机械新产品的设计确认。
4.6.1.1设计确认(预确认)内容使用方对制造方生产的制药机械(设备)的型号、规格、技术参数、性能指标等方面的适应性进行考察和对制造商进行优选,最后确认与选定订购的制药机械(设备)与制造商,并形成确认文件。
4.6.1.2制药机械新产品设计确认内容(1)对制药机械新产品的设计是否符合药品生产管理规范(GMP)、产品标准、用户需求标准(URS)及相应生产工艺等方面进行审查与确认。
其内容一般包括:a.产品的规格、参数和技术指标;b.产品的生产方式、能力与适用性;c.产品的材质、结构、外观、制造工艺性、噪音、传动机构、辅助系统、润滑系统、安全系统、运行性能等;d.电气和控制功能,含调速、显示、连锁保护、操作系统、安全报警、联机性等;e.对环境和设施与工艺的配套性;f.易清洗、易灭菌、易操作维护、不污染性能等。
(2)制药机械新产品设计确认的实施a. 制药机械新产品设计确认小组由制造方产品项目负责人、工程技术人员、使用方代表和相关专家组成,项目负责人负责组织编制新产品设计确认方案、审核设计文件与图样并提出设计确认的结论, 根据设计确认结论决定是否进入产品制造程序或进行新产品设计确认方案修改、再确认后进入制造程序。
b.制药机械(设备)新产品设计确认可作为新产品鉴定或投产鉴定的依据,也可作为使用方设备选型采购时设计确认的参考。
4.6.2安装确认(IQ)4.6.2.1安装确认内容制药机械(设备)安装确认主要是通过产品安装后,确认设备的安装符合设计及安装规范要求,确认设备的随机文件(产品图纸、备品清单、仪表校准等)以及附件齐全。
检验并用文件的形式证明产品的存在。
确认内容一般包括:(1)检查随机文件与附件齐全:①设备原始文件资料(使用说明书、购买合同、操作手册、合格证、装箱单等);②图纸索引(安装及地基基础图、电气原理图、备件明细、易损件图等);③设备清单(安装位置、设备编号、生产厂家、备品备件存放地及一览表);④相关配套系统(压缩空气、真空气体、水质与供水、蒸汽、制冷等);⑤公用工程检查表(公用工程清单、验收合格证);⑥润滑位置表和仪器仪表安装一览表(仪器清单、安装位置、编号、生产厂家、校验、校准周期)等。
(2)依据设备安装图的设计要求,检查下列几方面:①检查设备的安装位置和空间能否满足生产和方便维修的需要;②检查外接工艺管道是否符合匹配和满足要求;③检查外接电源;④检查主要零件的材质;⑤检查设备的完整性和其它问题。
4.6.2.2安装确认实施制药机械(设备)在安装完毕后,根据验证方案进行安装确认,经实施提出IQ结论。
制药机械制造方应提供给使用方内容详实、完整、有效的设备安装指导文件。
4.6.3运行确认(OQ)4.6.3.1运行确认内容制药机械(设备)运行确认,主要是通过空载或负载运行试验,检查和测试设备运行技术参数及运转性能,通过记录并以文件形式证实制药机械(设备)的能力、使用功能、控制功能、显示功能、连锁功能、保护功能、噪声指标,确认设备符合相应生产工艺和生产能力的要求。
确认内容一般包括:(1)运行前检查,如电源电压、安全接地、仪器仪表、过滤器、控制元件及其它需运行前检查;(2)验证用测试仪器仪表的确认;(3)设备运转确认,依据产品标准和设备使用说明书,在空载情况下,对空负荷运转状态、运转控制、运转密封、噪声等项确认;(4)设备操作控制程序确认;(5)机械及电气安全性能确认;(6)设备各项技术指标确认。
4.6.3.2运行确认的实施制药机械(设备)在安装确认后,根据验证方案进行运行确认,经实施提出OQ结论。
制药机械制造方应提供给使用方具体指导设备正确运行和各功能操作及控制程序的相关文件。
4.6.4性能确认(PQ)4.6.4.1性能确认内容制药机械(设备)性能确认是在制药工艺技术指导下进行工业性负载试生产,也可用模拟试验的方法,确认制药机械(设备)运行的可靠性和对生产的适应性。
在试验过程中通过观察、记录、取样检测,搜集及分析数据验证制药机械(设备)在完成制药工艺过程中达到预期目的。
确认内容一般包括:(1)在负载运行下产品性能的确认;(2)生产能力与工艺指标确认;(3)安全性确认;(4)控制准确性确认;(5)药品质量指标确认(包括药品内在质量、外观质量、包装质量等)。
(6)设备在负载运行下的挑战性试验。
4.6.4.4性能确认的实施性能确认应在IQ、OQ完成后,由使用方按照药品生产的工艺要求进行实际生产运行确认,经实施提出PQ结论。
4.7制造方应提供的文件资料4.7.1产品出厂文件(1)使用说明书。
使用说明书的编写和内容应符合GB9969.1的规定;(2)产品合格证(质量保证书)。
属压力容器和特种设备类产品的按《压力容器监督检验规程》的要求提供设计制造资质证书复印件和监检报告;(3)装箱单;(4)主要配套件与外协件的说明书、质保书和供应产商资料;(5)仪器仪表合格证和供应厂商提供的使用说明资料;(6)电气控制或PLC控制的使用说明书。
4.7.2相关技术资料(1)产品操作规程。
可单独以文本形式列出,也可在使用说明书中有专门章节。
(2)产品清洗规程。
可单独以文本形式列出,也可在使用说明书中有专门章节。
