海正药业:关于重组抗白介素-6受体人源化单克隆抗体注射液获得临床批件的公告
抗癌药物上市公司汇总

抗癌药物上市公司汇总生产抗癌药物的上市公司资料目前全球各国已批准上市的抗癌药物大约有130 ~150种。
各种抗癌药物制剂大约有1300~1500种。
目前在抗癌药物分为西药和中药两大类。
西药中包括化疗和生物靶向治疗药物等,中药包括临床上常用的方剂药物和中成药。
我国恶性肿瘤的发病率不断上升,成为第一位致疾病。
在众多抗肿瘤药中,天然植物类抗肿瘤药所占的比重最大,占据了27.0%的份额,其次为抗代谢类肿瘤药,占26.1%。
在单品排名前10位的抗肿瘤药中,植物类抗肿瘤药占据了前两个席位,为紫杉醇和多西他赛。
预计今后5~10年内,以单克隆抗体、生物工程疫苗和反义寡核苷这3类生物工程抗癌药将居世界抗癌药物市场的统治地位。
《生物产业发展“十二五”规划》确定了我国生物科技与产业发展的八个重点包括:⑴加强生命科学前沿技术研究;⑵加速推进农业生物技术,培育转基因动植物新品种,特别是培育抗旱抗盐碱的植物新品种,大幅度提高农作物的材质、质量品质,开发生物肥料、生物农药、可降解地膜、新型食品与饲料添加剂等新产品。
⑶大力发展生物医药技术,重点支持疾病预防、疾病诊断、新药研制、基因治疗、试管移植等技术,为全面提高人民健康水平提供有力支撑。
⑷大力发展工业生物技术,发展现代发酵、生物催化等新技术,促进传统产业的升级改造,推进绿色制造业发展。
⑸加速发展生物质能,缓解能源短缺的压力。
⑹加速环境生物技术研究与应用,不断改善生态环境。
⑺加强生物资源深度开发,培育一批新的生物产业。
⑻加强生物安全研究,确保国家生物安全。
生物医药“十二五规划”确定了生物医药发展的重点,包括基因药物、蛋白药物、单克隆抗体药物、治疗性疫苗、小分子化学药物等,同时国家将拿出100多亿元来支持重大新药创制。
国家将从100多个新药中遴选出10多个,作为重大新药创制重点支持对象,这些原创新药可能成为打入欧美市场的先锋。
在这些品种中,生物药和化学药居多,其中疫苗、单克隆抗体、蛋白质药物、抗癌药物等均有。
新药研发成功公告新闻稿

新药研发成功公告新闻稿尊敬的各位媒体朋友:我们荣幸地宣布,经过多年的努力和不懈的研发,我们公司成功研发出一种创新的新药,并通过了严格的临床实验验证。
现在我们正式向公众发布这一重大突破的消息。
这次新药的研发根据我们公司的科研团队所提出的方案进行。
我们的科研团队由一批资深的科学家组成,他们精通药理学、生物化学等领域,具备丰富的研发经验。
在整个研发过程中,我们团队紧密合作、互相配合,付出了大量的心血和努力。
我们的新药主要应用于治疗一些常见且难以根治的疾病,如癌症和心血管疾病等。
通过临床实验数据的统计和分析,我们发现该药物在治疗癌症和心血管疾病方面具有显著的疗效,并且表现出良好的安全性和耐受性。
这将为广大患者带来新的治疗选择和希望。
为了确保药物的质量和安全性,我们严格按照相关法律法规进行研发和生产,并通过了各项专业机构的审查和监管。
新药的上市,将得到相关政府部门的监管和认可,确保其安全有效以及对患者的良好疗效。
目前,我们已经完成了相关的生产和质量控制准备工作,并计划在不久的将来投入市场。
届时,我们将与各大医疗机构合作,确保新药能够及时供应给有需求的患者。
我们相信,这款新药将在医药领域引起重大的关注和影响,为人类的健康事业作出新的贡献。
新药研发是一项复杂而辛苦的工作,需要科研人员付出大量的心血和努力。
在这里,我们要感谢所有参与了这次研发工作的科研人员,你们的辛勤付出才是这个成果的基础。
我们也要感谢所有一直以来给予我们支持和鼓励的合作伙伴和社会各界人士。
未来,我们将继续致力于研发更多更优秀的药物,为人类的健康事业做出更大的贡献。
同时,我们也将秉承诚信和负责的原则,始终站在患者和社会的立场,不断提高产品质量和服务水平。
最后,再一次感谢各位媒体朋友的关注和支持。
我们相信,有你们的报道和宣传,将使更多的人了解到我们的新药,让更多的患者从中受益。
相信在不久的将来,我们将共同见证这一药物的辉煌。
谢谢大家!祝好!- 这是由新药研发公司发布的成功研发新药的公告新闻稿。
氟化工上市公司一览

!氟化工上市公司一览(萤石资源概念股)9月8日权威人士透露,作为化工新材料的氟化工将在十二五计划中单列一个专项,拟强制性资源整合,并实现基本停止出口萤石,氢氟酸出口也将减少一半以上。
除了限制出口,政策还酝酿对萤石资源进行整合、加强对资源的控制,基本思路是将资源由国家控制,具体担任整合主角的是大型国企。
具有国资背景的氟化工行业的企业包括中国化工、中国中化、巨化股份、三爱富等。
规划提出,企业应重点发展为锂离子电池配套的电解质六氟磷酸锂、含氟表面活性剂的关键原料氟碳醇、为医药农药新品种配套的新型含氟中间体等产品,实现产业转型升级。
萤石的主要成分是氟化钙,是“可用尽且不可再生”的资源。
我国萤石储量为世界的1/2,探明可采储量仅为1/10,而产量却高达1/2。
萤石(氟化钙CaF2)是氟化工之根本,工业上用萤石和浓硫酸来制造氢氟酸,加热到250摄氏度时,这两种物质便反应生成氟化氢(HF),氢氟酸溶解氧化物能力极强,在电解铝中用作电解液,而锂电池电解液也是氟化物。
氟化工上市公司一览(包括萤石资源上市公司——萤石资源概念股):1.巨化股份(),公司位于中国氟都浙江衢州(萤石资源全国最丰富地区,拥有全国60%左右萤石资源),拥有衢州80%的萤石资源;公司拥有先进的氟化工技术和丰富的氟化物原料及六氟磷酸锂全套生产技术,并生产六氟磷酸锂上游原料无水氟化氢;公司持有%股权的浙江巨圣氟化学拥有四氟乙烯单体(TFE)10000吨/年、聚四氟乙烯(PTFE)6250吨/年产能;公司持有76%股权的浙江凯圣氟化学拥有国内最先进的年产3万吨氟化氢生产装置(AHF纯度达%),拥有的两条无水氢氟酸生产线年生产能力分别为万吨和万吨,电子级高纯氢氟酸项目将形成年产3000吨高纯氢氟酸的能力;公司间接控股的凯恒电子(浙江凯圣氟化学拥有其51%股权)拥有目前国内唯一一套年产5000吨电子级高纯氢氟酸生产装置。
2.三爱富(),公司拥有国内最完整的氟化工产业链,产品涉及CFCs、CFC替代品、含氟聚合物和含氟精细化学品四大类产品;公司在国内有机氟的几乎所有主要领域均处于领先地位,氟聚合物市场占有率达17%,CFC市场占有率达50%以上,CFC替代品市场占有率达70%以上,其中,氟聚合物中的F46、氟橡胶等产品的国内市场占有率均达50%以上;公司持股70%的常熟三爱富中昊化工新材料是CFCs替代产品、氟化工基础原料及氟化学品的重要发展基地。
海正药业财务分析报告

上市公司财务分析考试报告题目海正药业公司财务分析报告学生姓名陈骏鹏学号0系部经济贸易系专业国际经济与贸易班级0915812主考老师包强考试时间2012年1月广东金融学院教务处制目录一、企业简介 (3)1.公司简介 (3)2.历史沿革 (4)3.经营范围 (4)4.人员构成 (4)5.科技优势 (5)6.股权结构 (5)7.企业发布的重大新闻和事件 (6)8.行业现状 (6)二、企业财务现状 (7)1.财务数据 (7)2.资产负债表11年 (9)3.11年利润表 (15)三、企业2012年半年报、2011年年报、半年报、2010年年报、半年报指标趋势分析 (18)四、总结 (21)五、财务报表分析学习心得 (22)一、简介1.公司简介始创于1956年的浙江[1]海正药业股份有限公司(股票代码600267,以下简称“海正药业”)秉承“执著药物创新,成就健康梦想”的使命和“成为广受尊重的全球化制药企业”的愿景,致力于整合药物研发与生产资源,为全球客户提供更好的产品和服务,通过FDA、欧盟EDQM、TGA、KFDA等官方认证的品种达到40多个,销往全球30多个国家和地区。
2009年,公司荣获“全国五一劳动奖状”,海正、HISUN及图形被认定为“”,入选“中国万种微生物基因组计划”和“国家重大(磅)级药物品种产业化技术创新联盟”。
因圆满完成“抗甲流药物中间体生产”的,受到省政府的通令嘉奖。
2009年,公司实现销售收入39亿元,利润总额3.5亿元,分别比去年同期增长27%和46%,全国医药行业20强。
海正作为国家首批创新型企业,早在 2001年建立了国家认定的和,目前拥有专职研发人员400多名。
技术中心设有50多个单元实验室,研发领域涵盖化学合成、发酵、生物技术、天然植物提取及制剂开发等多个方面,产品治疗领域涉及抗肿瘤、心血管系统、抗感染、抗寄生虫、内分泌调节、免疫抑制、抗抑郁等。
海正与国内30多家知名的科研院校保持着密切的协作关系,在多所大学建有实验室。
中国抗体药物

中国抗体药物---乘风破浪正当时报告来自海通证券,分析师刘宇,发表于2012年6月20日投资要点21世纪以来,单克隆抗体应用实现了从诊断试剂到抗体药物的飞跃。
单克隆抗体是B细胞产生的免疫球蛋白,特点是靶向、特效、低毒,因此被广泛用于肿瘤、自身免疫性疾病等疑难杂症的治疗。
全球抗体药物市场增长势头强劲。
全球抗体药物市场规模1997年为3.10亿美元,2010年为480亿美元,CAGR47%。
研发领域集中---主要集中在肿瘤和自身免疫性疾病;盈利品种集中---2010年全球畅销药前12名中,抗体药物占6个,前六大抗体药物占全球销售额65.21%;产业分布集中---90%的产品由美国公司开发,其他国家仅占10%。
中国抗体药物基数小,发展潜力巨大。
2007年我国抗体药物市场规模为2.3亿元,2010年为10亿元,CAGR 46%,由于起步晚,市场规模较小,抗体药物使用比例较低:在癌症领域使用比例仅占2.5%、在自身免疫疾病领域使用比例低于10%,未来中国抗体药物发展潜力巨大。
合同研发、技术创新利好中国抗体药物产业化。
国内形成了北京、上海、西安三大研发及产业化基地。
北京有百泰生物,上海有中信国健、张江生物、上海美恩,西安有华神集团。
近年来出现以哺乳动物细胞培养为核心的药物开发服务平台CRO、CMO,以及引进的国际一次性生物反应器、抗体纯度和回收率的提高突破了我国抗体产业化瓶颈。
进口药占主导,专利到期带来难得发展机会,国产药比例将提升。
我国国产单抗药物主要为仿制,2005和2008年益赛普、泰欣生上市后,国产份额由几乎空白提升至25%左右。
2011年全球抗体新药获批数小于专利到期药物数,2015年将有640亿美元生物专利药到期,单抗药物占比高达48%,因此我们认为中国“仿制”抗体药物将迎来千载难逢的发展机会。
政策、研发、资金合力助推抗体药物较快发展。
基因泰克的经验表明,高研发投入、合作研发策略、不断丰富的产品线和雄厚的资金实力是企业成功的要素,因此我们选择具有完备的高水平技术平台以及融资机会的企业,我们还应关注国内相关政策,在政策支持、研发产业化、资本助力三大因素合力下,我国抗体药物企业将乘风破浪。
海正药业:关于获得药品注册批件的公告

股票简称:海正药业股票代码:600267 公告编号:临2020-58号债券简称:15海正01 债券代码:122427债券简称:16海正债债券代码:136275浙江海正药业股份有限公司关于获得药品注册批件的公告近日,浙江海正药业股份有限公司(以下简称“公司”或“海正药业”)收到国家药品监督管理局(以下简称“国家药监局”)核准签发的盐酸多奈哌齐口崩片的《药品注册批件》。
现就相关情况公告如下:一、药品基本情况1、药品名称:盐酸多奈哌齐口崩片剂型:片剂规格:5mg申请事项:国产药品注册注册分类:化学药品4类申报阶段:生产药品生产企业:浙江海正药业股份有限公司受理号:CYHS1800118国批件号:2020S00300药品批准文号:国药准字H20203231审批结论:根据《中华人民共和国药品管理法》及有关规定,经审查,本品符合药品注册的有关要求,批准注册,发给药品批准文号。
2、药品名称:盐酸多奈哌齐口崩片剂型:片剂规格:10mg申请事项:国产药品注册注册分类:化学药品4类申报阶段:生产药品生产企业:浙江海正药业股份有限公司受理号:CYHS1800119国批件号:2020S00301药品批准文号:国药准字H20203232审批结论:根据《中华人民共和国药品管理法》及有关规定,经审查,本品符合药品注册的有关要求,批准注册,发给药品批准文号。
二、该药品其他相关情况盐酸多奈哌齐口崩片适用于轻度或中度阿尔茨海默病症状的治疗。
盐酸多奈哌齐口崩片原研药由日本エーザイ株式会社研发,国内生产厂商主要有辅仁药业集团有限公司、金日制药(中国)有限公司、四川升和药业股份有限公司等。
公司盐酸多奈哌齐口崩片为国内首家按新4类获得国家药监局批准上市,视同通过一致性评价。
经查询IMS数据库,盐酸多奈哌齐口崩片2019年全球销售额为27,593.89万美元,其中中国销售额为77.89万美元;2020年1-3月全球销售额为5,501.28万美元,其中中国销售额为20.79万美元。
国家药监局附条件批准纳鲁索拜单抗注射液上市

国家药监局附条件批准纳鲁索拜单抗注射液上市
佚名
【期刊名称】《中国处方药》
【年(卷),期】2024(22)1
【摘要】近日,国家药品监督管理局通过优先审评审批程序附条件批准上海津曼特生物科技有限公司申报的纳鲁索拜单抗注射液(商品名:津立生)上市。
该药品用于治疗不可手术切除或手术切除可能导致严重功能障碍的骨巨细胞瘤成人患者。
纳鲁索拜单抗注射液(JMT103)为重组全人源抗核因子-κB受体活化因子配体(RANKL)单克隆抗体,通过与细胞表面的RANKL特异性结合。
【总页数】1页(PI0001)
【正文语种】中文
【中图分类】R73
【相关文献】
1.国家药监局附条件批准卡度尼利单抗注射液上市
2.国家药监局批准佩索利单抗注射液上市
3.国家药监局附条件批准伊基奥仑赛注射液上市
4.国家药监局附条件批准纳基奥仑赛注射液上市
5.国家药监局批准仑卡奈单抗注射液上市
因版权原因,仅展示原文概要,查看原文内容请购买。
688177百奥泰关于BAT1006注射液获得临床试验通知书的公告2020-11-19

证券代码:688177 证券简称:百奥泰公告编号:2020-051百奥泰生物制药股份有限公司关于BAT1006注射液获得临床试验通知书的公告重要内容提示:百奥泰生物制药股份有限公司(以下简称“公司”)于近日收到国家药品监督管理局(以下简称“国家药监局”)核准签发的关于公司在研药品BAT1006注射液的《临床试验通知书》。
根据《Clinical Development Success Rates 2006-2015》公布的数据,通常情况下对于抗肿瘤药物,一般I/II期临床研究阶段持续约2年时间,I期完成进入II期的比率约62.8%,II期完成进入III期的比率约24.6%,考虑到临床研究周期长、投入大,过程中不可预测因素较多,临床试验、审评和审批的结果以及时间都具有一定的不确定性,容易受到一些不确定性因素的影响,敬请广大投资者谨慎决策,注意防范投资风险。
现将相关情况公告如下:一、《临床试验通知书》基本情况药品名称:BAT1006注射液剂型:注射液规格:150mg/5ml申请事项:临床试验申请人:百奥泰生物制药股份有限公司受理号:CXSL2000257审批结论:根据《中华人民共和国药品管理法》及有关规定,经审查,2020年9月7日受理的BAT1006注射液符合药品注册的有关要求,同意开展用于晚期恶性肿瘤治疗的临床试验。
二、药品相关情况BAT1006注射液是百奥泰生物制药股份有限公司自主研发的一种单抗药物,其活性成分是一种由中国仓鼠卵巢细胞表达的靶向人表皮生长因子受体-2(HER2)的抗体,属于免疫球蛋白IgG1κ亚型,能够以高亲和力特异性地结合人HER2胞外蛋白结构域II,阻断HER2与其他HER家族受体(EGFR/HER3/HER4)的异源二聚化作用,抑制与HER2受体活性相关的肿瘤细胞的增殖与生存。
BAT1006的抗体糖基化修饰不含岩藻糖,相比于普通IgG1κ抗体,其招募NK等免疫细胞杀伤肿瘤细胞的作用更强。
国内上市的单抗药物及相关情况
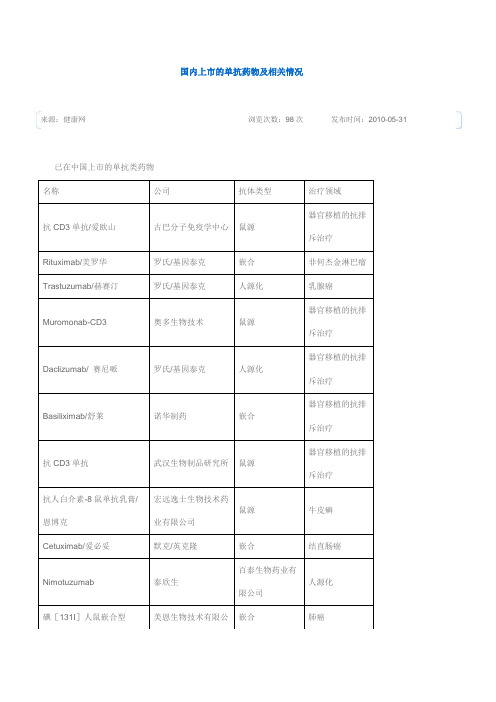
国内上市的单抗药物及相关情况来源:健康网浏览次数:98次发布时间:2010-05-31已在中国上市的单抗类药物以下是在中国上市的抗体药物应用现状:抗CD20单抗:(1)美罗华(利妥昔,Rituximab):是一种抗CD20的人鼠嵌合型单抗,该单抗通过识别B淋巴细胞表面标志(CD20)与其结合,达到杀伤肿瘤细胞的目的。
美罗华对于CD20表达量低、中度恶性的B细胞性淋巴瘤有较好疗效,对于老年体弱者,复发或化疗耐药者,美罗华联合化疗可以获得较高的缓解率。
(2)ZEVALIN:是德国先灵公司开发的一种治疗中低恶性B细胞淋巴瘤的新药,能有效杀死肿瘤细胞,副作用较小。
该药是抗体90Y 标记的放射免疫交联物,除了具有美罗华特异性结合B细胞淋巴瘤标志物(CD20)以外,其同位素90Y发挥了较好的电离杀伤肿瘤细胞的效应。
抗HER2单抗赫赛汀:HER2是原癌基因或C-erbB2编码一个单一的受体跨膜蛋白,分子量185kDa,其结构上与表皮生长因子受体相似。
在原发性乳腺癌患者中观察到有25%—30%%HER2过度表达,HER2基因扩增使肿瘤细胞表面HER2蛋白表达增加,导致HER2受体活化。
赫赛汀(Herceptin)是一种重组DNA衍生的人源化单克隆抗体,选择性地作用于人表皮生长因子受体-2(HER2)的细胞外部位。
在一项较大规模的多个国家参与的Ⅱ期临床试验(H0649g)报告中,采用Herceptin单药治疗既往使用1或2种细胞毒性化疗药物而失败的转移性乳腺癌,结果总体缓解率为15%、中位生存期缓解8个月,且所有患者对Herceptin的耐受性均较好。
Herceptin是第一个在乳腺癌中确认并显示有较好疗效的抗体药物。
抗VEGF单抗:由美国基因泰克公司研制的血管表皮生长因子(VEGF)抗体,成功地治疗了千余例晚期结肠癌患者,其平均生命延长了4个月。
这一结果为中国科学家的最新研究提供了佐证。
美国遗传技术研究公司开发和生产的抗癌新药Avastin是一种基因工程单抗药物,主要通过抑制血管表皮生长因子,并能阻断新生血管增生,使肿瘤组织无法获得所需营养而最终"饿死",达到抗癌功效。
抗体药物龙头企业

抗体药物龙头企业抗体药物龙头企业特指在抗体药物领域具有领先地位或取得重大成就的企业。
以下是一些被认为是抗体药物龙头企业的公司:1. 基因泰克(Genentech):Genentech是一家隶属罗氏集团的美国生物制药公司,致力于抗体药物的研发和生产。
该公司研发了多种成功的抗体药物,如人源化抗HER2阳性乳腺癌药物Herceptin和免疫检查点抑制剂Rituxan。
2. 强生制药(Johnson & Johnson):强生制药是一家全球知名的制药和医疗器械公司,其子公司Janssen Biotech在抗体药物领域具有重要地位。
Janssen Biotech研发了多个抗体药物,包括用于治疗自身免疫性疾病的Stelara和用于治疗白血病的Darzalex。
3. 霍夫曼-拉罗奇(Hoffmann-La Roche):霍夫曼-拉罗奇是一家瑞士制药公司,旗下的Roche Pharmaceuticals是抗体药物领域的领先企业之一。
Roche Pharmaceuticals开发的抗体药物包括治疗乳腺癌的Herceptin、Perjeta和Kadcyla,以及治疗淋巴瘤的Rituxan。
4. 雅培(AbbVie):雅培是一家美国制药公司,专注于抗体药物的研发和生产。
该公司最成功的抗体药物是用于治疗类风湿性关节炎和其他自身免疫性疾病的Humira,该药物一度是全球最畅销的药物之一。
5. 赛诺菲(Sanofi):赛诺菲是一家法国跨国制药公司,其子公司赛诺菲制药在抗体药物领域有一定地位。
赛诺菲制药研发的抗体药物包括治疗哮喘和过敏性鼻炎的Dupixent和治疗乳腺癌的Tecentriq。
这些企业在抗体药物领域具有雄厚的科研实力和丰富的产品线,是该领域的龙头企业。
关于国家食品药品监督管理总局批准

股票简称:海正药业股票代码:600267 公告编号:临2017-06号债券简称:15海正01 债券代码:122427债券简称:16海正债债券代码:136275浙江海正药业股份有限公司关于甘精胰岛素、甘精胰岛素注射液及注射用结核病变态反应原RP22获得临床批件的公告近日,浙江海正药业股份有限公司(以下简称“公司”)收到国家食品药品监督管理总局(以下简称“国家食药监总局”)核准签发的甘精胰岛素、甘精胰岛素注射液及注射用结核病变态反应原RP22的药物临床试验批件。
现就相关情况公告如下:一、临床试验批件主要内容1、药品名称:甘精胰岛素批件号:2016L10796剂型:原料药规格:----申请事项:国产药品注册申请人:浙江海正药业股份有限公司受理号:CXSL1600005浙注册分类:治疗用生物制品15类审批结论:根据《中华人民共和国药品管理法》及有关规定,经审查,本品符合药品注册的有关要求,批准本品制剂进行临床试验。
2、药品名称:甘精胰岛素注射液批件号:2016L10793剂型:注射剂规格:3ml:300单位(笔芯)申请事项:国产药品注册申请人:浙江海正药业股份有限公司受理号:CXSL1600006浙注册分类:治疗用生物制品15类审批结论:根据《中华人民共和国药品管理法》及有关规定,经审查,本品符合药品注册的有关要求,批准本品进行临床试验。
3、药品名称:注射用结核病变态反应原RP22批件号:2016L10792剂型:注射剂规格:10μg申请事项:国产药品注册申请人:浙江海正药业股份有限公司受理号:CXSL1400078浙注册分类:治疗用生物制品4类审批结论:根据《中华人民共和国药品管理法》及有关规定,经审查,本品符合药品注册的有关要求,批准本品进行临床试验。
二、该药品研发及相关情况1、甘精胰岛素注射液(甘精胰岛素为其原料药)是一种长效胰岛素,用于需要胰岛素治疗的糖尿病患者,本品上市原研药“来得时®”(英文商品名:“Lantus®”)由赛诺菲安万特公司开发,2000年在美国上市,2004年进入中国市场,2015年的全球销售额达到63.9亿欧元。
抗癌药上市公司-市场上常见的十大抗癌药

抗癌药上市公司市场上常见的十大抗癌药目前全球各国已批准上市的抗癌药物大约有130 ~150种。
用这些药物配制成的各种抗癌药物制剂大约有1300~1500种。
由于抗癌药稀缺,价格又昂贵,所以受到很多人的关注,近几年关于抗癌药的新闻也是很多,了解这些对于癌症这种疾病的治疗也是非常有帮助的,那下面我们就来详细为大家介绍下这些问题。
抗癌药上市公司一、康恩贝(600572)乙肝+癌症治疗,2012年7月公司出资1812.86万元取得四川辉阳18.13%股份,出资456.472万美元取得远东实验室18.13%股权(2012年9月投资主体变更为全资子公司香港康恩贝)。
四川辉阳注册资本3700万元,主要在研产品为重组高效复合干扰素(国家重大新药创制项目),目前尚处于新药研发阶段,该产品研发新药已取得新药临床研究批件,适应症为乙型病毒性肝炎的治疗。
远东实验室授权资本为72500美元,以重组高效复合干扰素为基础专注于癌症治疗研究,公司目前计划选择国外若干国家申报将rSIFN-co用于研发癌症治疗新药的临床研究。
二、恒瑞医药(600276)多西他赛、奥沙利铂、伊立替康、亚叶酸钙、来曲唑、替吉奥胶囊等。
我国抗肿瘤药龙头企业、在抗肿瘤药领域具有明显的研发和营销优势、靶向药物阿帕替尼有望在12 年或13 年获得新药证书并具有重磅炸弹潜力。
三、益佰制药(600594)艾迪注射液、复方斑蝥胶囊、洛铂、科博肽等具有突出的市场营销能力、艾迪和杏丁有望保持稳定增长、独家代理洛铂有望成为过10 亿元品种。
四、翰宇药业(300199)胸腺五肽,多肽领域龙头公司,是国内最早进入多肽领域的公司之一,在多肽领域技术、人才、产品储备丰富。
短期受益医保扩容,主要品种胸腺五肽全年有望增长70%,新产品叠加效应明显,未来持续成长可期。
公司在SFDA申报生产的多肽产品还有:免疫调节药胸腺法新、保胎药阿托西班、抗癌药西曲瑞克。
五、双鹭药业(002038)胸腺五肽、重组人白介素-2、重组人粒细胞集落刺激因子、重组人白介素-11、紫杉醇、三氧化二砷、氨酚曲马多、托烷司琼、格拉司琼等。
浙江海正药业股份有限公司 关于枸橼酸托法替布片获得临床

股票简称:海正药业股票代码:600267 公告编号:临2016-35号债券简称:11海正债债券代码:122094
债券简称:15海正01 债券代码:122427
债券简称:16海正债债券代码:136275
浙江海正药业股份有限公司
关于枸橼酸托法替布片获得临床批件的更正公告
浙江海正药业股份有限公司(以下简称“公司”)于2016年4月28日在《中
国证券报》、《上海证券报》、《证券时报》和上海证券交易所()
网站上刊登了《关于枸橼酸托法替布片获得临床批件的公告》(公告编号:临2016-29号),因工作人员疏忽,将公司枸橼酸托法替布片已投入研发费用单位“万
元”误写为“元”,现更正如下:
截至目前,公司枸橼酸托法替布片研发项目已投入研发费用270万元人民币
左右。
公告其他内容不变,由于我们的工作疏忽给投资者带来的不便,深表歉意。
特此公告。
浙江海正药业股份有限公司董事会
二○一六年四月二十九日。
生物医药板块上市公司一览

生物制药之首仿药、独家疫苗系列上市公司一览表1.首仿药系列:1、恒瑞医药(600276)奥沙利柏、多西他赛、伊利替康;2、恩华医药(002262)齐拉西酮,原研厂家辉瑞;3、白云山(000522)福泰(仿达菲);4、海南海药(000566)紫杉醇注射液、头孢西丁钠;5、信立泰(002294)泰嘉(硫酸氢氯吡格雷);6、上海医药(601607)仿达菲;7、海正药业(600267)达菲中间体;8、同仁堂(600085)3个仿制品种已进入审批生产程序;9、双鹤药业(600062)2009年3月27日正式推出了公司最新仿制药研发成果—“冠爽通用名:匹伐钙”;10、长春高新(000661)艾塞那肽产品在国内首家通过国家食品药品监督管理局的审批,该药被国际糖尿病专家列为四大潜力药物之首;11、康芝药业(300086)瑞芝清(尼美苏利颗粒)。
2.独家疫苗系列:1、天坛生物(600161)麻腮风三联疫苗为国内首创;2、长春高新(000661)水痘、抗艾疫苗;3、岳阳兴长(000819)胃病疫苗;4、重庆啤酒(600132)乙肝疫苗;5、沃森生物(300142)脑膜炎、肺炎等多种疫苗;6、力生制药(002393)肺炎、水痘、甲乙肝疫苗;7、智飞生物(300122)脑膜炎、维卡;8、科华生物 (002022) 乙型肝炎病毒、丙型肝炎病毒、人类免疫缺陷病毒(Ι型)核酸检测试剂盒(PCR-荧光法)获得药监局新药证书和生产批准文号。
新药证书编号:国药证字 S2*******,批准文号:国药准字S2*******,标志着公司在新品研发方面取得重大进展,巩固公司在诊断试剂领域的龙头地位。
生物制药之独家中药系列上市公司一览表独家中药系列:1、云南白药(000538)白药系列,国家绝密配方,国家一类中药保护品种;2、片子癀(600436)片子癀系列,国家绝密配方,国家一类中药保护品种;3、沃华医药(002107)心可舒片,国家中药保护品种;4、东阿阿胶(000423)阿胶系列,国家首批非物质文化遗产扩展项目名录;5、精华制药(002349)王氏保赤丸、季德胜蛇药片,国家中药保密品种;6、中恒集团(600252)血栓通注射液;7、千金药业(600479)妇科千金片;8、中新药业(600329)速效救心丸,国家级机密中药品种;9、广州药业(600332)消渴丸;10、马应龙(600993)麝香痔疮膏;11、独一味(002219)独一味系列;12、金陵药业(000919)脉络宁注射液;13、天士力(600535)复方丹参滴丸;14、华润三九(000999)999感冒灵、皮炎平、正天丸、胃泰,华蟾注射液,国家保密配;15、九芝堂(000989)驴胶补血冲剂、乙肝宁冲剂,国家二级中药保护品种。
舒泰神:关于BDB-001注射液获得印度临床试验批准及获得西班牙临床试验批准补充说明的公告

证券代码:300204 证券简称:舒泰神公告编号:2020-29-01舒泰神(北京)生物制药股份有限公司关于BDB-001注射液获得印度临床试验批准及获得西班牙临床试验批准补充说明的公告特别提示:1、公司及全资子公司德丰瑞近日获得BDB-001注射液在印度开展治疗进展期重型COVID-19的多中心、开放、随机平行对照的II期临床试验的批准;2、公司开展BDB-001注射液的国际多中心临床试验以支持BDB-001注射液在中国进行注册;3、BDB-001注射液是针对人C5a分子的单克隆抗体药物,能特异性结合C5a,使C5a丧失结合受体的能力,阻断其诱导的生物学功能,抑制炎症级联反应,从而控制炎症进一步发展;4、BDB-001注射液后续临床试验的有序进行、能否取得生产批件、顺利上市以及上市后与新冠疫情相关的营销等存在诸多不确定性;短期内,该项目会导致公司研发费用的增长,对公司业绩造成一定影响;敬请广大投资者谨慎决策,注意投资风险。
舒泰神(北京)生物制药股份有限公司(以下简称“舒泰神”或“公司”)及全资子公司北京德丰瑞生物技术有限公司(以下简称“德丰瑞”)取得了印度中央药品标准控制组织(CDSCO)关于授权临床试验申请的决定文件,批准BDB-001注射液在印度开展治疗进展期重型COVID-19的多中心、开放、随机平行对照的II期临床试验,以评估其在治疗中的有效性和安全性。
公司于2020年05月29日披露了《关于BDB-001注射液获得西班牙临床试验批准的公告》。
现将BDB-001注射液获批印度临床试验和西班牙临床试验的补充说明公告如下:一、临床试验获批的主要内容1、药品名称:BDB-001注射液2、申请人:舒泰神(北京)生物制药股份有限公司、北京德丰瑞生物技术有限公司3、临床试验内容:治疗进展期重型COVID-19的多中心、开放、随机平行对照的II期临床试验,以评估其在治疗中的有效性和安全性4、编号:No. CT/20/000045二、药品的其他相关情况近30年的超过4000篇PubMed研究报告提示补体C5a分子是急性感染、组织损伤炎症早期出现的最强因子,被公认为是广谱炎性放大器,是补体过度激活导致剧烈炎症反应的主要效应分子,是感染、损伤急救药的理想靶点。
GCSF市场
国内外GCSF(短效、长效)市场情况一、国外GCSF市场现状1991 年6 月美国FDA 批准了美国Amgen 公司生产的短效GCSF(NEUPOGEN)上市。
Amgen公司的长效GCSF(Neulasta)于2002年1月22日获美国食物与药品管理局(FDA)批准,同年4月9日,Neulasta在美国首次上市,当年就获4.635亿美元销售额佳绩,创2002年入市美国新药销售额/年的最高记录。
同年8月,该产品在欧洲和澳大利亚以相似的适应症获准上市。
2003年,该产品全球销售总额达12.6亿美元(美国11.8亿美元,其余市场7930万美元),坐上了美国市场新药上市第一年销售额领先排行榜的第一把交椅。
2004年Neulasta在市场继续畅通无阻,1季度全球销售额高达3.95亿美元,比去年同期猛增53%,其中美国市场增长33%达3.36亿美元;其他市场销售额为5800万美元。
据安进2010年的财务报表显示:世界范围内,Neulasta(长效)2006、2007、2008、2009、2010年的销售额分别为27亿美元、30亿美元、33亿美元、33.5亿美元及35.6亿美元,相应的NEUPOGEN (短效)的销售额分别为12亿美元、12亿美元、13亿美元、12.88亿美元及12.86亿美元。
由以上数据可以看出安进的普通GCSF全球销售额近三年来基本持平(有下降趋势),而长效GCSF Neulasta 的销售额则以每年10%的速度持续稳定增长。
二、国内GCSF市场现状粒细胞集落刺激因子(GCSF)是目前最有效的升白药物之一,在临床的肿瘤治疗中广泛使用。
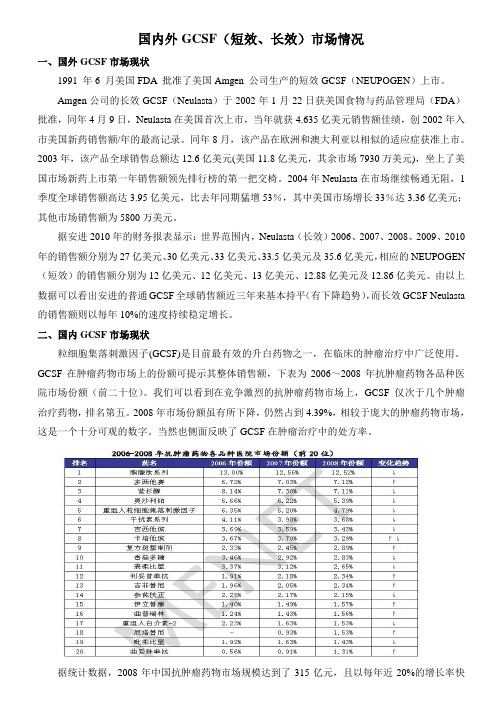
GCSF在肿瘤药物市场上的份额可提示其整体销售额,下表为2006~2008年抗肿瘤药物各品种医院市场份额(前二十位)。
我们可以看到在竞争激烈的抗肿瘤药物市场上,GCSF仅次于几个肿瘤治疗药物,排名第五。
2008年市场份额虽有所下降,仍然占到4.39%,相较于庞大的肿瘤药物市场,这是一个十分可观的数字。
创新药周报:从辉瑞收购GBT看上半年生物医药“并购热潮”

证券研究报告| 行业周报2022年08月14日医药生物创新药周报:从辉瑞收购GBT看上半年生物医药“并购热潮”一、本周聚焦:辉瑞收购GBT及上半年并购事件回顾8月8日,辉瑞公司(Pfizer)和Global Blood Therapeutics(GBT)宣布,辉瑞将收购GBT公司。
根据交易条款,辉瑞将以总价约54亿美元现金收购GBT公司所有已发行的股票。
让辉瑞溢价收购的GBT公司究竟拥有怎样的“硬实力”?今年上半年生物医药还有哪些重大收购交易发生?本周周报,让我们一探究竟。
Global Blood Therapeutics聚焦血液疾病领域的千里马:公司致力于发现、开发和商业化治疗严重的血液疾病的新疗法,提供治疗镰状细胞病的口服药。
其核心产品Oxbryta(voxelotor)已于2019年上市。
其他在研管线中,Inclacumab是新型的全人源单克隆抗体P-选择素抑制剂,具备成为同类最佳潜质;GBT601具备低剂量下更好疗效潜力,公司在血液疾病领域的未来前景广阔。
核心产品Oxbryta填补镰状细胞病(SCD)治疗空白:辉瑞本次收购的主要目标是GBT及其主要产品Oxbryta(voxelotor),以加强其自身的产品组合和管线,辉瑞的血液学重点是镰状细胞病(SCD)和血友病。
镰状细胞病(SCD) 是一种影响血红蛋白的终生遗传性血液疾病,血红蛋白是一种由红细胞(RBC) 携带的蛋白质,可向全身组织和器官输送氧气。
SCD生存成本高昂,给患者和社会带来重大负担,而GBT公司开发的Oxbryta(voxelotor)是一种直接针对SCD根源的药物。
面对治疗手段匮乏的SCD,voxelotor将面临极具潜力的商业前景。
上半年21起并购交易,生物医药并购热潮来袭:上半年共发生21起并购交易,肿瘤和中枢神经是热门领域,辉瑞和葛兰素史克各进行了两次并购:✓辉瑞116亿美元现金收购Biohaven达成上半年最大规模并购交易;✓首家被中国药企并购的美国上市医药公司:中国生物制药收购F-star;✓再生元溢价335% 2.5亿美元收购Checkmate开启并购之路;✓葛兰素史克33亿美元收购Affinivax加强疫苗快速研发。
海正药业2016以来获得的临床批件情况

泊沙康唑注射 液
抗真菌药品
2015 年 5 月申 报临床 2016 年 8 月获 批临床 研发费用: 780 万
2015 年 销 售 49,131.80 万 美 元
齐 鲁 制 药 (2016.3 临批) 奥 赛 康 药 业 (2016.3 临批) 成 都 海 博 锐 ( 2016.10 临 批) 上 海 宣 泰 ( 2016.11 临 批) 瑞 阳 制 药 (2017.3 临批) 江 西 青 峰 (2017.3 临批)
石家庄四药 (2016.10 临 批) 西安葛蓝新通 (2016.10 临 批) 昆 明 源 瑞 (2016.10 临 批) 西安天一秦昆 (2016.10 临 批) 湖 南 迪 诺 (2016.10 临
批) 通辽东北六药 (2016.10 临 批) 厦门恩成制药 (2016.10 临 批)
重组抗肿瘤坏 死因子-α 全人 源单克隆抗体 注射液 (修美乐类似 药)
2015 年超过 30 亿美元
甘李药业、 东阳 光、通化东宝、 诺和诺德
注射用罗米地 辛
用于治疗先前 至少接受过一 种全身治疗的 皮肤 T 细胞淋 巴瘤(CTCL)患 者,又于 2011 年 6 月经 FDA 批准了新的适 应症用于 治疗先前至少 接受过一种治 疗的外周 T 细 胞淋巴瘤(PTCL) 患者
2015 年 1.1 亿美 金
国内尚未上市
华 北 制 药 ( 2016.3 临 批) 、中美华东 (2016.5 临批)
注射用结核病 变 态 反 应 原 RP22
供结核病流行 病学调查及临 床疑似结核病 人诊断用
无 (类似的有安 徽龙科马、 北京 祥瑞)
缬沙坦片
片适015 年全球市
注射用重组人 鼠嵌合抗肿瘤 坏 死 因子 - α 单 抗 (类克类似药)
医药:海正药业牵手辉瑞百灵与百诺技术转让

医药:海正药业牵手辉瑞百灵与百诺
技术转让
第一农经讯9月13日,贵州百灵与海正药业可谓风光无限,把利好消息发挥的淋漓极致。
1、贵州百灵与济南百诺签订技术转让合同
9月13日,贵州百灵(002424)晚间公告,公司9月12日与济南百诺医药科技开发有限公司签订《技术转让合同书》,双方经过有效的协商,就治疗失眠的化药3类“美乐托宁原料及缓释片”项目临床批件技术转让事宜签订该合同。
按该合同,济南百诺将其拥有的“美乐托宁原料及缓释片”转让给公司,内容包括:临床批件及该品种相关的生产、开发全部权利,临床批件号为:2011L00537、2011L00536;该品种临床前研究工作由济南百诺负责,临床试验及申报生产工作由公司负责,济南百诺配合公司完成上述工作,使研制药品的工艺、质量及稳定性达到《药品注册管理办法》的技术要求。
公司向济南百诺提供本项目技术转让费,总计750万元。
2、海正药业牵手辉瑞设合资公司
9月13日,海正药业(600267)与全球最大的以研发为基础的制药企业辉瑞公司在杭州宣布,由双方合资组建的海正辉瑞制药有限公司正式成立。
据悉,海正辉瑞制药有限公司总投资2.95亿美元,注册资本2.5亿美元。
其中海正药业和辉瑞的持股比例分别为51%
和49%.双方将向合资企业注入现有产品线中经过精挑细选的产品。
合资企业成立伊始的产品组合将覆盖肿瘤、心血管、抗感染、神经系统、免疫抑制剂等治疗领域。
综上,受次利好消息影响,第一农经预计相关股都将备受投资者以及股民的青睐,被大肆拉高,节节攀升。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
股票简称:海正药业股票代码:600267 公告编号:临2016-104号债券简称:15海正01 债券代码:122427
债券简称:16海正债债券代码:136275
浙江海正药业股份有限公司关于
重组抗白介素-6受体人源化单克隆抗体注射液
获得临床批件的公告
近日,浙江海正药业股份有限公司(以下简称“公司”)收到国家食品药品监督管理总局(以下简称“国家食药监总局”)核准签发的重组抗白介素-6受体人源化单克隆抗体注射液的《药物临床试验批件》。
现就相关情况公告如下:
一、临床试验批件主要内容
药品名称:重组抗白介素-6受体人源化单克隆抗体注射液
批件号:2016L09574
剂型:注射剂
规格:4ml:80mg
申请事项:新药
申请人:海正药业(杭州)有限公司,浙江海正药业股份有限公司
受理号:CXSL1500025浙
注册分类:治疗用生物制品2类
审批结论:根据《中华人民共和国药品管理法》及有关规定,经审查,本品符合药品注册的有关要求,批准本品进行临床试验。
二、该药品研发及相关情况
重组抗白介素-6受体人源化单克隆抗体注射液是一种以白介素-6受体(IL-6R)为靶点的抗体药物。
作用机制和ACTEMRA® /雅美罗®(罗氏公司)相
同,用于治疗对改善病情的抗风湿药物(DMARDs)治疗应答不足的中到重度活动性类风湿关节炎的成年患者。
雅美罗®于2010年在美国上市,2013年在中国上市,2015年的全球销售额超过14.32亿瑞士法郎。
在国内,尚未有同类产品批准上市。
公司于2015年2月向国家食药监总局提交临床注册申请并获得受理,接下来公司将按照药物临床试验批件要求进行重组抗白介素-6受体人源化单克隆抗体注射液的临床试验研究。
截至目前,公司在该药品研发项目已投入研发费用1500万元人民币左右。
新药研发是项长期工作,受到技术、审批、政策等多方面因素的影响,临床试验进度及结果、未来产品市场竞争形势均存在诸多不确定性。
敬请广大投资者注意投资风险。
特此公告。
浙江海正药业股份有限公司董事会
二○一六年十一月十九日。
