cochrane纳入的RCT文献质量评价(风险偏倚评估工具)中英文对照版..
Cochrane协作网偏倚风险评价工具

表1Cochrane协作网偏倚风险评价工具评价条目评价内容描述具体评价问题1.随机分派措施具体描述产生随机分派序列旳措施,有助于评估组间可比性随机化分派序列旳产生与否对旳?2.分派方案隐藏具体描述隐藏随机分派序列旳措施,从而协助判断干预措施分派状况与否可预知分派方案与否有效地隐藏?3.盲法描述对受试者或实验人员实行盲法旳措施,以避免他们懂得受试者旳干预措施,提供判断盲法与否成功旳有关信息盲法与否完善?4.成果数据旳完整性报告每个重要结局指标旳数据完整性,涉及失访和退出旳数据。
明确与否报告以上信息及其因素,与否采用意向性分析(ITT)成果数据与否完整?5.选择性报告研究成果描述选择性报告成果旳也许性及状况研究报告与否提示无选择性报告成果?6.其他偏倚来源除以上5个方面,与否存在其他引起偏倚旳因素?若事先在计划中提到某个问题或因素,应在全文中作答研究与否存在引起高度偏倚风险旳其他因素?表2 Cochrane协作网偏倚风险评价旳具体原则评价条目评价成果评价内容描述1.随机分派措施对旳♦采用随机数字表、计算机产生随机数字、抛硬币、掷骰子或抽签等措施不对旳♦按患者生日、住院日或住院号等旳末位数字旳奇数或偶数;♦交替分派措施;♦根据医师、患者、实验室检查成果或干预措施旳可获得性分派患者入组不清晰♦根据干预措施旳可获得性;♦信息不详、难以判断对旳与否2.方案隐藏完善♦中心随机,涉及采用电话、网络和药房控制旳随机♦按顺序编号或编码旳相似容器♦按顺序编码、密封、不透光旳信封不完善♦公开随机分派序列如列出随机数字♦未密封、透光或未按顺序编号旳信封♦交替分派♦根据住院号、生日等末位数字旳奇数或偶数不清晰♦未提及分派方案隐藏♦提供旳信息不能判断与否完善,如使用信封,但未描述与否按顺序编码、密封、不透光3.盲法对旳♦没有采用盲法,但成果判断和测量不会受影响♦对患者和重要研究人员采用盲法,且盲法不会被破坏♦对成果测量者采用盲法,未对患者和重要研究人员采用盲法,但不会导致偏倚不对旳♦未采用盲法或盲法不完善,成果判断或测量会受影响♦对患者和重要研究人员采用盲法,但盲法也许被破坏♦对患者和重要研究人员均未采用盲法,也许导致偏倚不清晰♦信息不全,难以判断与否对旳♦文中未提及盲法4.成果数据旳完整性完整♦无缺失数据;缺失数据不影响成果分析(生存分析中缺失值) ♦组间缺失旳人数和因素相似♦缺失数据局限性以对效应值产生重要影响;缺失数据采用恰当措施赋值不完整♦组间缺失旳人数和因素不平衡♦缺失数据足以对效应值产生重要影响♦采用“as-treated”分析,但变化随机入组时干预措施旳人数较多♦不恰当应用简朴赋值不清晰♦信息不全,难以判断数据与否完整(缺失人数或因素未报告) ♦文中未提及数据完整性问题5.选择性报告研究成果无选择性报告♦有研究方案,且系统综述关怀旳方案中预告指定旳成果指标(重要和次要成果)均有报告♦没有研究方案,但所有盼望旳结局指标,涉及在刊登文献中预先指定旳指标均有报告有选择性报告♦未报告所有预先指定旳重要结局指标♦报告旳一种或多种重要结局指标采用预先未指定旳测量和分析措施♦报告旳一种或多种重要结局指标未预先指定♦系统综述关怀旳一种或多种结局指标报告不完善,以致不能纳入行Meta分析♦未报告重要旳结局指标不清晰♦信息不全、难以判断6.其他偏倚来源无♦纳入研究无其他偏倚来源有至少存在一种重要偏倚风险:♦与使用旳研究设计方案有关旳偏倚♦研究提前终结(数据因素或正规终结因素)♦基线明显不平衡♦声称有欺骗行为♦其他问题不清晰♦信息不全,难以判断与否存在重要偏倚♦发现旳问题与否导致偏倚,理由或根据局限性。
完整版)Cochrane协作网的RCT偏倚风险评价工具

完整版)Cochrane协作网的RCT偏倚风险评价工具评估随机对照试验偏倚风险是非常重要的,因为这些偏倚可能会影响试验结果的准确性和可靠性。
表Cochrane协作网提供了一些评价条目,以评估试验的随机序列产生、分配隐藏、施盲和结果数据完整性等方面的偏倚风险。
在随机序列产生方面,低风险的方法包括采用随机数字表、使用计算机随机数字发生器、最小化随机等。
而高风险的方法包括使用开放的随机分配表(如随机数字清单)和交替分配等。
如果关于随机序列产生过程的信息不充分,则无法判断其偏倚风险。
在分配隐藏方面,低风险的方法包括中心化分配(包括电话、基于网络和药房控制的随机化)、同一外观、连续编号的药物和按顺序编号、不透光、密封的信封等。
而高风险的方法包括使用无适当保护措施的分配信封(如信封未密封、透光信封、信封未按顺序编号)和任何其他明显未隐藏的方法。
如果信息不充分,则无法判断其偏倚风险。
在施盲方面,低风险的方法是确保对受试者和主要研究人员施盲,并且不太可能破盲。
而高风险的方法是尝试对受试者和主要研究人员施盲,但很可能破盲,并且结果很可能受缺乏盲法的影响。
如果信息不充分,则无法判断其偏倚风险。
在结果数据完整性方面,低风险的方法是未缺失结果数据,并且缺失的结果数据原因与真实结果不太可能相关。
对于二分类结果数据,缺失结果数据的比例不足以对干预效应估计产生临床相关影响。
对于连续性结果数据,缺失结果数据中似真的效应大小不足以对观测效应大小产生临床相关影响。
而高风险的方法是存在缺失结果数据,并且缺失结果数据的原因可能与真实结果相关。
如果缺失结果数据在各干预组的数量不均衡或组间缺失数据具有不同的原因,则可能会引入偏倚。
如果信息不充分,则无法判断其偏倚风险。
评估随机对照试验的偏倚风险是非常重要的,以确保试验结果的准确性和可靠性。
因此,在进行随机对照试验时,需要采用低风险的随机序列产生、分配隐藏和施盲方法,并确保结果数据的完整性。
cochrane纳入的RCT文献质量评价中文版教学内容

不全结局数据的数量,性质,处理方式导致失访偏倚
发表偏倚
Selective reporting.
说明如何审查选择性报道结局的可能性,以及审查结果
选择性报道结局导致发表偏倚
无缺失数据
缺失数据的产生不大可能与真实结局相关(对于生存数据,删失不大可能引入偏倚)
缺失数据的数目在各干预组相当,且各组缺失原因类似
对二分类变量,与观察事件的发生风险相比,缺失比例不足以影响预估的干预效应
对连续性结局数据,缺失数据的合理效应规模(均数差或标准均数差)不会大到影响观察的效应规模;
缺失的数据用合适的方法进行估算
无盲法或盲法不充分,但系统评价员判断结局很可能受到缺乏盲法的影响
尝试对关键的参与者和实施者行盲法,但盲法很可能被打破,结局很可能受到缺乏盲法的影响
风险未知
任何如下标准:
没有足够信息判断为低风险或高风险
研究未描述此情况
结局数据不完整
不全结局数据的数量,性质,处理方式导致失访偏倚
偏倚低风险标准
任何如下标准:
通过奇偶或出生日期产生序列
通过入院日期产生序列
通过类似住院号或门诊号产生序列
相对于上面提到的系统方法,其它非随机的方法少见的多,也更明显。通常包括对参与者进行判断或非随机的方法,例如:
临床医生判断如何分配
参与者判断如何分配
基于实验室检查或系列测试的结果分配
基于干预的可获取性进行分配
偏倚风险不清楚的判断标准
高风险判断标准
任何如下标准:
缺失数据的产生很大可能与真实结局相关,缺失数据的数目及缺失原因在各干预组相差较大
(完整版)Cochrane协作网研究质量评价工具

(完整版)Cochrane协作网研究质量评价工具Cochrane协作网是一个致力于提供高质量临床和流行病学研究的组织。
为了保证研究的可靠性和准确性,Cochrane协作网开发了一套研究质量评价工具,以帮助研究人员和读者判断研究的科学性和可靠性。
以下是Cochrane协作网研究质量评价工具的完整版:1. 研究设计的选择和描述:研究应明确阐述其研究设计,包括目的、研究问题、研究范围和参与对象等。
合适的研究设计能提供可靠的数据和结论。
研究设计的选择和描述:研究应明确阐述其研究设计,包括目的、研究问题、研究范围和参与对象等。
合适的研究设计能提供可靠的数据和结论。
2. 样本选择的合理性:研究应对样本选择的方法进行详细描述,包括样本的来源、选择标准和样本量的计算等。
样本的合理选择能提高研究结果的可靠性和普遍适用性。
样本选择的合理性:研究应对样本选择的方法进行详细描述,包括样本的来源、选择标准和样本量的计算等。
样本的合理选择能提高研究结果的可靠性和普遍适用性。
3. 数据收集和测量工具的可靠性和有效性:研究应清楚描述用于数据收集的方法和工具,并验证其可靠性和有效性。
合适的数据收集工具能提供准确和可比较的数据。
数据收集和测量工具的可靠性和有效性:研究应清楚描述用于数据收集的方法和工具,并验证其可靠性和有效性。
合适的数据收集工具能提供准确和可比较的数据。
4. 数据分析的方法和结果的解释:研究应明确描述所使用的数据分析方法,并对结果进行准确的解释。
合理的数据分析方法能提供可靠的研究结论。
数据分析的方法和结果的解释:研究应明确描述所使用的数据分析方法,并对结果进行准确的解释。
合理的数据分析方法能提供可靠的研究结论。
5. 偏倚的评估:研究应对偏倚的可能性进行评估,并采取适当的措施减少偏倚的影响。
合理的偏倚评估能提高研究的可靠性和可信度。
偏倚的评估:研究应对偏倚的可能性进行评估,并采取适当的措施减少偏倚的影响。
合理的偏倚评估能提高研究的可靠性和可信度。
循证医学名词术语中英文对照

循证医学名词术语中英文对照循证医学名词术语中英文对照安全性Safety半随机对照试验quasi- randomized control trial,qRCT背景问题background questions比值比odds ratio,OR标准化均数差standardized mean difference, SMD病例报告case report病例分析case analysis病人价值观patient value病人预期事件发生率patient’s expected event rate, PEER补充替代医学complementary and alternative medicine, CAM 不良事件adverse event不确定性uncertaintyCochrane图书馆Cochrane Library, CLCochrane系统评价Cochrane systematic review, CSR Cochrane协作网Cochrane Collaboration, CCCox比例风险模型Cox’ proportional hazard model参考试验偏倚References test bias肠激惹综合征irritable bowel syndrome,IRB测量变异measurement variation成本-效果cost-effectiveness成本-效果分析cost-effectiveness analysis成本-效益分析cost-benefit analysis成本-效用分析cost-utility analysis成本最小化分析(最小成本分析)cost-minimization analysis重复发表偏倚Multiple publication bias传统医学Traditional Medicine,TMD—L法DerSimonian & Laird methodthe number needed to harm one more patients from the therapy,NNH 对抗疗法allopathic medicine,AM对照组中某事件的发生率control event rate,CER多重发表偏倚multiple publication bias二次研究secondary studies二次研究证据secondary research evidence发表偏倚publication biasnumber needed to treat,NNT非随机同期对照试验non-randomized concurrent control trial 分层随机化stratified randomization分类变量categorical variable风险(危险度)risk干扰co-intervention工作偏倚Workup bias固定效应模型fixed effect model国际临床流行病学网International Clinical Epidemiology Network, INCLEN灰色文献grey literature后效评价reevaluation获益benefit机会结chance node疾病谱偏倚Spectrum bias技术特性Technical properties加权均数差weighted mean difference, WMD 假阳性率(误诊率)false positive rate假阴性率(漏诊率)false negative rate简单随机化simple randomization检索策略search strategy交叉对照研究(交叉设计)crossover design 经济学分析economic analysis经济学特性Economic attributes or impacts经验医学empirical medicine精确性precision决策结decision node决策树分析decision tree analysis绝对获益增加率absolute benefit increase, ABI 绝对危险度降低率absolute risk reduction, ARR 绝对危险度增加率absolute risk increase, ARI 可重复性repeatability,reproducibility可靠性(信度)reliability可信区间confidence interval ,CI可信限confidence limit ,CLLogistic回归模型Logistic regression model历史性对照研究historical control trial利弊比likelihood of being helped vs harmed, LHH连续性变量continuous variable临床对照试验controlled clinical trial, CCT临床结局clinical outcome临床经济学clinical economics临床决策分析clinical decision analysis临床流行病学clinical epidemiology, CE临床实践指南clinical practice guidelines, CPG临床试验clinical trial临床研究证据clinical research evidence临床证据clinical evidence临床证据手册handbook of clinical evidence零点Zero time灵活性flexibility临界点Cut off points漏斗图funnel plots率差(或危险差)rate difference,risk difference,RDMeta-分析Meta-analysis敏感度sensitivity敏感性分析sensitivity analysis墨克手册Merck manual脑卒中病房Stroke Unit内在真实性internal validity偏倚bias起始队列inception cohort前-后对照研究before-after study前景问题foreground questions区组随机化block randomization散点图scatter plots森林图forest plots伤残调整寿命年disability adjusted life year,DALY 生存曲线survival curves生存时间survival time生存质量(生活质量)quality of life世界卫生组织World Health Organization, WHO失安全数fail-Safe Number试验组某事件发生率experimental event rate,EER 似然比likelihood Ratio, LR适用性applicability受试者工作特征曲线(ROC曲线)receiver operator characteristic curve 随机对照临床试验randomized clinical trials, RCT随机对照试验randomized control trial, RCT随机化隐藏randomization concealment随机效应模型random effect model特异度specificity同行评价colleague evaluation统计效能(把握度)power同质性检验tests for homogeneity外在真实性external validity完成治疗分析per protocol,PP腕管综合征carpal tunnel syndrome, CTS卫生技术health technology卫生技术评估health technology assessment, HTA系统评价systematic review, SR相对获益增加率relative benefit increase, RBI相对危险度relative risk,RR相对危险度降低率relative risk reduction, RRR相对危险度增加率relative risk increase, RRI效果effectiveness效力efficacy效应尺度effect magnitude效应量effect size序贯试验sequential trial选择性偏倚selection bias循证儿科学evidence-based pediatrics循证妇产科学evidence-based gynecology & obstetrics 循证购买evidence-based purchasing循证护理evidence-based nursing循证决策evidence-based decision-making循证内科学evidence-based internal medicine循证筛选evidence-based selection循证外科学evidence-based surgery循证卫生保健evidence-based health care循证诊断evidence-based diagnosis循证医学evidence-based medicine, EBM亚组分析subgroup analysis严格评价critical appraisal验后比post-test odds验后概率post-test probability验前比pre-test odds验前概率pre-test probability阳性预测值positive predictive value原始研究primary studies异质性检验tests for heterogeneity意向治疗分析intention-to-treat, ITT阴性预测值negative predictive value引用偏倚citation bias尤登指数Youden’s index语言偏倚language bias预后prognosis预后因素prognostic factor预后指数prognostic index原始研究证据primary research evidence原始研究证据来源primary resources沾染contamination真实性(效度)validity诊断参照标准reference standard of diagnosis。
cochrane纳入的RCT文献质量评价(风险偏倚评估工具)中英文对照版

交替或循环
出生日期
病历号
其它明确的非隐藏过程
风险未知
没有足够信息判断为低风险或高风险。通常因分配隐藏的方法未描述或描述不充分。例如描述为使用信封分配,但为描述信封是否透明?密封?顺序编号?
对参与者和实施者的盲法
因参与者和实施者了解干预情况而导致实施偏倚
低风险判断标准
参与者以及纳入参与者的研究者因以下掩盖分配的方法或相当的方法,事先不了解分配情况
中心分配(包括电话,网络,药房控制随机)
相同外形的顺序编号的药物容器;
顺序编号、不透明、密封的信封
高风险判断标准
参与者以及纳入参与者的研究者可能事先知道分配,因而引入选择偏倚,譬如基于如下方法的分配:
使用摊开的随机分配表(如随机序列清单)
Selectionbias(biasedallocationtointerventions)duetoinadequateconcealmentofallocationspriortoassignment.
Performancebias.
BlindingofparticipantsandpersonnelAssessmentsshouldbemadeforeachmainoutcome(orclassofoutcomes).?
可能存在偏倚风险,但存在以下两种中的一种
没有足够信息评估是否存在其它重要的偏倚风险
没有足够的证据认为发现的问题会引入偏倚
summaryassessmentsoftheriskofbiasforeachimportantoutcome(acrossdomains)withinandacrossstudies
cochrane纳入的RCT文献质量评价英文原版

If particular questions/entries were pre-specified in the review’s protocol, responses should be provided for each question/entry.
Bias due to problems not covered elsewhere in the table.
Domain
Support for judgement
Review authors’ judgement
Selection bias.
Random sequence generation.
Describe the method used to generate the allocation sequence in sufficient detail to allow an assessment of whether it should produce comparable groups.
Detection bias due to knowledge of the allocated interventions by outcome assessors.
Attrition bias.
cochrane纳入的RCT文献质量评价(风险偏倚评估工具)中英文对照版
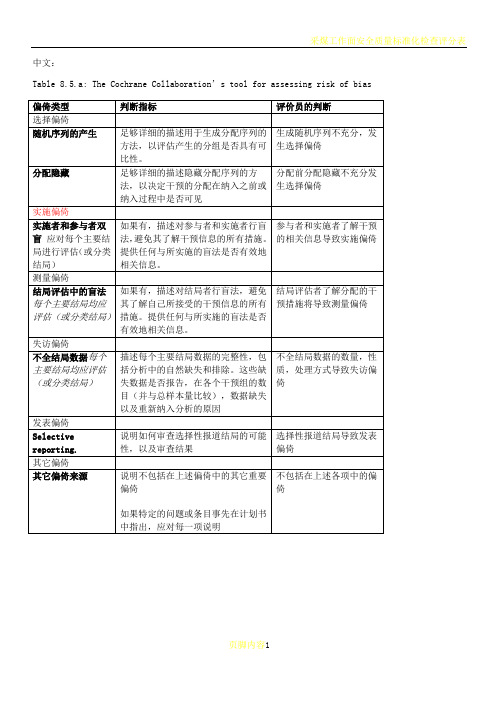
中文:Table 8.5.a: The Cochrane Collaboration’s tool for assessing risk of biasTable 8.5.d: Criteria for judging risk of bias in the ‘Risk of bias’ assessment tool研究者描述随机序列产生过程譬如:参考随机数字表使用计算机随机数字生成器扔硬币洗牌的卡片和信封掷骰子抽签最小化*最小化,可实现无随机元素,被认为相当于是随机的。
研究者描述序列的产生使用的是非随机的方法。
通常是系统的非随机方法,例如:通过奇偶或出生日期产生序列通过入院日期产生序列通过类似住院号或门诊号产生序列相对于上面提到的系统方法,其它非随机的方法少见的多,也更明显。
通常包括对参与者进行判断或非随机的方法,例如:临床医生判断如何分配参与者判断如何分配基于实验室检查或系列测试的结果分配基于干预的可获取性进行分配中心分配(包括电话,网络,药房控制随机)相同外形的顺序编号的药物容器;顺序编号、不透明、密封的信封参与者以及纳入参与者的研究者可能事先知道分配,因而引入选择偏倚,譬如基于如下方法的分配:使用摊开的随机分配表(如随机序列清单)分发信封但没有合适的安全保障(如透明、非密封、非顺序编号)交替或循环出生日期病历号其它明确的非隐藏过程任何如下标准:无盲法或盲法不充分,但系统评价员判断结局不太可能受到缺乏盲法的影响参与者和主要实施者均实施可靠的盲法,且盲法不太可能被打破任何如下标准:无盲法或盲法不充分,但系统评价员判断结局很可能受到缺乏盲法的影响尝试对关键的参与者和实施者行盲法,但盲法很可能被打破,结局很可能受到缺乏盲法的影响任何如下标准:没有足够信息判断为低风险或高风险研究未描述此情况任何如下标准:无盲法或盲法不充分,但系统评价员判断结局不太可能受到缺乏盲法的影响参与者和主要实施者均实施可靠的盲法,且盲法不太可能被打破任何如下标准:无盲法或盲法不充分,但系统评价员判断结局很可能受到缺乏盲法的影响尝试对关键的参与者和实施者行盲法,但盲法很可能被打破,结局很可能受到缺乏盲法的影响任何如下标准:没有足够信息判断为低风险或高风险研究未描述此情况任何如下标准:无缺失数据缺失数据的产生不大可能与真实结局相关(对于生存数据,删失不大可能引入偏倚)缺失数据的数目在各干预组相当,且各组缺失原因类似对二分类变量,与观察事件的发生风险相比,缺失比例不足以影响预估的干预效应对连续性结局数据,缺失数据的合理效应规模(均数差或标准均数差)不会大到影响观察的效应规模;缺失的数据用合适的方法进行估算任何如下标准:缺失数据的产生很大可能与真实结局相关, 缺失数据的数目及缺失原因在各干预组相差较大对二分类变量,与观察事件的发生风险相比,缺失比例足以影响预估的干预效应对连续性结局数据,缺失数据的合理效应规模(均数差或标准均数差)足以影响观察的效应规模;意向治疗分析中存在实际干预措施与随机分配的干预相违背的情况对缺失数据进行简单的不合适的估算任何如下标准:没有报道缺失或排除的情况,无法判断高风险或低风险(如未说明随机的数量,未提供数据缺失的原因)研究未描述此情况任何如下标准:实验的计划书可获取,系统评价感兴趣的所有首要或次要结局均按计划书预先说明的方式报道实验计划书不可得,但很明显发表的报告包括所有的结局,包括预先说明的结局(这种性质的有说服力的文字可能少见)任何如下标准:不是所有的预先说明的首要结局均被报道一个或多个首要结局为采用预先说明的测量方法、分析方法或数据子集来报道系统评价感兴趣的一个或多个首要结局报道不全,以至于不能纳入meta分析研究未报道此研究应当包含的主要关键结局具有与特殊试验设计相关的潜在偏倚来源或被指欺诈或其它问题可能存在偏倚风险,但存在以下两种中的一种没有足够信息评估是否存在其它重要的偏倚风险没有足够的证据认为发现的问题会引入偏倚Table 8.7.a: Possible approach for summary assessments of the risk of bias for each important outcome (across domains) within and across studies英文:Table 8.5.a: The Cochrane Collaboration’s tool for assessing risk of biasTable 8.5.d: Criteria for judging risk of bias in the ‘Risk of bias’ assessment toolprocess such as:Referring to a random number table;Using a computer random number generator;Coin tossing;Shuffling cards or envelopes;Throwing dice;Drawing of lots;Minimization*.*Minimization may be implemented without a random element, and this isconsidered to be equivalent to being random.judgement The investigators describe a non-random component in the sequence generation process. Usually, the description would involve somesystematic, non-random approach, for example:Sequence generated by odd or even date of birth;Sequence generated by some rule based on date (or day) of admission;Sequence generated by some rule based on hospital or clinic recordnumber.Other non-random approaches happen much less frequently than thesystematic approaches mentioned above and tend to be obvious. Theyusually involve judgement or some method of non-random categorization ofparticipants, for example:Allocation by judgement of the clinician;Allocation by preference of the participant;Allocation based on the results of a laboratory test or a seriesof tests;Allocation by availability of the intervention.Criteria for a judgement Participants and investigators enrolling participants could not foreseeassignment because one of the following, or an equivalent method, was usedto conceal allocation:Central allocation (including telephone, web-based andpharmacy-controlled randomization);Sequentially numbered drug containers of identical appearance;Sequentially numbered, opaque, sealed envelopes.judgement Participants or investigators enrolling participants could possiblyforesee assignments and thus introduce selection bias, such as allocationbased on:Using an open random allocation schedule (e.g. a list of randomnumbers);Assignment envelopes were used without appropriate safeguards(e.g. if envelopes were unsealed or nonopaque or not sequentiallynumbered);Alternation or rotation;Date of birth;Case record number;Any other explicitly unconcealed procedure.Criteria for a judgement Any one of the following:No blinding or incomplete blinding, but the review authors judgethat the outcome is not likely to be influenced by lack of blinding;Blinding of participants and key study personnel ensured, andunlikely that the blinding could have been broken.judgementAny one of the following:No blinding or incomplete blinding, and the outcome is likely tobe influenced by lack of blinding;Blinding of key study participants and personnel attempted, butlikely that the blinding could have been broken, and the outcomeis likely to be influenced by lack of blinding.judgement ‘Unclear risk’ ofAny one of the following:Insufficient information to permit judgement of ‘Low risk’ or ‘High risk’;The study did not address this outcome.Criteria for a judgement Any one of the following:No blinding of outcome assessment, but the review authors judge thatthe outcome measurement is not likely to be influenced by lack ofblinding;Blinding of outcome assessment ensured, and unlikely that theblinding could have been broken.judgementAny one of the following:No blinding of outcome assessment, and the outcome measurement islikely to be influenced by lack of blinding;Blinding of outcome assessment, but likely that the blinding couldhave been broken, and the outcome measurement is likely to beinfluenced by lack of blinding.judgement ‘Unclear risk’ ofAny one of the following:Insufficient information to permit judgement of ‘Low risk’ or‘High risk’;The study did not address this outcome.Criteria for a judgement Any one of the following:No missing outcome data;Reasons for missing outcome data unlikely to be related to trueoutcome (for survival data, censoring unlikely to be introducingbias);Missing outcome data balanced in numbers across interventiongroups, with similar reasons for missing data across groups;For dichotomous outcome data, the proportion of missing outcomescompared with observed event risk not enough to have a clinicallyrelevant impact on the intervention effect estimate;For continuous outcome data, plausible effect size (difference inmeans or standardized difference in means) among missing outcomesnot enough to have a clinically relevant impact on observed effectsize;Missing data have been imputed using appropriate methods.judgement Any one of the following:Reason for missing outcome data likely to be related to trueoutcome, with either imbalance in numbers or reasons for missingdata across intervention groups;For dichotomous outcome data, the proportion of missing outcomescompared with observed event risk enough to induce clinicallyrelevant bias in intervention effect estimate;For continuous outcome data, plausible effect size (difference inmeans or standardized difference in means) among missing outcomesenough to induce clinically relevant bias in observed effect size;‘As-treated’ analysis done with substantial departure of theintervention received from that assigned at randomization;Potentially inappropriate application of simple imputation.judgement ‘Unclear risk’ ofAny one of the following:Insufficient reporting of attrition/exclusions to permit judgement of ‘Low risk’ or ‘High risk’ (e.g. number ran domized not stated,no reasons for missing data provided);The study did not address this outcome.Criteria for a judgement Any of the following:The study p rotocol is available and all of the study’spre-specified (primary and secondary) outcomes that are of interestin the review have been reported in the pre-specified way;The study protocol is not available but it is clear that thepublished reports include all expected outcomes, including thosethat were pre-specified (convincing text of this nature may beuncommon).judgementAny one of the following:Not all of the study’s pre -specified primary outcomes have beenreported;One or more primary outcomes is reported using measurements,analysis methods or subsets of the data (e.g. subscales) that werenot pre-specified;One or more reported primary outcomes were not pre-specified(unless clear justification for their reporting is provided, suchas an unexpected adverse effect);One or more outcomes of interest in the review are reportedincompletely so that they cannot be entered in a meta-analysis;The study report fails to include results for a key outcome thatwould be expected to have been reported for such a study.judgementThere is at least one important risk of bias. For example, the study: Had a potential source of bias related to the specific study designused; orHas been claimed to have been fraudulent; orHad some other problem.judgement ‘Unclear risk’ ofThere may be a risk of bias, but there is either:Insufficient information to assess whether an important risk of bias exists; orInsufficient rationale or evidence that an identified problem willintroduce bias.Table 8.7.a: Possible approach for summary assessments of the risk of bias for each important outcome (across domains) within and across studies。
cochrne纳入RCT文献质量评价风险偏倚评估工具中英文对照
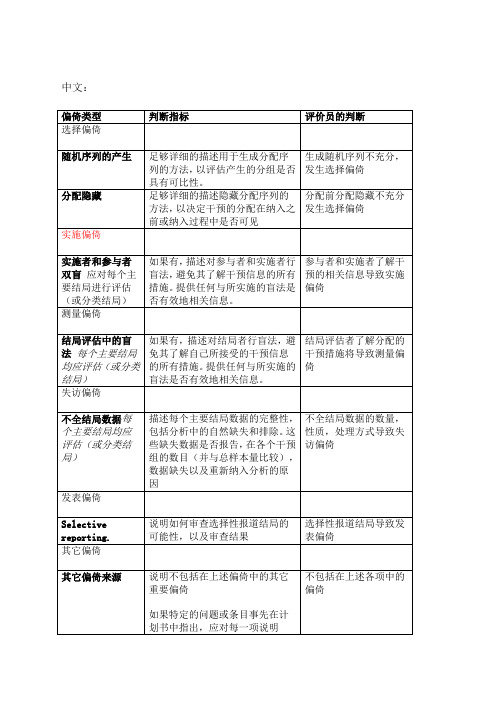
Detection bias.
Blinding of outcomeassessmentAssessments should be made for each main outcome (or class of outcomes).
Detection bias due to knowledgeof the allocated interventions by outcome assessors.
Attrition bias.
Incomplete outcome dataAssessments should be made for each main outcome (or class of outcomes).
Attrition bias due to amount, nature or handling of incomplete outcome data.
中文:
偏倚类型
判断指标
评价员的判断
选择偏倚
随机序列的产生
足够详细的描述用于生成分配序列的方法,以评估产生的分组是否具有可比性。
生成随机序列不充分,发生选择偏倚
分配隐藏
足够详细的描述隐藏分配序列的方法,以决定干预的分配在纳入之前或纳入过程中是否可见
分配前分配隐藏不充分发生选择偏倚
实施偏倚
实施者和参与者双盲应对每个主要结局进行评估(或分类结局)
Risk of bias
解释
对单个研究
对多个研究整体
Cochrane风险偏倚评估工具

Cochrane 偏倚风险评估工具水天之间2013年11月11日目录随机对照试验/临床对照试验 偏倚的来源偏倚风险评估工具的解读偏倚风险评价结果的总结 偏倚风险评估工具的软件实现 偏倚风险评估工具的实例Cochrane 手册将RCT (randomized controlled tril )和CCT (controlled clinical trial )进行了区分,判定标准为:1.在1个或多个患者中进行的一种研究;2.比较两种干预措施,试验措施可以为一种药物、外科手术、物理疗法、预防措施,对照措施为另一种药物、安慰剂或不做任何处理的空白对照;3.RCT 为采用随机分配方法如随机数字表法、计算机随机排序、抛硬币法等将受试者分入不同处理组,CCT 则为采用办随机分配法(按入院顺序、住院号、研究对象的生日的奇偶数交替分配)分配到对照或治疗组者;4.提示性术语有:随机(random )、交替(crossover/cross-over )或安慰剂(placebo )等。
符合这4条的文献将在美国国家医学图书馆(the US national library of medicine, NLM )指定其出版类型是RCT 或CCT ,并在取得NLM 的许可后纳入Cochrane 临床对照试验中心注册库(the Cochrane Central Register of Controlled Trials ,CENTRAL)选择性偏倚(selection bias ):发生在选择和分配研究对象时,因随机方法不完善造成的组间基线不可比,可夸大或缩小干预措施的疗效。
采用真正的随机方法并对随机进行分配隐藏可避免这类偏倚的影响。
实施偏倚(performance bias ):发生在干预措施的实施过程中,指除比较的措施外,向试验组和对照组对象提供的其他措施不一样。
标准化治疗方案和对研究对象及实施研究措施者采用盲法可避免实施偏倚。
Cochrane协作网的RCT偏倚风险评价工具
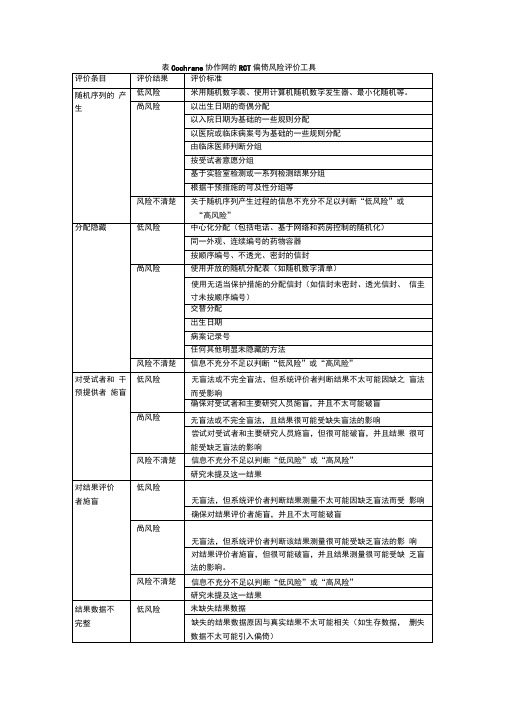
对于连续性结果数据,缺失结果数据中似真的效应大小(均数 差或标准均数差)足以对观测效应大小产生临床相关影响
米用 视为治疗(as-treated)分析,但改变随机入组时干预 措施的人数较多
可能不恰当地使用简单估算方法
风险不清楚
报告减员/排除的信息不充分不足以判断“低风险”或“高风 险'如随机人数未说明,未提供缺失数据的原因)
研究未提及这一结果
选择性结果 报告
低风险
有研究方案,且系统评价关心的方案中预先指定的(主要和次 要)结果指标均有报告
没有研究方案,但所有期望的结局指标,包括在发表文早中预 先指定的指标均有报告
风险不清楚
信息不充分不足以判断“低风险”或“高风险”。很可能大多
数研究都属于这一类别。
其他偏倚来 源
低风险
纳入研究看起来无其他偏倚来源
咼风险
至少有其中一个重要偏倚来源,如:
存在与使用的具体研究设计相关的潜在偏倚来源 声称有欺骗行为
有一些其他冋题
风险不清楚
信息不充分不足以判断是否存在重要偏倚风险
发现的问题是否导致偏倚,理由或依据不足
对结果评价者施盲,但很可能破盲,并且结果测量很可能受缺 乏盲法的影响。
风险不清楚
信息不充分不足以判断“低风险”或“高风险”
研究未提及这一结果
结果数据不
完整
低风险
未缺失结果数据
缺失的结果数据原因与真实结果不太可能相关(如生存数据, 删失数据不太可能引入偏倚)
缺失结果数据在各干预组的数量均衡,组间缺失数据具有相似 的原因
表Cochrane协作网的RCT偏倚风险评价工具
XXX纳入的RCT文献质量评价(风险偏倚评估工具)中英文对照版

XXX纳入的RCT文献质量评价(风险偏倚评估工具)中英文对照版根据XXX的“偏倚风险评估工具”,表8.5.a列出了评估偏倚类型的指标。
其中,选择偏倚包括评估随机序列的产生,以及对分组可比性的评估。
需要提供足够详细的描述,以便判断分组的产生是否具有可比性。
分配偏倚则需要提供足够详细的描述,以评估分配是否隐藏,并决定干预的分配是否可见。
实施偏倚则需要描述实施者和参与者是否采用了双盲方法,以避免其了解干预信息。
同时,需要提供与实施的盲法是否有效相关的信息。
测量偏倚则需要描述对结局者行盲法,避免其了解所接受的干预信息。
同时,需要提供与实施的盲法是否有效相关的信息。
失访偏差需要描述每个主要结局数据的完整性,以及缺失数据是否报告。
同时,需要说明重新纳入分析的原因。
发表偏差需要说明如何审查选择性报道结局的可能性,以及审查结果。
其他偏差则需要说明不包括在上述偏差中的其他重要偏差。
如果在计划书中指出了特定的问题或条目,需要对每一项进行说明。
表8.5.d列出了评估偏倚风险的标准。
其中,随机序列的产生不充分会导致选择偏差。
对于评判为低风险的标准,研究者需要描述随机序列产生的过程,例如参考随机数字表、使用计算机随机数字生成器、扔硬币、洗牌的卡片和信封、掷骰子、抽签、最小化等方法。
对于评判为高风险的标准,研究者需要描述使用的非随机方法,通常是系统的非随机方法,例如最小化,虽然可实现无随机元素,但被认为相当于是非随机的。
可能被打破,结局很可能受到缺乏盲法的影响风险未知任何如下标准:没有足够信息判断为低风险或高风险研究未描述此情况随机化是临床研究中重要的方法之一,但在实施随机化时,存在着一些潜在的风险和偏差。
在随机化的过程中,通常会采用系统方法或非随机的方法来产生序列。
其中,系统方法包括通过奇偶或出生日期、入院日期、住院号或门诊号等方式产生序列;非随机的方法则包括临床医生或参与者的判断、实验室检查或系列测试的结果、干预的可获取性等方式来分配。
(完整版)Cochrane协作网偏倚风险评价工具

表1 Cochrane协作网偏倚风险评价工具评价条目评价内容描述具体评价问题1.随机分配方法详细描述产生随机分配序列的方法,有助于评估组间可比性随机化分配序列的产生是否正确?2.分配方案隐藏详细描述隐藏随机分配序列的方法,从而帮助判断干预措施分配情况是否可预知分配方案是否有效地隐藏?3.盲法描述对受试者或试验人员实施盲法的方法,以防止他们知道受试者的干预措施,提供判断盲法是否成功的相关信息盲法是否完善?4.结果数据的完整性报告每个主要结局指标的数据完整性,包括失访和退出的数据。
明确是否报告以上信息及其原因,是否采用意向性分析(ITT)结果数据是否完整?5.选择性报告研究结果描述选择性报告结果的可能性及情况研究报告是否提示无选择性报告结果?6.其它偏倚来源除以上5个方面,是否存在其他引起偏倚的因素?若事先在计划中提到某个问题或因素,应在全文中作答研究是否存在引起高度偏倚风险的其他因素?表2 Cochrane协作网偏倚风险评价的具体标准评价条目评价结果评价内容描述1.随机分配方法正确♦采用随机数字表、计算机产生随机数字、抛硬币、掷骰子或抽签等方法不正确♦按患者生日、住院日或住院号等的末位数字的奇数或偶数;♦交替分配方法;♦根据医师、患者、实验室检查结果或干预措施的可获得性分配患者入组不清楚♦根据干预措施的可获得性;♦信息不详、难以判断正确与否2.方案隐藏完善♦中心随机,包括采用电话、网络和药房控制的随机♦按顺序编号或编码的相同容器♦按顺序编码、密封、不透光的信封不完善♦公开随机分配序列如列出随机数字♦未密封、透光或未按顺序编号的信封♦交替分配♦根据住院号、生日等末位数字的奇数或偶数不清楚♦未提及分配方案隐藏♦提供的信息不能判断是否完善,如使用信封,但未描述是否按顺序编码、密封、不透光3.盲法正确♦没有采用盲法,但结果判断和测量不会受影响♦对患者和主要研究人员采用盲法,且盲法不会被破坏♦对结果测量者采用盲法,未对患者和主要研究人员采用盲法,但不会导致偏倚不正确♦未采用盲法或盲法不完善,结果判断或测量会受影响♦对患者和主要研究人员采用盲法,但盲法可能被破坏♦对患者和主要研究人员均未采用盲法,可能导致偏倚不清楚♦信息不全,难以判断是否正确♦文中未提及盲法4.结果数据的完整性完整♦无缺失数据;缺失数据不影响结果分析(生存分析中缺失值)♦组间缺失的人数和原因相似♦缺失数据不足以对效应值产生重要影响;缺失数据采用恰当方法赋值不完整♦组间缺失的人数和原因不平衡♦缺失数据足以对效应值产生重要影响♦采用“as-treated”分析,但改变随机入组时干预措施的人数较多♦不恰当应用简单赋值不清楚♦信息不全,难以判断数据是否完整(缺失人数或原因未报告)♦文中未提及数据完整性问题5.选择性报告研究结果无选择性报告♦有研究方案,且系统综述关心的方案中预告指定的结果指标(主要和次要结果)均有报告♦没有研究方案,但所有期望的结局指标,包括在发表文献中预先指定的指标均有报告有选择性报告♦未报告所有预先指定的主要结局指标♦报告的一个或多个主要结局指标采用预先未指定的测量和分析方法♦报告的一个或多个主要结局指标未预先指定♦系统综述关心的一个或多个结局指标报告不完善,以致不能纳入行Meta分析♦未报告重要的结局指标不清楚♦信息不全、难以判断6.其他偏倚来源无♦纳入研究无其他偏倚来源有至少存在一种重要偏倚风险:♦与使用的研究设计方案相关的偏倚♦研究提前终止(数据原因或正规终止原因)♦基线明显不平衡♦声称有欺骗行为♦其他问题不清楚♦信息不全,难以判断是否存在重要偏倚♦发现的问题是否导致偏倚,理由或依据不足。
cochrane纳入的RCT文献质量评价(风险偏倚评估工具)中英文对照版讲解学习

缺失数据的产生不大可能与真实结局相关(பைடு நூலகம்于生存数据,删失不大可能引入偏倚)
缺失数据的数目在各干预组相当,且各组缺失原因类似
对二分类变量,与观察事件的发生风险相比,缺失比例不足以影响预估的干预效应
对连续性结局数据,缺失数据的合理效应规模(均数差或标准均数差)不会大到影响观察的效应规模;
缺失的数据用合适的方法进行估算
因参与者和实施者了解干预情况而导致实施偏倚
偏倚低风险标准
任何如下标准:
无盲法或盲法不充分,但系统评价员判断结局不太可能受到缺乏盲法的影响
参与者和主要实施者均实施可靠的盲法,且盲法不太可能被打破
偏倚高风险标准
任何如下标准:
无盲法或盲法不充分,但系统评价员判断结局很可能受到缺乏盲法的影响
尝试对关键的参与者和实施者行盲法,但盲法很可能被打破,结局很可能受到缺乏盲法的影响
实验计划书不可得,但很明显发表的报告包括所有的结局,包括预先说明的结局(这种性质的有说服力的文字可能少见)
高风险判断标准
任何如下标准:
不是所有的预先说明的首要结局均被报道
随机序列的产生
随机序列产生不充分导致选择偏倚
判断为低风险的标准
研究者描述随机序列产生过程譬如:
参考随机数字表
使用计算机随机数字生成器
扔硬币
洗牌的卡片和信封
掷骰子
抽签
最小化
*最小化,可实现无随机元素,被认为相当于是随机的。
判断为高风险的标准
研究者描述序列的产生使用的是非随机的方法。通常是系统的非随机方法,例如:
其它偏倚
其它偏倚来源
说明不包括在上述偏倚中的其它重要偏倚
如果特定的问题或条目事先在计划书中指出,应对每一项说明
cochrane纳入的RCT文献质量评价(风险偏倚评估工具)中英文对照版..

中文:Table 8.5.a: The Cochrane s tool for assessing riskTable 8.5.d: Criteria for judging risk ofbias in the assessment tool Risk of bias分配隐藏分配前不充足的分配隐藏导致选择偏倚Table 8.7.a: Possible approach for summarya ssessments of the risk of bias for each important outcome (across domains) within and across studies英文:Table 8.5.a: The Cochrane Collaboration ' s tool for assessing risk of biasTable 8.5.d: Criteria for judging risk of bias in the ‘Risk of bias ' assessment toolriskorsOTHER BIASTable 8.7.a: Possible approach for summary assessments of the risk of bias foreach important outcome (across domains) within and across studiesthose that were pre-specified (convincing text of this naturemay be uncommon).Criteria for theudgement o f ‘Highrisk of bias. Any one of the following: ' Not all of the study'-spse pcrifeied primary outcomes havebeen reported; One or more primary outcomes is reported using measurements,analysis methods or subsets of the data (e.g. subscales) thatwere not pre-specified;One or more reported primary outcomes were not pre-specified(unless clear justification for their reporting is provided,such as an unexpected adverse effect);One or more outcomes of interest in the review are reportedincompletely so that they cannot be entered in a meta-analysis;The study report fails to include results for a key outcomethat would be expected to have been reported for such a study.Criteria for the udgement of ‘ Unclear isk ' of bias.Insufficient information to permit judgement of ‘Low risk ' or ‘Hi It is likely that the majority of studies will fall into this category.gh risk。
cochrane纳入的RCT文献质量评价英文原版

Performance bias.
Blinding of participants and personnelAssessments should be made for each main outcome (or class of outcomes).
ALLOCATION CONCEALMENT
Selection bias (biased allocation to interventions) due to inadequate concealment of allocations prior to assignment.
Criteria for a judgement of ‘Low risk’ of bias.
Detection bias due to knowledge of the allocated interventions by outcome assessors.
Attrition bias.
Incomplete outcome dataAssessments should be made for each main outcome (or class of outcomes).
RANDOM SEQUENCE GENERATION
Selection bias (biased allocation to interventions) due to inadequate generation of a randomised sequence.
cochrane纳入的RCT文献质量评价(风险偏倚评估工具)中英文对照版..

cochrane纳⼊的RCT⽂献质量评价(风险偏倚评估⼯具)中英⽂对照版..中⽂:Table 8.5.a: The Cochrane s tool for assessing riskTable 8.5.d: Criteria for judging risk ofbias in the assessment tool Risk of bias分配隐藏分配前不充⾜的分配隐藏导致选择偏倚Table 8.7.a: Possible approach for summarya ssessments of the risk of bias for each important outcome (across domains) within and across studies英⽂:Table 8.5.a: The Cochrane Collaboration ' s tool for assessing risk of biasTable 8.5.d: Criteria for judging risk of bias in the ‘Risk of bias ' assessment toolriskorsOTHER BIASTable 8.7.a: Possible approach for summary assessments of the risk of bias foreach important outcome (across domains) within and across studiesthose that were pre-specified (convincing text of this naturemay be uncommon).Criteria for theudgement o f ‘Highrisk of bias. Any one of the following: ' Not all of the study'-spse pcrifeied primary outcomes havebeen reported; One or more primary outcomes is reported using measurements,analysis methods or subsets of the data (e.g. subscales) thatwere not pre-specified;One or more reported primary outcomes were not pre-specified(unless clear justification for their reporting is provided,such as an unexpected adverse effect);One or more outcomes of interest in the review are reportedincompletely so that they cannot be entered in a meta-analysis;The study report fails to include results for a key outcomethat would be expected to have been reported for such a study.Criteria for the udgement of ‘ Unclear isk ' of bias.Insufficient information to permit judgement of ‘Low risk ' or ‘Hi It is likely that the majority of studies will fall into this category. gh risk。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
随机序列的产生
随机序列产生不充分导致选择偏倚
判断为低风险的标准
研究者描述随机序列产生过程譬如:
参考随机数字表
使用计算机随机数字生成器
Selection bias (biased allocation to interventions) due to inadequate generation of a randomised sequence.
Allocation concealment.
Describe the method used to conceal the allocation sequence in sufficient detail to determine whether intervention allocations could have been foreseen in advance of, or during, enrolment.
测量偏倚
结局评估中的盲法每个主要结局均应评估(或分类结局)
如果有,描述对结局者行盲法,避免其了解自己所接受的干预信息的所有措施。提供任何与所实施的盲法是否有效地相关信息。
结局评估者了解分配的干预措施将导致测量偏倚
失访偏倚
不全结局数据每个主要结局均应评估(或分类结局)
描述每个主要结局数据的完整性,包括分析中的自然缺失和排除。这些缺失数据是否报告,在各个干预组的数目(并与总样本量比较),数据缺失以及重新纳入分析的原因
Selection bias (biased allocation to interventions) due to inadequate concealment of allocations prior to assignment.
Performance bias.
Blinding of participants and personnelAssessments should be made for each main outcome (or class of outcomes).
缺失数据的数目在各干预组相当,且各组缺失原因类似
对二分类变量,与观察事件的发生风险相比,缺失比例不足以影响预估的干预效应
对连续性结局数据,缺失数据的合理效应规模(均数差或标准均数差)不会大到影响观察的效应规模;
缺失的数据用合适的方法进行估算
高风险判断标准
任何如下标准:
缺失数据的产生很大可能与真实结局相关,缺失数据的数目及缺失原因在各干预组相差较大
参与者和主要实施者均实施可靠的盲法,且盲法不太可能被打破
偏倚高风险标准
任何如下标准:
无盲法或盲法不充分,但系统评价员判断结局很可能受到缺乏盲法的影响
尝试对关键的参与者和实施者行盲法,但盲法很可能被打破,结局很可能受到缺乏盲法的影响
风险未知
任何如下标准:
没有足够信息判断为低风险或高风险
研究未描述此情况
尝试对关键的参与者和实施者行盲法,但盲法很可能被打破,结局很可能受到缺乏盲法的影响
风险未知
任何如下标准:
没有足够信息判断为低风险或高风险
研究未描述此情况
结局数据不完整
不全结局数据的数量,性质,处理方式导致失访偏倚
偏倚低风险标准
任何如下标准:
无缺失数据
缺失数据的产生不大可能与真实结局相关(对于生存数据,删失不大可能引入偏倚)
研究应未引入其它来源的偏倚
高风险判断标准
至少有一种重要的偏倚风险,例如:
具有与特殊试验设计相关的潜在偏倚来源
或被指欺诈
或其它问题
风险未知
可能存在偏倚风险,但存在以下两种中的一种
没有足够信息评估是否存在其它重要的偏倚风险
没有足够的证据认为发现的问题会引入偏倚
Table 8.7.a: Possible approach forsummary assessmentsof the risk of bias for each important outcome (across domains) within and across studies
Describe the completeness of outcome data for each main outcome, including attrition and exclusions from the analysis. State whether attrition and exclusions were reported, the numbers in each intervention group (compared with total randomized participants), reasons for attrition/exclusions where reported, and any re-inclusions in analyses performed by the review authors.
Risk of bias
解释
对单个研究
对多个研究整体
Low risk of bias.
合理的偏倚不太可能严重改变结果
每一类偏倚均为低风险
绝大多数信息均来自偏倚低风险的研究
Unclear risk of bias.
合理的偏倚会对结果产生一定的怀疑
一类或多类偏倚风险未知
绝大多数信息均来自偏倚低风险或风险未知的研究
对二分类变量,与观察事件的发生风险相比,缺失比例足以影响预估的干预效应
对连续性结局数据,缺失数据的合理效应规模(均数差或标准均数差)足以影响观察的效应规模;
意向治疗分析中存在实际干预措施与随机分配的干预相违背的情况
对缺失数据进行简单的不合适的估算
风险未知
任何如下标准:
没有报道缺失或排除的情况,无法判断高风险或低风险(如未说明随机的数量,未提供数据缺失的原因)
Describe all measures used, if any, to blind outcome assessors from knowledge of which intervention a participant received. Provide any information relating to whether the intended blinding was effective.
扔硬币
洗牌的卡片和信封
掷骰子
抽签
最小化
*最小化,可实现无随机元素,被认为相当于是随机的。
判断为高风险的标准
研究者描述序列的产生使用的是非随机的方法。通常是系统的非随机方法,例如:
通过奇偶或出生日期产生序列
通过入院日期产生序列
通过类似住院号或门诊号产生序列
相对于上面提到的系统方法,其它Байду номын сангаас随机的方法少见的多,也更明显。通常包括对参与者进行判断或非随机的方法,例如:
Review authors’ judgement
Selection bias.
Random sequence generation.
Describe the method used to generate the allocation sequence in sufficient detail to allow an assessment of whether it should produce comparable groups.
不全结局数据的数量,性质,处理方式导致失访偏倚
发表偏倚
Selective reporting.
说明如何审查选择性报道结局的可能性,以及审查结果
选择性报道结局导致发表偏倚
其它偏倚
其它偏倚来源
说明不包括在上述偏倚中的其它重要偏倚
如果特定的问题或条目事先在计划书中指出,应对每一项说明
不包括在上述各项中的偏倚
High risk of bias.
偏倚严重削弱结果的可信度
一类或多类偏倚为高风险
来自高偏倚风险研究的信息比例足以影响结果的解释
英文:
Table8.5.a: The Cochrane Collaboration’s tool for assessing risk of bias
Domain
Support for judgement
中文:
Table 8.5.a: The Cochrane Collaboration’s tool for assessing risk of bias
偏倚类型
判断指标
评价员的判断
选择偏倚
随机序列的产生
足够详细的描述用于生成分配序列的方法,以评估产生的分组是否具有可比性。
生成随机序列不充分,发生选择偏倚
研究未描述此情况
选择性发表
选择性发表导致发表偏倚
偏倚低风险标准
任何如下标准:
实验的计划书可获取,系统评价感兴趣的所有首要或次要结局均按计划书预先说明的方式报道
实验计划书不可得,但很明显发表的报告包括所有的结局,包括预先说明的结局(这种性质的有说服力的文字可能少见)
高风险判断标准
任何如下标准:
不是所有的预先说明的首要结局均被报道
Detection bias due to knowledge of the allocated interventions by outcome assessors.
Attrition bias.
Incomplete outcome dataAssessments should be made for each main outcome (or class of outcomes).
中心分配(包括电话,网络,药房控制随机)
