乙酰乙酸乙酯的合成
乙酰乙酸乙酯的合成

⼄酰⼄酸⼄酯的合成⼄酰⼄酸⼄酯的合成学院:化⼯与材料学院班级:B1201姓名:康丽霞学号:15111201061 分⼦结构2 基本信息3物性数据1. 性状:⽆⾊液体,有芳⾹味。
2. 沸点(oC,101.3kPa):1813. 熔点(oC,酮式):-394. 熔点(oC,烯醇式):-445. 相对密度(g/mL,25/4oC):1.021266. 相对蒸汽密度(g/mL,空⽓=1):4.57. 折射率(20oC):1.41948. 黏度(mPa·s,25oC):1.50819. 闪点(oC,闭⼝):84.410. 燃点(oC):29511. 燃烧热(KJ/mol,25oC):3162.712. ⽐热容(KJ/(kg·K),24.5oC,定压):1.9213. 临界温度(oC):40014. 电导率(S/m,25oC):1×10-715. 蒸⽓压(kPa,40~41oC):0.2716. 热导率(W/(m·K),30oC):0.155817. 溶解性:微溶于⽔,溶于有机溶剂。
25℃时在⽔中溶解12%;⽔在⼄酰⼄酸⼄酯中溶解4.9%。
18. 相对密度(20℃,4℃):1.028219. 液相标准热熔(J·mol-1·K-1) :251.420. ⽓相标准燃烧热(焓)(kJ·mol-1):-3228.521. ⽓相标准声称热(焓)( kJ·mol-1) :-561.774 存储⽅法1.应远离⽕源置阴凉通风处贮存。
2.本品⽤铝桶包装,桶盖密封性要好,贮于阴凉通风处,防⽕。
按易燃有毒化学品规定贮运5 合成⽅法1. 双⼄烯酮与⼄醇酯化法双⼄烯酮和⽆⽔⼄醇在浓硫酸催化下进⾏酯化,得⼄酰⼄酸⼄酯粗品。
再经减压精馏得成品。
2.⼄酸⼄酯⾃缩合法由两分⼦⼄酸⼄酯在⾦属钠存在下⾃缩合⽽得。
2. 由⼄酸⼄酯在⼄醇钠存在下缩合后蒸馏⽽得。
由双⼄烯酮与⽆⽔⼄醇在浓硫酸催化下酯化后减压蒸馏⽽得。
乙酰乙酸乙酯的制备

酮式与烯醇式的互变异构:
O C H3C C H2 O C OEt H3C C C H C OEt H O O
酮式 ,92%
烯醇式 ,8%
bp: 41℃/266Pa(2mmHg)
33℃/266Pa
由上述反应机理看出,反应要求: 1.仪器、药品均需干燥,严格无水。 2.第一步反应中C2H5O-的多少由钠决定,故整个反应以钠 为基准。 3. 由于乙酰乙酸乙酯分子中亚甲基上的氢比乙醇的酸性 强的多(pKa =10.65),所以脱醇反应后生成的是乙酰乙酸
CH3COCH2COOC2H5 + NaOAc + CH3CH2OH
• Claisen酯缩合反应1887年由L.Claisen首先发现
• R.L.Claisen(1851-1930)生于德国科隆,曾在波恩大学 从师于凯库勒,博士毕业成为Kekule助手。在维勒(Wohl er)实验室短期学习。 1886年在慕尼黑于Von Baeyer指
常压蒸馏除乙酸乙酯等低沸点物质
降温至50以下 然后减压蒸馏 乙酸乙酯 回收处理
沸点(压力/mmHg) 300 压力(mmHg)
沸点(760mmHg) 400 2003 40 0 50 8 10 0 0
如:某化合物在常压(760mmHg)时沸点300℃, 则在12mmHg时沸点约160℃;
2—(3—硝基亚苄基)乙酰乙酸乙酯的合成

2—(3—硝基亚苄基)乙酰乙酸乙酯的合成2-(3-硝基苯基)乙酰乙酸乙酯的合成可以通过以下步骤实现:
1.将苯甲酸与乙酸酐反应得到苯乙酸乙酯。
2.将苯乙酸乙酯与溴乙酸乙酯在碱性条件下反应,得到2-溴乙酸苯乙酯。
3.将2-溴乙酸苯乙酯与硝酸在硫酸催化下反应,得到2-(3-硝基苯基)乙酸苯乙酯。
4.最后,将2-(3-硝基苯基)乙酸苯乙酯与乙酸乙酯和碳酸钾在无水乙醇中加热回流反应,得到目标产物2-(3-硝基苯基)乙酰乙酸乙酯。
整个合成过程中需要注意反应条件和操作方法,保证反应的高效和产物的纯度。
1/ 1。
乙酰乙酸乙酯的合成方程式

乙酰乙酸乙酯的合成方程式乙酰乙酸乙酯是一种常见的有机溶剂,也是一种重要的合成原料,它的合成方程式如下:CH3COOCH2CH3 + HCl → CH3COOH + CH3CH2ClCH3COOH + CH3CH2OH → CH3COOCH2CH3 + H2O上述合成方程式是乙酰乙酸乙酯的两步反应过程。
一、原料准备1. 乙酸乙酯(CH3COOCH2CH3)是由乙酸和乙醇经过酯化反应得到的化合物。
它是一种透明无色液体,带有类似于甜酸味的气味。
乙酸和乙醇的化学式分别为CH3COOH和CH3CH2OH。
2. 氯化乙烷(CH3CH2Cl)氯化乙烷是一种有机化合物,分子式为CH3CH2Cl。
它是一种无色气体,在常温常压下常温沸热。
氯化乙烷是制备乙酰乙酸乙酯的重要原料之一。
二、反应步骤制备乙酰乙酸乙酯需要两步反应,第一步是氯化乙烷与乙酸乙酯发生酯化反应,生成乙酸和氯化乙基。
CH3COOCH2CH3 + HCl → CH3COOH + CH3CH2Cl第二步是乙酸和乙醇发生酯化反应,生成乙酰乙酸乙酯和水。
CH3COOH + CH3CH2OH → CH3COOCH2CH3 + H2O三、反应条件该反应需要在适宜的反应条件下进行,具体条件如下:1. 酯化反应条件:反应时间:2-4小时反应温度:60-80℃反应物比例:1:1.2(乙酸乙酯:氯化乙烷)酯化反应催化剂:HCl2. 酯交换反应条件:反应时间:3-4小时反应温度:70-80℃反应物比例:1:1(乙酸:乙醇)酯交换反应催化剂:硫酸、盐酸等四、反应机理1. 酯化反应机理酯化反应是一种酸催化反应,HCl催化剂可以将氯离子引入乙酸乙酯中,使其易于与氯化乙烷进行反应,产生水和氯化乙基。
同时,水也可以与氯化乙基反应,生成HCl和乙醇。
这个平衡反应可以通过蒸馏来实现。
2. 酯交换反应机理酯交换反应也是一种酸催化反应,硫酸或盐酸可以抑制乙酸与水的反应,从而使乙酸和乙醇之间发生酯化反应,生成乙酰乙酸乙酯和水。
乙酰乙酸乙酯的制备 实验报告

乙酰乙酸乙酯的制备前言:乙酰乙酸乙酯,无色至淡黄色的澄清液体.微溶于水,易溶于乙醚,乙醇。
有刺激性和麻醉性。
可燃,遇明火、高热或接触氧化剂有发生燃烧的危险。
有醚样和苹果似的香气。
广泛应用于食用香精中,主要用以调配苹果、杏、桃等食用香精.制药工业用于制造氨基比林、维生素B等。
染料工用作合成染料的原料和用于电影基片染色。
涂料工业用于制造清。
有机工业用作溶剂和合成有机化合物的原料。
减压蒸馏基本原理:某些沸点较高的有机化合物在未达到沸点时往往发生分解或氧化的现象,所以,不能用常压蒸馏。
在较低压力下进行蒸馏的操作称为减压蒸馏.当蒸馏系统内的压力降低后,其沸点便降低,当压力降低到1。
3~2.0 kPa (10~15 mmHg)时,许多有机化合物的沸点可以比其常压下的沸点降低80~100℃.因此,减压蒸馏对于分离提纯沸点较高或高温时不稳定的液态有机化合物具有特别重要的意义。
反应方程式:CH3COOC2H5乙醇钠CH3COCH2COOC2H5+C2H5OH1、实验部分1。
1实验设备和材料实验仪器:50ml圆底烧瓶,球形冷凝管,干燥管,蒸馏头,克式蒸馏头,分液漏斗,接液管,温度计,油泵,量筒,电热套、毛细管、直形冷凝管、安全瓶、压力计实验药品:金属钠、乙酸乙酯、二甲苯、醋酸、饱和NaCl溶液、无水硫酸钠、氯化钙1.2实验装置回流装置减压蒸馏装置1.3实验过程(1)制钠珠:将0.9g 金属钠和5mL 干燥二甲苯放入装有回流冷凝管的50ml原定烧瓶中。
加热使钠熔融.拆去冷凝管,用磨口玻塞塞紧圆底烧瓶,趁热用力振摇(两下)得细粒状钠珠。
(2回流、酸化:稍经放置钠珠沉于瓶底,将二甲苯倒入指定回收瓶中。
迅速向瓶中加入10mL 乙酸乙酯,装上冷凝管,并在其顶端装一氯化钙干燥管。
反应开始有氢气泡逸出。
如反应很慢时,可稍加温热。
待激烈的反应过后,则小火加热,保持微沸状态,直至所有金属钠全部作用完为止。
此时生成的乙酰乙酸乙酯钠盐为桔红色透明溶液。
乙酰乙酸乙酯的制备-实验报告

乙酰乙酸乙酯的制备前言:乙酰乙酸乙酯,无色至淡黄色的澄清液体。
微溶于水,易溶于乙醚,乙醇。
有刺激性和麻醉性。
可燃,遇明火、高热或接触氧化剂有发生燃烧的危险。
有醚样和苹果似的香气。
广泛应用于食用香精中,主要用以调配苹果、杏、桃等食用香精。
制药工业用于制造氨基比林、维生素B等。
染料工用作合成染料的原料和用于电影基片染色。
涂料工业用于制造清。
有机工业用作溶剂和合成有机化合物的原料。
减压蒸馏基本原理:某些沸点较高的有机化合物在未达到沸点时往往发生分解或氧化的现象,所以,不能用常压蒸馏。
在较低压力下进行蒸馏的操作称为减压蒸馏。
当蒸馏系统内的压力降低后,其沸点便降低,当压力降低到1.3~2.0 kPa (10~15 mmHg)时,许多有机化合物的沸点可以比其常压下的沸点降低80~100℃。
因此,减压蒸馏对于分离提纯沸点较高或高温时不稳定的液态有机化合物具有特别重要的意义。
反应方程式:CH3COOC2H5乙醇钠CH3COCH2COOC2H5+C2H5OH1、实验部分1.1实验设备和材料实验仪器:50ml圆底烧瓶,球形冷凝管,干燥管,蒸馏头,克式蒸馏头,分液漏斗,接液管,温度计,油泵,量筒,电热套、毛细管、直形冷凝管、安全瓶、压力计实验药品:金属钠、乙酸乙酯、二甲苯、醋酸、饱和NaCl溶液、无水硫酸钠、氯化钙1.2实验装置回流装置减压蒸馏装置1.3实验过程(1)制钠珠:将0.9g 金属钠和5mL 干燥二甲苯放入装有回流冷凝管的50ml原定烧瓶中。
加热使钠熔融。
拆去冷凝管,用磨口玻塞塞紧圆底烧瓶,趁热用力振摇(两下)得细粒状钠珠。
(2回流、酸化:稍经放置钠珠沉于瓶底,将二甲苯倒入指定回收瓶中。
迅速向瓶中加入10mL 乙酸乙酯,装上冷凝管,并在其顶端装一氯化钙干燥管。
反应开始有氢气泡逸出。
如反应很慢时,可稍加温热。
待激烈的反应过后,则小火加热,保持微沸状态,直至所有金属钠全部作用完为止。
此时生成的乙酰乙酸乙酯钠盐为桔红色透明溶液。
乙酰乙酸乙酯制备

+
OH
H3COCH2COOC
其中乙酰乙酸乙酯用途极广,可用于合成抗过敏药、止咳药物、抗凝血药、 血管扩张药等多种医药中间体,还可用作香味剂。
以双乙烯酮为原料,还可以合成多种氨基酸。例如将双乙烯酮氨化生成丁酮 酰胺,再进行烷基化,然后低温下在氢氧化钾溶液中用次溴酸钠处理得到氨基酸 。 反应如下:
OCO
乙酰乙酸乙酯的工业合成
乙酰乙酸乙酯工业上的合成是由双乙烯酮通过乙醇醇解而得到的:
O C O C2H5OH
OO
H2C C O
CH3CCH2COC2H5
双乙烯酮又名乙酰基乙烯酮或乙烯基乙酰β–内酯。为无色或淡黄色有刺激
气味的可燃液体。不溶于水也不吸水,能溶于大部分有机溶剂。由于双乙烯酮分
子结构中有两个双键,使其具有高度的不饱和性,化学性质极为活泼,可进行加
NH3
H2C C O
R
NH2
NH2 RCl
NH2 ROBr R
NH2
OO
C2H5OH O O
KOH
O
双乙烯酮可与各种芳胺缩合生成乙酰乙酰产品,其反应通式为:
NH2
NHCOCH2COCH3
OCO
X
+
X
H2C C O X'
X'
Y
Y
其中 X、X′、Y 可以为各种不同的取代基,比较重要的产品有乙酰乙酰苯胺等 。
H2C C O
OCO H2C C O
双乙烯酮在工业上的主要用途是将其与醇反应制备乙酰乙酸酯类:
+CH3OH
CH3COCH2COOCH3
+ C2H5OH
CH3COCH2COOC2H5
OCO H2C C O
乙炔合成乙酰乙酸乙酯合成路线

乙炔合成乙酰乙酸乙酯合成路线乙炔是一种重要的化学原料,在化工领域有着广泛的应用。
而乙酰乙酸乙酯是一种常见的有机溶剂和合成材料,其合成路线多种多样。
本文将介绍一种常用的乙炔合成乙酰乙酸乙酯的合成路线。
乙炔是一种无色、有毒、易燃的气体,它是由乙烯经过裂解反应得到的。
乙炔的制备过程基本可以分为两步,即乙烯的制备和乙烯的裂解。
首先,乙烯的制备是乙炔合成乙酰乙酸乙酯的第一步。
乙烯是一种常见的有机物,可以通过石油、天然气等化石燃料的加热裂解得到。
在工业上,常用的方法是通过催化剂的作用,将乙烷转化为乙烯。
乙烯是一种无色、有毒、易燃的气体,可以作为化工原料用于合成其他有机物。
第二步是乙烯的裂解。
乙烯在高温下经过裂解反应可以得到乙炔。
乙烯裂解的条件包括温度、压力、催化剂等。
一般来说,乙烯裂解的温度要高于600摄氏度,压力一般在1-2兆帕左右。
在催化剂的选择上,常用的是氧化锌、氧化镁等金属氧化物。
乙炔合成乙酰乙酸乙酯的第三步是通过化学反应将乙炔转化为乙酰乙酸乙酯。
乙酰乙酸乙酯是一种无色液体,具有香气,可溶于水和多种有机溶剂。
乙酰乙酸乙酯的合成方法有多种,其中一种常用的方法是通过乙炔和乙醇的酯化反应得到。
在酯化反应中,乙炔和乙醇在催化剂的作用下发生酯化反应,生成乙酰乙酸乙酯。
常用的催化剂包括硫酸、磷酸等。
乙酰乙酸乙酯是一种重要的有机溶剂和合成材料,在化工、制药、食品等行业有着广泛的应用。
它具有挥发性小、溶解力强、熔点低等特点,适用于溶解和提取多种有机物。
乙炔合成乙酰乙酸乙酯的路线是通过乙烯的制备、乙烯的裂解以及乙炔的酯化反应三个步骤来完成的。
这种合成路线简单、成本低、操作方便,因此被广泛应用于工业生产中。
乙酰乙酸乙酯的应用领域广泛,对于提高化工生产效率和产品质量有着重要意义。
乙酰乙酸乙酯的制备

有机化学实验报告学院化学化工学院班级12化师学号成绩实验日期指导老师实验题目乙酰乙酸乙酯的制备一实验目的1、学习乙酰乙酸乙酯的制备原理和方法;2、掌握无水操作及减压蒸馏等操作。
二实验原理利用Claisen缩合反应,将两分子具有α-氢的酯在醇钠的催化作用下可以制得β-酮酸酯,其反应如下:1、通常以酯和金属钠为原料,且酯过量(同时作为溶剂),钠为计量依据物。
2、利用酯中含有的微量醇与钠反应来生成醇钠,随着反应的进行,醇不断生成,钠不断溶解,醇钠不断产生,反应能不断进行,直至钠消耗完毕。
作为原料的酯中含醇量过高又会影响产率的得率,一般要求酯中的含醇量在3%以下。
3、反应体系中如有水存在,对反应不利。
钠的损失降低了产率,也抑制了反应的进行,故要求反应体系无水。
4、反应中使用钠珠或钠丝可使其与酯的接触面增大,故先用二甲苯作溶剂制成细小的钠珠,以利于反应的进行。
乙酰乙酸乙酯在常压蒸馏下很易分解,产生“去水乙酸”,故应采用减压蒸馏法。
三、主要试剂及产物的物理常数试剂名称性状分子量M密度熔点(mp/℃)沸点(bp/℃)折射率(n D20)溶解度乙酰乙酸乙酯有果子香味无色或微黄色透明液体130.14 1.025-45~-43180.4分解1.4194溶于水,能与一般有机溶剂混溶乙酸乙酯有果子香气无色可燃性液体88.12 0.9005 -83.6 77.1 1.3723微溶于水,溶于乙醇、乙醚、氯仿和苯等甲苯无色易挥发液体有芳香气味92.14 0.866 -95 110.8 1.4967不溶于水,溶于乙醇、乙醚和丙酮主要试剂及用量名称规格用量备注g mL mol金属钠去掉表面氧化膜0.9 0.04二甲苯干燥 5乙酸乙酯精制10 0.1醋酸50% 调pH5~6食盐水饱和等体积醋酸用量苯8 萃取用四实验装置图图2:减压蒸馏装置图五、实验步骤及现象记录步骤现象备注钠珠的制备:干燥的圆底烧瓶中放入0.9g去掉表面氧化膜的金属钠、5ml干燥的二甲苯,冷凝回流加热至Na熔融由于二甲苯温度逐渐下降,蒸气压随之下降,因此,要不时开启瓶盖或在瓶口夹一纸条,否则塞子难以打开。
缩合反应乙酰乙酸乙酯的合成
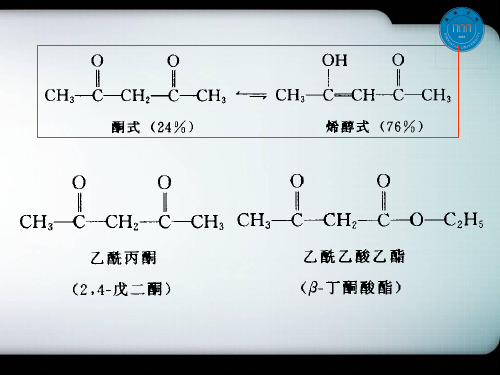
-丁酮酸酯
(2)克莱森(酯)缩合反应历程——亲核加成-消除
乙酸乙酯
• 凡有-H原子的酯,在乙醇钠或其他碱性催化剂(如 氨基钠)存在下,都能进行克莱森(酯)缩合反应。 • 克莱森(酯)缩合反应是合成-二羰基化合物的方法。
补充4:含有-H原子的酯与无-H原子的酯之间缩合 (1):与苯甲酸酯缩合——位引入:苯甲酰基 作业5(2)
苯甲酰基
(2):与草酸酯缩合——位引入:酯基(加热) 作业5(3)
加热生成酯基
(3):与甲酸酯缩合——位引入:醛基 Ph-CH2COOC2H5 + HCOOC2H5 C2H5ONa
Ph-CHCOOC2H5 + C2H5ONa CHO 醛基
(4):分子内酯缩合——成环
作作用下的反应 类似克莱森(酯)缩合反应:
与“三乙”可再 反应合成二酮!
(5) 与酰卤或酸酐作用——羰基亲核加成-消除反应
例:与酰氯的反应(得到酰基化产物)
NaH
•在 非 质 子 溶 液中进行
• 酮式分解得:-二酮
• 在合成上乙酰乙酸乙酯更多的用来合成 酮类。(合成羧酸时,常有酮式分解)
补充7
与酰卤作用
• 酮式分解得:-二酮
补充8
酮 -H活泼
• 常用丙酮或其他甲基酮和酯缩合来合成 -二酮。
• 注意:与羟醛缩合反应不同(稀碱条件下,生成 ,-不饱和醛)。P286
(4)克诺文格尔缩合反应 *——制备,-不饱和酸
• 醛、酮还可以和-二羰基化合物(一般是丙二酸及 其衍生物),在弱碱(氨或胺)作用下缩合:
亲核加成-消除
补充1:
解:
如三级卤代烃易 消除!不行!
烃基不同,分 步取代!
解:
乙酰乙酸乙酯及丙二酸乙酯在有机合成的应用

生命科学与理学院乙酰乙酸乙酯、丙二酸乙酯在有机合成的应用专业:生物科学班级:2012级1班学号:姓名:张昆乙酰乙酸乙酯一、乙酰乙酸乙酯的性质物理性质无色液体,熔点<-45℃,沸点181℃,相对密度(20/4℃),折射率,蒸气压(20℃)。
与乙醇、乙醚、苯等一般有机溶剂混溶,易溶于水。
具有愉快的水果香气。
化学性质互变异构一般的乙酰乙酸乙酯是酮式和烯醇式互变异构体和平衡混合物,酮式占93%,烯醇式占7%。
酮式乙酰乙酸乙酯沸点为41℃(),不能与溴起加成反应,也不使三氯化铁显色,但能与酮试剂作用。
烯醇式乙酰乙酸乙酯沸点为33℃(),不与酮试剂作用,但能使三氯化铁显色,烯醇分子内发生氢键缔合,形成螯合环。
因此,烯醇式都以单分子形态存在,沸点较低。
乙酰乙酸乙酯的分解反应乙酰乙酸乙酯在不同条件下不同反应条件下发生不同类型的分解反应,生产酮或酸。
乙酰乙酸乙酯在稀碱作用下,发生酯的水解反应,受热后脱羧成酮,这种分解称为酮式分解。
+ CO 2在浓碱条件下,OH -浓度高,除了和酯作用外,还可以使乙酰乙酸乙酯中α-与β-碳原子之间的键断裂,生成两分子羧酸,这种分解称为酸式分解。
取代反应乙酰乙酸乙酯亚甲基上的氢受到相邻两个吸电子基的影响,变得非常活泼,1)5%NaOH2)H1)浓NaOH2)H +在金属钠或乙醇钠的作用下可以被烷基或酰基取代。
选择适当的烷基化试剂或酰基化试剂与乙酰乙酸乙酯反应,然后酮式分解或酸式分解就可以得到不同结构的酮或酸。
二、乙酰乙酸乙酯的合成乙酰乙酸乙酯(俗名三乙)具有典型的β-酮酸酯结构,可用于多种合成反应,是一种重要的有机及药用合成的中间体。
在医药上用于合成氨基吡啉、维生素B 等,还广泛用于配制草莓、苹果、杏、樱桃、桃等水果型和酒型(朗姆、威士忌等)香精。
在农药生产上用于合成有机磷杀虫剂蝇毒磷的中间体α-氯代乙酰乙酸乙酯、嘧啶氧磷的中间体,杀菌剂恶霉灵等,也是杀菌剂新品种嘧菌环胺、氟嘧菌胺、呋吡菌胺及植物生长调节剂杀雄啉的中间体。
乙酰乙酸乙酯的制备 实验报告

乙酰乙酸乙酯的制备前言:乙酰乙酸乙酯,无色至淡黄色的澄清液体。
微溶于水,易溶于乙醚,乙醇。
有刺激性和麻醉性。
可燃,遇明火、高热或接触氧化剂有发生燃烧的危险。
有醚样和苹果似的香气。
广泛应用于食用香精中,主要用以调配苹果、杏、桃等食用香精。
制药工业用于制造氨基比林、维生素B等。
染料工用作合成染料的原料和用于电影基片染色。
涂料工业用于制造清。
有机工业用作溶剂和合成有机化合物的原料。
减压蒸馏基本原理:某些沸点较高的有机化合物在未达到沸点时往往发生分解或氧化的现象,所以,不能用常压蒸馏。
在较低压力下进行蒸馏的操作称为减压蒸馏。
当蒸馏系统内的压力降低后,其沸点便降低,当压力降低到1.3~2.0 kPa (10~15 mmHg)时,许多有机化合物的沸点可以比其常压下的沸点降低80~100℃。
因此,减压蒸馏对于分离提纯沸点较高或高温时不稳定的液态有机化合物具有特别重要的意义。
反应方程式:CH3COOC2H5乙醇钠CH3COCH2COOC2H5+C2H5OH1、实验部分1.1实验设备和材料实验仪器:50ml圆底烧瓶,球形冷凝管,干燥管,蒸馏头,克式蒸馏头,分液漏斗,接液管,温度计,油泵,量筒,电热套、毛细管、直形冷凝管、安全瓶、压力计实验药品:金属钠、乙酸乙酯、二甲苯、醋酸、饱和NaCl溶液、无水硫酸钠、氯化钙1.2实验装置回流装置减压蒸馏装置1.3实验过程(1)制钠珠:将0.9g 金属钠和5mL 干燥二甲苯放入装有回流冷凝管的50ml原定烧瓶中。
加热使钠熔融。
拆去冷凝管,用磨口玻塞塞紧圆底烧瓶,趁热用力振摇(两下)得细粒状钠珠。
(2回流、酸化:稍经放置钠珠沉于瓶底,将二甲苯倒入指定回收瓶中。
迅速向瓶中加入10mL 乙酸乙酯,装上冷凝管,并在其顶端装一氯化钙干燥管。
反应开始有氢气泡逸出。
如反应很慢时,可稍加温热。
待激烈的反应过后,则小火加热,保持微沸状态,直至所有金属钠全部作用完为止。
此时生成的乙酰乙酸乙酯钠盐为桔红色透明溶液。
乙酰乙酸乙酯的制备 实验报告

乙酰乙酸乙酯的制备前言:乙酰乙酸乙酯,无色至淡黄色的澄清液体。
微溶于水,易溶于乙醚,乙醇。
有刺激性和麻醉性.可燃,遇明火、高热或接触氧化剂有发生燃烧的危险。
有醚样和苹果似的香气.广泛应用于食用香精中,主要用以调配苹果、杏、桃等食用香精。
制药工业用于制造氨基比林、维生素B等。
染料工用作合成染料的原料和用于电影基片染色.涂料工业用于制造清。
有机工业用作溶剂和合成有机化合物的原料.减压蒸馏基本原理:某些沸点较高的有机化合物在未达到沸点时往往发生分解或氧化的现象,所以,不能用常压蒸馏。
在较低压力下进行蒸馏的操作称为减压蒸馏.当蒸馏系统内的压力降低后,其沸点便降低,当压力降低到1。
3~2.0 kPa(10~15 mmHg)时,许多有机化合物的沸点可以比其常压下的沸点降低80~100℃.因此,减压蒸馏对于分离提纯沸点较高或高温时不稳定的液态有机化合物具有特别重要的意义。
反应方程式:CH3COOC2H5乙醇钠CH3COCH2COOC2H5+C2H5OH1、实验部分1.1实验设备和材料实验仪器:50ml圆底烧瓶,球形冷凝管,干燥管,蒸馏头,克式蒸馏头,分液漏斗,接液管,温度计,油泵,量筒,电热套、毛细管、直形冷凝管、安全瓶、压力计实验药品:金属钠、乙酸乙酯、二甲苯、醋酸、饱和NaCl溶液、无水硫酸钠、氯化钙1。
2实验装置回流装置减压蒸馏装置1.3实验过程(1)制钠珠:将0。
9g 金属钠和5mL干燥二甲苯放入装有回流冷凝管的50ml原定烧瓶中。
加热使钠熔融。
拆去冷凝管,用磨口玻塞塞紧圆底烧瓶,趁热用力振摇(两下)得细粒状钠珠.(2回流、酸化:稍经放置钠珠沉于瓶底,将二甲苯倒入指定回收瓶中.迅速向瓶中加入10mL 乙酸乙酯,装上冷凝管,并在其顶端装一氯化钙干燥管。
反应开始有氢气泡逸出.如反应很慢时,可稍加温热。
待激烈的反应过后,则小火加热,保持微沸状态,直至所有金属钠全部作用完为止。
此时生成的乙酰乙酸乙酯钠盐为桔红色透明溶液.待反应物稍冷后,在摇荡下加入50%的醋酸溶液,直到反应液呈弱酸性(pH=5—6)为止。
2-(3-硝基亚苄基)乙酰乙酸乙酯的合成

2-(3-硝基亚苄基)乙酰乙酸乙酯的合成
硝基亚苄基乙酰乙酸乙酯是一种重要的有机化合物,在化工、农药、医药等领域有着广泛的应用。
本文将给出 2-(3-硝基亚苄基)乙酰乙酸乙酯的合成方法。
首先,我们需要准备一些原料,包括 3-硝基亚苄基胺、乙酸乙酯和碳酸钠。
将 3-硝基亚苄基胺放入反应容器中,加入足量的乙酸乙酯。
然后加入适量的碳酸钠,作为催化剂使用。
接下来,将反应容器的温度升高至80 ℃左右,保持一段时间,使反应物完全溶解。
然后,加入足量的磷酸作为调节剂,使反应更加顺利进行。
在保持一定温度的情况下,继续反应若干小时,直到反应终点。
最后,将得到的混合物冷却至室温,过滤干净,即可得到所需的 2-(3-硝基亚苄基)乙酰乙酸乙酯。
在本文所述的合成过程中,需要注意几点:首先,反应温度的控制是十分重要的,如果温度过高或过低都会导致反应不顺利;其次,选择合适的催化剂是十分关键的,碳酸钠是常用的催化剂,但也可以使用其他的催化剂,如磷酸等;最后,在进行反应的过程中,应该注意反应的安全,避免反应过程中的意外发生。
总的来说,2-(3-硝基亚苄基)乙酰乙酸乙酯的合成并不复杂,只需要注意一些细节就可以得到所需的产物。
这种有机化合物在工业应用中十分广泛,具有重要的经济价值。
乙酰乙酸乙酯的合成及其波谱分析

乙酰乙酸乙酯的合成及其波谱分析一、乙酰乙酸乙酯的合成㈠ 实验目的1.了解酯缩合反应制备β-酮酸酯的原理及方法。
2.掌握无水反应的操作要点。
3.掌握蒸馏、减压蒸馏等基本操作。
㈡ 实验原理(半微量实验)含有α-氢的酯在碱性催化剂存在下,能与另一分子的酯发生克莱森酯缩合反应,生成β-酮酸酯,乙酰乙酸乙酯就是通过这个反应来制备的。
本实验是用无水乙酸乙酯和金属钠为原料,以过量的乙酸乙酯为溶剂,通过酯缩合反应制得乙酰乙酸乙酯。
反应机理为,利用乙酸乙酯中含有的少量乙醇与钠作用生成乙醇钠。
↑+→+25252222H ON H C N OH H C a a随着反应的进行不断地生成乙醇,反应就不断地进行,直至钠消耗完。
在乙醇钠作用下,具有α-氢原子的乙酸乙酯自身缩合,生成烯醇型钠盐,再经醋酸酸化即得乙酰乙酸乙酯。
金属钠极易与水反应,并放出氢气和大量热,易导致燃烧和爆炸,故反应所用仪器必须是干燥的,试剂必须是无水的。
㈢ 实验装置乙酰乙酸乙酯合成的实验装置包括反应装置和减压蒸馏装置。
反应装置如图3-1所示,其回流冷凝管上须加干燥管。
减压蒸馏装置图3-2所示。
包括蒸馏、抽气、测压和保护四部分。
蒸馏部分由圆底烧瓶、克氏蒸馏头、冷凝管、接引管和接受器组成。
在克氏蒸馏头带有支管一侧的上口插温度计,另一口则插一根末端拉成毛细管的厚壁玻璃管。
毛细管下端离瓶底约1~2mm ,在减压蒸馏中,毛细管主要起到沸腾中心和搅动作用,防止爆沸,保持沸腾平稳。
在减压蒸馏装置中,接引管一定要带有支管。
该支管与抽气系统连接。
在蒸馏过程中若要收集不同馏分,则可用带支管的多头接引管。
根据馏程范围可转动多头接引管集取不同馏分。
接受器可用圆底烧瓶。
吸滤瓶等耐压容器,但不可用锥形瓶。
实验室里常用的抽气减压设备是水泵或油泵。
水泵常因其结构、水压和水温等因素,不易得到较高的真空度。
油泵可获得较高的真空度,好的油泵可达到13.3Pa 的真空度。
油泵的结构较为精密,如果有挥发性有机溶剂。
乙酰乙酸乙酯合成法机理

乙酰乙酸乙酯合成法机理乙酰乙酸乙酯的合成法机理可说是一场化学界的小冒险。
想象一下,咱们就像一群探险家,正准备踏上寻宝之旅。
这个小家伙叫乙酰乙酸乙酯,听名字就觉得它不简单。
它的结构其实挺有趣,里面有个小“乙酰”和个“乙酸”,它们像好朋友一样紧紧相拥。
咱们今天就来聊聊它的合成方法,这可是一门精妙的艺术,绝对不是随便混搭的哦。
咱们得从原料说起。
你想,要做出美味的菜肴,得先备齐材料嘛。
在这个过程中,咱们需要乙酰乙酸和醇,这里选的是乙醇。
二者相遇,就像火星撞地球一样,瞬间火花四溅。
哎呀,这时候要用到一些催化剂,比如氢氧化钠,别看它不起眼,但却是化学反应的推手。
就像比赛时的教练,默默地在背后给你加油助威。
反应开始了,咱们可以想象一下,化学分子们像在跳舞一样,优雅而迅速。
乙酰乙酸和醇的结合就像一对热恋中的小情侣,一碰就火花四溅。
它们之间的电子云开始重新组合,形成了一种新的化合物。
这个过程看似简单,却充满了不可思议的化学魔力。
你能想象吗?在显微镜下,那些小分子们可是在进行一场精心编排的舞蹈呢!当这个新的化合物生成后,咱们就得把它分离出来。
想象一下,派对上总会有一些人想要单独跳舞,不想跟大伙儿挤在一起。
分离过程就像筛选嘉宾,得让那些不需要的杂质离开,最后只留下咱们的明星——乙酰乙酸乙酯。
可以说,经过一番折腾,终于把这颗璀璨的明珠找出来了,真是让人兴奋!在这个过程中,反应条件也得掌握得当。
温度、浓度、时间,每一个环节都关系重大。
就好比做菜,火候掌握不好,可能就成了黑暗料理。
温度过高,反应可能会失控,温度过低,反应又可能进展缓慢,最后让人等得心急如焚。
所以,实验室里的化学家们可得小心翼翼,像对待小宝宝一样,细心呵护每一个反应步骤。
除了这些,搅拌速度也很关键。
想想在舞池里,大家跳得欢快,突然来了个慢舞,气氛立马变得尴尬。
所以,适当的搅拌能保证反应均匀,避免局部浓度过高,导致反应不完全。
化学反应可不是一个人的独舞,而是需要每个分子都参与进来,才能成就这场盛大的化学派对。
实验报告-醇钠的制备及乙酰乙酸乙酯的合成

醇钠的制备及乙酰乙酸乙酯的合成
一:实验目的
1.了解乙酰乙酸乙酯的制备的原理和方法。
2.熟悉在酯缩合反应中金属钠的应用和操作。
3.初步掌握减压蒸馏的操作技术。
二:实验原理
1.反应式
2CH 3CO 2C 2H
5 Na +[CH 3COCHCO 2C 2H 5]_ CH 3C0CH 2CO 2C 2H 5+NaOAc
2.反应机理
三.实验步骤及现象
四.结果与讨论
1.产量与产率
产量:无色透明液体0.7g
产率0.6/1.3×100%=46%
2.分析
乙酰乙酸乙酯在常压蒸馏时很易分解, 影响产率。
五.注意事项
NaOC 2H 5 HOAc
1.仪器干燥,严格无水。
金属钠易与水反应生成放出氢气及大量的热易导致燃烧和爆炸;氢氧化钠的存在易使乙酸乙酯水解;水的存在使金属钠消耗难以形成碳负离子中间体。
2.摇钠时应握紧烧瓶及橡胶塞,防止喷溅;钠珠应该越细越好。
3.醋酸不能多加,否则会造成乙酰乙酸乙酯的溶解损失。
用醋酸中和时,若有少量固体未溶解,可加少量水使其溶解。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
1.m乙酰乙酸乙酯=9.6g产率为35.5%
2.本次试验容易发生失败在于钠要在无水无氧条件下进行,会使得产率很低,甚至得不到产物。
参考文献:《大学有机化学实验》,复旦大学出版社
引言:
实验原理:将金属钠投入乙酸乙酯中,由于乙酸乙酯中混有乙醇,得到乙醇钠,在乙醇钠的作用下,两分子乙酸乙酯反应,发生Claisen酯缩合反应,最终得到乙酰乙酸乙酯,再通过萃取、蒸馏等方法得到纯净的产物。
反应式:
反应机理:
实验部分:
实验步骤:
1.用一个干燥的250ml的三口瓶,装取4.78g金属钠,装上球形冷凝管和氯化钙干燥管,搭好实验装置。
2.从三口瓶的另一个口迅速加入乙酸乙酯52.58ml。待反应缓和后,用石棉网小火加热,使溶液微沸,直至钠全部溶完。得到橙红色透明液体。
3.待稍冷后,振摇下加入50%乙酸溶液28.68ml,使溶液呈酸性,不溶物可用玻棒搅拌使之溶解。将溶液倒入分液漏斗,加入等体积的饱和氯化钠溶液,用力振摇,静止后分出酯层。用无水硫酸镁干燥。
乙酸乙酯:无色澄清液体,微溶于水,溶于醇、酮、醚、氯仿等多数有机溶剂,有强烈的醚似的气味,清灵、微带果香的酒香,易扩散,不持久。
钠:钠单质很软,可以用小刀切割。切开外皮后,可以看到钠具有银白色的金属光泽。钠是热和电的良导体。钠的密度是0.97g/cm3,比水的密度小,钠熔点是97.81℃,沸点是882.9℃。钠单质还具有良好的延展性。
乙酰乙酸乙酯的合成
摘要:在无水干燥条件下,乙醇钠的作用于两分子的乙酸乙酯,两分子的乙酸乙酯发生Claisen酯缩合反应,脱去一分支的乙醇,得到乙酰乙酸乙酯。再通过萃取、干燥、旋转蒸发、减压蒸馏最终得到比较纯净的乙酰乙酸乙酯。
关键词:乙酰乙酸乙酯乙酸乙酯钠
乙酰乙酸乙酯:无色至淡黄色的澄清液体,微溶于水,能溶于乙醇。有刺激性和麻醉性。可燃,遇明火、高热或接触氧化剂有发生燃烧的危险。中等毒性。
