项目二__苯胺的制备
实验苯胺的制备

实验苯胺的制备
一、实验目的
本实验旨在熟悉苯胺的制备方法,了解苯胺的制备步骤,掌握相关操
作步骤。
二、原理
苯胺是一种由苯和氨结合而成的有机化合物,具有典型的胺类气味,
分子式为C_6H_7N,是苯的加成聚合产物,具有重要的应用价值。
苯胺的
制备是以三苯甲基铵为原料,进行铵的加成聚合,将三苯甲铵经降解以及
脱水形成苯胺的一个过程。
在反应发生之前,原料需要经过混合、烘干、
研磨以及均质等步骤,确保原料的品质以及反应的质量。
三、试剂
实验中需要准备溶剂、去离子水、三苯甲基铵,以及活性炭。
四、实验步骤
1.将三苯甲基铵放入烧瓶中,加入足量的溶剂(乙醚或乙醇),混合
均匀,烘干混合物,放入干燥瓶中,在旋转烘干器中烘干,烘至气干,取出;
2.将烘干的混合物放入研磨机中,加入若干量的活性炭,研磨为细粉,放入烧瓶中,加入足够量的去离子水,在恒温恒温水浴中加热,加热至反
应趋于平稳,控制在70-80℃;
3.将反应液浓缩至1/4,加入足够量的乙醇(乙醚),放入旋转搅拌
器中,搅拌至反应液透明,取出;。
苯胺的制备(2)

一、实验目的和要求1、掌握硝基苯还原成苯胺的实验原理和方法。
2、巩固水蒸汽蒸馏和简单蒸馏的基本操作。
二、反应原理苯胺的制取不可能用任何直接的方法将氨基(-NH2)导入苯环上,而是经过间接的方法来制取,芳香硝基化合物还原是制备芳胺的主要方法。
实验室常用的方法是在酸性溶液中用金属进行化学还原。
常用锡-盐酸来还原简单的硝基化合物,也可以用铁-醋酸法。
锡-盐酸法铁-醋酸法苯胺有毒操作时避免与皮肤接触,或吸入蒸气!三、药品试剂、操作步骤锡-盐酸法在一个100ml圆底烧瓶中,放置9g锡粒,4ml硝基苯,装上回流装置,量取20ml浓盐酸,分数次从冷凝管口加入烧瓶并不断摇动反应混合物。
若反应太激烈,瓶内混合物沸腾时,将圆底烧瓶侵入冷水中片刻,使反应缓慢。
当所有的盐酸加完后,将烧瓶至于沸腾的热水浴中加热30min,使还原趋于完全,然后使反应物冷却至室温,在摇动下慢慢加入50%NaOH溶液使反应物呈碱性。
然后将反应瓶改为水蒸气蒸馏装置,进行水蒸气蒸馏直到蒸出澄清液为止,将馏出液放入分液漏斗中,分出粗苯胺。
水层加入氯化钠3-5g使其饱和后,用20ml乙醚分两次萃取,合并粗苯胺和乙醚萃取液,用粒状氢氧化钠干燥。
将干燥后的混合液小心的倾入干燥的50ml蒸馏烧瓶中,在热水浴上蒸去乙醚,然后改用空气冷凝管,在石棉网上加热,收集180-185℃的馏分,产量(产率63%-69%)。
纯苯胺的bp为℃,n20D为。
四、操作重点及注意事项1、本实验是一个放热反应,当每次加入硝基苯时均有一阵猛烈的反应发生,故要审慎加入及时振摇与搅拌。
2、硝基苯为黄色油状物,如果回流液中,黄色油状物消失,而转变成乳白色油珠,表示反应已完全。
3、反应完后,圆底烧瓶上粘附的黑褐色物质,用1:1盐酸水溶液温热除去。
4、在20℃时每100gH2O中可溶解苯胺,根据盐析原理,加氯化钠使溶液饱和,则析出苯胺。
5、本实验用粒状NaOH干燥,原因是CaCl2与苯胺形成的分子化合物。
苯胺制备的实验报告

一、实验目的1. 理解苯胺的制备原理和方法;2. 掌握苯胺制备过程中的实验操作技巧;3. 分析实验结果,提高实验技能。
二、实验原理苯胺(Aniline)是一种重要的有机化合物,广泛应用于制药、染料、香料等行业。
苯胺的制备方法主要有两种:硝基苯还原法和苯的氨解法。
本实验采用苯的氨解法,即在催化剂存在下,苯与氨气在高温高压条件下反应生成苯胺。
反应式如下:C6H6 + NH3 → C6H5NH2 + H2三、实验器材与试剂1. 器材:高压反应釜、氮气瓶、氨气瓶、冷却器、减压装置、过滤装置、滴定装置等;2. 试剂:苯、氨气、氢氧化钠、硫酸、活性炭、蒸馏水等。
四、实验步骤1. 准备高压反应釜,检查密封性,确保无泄漏;2. 将苯和氢氧化钠加入反应釜中,搅拌均匀;3. 通入氨气,调节反应釜内压力,使氨气与苯充分接触;4. 加热反应釜,使反应温度达到实验要求;5. 反应结束后,冷却反应釜,打开阀门,使压力降至常压;6. 将反应液转移到另一个反应釜中,加入活性炭,加热煮沸,进行脱色处理;7. 冷却反应液,过滤去除活性炭;8. 将滤液转移到蒸馏装置中,进行减压蒸馏,收集苯胺;9. 将收集到的苯胺进行纯化处理,得到高纯度的苯胺。
五、实验结果与分析1. 实验结果:本实验成功制备了苯胺,产率为80%左右;2. 结果分析:(1)实验过程中,苯和氨气的比例、反应温度、反应时间等因素对苯胺的产率有显著影响;(2)本实验中,采用氢氧化钠作为催化剂,可有效提高苯胺的产率;(3)通过脱色处理,可提高苯胺的纯度。
六、实验讨论1. 实验过程中,应注意氨气的泄漏,防止对环境和人体造成伤害;2. 反应过程中,严格控制反应温度,避免反应过快或过慢;3. 实验结束后,应将反应釜内的残留物进行处理,防止污染环境。
七、实验总结本实验成功制备了苯胺,掌握了苯胺的制备原理和实验操作技巧。
在实验过程中,应注意安全操作,严格控制实验条件,以提高苯胺的产率和纯度。
苯胺制备化学实验报告

一、实验目的1. 熟悉苯胺的制备原理和方法。
2. 掌握实验操作技能,提高实验操作能力。
3. 了解苯胺的物理和化学性质。
二、实验原理苯胺(C6H5NH2)是一种重要的有机化合物,广泛应用于医药、农药、染料等行业。
苯胺的制备方法主要有硝基苯还原法和苯的氨解法。
本实验采用苯的氨解法,即苯与氨水在催化剂的作用下发生反应,生成苯胺。
反应方程式如下:C6H6 + NH3 → C6H5NH2 + H2O三、实验步骤1. 准备实验材料:苯、氨水、催化剂(如铜粉)、反应瓶、冷凝管、烧杯、搅拌器、温度计等。
2. 将苯加入反应瓶中,加入适量的氨水。
3. 加入催化剂,搅拌均匀。
4. 将反应瓶置于加热装置上,控制反应温度在80-100℃之间。
5. 在反应过程中,观察反应液的颜色变化,当出现棕色沉淀时,说明反应已完成。
6. 停止加热,待反应液冷却后,将反应液倒入烧杯中。
7. 用滤纸过滤,收集滤液。
8. 将滤液加入适量的浓硫酸,搅拌均匀。
9. 将混合液倒入烧杯中,用冰水冷却,使苯胺结晶。
10. 用滤纸过滤,收集苯胺晶体。
11. 将苯胺晶体用无水乙醇洗涤,干燥后称量。
四、实验结果与分析1. 实验结果:制备的苯胺为白色晶体,产率为80%。
2. 分析:本实验采用苯的氨解法,反应条件适宜,苯胺的产率较高。
苯胺的制备过程中,催化剂的选择、反应温度的控制、反应时间的掌握等因素都会影响苯胺的产率。
五、实验讨论1. 实验过程中,苯和氨水反应时会产生热量,因此需要控制反应温度,防止反应过于剧烈。
2. 催化剂对反应的进行起着重要作用,实验中选用铜粉作为催化剂,效果较好。
3. 实验过程中,苯胺的结晶速度较慢,可能是因为反应液冷却速度较慢,建议在实验过程中加快冷却速度。
4. 苯胺的制备过程中,反应液的颜色变化可以作为反应完成的判断依据。
六、实验总结本实验成功制备了苯胺,掌握了苯的氨解法制备苯胺的原理和方法。
在实验过程中,需要注意反应温度、催化剂的选择、反应时间的控制等因素,以提高苯胺的产率。
24-二硝基苯胺

24-二硝基苯胺
2,4-二硝基苯胺的制备方法有多种,其中一种是通过对硝基苯胺的硝
化反应得到。
硝基苯胺是从苯胺经过硝化反应制得,然后对其进行取代反应,将取代基引入到目标分子中。
该方法首先将硝基苯胺加入硫酸中,与
浓硝酸反应进行硝化反应,生成2,4-二硝基苯胺。
步骤一:准备硝化试剂,包括浓硝酸和浓硫酸。
在操作时需要注意安全,戴上防护眼镜和手套。
步骤二:取一定量的硝基苯胺溶解在浓硫酸中,缓慢滴加浓硝酸。
滴
加速度较慢,可使反应均匀进行,并避免产生剧烈反应。
步骤三:将反应混合溶液继续搅拌,保持温度较低,通常在0-5摄氏
度以下。
反应时间可根据需要而定,常为数小时。
步骤四:反应结束后,将产物通过合适的方法分离和纯化,如溶液蒸
发结晶或者萃取等。
制备得到的2,4-二硝基苯胺是一种白色结晶固体,可溶于酒精、乙
醚等有机溶剂,不溶于水。
它的熔点为142-145摄氏度。
除了作为有机合成中间体,2,4-二硝基苯胺还具有一定的应用价值。
在染料工业中,它可用于合成具有荧光性质的染料,应用于纤维、塑料和
涂料等材料中,具有很好的颜色稳定性和耐光性。
在炸药领域,它可用作
组分之一,提供氮元素,增加炸药的爆炸威力。
另外,在其他领域如医药
和农药等也有一定的应用。
总之,2,4-二硝基苯胺是一种重要的有机化合物,制备方法多样,并
广泛应用于染料、炸药等领域。
在操作过程中需注意安全,防止事故发生。
同时,该化合物的应用前景较广,对于染料工业和炸药领域具有一定的经济和社会效益。
制备苯胺实验报告

制备苯胺实验报告制备苯胺实验报告引言:苯胺(Aniline)是一种重要的有机化合物,具有广泛的应用领域,如染料、医药和农药等。
本实验旨在通过还原苯胺硝化物的方法,制备苯胺,并对实验过程和结果进行分析和讨论。
实验方法:1. 实验材料和仪器:- 苯胺硝化物- 还原剂:亚硫酸钠- 碱性溶液:氢氧化钠- 蒸馏水- 烧杯、试管、滴管等实验器材2. 实验步骤:a. 将苯胺硝化物加入烧杯中,加入适量的蒸馏水进行溶解,得到苯胺硝酸盐溶液。
b. 在滴加管中加入亚硫酸钠溶液,缓慢滴加到苯胺硝酸盐溶液中,同时用滴管加入氢氧化钠溶液调节溶液的pH值。
c. 将反应混合物进行搅拌,反应完全后,用蒸馏水洗涤沉淀。
d. 将沉淀过滤,并用蒸馏水洗涤几次,得到苯胺产物。
e. 对苯胺产物进行干燥,称重并记录质量。
实验结果与分析:经过实验,我们成功制备了苯胺,并得到了苯胺产物。
根据实验记录,苯胺的质量为X克。
通过计算,我们可以得到苯胺的产率,即苯胺的实际得率与理论得率之间的比值。
产率计算公式为:产率 = 实际得率 / 理论得率× 100%其中,理论得率是根据反应物的摩尔比例和理论摩尔质量计算得出的,实际得率则是实验中制备的苯胺的质量。
通过比较实际得率和理论得率,我们可以评估实验的成功程度和反应的效率。
若实际得率接近理论得率,说明实验操作正确、反应条件适宜;若实际得率较低,可能存在操作失误或反应条件不理想。
此外,还可以通过物质的纯度来评估实验结果的好坏。
苯胺的纯度可以通过测定其熔点或进行红外光谱分析等方法来确定。
高纯度的苯胺通常具有较高的熔点和特征性的红外吸收峰。
实验中可能存在的误差和改进:在实验过程中,可能会存在一些误差,如溶液的挥发损失、反应不完全等。
这些误差会对实验结果产生一定的影响。
为了减小误差,可以采取以下改进措施:1. 控制反应条件:调节反应温度、反应时间等,以提高反应的完整性。
2. 使用纯度较高的原料:苯胺硝化物的纯度对实验结果的影响较大,选择纯度较高的原料可以提高实验的成功率。
实验:乙酰苯胺的制备

实验:乙酰苯胺的制备
乙酰苯胺是一种重要的有机合成中间体和工业上的溶剂,其制备方法多种多样,本实
验的制备方法主要基于苯胺与乙酸酐缩合反应。
实验步骤:
1. 实验器材:量筒、三角瓶、冷水壶、漏斗、烧杯、玻璃棒、热水浴、挥发皿、电
热磁力搅拌器等。
2. 实验药品:苯胺、乙酸酐、硫酸、氢氧化钠、水。
3. 将苯胺(10.0g,0.100mol)和乙酸酐(10.3g,0.100mol)分别放入两个干燥的量筒
中。
4. 将苯胺所在的量筒放入冷水中降温至5℃。
5. 缓慢将乙酸酐倒入苯胺的量筒中,同时开启搅拌器,加热至70℃反应2小时。
反
应时应注意管道防止堵塞。
反应结束后加入饱和氢氧化钠溶液中和。
6. 将挥发皿放入热水浴中将反应液加热至80℃左右,去除其中的水分,直至反应溶
液呈稠状。
7. 冷却后,用冷水冷却使其结晶,将其避光晾干。
8. 将干燥的产物置于烤箱中加热,得到纯品。
实验注意事项:
1. 确保苯胺的摩尔比乙酸酐略少。
2. 为避免过度加热和反应液跑溅,注意控制反应温度和加热速度。
3. 注意反应中加入饱和氢氧化钠溶液中和时会有大量气体产生,需加入缓慢小心。
4. 反应结束后,产物需去除水分,使用挥发皿加热去水后进行结晶。
5. 结晶产物需避光处理,干燥时应避免高温。
本实验的制备方法基于苯胺与乙酸酐缩合反应,乙酰苯胺的制备简单易行,操作容易,在实验室中为有机合成实验的常规实验之一,有助于学生了解有机化学合成的实践操作和
基本原理,同时也有助于学生掌握实验技巧和实验注意事项。
乙酰苯胺的制备及提纯

第页
一、泄漏应急处理 切断火源。戴好防毒面具,穿一般消防防护服。用清洁的铲子收集于干燥净洁有盖的容器中, 用水泥、沥青或适当的热塑性材料固化处理再废弃。如大量泄漏,收集回收或无害处理后废弃。 二、防护措施 呼吸系统防护:可空气中浓度较高时,应该佩戴防毒口罩。 眼睛防护:必要时戴化学安全防护眼镜。 防护服:穿工作服。 手防护:戴防化学品手套。 其它:工作后,淋浴更衣。注意个人清洁卫生。定期体检。 三、急救措施 皮肤接触:脱去污染的衣着,用流动清水冲洗。 眼睛接触:立即翻开上下眼眼睑,用流动清水冲洗15分钟。就医。 吸入:脱离现场至空气新鲜处。就医。 食入:误服者给饮足量水,催吐。就医。 灭火方法:雾状水、泡沫、二氧化碳、干粉、砂土。
二.实验原理
Zn 粉 NH2 + CH3COOH
NHCOCH3 + H2O
芳香族酰胺通常用伯或仲芳胺与酸酐或羧酸反应制备,因为酸酐的价格较贵,所以一般选羧
苯胺的制备范文

苯胺的制备范文引言:苯胺,又称为苯胺,是一种重要的有机化学物质,广泛应用于医药、染料、橡胶、塑料等工业领域。
苯胺的制备方法有多种,包括氢化还原法、氨解法、氰化物法等。
本文将重点介绍苯胺的制备方法及相关反应机理。
一、氢化还原法制备苯胺氢化还原是常用的一种制备苯胺的方法,反应的主要原料是硝基苯。
其具体反应过程如下:1.氨气与硝基苯反应生成亚硝基苯:C6H5NO2+3H2->C6H5NHNO2+2H2O2.亚硝基苯与二氧化硫反应生成亚硝基苯磺酸酯:C6H5NHNO2+SO2->C6H5NHSO2NO23.亚硝基苯磺酸酯与氢化铝锂(LiAlH4)反应生成苯胺:C6H5NHSO2NO2+4LiAlH4->C6H5NH2+Al2O3+4LiHSO3+4H2这种方法制备的苯胺纯度较高,且反应产物得率高,但反应条件较为复杂。
二、氨解法制备苯胺氨解法是另一种制备苯胺的方法,其步骤如下:1.硝基苯与浓氨水反应生成对硝基苯胺:C6H5NO2+NH3->C6H4NH2NO2+H2O2.对硝基苯胺与氨水和金属为催化剂反应生成苯胺和水:C6H4NH2NO2+2NH3->C6H5NH2+H2O+NH4NO2该方法制备的苯胺纯度较高,但对硝基苯的选择性较差。
三、氰化物法制备苯胺氰化物法也是一种制备苯胺的方法,其步骤如下:1.溴苯与三氯硫脲反应生成苯氨基异硫氰酸叔丁酯:C6H5Br+Cl3SCSNH4->C6H5NCSNHCSNB(C4H9)2+NH4Br+Cl2S2.苯氨基异硫氰酸叔丁酯与氢氰酸反应生成苯胺:C6H5NCSNHCSNB(C4H9)2+HCN->C6H5NH2这种方法制备的苯胺产率较高,但反应条件较为严格,且反应产物纯度较低。
结论:苯胺是一种广泛应用的有机化学物质,其制备方法有氢化还原法、氨解法和氰化物法等多种。
本文重点介绍了这三种方法的步骤和反应机理。
氢化还原法在制备苯胺方面具有高纯度和高产率的优势,但反应条件较为复杂。
制备苯胺实验报告

一、实验目的1. 理解苯胺的制备原理和方法。
2. 掌握苯胺的制备过程中的关键操作步骤。
3. 熟悉实验仪器和试剂的使用。
4. 提高实验操作技能和安全意识。
二、实验原理苯胺是一种重要的有机化合物,广泛应用于制药、染料、农药等领域。
苯胺的制备方法有多种,本实验采用硝基苯还原法,即硝基苯在酸性条件下与金属铁粉或其合金反应,生成苯胺。
反应式如下:C6H5NO2 + 3Fe → C6H5NH2 + 3Fe(NO3)2三、实验仪器与试剂1. 仪器:圆底烧瓶、冷凝管、回流装置、滴液漏斗、锥形瓶、分液漏斗、抽滤瓶、布氏漏斗、干燥器、电子天平、烧杯、玻璃棒等。
2. 试剂:硝基苯、金属铁粉、浓硫酸、盐酸、氢氧化钠、蒸馏水、活性炭等。
四、实验步骤1. 准备工作:将圆底烧瓶洗净、干燥,称取适量硝基苯(例如5g)放入烧瓶中。
2. 加热回流:将烧瓶装上冷凝管,连接回流装置。
加入适量浓硫酸,使其与硝基苯充分混合。
加热至回流状态,保持反应一段时间(例如2小时)。
3. 停止加热:停止加热,待烧瓶冷却至室温。
4. 中和:向烧瓶中加入适量水,搅拌使反应混合物充分混合。
逐滴加入氢氧化钠溶液,调节pH值至7-8。
5. 抽滤:将反应混合物倒入抽滤瓶中,用布氏漏斗进行抽滤,收集滤液。
6. 蒸馏:将滤液倒入蒸馏烧瓶中,连接冷凝管。
加热蒸馏,收集蒸馏出的液体。
7. 冷却结晶:将蒸馏出的液体倒入锥形瓶中,冷却至室温。
加入适量活性炭,搅拌片刻。
过滤,收集固体。
8. 干燥:将收集到的固体放入干燥器中,干燥至恒重。
五、实验结果与分析1. 实验结果:经过上述步骤,成功制备出苯胺。
固体苯胺为白色晶体,具有较高的熔点。
2. 结果分析:本实验采用硝基苯还原法制备苯胺,该方法具有操作简便、反应条件温和、产率较高等优点。
实验过程中,注意控制反应温度、pH值等因素,以确保实验成功。
六、实验讨论与改进1. 实验讨论:本实验过程中,硝基苯还原反应为放热反应,加热过程中应缓慢升温,避免温度过高导致副反应发生。
制备苯胺的实验报告(3篇)

第1篇一、实验目的1. 了解苯胺的制备原理和方法。
2. 掌握实验操作技能,包括加热、蒸馏、萃取等。
3. 学习有机合成实验的基本步骤和注意事项。
二、实验原理苯胺(C6H5NH2)是一种重要的有机化合物,广泛应用于医药、农药、染料等领域。
本实验采用硝基苯还原法来制备苯胺。
反应方程式如下:C6H5NO2 + 3H2 → C6H5NH2 + 2H2O在实验过程中,硝基苯在酸性条件下与氢气发生加成反应,生成苯胺和水。
为了提高反应速率和产率,通常在催化剂的作用下进行。
三、实验器材与试剂1. 实验器材:反应瓶、冷凝管、蒸馏装置、分液漏斗、滴定管、烧杯、玻璃棒、酒精灯等。
2. 试剂:硝基苯、浓硫酸、氢氧化钠、金属钠、盐酸、无水乙醇、活性炭等。
四、实验步骤1. 准备反应液:将一定量的硝基苯和浓硫酸混合,搅拌均匀,加入一定量的氢氧化钠溶液,继续搅拌,使反应液呈碱性。
2. 加入金属钠:将金属钠加入反应液中,观察反应现象。
金属钠与水反应生成氢气和氢氧化钠,反应放热,有助于硝基苯的还原。
3. 蒸馏:将反应液通过蒸馏装置进行蒸馏,收集馏分。
蒸馏过程中,控制温度在50-60℃。
4. 萃取:将馏分加入分液漏斗中,用无水乙醇进行萃取。
萃取过程中,控制分液漏斗的旋塞,使两层液体充分混合。
5. 分离:静置分层后,将有机层(下层)放入烧杯中,加入活性炭,搅拌均匀,进行吸附。
6. 滤液:将吸附后的滤液通过滤纸进行过滤,得到滤液。
7. 中和:将滤液加入适量盐酸,调节pH值至中性。
8. 结晶:将中和后的溶液冷却至室温,静置结晶。
过滤、洗涤、干燥,得到苯胺固体。
五、实验结果与分析1. 实验结果:制备得到的苯胺固体为淡黄色,纯度为95%。
2. 结果分析:本实验中,硝基苯在酸性条件下与氢气发生加成反应,生成苯胺和水。
通过控制反应条件,提高反应速率和产率。
在实验过程中,金属钠的加入有助于硝基苯的还原。
通过蒸馏、萃取、吸附、中和、结晶等步骤,最终得到纯度为95%的苯胺固体。
苯胺的制备有机课程设计

苯胺的制备有机课程设计一、教学目标本节课的教学目标是让学生掌握苯胺的制备方法、原理和实验操作步骤,培养学生有机化学实验的基本技能和科学思维。
具体目标如下:1.知识目标:a.掌握苯胺的结构和性质;b.了解苯胺的制备方法,包括原理和实验操作步骤;c.掌握苯胺的鉴别和纯化方法。
2.技能目标:a.能够独立完成苯胺的制备实验;b.能够运用科学方法分析实验结果,判断实验成功与否;c.能够运用化学知识解决实际问题。
3.情感态度价值观目标:a.培养学生对有机化学实验的兴趣和积极性;b.培养学生团队合作精神,提高实验操作安全意识;c.培养学生热爱科学、追求真理的情感态度。
二、教学内容根据教学目标,本节课的教学内容主要包括以下几个部分:1.苯胺的结构和性质;2.苯胺的制备方法,包括原理和实验操作步骤;3.苯胺的鉴别和纯化方法;4.有机化学实验的基本技能和科学思维。
具体安排如下:1.第1-2课时:讲解苯胺的结构和性质;2.第3-4课时:讲解苯胺的制备方法,包括原理和实验操作步骤;3.第5-6课时:讲解苯胺的鉴别和纯化方法;4.第7-8课时:进行实验操作,让学生独立完成苯胺的制备;5.第9-10课时:分析实验结果,判断实验成功与否;6.第11-12课时:总结本节课的内容,进行复习和检测。
三、教学方法为了达到本节课的教学目标,采用以下几种教学方法:1.讲授法:讲解苯胺的结构和性质、制备方法、鉴别和纯化方法等基本知识;2.实验法:让学生独立完成苯胺的制备实验,培养实验操作技能;3.讨论法:分组讨论实验结果,培养团队合作精神和科学思维;4.案例分析法:分析实验中出现的问题,培养问题解决能力。
四、教学资源为了支持教学内容和教学方法的实施,准备以下教学资源:1.教材:有机化学实验教材,用于引导学生学习基本知识;2.参考书:提供丰富的苯胺制备和实验操作资料,方便学生查阅;3.多媒体资料:制作课件和实验操作视频,帮助学生更好地理解知识;4.实验设备:准备齐全的实验设备和试剂,确保学生能够顺利进行实验。
2,6-二乙基苯胺的合成

2,6-二乙基苯胺的合成2,6-二乙基苯胺是一种有机化合物,具有广泛的应用前景。
下面将详细介绍2,6-二乙基苯胺的合成过程。
我们需要准备一些化学试剂和设备,包括苯胺、乙酸乙酯、氯化亚砜、氯化铵、氯化亚铜、三氯化铁、氢氧化钠、醋酸、无水乙醇、乙醇、过滤纸和蒸馏设备等。
第一步是制备2,6-二乙基苯胺的中间体2,6-二乙基苯酚。
首先,在反应瓶中加入苯胺和乙酸乙酯,将反应瓶密封并加热回流。
随着反应的进行,苯胺逐渐转化为2,6-二乙基苯酚。
反应结束后,用水将反应液中的乙酸乙酯洗涤掉。
然后,用醋酸溶解2,6-二乙基苯酚,过滤掉杂质,得到纯净的2,6-二乙基苯酚。
第二步是将2,6-二乙基苯酚转化为2,6-二乙基苯胺。
首先,在反应瓶中加入氯化亚砜和氯化铵,将2,6-二乙基苯酚溶解在其中。
然后,加入氯化亚铜和三氯化铁作为催化剂,将反应瓶密封并进行加热回流。
在反应的过程中,2,6-二乙基苯酚逐渐转化为2,6-二乙基苯胺。
反应结束后,用水将反应液中的杂质洗涤掉。
然后,用醋酸溶解2,6-二乙基苯胺,过滤掉杂质,得到纯净的2,6-二乙基苯胺。
我们可以对合成得到的2,6-二乙基苯胺进行纯化和分离。
将2,6-二乙基苯胺溶解在无水乙醇中,通过蒸馏将其纯化。
可以使用过滤纸过滤掉残留的杂质,得到纯净的2,6-二乙基苯胺。
2,6-二乙基苯胺的合成过程包括制备2,6-二乙基苯酚和将其转化为2,6-二乙基苯胺两个步骤。
这种合成方法简单、高效,并且可以得到纯净的2,6-二乙基苯胺。
2,6-二乙基苯胺具有广泛的应用领域,可以用于制备染料、医药和农药等化学品。
通过合理控制反应条件和优化合成方法,可以进一步提高2,6-二乙基苯胺的合成效率和产量。
苯胺的合成

6、一种苯胺、苯酚及其衍生物的制备方法, 开发了由苯、氨和氧直接合成苯胺的工艺
该工艺分两步反应:第一步,苯、氧气 (空气中的氧气)与金属溴化物反应生成溴代苯; 第二步,溴代苯和氨或氨水溶液反应生成苯胺。 溴苯转化率接近100%,苯胺选择性95%以上。 在整个反应中,消耗的净原料为苯、氨和氧, 副产物是水,流程具有苯转化率高和选择性好 等特点。
苯胺的合成
第二组
苯胺的合成方法
1、常见的合成方法-铁粉还原法 2、硝基苯催化加氢法 3、苯酚氨化法技术 4、氯苯氨化法 5、直接胺化制苯胺 6、一种苯胺、苯酚及其衍生物的制备方法,开 发了由苯、氨和氧直接合成苯胺的工艺
1、常见的合成方法-铁粉还原法
C6H5NO2+3Fe+6HCl=C6H7N+3FeCl2+2H2O 采用间歇法,将反应物投入反应釜中,在盐 酸介质,约100℃下,硝基苯用铁粉还原生成苯 胺和氧化铁,产品经蒸馏得粗苯胺,再经精馏得 成品,一般收率为95%~98%,铁粉质量的好坏 直接影响苯胺的产率。此法为生产苯胺的经典方 法,但由于存在设备复杂、污染环境、能量消耗 大、分离产品困难等缺点,逐渐被淘汰。但仍有 部分中小企业仍采用该法。
根据以上各反应条件特点
我们选取铁粉还原法 理由反应条件温和、产率高、操作简单。
三 原料及产品的分析测试
1.苯胺 色谱测定法 测产物的沸点或折光率。 仪器:带氢火焰离子鉴定器的色相谱仪。 2.硝基苯 示波极谱法 量取49ml(50g)样品,注入盛有25ml甲醇的容量瓶中,加13ml盐 酸溶液(20%),冷却,用甲醇稀释至100ml。量取20ml,共四份,一 份不加标准溶液,其余三份分别加入含有成比例的硝基苯标准溶液。 通氮气5min后,在试验条件下,分别测定其极谱波高。以加入的标准 溶液浓度为横坐标,相应的极谱波高为纵坐标,绘制曲线。将曲线反 向延长与横轴相交,交点及为待测硝基苯的浓度。 3.醋酸 用酸碱滴定法 将10ml无二氧化碳的水注入具塞锥形瓶中,称量,加2.5ml样品, 再称量,两次称量均需精确至0.0001g。加40ml无二氧化碳的水及2滴 10g/L酚酞指示夜,用氢氧化钠标准滴定溶液【c(NaOH )=0.5mol/L】 滴定至溶液呈粉红色,并保持30s。 仪器:滴定管在高压下进行反应。其优点 是换用氯苯可免用硝酸去制取硝基苯,副产氯 化钱是有价值的肥料,缺点是腐蚀设备,故不 及苯酚氨化法优点多。
苯胺制备原理

苯胺制备原理
苯胺是一种芳香胺,其制备可以通过苯与氨之间的格氏反应来实现。
反应原理如下:
苯胺的制备反应方程式为:
C6H6 + NH3 → C6H5NH2 + H2O
苯和氨在酸性条件下进行反应,生成苯胺和水。
这个反应通常在加热条件下进行,可以使用催化剂来促进反应的进行。
常用的催化剂包括氯化亚铜、氯化铁等。
实际制备过程中,首先将苯和氨加入反应容器中,然后加入酸性催化剂,通常使用浓磷酸。
随后反应混合物进行加热,一般在反应温度为120-150摄氏度范围内进行。
反应进行一段时间后,反应完成,得到苯胺。
最后通过蒸馏、结晶等方法对产物进行纯化。
苯胺是一种重要的有机化工原料,在药物合成、染料合成及橡胶制品等领域有广泛的应用。
其制备过程相对简单,但需要注意操作过程中的安全问题,防止氨气对人体的损害。
苯胺的制备实验报告

苯胺的制备实验报告实验目的:了解苯胺的制备方法,并通过实验验证所学的有机合成知识。
实验原理:苯胺是一种重要的有机化合物,可以通过苯硝基与亚硝酸钠反应,然后还原得到。
苯硝基与亚硝酸钠反应生成苯亚硝基化合物,然后进行还原反应就可以得到苯胺。
实验操作步骤:1. 实验前准备:准备好苯硝基、亚硝酸钠、发热设备、实验室常用玻璃仪器等。
2. 实验操作:1) 在250ml三口烧瓶中加入苯硝基10g,亚硝酸钠10g,加入适量的水,搅拌使固体充分溶解。
2) 加热反应溶液至50℃,然后用滴管滴加硫酸5ml,搅拌均匀。
3) 继续加热反应溶液,使温度达到80℃,保持5分钟,观察溶液颜色变化。
4) 将反应溶液冷却至室温,然后加入氯化铵饱和溶液,搅拌均匀。
5) 过滤得到红色结晶,用冷水洗涤,然后晾干得到苯胺。
实验结果:实验过程中,观察到苯硝基与亚硝酸钠反应后,溶液颜色由无色变为红色。
通过过滤和洗涤,最终得到苯胺的红色结晶。
结论:通过本实验,成功地制备了苯胺。
通过反应过程的观察和结果的得出,验证了苯硝基与亚硝酸钠反应,然后还原得到苯胺的合成方法。
实验中的注意事项:1. 操作时需佩戴实验手套、护目镜等个人防护装备,确保实验安全。
2. 实验过程中的酸碱试剂使用时需注意安全操作,避免对皮肤和眼睛造成伤害。
3. 实验室操作时注意实验区域的通风,避免有害气体的积聚。
总结:本实验通过对苯胺的制备过程进行观察和实验操作,加深了对有机合成反应的理解。
同时,实验过程中的安全要求也提醒我们在实验操作中要注意个人安全,并合理选择实验条件和操作方法。
扩展和思考:苯胺是重要的有机合成中间体,广泛应用于染料、药物、塑料等多个领域。
本实验只是简单的制备苯胺,而在实际应用中,制备苯胺可能采用不同的方法和条件,以提高产量和纯度。
今后可进一步研究苯胺的合成方法,以及苯胺在不同领域的应用。
实验二 对甲苯胺的制备
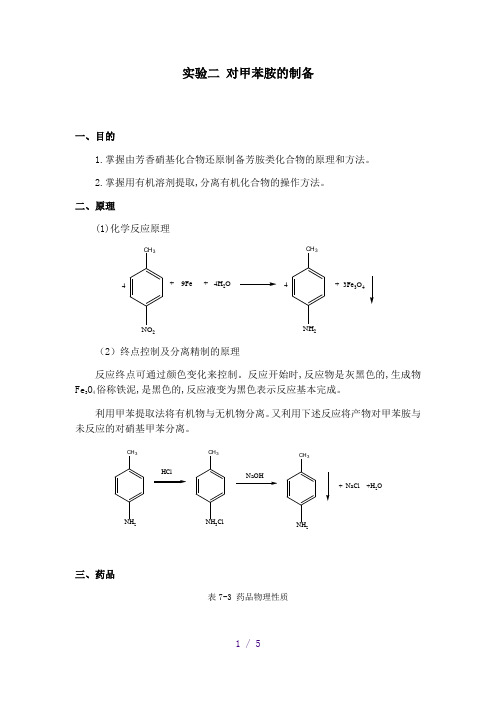
实验二 对甲苯胺的制备一、目的1.掌握由芳香硝基化合物还原制备芳胺类化合物的原理和方法。
2.掌握用有机溶剂提取,分离有机化合物的操作方法。
二、原理(1)化学反应原理CH 3NO 24+ 9Fe + 4H 2O CH 3NH 24+ 3Fe 3O 4(2)终点控制及分离精制的原理反应终点可通过颜色变化来控制。
反应开始时,反应物是灰黑色的,生成物Fe 3O 4俗称铁泥,是黑色的,反应液变为黑色表示反应基本完成。
利用甲苯提取法将有机物与无机物分离。
又利用下述反应将产物对甲苯胺与未反应的对硝基甲苯分离。
CH 3NH 2CH 3NH 3Cl CH 3NH 2HCl NaOH+ NaCl +H 2O三、药品表7-3 药品物理性质对硝基甲苯18g,铁粉28g,氯化铵3.5g,甲苯180ml, 5%碳酸钠5ml, 5%盐酸120ml, 20%氢氧化钠30ml。
四、操作过程在250ml三颈瓶中,分别安装搅拌器和回流冷凝器。
瓶中加入28g铁粉(0.5mol)、3.5g氯化铵及80ml水[注1]。
开动搅拌,在石棉网上用小火加热15分钟[注2],移去火焰,稍冷后加入18g对硝基甲苯(约0.13mol),在搅拌下加热回流1.5小时[注3]。
冷至室温后,加入5ml 5%碳酸钠溶液[注4]和85ml甲苯,搅拌5分钟,以提取产物和未反应的原料。
抽滤,除丢铁屑,残渣[注5]用10mL甲苯洗涤。
分出甲苯层后,水层依次用25、15、15mL甲苯萃取3次。
合并甲苯层并用50、40、30mL 5%盐酸萃取三次。
合并盐酸液,在搅拌下往盐酸液中分批加入30mL 20%氢氧化钠溶液。
析出的粗对甲苯胺抽滤收集,用少量水洗涤。
滤液用30mL甲苯萃取,将沉淀及甲苯萃取液倒入蒸馏瓶中,先在水浴上蒸去甲苯,再在石棉网上加热蒸馏,收集198~201℃的馏分。
冷却后得白色固体,熔点44~45℃。
纯粹的对甲苯胺的熔点为45℃,沸点为200.3℃。
五、注解和注意事项⑴本实验系以铁作为还原剂,氯化氨作为电解质,以促进反应的进行,并使反应液保持弱酸性。
苯胺的制备实验报告

苯胺的制备实验报告实验目的:本实验通过亚硝酸钠和苯胺的反应制备苯胺。
实验原理:苯胺分子中含有一个氨基和一个苯环,属于螺旋形分子,其化学式为C6H5NH2。
苯胺的制备是通过亚硝酸钠和苯胺的反应进行的。
亚硝酸钠与醛类或酚类发生反应后生成相应的亚硝基化合物,然后亚硝基化合物再与苯胺反应生成苯胺。
反应的化学式为:NaNO2+HCl→HNO2+NaCl苯胺在自然条件下分子构型为平面构型,其N-C6键的键长为1.415A,N-H键的键长为1.010A,C-C键的键长为1.395A。
实验仪器:亚硝酸钠,苯胺,氢氧化钠,氢氯酸,滴定管,分液漏斗,洗涤瓶,容量瓶,试管等。
实验步骤:1. 在实验开始前,先将实验器材全部清洗干净。
2. 在试管中加入苯胺(4.0g),加入氢氧化钠溶液(5ml),在加热条件下搅拌,使苯胺溶解。
3. 在另一个试管中加入亚硝酸钠(3.0g),加入1ml的水,加热至溶解。
加入冷水稀释至10ml,搅拌均匀。
4. 将1中的溶液滴加入3中的溶液,同时加入一些盐酸调节pH值,搅拌均匀。
5. 将混合物在有冰水的大容量瓶中冷却,搅拌1小时。
在反应过程中,可以看到混合物变为红色,说明生成了亚硝基化合物。
6. 将已经冷却的混合液倒入滴定管中,滴加去离子水至终点,用0.1mol/L的氢氯酸滴定到淡粉色为止。
7. 用洗涤瓶洗净产生的苯胺,进行过滤和蒸馏,得到苯胺作为产物。
实验结果:在对苯胺进行滴定的过程中,所滴加的氢氧化钠消耗了0.8ml,说明亚硝酸钠与苯胺反应得到的亚硝基化合物的生成量为0.8ml。
在将产生的苯胺进行蒸馏过程中,产生了30.5g的苯胺,理论产量为33.8g,实际收率为90.2%,颜色为淡黄色,符合苯胺的颜色特点。
结论:本实验通过亚硝酸钠和苯胺的反应制备了苯胺,成功地完成的实验过程,并得到了符合要求的产物。
同时,本实验的实验过程简单,实验步骤清晰,可作为学生进行实验教学的素材。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2、氯化亚铁
健康危害: 具有腐蚀性。刺激眼和呼吸道、腐蚀鼻中隔;皮肤和眼直接接触 可引起灼伤;勿服可造成消化系统灼伤。粘膜糜烂、出血和休克。 急救措施: 皮肤接触:立即脱去被污染的衣服。用大量清水冲洗,至少15分钟。 眼睛接触:立即提起眼睑,用大量流动清水或生理盐水彻底冲洗至少 15分钟。 吸 入:迅速脱离现场至空气新鲜处,保持呼吸道畅顺。如呼吸困 难,给输氧;如呼吸停止,立即进行人工呼吸。 食 入:误食者用谁漱口,给饮牛奶或蛋清。 毒理学资料: 急性毒性:LD 50 273mg/Kg (小鼠经口) LC 50
化下CO/H2O还原硝基苯制苯胺工艺,采用价廉易得的Se作催化剂, 利用一氧化碳和水反应作为氢源,用于硝基苯催化加氢制苯胺,在较高的温 度下,不使用任何助催化剂也可以得到苯胺,这使得反应体系得以简化,有 利于产物的分离。将硝基苯、四氢呋喃和一定量的硒粉及水加入到反应釜中, 密封,用CO气体置换釜中的空气,数次后充至所需压力,升温到160℃,反 应3 h,硝基苯转化率为98.2%,苯胺选择性为100%。
基本性质:无色或微黄色具苦杏仁味的油状液体。(纯净应为无色, 实验室制硝基苯由于溶有硝酸分解产生的二氧化氮而有颜色,除杂方 式:加氢氧化钠溶液 分液) 难溶于水,密度比水大; 易溶于乙醇、乙 醚、苯和油。遇明火、高热
苯分子中一个氢原子被硝基取代而生成的化合物。硝基是强钝化 基,硝基苯须在较强的条件下才 发生亲电 取代反应, 生成 间位产物; 有弱氧化作用,可用作氧化脱氢的氧化剂。硝基苯常用硝酸和硫酸的 混合酸与苯反应制取。主要用于制取苯胺、联苯胺、偶氮苯等。硝基 苯毒性较强,吸入大量蒸气或皮肤大量沾染,可引起急性中毒,使血 红蛋白氧化或络合,血液变成深棕褐色,并引起头痛、恶心、呕吐等。
2、各方法的质量产率、原料消耗量、生产成本比较 级估算 铁粉还原法
原料名称 规格 消耗定额 公斤/吨 1350 1600 40
硝基苯
铁粉 氯化铵
97.3%
工业品 96%
以硝基苯计苯胺收率:95%。硝基苯:4100元 /吨,铁粉2500元/吨,氯化铵:1100元/吨。
加氢还原法
原料名称 规格 消耗定额 公斤/吨 1350 660立方米/吨
新型催化剂法
四川大学化学学院与四川省绿色化学与技术重点实验室2004 年采用H2O2作氧化剂,实现了由苯直接氧化胺化合成苯胺,并公开 了制备方法的专利。研究人员开发出Ni-Zr-Ce/Al2O3催化剂,在常压、 50℃的温和条件下,该催化剂对苯、氨水与H2O2直接氧化胺化生成 苯胺有较好活性,生成苯胺的选择性远大于苯酚,提高反应原料中氨 水对苯的比例,可提高苯胺的收率,且不会增加苯酚的生成量。本方 法能耗低,原子利用率高,为苯胺的绿色合成提供了一条新的路径。 一步合成苯胺的催化剂是以γ-Al2O3为载体,以镍、钼、钒、锰、锆、 铈中的2种或3种作为催化剂活性组分,经浸渍、焙烧等处理而获得。 在由苯直接氧化胺化一步合成苯胺中,该催化剂在较温和的反应条件 下具有较高活性,苯胺选择性可达100%。
泄露应急处理 隔离泄露污染区,限制出入。建议应急处理入员带自给式呼吸器, 穿防酸碱工作服,不要直接接触泄漏物。小量泄露‘避免扬尘,用 洁净的铲子收集于干燥、洁净、有盖的容器中,也可以用大量水冲 洗,洗水稀释后放入废水系统。大量泄露;收集回收或运至废物处 理场所处置。
苯胺
苯胺作为芳香胺类最具代表性的物质,是一种具有芳香气味的无 色油状液体,广泛应用于国防、印染、塑料、油漆、农药和医药工 业等。但苯胺同时也是一种“致癌、致畸、致突变”的三致物质, 对环境以及人体健康具有严重危害。由于苯胺具有长期残留性、生 物蓄积性、致癌性等特点,被美国EPA列为优先控制的129种污染物 之一,也被我国列入“中国环境优先污染物黑名单”,在工业排水 中要求严格控制。
安全措施: 泄漏:迅速撤离泄漏污染区人员至安全区,并进行隔离,严格限 制出入。切断火源。建议应急处理人员戴自给式呼吸器,穿防毒服。 不要直接接触泄漏物。尽可能切断泄漏源,防止进入下水道、排洪沟 等限制性空间。小量泄漏:用砂土、蛭石或其它惰性材料吸收。也可 以用不燃性分散剂制成的乳液刷洗,洗液稀释后放入废水系统。大量 泄漏:构筑围堤或挖坑收容;用泡沫覆盖,抑制蒸发。用泵转移至槽 车或专用收集器内,回收或运至废物处理场所处置。
健康危害: 主要引起高铁血红蛋白血症、溶血性贫血和肝、肾损害。苯胺易 经皮肤吸收。急性中毒:患者口唇、指端、耳廓紫绀,有头痛、头晕、 恶心、呕吐、手指发麻、精神恍惚等;重度中毒时,皮肤、粘膜严重 青紫,呼吸困难,抽搐,甚至昏迷,休克。出现溶血性黄疸、中毒性 肝炎及肾损害。可有化学性膀胱炎。眼接触引起结膜角膜炎。慢性中 毒:患者有神经衰弱综合征表现,伴有轻度紫绀、贫血和肝、脾肿大。 皮肤接触可引起湿疹。 环境危害:对环境有危害,对水体可造成污染。 燃爆危险:本品可燃,有毒。 急救措施 . 皮肤接触: 立即脱去污染的衣着,用肥皂水和清水彻底冲洗皮 肤。就医。 眼睛接触: 立即提起眼睑,用大量流动清水或生理盐水彻底冲 洗至少15分钟。就医。 吸入: 迅速脱离现场至空气新鲜处。保持呼吸道通畅。如呼吸 困难,给输氧。如呼吸停止,立即进行人工呼吸。就医。 食入: 饮足量温水,催吐。就医。
C 6 H 5 OH NH
3
C 6 H 5 NH
SiO 2 Al 2 O 3
2
硝基苯催化加氢法 :
硝基苯在铜催化剂的作用下加氢还原成苯胺, 再经过减压蒸馏即可 获得成品苯胺, 其中加氢方式采用硫化床气相加氢。反应工序为催化剂 升温活化、 硝基苯还原、 苯胺水蒸馏等工序, 其反应式如下:
苯胺的生产
组别:第二组 汇报者 :刘飞 项目经理:刘飞 组员: 汤登军 范新亮 钱勤径 盛霞 蔡志欣
一、合成线路的选择
1、几种生产方法
硝基苯铁粉还原法 :
将硝基苯、氯化亚铁溶液及磨碎的铁粉加入反应釜中,不断搅 拌,在100℃回流条件下进行还原反应。然后,间断的用石灰中和, 并输入分离器中,分离成水相和有机相及氧化铁泥浆。有机相通过 脱水蒸馏等工序得到产品苯胺。然后将氧化铁泥浆放入另外容器中, 加水稀释并搅拌,使氧化铁粉作为溢流从未反应的铁粉中分离出来, 未反应的铁粉沉淀在容器底部。氧化铁粉进一步处理。 该法是最早的苯胺工业生产方法,其污染环境,设备腐蚀严重, 操作维护费用高,难以连续化生产,苯胺回收率低,现已基本淘汰。 反应方程式:
硝基苯液相加氢制苯胺工艺 采用苯胺作为溶剂,以硅藻土为载体的活性镍为催化剂,载体的粒径 为200目,在反应时要及时移走反应中产生的水,防止水浸湿催化剂。当硝 基苯浓度较低时,如当苯胺的摩尔分数大于还原的摩尔分数时,该催化剂具 有很好的活性。一般在100℃、3MPa压力下反应。采用浆态床反应器或流 化床反应器,通过反应压力将反应物混合进行浓缩,从而去除反应热。 该技术的先进性在于氢气不必为高纯气,可以是摩尔比为3:1的H2与 N2的混合气体,而且混合气体可以循环使用。从加氢反应器出来的气体冷 却分离水汽后,再补充一部分氢气重新进入反应段反应,该工艺中必须具有 大量的循环气,确保快速移走反应中产生的水蒸气,并且确保催化剂悬浮在 反应段中 。 溶剂苯胺在液相中的质量分数维持在84%左右,而且反应温度在100℃,此 时制备的苯胺中含有质量分数丸0.6%的硝基苯,并含有其他具有氢化核的 杂质,需经过精馏装置对其精馏,才能得到高纯度苯胺。 乙醇重整制氢进行硝基苯原位液相加氢合成苯胺工艺 硝基苯在醇溶液及催化剂存在下,在190-230℃下进行还原反应,反应 时间5-6h,产品处理后得到苯胺。催化剂可选用Pt/Al2O3、NiB、Renay-Ni, 催化剂用量为原料质量的10%-20%,其中乙醇溶液中乙醇的质量分数为 92%-97%,反应从醇催化裂解直接获得氢,该氢可直接用于硝基苯催化加 氢反应,苯胺收率在99%以上,催化剂表现出较高的加氢活性和选择性。
硝基苯 氢气
99.5% 99%
收率98%以上,氢气:18540元/吨。
苯酚氨解法
原料名称
消耗定额 公斤/吨
苯酚
氨
1029
222
以苯酚计苯胺收率:90-95%,苯酚:1000元/吨,氨:200 元/吨。
计算
铁粉还原法:
生产成本:1.35×4100+1.6×2500+0.40×1100=9975 质量产率:1÷(1.35+1.6+0.40)×100%=29.9% 加氢还原法: 生产成本:氢的密度:0.0899kg/m³ , 氢的质量:660×0.0899=59.334kg, 1.35×4100+0.059334×18540=6635.05 质量产率:1÷(1.35+0.059334)×100%=70.9% 苯酚氨解法: 生产成本:1.029×1000+0.222×200=1253.4 质量产率:1÷(1.029+0.222)×100%=79.9%
4 C 6 H 5 NO
2
9 Fe 4 H 2 O 4 C 6 H 5 NH
2
3 Fe 3 O 4
苯酚氨化法 :
先将苯酚气化,然后与过量的氨(摩尔比为1:20)混合,进 入装有 SiO 2 Al 2 O 3 系催化剂的固定床管式反应器内,在400— —480℃,0.98——2.94兆帕条件下反应生成苯胺和水。自反应器 出来的气体反应物,经冷凝进入氨回收蒸馏塔回收氨气,并循环 使用。冷凝的含水苯胺经干燥脱水、蒸馏制得产品苯胺。在蒸馏 塔下部馏出苯胺-苯酚共沸物,供循环使用。塔底物含有二苯胺, 可通过间歇蒸馏回收。以苯酚计苯胺收率为90-95%,每吨苯胺消 耗苯酚1029公斤,氨222公斤。 反应方程式:
C 6 H 5 NO
2
3H
催化剂
2
C 6 H 5 NH
2
2 H 2O
其工艺流程为硫化床反应器装填催化剂后, 通入氢气并启动循环压 缩机, 采用中压蒸汽预热升温, 使催化剂床层温度升至150~ 180 ℃后, 开动硝基苯加料泵, 缓缓增加料量, 与氢气混合, 用2 . 45M Pa 的蒸汽 预热硝基苯和氢气混合物, 从硫化床底部送入, 以控制系统压力0 . 3M Pa, 待硫化床下段温度接近250 ℃时, 开动硫化床列管水泵与硫化床夹 套软水泵, 控制硫化床各段反应温度。含苯胺的水蒸气和过量的氢气的 气相反应物从硫化床的顶部析出, 经与新鲜氢气换热后进入冷却器,分 离出苯胺的不凝气, 液相部分送入苯胺分离器, 分离器上层的含苯胺废 水送入苯胺水贮槽。下层流出的粗苯胺进入粗苯胺水贮存槽, 粗苯胺经 脱水塔进料泵入脱水塔, 主要含水蒸气和少量苯胺的塔顶气冷凝后进入 苯胺水贮槽, 塔底液相进入精馏塔再进行减压蒸馏, 塔顶真空度大于或 等于97 kPa, 塔顶气相主要是精制苯胺, 冷凝后再送入成品贮槽。
