校园空气质量监测综合实验报告
环境大气实验报告

一、实验目的1. 了解大气环境监测的基本原理和方法。
2. 掌握大气中主要污染物(SO2、NOx、TSP)的测定方法。
3. 分析校园空气质量状况,为校园环境治理提供数据支持。
二、实验时间与地点2023年X月X日,山西大学校园内三、实验原理本次实验采用重量法测定大气中的SO2、NOx和TSP浓度。
具体原理如下:1. SO2测定:将空气通过装有硫酸溶液的吸收管,SO2被吸收生成硫酸氢钠,通过测定溶液中硫酸氢钠的浓度,计算出SO2的浓度。
2. NOx测定:将空气通过装有过硫酸钾溶液的吸收管,NOx被氧化成硝酸,通过测定溶液中硝酸的浓度,计算出NOx的浓度。
3. TSP测定:将空气通过中流量总悬浮颗粒物采样器,颗粒物被收集在滤膜上,通过称量滤膜的质量,计算出TSP的浓度。
四、实验材料与仪器1. 实验材料:硫酸溶液、过硫酸钾溶液、滤膜、蒸馏水等。
2. 仪器:空气采样器、酸度计、电子天平、温度计、湿度计等。
五、实验步骤1. SO2测定:a. 将空气采样器放置在实验地点,设定采样流量和采样时间。
b. 将装有硫酸溶液的吸收管连接到空气采样器,开始采样。
c. 采样结束后,将吸收管中的溶液转移到容量瓶中,用蒸馏水定容。
d. 使用酸度计测定溶液的pH值,根据pH值计算SO2的浓度。
2. NOx测定:a. 将空气采样器放置在实验地点,设定采样流量和采样时间。
b. 将装有过硫酸钾溶液的吸收管连接到空气采样器,开始采样。
c. 采样结束后,将吸收管中的溶液转移到容量瓶中,用蒸馏水定容。
d. 使用酸度计测定溶液的pH值,根据pH值计算NOx的浓度。
3. TSP测定:a. 将空气采样器放置在实验地点,设定采样流量和采样时间。
b. 将滤膜固定在中流量总悬浮颗粒物采样器上,开始采样。
c. 采样结束后,将滤膜取出,放入干燥器中干燥。
d. 使用电子天平称量干燥后的滤膜质量,根据质量差计算TSP的浓度。
六、实验结果与分析1. SO2浓度:实验测得SO2浓度为X mg/m³。
校园环境空气质量监测报告.

理工大学环境检测实验报告实验名称:校园环境空气质量测定姓名:学号:201班级:环境工程卓越132组号:第一组实验日期:2015-11-26指导教师:邓春玲一.实验目的和要求1.根据布点采样原则,选择适宜方法进行布点,确定采样频率及采样时间,掌握测定空气中的SO2、NOx、PM10的采样和监测方法。
2.根据三项污染物监测结果,计算空气污染指数(API),描述空气质量状况。
3.预习教材第三章中的相关内容,掌握环境监测理论和实验环节,通过课堂教学与实验教学结合,培养学生的组织能力、动手能力、培养分工合作、互相配合和团结协作的精神以及综合分析与处理问题的能力。
二.环境监测方案2.1监测资料的收集昆明理工大学呈贡校区位于云南省昆明市呈贡区,呈贡区空气质量常年保持良好及以上,极少出现轻度或重度污染状况,在全市空气质量排行榜中始终占据前两席。
整体空气质量呈现良好态势。
2.2 理工大学呈区南片区环境空气质量监测布点图监测地点如图为恬园七个地点,分别是:学生宿舍I,食堂,交通学院,环工学院,学生宿舍2,农工学院,化工学院。
人口分布于楼内,街道,大约在1.1万人。
车辆(轿车,摩托车)流量在2000辆左右,测量天气为雨天。
大学呈贡校区南片区环境空气质量监测布点图监测点○1:学生宿舍2;监测点○2:食堂监测○3:环工学院监测○4:交通学院;图1 昆明理工大学呈贡校区南片区平面图本次监测数据取自监测点○1:学生宿舍2;2.3监测因子SO2、NOx、PM102.4采样时间和频率按照环境空气质量监测技术规范,SO2、NOx日平均值的数值有效性规定为:每日至少有18h的采样时间;PM10日平均值有效性规定为:每日至少有12h的采样时间。
本次实验考虑以教学为主,根据实际情况每日采样时间调整为3h。
2015年11月26日(1)8:30 到达监测点(2)9:15-10:00 第一时段(3)10:30-11:15 第二时段(4)11:45-12:30 第三时段(5)13:00-13:45 第四时段2.5采样流量表1 各因子监测流量SO2 NOx PM10 TSP0.5L/min 0.3L/min 100L/min 100L/min2.6准备工作A.样品准备1.称量滤膜:(1)每组5个*2=10个;(2)称量;(3)封装:PM10。
环境监测综合性实验 (校园空气质量报告)

校园空气质量监测综合实验报告学院环境与资源学院学生姓名专业环境科学年级指导教师二Ο一Ο年十二月十八日校园空气质量监测综合实验报告前言山西省为产煤燃煤大省, 煤和其他化石燃料的的燃烧产生大量的SO2.NOx。
山西大学位于山西省省会太原市东南方向的城乡结合带, 紧临交通主干道坞城路, 附近有许西, 北张两个自主燃煤采暖的的城中村, 和一个垃圾焚烧厂。
煤和垃圾燃烧产生了大量的SO2.NOx, 同时汽车尾气液排放了大量的NOx。
其中SO2是主要空气污染物之一, 它能通过呼吸进入气管, 对局部组织产生刺激和腐蚀作用, 是诱发支气管炎等疾病的原因之一, 特别是当它与烟尘等气溶胶共存时可加重对呼吸道黏膜的损伤。
而NOx是引起支气管炎、肺损伤等疾病的有害物质。
TSP是大气环境中的主要污染物, 它可由燃煤、燃油、工业生产过程等人为活动排放出来, 也可以通过土壤、扬尘、沙尘经风力的作用输送到空气中而形成。
SO2.NOx和TSP都是环境监测必测项目, 通过对它们的测定可以及时全面地反映环境质量现状及发展趋势, 为保护人类健康和环境等服务。
一、实验目的和要求1.根据布点采样原则, 选择适宜方法进行布点, 确定采样频率及采样时间, 掌握测定空气中SO2.NOx 和TSP 的采样和监测方法。
2、根据三项污染物监测结果, 计算空气污染指数(API), 描述空气质量状况。
3、通过实验及计算直观的反映出山西大学校园的空气质量, 掌握环境监测的基本方法。
二、空气中SO2的测定(一)目的:1.掌握甲醛缓冲溶液吸收——盐酸副玫瑰苯胺分光光度法测定大气中SO2的方法;2.测量校园中SO2的浓度。
(二)原理:空气中的二氧化硫被四氯汞钾溶液吸收后, 生成稳定的二氯亚硫酸盐络合物, 此络合物再与甲醛及盐酸副玫瑰苯胺发生反应, 生成紫红色的络合物, 其最大吸收波长为577nm, 据其颜色深浅, 用分光光度法测定其吸光度, 与标准曲线对比, 对SO2进行含量回归, 从而测得空气中SO2的浓度。
大气污染PM2.5实验报告
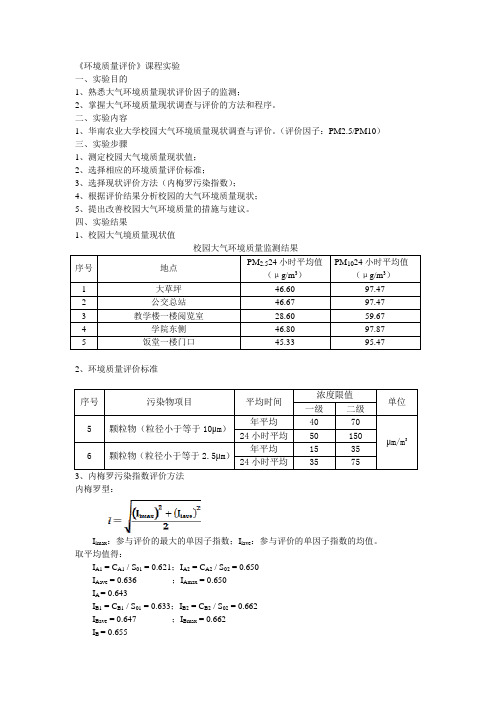
《环境质量评价》课程实验 一、实验目的1、熟悉大气环境质量现状评价因子的监测;2、掌握大气环境质量现状调查与评价的方法和程序。
二、实验内容1、华南农业大学校园大气环境质量现状调查与评价。
(评价因子:PM2.5/PM10) 三、实验步骤1、测定校园大气境质量现状值;2、选择相应的环境质量评价标准;3、选择现状评价方法(内梅罗污染指数);4、根据评价结果分析校园的大气环境质量现状;5、提出改善校园大气环境质量的措施与建议。
四、实验结果1、校园大气境质量现状值校园大气环境质量监测结果 序号 地点 PM 2.524小时平均值(μg/m 3)PM 1024小时平均值(μg/m 3)1 大草坪 46.60 97.472 公交总站 46.67 97.473 教学楼一楼阅览室28.60 59.67 4 学院东侧 46.80 97.87 5饭堂一楼门口45.3395.472、环境质量评价标准序号 污染物项目平均时间浓度限值 单位一级 二级 5颗粒物(粒径小于等于10μm )年平均 40 70 μm/m 324小时平均 50 150 6 颗粒物(粒径小于等于2.5μm )年平均15 35 24小时平均35 753、内梅罗污染指数评价方法 内梅罗型:I imax :参与评价的最大的单因子指数;I iave :参与评价的单因子指数的均值。
取平均值得:I A1 = C A1 / S 01 = 0.621;I A2 = C A2 / S 02 = 0.650 I Aave = 0.636 ;I Amax = 0.650 I A = 0.643I B1 = C B1 / S 01 = 0.633;I B2 = C B2 / S 02 = 0.662 I Bave = 0.647 ;I Bmax = 0.662 I B = 0.655I C1 = C C1 / S01 = 0.422;I C2 = C C2 / S02 = 0.441I Cave = 0.432 ;I Cmax = 0.441I C = 0.437I D1 = C D1 / S01 = 0.624;I D2 = C D2 / S02 = 0.652I Dave = 0.638 ;I Dmax = 0.652I D= 0.645I E1 = C E1 / S01 = 0.604;I E2 = C E2 / S02 = 0.632I Eave = 0.618 ;I Emax = 0.632I E = 0.6254、根据评价结果分析校园的大气环境质量现状;本次现状监测评价中,用综合污染指数法对校区的5个大气评价因子评价所得综合污染指数都小于1。
校园环境空气质量监测报告

校园环境空气质量监测报告
校园地处小谷围岛,四面环水,与市区分隔,有一条高速公路横跨校园与市区相连。
岛上是一个文化教育区,没有工业,绿化覆盖率较高,但树木还比较低矮,岛上空气质量比市区好。
为了进一步定量考察校园环境空气质量,本报告在前面方案的基础上选择了人口与商铺密集的生活商业区作为监测区,进行了4天空气质量监测,结果报告如下。
一、污染源调查结果
该区集中了本校所有的商铺、饭店、大排档及学生宿舍,周边有两条校园道路通过,污染源有:
(1)固定污染源:商业中心饭店、大排档、学生食堂及商业中心旁的停车场。
(2)流动污染源:广大路上机动车废弃排放
排放情况:一般在上午8:00-9:00,中午11:30-13:30,下午16:30-17:30时段车流量较大,其余时段相对较小
二、监测结果
采样日期:5月4日,气压=101.29KPa 温度=300.5K
5月5日,气压=101.11KPa 温度=301.4K
5月6日,气压=101.11KPa 温度=301.4K
应用标准:
三、监测结果与标准比较
将监测结果与环境空气标准做比较:
(1)二氧化硫:空气中含量太低,超过此方法的极限值,可认定为1级标准
(2)氮氧化物:未达标
(3)TSP:达到1级标准
四、空气质量评价:
空气质量达到预期结果,但由于校园附近有一条高速公路以及大气的流动性问题,氮氧化物超标也在预期之内。
五、建议
在学校与高速公路之间多种植树木对污染物吸附。
校园空气质量监测综合实验报告

校园空气质量监测综合实验报告学院学生姓名专业学号年级指导教师年 月校园空气质量监测综合实验报告前言基于我国城市空气以煤烟型污染为主的现状,规定用2SO 、X NO 和TSP 三项主要污染物指标计算空气污染指数(API ),表征空气质量状况。
一、实验目的和要求本实验为综合性实验,其内容包括:在欲监测环境内进行布点和采样;测定2SO 、XNO 和TSP 日均浓度;计算空气污染指数(API )。
二、空气中SO 2的测定(一)目的:(1) 掌握甲醛缓冲溶液吸收-盐酸副玖瑰苯胺分光光度法测大气2SO 的方法原理。
(2) 掌握大气采样及吸收液采集大气样品的操作技术。
(二)原理:2SO 被甲醛缓冲液吸收后,生成稳定的羟基甲磺酸碱化合物在样品溶液中加a N OH 使加成化合物分解,释放出的2SO 与盐酸副玖瑰苯胺作用,生成紫红色化合物,根据颜色深浅,用分光光度计在波长577nm 处用10cm 比色皿,以水为参比测定吸光度。
(三)干扰与消除:添加氨基磺酸钠,放置20min ,除去氮氧化物;放置30min 使3O 自行分解;添加二胺四乙酸钠盐,除去金属离子,如Fe 、Al 。
(四)实验步骤:1. 采样:用移液管移取5mL 吸收液,加入U 形多孔玻板吸收管内,然后将吸收瓶的出口(大肚口一端)与空气采样品相联接,以0.3L/min 流量采样1h ,记下采样时间,在采样的同时测定采样点现场的温度和大气压力,并做好记录,采样时间到了之后,密封好采样管,带回实验室测定。
2. 标线绘制(1) 取14支10mL 具塞比色管,分A 、B 两组,分别对应编号。
A 按表配标准色列,配好后再向各管中加0.25mL 氨磺酸钠溶液,放10min (消除x NO 干(2) 在B 组各管中加0.5mL 盐酸副玖瑰苯胺(PRA )使用液。
(3) 10min 后在A 管分别加入0.25mL a N OH 溶液(使加成化合物分解),混匀(仅摇一次或不摇使其自然混匀,摇晃过度会将生成的2SO 溢出),立即倒入对应的盛有PRA 使用溶液的B 管中,加一管倒一管,立即混匀,放入20C 恒温箱中显色20min 。
校园空气质量监测实验报告

校园空气质量监测综合实验报告学院环境与资源学院学生姓名专业环境科学学号年级 07 级指导教师二00九年十二月校园空气质量监测综合实验报告前言:山西大学位于太原市小店区,周围是生活区、商业区结合地段。
进入冬季采暖期后,校园内空气质量较差。
为了解校园空气质量状况,故设计了这次实验。
基于我国城市空气以煤烟型污染为主的现状,规定用SO2、NO X和TSP三项要紧污染物指标计算空气污染指数(API),表征空气质量状况。
本实验将采纳空气污染指数(API)表征校园空气质量状况。
TSP 是总悬浮颗粒物的简称。
按我国现行大气环境质量标准规定,为空气动力学当量直径在100μm以下的液体和固体微粒的总称。
微粒的直径在10μm 以下的(~10μm)称为可吸入颗粒物(MP10),而大于10μm 小于100μm的微粒因重力作用而易于沉降者称为降尘。
SO2的相对分子质量是,为无色、有强烈刺激必气味的气体,相对密度是,1L SO2气体在标准状况下重为2.93g,在0℃和20℃ 1L水中,别离能溶解、 SO2,熔点为℃,沸点为℃。
空气中含氮的氧化物有一氧化二氮、一氧化氮、二氧化氮、三氧化二氮等,其中占要紧成份的是一氧化氮和二氧化氮,以NOx(氮氧化物)表示。
氮氧化物主若是对呼吸器官有刺激作用。
由于氮氧化物较难溶于水,因此能侵入呼吸道深部细支气管及肺泡,并缓慢地溶于肺泡表面的水分中,形成亚硝酸、硝酸,对肺组织产生强烈的刺激及侵蚀作用,引发肺水肿。
亚硝酸盐进入血液后,与血红蛋白结合生成高铁血红蛋白,引发组织缺氧。
在一样情形,当污染物以二氧化氮为主时,对肺的损害比较明显,二氧化氮与支气管哮喘的发病也有必然的关系;当污染物以一氧化氮为主时,高铁血红蛋白症和中枢神经系统损害比较明显。
本次实验为综合性实验,其内容为在环境与资源学院周围进行采样,对SO2、NO X和TSP 一小时平均浓度进行测定,并计算空气污染指数(API)。
一、实验目的和要求1、依照布点采样规那么,选择适宜的方式进行布点,确信采样频率及采样时刻,把握测定空气中SO2、NO X和TSP的采样和监测方式。
校内空气监测实训总结报告

一、引言随着我国经济的快速发展,环境问题日益突出,空气质量问题更是备受关注。
为了提高学生的环保意识,培养具有环保技能的专业人才,我校开展了校内空气监测实训活动。
本次实训旨在让学生了解空气监测的基本原理、方法及设备操作,提高学生对空气质量的认识,为我国环保事业贡献一份力量。
以下是对本次实训的总结报告。
二、实训目的1. 让学生了解空气质量对人类健康的影响,提高环保意识。
2. 掌握空气监测的基本原理、方法及设备操作。
3. 培养学生独立分析问题和解决问题的能力。
4. 提高学生的团队协作精神。
三、实训内容1. 空气质量基础知识讲解2. 空气监测设备操作培训3. 校内空气监测实地操作4. 数据分析及报告撰写四、实训过程1. 空气质量基础知识讲解在实训开始前,教师首先向学生介绍了空气质量的基本概念、空气污染物的种类、空气质量指数(AQI)等相关知识,使学生了解空气质量对人类健康的影响,提高环保意识。
2. 空气监测设备操作培训教师详细讲解了空气监测设备的使用方法,包括PM2.5、PM10、SO2、NO2、CO等监测仪器的操作步骤。
学生通过实际操作,掌握了设备的正确使用方法。
3. 校内空气监测实地操作在教师指导下,学生分组进行校内空气监测。
监测地点包括教室、操场、食堂等。
学生按照操作规程,使用监测设备对空气中的污染物进行实时监测,并记录数据。
4. 数据分析及报告撰写实训结束后,学生将监测到的数据进行分析,整理成报告。
报告内容包括监测地点、监测时间、污染物浓度、空气质量评价等。
通过数据分析,学生了解了校内空气质量状况,为改善空气质量提供依据。
五、实训成果1. 学生掌握了空气监测的基本原理、方法及设备操作。
2. 学生提高了环保意识,关注空气质量问题。
3. 学生培养了独立分析问题和解决问题的能力。
4. 学生增强了团队协作精神。
六、实训体会1. 空气质量问题对人类健康影响巨大,我们要关注并改善空气质量。
2. 空气监测是一项重要的环保工作,需要我们共同努力。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
校园空气质量监测综合实验报告学院学生姓名专业学号年级指导教师XXXX年XX月前言基于我国城市空气以煤烟型污染为主的现状,规定用2SO、XNO和TSP三项主要污染物指标计算空气污染指数(API),表征空气质量状况。
本实验为综合性实验,其内容包括:在欲监测环境内进行布点和采样;测定SO2、NO X和TSP日均浓度;计算空气污染指数(API)。
一、实验目的和要求1.根据布点采样原则,选择适宜方法进行布点,确定采样频率及采样时间,掌握测定空气中的SO2、NO X、TSP的采样和监测方法。
2.根据三项污染物监测结果,计算空气污染指数(API),描述空气质量状况。
3.预习教材第三章中的相关内容,掌握环境监测理论和实验环节,通过课堂教学与实验教学结合,培养学生的组织能力、动手能力、培养分工合作、互相配合和团结协作的精神以及综合分析与处理问题的能力。
二、空气中NO2的测定(一)目的1.掌握盐酸萘乙二胺分光光度法测定大气中二氧化氮的方法和原理;2.了解主要干扰物及其消除方式;3.掌握大气采样器的操作技术;4.熟悉分光光度计的使用方法。
(二)原理用无水乙酸、对氨基苯磺酸和盐酸萘乙二胺配成吸收液,空气中的二氧化氮被吸收转变为亚硝酸、硝酸。
亚硝酸在无水乙醇存在下与对氨基苯磺酸发生重氮反应,然后再与氨基苯乙二胺偶合,生成玫瑰红色偶氮染料,其颜色深浅与NO2浓度成正比,可用分光光度法测定,由第一步反应可知,吸收液吸收空气中的NO2后,并未完全生成亚硝酸,故计算时应除以转化系数f=0.88。
(三)实验步骤1.采样。
取4ml显色液于多孔筛板吸收管中,再放入1ml重蒸水,用硅橡胶管将其串联在采样器上,调节流量至0.4L/min,置于采样点40min。
在采样的同时,应记录现场温度及大气压强,并设置空白对照(加入4ml显色液,1ml重蒸水,用一根橡胶管套住出气口及进气口,同时采样40min)。
2.绘制标准曲线。
取6支10ml具塞比色管,按下表参数和方法配制NO2标准溶液系列(2.5μg/ml)。
配好混匀置于暗处20min,用1cm比色皿于波长540nm处以水为参比,测量吸光度,扣除空白试剂吸光度后,绘制标准曲线并计算回归方程。
3.样品测定。
采样后置于暗处20min,混匀后按绘制标准曲线的方法测定样品与空白组的吸光度值,依式计算:C NOX=(A-A0-a)/bfV0式中:C NOX:空气中NO X的浓度(mg/m3);A、A0:分别为羊皮溶液和试剂空白溶液的吸光度;b、a:分别为标准曲线的斜率和截距;V0:换算成标准状况下的采样体积L;f:Saltzman实验系数,0.88。
1.标准曲线数据表NO 2-含量(μg)杯差吸光度 校正杯差和空白后吸光度A0 -0.056 -0.040 0 0.50 0.063 0.103 1.00 0.148 0.188 1.50 0.245 0.285 2.00 0.329 0.369 2.500.4310.4712.吸光度-甲醛含量标准曲线图3.样品测定结果吸光度A 减去空白后吸光度A平均值 空白 0.019 样品1 0.049 0.03 0.029样品20.0470.028采样地点:学院门口 温度:15.5℃ 大气压强:92.2Kpa 天气:晴朗、有风 采样流量:0.4L/min 采样时间:40min=⨯+⨯⨯=∴325.1012.925.15273273)404.0(0V 13.78 L=⨯⨯-=∴78.1388.0183.0008.0029.0c 0.0095 mg/m 31.干扰物及其去除:①大气中臭氧浓度超过0.25mg/m3时,会使吸收液略显红色,产生干扰,可以在采样时在吸收瓶入口端接一段15-20cm的硅胶管,即可将臭氧浓度降低到不干扰二氧化氮测定的水平。
②大气中二氧化硫浓度为二氧化氮浓度的10倍时,就会干扰二氧化氮测定,当超过其30倍时,会产生负干扰,可在采样管前接一个氧化管以消除二氧化硫的干扰。
③PAN也会使试剂显色而产生干扰,但一般环境大气中PAN的浓度很低,可以忽略其影响。
2.吸收液应避光,且不能长时间暴露在空气中,以防止光照时吸收液显色或吸收空气中的氮氧化物,而使试管空白值增高。
3.实验所用的亚硝酸钠固体应密封保存,防止空气及湿气侵入。
三、空气中SO2的测定(一)目的1.掌握甲醛吸收——盐酸副玫瑰苯胺分光光度法测定大气中SO2的原理和方法;2.了解主要的干扰物及其消除方法。
(二)原理空气中的SO2被甲醛缓冲溶液吸收后,生成稳定的羟基甲基磺酸加成化合物,加入氢氧化钠溶液使加成化合物分解,释放出SO2与盐酸副玫瑰苯胺反应,生成紫红色络合物,其最大吸收波长为577nm,用分光光度法测定。
(三)干扰与消除1.臭氧。
样品放置一段时间后可自行分解。
2.二氧化氮。
利用氨基磺酸钠来消除氮氧化物的干扰。
3.金属离子。
利用磷酸及环乙二胺四乙酸二钠盐来消除或减少某些金属离子的干扰。
(四)实验步骤1.采样。
(1)吸取5ml吸收液,于多孔筛板吸收管中,用硅橡胶管将其串联在空气采样器上,调节采样器流量为0.4L/min。
(2)设置采样时间为60min。
(3)在采样的同时,记录现场的温度和大气压,并设置空白对照组。
2.绘制标准曲线。
(1)取14支具塞比色管分成A、B两组分别对应编号。
(2)A组标液配好后加入6.0g/L的氨磺酸钠0.25ml,摇匀,放置10min。
(3)这10min期间向B组7支具塞比色管中均加入0.5ml盐酸副玫瑰苯胺(PRA)。
(4)10min后,向A组7支具塞比色管中加入0.25ml氢氧化钠溶液,迅速倒入A对应编号的B组试管中,按顺序加一管氢氧化钠倒一管,尽量将A组试管中的氢氧化钠倒干净,摇匀,从倒入的第一管开始计时,放置20min。
(5)显色时间到后,立即在577nm的波长下测吸光度,以SO2含量为横坐标,扣除空白的吸光度为纵坐标,作标准曲线。
3.样品测定。
将采样后的吸收液放置20min后,转入10ml比色管中,再加入0.25ml氨基磺酸钠,摇匀,放置min,以消除NO2的干扰。
以下同标准曲线绘制步骤。
按下式计算空气中SO2的浓度:c=(A-A0-a)/bV0式中:c:空气中SO2的质量浓度,mg/m3;A:样品溶液的吸光度;A0:试剂空白溶液的吸光度;a:所绘制标准曲线的截距;b:所绘制标准曲线的斜率;V0:换算成标况下的采样体积,L。
1.标准曲线数据表SO 2含量(μg)杯差吸光度 校正杯差和空白后吸光度A0 -0.001 0.041 0 0.50 0.079 0.038 1.00 0.120 0.079 2.00 0.227 0.186 3.00 0.300 0.259 4.00 0.368 0.327 5.000.4590.4182.吸光度-SO 2含量标准曲线图3.样品测定结果吸光度A 减去空白后吸光度A平均值 空白 0.044 样品1 0.054 0.01 0.01样品20.0540.01采样地点:学院门口 温度:18.9℃ 大气压强:93.05Kpa 天气:晴朗、无风 采样流量:0.4L/min 采样时间:60min=⨯+⨯⨯=∴325.10105.939.182********.00)(V 20.61 L=⨯-=∴61.20083.0002.001.0c 0.0047 mg/m 31.实验测得SO2浓度较低,很大可能是因为实验当天天气晴朗,空气质量较好,因此SO2浓度较低。
2.温度对此显色反应的影响较大,温度越高,空白值越大,且温度高时稳定时间短,应尽量控制恒温在15-25℃,并且根据实验室条件和不同季节的室温选择适宜的显色温度和时间;达到显色时间后立即测定。
3.实验中用到的氢氧化钠固体或溶液极易吸收空气中的SO2,使试剂空白值升高,应密封保存,或者使用小瓶分装,避免取液时间较长导致过程中吸收SO2或者试剂间通过移液管交叉污染,对于其他显色用试剂也应如此。
4.实验中观察到标准曲线空白试剂和空白样品测定的两组比色管中,溶液均呈轻微淡紫色,或许与3所述原因有关。
四、空气中总悬浮颗粒物(TSP)的测定(一)实验目的1.掌握重量法测定空气中TSP的方法和原理;2.练习使用中流量采样器。
(二)实验原理滤膜捕集——重量法:用抽气动力抽取一定体积的空气通过已恒重的滤膜,则空气中的悬浮颗粒物被阻留在滤膜上,根据采样前后滤膜质量之差及采样体积,即可计算TSP的浓度。
根据采样流量不同分为大流量、中流量、小流量采样法,本实验采用中流量采样器法。
(三)干扰和消除1.空气中的水分2.物理损伤(四)实验步骤1.用孔口流量计校正采样器的流量。
2.采样:用镊子取出称过的滤膜平放在采样器内的滤膜支持网上(毛面朝上),用滤膜夹夹紧,以100L/min的流量采样60min,记录采样流量和现场的温度及大气压,时间到后,用镊子轻轻取出滤膜,毛面向里对折放入滤膜袋内。
3.称量和计算:将采样滤膜和空白滤膜在相同的平衡条件下平衡24h后,用分析天平称量(精确到0.1mg),记下重量(增重不应小于10mg),按下式计算TSP含量。
TSP含量(μg/m3)=(W1-W2)×109/(Q×T)式中:W1:采样后的滤膜重量W2:空白滤膜的重量Q:采样器平均采样流量(L/min)T:采样时间(min)(五)实验结果1.采样地点;学院门口 温度:24℃; 大气压强:92.4Kpa ; 天气:晴朗、有风。
采样流量:100L/min 采样时间:60min 2.空白滤膜质量:0.3308g 采样滤膜质量:0.3321g393/67.2166010010)3308.03321.0(m /m g g TSP μ)含量(μ=⨯⨯-==0.2167mg/m 3(六)实验分析1.采样地点当时本身空气质量较好,并且有风,且风速较大,有利于空气中污染物质的稀释扩散,因此,测定结果较小。
2.误差分析:①由于滤膜采样前后只相差13mg ,因此,分析天平的精密度和准确度会对结果产生一定误差;②在将载有TSP 的滤膜从采样器取下到向天平转移的过程中也会产生少量损失。
3.TSP 主要影响因素:大气中TSP 的组成十分复杂,且变化很大,燃煤排放烟尘、工业废气中的粉尘及地面扬尘是大气中总悬浮颗粒的重要来源,因此,其含量主要受污染源影响如冬季燃煤供暖等。
另外气象条件如风速风向、雨、雪、雾等,城区规模、人口密度,地形、能源消费结构等也会对TSP 含量产生一定影响。
五、空气污染指数(API )计算表1 空气污染指数对应的污染物质量浓度限值① C (NO 2)=0.0095 mg/m 3<0.080 mg/m 3∴I NO2<50②C (SO 2)=0.0047 mg/m 3<0.050mg/m 3∴I SO2<50③C(TSP )=0.2167 mg/m 37750)50100(120.0300.0120.02167.0=+-⨯--=TSP I77),,(max 22==∴TSP NO SO I I I API∴校园空气首要污染物为总悬浮颗粒物,因风速较大,附近又无其他显著污染源,因此判断其主要来源是地面扬尘。
