酶底物试剂盒
α-淀粉酶测定试剂盒(CNPG3底物法)产品技术要求beiken
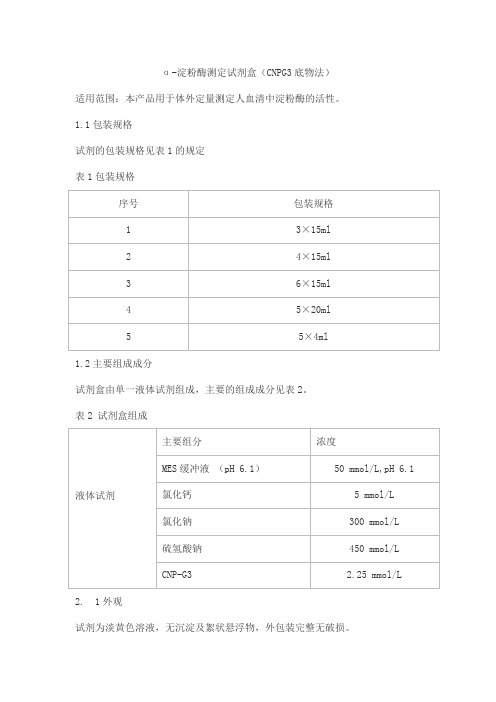
α-淀粉酶测定试剂盒(CNPG3底物法)适用范围:本产品用于体外定量测定人血清中淀粉酶的活性。
1.1包装规格试剂的包装规格见表1的规定表1包装规格1.2主要组成成分试剂盒由单一液体试剂组成,主要的组成成分见表2。
表2 试剂盒组成2. 1外观试剂为淡黄色溶液,无沉淀及絮状悬浮物,外包装完整无破损。
2. 2 净含量试剂的净含量应不少于标示值。
2. 3 试剂空白2.3.1试剂空白吸光度:用生理盐水测试试剂盒,在405nm的波长下记录试剂空白吸光度,应不大于0.35。
2.3.2 试剂空白吸光度变化率用生理盐水测试试剂盒,试剂空白吸光度变化率(ΔA/min)应不超过0.002。
2.4分析灵敏度测试校准品,1U/L的α-淀粉酶引起的吸光度变化值应≥0.0002。
2.5线性范围测试血清样本,试剂线性在[5,1000] U/L(37℃)范围内;a) 线性相关系数(r)应不小于0.990;b) 在[5,50]U/L范围内的绝对偏差不超过±5U/L,在(50,1000] U/L范围内的相对偏差应不超过±10%。
2.6精密度2.6.1重复性用质控品重复测试所得结果的重复性(变异系数,CV)应不大于5%。
2.6.2批间差试剂盒批间差应不大于10%。
2.7准确度:测试专用的标准物质(GBW(E)090286、GBW(E)090595、GBW(E)090593、GBW09177),所得准确度偏差不超过±10%.2.8 稳定性:试剂盒贮存在2℃~8℃条件下,有效期为24个月。
产品在有效期末测试2.1、2.3、2.4、2.5、2.6.1、2.7,结果符合各项要求。
天门冬氨酸氨基转移酶测定试剂盒(天门冬氨酸底物法)产品技术要求华宇亿康

天门冬氨酸氨基转移酶测定试剂盒(天门冬氨酸底物法)适用范围:本试剂用于体外定量测定人血清中天门冬氨酸氨基转移酶(AST)的活性。
1.1 产品型号/规格1×10mL;1×20mL;1×40mL;2×50mL;4×40mL;4×50mL;5×50mL;2×100mL;4×100mL;2×40mL;1×20L;1×10L;1×5L;1×1L。
1.2 主要组成成分试剂:Tris缓冲液 5.0mmol/L乳酸脱氢酶≥6000U/L苹果酸脱氢酶≥3000U/Lα-酮戊二酸 14.0mmol/LL-天门冬氨酸 210.0mmol/L烟酰胺嘌呤二核苷酸 0.18mmol/L2.1 外观和性状2.1.1 试剂盒各组分应齐全、完整、液体无渗漏;中文包装标签应清晰、准确、牢固。
2.1.2 试剂应为无色至浅黄色澄清液体。
2.2 净含量不少于标示值。
2.3 试剂空白2.3.1 试剂空白吸光度在光径1cm、主波长340nm下,以纯化水为检测样本时,吸光度应不小于1.000。
2.3.2 试剂空白吸光度变化率在光径1cm、主波长340nm下,以纯化水为检测样本时,吸光度变化率(△A/min)应不大于0.004。
2.4 分析灵敏度AST含量为100U/L时,测定吸光度变化率(△A/min)应在0.030~0.090范围内。
2.5 线性范围2.5.1 在[5,500]U/L范围内,相关系数r应不小于0.990;2.5.2 在[5,100]U/L范围内,线性绝对偏差应不超过±10U/L;在(100,500]U/L 范围内,线性相对偏差应不超过±10%。
2.6 测量精密度2.6.1 重复性分别重复测定高、低值两个浓度样本,测定结果的变异系数(CV)均应不大于5%。
2.6.2 批间差用三个批号的试剂盒测定同一浓度样本,测定结果的相对极差(R)应不大于10%。
γ-谷氨酰基转移酶测定试剂盒(GCANA底物法)产品技术要求zenmeixikema

γ-谷氨酰基转移酶测定试剂盒(GCANA底物法)适用范围:用于体外定量检测人血清中γ-谷氨酰基转移酶的活性。
1.1规格a) 试剂1:2×40ml,试剂2:2×10ml;b) 试剂1:2×80ml,试剂2:2×20ml;c) 试剂1:4×60ml,试剂2:4×15ml;d) 试剂1:2×60ml,试剂2:2×15ml;e) 试剂1:2×72ml,试剂2:2×18ml;f) 试剂1:12×16ml,试剂2:12×4ml;g) 试剂1:2×400ml,试剂2:2×100ml;h) 试剂1:8×60ml,试剂2:2×60ml;i) 试剂1:3×80ml,试剂2:3×20ml;j) 试剂1:1×40ml,试剂2:1×10ml;k) 试剂1:4×40ml,试剂2:4×10ml。
1.2 组成试剂主要组分见表1:表1 试剂主要组分2.1 外观外包装完整无破损,标签清晰;试剂1应为无色或淡黄色透明溶液;试剂2应为淡黄色溶液。
2.2 净含量应不低于试剂瓶标示装量。
2.3 试剂空白2.3.1 试剂空白吸光度在405nm处测定试剂空白吸光度,应<0.8。
2.3.2 试剂空白吸光度变化率试剂空白吸光度变化率(△A/min)应≤0.005。
2.4 分析灵敏度测定浓度为50U/L的样品,吸光度变化率(△A/min)应不低于0.012。
2.5 线性2.5.1在[5,450]U/L范围内,线性回归的相关系数应不低于0.990;2.5.2测试浓度(50,450]U/L的样品,相对偏差应不超过±10%;测试浓度[5,50]U/L的样品,绝对偏差应不超过±5U/L。
2.6 重复性2.6.1 批内重复性变异系数(CV)应不超过5%。
γ-谷氨酰基转移酶测定试剂盒(GCANA底物法)产品技术要求lepu

γ-谷氨酰基转移酶测定试剂盒(GCANA底物法)适用范围:用于体外定量测定人血清中的γ-谷氨酰基转移酶的活性。
1.1 规格试剂盒是由试剂1和试剂2组成的液体双试剂。
规格及装量见表1。
表1 规格及装量1.2主要组成成分试剂1主要组分:试剂2主要组分:2.1 净含量应不低于试剂瓶标示装量。
2.2 外观试剂1:无色或淡黄色透明溶液;试剂2:淡黄色或黄色溶液。
外包装完好、无破损,标签完好、字迹清晰。
2.3 试剂空白2.3.1试剂空白吸光度在405nm处测定试剂空白吸光度,应≤1.5。
2.3.2试剂空白吸光度变化率在37℃、405nm波长、1cm光径条件下,用生理盐水作为样品加入试剂测试时,试剂空白吸光度变化率△A/min应不大于0.005。
2.4 分析灵敏度测试50U/L的被测物时,吸光度变化率(ΔA/min)应不低于0.0015。
2.5 准确度用参考物质(GBW09177)对试剂(盒)进行测试,相对偏差不超过±10%。
2.6 重复性用血清样品或质控样品重复测试所得结果的变异系数(CV)应不大于5%。
2.7 线性2.7.1测试血清样本在[3,1200]U/L(37℃)区间内,线性相关系数r应不小于0.990;2.7.2 [3,50]U/L区间内,线性绝对偏差应不超过±5U/L;(50,1200]U/L区间内,线性相对偏差应不超过±10%。
2.8 批间差试剂(盒)批间相对极差应不大于10%。
2.9 稳定性取在2℃~8℃条件下贮存达到12个月后的试剂进行检测,检测结果应符合2.2、2.3、2.4、2.5、2.6、2.7的要求。
α-淀粉酶(AMY)测定试剂盒(EPS底物法)产品技术要求sainuopu
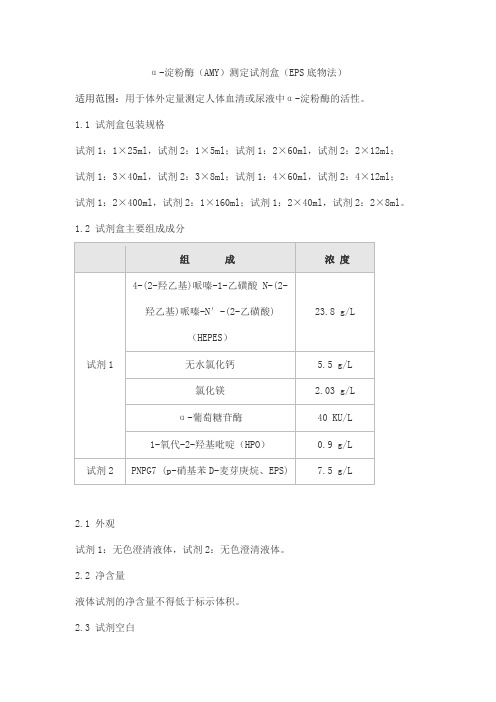
α-淀粉酶(AMY)测定试剂盒(EPS底物法)适用范围:用于体外定量测定人体血清或尿液中α-淀粉酶的活性。
1.1 试剂盒包装规格试剂1:1×25ml,试剂2:1×5ml;试剂1:2×60ml,试剂2:2×12ml;试剂1:3×40ml,试剂2:3×8ml;试剂1:4×60ml,试剂2:4×12ml;试剂1:2×400ml,试剂2:1×160ml;试剂1:2×40ml,试剂2:2×8ml。
1.2 试剂盒主要组成成分2.1 外观试剂1:无色澄清液体,试剂2:无色澄清液体。
2.2 净含量液体试剂的净含量不得低于标示体积。
2.3 试剂空白2.3.1试剂空白吸光度在37℃、405nm波长、1cm光径条件下,试剂空白吸光度应不大于0.35。
2.3.2试剂空白吸光度变化率在37℃、405nm波长、1cm光径条件下,试剂空白吸光度变化率(ΔA/min)应不大于0.002。
2.4 分析灵敏度测定活性为100U/L样本时,吸光度变化率(ΔA/min)应不小于0.006。
2.5 线性范围在(5,1000)U/L线性范围内,线性相关系数r不小于0.996。
在[50,1000)U/L,范围内的线性相对偏差不大于±10%;测定结果(5,50)U/L时,线性绝对偏差不大于±5U/L。
2.6 重复性重复测试两份高低浓度的样本,所得结果的变异系数(CV%)应不大于5%。
2.7 批间差不同批号试剂测试同一份样本,测定结果的批间相对极差应不大于6%。
2.8 准确度相对偏差:相对偏差应不大于±10%。
2.9 稳定性效期稳定性:试剂盒在2℃~8℃下有效期为12个月,取失效期的试剂盒进行检测,试验结果应满足2.1、2.3、2.4、2.5、2.6、2.8要求。
α-淀粉酶测定试剂盒(EPS底物法)产品技术要求huayuyikang

α-淀粉酶测定试剂盒(EPS底物法)适用范围:用于体外定量测定人血清、尿液中α-淀粉酶的含量。
1.1 产品型号/规格试剂1:1×15 ml、试剂2:1×5 ml;试剂1:1×30 ml、试剂2:1×10 ml;试剂1:2×30 ml、试剂2:2×10 ml;试剂1:4×30 ml、试剂2:4×10 ml;试剂1:4×60 ml、试剂2:4×20 ml;试剂1:2×60 ml、试剂2:2×20 ml;试剂1:5×60 ml、试剂2:5×20 ml;试剂1:2×45 ml、试剂2:2×15 ml;试剂1:6×60 ml、试剂2:3×40 ml;试剂1:5×30 ml、试剂2:1×50 ml;试剂1:4×30 ml、试剂2:2×20 ml;试剂1:3×50 ml、试剂2:1×50 ml;试剂1:8×16.8 ml、试剂2:8×5.6 ml。
1.2 主要组成成分主要组成成分见表2。
表2 主要组成成分试剂1为无色澄清液体,目测不得有任何沉淀及絮状悬浮物;试剂2为无色澄清液体,目测不得有任何沉淀及絮状悬浮物;试剂盒标签标识清晰,外包装完整无损。
2.2 净含量试剂的净含量应不少于标称量。
2.3 试剂空白2.3.1 试剂空白吸光度试剂空白:A405nm(主)/A700nm(副)下测定空白吸光度应≤0.1000。
2.3.2 试剂空白吸光度变化率用生理盐水作为样品加入试剂测试时,试剂空白吸光度变化率(△A/min)应不超过0.002。
2.4 准确度用国际参考物质IRMM/IFCC 456,对试剂盒进行测试,相对偏差应不大于±10%。
2.5 分析灵敏度试剂盒测试290U/L淀粉酶时,吸光度变化率(△A/min)应在0.0300~0.0600之间。
α-淀粉酶测定试剂盒(EPS底物法)产品技术要求wantaiderui

α-淀粉酶测定试剂盒(EPS底物法)适用范围:用于体外定量测定人血清中淀粉酶的活性。
1.1包装规格1)试剂1:60mL×8 、试剂2:48mL×2;2)试剂1:65mL×3 、试剂2:39mL×1;3)试剂1:50mL×4 、试剂2:20mL×2;4)试剂1:50mL×1 、试剂2:10mL×1;5)试剂1:100mL×2 、试剂2:20mL×2。
1.2组成成分试剂1:HEPES缓冲液(pH 7.25) 50 mmol/L氯化钠 50 mmol/La-葡糖苷酶>4500 U/L试剂2:HEPES缓冲液(pH 7.15) 50 mmol/L4,6-Ethylidene-G7PNP 5mmol/L2.1试剂装量应不低于瓶签标示装量。
2.2外观试剂1:无色澄清液体;试剂2:无色或微黄色澄清液体。
2.3试剂空白吸光度测定温度:37℃;测定波长:405nm;比色杯光径:1.0cm;其空白吸光度应<0.35,空白吸光度变化率︱△A︱<0.002/min。
2.4准确度按试剂盒的说明书操作,测试国家标准物质GBW(E) 09053,计算检测结果与标准物质标示值的偏差,偏差应不超过±10%。
2.5精密度2.5.1重复性重复测定一个浓度水平质控血清,其结果的变异系数(CV)应不超过5%。
2.5.2 批间差重复测定质控血清,其结果相对极差R不超过10%。
2.6线性在[5,1000]U/L范围内,线性回归的相关系数应不低于0.99,[5,50]U/L 浓度的线性绝对偏差不超过±5U/L,(50,1000]U/L浓度的线性相对偏差应不超过±10%。
2.7分析灵敏度1U/L淀粉酶样本的吸光度差值为:0.0001≤︱△A︱≤0.01。
2.8稳定性原包装试剂盒在2℃~8℃条件下贮存达到12个月,性能指标应符合2.2、2.3、2.4、2.5.1、2.6、2.7之规定。
ABP海肾萤光素酶检测试剂盒

1ABP 海肾萤光素酶检测试剂盒货号: FP306, FP307表 1. 试剂盒组分和储存条件 材料 体积 浓度 储存条件 有效期ABP 海肾萤光素酶检测试剂盒 (货号 FP306)按照推荐的储存条件保存有效期为6个月,请注意避免反复冻融。
海肾荧光素酶底物 (组分 A)100 µL 100X -20 o C ,避光海肾荧光素酶Buffer (组分 B) 10 mL1X ABP 海肾萤光素酶检测试剂盒 (货号 FP307)海肾荧光素酶底物 (组分 A)500 µL 100X -20 oC ,避光海肾荧光素酶Buffer (组分B) 50 mL1X产品介绍通过检测报告基因的表达来研究真核基因表达调控是在生物技术和制药工业中常用的方法。
其中萤火虫荧光素酶是最常用的报告基因,目前通过寻找更小的报告基因及不需要ATP 作为辅酶的报告基因产生了一些其它报告基因。
海肾荧光素酶来源于海肾,是一个分子量为36 kDa 的单体蛋白。
这个酶不依赖于ATP (图1),并且信号强度与荧光素酶含量成正比。
图1. 海肾荧光素酶反应.ABP 海肾荧光素酶检测试剂盒是一种简单可靠的用于测定样品中含海肾荧光素酶报告基因的检测系统。
试剂盒中的海肾荧光素酶底物和Buffer 混合后形成海肾荧光素酶检测试剂,可直接加入到细胞生长的培养基中,无需清洗和预处理。
检测试剂与细胞培养常用的培养基兼容,并且光信号的半衰期在1个小时左右。
海肾荧光素酶检测试剂可在培养基中直接裂解细胞并产生发光的信号具有以下特征 :简单: 可在培养基中直接裂解细胞并测定荧光素酶活性,无需清洗。
信号稳定: 发光信号稳定性强,半衰期在1h 左右。
适应性强: 试剂盒适用于多种真核细胞 (包括贴壁的和悬浮的)。
高通量: "add-and-read"模式适用于高通量检测。
注意事项1. 用于细胞培养的多孔板(96- 或384- 孔板)必须与用于检测化学发光的仪器兼容。
化学发光检测试剂盒原理

化学发光检测试剂盒原理
化学发光检测试剂盒是一种用于检测目标物质浓度的分析试剂盒。
其原理是通过化学反应产生发光信号,并利用发光信号的强度与目标物浓度之间的关系进行定量分析。
一般来说,化学发光检测试剂盒包含两种试剂:底物和酶。
底物是指与目标物质发生化学反应后产生发光信号的化合物,酶则是催化这个反应的催化剂。
当目标物存在于待测样品中时,它与底物发生特定的化学反应。
这个化学反应可以是酶促反应、氧化还原反应或其他与目标物质的性质有关的反应。
反应产物中的底物会发生发光反应,产生可检测的发光信号。
发光信号可以利用光学仪器进行测量和定量分析。
一般采用光电倍增管或光电二极管测量发光信号的强度,然后与已知浓度的标准曲线相比较,从而确定待测样品中目标物质的浓度。
化学发光检测试剂盒具有灵敏度高、选择性好、操作简便快速等优点,广泛应用于生物医学、环境监测、食品安全等领域。
酶联免疫试剂盒检测通则

酶联免疫试剂盒检测通则
酶联免疫试剂盒(enzyme-linked immunosorbent assay, ELISA)是一种用于检测生物样本中特定目标物质(如蛋白质、抗原、抗体等)的常用技术。
以下是酶联免疫试剂盒的一般检测通则:
1. 样本准备:收集并处理生物样本,如血清、尿液、细胞上清等。
根据试剂盒说明书的指导,稀释样本,以确保目标物质在检测范围内。
2. 试剂准备:根据试剂盒说明书的指导,将试剂盒中的各种试剂(包括标准品、检测抗体、底物等)进行适当的稀释和混合。
3. 建板:将稀释好的样本和试剂加入孔板中。
通常,在每一孔中加入相同体积的样本或试剂。
4. 孵育:用适当的温度和时间孵育孔板中的样本和试剂,以使目标物质与检测抗体结合形成复合物。
5. 清洗:将孔板中的溶液倒掉,并用缓冲液彻底洗涤孔板,以去除未结合的物质。
6. 加底物:将底物加入孔板中,底物在酶的作用下转化为可测量的信号物质。
7. 反应终止:根据试剂盒说明书的指导,选择适当的反应终止剂,并将其加入孔板中,以停止底物的反应。
8. 读板:使用专门的读板仪器,测量孔板中的信号物质的光学密度或发光强度。
这些数据将用于计算目标物质在样本中的浓度。
9. 数据分析:根据试剂盒提供的标准品曲线,将测量得到的光学密度或发光强度值转化为目标物质的浓度。
需要注意的是,具体的操作步骤可能因试剂盒的不同而有所变化,因此,在使用酶联免疫试剂盒之前,请仔细阅读和遵循试剂盒说明书中的操作指南。
γ-谷氨酰基转移酶测定试剂盒(GCANA底物法)产品技术要求shouyi

γ-谷氨酰基转移酶测定试剂盒(GCANA底物法)适用范围:本试剂用于体外定量测定人血清中γ-谷氨酰基转移酶的活性。
1.1产品规格试剂1:3×80ml,试剂2:3×20ml;试剂1:4×60ml,试剂2:4×15ml;试剂1:6×40ml,试剂2:3×20ml;试剂1:2×80ml,试剂2:2×20ml 1.2产品组成成分试剂1:Tris缓冲液100mmol/L,甘氨酰甘氨酸150mmol/L。
试剂2:γ-谷氨酰-3-羧基-4硝基苯胺 5.0mmol/L。
2.1 外观试剂1为无色透明溶液,试剂2为略带黄色透明溶液。
2.2 装量液体试剂的净含量应不少于标示值。
2.3 试剂空白2.3.1试剂空白吸光度A≤0.70(光径1.0cm,405nm波长)。
2.3.2 试剂空白吸光度变化率ΔA/5min≤0.01。
2.4分析灵敏度测定93.8U/L被测物,吸光度变化率在0.0278/min~0.057/min范围内。
2.5 准确度相对偏差在±13%范围内。
2.6 精密度2.6.1 重复性变异系数CV≤5%。
2.6.2 批间差批间相对极差≤6%。
2.7 线性区间a)(0,500]U/L(37℃)。
在规定的线性区间内,测定值与样本浓度值的相关系数(r)应不低于0.990。
b)(0,80]U/L区间内,线性绝对偏差应不超过±8U/L;(80,500]U/L 区间内,线性相对偏差应不超过±10%。
2.8稳定性原装试剂2~8℃避光保存,有效期12个月,有效期满后两个月内测定结果应符合2.3、2.4、2.5、2.6.1、2.7的要求。
碱性磷酸酶测定试剂盒(NPP底物—AMP缓冲液法) 产品技术要求广州市伊川生物科技

碱性磷酸酶测定试剂盒(NPP 底物-AMP 缓冲液法)
性能指标
1.外观和性状
1.1试剂盒各组分应齐全、完整、无液体渗漏;中文包装标签应清晰,准确、牢固;
1.2试剂R1 应为无色澄清液体、无沉淀、无悬浮物、无絮状物。
1.3试剂R2 应为无色或淡黄色澄清液体,无沉淀、无悬浮物、无絮状物。
2.装量
液体试剂的净含量应不小于标示量。
3.准确度
采用对比试验,相关系数r2 应≥0.95;[0,100]U/L 区间内,偏差应不超过±10U/L;(100,1000] U/L 区间内,偏差应不超过±10%。
4. 分析灵敏度
ALP活性为120U/L时,平均每分钟吸光度变化率(△A/min)应≥0.03。
5.试剂空白
5.1试剂空白吸光度
在温度37℃、波长405nm条件下检测,试剂工作液空白吸光度应≤0.50(比色杯光径1.0cm)。
5.2试剂空白吸光度变化率
用生理盐水作为样品测试时,试剂空白吸光度变化率(△A/min)≤0.005 (比色杯光径1.0cm)。
6.线性区间
线性区间在0~1000 U/L区间内:
a)理论浓度与实测浓度的线性相关系数︱r︳应≥0.990。
b)[0,100] U/L区间内,线性偏差应不超过±10 U/L;(100,1000] U/L区间内,线性偏差应不超过±10%。
(温度37℃、波长405nm、比色杯光径1.0cm) 7.精密度
7.1重复性
变异系数(CV)≤5%。
7.2批间差
相对极差(R)≤10%。
丙氨酸氨基转移酶测定试剂盒原理

丙氨酸氨基转移酶测定试剂盒原理一、引言丙氨酸氨基转移酶(Aspartate Aminotransferase,简称AST)是一种存在于多种组织和细胞内的酶。
AST的测定对于诊断和评估多种疾病具有重要意义,特别是与心肌梗死、肝疾病和肝细胞损伤相关的疾病。
丙氨酸氨基转移酶测定试剂盒是用于测定血清或血浆中AST水平的一种常用试剂盒。
本文将详细讨论丙氨酸氨基转移酶测定试剂盒的原理及其应用。
二、试剂盒原理试剂盒主要包括两个试剂:底物和辅酶。
底物一般为丙氨酸和α-酮戊二酸。
辅酶则为重要的催化底物转化过程的参与者。
1. 底物的使用丙氨酸和α-酮戊二酸是常用的AST底物。
丙氨酸是AST的氨基供体,而α-酮戊二酸是AST的接受者。
2. 丙氨酸氨基转移酶的反应过程丙氨酸氨基转移酶催化的反应是丙氨酸和α-酮戊二酸之间的转氨基反应。
该反应的化学方程式如下:丙氨酸+ α-酮戊二酸⇌ L-谷氨酰基丙酮酸 + L-天冬氨酸该反应是可逆的,AST能够在体液中进行反应转化。
通过测定该反应中生成的L-谷氨酰基丙酮酸或L-天冬氨酸的含量,就可以间接反映出AST的活性。
3. 辅酶的作用辅酶在丙氨酸氨基转移酶的催化反应中起到重要的作用,可以促进底物的转化并催化产生特定的化合物。
辅酶的种类有很多,其中比较常见的有辅酶A、辅酶B6等。
三、测定原理丙氨酸氨基转移酶测定试剂盒的原理是基于酶促反应和光度法测定酶的活性。
其测定步骤如下:1. 取样和预处理取待测样品(血清或血浆),并根据试剂盒的要求进行预处理。
预处理过程可能包括稀释、离心等步骤,以确保样品符合试剂盒的操作要求。
2. 添加试剂将试剂盒提供的底物和辅酶加入到样品中。
底物和辅酶的浓度在试剂盒中已经根据实验要求进行了优化。
3. 酶促反应在试剂的催化下,丙氨酸和α-酮戊二酸发生酶促反应。
该反应生成的产物L-谷氨酰基丙酮酸或L-天冬氨酸的浓度与AST的活性相关。
4. 光度法测定使用光度计测定反应产物浓度的变化。
菌落总数酶底物法原始记录

菌落总数酶底物法原始记录一、引言菌落总数酶底物法是一种常用的微生物计数方法,通过将菌落作为菌落酶底物来测定菌落总数。
本文旨在介绍菌落总数酶底物法的原始记录方法。
二、实验材料与方法1. 实验材料- 菌落总数酶底物试剂盒- 菌落计数平板- 培养基- 无菌培养皿- 秤量纸- 管口塞瓶2. 实验步骤1) 将菌落计数平板标记编号,并在每个平板上绘制三个待测试样品的三倍稀释液。
2) 使用无菌技术将待测试样品依次转移到各个平板上。
3) 使用菌落计数器对每个平板上的菌落进行计数,并将结果记录下来。
4) 使用菌落总数酶底物试剂盒来测定菌落总数,并将结果记录下来。
5) 将实验过程中的所有废液和废物进行处理,确保不对环境造成污染。
三、实验结果记录样品编号平板编号菌落计数菌落总数-------------------------------------1 A1 30 5.36×10^3 CFU/ml1 A2 26 4.64×10^3 CFU/ml1 A3 33 5.86×10^3 CFU/ml2 B1 62 1.10×10^4 CFU/ml2 B2 57 1.02×10^4 CFU/ml2 B3 60 1.07×10^4 CFU/ml3 C1 18 3.20×10^3 CFU/ml3 C2 22 3.92×10^3 CFU/ml3 C3 20 3.56×10^3 CFU/ml四、数据分析与讨论根据实验结果,我们可以得出以下结论:1. 样品1的菌落总数分别为5.36×10^3 CFU/ml、4.64×10^3 CFU/ml和5.86×10^3 CFU/ml。
2. 样品2的菌落总数分别为1.10×10^4 CFU/ml、1.02×10^4 CFU/ml和1.07×10^4 CFU/ml。
肌酸激酶测定试剂盒(磷酸肌酸底物法)产品技术要求zhongshengbeikong

肌酸激酶测定试剂盒(磷酸肌酸底物法)适用范围:本产品用于体外定量测定人血清中肌酸激酶的活性。
1.1包装规格液体双剂型试剂1(R1):80mL×2,试剂2(R2):40mL×2;试剂1(R1):80mL×2,试剂2(R2):20mL×4;试剂1(R1):60mL×2,试剂2(R2):30mL×2;试剂1(R1):50mL×2,试剂2(R2):25mL×2;试剂1(R1):4mL×1,试剂2(R2):2mL×1。
1.2主要组成成分试剂1(R1)液体:己糖激酶(HK)≥3000U/L葡萄糖-6-磷酸脱氢酶≥2000U/LADP 2mmol/LAMP 5mmol/LApA 10μmol/L5NAC 20mmol/L磷酸肌酸 30mmol/L试剂2(R2)液体:NADP 2mmol/L葡萄糖 20mmol/L2.1 外观试剂盒中各组件的外观应满足:2.1.1试剂1(R1)应为无色透明溶液,无杂质、无絮状物,外包装完整无破损。
2.1.2试剂2(R2)应为无色透明溶液,无杂质、无絮状物,外包装完整无破损。
2.2 净含量液体试剂净含量应不少于标示值。
2.3 试剂空白吸光度在波长340nm(光径1cm)处,试剂空白吸光度(A)应≤0.500;试剂空白吸光度变化率(△A/min)应≤0.002。
2.4准确度测定GBW(E)090593,相对偏差应不超过±10%。
2.5分析灵敏度对应于活性为300U/L的肌酸激酶所引起的吸光度变化率(△A/min)的绝对值应在0.035~0.070的范围内。
2.6重复性重复测试同一样本,变异系数(CV)应≤5%。
2.7批间差测试同一样本,批间差(R)应≤6%。
2.8线性范围在[24,1500]U/L范围内,线性相关系数(r)应≥0.990;在(100,1500]U/L范围内,线性相对偏差应不超过±10%;在[24,100]U/L范围内,线性绝对偏差应不超过±10U/L。
酶活试剂盒原理

酶活试剂盒原理悄悄地告诉你一个小秘密:酶活试剂盒是生物学实验中常用的一种工具,它能够帮助科研人员快速、准确地检测酶的活性。
那么,酶活试剂盒是如何实现这一目标的呢?让我们来了解一下酶的活性是什么意思。
酶是一类特殊的蛋白质,它们在生物体内发挥着催化反应的作用。
而酶的活性则是指单位时间内酶能够催化的反应物数量。
酶活试剂盒的原理就是利用一种特殊的底物和检测方法来测定酶的活性。
酶活试剂盒中的底物通常是一种与酶特异性反应的物质,可以被酶催化产生某种可测定的产物。
例如,对于乳酸脱氢酶活性的检测,底物就是乳酸和辅酶NAD+,而产物则是产生的丙酮酸和还原的辅酶NADH。
通过测定产生的NADH的光密度或荧光强度,就可以间接地测定酶的活性。
在实验过程中,科研人员将待测酶样品与特定底物和辅酶混合,然后加入试剂盒中提供的试剂,如缓冲液、显色剂等。
这些试剂能够在一定条件下,与产生的产物发生化学反应,形成可以测量的信号。
通过测量这些信号的强度,就可以推断出酶的活性。
酶活试剂盒的优势在于其快速、准确、灵敏的特点。
与传统的酶活性测定方法相比,酶活试剂盒不仅操作简便,而且能够在短时间内完成试验,并且结果可靠。
这使得科研人员能够更加高效地进行实验研究,提高实验数据的可信度。
当然,酶活试剂盒也有一些限制。
首先,由于底物的选择受到限制,所以只有特定酶的活性可以被测定。
其次,酶活试剂盒的结果受到许多因素的影响,如温度、pH值等。
因此,在使用酶活试剂盒时,科研人员需要严格控制这些因素,以确保实验结果的准确性。
酶活试剂盒通过特定底物和检测方法,可以快速、准确地测定酶的活性。
它为科研人员提供了一种便捷而可靠的实验工具,促进了生物学研究的发展。
在未来,酶活试剂盒将继续发挥重要的作用,助力科学家们更好地理解和探索生命的奥秘。
磷酸酶试剂盒法的原理

磷酸酶试剂盒法的原理
磷酸酶试剂盒法是一种用于检测磷酸酶活性的常用方法。
其原
理是利用磷酸酶对底物的催化作用来产生可测量的信号,从而间接
地测定样品中磷酸酶的活性水平。
首先,磷酸酶试剂盒通常包含底物、缓冲液和检测试剂。
底物
是磷酸酶的底物类似物,一般为对硝基苯磷酸酯(pNPP)或者其他
类似底物。
当磷酸酶存在时,它会催化底物的水解反应,产生一个
可测量的产物,比如对硝基苯酚。
检测试剂可以用于测定产物的浓度,一般是通过比色反应或者荧光信号来实现。
在进行实验时,首先将样品加入含有底物的反应体系中,然后
经过一定时间的反应,停止反应并加入检测试剂。
产生的产物会导
致溶液颜色的变化或者荧光强度的变化,其变化程度与磷酸酶活性
的水平成正比。
通过比较样品产生的信号与标准曲线或对照样品的
信号,可以计算出样品中磷酸酶的活性。
总的来说,磷酸酶试剂盒法利用磷酸酶对底物的催化作用来间
接测定样品中磷酸酶的活性水平,是一种常用的生物化学分析方法。
通过测定磷酸酶活性,可以在许多生物学和医学研究领域中对细胞信号转导、疾病诊断和药物筛选等方面提供重要信息。
谷胱甘肽还原酶测定试剂盒(谷胱甘肽底物法)产品技术要求jiuqiang

谷胱甘肽还原酶测定试剂盒(谷胱甘肽底物法)适用范围:本试剂盒用于体外定量测定人血清谷胱甘肽还原酶的含量。
1.1 包装规格包装规格见表1。
表1 包装规格1.2 主要组成成分主要组成成分见表2。
表2 主要组成成分2.1 外观试剂1a为无色澄清液体,目测不得有任何沉淀及絮状悬浮物;试剂1b为无色或浅黄色粉末状物质,复溶后为无色或浅黄色液体,目测不得有任何沉淀及絮状悬浮物;试剂2为无色或浅黄色粉末状物质,复溶后为无色或浅黄色液体,目测不得有任何沉淀及絮状悬浮物;质控品为无色或浅黄色粉末状物质,复溶后为无色或浅黄色液体,目测不得有任何沉淀及絮状悬浮物。
试剂盒标签标识清晰,外包装完整无损。
2.2 净含量液体试剂的净含量应不少于标称量。
2.3 试剂空白吸光度2.3.1 试剂空白吸光度A340nm下测定空白吸光度应≤1.5000。
2.3.2 试剂空白吸光度变化率A340nm下测定试剂空白吸光度变化率(ΔA/min)应≤ 0.0100。
2.4 准确度与已上市产品进行比对试验:在[12,184] U/L区间内,相关系数r≥0.975,在[12,50] U/L区间内测定的绝对偏差应不超过±7.5 U/L,在(50,184]U/L区间内测定的相对偏差应不超过±15%。
2.5 分析灵敏度样本浓度为70U/L时,其吸光度变化率应不超过0.5000。
2.6 线性范围在[12,184] U/L区间内,线性相关系数r≥0.990,在[12,50]U/L区间内线性绝对偏差应不超过±7.5U/L,在(50,184] U/L区间内线性相对偏差应不超过±15%。
2.7 测量精密度2.7.1 重复性使用高、低不同浓度的血清样本或质控品重复测定10次,其测定值的变异系数(CV%)应不大于10%。
2.7.2 批间差随机抽取三批试剂盒的批间相对极差(R)应不大于10%。
2.8 瓶间差试剂1b、试剂2、质控品的瓶间差应≤10%。
α-淀粉酶测定试剂盒(EPS底物法)产品技术要求aiweide

α-淀粉酶测定试剂盒(EPS底物法)适用范围:本试剂适用于体外定量测定人体血清中淀粉酶的活性。
1.1 包装规格a) 试剂1:2×45 mL,试剂2:2×15mL;b) 试剂1:4×45 mL,试剂2:4×15mL;c) 试剂1:2×60mL,试剂2:2×20mL。
1.2 主要组成成分1.2.1试剂1主要组分Tris缓冲液50 mmol/L葡糖苷酶25000 U/L氯化钠50 mmol/L牛血清白蛋白适量1.2.2试剂2主要组份Tris缓冲液50 mmol/LP-硝基苯D-麦芽庚烷(PNPG7)0.9 mmol/L氯化钙 5 mmol/L牛血清白蛋白适量2.1外观试剂1:无色澄清液体;试剂2:无色或微黄色澄清液体。
2.2试剂装量应不低于试剂瓶标示装量。
2.3 试剂空白2.3.1试剂空白吸光度在405nm处测定试剂空白吸光度,应≤0.7。
2.3.2试剂空白吸光度变化率在405nm处测定空白吸光度变化率|△A/min|≤0.05。
2.4分析灵敏度测定AMY含量为200U/L样本时,其|△A/min|应≥0.02。
2.5线性范围2.5.1测试浓度在[0,1000] U/L范围内,线性回归的相关系数(r)应不低于0.990;2.5.2测试浓度在[0,100] U/L范围内,线性绝对偏差应不超过±10U/L;测试浓度在(100,1000]U/L范围内,线性相对偏差应不超过±10%。
2.6 测量精密度2.6.1重复性:重复测试三个水平样本,所得结果的变异系数(CV)应不大于5%。
2.6.2批间差:抽取3个不同批号的试剂,对同一份样本进行重复测定,相对极差≤10%。
2.7准确度以国家标准物质为检测样本时,测定结果相对偏差不超过±10%。
2.8 稳定性取在2℃~8℃条件下贮存达到18个月的试剂进行检测,应符合2.1、2.3、2.4、2.5、2.6.1、2.7的要求。
丙氨酸氨基转移酶试剂盒(丙氨酸底物法)

丙氨酸氨基转移酶试剂盒(丙氨酸底物法)标准化操作规程1 目的规范实验室操作,保证检验工作顺利有效进行特制定此规程。
2 授权操作人经培训且考核通过的实验室检验人员。
3 适用范围:本试剂适用于体外定量检测人血清或血浆中丙氨酸氨基转移酶(ALT)的活力。
4 检验方法本试剂反应原理采用国际临床化学联合会(IFCC)推荐的方法。
5 检验原理在丙氨酸氨基转移酶的作用下,L-丙氨酸与α-酮戊二酸反应,生成丙酮酸和L-谷氨酸。
丙酮酸被试剂中的乳酸脱氢酶(LDH)还原为L-乳酸,同时NADH 被氧化为NAD+,使340nm处的光吸收值下降,通过监测340nm处光吸收值下降的速率,可以测定丙氨酸氨基转移酶活力。
样品中内源性丙酮酸的干扰可由试剂中LDH在反应延迟时间内消除,不会干扰测定。
ALTL-丙氨酸+α-酮戊二酸丙酮酸+L-谷氨酸LDH丙酮酸+NADH L-乳酸+NAD+6 检验标本要求6.1 样本为血清。
6.2 不得使用溶血或被污染的样本。
6.3 样本在2℃~8℃条件下可保存7天、室温条件下可保存1天。
7 试剂及配套品7.1试剂来源长春迪瑞医疗科技股份有限公司丙氨酸氨基转移酶试剂盒7.2试剂组成7.3试剂的稳定性与贮存:7.3.1 试剂在2℃~8℃条件下,干燥、避光、密封贮存,有效期为18个月。
7.3.2 试剂开封后在2℃~8℃条件下可稳定30天,试剂不可冷冻。
7.3.3 反应液在2℃~8℃可稳定30天。
7.4试剂的变质指示:若试剂混浊,或在340 nm处试剂空白吸光度值低于1.000A 时,不能使用。
8 实验仪器及性能指标8.1实验仪器迪瑞CS系列全自动生化分析仪8.2试剂性能指标8.2.1 空白吸光度:A≥1.000。
8.2.2 空白吸光度变化率:︱△A︱/min≤0.002/min。
8.2.3 分析灵敏度:测试1U/L被测物时,吸光度变化率(△A/min)<-0.0001。
8.2.4 线性范围:4U/L~1000U/L;线性相关系数r≥0.9900;[4,200]U/L范围内,线性绝对偏差应不超过±40U/L;(200,1000]范围内,线性相对偏差不超过±15%。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
酶底物试剂盒
水质大肠菌群酶底物法检测系统:
由2010A程控定量封口机、51或97孔检测板、100mL定量瓶、酶底物试剂四部分组成。
检测水样范围:饮用水、源水、瓶装水、中水、二次供水、管网水、废水、食品水、畜牧用水、医疗用水等。
该检测方法采用大肠杆菌产生β-半乳糖苷酶分解色源底物-ONPG(Ortho-nitrophenyl-β-D-galactopyranoside) 使培养液呈黄色。
大肠埃希氏菌产生β-葡萄糖醛酸酶(β-glucuronidase)分解MUG(4 - methyl-umbelliferyl-β-glucuronide)使培养液在波长366 nm 紫外光下产生荧光的原理,来定性定量水中总大肠菌群、粪大肠菌群(耐热大肠菌群)及大肠埃希氏菌。
该检测方法是国际上发达国家普遍采用的检测方法,相比我国标准的检测方法,如多管发酵及滤膜法具简便快捷,其选择性培养基具有抑制杂菌的作用,假阳性低,定量准确。
由于该方法的方便快速,在实验室日常检测中能提高效率,缩短检测时间,在应急监测中能及时报出数据,避免造成大的公共安全事故.。
