高中化学各类有机物之间的相互转化关系(精装版)
高中化学各类有机物之间的相互转化关系(精装版)
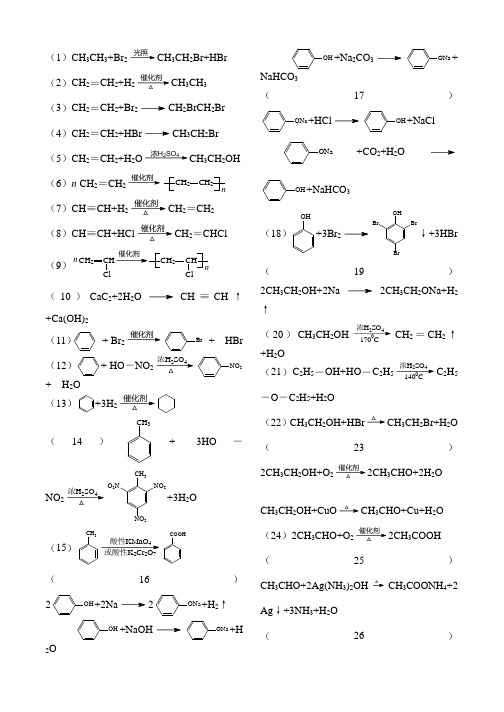
(1)CH 3CH 3+Br 2光照CH 3CH 2Br+HBr (2)CH 2=CH 2+H 2催化剂△CH 3CH 3 (3)CH 2=CH 2+Br 2CH 2BrCH 2Br(4)CH 2=CH 2+HBr CH 3CH 2Br(5)CH 2=CH 2+H 2O 浓H 2SO 4CH 3CH 2OH(6)n CH 2=CH 2催化剂CH 2CH 2n(7)CH ≡CH+H 2催化剂△CH 2=CH 2 (8)CH ≡CH+HCl 催化剂△CH 2=CHCl(9)CH 2CH Cl2CH Cln n(10)CaC 2+2H 2O CH ≡CH ↑+Ca(OH)2 (11) + Br 2催化剂Br+ HBr(12)+ HO -NO 22SO 4△NO 2+ H2O (13)+3H 2催化剂△(14)CH 3+ 3HO -NO 22SO 4△CH 3O 2N NO 2NO 2+3H 2O(15)CH 34或酸性K 2Cr 2O 7COOH(16)2OH +2Na2ONa +H 2↑OH +NaOH ONa+H2OOH +Na 2CO 3ONa+NaHCO 3 (17)ONa +HClOH +NaClONa+CO 2+H 2OOH +NaHCO 3(18)OH+3Br 2OHBrBrBr↓+3HBr(19)2CH 3CH 2OH+2Na 2CH 3CH 2ONa+H 2↑(20)CH 3CH 2OH 2SO 40CH 2=CH 2↑+H 2O(21)C 2H 5-OH+HO -C 2H 5浓H 2SO 40C 2H 5-O -C 2H 5+H 2O (22)CH 3CH 2OH+HBr△CH 3CH 2Br+H 2O(23)2CH 3CH 2OH+O 2催化剂△2CH 3CHO+2H 2OCH 3CH 2OH+CuO△CH 3CHO+Cu+H 2O(24)2CH 3CHO+O 2催化剂△2CH 3COOH(25)CH 3CHO+2Ag(NH 3)2OH △CH 3COONH 4+2Ag ↓+3NH 3+H 2O (26)CH 3CHO+2Cu(OH)2△CH 3COOH+Cu 2O ↓+2H 2O(27)CH 3CHO+H 2催化剂△CH 3CH 2OH(28)CH 3COOH+HOC 2H 5浓H 2SO 4△CH 3COOC 2H 5+H 2O (29)CH 3COOC 2H 5+H 2O 稀H 2SO 4△CH 3COOH+C 2H 5OH (30)2CH 3COOH+2Na2CH 3COONa+H 2↑2CH 3COOH+Na 2O2CH 3COON a+H 2OCH 3COOH+NaOHCH 3COONa +H 2O2CH 3COOH+Na 2CO 32CH 3COONa+H 2O+CO 2↑CH 3COOH+NaHCO 3CH 3COONa+H 2O+CO 2↑ (31)CH 3COOC 2H 5+NaOH△CH 3COONa+C 2H 5OH (32)CH 3CH 2Br+NaOH△水CH 3CH 2OH+NaBr(33)CH 3CH 2Br+NaOH △乙醇CH 2=CH 2↑+NaBr+H 2O (34)CH 2BrCH 2Br + 2NaOH△水CH 2OH CH 2OH+2NaBr (35)CH 2BrCH 2Br+2NaOH △乙醇CH ≡CH↑+2NaBr+2H 2O(36)CH 2OH CH 2OH +O 2催化剂△CHO CHO+2H 2O(37)CHO CHO+O 2催化剂△COOH COOH(38)CHOCHO +2H 2催化剂△CH 2OH CH 2OH(39)COOH COOH +CH 2OH CH 2OH2SO 4△C O C O OO CH 2CH 2+2H 2O(40)n COOHCOOH +n CH 2OH CH 2OH 浓H 2SO 4△C HO O C OO CH 2CH 2O H n+(2n -1)H 2O各类有机物之间的相互转化关系CHCH3323高聚酯CH3CH2ONaCH32233。
高三有机化学中有机物间相互转化关系图

一、有机物间相互转化关系二、能与溴水发生化学反应而使溴水褪色或变色的物质1、有机物:⑴ 不饱和烃(烯烃、炔烃、二烯烃等)⑵ 不饱和烃的衍生物(烯醇、烯醛、烯酸、烯酯、油酸、油酸酯等) ⑶ 石油产品(裂化气、裂解气、裂化汽油等)⑷ 含醛基的化合物(醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖等) ⑸ 天然橡胶(聚异戊二烯)2、无机物:⑴ -2价的S (硫化氢及硫化物)⑵ + 4价的S (二氧化硫、亚硫酸及亚硫酸盐) ⑶ + 2价的Fe6FeSO 4 + 3Br 2 = 2Fe 2(SO 4)3 + 2FeBr 36FeCl 2 + 3Br 2 = 4FeCl 3 + 2FeBr 32FeI 2 + 3Br 2 = 2FeBr 3 + 2I 2⑷ Zn 、Mg 等单质 如 ⑸ -1价的I (氢碘酸及碘化物)变色 ⑹ NaOH 等强碱、Na 2CO 3和AgNO 3等盐 Br 2 + H 2O = HBr + HBrO2HBr + Na 2CO 3 = 2NaBr + CO 2↑+ H 2O HBrO + Na 2CO 3 = NaBrO + NaHCO 3三、能萃取溴而使溴水褪色的物质上层变无色的(ρ>1):卤代烃(CCl 4、氯仿、溴苯等)、CS 2等;下层变无色的(ρ<1):直馏汽油、煤焦油、苯及苯的同系物、低级酯、液态环烷烃、液态饱和烃(如己烷等)等 四、能使酸性高锰酸钾溶液褪色的物质1、有机物:⑴ 不饱和烃(烯烃、炔烃、二烯烃等)⑵ 不饱和烃的衍生物(烯醇、烯醛、烯酸、烯酯、油酸、油酸酯等) ⑶ 石油产品(裂化气、裂解气、裂化汽油等) ⑷ 醇类物质(乙醇等)⑸ 含醛基的化合物(醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖等) ⑹ 天然橡胶(聚异戊二烯) ⑺ 苯的同系物变色 Mg + Br 2 === MgBr 2 (其中亦有Mg 与H +、Mg 与HBrO 的反应)△2、无机物:⑴ 氢卤酸及卤化物(氢溴酸、氢碘酸、浓盐酸、溴化物、碘化物) ⑵ + 2价的Fe (亚铁盐及氢氧化亚铁) ⑶ -2价的S (硫化氢及硫化物)⑷ + 4价的S (二氧化硫、亚硫酸及亚硫酸盐) ⑸ 双氧水(H 2O 2)五、常见的各类有机物的官能团,结构特点及主要化学性质(1) 烷烃A) 官能团:无 ;通式:C n H 2n +2;代表物:CH 4B) 结构特点:键角为109°28′,空间正四面体分子。
高三有机化学中有机物间相互转化关系图word版本

高三有机化学中有机物间相互转化尖系图、有机物间相互转化尖系HOCH地0HBrCH.CHM-ECHrCHC 比241CH3CH2ONa WC£H5GH3COOC2H5、能与漠水发生化学反应而使漠水褪色或变色的物质1有机物:(1)不饱和坯(烯泾、決屋、二烯怪等)⑵不饱和疑的衍生物(烯醇、烯醛、烯酸、烯酯、油酸、油酸酯等)⑶石油产品(裂化气、裂解气、裂化汽油等)⑷含醛基的化合物(醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖等)⑸天然橡胶(聚异戊二烯)2、无机物:(1)—2价的S (硫化氢及硫化物)(2) + 4价的S (二氧化硫、亚硫酸及亚硫酸盐)(3) + 2 价的Fe6FeS0 4- 3Br2= 2F® (S04)3 +2FeB I6FeCl2 + 3Br2 = 4FeCla + 2FeBr3 J 父巳2Fel2 + 3Br2 = 2FeBr3 + 2b+,Mg + Br 2 === MgBr 2 (其中亦有Mg 与H+、Mg 与HBrO 的反应)(4) Zn、Mg等单质女口(5) -1价的I (氢碘酸及碘化物)变色(6)NaOH 等强碱、Na2CO3和AgNO3等盐Br2+H2O = HBr + HBrO2HBr + Na2CO3 = 2NaBr + CO21 + H2OHBrO + Na2CO3 = NaBrO + NaHCOa、能萃取漠而使漠水褪色的物质上层变无色的(P>1):卤代坯(CCI4、氯仿、漠苯等)、CS2等;下层变无色的(P V1 ):直镭汽油、煤焦油、苯及苯的同系物、低级酯、液态环烷怪、液态饱和姪(如己烷等)等四、能使酸性高镒酸钾溶液褪色的物质1、有机物:(1)不饱和坯(烯怪、快姪、二烯坯等)(2)不饱和泾的衍生物(烯醇、烯醛、烯酸、烯酯、油酸、油酸酯等)(3)石油产品(裂化气、裂解气、裂化汽油等)(4)醇类物质(乙醇等)(5)含醛基的化合物(醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖等)(6)天然橡胶(聚异戊二烯)⑺苯的同系物2、无机物:(1)氢卤酸及卤化物(氢漠酸、氢碘酸、浓盐酸、漠化物、碘化物)(2)+ 2价的Fe (亚铁盐及氢氧化亚铁)(3)-2价的S (硫化氢及硫化物)(4)+4价的S (二氧化硫、亚硫酸及亚硫酸盐)⑸双氧水(H2O2 )五、常见的各类有机物的官能团,结构特点及主要化学性质(1)烷姪A ) 官能团:无;通式:CnH2n +2 ;代表物:CH4B ) 结构特点:键角为109。
各类有机物之间的转化关系

NO2
OH
乙炔
SO 3H
OH
Br
Br
Br
CH3Cl
CHO
CH3
COOH
Cl
OH
苯甲酸苯甲酯
CH2=CH2 CH2Cl-CH2Cl
三、乙二醇线
环状的乙二 CH2OH-CH2OH OHC-CHO HOOC-COOH 聚乙二酸 乙二醇酯 酸乙二酯
CH2=CH2 CH3-CHO
四、有机玻璃线
①CH3MgCl ②H2O HCN CH3-CHOHCH3
八、聚己二酸乙二醇酯线
CH≡ CH CH2=CH2 CH2=CH-C ≡ CH CH2=CH-CH=CH2 环己烯 己二酸 CH2OH-CH2OH
乙 二 醇 酯
聚 己 二 酸
已知: 已知: 醛或酮与HCN的加成反应; 的加成反应; ①醛或酮与 的加成反应 腈的水解规律 规律。 ②腈的水解规律。 以苯为唯一的有机原料, 以苯为唯一的有机原料,合成
CH3-CO-CH3
2-甲基-2-羟 甲基- - 甲基 基丙腈 2-甲基丙烯酸 甲基丙烯酸 有机玻璃
2-甲基-2-羟 甲基- - 甲基 基丙酸 2-甲基丙烯酸甲酯 甲基丙烯酸甲酯
五、聚乳酸线
CH3-CHOHCH3 CH3-CHCl-CH2Cl CH3-CO-CHO CH3-CH=CH2 = CH3-CHOH-CH2OH CH3-CO-COOH 环状酯 CH3-CHOH-COOH 聚乳酸
六、涤纶线
对二甲苯
对苯二 氯甲烷
对苯二 甲醇
对 苯 二 甲 醇 酯 涤 纶
聚 对 苯 二 甲 酸
对苯二甲醛
对苯二甲酸 二醇
1,2-二氯 烷 二氯
七、丁苯橡胶线
高三有机化学中有机物间相互转化关系图解析
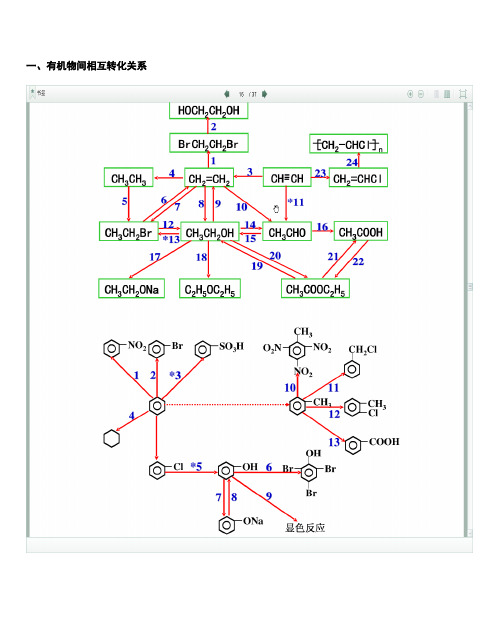
一、有机物间相互转化关系二、能与溴水发生化学反应而使溴水褪色或变色的物质1、有机物:⑴ 不饱和烃(烯烃、炔烃、二烯烃等)⑵ 不饱和烃的衍生物(烯醇、烯醛、烯酸、烯酯、油酸、油酸酯等) ⑶ 石油产品(裂化气、裂解气、裂化汽油等)⑷ 含醛基的化合物(醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖等) ⑸ 天然橡胶(聚异戊二烯)2、无机物:⑴ -2价的S (硫化氢及硫化物)⑵ + 4价的S (二氧化硫、亚硫酸及亚硫酸盐) ⑶ + 2价的Fe6FeSO 4 + 3Br 2 = 2Fe 2(SO 4)3 + 2FeBr 36FeCl 2 + 3Br 2 = 4FeCl 3 + 2FeBr 32FeI 2 + 3Br 2 = 2FeBr 3 + 2I 2⑷ Zn 、Mg 等单质 如 ⑸ -1价的I (氢碘酸及碘化物)变色 ⑹ NaOH 等强碱、Na 2CO 3和AgNO 3等盐 Br 2 + H 2O = HBr + HBrO2HBr + Na 2CO 3 = 2NaBr + CO 2↑+ H 2O HBrO + Na 2CO 3 = NaBrO + NaHCO 3三、能萃取溴而使溴水褪色的物质上层变无色的(ρ>1):卤代烃(CCl 4、氯仿、溴苯等)、CS 2等;下层变无色的(ρ<1):直馏汽油、煤焦油、苯及苯的同系物、低级酯、液态环烷烃、液态饱和烃(如己烷等)等 四、能使酸性高锰酸钾溶液褪色的物质1、有机物:⑴ 不饱和烃(烯烃、炔烃、二烯烃等)⑵ 不饱和烃的衍生物(烯醇、烯醛、烯酸、烯酯、油酸、油酸酯等) ⑶ 石油产品(裂化气、裂解气、裂化汽油等) ⑷ 醇类物质(乙醇等)⑸ 含醛基的化合物(醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖等) ⑹ 天然橡胶(聚异戊二烯) ⑺ 苯的同系物变色 Mg + Br 2 === MgBr 2 (其中亦有Mg 与H +、Mg 与HBrO 的反应)△2、无机物:⑴ 氢卤酸及卤化物(氢溴酸、氢碘酸、浓盐酸、溴化物、碘化物) ⑵ + 2价的Fe (亚铁盐及氢氧化亚铁) ⑶ -2价的S (硫化氢及硫化物)⑷ + 4价的S (二氧化硫、亚硫酸及亚硫酸盐) ⑸ 双氧水(H 2O 2)五、常见的各类有机物的官能团,结构特点及主要化学性质(1) 烷烃A) 官能团:无 ;通式:C n H 2n +2;代表物:CH 4B) 结构特点:键角为109°28′,空间正四面体分子。
高考化学 第十一章 本章重要有机物之间的转化关系
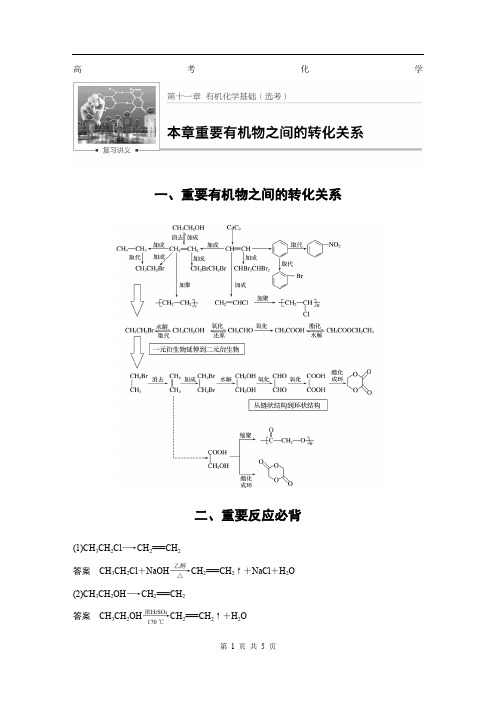
高考化学一、重要有机物之间的转化关系二、重要反应必背(1)CH 3CH 2Cl ―→CH 2===CH 2答案 CH 3CH 2Cl +NaOH ――→乙醇△CH 2===CH 2↑+NaCl +H 2O (2)CH 3CH 2OH ―→CH 2===CH 2答案 CH 3CH 2OH ―――→浓H 2SO 4170 ℃CH 2===CH 2↑+H 2O(3)CH 3CH 2OH ―→CH 3CHO答案 2CH 3CH 2OH +O 2――→Cu △2CH 3CHO +2H 2O (4)CH 3CH 2OH 和CH 3COOH 生成乙酸乙酯答案 CH 3COOH +CH 3CH 2OH浓H 2SO 4△CH 3COOC 2H 5+H 2O(5)OHC —CHO ―→HOOC —COOH答案 OHC —CHO +O 2――→催化剂△HOOC —COOH (6)乙二醇和乙二酸生成聚酯答案 n HOCH 2—CH 2OH +n HOOC —COOH 一定条件(7)乙醛和银氨溶液的反应答案 CH 3CHO +2Ag(NH 3)2OH ――→△CH 3COONH 4+2Ag ↓+3NH 3+H 2O(8)乙醛和新制Cu(OH)2悬浊液的反应答案 CH 3CHO +2Cu(OH)2+NaOH ――→△CH 3COONa +Cu 2O ↓+3H 2O(9)答案 +2NaCl +2H 2O(10)答案(11) 和饱和溴水的反应答案(12) 和溴蒸气(光照)的反应答案(13)OH 和HCHO 的反应答案+(n -1)H 2O(14)酯在碱性条件的水解(以乙酸乙酯在NaOH 溶液中为例)答案 CH 3COOC 2H 5+NaOH ――→△CH 3COONa +C 2H 5OH(15)+NaOH ――→△答案 +2NaOH ――→△CH 3COONa ++H 2O三、有机物的检验辨析1.卤代烃中卤素的检验取样,滴入NaOH 溶液,加热至分层现象消失,冷却后加入稀硝酸酸化,再滴入AgNO 3溶液,观察沉淀的颜色,确定是何种卤素。
(完整word版)高三有机化学中有机物间相互转化关系图

(完整word版)高三有机化学中有机物间相互转化关系图一、有机物间相互转化关系二、能与溴水发生化学反应而使溴水褪色或变色的物质1、有机物:⑴ 不饱和烃(烯烃、炔烃、二烯烃等)⑵ 不饱和烃的衍生物(烯醇、烯醛、烯酸、烯酯、油酸、油酸酯等)⑶ 石油产品(裂化气、裂解气、裂化汽油等)⑷ 含醛基的化合物(醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖等)⑸ 天然橡胶(聚异戊二烯)2、无机物:⑴ -2价的S (硫化氢及硫化物)⑵ + 4价的S (二氧化硫、亚硫酸及亚硫酸盐)⑶ + 2价的Fe6FeSO 4 + 3Br 2 = 2Fe 2(SO 4)3 + 2FeBr 36FeCl 2 + 3Br 2 = 4FeCl 3 + 2FeBr 32FeI 2 + 3Br 2 = 2FeBr 3 + 2I 2⑷ Zn 、Mg 等单质如⑸ -1价的I (氢碘酸及碘化物)变色⑹ NaOH 等强碱、Na 2CO 3和AgNO 3等盐 Br 2 + H 2O = HBr + HBrO2HBr + Na 2CO 3 = 2NaBr + CO 2↑+ H 2O HBrO + Na 2CO3 = NaBrO + NaHCO 3三、能萃取溴而使溴水褪色的物质上层变无色的(ρ>1):卤代烃(CCl 4、氯仿、溴苯等)、CS 2等;下层变无色的(ρ<1):直馏汽油、煤焦油、苯及苯的同系物、低级酯、液态环烷烃、液态饱和烃(如己烷等)等四、能使酸性高锰酸钾溶液褪色的物质1、有机物:⑴ 不饱和烃(烯烃、炔烃、二烯烃等)⑵ 不饱和烃的衍生物(烯醇、烯醛、烯酸、烯酯、油酸、油酸酯等)⑶ 石油产品(裂化气、裂解气、裂化汽油等)⑷ 醇类物质(乙醇等)⑸ 含醛基的化合物(醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖等)⑹ 天然橡胶(聚异戊二烯)⑺ 苯的同系物变色 Mg + Br 2 === MgBr 2 (其中亦有Mg 与H +、Mg 与HBrO 的反应)△2、无机物:⑴ 氢卤酸及卤化物(氢溴酸、氢碘酸、浓盐酸、溴化物、碘化物)⑵ + 2价的Fe (亚铁盐及氢氧化亚铁)⑶ -2价的S (硫化氢及硫化物)⑷ + 4价的S (二氧化硫、亚硫酸及亚硫酸盐)⑸ 双氧水(H 2O 2)五、常见的各类有机物的官能团,结构特点及主要化学性质(1) 烷烃A) 官能团:无;通式:C n H 2n +2;代表物:CH 4B) 结构特点:键角为109°28′,空间正四面体分子。
高三有机化学中有机物间相互转化关系图

一、有机物间相互转化关系二、能与溴水发生化学反应而使溴水褪色或变色的物质1、有机物:⑴不饱和烃(烯烃、炔烃、二烯烃等)⑵不饱和烃的衍生物(烯醇、烯醛、烯酸、烯酯、油酸、油酸酯等)⑶石油产品(裂化气、裂解气、裂化汽油等)⑷含醛基的化合物(醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖等)⑸天然橡胶(聚异戊二烯)2、无机物:⑴-2价的S (硫化氢及硫化物)⑵+ 4价的S (二氧化硫、亚硫酸及亚硫酸盐)⑶+ 2价的Fe6FeSO 4 + 3Br 2 = 2Fe 2(SO 4)3 + 2FeBr 36FeCl 2 + 3Br 2 = 4FeCl 3 + 2FeBr 32FeI 2 + 3Br 2 = 2FeBr 3 + 2I 2⑷Zn 、Mg 等单质如⑸-1价的I (氢碘酸及碘化物)变色⑹NaOH 等强碱、Na 2CO 3和AgNO 3等盐Br 2 + H 2O = HBr + HBrO2HBr + Na 2CO 3 = 2NaBr + CO 2↑+ H 2O HBrO + Na 2CO 3 = NaBrO + NaHCO 3三、能萃取溴而使溴水褪色的物质上层变无色的(ρ>1):卤代烃(CCl 4、氯仿、溴苯等)、CS 2等;下层变无色的(ρ<1):直馏汽油、煤焦油、苯及苯的同系物、低级酯、液态环烷烃、液态饱和烃(如己烷等)等四、能使酸性高锰酸钾溶液褪色的物质1、有机物:⑴不饱和烃(烯烃、炔烃、二烯烃等)⑵不饱和烃的衍生物(烯醇、烯醛、烯酸、烯酯、油酸、油酸酯等)⑶石油产品(裂化气、裂解气、裂化汽油等)⑷醇类物质(乙醇等)⑸含醛基的化合物(醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖等)⑹天然橡胶(聚异戊二烯)⑺苯的同系物变色Mg + Br 2 === MgBr 2(其中亦有Mg 与H +、Mg 与HBrO 的反应)△2、无机物:⑴氢卤酸及卤化物(氢溴酸、氢碘酸、浓盐酸、溴化物、碘化物)⑵+ 2价的Fe (亚铁盐及氢氧化亚铁)⑶-2价的S (硫化氢及硫化物)⑷+ 4价的S (二氧化硫、亚硫酸及亚硫酸盐)⑸双氧水(H 2O 2)五、常见的各类有机物的官能团,结构特点及主要化学性质(1) 烷烃A)官能团:无;通式:C n H 2n+2;代表物:CH 4B) 结构特点:键角为109°28′,空间正四面体分子。
高中化学重要有机物之间的相互转化课件苏教选修5.ppt
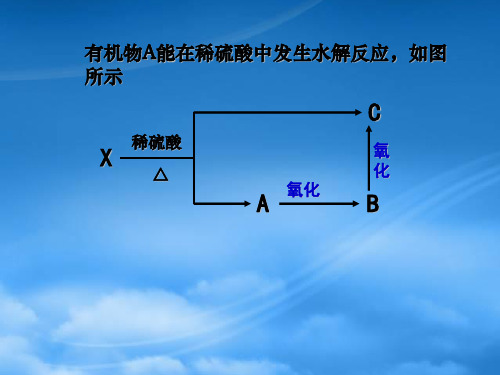
X NaOH溶液 △
D 稀硫酸 E A 氧化 B
试写出A、B、C的结构式
变化10:X的分子式为C4H8O2, B不能发生银
镜反应,则X的结构为?
讨论:
RCH2OH RCHO
RCOOH
RCOOCH2R
①一定要有CH2OH ② 碳架不变 ③ 式量变化分析
见例1 见例2 见例3
例1. 羧酸A(分子式为C5H10O2)可由醇B氧化得 到。A和B可生成酯C(相对分子质量为172), 符合这些条件的酯有多少种?
还原
乙酸
酯水 化解
乙酸乙酯
主要代表物之间的转化关系 二溴乙烷 水解 乙二醇 氧化 乙二醛 氧化 乙二酸
还原
乙烯
溴乙烷
水解 乙醇 氧化 乙醛 氧化
还原
乙酸
主要有机物之间的转化关系
烷
烯
炔
卤代烃
水解 醇 氧化
还原
醛 氧化
羧酸
酯水 化解
酯
重要知识规律
(1)卤代烃的消去反应规律 例.既能发生消去反应生成烯烃,又能发生水解反 应的是
D 稀硫酸 C
氧
化
A 氧化
B
试写出A、B、C、X的结构简式
变化5:
X的分子式为C10H20O2 A不能发生消去反应
X NaOH溶液 △
D 稀硫酸 C
氧 化
A 氧化 B
试写出A、B、C的结构式
变化6: X的分子式为C14H12O2
X NaOH溶液 △
D 稀硫酸 C
氧 化
A 氧化 B
试写出A、B、C的分子式 变化7: X的分子式为C16H14O4
(2)分子式为C6H14O的醇A经催化氧化得一分子 式为C6H12O的有机物B,已知B能发生银镜反应, 则写出A可能的结构简式_________________
(完整版)各类有机物的转化关系图
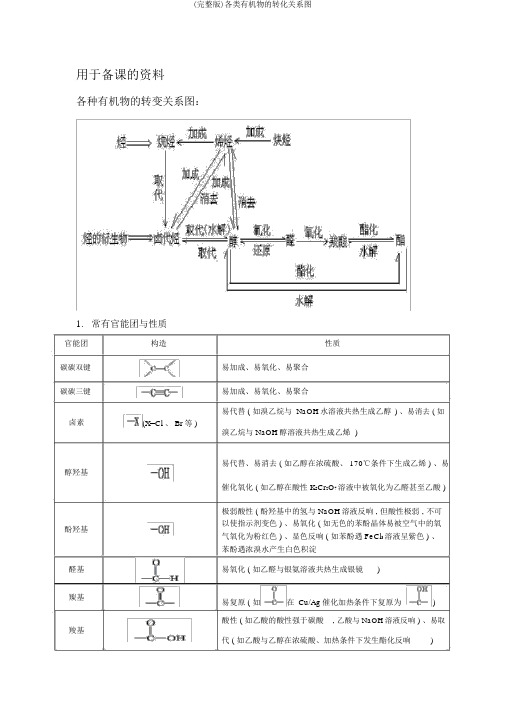
用于备课的资料各种有机物的转变关系图:1.常有官能团与性质官能团碳碳双键碳碳三键卤素醇羟基酚羟基醛基羰基羧基构造性质易加成、易氧化、易聚合易加成、易氧化、易聚合易代替 ( 如溴乙烷与 NaOH水溶液共热生成乙醇) 、易消去 ( 如(X=Cl 、 Br等 )溴乙烷与 NaOH醇溶液共热生成乙烯)易代替、易消去 ( 如乙醇在浓硫酸、 170℃条件下生成乙烯 ) 、易催化氧化 ( 如乙醇在酸性 K2Cr2O7溶液中被氧化为乙醛甚至乙酸 )极弱酸性 ( 酚羟基中的氢与 NaOH溶液反响 , 但酸性极弱 , 不可以使指示剂变色 ) 、易氧化 ( 如无色的苯酚晶体易被空气中的氧气氧化为粉红色 ) 、显色反响 ( 如苯酚遇 FeCl3溶液呈紫色 ) 、苯酚遇浓溴水产生白色积淀易氧化 ( 如乙醛与银氨溶液共热生成银镜)易复原 ( 如在Cu/Ag催化加热条件下复原为)酸性 ( 如乙酸的酸性强于碳酸, 乙酸与 NaOH溶液反响 ) 、易取代 ( 如乙酸与乙醇在浓硫酸、加热条件下发生酯化反响)易水解 ( 如乙酸乙酯在稀硫酸、加热条件下发生酸性水解, 酯基乙酸乙酯在 NaOH溶液、加热条件下发生碱性水解 )烷氧基如环氧乙烷在酸催化下与水一同加热生成乙二醇硝基复原 ( 如酸性条件下 , 硝基苯在铁粉催化下复原为苯胺) 2.有机反响种类与重要的有机反响反响种类重要的有机反响代替反响代替反响反响种类加成反响烷烃的卤代 :CH4+Cl 2CH3Cl+HCl烯烃的卤代 :卤代烃的水解 :CH3CH2Br+NaOH CH3CH2OH+NaBr皂化反响 :+3NaOH3C17H35COONa+酯化反响 : +CH OH +H O2 5 2糖类的水解 :C12H22O11+HOC6H12O6+C6H12O6蔗糖果糖葡萄糖2二肽的水解 :+H2O苯环上的卤代 :+Cl 2+HCl苯环上的硝化 :++H2O苯环上的磺化 :++H2O( 续表 )重要的有机反响烯烃的加成 :+HCl炔烃的加成 :+H2O苯环的加氢 :+3H2醇分子内脱水生成烯烃:C 2H5OH+H2O消去反响卤代烃脱 HX生成烯烃 :CH3CH2Br+NaOH+NaBr+H2O 单烯烃的加聚 :n加聚反响缩聚反响缩聚反响共轭二烯烃的加聚:( 别的 , 需要记着丁苯橡胶、氯丁橡胶的单体 )二元醇与二元酸之间的缩聚:n+nHOCH2CH2OH+2nH2O羟基酸之间的缩聚:+nH2 O氨基酸之间的缩聚:苯酚与 HCHO的缩聚 :n+nHCHO+nH2O氧化催化氧化 :2CH3 CH2OH+O22CH3CHO+2HO反响醛基与银氨溶液的反响:CH3CHO+2[Ag(NH3) 2 ]OH CH3COONH4+2Ag↓+3NH+H2O(注意配平 )醛基与新制氢氧化铜的反响:CH3CHO+2Cu(OH)+NaOH CH3COONa+Cu2↓ +3H2O醛基加氢 :CH3CHO+H2CH3CH2OH复原反响硝基复原为氨基:。
(完整版)高中化学各类有机物之间的相互转化关系

+3NH 3+H 2O
△
( 26) CH3CHO+2Cu(OH) 2 CH3COOH+Cu 2O↓+2H 2O
( 27) CH3CHO+H 2
催化剂 △
CH 3CH 2OH
( 28) CH3COOH+HOC 2H5
浓 H 2SO4 △
CH3COOC2H 5+H 2O
( 29) CH3COOC2H5+H 2O
CH 2Br
( 34) CH2Br + 2NaOH
水 △
CH2OH
CH2OH +2NaBr
( 35) CH 2BrCH 2Br+2NaOH
乙醇 △
CH≡ CH↑ +2NaBr+2H 2O
CH2OH
( 36) CH2OH +O2
催化剂 △
CHO
CHO +2H 2O
CHO
( 37) CHO +O2
催化剂 △
(31)
CH3COOCH 2CH3
CH 3 COONa
CH 3
O2N
(14)
CH 3 NO 2
(15) COOH
NO 2
Br
OH
ONa
NO 2
(16) (17) (18)
OH
Br
Br
Br
( 1)CH3CH3+Br 2 光照 CH3CH2Br+HBr
( 2)CH2=CH2+H2
催化剂 △
CH 3CH 3
CH 3
O2N
+
3HO -NO 2
浓 H 2SO4 △
