猪口蹄疫病毒O型抗体检测试剂盒
猪O型口蹄疫疫苗免疫效果试验报告

11 试 验 时 间与 试 验 动 物 .
型 口蹄疫抗体间接正 向血凝试 验试剂 盒说明书进行
记录 。结果判定: 根据 农业部 下达 的标准 , 检测猪 口 蹄疫免疫抗体滴度 ≥5为合格 ,5为不合格 , < 并经过 重复检验 , 确定抗体滴度 。
15 试 验 猪 分 组 与 试 验 方 法 .
330) 6 00
文 章 编  ̄ :0 2 15 (0 20 — 1 3 0 -10 — 9 72 1)3 0 1 — 2
摘 要: 随机选 择规模猪 场 4 2日龄左右 的仔猪 3 0头和散养 户的 8 6日龄散养猪 6头 , 分别进行两 次 0型 口蹄 疫灭活疫苗 免疫 , 间接正 向血凝检 测 口蹄疫 免疫抗体 。结果 显示 , 用 规模猪场 的仔猪 免疫抗体检 测 , 首免 后 2 均滴度超 过 53 均 为合格 ; 8d平 -, 二免后 2 均滴度 超过 81 均为合 8d平 ., 格 。散养 猪只免疫抗体检测 , 首免后 2 8d平均滴度 3 2 为不合格 ; ., 5 二免后 2 8d平均 滴度 91 , . 为 7 合格 。试验表 明, 0型 口蹄疫灭 活疫苗 经过 两次免疫 可获得 满意效果 。 猪 关键词 : 0型 1蹄疫疫苗 ; : 3 免疫 ; 抗体
1 . 采血 次数 与 时 间 6
1 . 规 模猪 场 首 免 当天 ( .1 6 指未注 射 疫苗 前 当 天)首免后第 2 天、8 , 免后第 2 , 1 2 天 二 8天 , 前 腔 经 静脉或耳静脉采血 1 , 次 分离血清 , 于抗体检测 。 用 下简称 中牧 0型 口蹄疫灭活疫苗) ,批 号 0 00 4 9 20 ,
21 0 2第 3期
养猪 S N R U T O WI E P OD C I N
口蹄疫O型抗体不同检测方法的比较和分析

1 ∶ 16 1 ∶ 64 1∶8 1 ∶ 64 1 ∶ 64
1 ∶ 180 1 ∶ 360 1 ∶ 45 1 ∶ 360 1 ∶ 720
1 ∶ 64 1 ∶ 64 1 ∶ 64 1 ∶ 64 1 ∶ 64
1 ∶ 360 1 ∶ 360 1 ∶ 720 1 ∶ 360 1 ∶ 360
1 ∶ 16 1 ∶ 64 1 ∶ 64 1 ∶ 64
1 ∶ 180 1 ∶ 360 1 ∶ 720 1 ∶ 360
表 3 间接血凝和液相阻断 ELISA 方法检测结果的一致性比较
合格 不合格
间接血凝 43 5
2019 年第 2 期 兽医实验室
样品编号
13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48
金标试纸条 1 ∶ 16 1∶8 1 ∶ 32 1 ∶ 64 1 ∶ 64 1 ∶ 16 1 ∶ 32 1 ∶ 32 1 ∶ 64 1 ∶ 16 1 ∶ 32 1 ∶ 64 1∶8 1 ∶ 64 1 ∶ 64 1 ∶ 32 1 ∶ 32 1 ∶ 32 1∶8 1 ∶ 32 1 ∶ 32 1 ∶ 64 1 ∶ 16 1 ∶ 32 1∶8 1 ∶ 32 1 ∶ 64 1 ∶ 32 1 ∶ 32 1 ∶ 64 1 ∶ 32 1 ∶ 32 1∶8 1 ∶ 32 1 ∶ 64 1 ∶ 32
剂盒。 3. 判定标准。根据各试剂盒操作规程,最终试验数
据依据各说明书判定标准确定。 正向间接血凝抗体效价≥ 1:25 判定为免疫合格 ; 液相阻断 ELISA 抗体(猪)效价≥ 1 ∶ 64,保护
口蹄疫O型抗体检测试剂盒(酶联免疫法) 使用说明书
口蹄疫O型抗体检测试剂盒(酶联免疫法)使用说明书【产品名称】通用名:口蹄疫O型抗体检测试剂盒(酶联免疫法)英文名:Test Kit for Antibodies to Foot and Mouth Disease Virus Asia O(ELISA)【包装规格】96T×1/盒、96T×2/盒、96T×5/盒【预期用途】口蹄疫是由口蹄疫病毒(Foot and Mouth Disease Virus,FMDV)引起的偶蹄动物的一种急性、热性、高度接触性传染病,其特征为口腔黏膜、蹄部、乳房皮肤发生水泡和烂斑。
本试剂用于检测牛、羊、猪血清中口蹄疫O型抗体,可用于口蹄疫O型疫苗免疫效果评价。
【原理】本试剂盒由预包被口蹄疫O型抗体的酶标板、抗体工作液、抗原液、酶标记物及其他配套试剂组成,应用阻断酶联免疫法(ELISA)原理检测牛、羊、猪血清样本中口蹄疫O型抗体。
实验时将稀释的样本与抗原液同时加入酶标板中孵育,样本中的抗体与酶标板上的抗体竞争抗原,阻断抗原与板的结合;经洗涤后,再加抗体工作液孵育;经洗涤后加入酶标记物孵育;再经洗涤除去未结合的酶标记物,在孔中加底物液,与酶标结合物反应形成蓝色产物,显色深浅与样品中的特异性抗体含量成负相关;加入终止液终止反应后,产物变为黄色;用酶标仪在450nm波长测定各反应孔中的吸光值,即可知样品是否含有口蹄疫O型抗体。
【试剂盒组成】【储存及有效期】2~8℃保存,有效期12个月。
包被板开封后请于2~8℃避光保存,避免受潮。
使用期限为2个月。
【适用仪器】含450nm、630nm波长的酶标仪,37℃恒温设备,可调微量移液器。
【样品准备】1.取动物全血按常规方法制备血清,要求血清清亮,无溶血、无污染。
样品1周内可于2~8℃保存,长期需置-20℃保存。
2.用工作洗涤液将待检牛、羊血清先按32倍稀释(如5μl 血清加入155μl 工作洗涤液中,混匀),待检猪血清按16倍稀释(如5μl 血清加入75μl 洗涤液中,混匀),阴、阳性对照不用稀释。
三种猪O型口蹄疫免疫抗体检测方法的比较

即样 品 O 6 0 m 值 ≥04时 判 为 阳性 . D 3n . 为 免 疫 合 格 :样 品 O 6 0 m 值 < - D 3n 04时
判为阴性。
2 结 果
差异不显著 (> . ) P 0 5 ,且 具 有 良好 的 0
相 关性
份 ,分离 血清 ,一 0 冰箱 冻 存 。 2℃
让 兔 子在 中午 高 温 期 间 少 活 动 多休 息 。
5 供 应 充足 饮 水 高 温 期 间要 满 足清 洁饮 水 的供 应 。还
王敏生 华 玉新 一 江苏省 金湖县塔 集中 心畜牧兽 医站 1 1 1 )
可 以 自制 清 凉 的植 物饮 料 i 兔 子 饮 用 : 卜
( ) 西瓜 皮 汤 : 西 瓜 皮 洗 净 l千 克 , 1 水 5干 克 ,煮 开 后 放 凉 饮用 :
时 即 可 发 生 红 细 胞 凝 集 现 象 。 可 检 测
正 向 间接 血凝 ( A)试 验 、阻 断 I H
夹 心 EUS 和 间 接 E A 按 生 产 厂 家 A US
说 明 书进 行 操 作 。
122・ 疫 判 定 标 准 .- 免
测 方 法 的 相 关 性 和 特 点 ,本 试 验 选 用
附 表
3 讨 论
121 检 测 方法 ..
正 向 间接 血凝 是 当 前最 为快 速 、 简 便 和 经 济 的 检 测 血 清 方 法 1。 是 将 2 l 灭 活 的 各 型 病 毒 致 敏 绵 羊 红 细 胞 制 备 的 诊 断 试 剂 , 当 其 遇 到 相 应 型 的 血 清
4 科 学 饲 养
饲养管理 l
早 上 要 喂 得早 ,晚 上要 喂得 迟 ,中 午
猪口蹄疫病毒(FMDV)Elisa试剂盒说明书

猪口蹄疫病毒(FMDV)Elisa试剂盒说明书本试剂盒仅供研究使用。
检测范围: 96T15ng/L – 480ng/L使用目的:本试剂盒用于测定猪血清、血浆及相关液体样本中口蹄疫病毒(FMDV)含量。
猪口蹄疫病毒(FMDV)Elisa试剂盒说明书实验原理本试剂盒应用双抗体夹心法测定标本中猪口蹄疫病毒(FMDV)水平。
用纯化的猪口蹄疫病毒(FMDV)抗体包被微孔板,制成固相抗体,往包被单抗的微孔中依次加入口蹄疫病毒(FMDV),再与HRP标记的口蹄疫病毒(FMDV)抗体结合,形成抗体-抗原-酶标抗体复合物,经过彻底洗涤后加底物TMB显色。
TMB在HRP酶的催化下转化成蓝色,并在酸的作用下转化成最终的黄色。
颜色的深浅和样品中的口蹄疫病毒(FMDV)呈正相关。
用酶标仪在450nm波长下测定吸光度(OD值),通过标准曲线计算样品中猪口蹄疫病毒(FMDV)浓度。
试剂盒组成1 30倍浓缩洗涤液20ml×1瓶 7 终止液6ml×1瓶2 酶标试剂6ml×1瓶 8 标准品(960ng/L) 0.5ml×1瓶3 酶标包被板 12孔×8条 9 标准品稀释液1.5ml×1瓶4 样品稀释液6ml×1瓶 10 说明书 1份5 显色剂A液6ml×1瓶 11 封板膜 2张6 显色剂B液6ml×1/瓶 12 密封袋 1个标本要求1.标本采集后尽早进行提取,提取按相关文献进行,提取后应尽快进行实验。
若不能马上进行试验,可将标本放于-20℃保存,但应避免反复冻融2.不能检测含NaN3的样品,因NaN3抑制辣根过氧化物酶的(HRP)活性。
操作步骤1. 标准品的稀释:本试剂盒提供原倍标准品一支,用户可按照下列图表在小试管中进行稀释。
480 ng/L 5号标准品 150μl的原倍标准品加入150μl标准品稀释液240 ng/L 4号标准品 150μl的5号标准品加入150μl标准品稀释液120ng/L 3号标准品 150μl的4号标准品加入150μl标准品稀释液60 ng/L 2号标准品 150μl的3号标准品加入150μl标准品稀释液30 ng/L 1号标准品 150μl的2号标准品加入150μl标准品稀释液2. 加样:分别设空白孔(空白对照孔不加样品及酶标试剂,其余各步操作相同)、标准孔、待测样品孔。
不同试剂盒检测猪口蹄疫O型合成肽疫苗免疫抗体的对比试验

不同试剂盒检测猪口蹄疫O型合成肽疫苗免疫抗体的对比试验廖美娜;袁敏【摘要】使用口蹄疫O型正向间接血凝抗体试剂盒(IHA)和2个厂家生产的猪口蹄疫病毒VP1结构蛋白抗体酶联免疫吸附试验诊断试剂盒(VP1-ELISA)分别检测接种猪口蹄疫O型合成肽疫苗免疫后不同时间的抗体合格率,以探讨3种抗体检测试剂盒的相关性.结果显示,IHA试剂盒与两种VP1-ELISA的符合率较差,分别为11.7%、12.5%,IHA试剂盒不能用于检测合成肽疫苗免疫抗体;VP1-ELISA试剂盒可以科学评价合成肽疫苗免疫抗体,两种VP1-ELISA试剂盒的平均符合率为93.6%,但是VP1-ELISA (UBI)试剂盒的稳定性高于VP1-ELISA(Z)试剂盒.【期刊名称】《广东畜牧兽医科技》【年(卷),期】2016(041)001【总页数】4页(P24-26,29)【关键词】猪口蹄疫;O型抗体;试剂盒;对比【作者】廖美娜;袁敏【作者单位】河源市龙川县动物卫生监督所赤光分所,广东河源517349;河源市龙川县畜牧兽医渔业局,广东河源517300【正文语种】中文【中图分类】S851.3口蹄疫(Foot-an-mouth isease,FM)是一种急性、热性、高度接触性传染病[1],严重危害我国畜牧业的发展[2-3]。
目前,我国对口蹄疫实行预防为主、扑杀为辅的防控政策,对口蹄疫实行强制免疫。
免疫抗体检测是科学评价免疫质量的有效手段,也是制定免疫程序的可靠依据。
在实际工作中,因受到检测方法、检测试剂的不同而导致检测结果常有差异。
近几年,猪口蹄疫O型合成肽疫苗作为一种新型疫苗在市场上得到广泛的应用[4]。
为了选择科学评估此种疫苗免疫质量的检测方法,本试验通过使用猪口蹄疫O型合成肽疫苗免疫猪群后,采集不同时间的血清,分别使用正向间接血凝试验试剂盒(IHA)和2个厂家生产的猪口蹄疫病毒VP1结构蛋白抗体酶联免疫吸附试验诊断试剂盒(VP1-ELISA),进行了猪口蹄疫O型抗体检测的对比试验。
影响口蹄疫O型液相阻断ELISA抗体检测实验结果因素的研究

有排空后 直接连续倍 比稀 释移液 ; 2 号 酶标板上每孔抗原抗 体混合 液经稀释后 排空移液 器 , 然后再进行 吸液移液 , 进行
下一孔 的再次稀释移液 。
蹄疫的主要手段 。在 当前 的动 物疫 病预防控制工作 中, 口蹄
试 验 研 究
影 响 口蹄 疫 。 型 液相 阻断 E L I S A 抗体检测实验结果 因素 的研究
单 以军
( 江 苏 省 响水 县 畜牧 兽 医 总站 ,响 水 2 2 4 6 0 0)
关键词 : 口蹄 疫; 免疫抗体 ; 液相 阻断 E L I S A抗体检测 ; 试验 结果 ; 试剂盒 ; 酶标仪
操作过程 中实验 人员注意力要高度集 中, 每一个环节稍有不
慎, 就有可能影响到实验 的准确性 , 导致试验失败 、 实验不成 立, 或者实验数据不准确。 本人经充分准备 , 在县兽 医实验室 进行 了影 响实验结果 的研究性试验 。
1 材 料 与 方 法
O D值 ; 2号酶标板底部背面及时清除干净后进行读值 。
紧, 然后再进行相关实验操作 。 ( 2 )混匀后做 连续 2倍稀 释时 , 1 号酶标 板上移液器 没
的免疫抗体水平 的高低 , 直接关系到能否对动物进行保 护的 效果 , 这 只能通过抗体 水平 的检测来判断 。 口蹄疫 的液相阻 断E L I S A检测 技术 , 是一种成熟 的检测技术 , 是 当前 国际上
离 子水 、 加样 槽 、 冷藏箱 、 电热恒温 培养箱 、 R T 一 6 0 0酶标 仪 、
打印机等。 1 . 2 实验 方 法
1 . 2 . 1 设 定 实验 过 程 中 的操作 比对环 节及 具 体 实验 过 程
两种试剂盒分别检测猪口蹄疫O型、A型疫苗抗体的对比试验

2018 年第 8 期 兽医实验室
两种试剂盒分别检测猪口蹄疫 O 型、A 型 疫苗抗体的对比试验
杨虹 1 吴聪 2 1. 南昌市动物疫病预防控制中心 2. 江西农业大学动物科技学院
口蹄疫是由口蹄疫病毒引起偶蹄动物的一种急性、 对猪口蹄疫 O 型、A 型二价疫苗免疫抗体进行了免疫效
二、结果
1. 抗 体 检 测 合 格 率。 使 用 VP1-ELISA 诊 断 试 剂 盒 检 测 O 型、A 型 口 蹄 疫 抗 体 合 格 率 分 别 为 86.67%、 80.00%,使用 SPC-ELISA 检测试剂盒检测 O 型、A 型 口蹄疫抗体合格率分别为 90.00%、83.33%(表 1)。
最好的水平。 选择合适的接毒时间至关重要,进行 PCV2 培养时 ,
应在细胞接种或未形成单层之前接种。细胞接种后 0 h 以 MOI 为 0.05 接种 PCV2 病毒,接种病毒时间较早 , 严重影响了细胞的正常生长,病毒毒价较低 ;细胞接种 后 12 h 以 MOI 为 0.05 接种 PCV2 病毒,细胞密度有所 提高,虽然理论上细胞数越多 , 其所收获的病毒也应该 最多 , 但病毒毒价并没有细胞接种后 6 h 接种 PCV2 高。 说明细胞密度并不是决定病毒滴度的决定性因素 , 而是 细胞的生长状态。这主要是由于 PCV2 病毒在增值子代
3. 检 测 试 剂 盒。(1) 猪 口 蹄 疫 O 型 病 毒 VP1 结
2018 年以前,我国对猪一直进行 O 型口蹄疫的强 构 蛋 白 抗 体 ELISA 诊 断 试 剂 盒(VP1-ELISA):批 号
制免疫,但根据农医发 [2018]1 号文件“农业部关于印发 20180302,购自郑州中道生物技术有限公司 ;猪口蹄疫
病毒时需要宿主细胞 DNA 复制相关的酶参与,只有细胞 处于指数生长前期时其 DNA 复制酶的活性最局,数量 最多。
口蹄疫液相ELISA抗体检测试剂盒加样操作说明
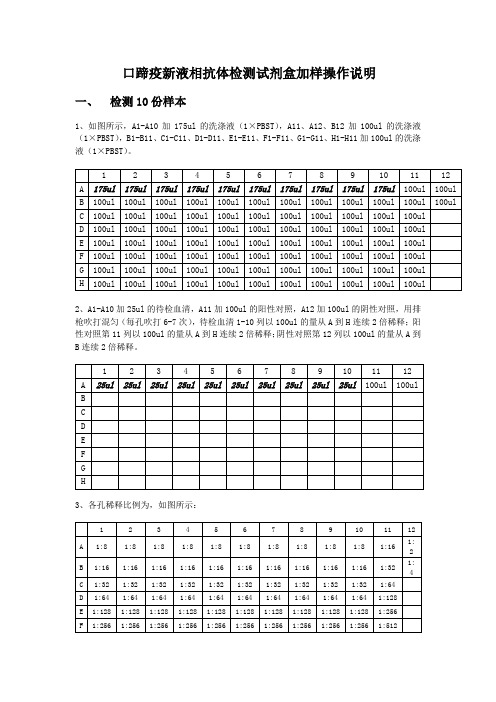
口蹄疫新液相抗体检测试剂盒加样操作说明一、检测10份样本1、如图所示,A1-A10加175ul的洗涤液(1×PBST),A11、A12、B12加100ul的洗涤液(1×PBST),B1-B11、C1-C11、D1-D11、E1-E11、F1-F11、G1-G11、H1-H11加100ul的洗涤液(1×PBST)。
2、A1-A10加25ul的待检血清,A11加100ul的阳性对照,A12加100ul的阴性对照,用排枪吹打混匀(每孔吹打6-7次),待检血清1-10列以100ul的量从A到H连续2倍稀释;阳性对照第11列以100ul的量从A到H连续2倍稀释;阴性对照第12列以100ul的量从A到B连续2倍稀释。
3、各孔稀释比例为,如图所示:4、转板,从血清稀释板转到包被板的对应孔,每孔50ul。
再加稀释后的病毒抗原,1-11列各加入50ul,A12、B12各加入50ul,E12、F12、G12、H12各加入100ul。
5、加样完毕后,每孔的最终量均为100ul,待检血清、阳性对照、阴性对照的稀释度翻倍,如图所示:二、检测20份样本1、如图所示,A1-A10、E1-E10加175ul的洗涤液(1×PBST),A11、E11、A12、B12加100ul 的洗涤液(1×PBST),B1-B11、C1-C11、D1-D11、F1-F11、G1-G11、H1-H11加100ul的洗涤液(1×PBST)。
2、A1-A10、E1-E10加25ul的待检血清,A11加100ul的阳性对照,A12加100ul的阴性对照,用排枪吹打混匀(每孔吹打6-7次),待检血清1-10列以100ul的量从A到D、从E到H连续2倍稀释;阳性对照第11列以100ul的量从A到H连续2倍稀释;阴性对照第12列以100ul的量从A到B连续2倍稀释。
3、各孔稀释比例为,如图所示:4、转板,从血清稀释板转到包被板的对应孔,每孔50ul。
不同品牌ELISA试剂盒对口蹄疫抗体检测的试验

不同品牌 ELISA试剂盒对口蹄疫抗体检测的试验摘要:用不同品牌的口蹄疫O型ELISA试剂盒,对免疫口蹄疫疫苗后的猪群进行口蹄疫抗体检测,发现检测结果阳性率各不相同。
结果表明不同品牌试剂盒因制备方法、包被抗原不同对猪群的抗体检测结果不同,所以,建议在实践中用口蹄疫ELISA试剂盒检测抗体效价应根据情况有选择使用。
关键词:试剂盒;抗体效价检测;阳性率;有选择使用;口蹄疫(Foot-and-Mouth Disease,FMD)是由口蹄疫病毒(Foot-and-mouth disease virus)引起的偶蹄动物烈性传染病,是世界卫生组织(OIE)规定必报的烈性传染病,我国将其排在一类传染病之首。
口蹄疫病毒共有七个血清型,分别为O、A、C、Asia1、SAT1、SAT2、SAT3型。
每个血清型又有许多不同的亚型,各血清型之间没有交叉保护,同一血清型的各亚型之间仅有部分交叉保护,这使得对口蹄疫的防控更加困难。
目前我国主要流行O型和A型口蹄疫。
目前,我国防控口蹄疫主要采取疫苗免疫与扑杀相结合的综合防治措施,对所有易感动物猪、牛、羊进行口蹄疫灭活疫苗免疫接种。
但是在给动物注射疫苗后能否预防口蹄疫的发生一直的广大养殖户迫切需要知道的问题。
所以免疫后的效果评价就显得特别重要。
目前主要有以下几种检测方法:1.免疫动物攻毒实验;这一方法是判断疫苗免疫效果的金标准,但因需要在生物安全三级实验室内进行,一般养殖企业和研究单位都没法实施。
2.免疫动物血清中和实验;这一方法相对准确些,但同样也受一定条件限制,一般的研究检测单位也不完全具备检测条件。
3.免疫动物血清ELISA抗体检测;这一方法的准确性比前两种方法相对较差,但也是一般检测单位都容易实施的检测方法,因此也被广泛用于疫苗免疫效果的评价。
但由于这一方法的存在的一定的缺陷,评价结果也一直存在争议。
本文所研究的就是使用第三种方法对疫苗免疫效果进行检测,根据检测结果进一步分析这一方法的准确性,对使用单位给予一些指导建议。
O型口蹄疫液相阻断 ELISA检测记录(兰州所)

7、结果判定:
(1)试验认可标准:病毒抗原对照至少2孔D492nm值应在1.0-2.0内。阳性对照效价应在1:1024±1内,阴性效价应<1:8
。
(2)临界值计算:抗原对照4孔,弃去最高和最低D492nm值,计算剩余2孔的平均值,再除以2,即50%对照值(临界值)。
3、连续洗ELISA板5次。再将抗原抗体混合物从抗原抗体反应板上按次序转移至ELISA对应孔,50ul/孔,封板37℃温育1h 。
4、同上洗板5次。用豚鼠抗血清稀释液稀释O型口蹄疫病毒豚鼠抗血清至工作浓度,每孔加50ul,封板37℃温育1h。
5、洗板5次。用PBST稀释兔抗豚鼠酶结合物至工作浓度,每孔加50ul,封板37℃温育1h。
2、抗原抗体反应:根据不同需要选择适当布局在抗原抗体反应板上操作。如在U型血凝板上按50ul/孔量用PBST将待检血
清从1:4开始做2倍连续稀释至1:512。同时,按图示稀释阴阳性对照血清,然后每孔加入50ul用PBST稀释到使用浓度的
亚洲1型口蹄疫病毒擵,病毒抗原对照孔加100ul。混匀,封板,4℃过夜。
检验时间 年月 日
年 月日
检验环境 (温度: ℃ 湿度: ﹪) 检验依据 猪瘟防治技 术规范—猪 瘟病毒间接
温度: ℃ 湿度: % 农医发[2012]2号文件
生产厂家 试剂批号
有效期
个月
主要检验步骤及结果判定:
1、用包被缓冲液稀释O型口蹄疫病毒兔抗血清至工作浓度(1:1000),在ELISA板上每孔加50ul,振荡,封板温室过夜。
xx区 动物疫病预防控制中心
四种口蹄疫分型试剂盒的检测效果比对

四种口蹄疫分型试剂盒的检测效果比对
凌洪权;骆璐;黎朝燕;陈忠琼;蒋佳利;谢建华
【期刊名称】《四川畜牧兽医》
【年(卷),期】2024(51)6
【摘要】目前市场上销售的口蹄疫O型和A型双重荧光RT-PCR分型试剂盒比较多,为了找到一种效果理想的分型试剂盒,使用4个厂家(分别用A、B、C、D代替)
的试剂盒对6份国家口蹄疫比对盲样(编号分别为S1、S2、S3、S4、S5、S6)进行检测效果比对。
结果发现,不同厂家试剂盒的检测效果各不相同,且差别较大,D厂家试剂盒的检测结果与比对盲样的标准值完全吻合,A、B、C 3个厂家试剂盒的检测
结果与比对盲样的标准值有不同程度的差异。
【总页数】2页(P27-28)
【作者】凌洪权;骆璐;黎朝燕;陈忠琼;蒋佳利;谢建华
【作者单位】重庆市动物疫病预防控制中心;重庆市璧山区现代农业发展促进中心【正文语种】中文
【中图分类】S854.43
【相关文献】
1.四种试剂盒检测猪口蹄疫O型合成肽疫苗抗体的对比试验
2.牛口蹄疫O型-亚I
型双价灭活疫苗、A型灭活疫苗和牛口蹄疫三价灭活疫苗免疫效果比对试验3.便
捷式液相阻断ELISA试剂盒检测牛O型口蹄疫抗体水平的效果试验4.口蹄疫O型抗体液相阻断ELISA检测试剂盒与其改进型试剂盒的比对试验5.两种口蹄疫O型、A型抗体检测试剂盒检测猪口蹄疫抗体的应用研究
因版权原因,仅展示原文概要,查看原文内容请购买。
口蹄疫病毒O型抗体检测注意事项及结果分析

健康养殖·诊疗畜牧业环境 2021.0286摘 要:口蹄疫是由口蹄疫病毒引起的急性、热性传染性疫病,此病常发生于偶蹄动物,被世界卫生组织列为传染病,又被我国列为一类动物疫病。
文章主要介绍口蹄疫阻断ELISA 抗体检测实验步骤和注意事项,为洛南县生畜养殖场或户的免疫抗体水平做好分析,为口蹄疫抗体监测工作提供依据和参考。
关键词:口蹄疫病毒;O型抗体检测;注意事项;结果分析1 样品来源该实验样品来自于全县16个镇,随机抽取生猪养殖场20个,每场采集血清样品15份;零散养殖户随机抽取16户,每户采集血清样品5份,共计380份。
2 实验仪器量筒、烧杯、离心管架、超纯水机、电热恒温箱、洗板机、酶标分析仪、移液枪头、单道移液器、多道移液器、离心管、一次性洗液皿、一次性吸水纸。
3 洗涤液配制用量筒取900ml蒸溜水或去离子水与100ml洗涤液混合(洗涤液是浓缩洗液,需要稀释),充分混匀即为工作浓度洗涤液。
4 具体实验步骤4.1 实验前的准备工作将阻断ELISA抗体检测试剂盒和待检血清从冷藏和冷冻箱中取出,将待检血清竖行排列于离心管架上,并做好编码,等试剂和血清样品温度恢复到室温20℃~25℃,在进行实验。
4.2 操作步骤4.2.1 加样(1)预先取出包被板,取出样品稀释液,在每孔加入样品稀释液50 µl。
(2)再用10 µl的移液器添加50µl待检样品。
(3)在包被板最后加入50µl阴性和阳性对照品各2孔,盖膜,避光在37℃反应60min。
4.2.2 洗板60min时间到取包被板,揭掉封板膜,倒掉孔内液体,用预先配制好的洗涤液洗涤3次,每次停留1min;最后一次倒干净后,用吸水纸将包被板内液体拍干。
4.2.3 检测(1)在包被板中加酶标结合物(1号液)100µl,盖膜,避光在37℃反应60min。
60min时间到后取出包被板,揭膜,倒掉孔内液体,用预先配制好的洗涤液洗涤3次,每次停留1min;最后一次倒干净后,用吸水纸将包被板内液体拍干。
口蹄疫O 型抗体ELISA 检测血清稀释方法优化比较

资金项目:山东省农科院农业科技创新工程项目“畜禽重要疫病防控关键技术(CXGC2016B14)”;山东省现代农业产业技术体系生猪创新团队项目(SDAIT-08-17)。
作者简介:李玲(1983—),女,助理研究员,硕士,研究方向为畜禽疫病防控与生物制品研发。
*通讯作者口蹄疫O型抗体ELISA检测血清稀释方法优化比较李玲1,魏凤2,郝胜楠3,吕素芳2,李峰2*(1.山东绿都生物科技有限公司山东滨州256600;2.山东省滨州畜牧兽医研究院山东滨州;3.东营市河口区畜牧业发展服务中心山东东营257200)试验选择液相阻断ELISA检测试剂盒,对20份血清样品检测口蹄疫O型抗体。
试验比较了1:8起始稀释8个梯度,1:16起始稀释4个梯度,1:32起始稀释4个梯度,1:64起始稀释4个梯度4种方法抗体效价测定结果,其阳性率分别为70%、65%、70%、70%,组间差异不显著。
提出了针对不同检测需求,合理选择血清稀释方法的建议,有助于指导临床应用。
蹄疫;O型抗体;血清;稀释方法口蹄疫(FMD)具有传染性强、传播速度快、感染动物种类多等特点[1],世界动物卫生组织(OIE)将其列为必须报告的动物疫病,我国将其列为一类动物疫病。
我国制定实施了“国家口蹄疫防治计划”(2016—2020年),对O型口蹄疫,采取分阶段、分区域控制策略[2]。
2020年国家动物疫病强制免疫计划,要求口蹄疫的群体免疫密度应常年保持在90%以上,免疫抗体合格率全年保持在70%以上[3]。
此外,农业农村部明确对跨省调运乳用种用动物需依据“口蹄疫防治技术规范”等开展口蹄疫抗体检测[4]。
因此,牛、羊、猪口蹄疫抗体检测已成为基层常规检测项目,其中以液相阻断ELISA方法应用较多,李小明等[5]研究表明该方法灵敏性和特异性高,重复性好,结果判定科学且不受检验人员主观性影响。
我们在该方法检测口蹄疫O型抗体时,选择不同的血清稀释方法,并就其结果差异性进行了比较,旨在根据检测对象与检测目的,选择合适的血清稀释方法,实现提高检测效率、节约实验室资源的目的。
两种试剂盒分别检测猪口蹄疫O型、A型疫苗抗体的对比试验

2018 年第 8 期 兽医实验室
两种试剂盒分别检测猪口蹄疫 O 型、A 型 疫苗抗体的对比试验
杨虹 1 吴聪 2 1. 南昌市动物疫病预防控制中心 2. 江西农业大学动物科技学院
口蹄疫是由口蹄疫病毒引起偶蹄动物的一种急性、 对猪口蹄疫 O 型、A 型疫苗强制免疫为主的综合措施来防控口蹄疫,
2. 血清样品背景。血清来自本市一个接种猪口蹄疫
主要是通过疫苗免疫使动物产生抵抗该病的有效抗体, O 型、A 型二价疫苗的规模化猪场,随机从一次免疫后
以达到预防的目的。疫苗免疫后抗体水平检测是评价疫 28 天的猪群中采集 30 份血样。
苗免疫效果最简单最直接的方法。
病毒时需要宿主细胞 DNA 复制相关的酶参与,只有细胞 处于指数生长前期时其 DNA 复制酶的活性最局,数量 最多。
本研究摸索了利用微载体规模培养 PK-15 细胞增 殖 PCV2 LG 株的条件,根据试验结果确定最佳接毒时 间为细胞接种后 6 h,最佳接毒剂量为 MOI=0.05,在此 条件下增殖病毒含量最高可达 106.5,表明 PCV2 LG 株 适应在 PK-15 细胞内大规模增殖,为以哺乳动物细胞为 基质大规模增殖病毒及制备猪圆环病毒疫苗提供依据。
二、结果
1. 抗 体 检 测 合 格 率。 使 用 VP1-ELISA 诊 断 试 剂 盒 检 测 O 型、A 型 口 蹄 疫 抗 体 合 格 率 分 别 为 86.67%、 80.00%,使用 SPC-ELISA 检测试剂盒检测 O 型、A 型 口蹄疫抗体合格率分别为 90.00%、83.33%(表 1)。
4. 检 测 方 法。 采 集 的 30 份 猪 血 液 样 品 经 4 ℃, 3 000 r/min 离心 3 min 后取上清液,按试剂盒使用说明 书进行检测。
国家口蹄疫参考实验室诊断检疫技术简介

国家口蹄疫参考实验室诊断检疫技术简介(一)现有诊断检疫技术(试剂盒)本实验室经过多年的研究和实践,建立了病毒分离、补体结合试验(CFT)病毒中和试验(VNT)、血清中和试验等诊断方法,并形成了一套完善的诊断程序,符合国际通用的操作标准。
同时发展了O型口蹄疫正向间接血凝诊断法,口蹄疫和猪水泡病反向间接血凝诊断法,琼脂扩散试验,以及口蹄疫VIA诊断和RT-PCR诊断试剂盒,满足口蹄疫样品的诊断和定型。
近年来,本实验室根据科学技术发展,结合国际组织推荐的口蹄疫诊断检疫技术,研制出了多种试剂盒和检测方法。
1、O型口蹄疫液相阻断ELISA诊断试剂盒液相阻断ELISA是国际兽疫局(OIE)推荐的检测口蹄疫病毒抗体的标准方法。
用分离于我国的口蹄疫O型毒株研制出液相阻断ELISA试剂盒,用于测定牛、猪、羊血清中针对O型口蹄疫病毒结构蛋白的抗体。
本试剂盒主要用途,一是对进出口动物口蹄疫病毒抗体监测;二是监测口蹄疫疫苗免疫抗体,以评价动物群体抗感染能力。
2、口蹄疫病毒非结构蛋白抗体检测试剂盒(3ABC-I-ELISA)区分口蹄疫感染和免疫动物是国际活畜进出口贸易的必检项目,也是OIE 判定疫情国家和非疫情国家的依据。
本试剂盒适用于活畜进出口调运、疫区净化检疫和群体无症状感染评价,检测活畜血清中口蹄疫病毒非结构蛋白3ABC抗体,以区分感染和免疫动物。
本试剂盒可测出牛感染后长达480天(16个月)的感染抗体,其多项技术指标已超过国外同类产品。
3、口蹄疫多重RT-PCR诊断试剂盒(FMD Multi RT-PCR)本试剂盒适用于病料诊断、反刍活畜和肉品等畜产品染毒检测,特异性扩增病料、O/P液和肉品中的口蹄疫病毒基因片段,确认样品供体是否染毒。
本试剂盒含有三对引物,可扩增多个口蹄疫病毒基因片段,至少适用于口蹄疫O型、A 型和AsiaⅠ型的三个血清型的检测,可查出0.07LD50的病毒量。
4、口蹄疫原位杂交检测法原位杂交是借助核酸分子杂交的方法,在显微镜水平检测和定位特异的核酸片段。
三种试剂盒检测猪口蹄疫O型抗体的对比试验

以探 讨三种抗体检 测试剂盒的相 关性 。 结果发 现 , 口蹄疫 病毒VP 结构蛋 白抗体 E IA试剂 盒和猪 口蹄 疫0型液相 阻断E IA 猪 1 LS LS 试剂 盒都可检 测猪 口蹄 疫O型合成肽疫 苗, 两种试剂盒的相关性达9 .%, 间接血凝试剂盒不能用来检测猪 口蹄疫0 08 而 型合成肽疫 苗; 口蹄 疫O型 液相 阻断E IA试剂盒和 间接血凝试剂 盒可用来检测猪 口蹄疫O 灭活疫 苗, 猪 LS 型 两种试剂盒 的相 关性达9 . 而猪 37 %, 口蹄疫病毒V 1 P 结构蛋 白抗体E IA试剂盒 不能用来检测猪 口蹄疫O LS 型灭活疫 苗。
关键词 : 剂盒: 口蹄疫; 试 猪 0型; 抗体 ; 比 对 中图分类号 : 8 8 8 文献标识码 : 文章编号 :0 59 4 2 1 )05 —3 ¥5. 2 B 10 .4 X(0 2 1.40
Co pa io e to e isf r d t c i wi y f o - nd- o h die s ntbo y m rs n t s f hr ek t o e e tng s net pe0 o ta - ut s a ea i d t - m
mo t ie s pe0 y tei e td a cn ,t i fc reaino 08 ,u HA i a o eu e od tc :LB. LIA uhds aet snh t p piev c ie wokt o orlto f9 .% b t y c s I kt c nn t sdt eeti s b t E S
Ab t a t ]} e wi e f o n u h d s a e t p a t o y d t ci n k twe e u e o d tc h n i o y o e i o u ae wi e sr c .r r e s n o t d mo t ie s y e O n i d e e to i 1 a b r s d t ee t e a tb d f h n c ltd s n t t f o n u h d s a e t e O y t e i e t ev c ie a d t es n o n u h d s a etp i a t ae a c n ,a d t x lr o t d mo t ie s a yp s nh t p p i a c n n wi e f t dmo t ie s e O c i t d v c i e n oe p o e c d h o a y n v t ec rea i n o t et r e a t o y d t c in k t T er s l h we a eVP1 E S k t n B. I A i c n d t c wi ef o d h o r lt f h e n i d ee t i h u t s o dt t h o h b o — e s h t - LI A i a d L EL S k t a ee t s n o t n a
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
仅供科研使用,不得用于临床检验。
猪口蹄疫病毒O型抗体定性检测试剂盒(ELISA)说明书
【产品名称】
通用名称:猪口蹄疫病毒O型抗体定性检测试剂盒(ELISA)
英文名称:Test Kit for Antibodies to Porcine Foot and Mouth Disease Virus O ELISA KIT
【包装规格】
96人份/盒
【预期用途】
仅供科研使用,口蹄疫是由口蹄疫病毒(Foot and Mouth Disease Virus,FMDV)引起的偶蹄动物的一种急性、热性、高度接触性传染病,其特征为口腔黏膜、蹄部、乳房皮肤发生水泡和烂斑。
本试剂用于检测猪血清中口蹄疫病毒O型抗体,可用于口蹄疫病毒O型疫苗免疫效果评价。
【检验原理】
本试剂盒系由预包被口蹄疫病毒O型VP1抗原的酶标板、酶标记物及其他配套试剂组成,应用酶联免疫法(ELISA)原理检测猪血清、血浆样本中猪口蹄疫病毒O型抗体。
实验时在酶标板中加入对照血清和待检样本,经温育后若样品中含有猪口蹄疫病毒O型抗体,则将与酶标板上抗原结合,经洗涤除去未结合的其他成分后;再加入酶标记物,与酶标板上抗原抗体复合物发生特异性结合;再经洗涤除去未结合的酶标记物,在孔中加TMB底物液,与酶反应形成蓝色产物,显色深浅与样品中的特异性抗体含量成正相关;加入终止液终止反应后,产物变为黄色;用酶标仪在450nm波长测定各反应孔中的吸光值,即可知样品是否含有口蹄疫病毒O型抗体。
【主要组成成分】
主要成分
需要但未提供的材料及耗材
1、酶标仪
2、精密移液器及一次性吸头
3、蒸馏水
4、洗瓶或者自动洗板机
5、37℃水浴锅或恒温箱
6、500ml量筒
7、无粉一次性乳胶手套
【储存条件及有效期】
1、2-8℃保存,切勿冷冻,有效期6个月。
2、开封使用后,包被微孔板放入带有干燥剂的自封袋中,密闭自封袋,并将全部试剂放回2-8℃冰箱。
3、开封后,按照建议的条件保存,校准品、包被微孔板和HRP标记抗体,有效期为14天,其他成分在标签标明的有效期内是稳定的。
【适用仪器】
半自动的酶标仪,如Thermo MK3,或者国产酶标仪。
【样本要求】
样本类型和采集
以下只是列出样品采集的一般指南。
所有样本采集过程中,不得使用叠氮钠做为防腐剂。
1、细胞培养上清:4000rpm条件下离心20min,去除细胞颗粒和聚合物,上清液保存在- 20℃以下,避免反复冻融。
2、血清:使用不含热原和内毒素的试管,操作过程中避免任何细胞刺激,4000rpm条件下离心20min,小心地分离出血清,保存在- 20℃以下,避免反复冻融。
3、血浆:肝素,EDTA,或柠檬酸钠作为抗凝剂。
在4000rpm条件下,离心20分钟取上清,血浆保存在-20℃以下,避免反复冻融。
样本在2-8℃条件下,可以储存72h,或者在- 20℃储存6个月。
样本收集后,不是一次检测完,请按一次用量分装冻存,避免反复冻融,使用时在室温下解冻,确保样品均匀充分解冻。
【样品准备】
1.取动物全血按常规方法制备血清,要求血清清亮,无溶血、无污染。
样品1周内可于2~8℃保存,长期需置-20℃保存。
2.用样品稀释液将待检血清按40倍稀释(如5μl血清加入195μl样品稀释液中,混匀)。
阴、阳性对照不用稀释。
3.浓缩洗涤液使用前应恢复至室温使沉淀溶解,然后用蒸馏水或去离子水作20倍稀释。
【检验方法】
1.使用前将试剂盒置室温30分钟,恢复至室温。
2.取所需用量酶标板条,设空白对照1孔、阴性/阳性对照各2孔,未用的板条尽快密封,2~8℃保存。
3.空白对照孔加样品稀释液100μl;阴、阳性对照孔分别加入阴、阳性对照100μl;样品孔每孔加入稀释后的样品100μl。
4.混匀,置37℃反应30分钟。
5.扣去孔内液体,每孔加满洗涤液,静置30秒后弃去,重复洗涤5次,拍干。
6.每孔加酶标记物100μl(空白孔除外)。
置37℃反应30分钟。
7.洗涤,同步骤5。
8.每孔依次加底物液A、底物液B各50μl,混匀,37℃避光反应10分钟。
9.每孔加终止液50μl,混匀,于450nm(可用630nm作参比波长)测定各孔吸光值(A 值),无参比波长用空白孔调零(即所有孔吸光值减去空白孔吸光值)。
【参考值】实验正常的情况下,阴性对照≤0.10,阳性对照≥0.6。
【检验结果的解释】
1.样品A值≥0.38为阳性;样品A值在0.2到0.38之间为可疑;样品A值<0.2为阴性。
2.本实验结果为阴性或可疑时表明猪只抗体水平不足,建议补打相应疫苗。
【试验方法的局限性】
该试验仅作为定性检测猪血清、血浆中猪口蹄疫病毒O型抗体,根据A值高低可作抗体水平强、中、弱的粗略评估。
【保存条件】
2℃-8℃保存,有效期6个月。
【注意事项】
生物安全
1、检测必须符合实验室管理规范的规定,严格防止交叉污染,所有样品、洗弃液和各种废弃物都应按照传染物进行处置。
2、试剂盒的液体组分中,含有proclin-300防腐剂,可能引起皮肤过敏反应,避免吸入烟雾与皮肤接触。
3、底物液对皮肤、眼睛和上呼吸道有刺激作用,避免吸入烟雾。
戴上防护手套,实验完成后彻底洗手。
技术提示
1、混合蛋白溶液时,避免起泡。
2、加校准品与样本时,每个校准品浓度和样本都要更换移液枪头,公共组分应该悬臂加样,避免交叉污染。
3、合适的温育时间,和充分的洗涤步骤,是保证实验结果准确性的必要条件。
4、底物溶液为无色液体,保存过程中变为蓝色,代表底物溶液已经失效,不得使用。
5、终止液加样顺序与底物溶液加样顺序一致,加入终止液后,蓝色底物产物,会瞬间变为黄色。
6、实验中,用剩的板条,应立即放回自封袋中,密封(低温干燥)保存。
7、所有液体组分,使用前充分摇匀,严格按照说明书标明的时间、加样量及加样顺序进行
温育操作。
废物处理
所有使用或未使用的试剂,所有污染性的一次性材料,应当遵循传染性或潜在传染性产品的处理程序,每个实验室都有责任根据其实验的类型和危险性级别,进行废物和污物的处理,同时要严格依照有关规定对待所有的废物和污物。
