4型禽腺病毒抗体ELISA检测规程湖北标准2020版
禽流感的流行特点和检测技术

中国动物保健2021.06禽流感(avian influenza ,AI )的潜伏期一般较短,通常为4~5d 。
发病时精神沉郁,食欲、饮欲降低甚至废绝,被毛散乱,体温升高,趴卧不动,偶有流泪。
头部、面部水肿,脚鳞发紫出血,肉垂和鸡冠呈干枯紫色,甚至坏死。
呼吸困难,咳嗽,听诊呈啰音;下痢,粪便呈淡黄或白色。
出现神经症状,共济失调,不能站立或行走。
并且该病为人畜共患病,处理不好不但会危害养禽业的经济发展,还会危害人类身体健康。
1禽流感的流行病学特点1.1传染源主要由感染或携带禽流感病毒的鸡、鸭、鹅等家禽,野外野生鸟类,特别是迁徙性水禽相互传染所致。
1.2传播途径主要通过病禽的分泌物、排泄物、尸体,污染的饮水、饲料和其他物体,直接或间接接触引发感染,主要感染途径为呼吸道和消化道,以及直接接触病毒毒株感染。
人工接种可通过气溶胶经口鼻内、气管内、眼结膜、腹腔、肌肉、静脉和泄殖腔内等途径使易感禽类感染。
1.3易感动物禽流感病毒在世界范围内广泛分布。
许多家禽、野禽、人类、特别是鸭等迁徙水禽,发生病毒感染的概率比其他禽类高,而家养的鸡和火鸡所发生的流感最为严重。
1.4特点多为大流行,世界范围流行。
过去呈三年小流行,五年大流行。
该病主要在寒流较多,气温变化大的秋冬、冬春交替季节流行。
2禽流感的检测技术2.1血清学诊断技术中和试验中和试验的操作步骤复杂,容易造成材料的浪费,临床上不常用,但其为最原始的病毒检测技术,常用来做标准与其他检测方法作比较。
本试验常用鸡胚或组织培养细胞作为样本鉴定禽流感病毒。
中和试验是具有高度的灵敏性和特异性的血清学方法,抗体只和病毒上表面抗原相对应,特别是已吸附的宿主细胞上的病毒颗粒表面的抗原相对应。
所以,在某种特定血清型的中和实验中,抗体只和组内的其他病原发生有限的交叉反应。
琼脂扩散试验琼脂扩散试验检测禽流感时,以具有血凝素活性的鸡胚尿囊液作为样品,采用已知的阳性血清和未知抗原进行病毒抗原型的特异性鉴定。
禽腺病毒Ⅰ群的研究现状

禽腺病毒Ⅰ群的研究现状王亚楠;韩涛;李纯玲;刘中奇;宋楠;刘瑞凿;雷娜;吴培星【摘要】近年来,全国各地相继暴发禽腺病毒I群疾病,给养殖业造成了很大的经济损失.本文将从病原学、流行病学、病毒的分离培养、诊断技术及预防等方面对该病的研究现状进行总结.【期刊名称】《中国动物保健》【年(卷),期】2017(019)001【总页数】4页(P61-64)【关键词】腺病毒;禽;研究现状【作者】王亚楠;韩涛;李纯玲;刘中奇;宋楠;刘瑞凿;雷娜;吴培星【作者单位】北京天之泰生物科技有限公司北京100194;北京天之泰生物科技有限公司北京100194;北京天之泰生物科技有限公司北京100194;北京天之泰生物科技有限公司北京100194;北京天之泰生物科技有限公司北京100194;北京天之泰生物科技有限公司北京100194;北京天之泰生物科技有限公司北京100194;北京天之泰生物科技有限公司北京100194;中国农业科学院兰州畜牧与兽药研究所甘肃兰州730050【正文语种】中文禽腺病毒(Fowl adenovirus,FADV)属于腺病毒科,根据群特异性抗原的不同,分为三个群,分别是Ⅰ亚群、Ⅱ亚群和Ⅲ亚群。
禽腺病毒Ⅰ群(Fowl adenovirus group I,FADV-I)具有共同的群抗原,共12个血清型,普遍存在于鸡、鸭、鹅体内,一些血清型在肉鸡、野鸡、火鸡、鸽子、鹦鹉、长尾鸭、猎鹰中也有发现。
临床主要表现为包涵体肝炎(Inclusion body hepatitis,IBH)、心包积液综合症(hydropericardium syndrome,HPS)和肌胃糜烂症(adenoviral gizzard erosion,AGH)。
禽腺病毒Ⅱ群可引起火鸡出血热和雉鸡大理石脾病,禽腺病毒Ⅲ群仅引起减蛋综合征。
在免疫学上,禽腺病毒I群能够诱导已感染的禽类产生高水平的中和循环抗体,并可在局部黏膜系统长期复制并持续少量排毒。
2020年主要动物疫病的检测方法及判定标准
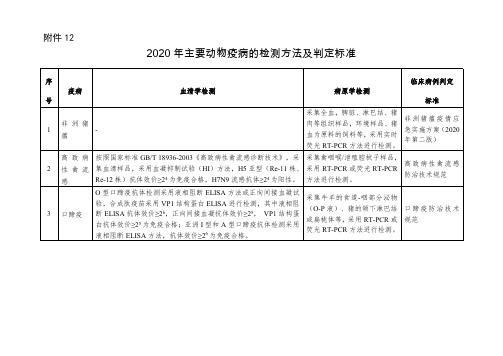
采集扁桃体或颌下淋巴结,采 用猪瘟病毒 RT-NPCR、猪瘟病 毒荧光 RT-PCR 或猪瘟荧光抗 体检测方法进行检测。
猪瘟防治技术规 范
6 新城疫 采用血凝抑制试验方法,抗体效价≥25 的判为免疫合格
采集禽蛋咽喉/泄殖腔拭子,采 新城疫防治技术
用 RT-PCR 或荧光 RT-PCR 方 规范
法进行检测。
8
-
菌病
凝集试验或补体结合试验或采用 OIE 推荐的竞争酶联免疫吸附试验
(cELISA 试验)进行确诊。
按照国家标准(GB/T 18645-2002),用牛型结核分枝杆菌 PPD 皮内
变态反应试验或用外周血-干扰素体外释放检测法进行检测。对皮内
9 奶 牛 结 变态反应检测阳性结果疑似的动物,45 天后用牛型和禽型结核分枝
采集鼻腔/眼拭子或淋巴结、脾 4 小 反 刍 采用竞争 ELISA、阻断 ELISA 方法进行检测,结果判定参照试剂盒 脏等组织样品,采用 RT-PCR 小 反 刍 兽 疫 防 治
兽疫
说明书
或者荧光 RT-PCR 方法进行检 技术规范
测。
5 猪瘟
采用阻断 ELISA、间接 ELISA 或正向间接血凝试验;猪瘟抗体阻断 ELISA 和猪瘟抗体间接 ELISA 检测,抗体阳性即判定为合格,正向 间接血凝试验抗体效价≥25 为免疫合格
高致病性禽流感
2 性 禽 流 集血清样品,采用血凝抑制试验(HI)方法,H5 亚型(Re-11 株、 采用 RT-PCR 或荧光 RT-PCR
防治技术规范
感
Re-12 株)抗体效价≥24 为免疫合格,H7N9 流感抗体≥24 为阳性。 方法进行检测。
3 口蹄疫
O 型口蹄疫抗体检测采用液相阻断 ELISA 方法或正向间接血凝试 验,合成肽疫苗采用 VP1 结构蛋白 ELISA 进行检测,其中液相阻 断 ELISA 抗体效价≥26,正向间接血凝抗体效价≥25, VP1 结构蛋 白抗体效价≥25 为免疫合格;亚洲 I 型和 A 型口蹄疫抗体检测采用 液相阻断 ELISA 方法,抗体效价≥26 为免疫合格。
禽腺病毒的结构及其血清4型检测方法研究进展

禽腺病毒的结构及其血清4型检测方法研究进展
王凯莉;刘成;楚肖冉;司振书;路建彪;李玉保;曹胜亮
【期刊名称】《动物医学进展》
【年(卷),期】2023(44)1
【摘要】近年来,由血清4型禽腺病毒引起的肝炎-心包积液综合征给养禽业带来严重的经济损失,该病毒的主要结构蛋白有六邻体、纤突和五邻体,可通过琼脂胶聚免疫扩散试验(AGIDT)、聚合酶链反应(PCR)、酶联免疫吸附试验(ELISA)等进行诊断,其中聚合酶链反应是最常用的分子生物学诊断方法;血清学检测方法中将禽腺病毒重组蛋白作为包被抗原建立的ELISA方法最为常用。
论文对禽腺病毒基因组和蛋白结构及FAdV-4检测方法进行了综述,以期为该病的快速检测及科学防控提供理论和技术支持。
【总页数】6页(P111-116)
【作者】王凯莉;刘成;楚肖冉;司振书;路建彪;李玉保;曹胜亮
【作者单位】聊城大学农学院
【正文语种】中文
【中图分类】S852.659.1;S852.657
【相关文献】
1.Ⅰ群禽腺病毒血清4型TaqMan探针实时荧光定量PCR检测方法的建立及应用
2.禽腺病毒血清4型纳米PCR检测方法的建立与初步应用
3.禽腺病毒血清4型TaqMan荧光定量PCR检测方法的建立与应用
4.血清4型禽腺病毒POCT荧光微
球免疫层析检测方法的建立5.禽腺病毒血清4型SYBR GreenⅠ荧光定量PCR检测方法的建立与应用
因版权原因,仅展示原文概要,查看原文内容请购买。
《禽流感病毒ELISA抗体检测技术规范》标准文本

禽流感病毒ELISA抗体检测技术规范前言本标准按GB/T 1.1-2009《标准化工作导则第1部分:标准的结构和编写》给出的规则起草。
本标准的附录A为规范性附录。
本标准起草单位:贵州省动物疫病预防控制中心。
本标准由贵州省动物疫病预防控制中心提出并归口。
本标准主要起草人:刘霞、王慧、李照伟、孙鹃、倪兴维、张霞、蒲同灿、汪忠荣。
禽流感病毒ELISA抗体检测技术规范1 范围本标准规定了禽流感病毒H5亚型、H7亚型抗体的竞争ELISA检测方法。
本标准适用于检测免疫的鸡、鸭、鹅等禽类血清中H5亚型或H7亚型禽流感病毒的抗体水平。
2 缩略语下列缩略语适用于本文件。
ELISA 酶联免疫吸附试验(Enzyme-linked immunosorbent test)OD4500nm值 450纳米波长处的吸光值3实验原理本标准采用竞争酶联免疫吸附法(竞争ELISA),该方法利用抗原抗体反应具有特异性的特点,将特异性的H7亚型(或H5亚型)禽流感病毒血凝抑制试验抗原吸附到固相载体的表面,将待检血清和特异性酶标单抗同时加入包被板孔。
待检血清中的抗体与酶标单抗竞争与包被抗原结合,因此,待检血清中抗体越多结合在包被抗原上的酶标单抗就越少,阳性血清反应呈色浅于阴性血清。
4 材料准备4.1 试剂见附录A。
4.2 仪器与器材酶标检测仪、台式低温高速离心机、37℃恒温培养箱、冰箱、微量移液器及配套洗头等。
4.3 样品动物血清或动物全血(待血液充分凝固后,4000r/min离心10分钟,收集上清),要求血清清亮,无溶血。
5 实验方法5.1 包被用包被液将包被抗原稀释至工作浓度(2μg/ml)加至抗原包被板中100μl/孔,置37℃下温育45分钟(或2℃~8℃包被15小时)。
5.2 封闭弃去包被液,每孔加入封闭液200μl,置37℃ 2小时;拍干,再置37℃干燥2小时。
5.3 1×洗涤液的配制使用前,将20倍浓缩洗涤液恢复至室温(15℃~25℃)并摇动使沉淀溶解(最好在37℃水浴锅中加热5~10分钟),然后用去离子水作20倍稀释(例如30ml 20倍浓缩洗涤液加上570ml去离子水),混匀,稀释好的洗涤液在2℃~8℃下存放7日。
Ⅰ群禽腺病毒4型IgG抗体间接ELISA检测方法的建立

Ⅰ群禽腺病毒4型IgG抗体间接ELISA检测方法的建立张启龙;孙丹;韦海涛;宋彦军;周德刚;冯小宇;王林【摘要】利用纯化的Ⅰ 群禽腺病毒4型重组Hexon蛋白,通过各反应条件筛选,建立了Ⅰ 群禽腺病毒4型IgG抗体间接ELISA检测方法.结果显示,抗原最佳包被浓度为1μg/mL;最佳封闭液为1%牛血清白蛋白;待检血清最佳作用浓度是400倍稀释,37℃孵育60 min;酶标抗体的最佳作用条件为稀释度1:8000,37℃孵育60 min;最佳显色时间为10 min.用所建方法对160只临床鸡只进行检测,同时与拭子PCR检测对比,一致性较好,表明该方法可有效用于临床检测.【期刊名称】《中国兽药杂志》【年(卷),期】2019(053)008【总页数】7页(P1-7)【关键词】Ⅰ群禽腺病毒4型;Hexon蛋白;间接ELISA;检测【作者】张启龙;孙丹;韦海涛;宋彦军;周德刚;冯小宇;王林【作者单位】北京市动物疫病预防控制中心,北京 102629;北京市兽药监察所,北京102629;北京市动物疫病预防控制中心,北京 102629;北京市动物疫病预防控制中心,北京 102629;北京市动物疫病预防控制中心,北京 102629;北京市动物疫病预防控制中心,北京 102629;北京市动物疫病预防控制中心,北京 102629【正文语种】中文【中图分类】S852.65肝炎-心包积液综合征(Hepatitis and hydropericardium syndrome,HHS)是由禽腺病毒4型(Fowl adenovirus serotype 4, FAdV-4)新基因型引起的以禽心包积液、肝脏黄染、肿大和出血为特征的传染病[1]。
HHS首次于1987年在巴基斯坦的安卡拉地区发生,又名安卡拉病,随后在亚洲、欧洲和南美洲等地区流行[2-4]。
2013年以来该病在我国河南、山东、江苏、河北、陕西等地大面积流行,给家禽养殖业造成了巨大经济损失[5-7]。
腺病毒

生活周期
腺病毒的生活周期可以分为两个截然不同却又不能割裂开来的两个阶段。第一阶段包括腺病毒颗粒粘附和进 入宿主细胞,将基因组释放到宿主细胞核中,以及有选择性地转录和翻译早期基因。在这个阶段,细胞为病毒基 因组复制和腺病毒晚期基因表达并最终释放成熟的感染颗粒,即第二阶段,作好了准备。第一阶段将在6~8个小 时内完成,第二阶段则更快,只需4~6个小时。
分类
分类及自上个世纪50年代发现并成功分离腺病毒以来,已陆续发现了100余个血清型,其中人腺病毒有52种, 分为A、B、C、D、E和F六个亚群(subgroup)。基因治疗常用的人的2型及5型腺病毒在血清学分类上均属C亚群, 在DNA序列上有95%的同源性。二者的增殖能力非常强,滴度通常可以达到109pfu (plaque forming unit)/ml, 其在单个细胞中的基因组拷贝数可达104(约占细胞总DNA的10%)。病毒颗粒比较稳定,通过CsCl梯度离心可以 达到1010~1011pfu/ml,满足动物实验的要求。
防治原则
腺病毒的甲醛灭活疫苗已被用于某些人群的预防,而且将来有被用人二倍体细胞培养的减毒活疫苗所替代的 可能。但因腺病毒对动物具有致癌作用,人们对全病毒疫苗的作用与安全性存有疑虑。此外加强游泳池和浴池水 的消毒,可使水传播性结膜炎爆发的危险性降至最小,在作眼的检查时应严格无菌操作,对所用设备充分灭菌, 也可控制流行性结膜炎的发生。对腺病毒感染的治疗仍无有效药物。
许多腺病毒在肠道细胞中复制,随粪便排出,但大多血清型与胃肠道疾病无关。而40型和41型腺病毒可引起 婴幼儿与年少(4岁以下)儿童的胃肠炎,致腹痛、腹泻。C组腺病毒能引起某些婴幼儿肠套叠。
腺病毒11、12型能引起儿童急性出血性膀胱炎,尿中出现病毒。37型可引起女性宫颈炎和男性尿道炎,常由 性传播感染。在免疫功能低下者可引起偶发或严重的病毒感染,尤其在器官移植病人中发生严重呼吸道感染和病 毒性肝炎,多由1、5和7型腺病毒引起。艾滋病患者可感染多种血清型腺病毒,并能出现抗原性介于中间的杂合 型毒株,而且常为致死性腺病毒感染。主要原因是腺病毒的E1A蛋白可反式激活HIV的转录,加速HIV的复制。临 床发现37%的艾滋病患者病毒性腹泻是由腺病毒所致。
标准操作规程(SOP)——流感禽流感微量中和抗体检测

标准操作规程(SOP)——一、目的微量中和试验是一种敏感性高、特异性强的血清学方法,用于测定血清中的病毒特异性中和抗体水平。
中国国家流感中心的所有技术人员,必须按照本文件相关的操作规程,进行流感/禽流感微量中和抗体检测实验,以确保实验的准确性。
二、范围适用于中国国家流感中心的所有技术人员进行流感/禽流感微量中和抗体检测。
三、责任进行流感/禽流感微量中和抗体检测的技术人员需严格按照规定进行操作。
四、程序(一)生物安全要求H5,H7亚型高致病性禽流感病毒,H2N2亚型流感病毒的操作需要在生物安全3级(BSL-3)实验室中进行。
其余流感病毒的操作需要在生物安全2级(BSL-2级)实验室中进行。
操作人员必须严格按照相应实验室的要求做好个人防护。
(二)材料1.中和反应实验材料(1)病毒:一般采用接种鸡胚尿囊腔后收获的流感/禽流感病毒液,在-70℃中保存,并且注意避免反复冻融。
进行中和试验之前,需先进行病毒滴度(TCID50)的滴定。
具体步骤如下,1)病毒的稀释:可采取对数或者半对数稀释的方法。
以下介绍半对数稀释法。
取1管冻存病毒尿囊液,用病毒培养液进行1:100稀释。
第一列4个孔每孔加入146μL 1:100稀释过的病毒液,其它各列每孔加入100 μL 病毒培养液。
然后用多道加样器从第一孔吸46μL 至第二孔,做系列半对数稀释,使之成为10-2、10-2.5、10-3、10-3.5……10-7。
每孔含有100μL 病毒液。
2)每孔加入100μL MDCK 细胞悬液(1.5×104细胞/孔),37℃,5%CO 2培养箱孵育18~22h 。
每一滴度作平行4孔。
3)细胞固定、ELISA 操作如下述。
4)OD 值 〉2倍MDCK 细胞对照OD 值判定为阳性5)病毒滴度计算见组织细胞半数感染量滴定SOP 。
(2)血清样品:包括待检血清、阳性及阴性血清对照。
如果待检血清有可能需要多次检测,则需将待检血清进行小量分装,-20℃至-70℃保存均可,避免多次反复冻融。
《中国药典》2020版—禽源性病毒荧光定量 PCR(Q-PCR)检查法

禽源性病毒荧光定量PCR(Q-PCR)检查法本法适用于禽源性生物制品的检测,包括流感全病毒灭活疫苗、流感病毒裂解疫苗种子批毒种的外源性禽病毒检测。
本法用提取的供试品RNA,反转录成cDNA后,或用提取的供试品DNA,针对3种外源性禽病毒设计特异性引物探针,进行荧光定量PCR 检测特异性扩增信号,从而测定供试品中外源性禽源病毒核酸序列,以检查供试品的外源性禽病毒污染。
要求检测的 3 种禽源性病毒:(1)禽腺病毒I 型(DNA 病毒)(2)禽腺病毒III 型(DNA 病毒)(3)外源性禽白血病病毒(逆转录病毒)试剂(1)RNA/DNA 提取试剂:RNA/DNA 的提取可使用酚-氯仿法、磁珠法、离心柱法等。
提取试剂中应含裂解液、洗涤液、洗脱液等,按试剂说明书要求配制。
(2)反转录试剂:含逆转录酶、RNA 酶抑制剂、dNTP 混合液、随机引物、逆转录反应缓冲液等,按试剂说明书要求配制。
(3)引物序列、探针序列见表1。
表 1 引物序列及探针序列(4)扩增缓冲液每20µl 反应体系中,含有上下游引物各5µmol,探针2.5µmol及适量荧光定量PCR混合液(Mix)。
(5)质粒标准品稀释液为DNA 稀释缓冲液或无RNA 酶水稀释。
(6)对照溶液以失活后无感染性的禽源性病毒为阳性对照。
以无RNA 酶水作为阴性对照。
提取核酸和逆转录步骤同(1),置-70℃保存备用。
(7)质粒标准品溶液及灵敏度供试品的制备选择病毒目的核酸序列,人工合成DNA,目的序列转入pMD19-T 质粒中,作为质粒标准品。
测定质粒标准品的DNA 核酸浓度后,对其进行10 倍稀释,从109Copies/µl 稀释至100Copies/µl。
取107Copies/µl~103Copies/µl 质粒标准品溶液作标准曲线各点。
101Copies/µl 稀释度作为灵敏度对照。
Ⅰ群4型禽腺病毒卵黄抗体实验室产品制备

Ⅰ群4型禽腺病毒卵黄抗体实验室产品制备于洪涛;赵丽;王昊【摘要】试验应用自行分离鉴定的Ⅰ群4型禽腺病毒HY株,制备了3批Ⅰ群4型禽腺病毒卵黄抗体,并进行了性状、装量、无菌、支原体、外源病毒、安全、效力、甲醛和辛酸残留量检测.试验结果表明,试制的3批卵黄抗体呈淡黄色澄明液体;装量符合规定标准要求;无细菌、霉菌、支原体及外源病毒污染,安全性好,预防效果好.【期刊名称】《饲料博览》【年(卷),期】2018(000)001【总页数】5页(P36-40)【关键词】卵黄抗体;实验室产品【作者】于洪涛;赵丽;王昊【作者单位】哈药集团生物疫苗有限公司,哈尔滨150069;哈药集团生物疫苗有限公司,哈尔滨150069;哈药集团生物疫苗有限公司,哈尔滨150069【正文语种】中文【中图分类】S852.65;S83腺病毒是全球家禽和野禽常见的传染病原之一[1-3]。
多数腺病毒可在健康禽体内存在并复制,不表现临床症状或临床症状非常轻微,但可成为混合感染时的条件性病原;腺病毒有时也可作为原发性病原,引起禽类的多种病症[4-6]。
腺病毒可分为A、B、C、D、E 5个种12个血清型,我国主要流行A、B、C 3种基因型,共6个血清型(火鸡1型、1型、4型、5型、8a/b型),但是近期在豫南、皖北、苏北、鲁西北和胶东地区流行的禽腺病毒主要是血清4型和8a/b型,造成鸡群的死亡率较高,并且发病急,有蔓延的趋势。
安卡拉病(心包积水-肝炎综合征)就是由Ⅰ群腺病毒,血清4型引起来的。
该病多发于肉鸡,近期也开始感染麻鸡以及产蛋鸡的育成鸡,并且育成鸡发病死亡率还非常高。
Ⅰ群禽腺病毒的12个血清型交叉保护性较差,因此在防控上必须选用与流行株匹配的疫苗株和卵黄抗体才能有效遏制疫情的蔓延。
并目前市场上没有商品化的疫苗或卵黄抗体,我公司通过自行分离的Ⅰ群4型禽腺病毒HY株,制备免疫原免疫蛋鸡,制备了3批Ⅰ群4型禽腺病毒卵黄抗体实验室制品,并且经过检验,该3批制品有较好的安全性及效力,为公司下一步申报该产品的新兽药注册证书奠定基础。
DB13_T2593-2017禽腺病毒4型PCR检测方法

ICS11.220B 43 DB13 河北省地方标准DB13/T 2593—2017 禽腺病毒4型PCR检测方法2017-11-22发布2017-12-22实施前言本标准按照GB/T 1.1-2009给出的规则起草。
本标准由河北农业大学提出。
本标准起草单位:河北农业大学。
本标准主要起草人:袁万哲、王建昌、孙继国、刘聚祥、李丽敏、陈立功、李睿文、张磊、白云、陈赛娟、李杰峰。
禽腺病毒4型PCR检测方法1 范围本标准规定了禽腺病毒4型PCR检测方法的技术要求。
本标准适用于检测家禽咽喉拭子、肛拭子,发病禽组织和这些采集样品培养物中的禽腺病毒4型。
2 术语和定义下列术语和定义适用于本文件。
2.1DNA脱氧核糖核酸(deoxyribonucleic acid)2.2EB溴化乙锭(ethidium bromide)2.3PCR聚合酶链式反应(polymerase chain reaction)2.4dNTP脱氧核苷酸三磷酸(deoxy-ribonucleoside triphosphate)3 试剂或材料包括各种市售病毒核酸提取试剂盒,1.0%琼脂糖凝胶,50×TAE缓冲液,溴化乙锭(EB,10 ug/μL)或核酸染料,焦碳酸二乙酯(DEPC)处理的灭菌的双蒸水,DNA分子量标准(100 bp),2×Taq MasterMix 或商品化的一步法PCR反应试剂。
警示:电泳中用到的EB在操作中应戴手套和口罩。
试验中被EB污染的物品要进行无害化处理;DEPC 在操作中应在通风条件下进行,使用时戴手套和口罩,不小心沾到皮肤应立即冲洗。
3.1 病毒核酸提取试剂盒。
3.2 1.0 %琼脂糖凝胶,配制方法见附录A中A.1。
3.3 50×TAE缓冲液,配制方法见附录A中A.2。
3.4 溴化乙锭(EB,10 ug/μL)或核酸染料,配制方法见附录A中A.3。
3.5 焦碳酸二乙酯(DEPC)处理的灭菌的双蒸水,配制方法见附录A中A.4。
禽Ⅰ群腺病毒血清4型感染的诊断与防治

图1 病死鸡心包积液、肝色浅质脆、肿大充血二、病理剖检病变IBH 特征性病理剖检变化表现在肝脏和骨髓。
肝脏肿大,边缘钝圆,表面有不同程度的出血点或条索状出血斑,质脆,褪色,呈淡黄色,胆囊充盈,内有大量胆汁淤积。
偶尔可见肝脏有大小不一的坏死灶,并伴随血细胞浸润,使肝脏触之有凹凸不平的感觉。
骨髓呈灰白色或黄色胶冻样病变、体积变小,法氏囊萎缩,内膜有出血点或出血斑,且切面无光泽。
胸腺点状出血、萎缩、且颜色变深。
脾脏体积变化不大,偶见个别病例脾脏肿大、出血。
肾脏呈灰白色、肿大,表面有癖斑和疲点。
肺充血、水肿,除此之外,可见大腿部肌肉、胸肌以及皮下组织图2 病死鸡的心、肝、法氏囊、肾、脾、肺病理切片四、实验室诊断1.引物的设计合成。
根据 GenBank 中已发表的Ⅰ群禽腺病毒 Hexon 基因核酸序列设计完成两对引物,预计扩增片段为500 bp。
上游引物为P1: 5'CGAGGTCTATACCAACACG-AGCA-3';下游引物为P2: 5'-CGGCGCAGG TTAA-TGAAGTTATC-3'。
引物由吉林库美生物工程技术有限公司合成。
2.病毒分离与鉴定。
取疑似鸡包涵体肝炎病鸡的肝脏剪碎,按 1∶5(W/V)比例加入灭菌PBS进行匀浆处理,将匀浆液反复冻融 3次,4 000 r/min离心30 min,取上清液备用。
上清液中加双抗(青霉素、链霉素)各3 000 U/ml,置4℃过夜,以8 000 r/min离心10 min,取制备的上清液以卵黄囊途径接种5日龄SPF 鸡胚,0.2 ml/胚,于 37℃孵育,每日观察2次,收获 24~144 h内死亡的鸡胚尿囊液,收集死胚尿囊液,进行HA试验及PCR鉴定。
3.病毒DNA的提取及PCR扩增。
病毒液采用TaKaRa MiniBEST Viral RNA DNA Extraction Kit Ver.5.0 提取试剂盒,按说明书进行病毒DNA的提取。
血清4型禽腺病毒研究进展

血清4型禽腺病毒研究进展朱庆贺;张鹏宇;王观悦;王爽;陈曦;杨旭东;史同瑞【摘要】近年来,血清4型禽腺病毒( FAdV-4)在我国爆发,造成家禽行业严重的经济损失.病毒感染引起死亡率高,临床剖检可见明显的心包积液综合征的症状.病毒极具传染性,可垂直及水平传播,通过受感染肝脏组织匀浆可以分离和检测病毒.目前实验室诊断主要通过琼脂扩散试验、酶联免疫吸附试验、限制酶分析、聚合酶链式反应、实时荧光定量PCR、高分辨率的融化曲线分析等进行检测.疾病预防主要通过灭活疫苗的接种,而减毒活疫苗和亚单位疫苗也相继被开发.对FAdV-4的流行病学、发病特征、病毒诊断方法以及预防策略等方面进行了综述,以期为FAdV-4的深入研究奠定基础.【期刊名称】《中国兽药杂志》【年(卷),期】2018(052)011【总页数】6页(P80-85)【关键词】4型禽腺病毒;流行;诊断;疫苗【作者】朱庆贺;张鹏宇;王观悦;王爽;陈曦;杨旭东;史同瑞【作者单位】黑龙江省兽医科学研究所,黑龙江齐齐哈尔161000;黑龙江八一农垦大学,黑龙江大庆163000;黑龙江省兽医科学研究所,黑龙江齐齐哈尔161000;黑龙江省兽医科学研究所,黑龙江齐齐哈尔161000;黑龙江省兽医科学研究所,黑龙江齐齐哈尔161000;黑龙江省兽医科学研究所,黑龙江齐齐哈尔161000;黑龙江省兽医科学研究所,黑龙江齐齐哈尔161000【正文语种】中文【中图分类】S852.654型禽腺病毒(Fowl avianadenovirus serotype 4,FAdV-4)主要是以心包积水为主要临床症状的鸡急性传染病,临床中又称为“鸡心包积水综合征(Hydropericardium syndrome,HPS)”。
该病发病急,传播速度快,主要引起4~8周龄肉鸡感染,死亡率可达40%~90%。
该病最早于巴基斯坦的安卡拉被报道,由此又成为“安卡拉病”。
近年来,我国河南、山东、安徽、辽宁、吉林、江西和湖北等省份出现大面积爆发,给我国养鸡业造成了严重的经济损失。
Ⅰ群禽腺病毒检测方法研究进展

Ⅰ群禽腺病毒检测方法研究进展殷国政;段世豪;司振书;李玉保【摘要】Ⅰ群禽腺病毒感染可引起鸡的包涵体肝炎(IBH)或包涵体肝炎心包积液综合症(HHS)等疫病,该病毒分布广泛.近年来,我国鸡群发生IBH和HHS的病例较多,严重危害我国养禽业的健康发展,造成巨大的经济损失.综述Ⅰ群禽腺病毒的分离培养、形态学检测、血清学检测及分子生物学检测方法,以对Ⅰ群禽腺病毒感染进行有效防控.【期刊名称】《安徽农业科学》【年(卷),期】2018(046)030【总页数】3页(P21-23)【关键词】Ⅰ群禽腺病毒;分离培养;诊断【作者】殷国政;段世豪;司振书;李玉保【作者单位】聊城大学农学院,山东聊城252000;聊城大学农学院,山东聊城252000;聊城大学农学院,山东聊城252000;聊城大学农学院,山东聊城252000【正文语种】中文【中图分类】S852.65+7Ⅰ 群禽腺病毒(Fowl adenovirus group I,FAV-I)属于腺病毒科禽腺病毒属,在禽群中分布广泛。
Ⅰ群禽腺病毒具有共同的群抗原,其根据分子结构可将血清型分为A、B、C、D、E 5个种,基于交叉中和试验和限制性内切酶酶切分析,又分为A(血清1型)、B(血清5型)、C(血清4、10型)、D(血清2、3、9、11型)、E(血清6、7、8a、8b型)等12个血清型[1]。
其中,鸡腺病毒1型,又名鸡胚致死孤儿病毒(chicken embryo lethal orphan virus,CELO),引致鹌鹑支气管炎;鸡腺病毒4型,可引起鸡心包积液与包涵体肝炎综合征(hepatitis-hydropericardium syndrome,HHS);鸡腺病毒8型,可引致鸡包涵体肝炎(inclusion body hepatitis,IBH)。
Ⅰ群禽腺病毒通过候鸟水禽等传播于世界各地,难以控制,并且可以与其他病毒混合感染,给养禽业造成严重的经济损失。
综述国内外I群禽腺病毒的分离培养、形态学检测、血清学检测及分子生物学检测方法,以促进对该类病毒感染进行及时确诊和有效防控。
兽医实验室常见疫病诊断方法与标准

兽医实验室常见疫病诊断方法与标准展开全文编号疫病种类诊断方法检测标准及编号(含年号)序号名称一多种动物共患病口蹄疫1反转录聚合酶链反应(RT-PCR)试验GB/T 18935-20032液相阻断 - 酶联免疫吸附试验(LpB-ELISA)3病毒感染相关(VIA)抗原琼脂凝胶免疫扩散试验(VIA-AGID)医学教|育网搜集整理4正向间接血凝试验农(牧)字第( 17 )号( 1988 )5非结构蛋白抗体单抗阻断酶联免疫吸附试验(ELISA)NY/SY548-2005二伪狂犬病1聚合酶链反应(PCR)试验GB/T 18641-20022免疫酶组织化学法(猪)NY/T 678-20033E 糖蛋白酶联免疫吸附试验(gE-ELISA)(猪)4酶联免疫吸附试验(ELISA)(gB)(猪)NY/SY569-2005三弓形虫病1猪弓形虫抗体酶联免疫吸附试验(ELISA)NY/SY542-20052聚合酶链反应(PCR)试验四动物衣原体病1间接血凝试验( IHA )NY/T 562-2002五流行性乙型脑炎1乳胶凝集试验NY/SY536-20052反转录聚合酶链反应(RT-PCR)试验六动物布鲁氏菌病1虎红平板凝集试验GB/T 18646-20022试管凝集试验GB/T 18646-20023聚合酶链反应(PCR)试验七猪病猪瘟1猪瘟病毒( CSFV )抗原酶联免疫吸附试验(ELISA)NY/SY576-20052正向间接血凝试验3猪瘟抗体酶联免疫吸附试验(ELISA)4反转录聚合酶链反应(RT-PCR)试验八猪繁殖和呼吸综合症(蓝耳病)1间接酶联免疫吸附试验(间接ELISA )医学教|育网搜集整理GB/T 18090-20002免疫酶组织化学法NY/T 679-20033反转录聚合酶链反应( RT-PCR )试验方法NY/SY533-2005九猪细小病毒病1猪细小病毒乳胶凝集试验NY/SY535-20052猪细小病毒病酶联免疫吸附试验(ELISA)3猪细小病毒聚合酶链反应(PCR)试验十猪喘气病(支原体肺炎)1酶联免疫吸附试验(ELISA)NY/SY573-2005十一猪萎缩性鼻炎1乳胶凝集试验方法NY/SY575-2005十二猪流感1酶联免疫吸附试验(ELISA)NY/SY574-20052反转录聚合酶链反应(RT-PCR)试验十三猪圆环病毒病1猪圆环病毒 II 型抗体酶联免疫吸附试验(ELISA)NY/SY577-20052猪圆环病毒聚合酶链反应(PCR)试验十四猪放线杆菌胸膜肺炎1病原学检查NY/T 537-20022酶联免疫吸附试验(ELISA)十五禽病新城疫1微量红细胞凝集抑制试验GB 16550-19962反转录聚合酶链反应(RT-PCR)试验方法NY/SY570-2005十六高致病性禽流感1琼脂凝胶免疫扩散(AGID)试验GB/T 18936-20032血凝(HA)和血凝抑制(HI)试验技术3禽流感病毒 RT-PCR 试验方法NY/T 772-2004十七鸡马立克氏病1马立克病诊断技术NY/SY534-2005十八禽白血病1病理学诊断方法NY/SY559-2005十九禽脑脊髓炎1反转录聚合酶链反应(RT-PCR)试验NY/SY560-2005二十鸡病毒性关节炎(禽呼肠孤病毒感染)1反转录聚合酶链反应( RT-PCR )试验方法NY/SY543-2005二十一鸡传染性支气管炎1病毒分离鉴定NY/SY546-20052反转录聚合酶链反应(RT-PCR)试验鸡传染性贫血1聚合酶链反应( PCR )试验方法NY/SY545-2005二十二鸡传染性喉气管炎1聚合酶链反应( PCR )试验方法NY/SY544-2005二十三禽网状内皮组织增殖病1病理学诊断方法NY/SY561-2005二十四禽支原体病1禽败血支原体平板凝集试验( MG-Ab )NY/SY562-20052禽败血支原体平板凝集试验( MG-Ab )二十五鸡伤寒和鸡白痢1全血平板凝集试验NY/T 536-2002二十六产蛋下降综合症1聚合酶链反应( PCR )试验NY/SY538-2005二十七牛病牛病毒性腹泻/粘膜病1反转录聚合酶链反应(RT-PCR )试验NY/SY557-20052牛病毒性腹泻 /粘膜病病毒抗体ELISA试验二十八马病马传染性贫血1琼脂凝胶免疫扩散(AGID)试验医学教|育网搜集整理NY/T 569-2002二十九犬猫病犬细小病毒病1血凝抑制试验(HI )GB/T 14926.57-20012聚合酶链反应( PCR )试验NY/SY566-20053胶体金检测试验三十犬瘟热1免疫酶试验GB/T 14926.59-20012免疫酶组织化学法GB/T 14926.55-20013反转录聚合酶链反应( RT-PCR )试验方法NY/SY565-2005三十一犬腺病毒Ⅰ型、Ⅱ型感染(传染性犬肝炎 \ 犬病毒性鼻气管炎)1血凝抑制试验( HI )GB/T 14926.58-20012免疫酶组织化学法GB/T14926.55-20013聚合酶链反应( PCR )试验方法NY/SY567-2005三十二犬冠状病毒病1反转录聚合酶链反应( RT-PCR )试验方法NY/SY564-2005三十三犬狂犬病1酶联免疫吸附试验(ELISA)方法NY/SY549-2005三十四猫传染性腹膜炎1反转录聚合酶链反应( RT-PCR )试验方法NY/SY554-2005三十五猫白血病1反转录聚合酶链反应(RT-PCR )试验方法NY/SY551-2005三十六猫病毒性鼻气管炎(猫疱疹病毒Ⅰ型)1聚合酶链反应( PCR )试验方法NY/SY553-2005三十七猫瘟热1聚合酶链反应( PCR )试验NY/SY556-2005三十八细菌病副猪嗜血杆菌病1副猪嗜血杆菌诊断技术NY/SY541-2005三十九大肠菌群1大肠菌群测定GB/T 4789.3-2003大肠杆菌病2大肠杆菌病诊断技术NY/SY539-2005四十沙门氏菌1沙门氏菌检验GB/T 4789.4-2003沙门氏菌病2沙门氏菌病诊断技术NY/SY568-2005四十一葡萄球菌病1葡萄球菌病诊断技术NY/SY558-2005四十二链球菌病1链球菌病诊断技术NY/SY550-2005四十三猪巴氏杆菌病1病原分离鉴定NY/T 564-2002四十四禽霍乱(巴氏杆菌病)1病原分离鉴定NY/T 563-2002四十五禽曲霉菌病1病理学检查NY/T 559-2002。
I 群禽腺病毒(4 型)Fiber-2 蛋白亚单

·研究论文·Chinese Journal of Animal Infectious Diseases中国动物传染病学报摘 要:为评价I 群禽腺病毒(4型)Fiber-2重组蛋白亚单位疫苗的免疫保护效果,本研究利用FAV-HN 株Fiber-2基因构建pET-30a-Fiber-2重组质粒,转化至BL21感受态诱导表达Fiber-2重组蛋白;Fiber-2蛋白纯化后制备不同抗原含量的亚单位疫苗,免疫SPF 鸡进行免疫效力评价。
结果表明,Fiber-2蛋白部分为可溶性表达,纯化后纯度约90%,AGP 效价达1∶64。
亚单位疫苗抗原含量AGP 效价不低于1∶2时,SPF 鸡免疫后第21 d AGP 抗体10/10阳性,可抵抗Ⅰ群禽腺病毒(4型)强毒株的攻击,提供100%的免疫攻毒保护。
关键词:禽腺病毒;Fiber-2蛋白;亚单位疫苗;免疫攻毒保护中图分类号:S859.797 文献标志码:A 文章编号:1674-6422(2022)06-0077-06Immunogenicity of a Subunit Vaccine of Fiber-2 Protein against Fowl AdenovirusSerotype 4 of Group IDU Dongying 1, SHENG Dongbei 1, HUO Huanyan 1, DUAN Jialei 1, WANG Mengyue 1, TAN Jingming 2,CHEN Yuming 2, HU Penghui 2, LIU Wujie 1, TIAN Kegong 1(1. National Research Center for Veterinary Medicine, Luoyang 471000, China; 2. Bureau of Changsha Administration and ComprehensiveLaw Enforcement in Agricultural, Changsha 410205, China)收稿日期:2022-01-13基金项目:郑洛新自创区创新引领型产业集群专项(201200211200);云南省田克恭专家工作站(2019IC062)作者简介:杜东颖,女,兽医师,硕士,主要从事禽病毒病疫苗研究;盛东北,男,兽医师,本科,主要从事禽病毒病疫苗研究通信作者:刘武杰,E-mail:***************;田克恭,E-mail:**************I 群禽腺病毒(4型)Fiber-2蛋白亚单位疫苗免疫效果研究杜东颖1,盛东北1,霍环艳1,段佳蕾1,王孟月1,谭镜明2,陈宇明2,胡鹏辉2,刘武杰1,田克恭1(1.国家兽用药品工程技术研究中心,洛阳471000;2.长沙市农业综合行政执法局,长沙 410205)2022,30(6):77-82Abstract: To evaluate the immunogenicity of a subunit vaccine prepared with the recombinant Fiber-2 protein, the Fiber-2 gene of the FA V-HN strain was cloned into the pET-30a vector and recombinant pET-30a-Fiber-2 plasmid was constructed and transformed into BL21 for protein expression. After purifi cation of Fiber-2 protein, subunit vaccines with different antigen doses were prepared for immunization of SPF chickens. The results showed that the recombinant Fiber-2 protein with a purity of about 90% was obtained and the AGP titer was 1: 64. When the AGP titer of the subunit vaccine antigen content was not less than 1:2, all immunized 10 SPF chickens produced antibodies at 21 days post immunization and resisted the challenge of the virulent strain of avian adenovirus type 4 (type 4).Key words: Avian adenovirus; Fiber-2 protein; subunit vaccine; protection· 78 ·中国动物传染病学报2022年12月鸡肝炎-心包积液综合征(h e p a t i t i s-hydropericardium syndrome, HHS)是由血清4型禽腺病毒(Flow adenovirus serotype 4, FAdV-4)引起的高致病性传染病[1],该病首次在巴基斯坦的安卡拉地区发生,随后陆续在美国、印度、韩国等地区流行[2-5],HHS可感染不同品种的鸡,临床剖检特征性病变主要包括心包积液,肝脏肿大、颜色变浅等[6-8]。
跨省调运种禽产地检疫规程 - 中华人民共和国农业部

跨省调运种禽产地检疫规程1.适用范围本规程适用于中华人民共和国境内跨省(区、市)调运种鸡、种鸭、种鹅及种蛋的产地检疫。
2.检疫合格标准2.1符合农业部《家禽产地检疫规程》要求。
2.2符合农业部规定的种用动物健康标准。
2.3提供本规程规定动物疫病的实验室检测报告,检测结果合格。
2.4种蛋的收集、消毒记录完整,其供体动物符合本规程规定的标准。
2.5种用雏禽临床检查健康,孵化记录完整。
3.检疫程序3.1申报受理动物卫生监督机构接到检疫申报后,确认《跨省引进乳用种用动物检疫审批表》有效,并根据当地相关动物疫情情况,决定是否予以受理。
受理的,应当及时派官方兽医到场实施检疫;不予受理的,应说明理由。
3.2查验资料3.2.1查验饲养场《种畜禽生产经营许可证》和《动物防疫条件合格证》。
3.2.2按《家禽产地检疫规程》要求查验养殖档案。
13.2.3调运种蛋的,还应查验其采集、消毒等记录,确认对应供体及8其健康状况。
3.3 临床检查按照《家禽产地检疫规程》要求开展临床检查外,还需做下列疫病检查。
3.3.1发现跛行、站立姿势改变、跗关节上方腱囊双侧肿大、难以屈曲等症状的,怀疑感染鸡病毒性关节炎。
3.3.2发现消瘦、头部苍白、腹部增大、产蛋下降等症状的,怀疑感染禽白血病。
3.3.3发现精神沉郁、反应迟钝、站立不稳、双腿缩于腹下或向外叉开、头颈震颤、共济失调或完全瘫痪等症状,怀疑感染禽脑脊髓炎。
3.3.4 发现生长受阻、瘦弱、羽毛发育不良等症状的,怀疑感染禽网状内皮组织增殖症。
3.4实验室检测3.4.1实验室检测须由省级动物卫生监督机构指定的具有资质的实验室承担,并出具检测报告 (实验室检测具体要求见附表)。
3.4.2实验室检测疫病种类3.4.2.1种鸡高致病性禽流感、新城疫、禽白血病、禽网状内皮组织增殖症。
3.4.2.2种鸭高致病性禽流感、鸭瘟。
3.4.2.3种鹅高致病性禽流感、小鹅瘟。
4.检疫后处理4.1参照《家禽产地检疫规程》做好检疫结果处理。
野生动物禽流感标准以及监测方法

野生动物禽流感标准以及监测方法
野生动物禽流感是一种由禽流感病毒感染引起的传染病,
对野生动物和家禽都具有较高的致病性。
为了及时监测和控制野生动物禽流感的传播,制定相关的标准和监测方法是非常重要的。
一、野生动物禽流感标准
1. 病原学检测标准:采用酶联免疫吸附试验(ELISA)、
聚合酶链式反应(PCR)等方法,检测野生动物体内是否含有禽流感病毒的核酸或抗体。
2. 病理学诊断标准:通过野生动物的组织病理学检查,观
察是否存在禽流感病毒引起的病变,如肺部炎症、充血、出血等。
3. 流行病学调查标准:采集野生动物和其周围环境的样本,并结合病毒遗传学分析,确定野生动物禽流感的传播途径和传播范围。
二、野生动物禽流感监测方法
1. 采集样本:野生动物监测主要采集野生动物的血液、粪便、鼻腔和咽喉等样本,通过核酸提取和孵化等技术,检测样本中是否含有禽流感病毒。
2. 感染病毒检测:常用的检测方法包括ELISA、PCR和序
列比对等技术,通过检测野生动物样本中的禽流感病毒核酸或禽流感病毒特异性抗体,确诊野生动物是否感染禽流感病毒。
3. 病理学检查:对于有禽流感病变症状的野生动物,进行
病理学检查,观察组织病变情况和禽流感病毒的存在与否。
4. 流行病学调查:结合监测样本的采集地点、时间和野生动物的传播行为等信息,进行流行病学调查,追溯病毒的来源和传播链路。
以上是关于野生动物禽流感标准以及监测方法的描述。
准确的标准和监测方法可以帮助科研人员和防控部门及时了解野生动物禽流感的流行状况,在有效控制疫情扩散和保护野生动物和家禽健康方面起到重要作用。
禽支原体病诊断技术标准

禽支原体病诊断技术标准一、前言禽支原体病是一种由禽支原体引起的传染性疾病,主要感染家禽,尤其是鸡。
禽支原体病的早期症状往往不明显,在疾病发展到一定程度后,才会出现典型的症状,因此准确的诊断技术对于预防和控制疾病的传播至关重要。
为此,制定禽支原体病诊断技术标准,对于提高禽支原体病的诊断准确性和及时性具有重要意义。
二、标本采集与处理1. 采样对象:疑似感染禽类动物,包括鸡、鸭、鹅等。
2. 采样部位:疑似受感染的鸟类,可选择鼻拭子、咽拭子、肛拭子、粪便、血清等作为样本。
3. 采样方法:采用无菌拭子或器具采集样本,避免受到外界污染。
三、实验室诊断技术1. 细菌培养:将采集的样本接种在适宜的培养基上进行培养,并对培养物进行形态、生化等鉴定。
2. PCR技术:使用PCR技术检测禽支原体DNA,以确定感染情况。
3. 免疫学检测:包括ELISA、免疫印迹等检测方法,用于检测禽支原体的抗体水平。
四、诊断标准1. 细菌学诊断:通过细菌培养和鉴定,确定禽支原体是否存在。
2. 分子生物学诊断:检测样本中的禽支原体DNA,确认感染情况。
3. 免疫学诊断:通过检测血清中的禽支原体抗体水平,确定感染情况。
五、诊断流程1. 标本采集:按照标准采集相应样本。
2. 实验室处理:进行样本的处理、提取、培养等操作。
3. 实验室诊断:进行细菌学、分子生物学和免疫学诊断。
4. 结果判读:根据诊断结果进行病情判读和报告。
六、质量控制1. 实验室操作:严格按照规范操作程序进行实验室诊断。
2. 对照组:使用阳性和阴性对照样本进行质量控制。
3. 实验室设备:保证所有实验室设备的正常运行和定期维护,确保诊断准确性。
七、报告和记录1. 报告标准:诊断报告应包括标本信息、实验室诊断结果和诊断结论等内容。
2. 记录保存:诊断报告和实验记录等应妥善保存,作为后续参考和追溯的依据。
八、结语禽支原体病的快速、准确诊断是预防和控制疾病传播的关键。
通过制订禽支原体病诊断技术标准,提高诊断技术水平,对于确保养禽业的健康发展和公共卫生安全具有极其重要的意义。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
DB42/T—2020 4型禽腺病毒抗体ELISA检测规程
1范围
本文件规定了4型禽腺病毒抗体ELISA检测的术语和定义、实验原理、检测条件、检测方法、结果判定、废弃物处理和防止污染的措施。
本文件适用于4型禽腺病毒鸡血清抗体的检测。
2规范性引用文件
下列文件对于本文件的应用是必不可少的。
凡是注日期的引用文件,仅所注日期的版本适用于本文件。
凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
GB/T6682-2008分析实验室用水规格和试验方法。
3术语和定义
本文件没有需要界定的术语和定义。
4实验原理
本文件采用酶联免疫吸附法(ELISA),该方法利用抗原抗体反应具有特异性,将特异性的4型禽腺病毒五邻体蛋白(penton)吸附到固相载体的表面后,待测物中若含有相应的4型禽腺病毒抗体,则可与所包被的五邻体蛋白(penton)相结合,并能继续和相应的辣根过氧化物酶标记的鸡IgG抗体结合形成复合物。
加入酶反应的底物后,底物被酶催化成为有色产物,产物的量与待测物中4型禽腺病毒抗体的量直接相关,故可根据呈色的深浅进行定性或定量分析。
由于酶的催化效率很高,间接地放大了免疫反应的结果,使测定方法达到很高的敏感度。
5检测条件
5.1试剂及耗材
5.1.1试剂
纯化的4型禽腺病毒五邻体蛋白(penton)、酶标记物(辣根过氧化物酶标记的鸡IgG抗体)、底物液显色液、终止液、阳性对照、阴性对照、样品稀释液、20倍浓缩洗涤液、包被液、封闭液。
试剂配方及4型禽腺病毒五邻体蛋白、阳性对照、阴性对照的制备见附录A。
5.1.2耗材
酶标板(96孔)。
5.2设备
1
DB42/T—2020
2酶标检测仪(配备450nm滤光片)、单道移液器(10μL)、8道移液器(300μL)、微量振荡器、恒
温箱(37℃)。
6检测方法
6.1抗原包被板的制备
6.1.1包被
将纯化的4型禽腺病毒五邻体蛋白(penton)用包被液稀释到0.625ng/μL,加入酶标板中,每孔加100μL,2℃~8℃包被12-15h。
6.1.2封闭
弃去包被液,每孔加入封闭液200μL,置37℃恒温箱中温育2h;弃去孔中液体,再置37℃恒温箱中干燥2h,密封2℃~8℃保存。
6.2洗涤液的配制
使用前,将20倍浓缩洗涤液恢复至室温22℃~25℃,并摇动使沉淀溶解,按照50mL20倍浓缩洗涤液加入950mL去离子水的比例稀释,稀释好的洗涤液在2℃~8℃保存,有效期为7日。
6.3待检血清的稀释
将5μL血清加入到95μL样品稀释液中,微量振荡器混匀,再取5μL混匀后的血清加入到120μL样品稀释液中,微量振荡器混匀备用。
6.4检测步骤
6.4.1待检样品温育
从冷藏环境中取出包被板,平衡至室温22℃~25℃后打开使用。
先用洗涤液洗涤抗原包被板1次,弃去孔中洗涤液,将稀释好的待检血清、阴性对照和阳性对照各取100μL,加至抗原包被板中,阴、阳性对照各设2孔,置37℃恒温箱中温育45min。
阴性对照血清和阳性对照血清无需稀释。
6.4.2洗涤
弃去孔中液体,每孔加入洗涤液300μL/孔,重复洗涤4次,最后一次拍干。
6.4.3酶标记物的温育
将辣根过氧化物酶标记的鸡IgG抗体用封闭液作1:20000倍稀释,每孔加入100μL,置37℃恒温箱中温育45min。
6.4.4洗涤
重复步骤5.4.2。
6.4.5底物显色
每个反应孔加入底物显色液100μL,置22℃~28℃下避光显色15min。
DB42/T —2020
36.4.6终止
每孔加终止液50μL,10min内用酶标仪在波长450nm处测定各孔的OD值结果。
7
结果判定7.1试验成立条件
两个阳性对照孔的OD 450nm 值均>1.0,且相差<0.2;阴性对照孔OD 450nm 值均<0.3时试验成立。
7.2结果计算Cut-off值按式(1)确定:
N P N S CO off Cut --=
-)值( (1)
式中:
CO ——阴阳性判定临界值;
S ——样品测定孔OD 450nm 值;
P ——阳性对照孔平均OD 450nm 值;
N ——阴性对照孔平均OD 450nm 值。
7.3结果判定CO>0.15判定为阳性;CO≤0.15判定为阴性。
8废弃物处理和防止污染的措施
实验过程中注意做好个人的安全防护工作,废弃物应做好无害化处理。
