消毒剂细菌检测操作流程图
医院感染相关流程图

医疗废物分类、收集、回收、处理流程医院感染散发病例监测流程医院感染暴发病例监测流程医院感染漏报病例监测流程无菌手术切口甲级愈合率和感染率监测流程抗菌药物使用监测流程导管相关性血流感染监测流程外科手术部位感染监测流程门(急)诊预检分诊服务流程空气监测流程注:重点科室需做空气培养,其他科室只有当发现考虑有因空气质量问题引起医院感染时,才做空气培养。
物体表面污染监测流程医务人员手监测流程采样:被检人员五指并拢注:各类环境医务人员手细菌菌落总数卫生标准环境类别医务人员手(cfu/cm2)Ⅰ≤5Ⅱ≤5Ⅲ≤10Ⅳ≤15血液透析水和透析液染菌量监测流程紫外线辐射强度监测流程使用中消毒剂的监测流程压力蒸汽灭菌效果监测流程(参照《中华人民共和国国家标准》GB15981-1995)下排气式压力蒸汽灭菌器或预真空压力灭菌器内镜消毒效果监测流程采样:用无菌注射器抽取10ml缓冲液,采内镜的内腔面注:采样时必须注意无菌操作及手卫生。
特殊感染手术的应急预案1.手术科室应于术前1天或术前提前通知手术室做准备2.在手术通知单电脑开单的备注栏内注明传染病的名称 评估 (1)为何种特殊感染 (2)感染部位、程度(3)手术方式、预计手术历时 (4)术中所需手术用物和器械 (5)所需护士人数用物准备 手术用物、手术器械、感染手术警示牌 1.安排在专用手术间实施手术2.病人入室前将室内暂时可能不用的物品全部移出该室3.病人入室前巡回和器械护士将所有手术所需用物全部放入该手术间4.巡回在手术间门外悬挂“感染手术,谢绝参观“的警示牌5.接触病人血液和体液时需戴双层手套术后器械密闭运送至供应室统一洗消 锐利器械直接投入锐器盒中器械车、手术推车 用0.1%的含氯消毒剂擦洗,再用清污染的被服及手术布类 均放入有标记的袋中封口。
在其手术间地面和墙壁用0.1%的含氯消毒剂擦拭,再用清水擦手术间净化3小时医疗废物处理流程医院感染知识培训流程外来器械管理流程一次性无菌用品管理流程使用科室将医疗用品申请表(需科室负责人签字)交医学工程科→通知中标公司送货→医学工程科进行清点、验收(包括:产品名称、规格、生产厂商、供货单位、生产批号、灭菌批号、注册证号、有效期、数量、接收人)→送往供应室、手术室医务人员职业暴露应急预案、应急处理、报告流程。
细菌内毒素检查SOP(动态浊度法)

细菌内毒素检查SOP(动态浊度法)1.目的为规范细菌内毒素含量测定的操作,特制定本SOP。
2.范围本SOP适用于细菌内毒素含量测定的操作。
3.定义3.1.动态浊度法是检测反应混合物的浊度到达某一预先设定的吸光度所需要的反应时间,或是检测浊度增加速度的方法。
3.2.细菌内毒素国家标准品系自大肠埃希菌提取精制而成,用于标定、复核、仲裁鲎试剂灵敏度和标定细菌内毒素工作标准品的效价。
3.3.细菌内毒素工作标准品系以细菌内毒素国家标准品为基准标定其效价,用于试验中的鲎试剂灵敏度复核、干扰试验及各种阳性对照。
3.4.细菌内毒素检查用水系指内毒素含量小于0.015 EU/ml(用于凝胶法)或0.005 EU/ml (用于光度测定法)且对内毒素试验无干扰作用的灭菌注射用水。
4.职责4.1.QC负责本规程的起草、修订、培训及执行。
4.2.QA、QC组长、质量管理部经理负责本规程的审核。
4.3.质量负责人/质量受权人负责本规程的批准。
4.4.QA负责本规程执行的监督。
5.引用标准《中华人民共和国药典》2020年版三部。
6.材料6.1.仪器设备细菌内毒素测定仪、漩涡混合器、干烤箱6.2.试剂及溶液6.2.1.鲎试剂6.2.2.细菌内毒素工作标准品:国家标准品或经过国家标准品标定的工作标准品。
6.2.3.细菌内毒素检查用水:内毒素含量应小于0.005EU/ml。
6.3.使用的器具移液器、无热原稀释管和反应管、无热原枪头。
7.流程图无8.程序8.1.原理细菌内毒素能激活鲎试剂(TAL)中的酶系统,使凝固酶原变成凝固酶,进而凝固酶再激活其中的凝固蛋白原变成凝固蛋白,呈现凝胶反应,动态浊度法是检测反应混合物的浊度到达某一预先设定的吸光度所需要的反应时间,计算内毒素浓度与反应时间关系的双对数标准曲线,利用标准曲线对供试品的内毒素含量进行定量测定。
8.2.试验前准备8.2.1.采样管用硅胶塞塞口,经180℃干烤2小时,除内毒素备用。
沙门氏菌检验详细流程图

1 mL+SC10 mL 36 ℃±1 ℃,18 h~24 h
BS
XLD(或HE、科玛嘉显色培养基)
36 ℃±1 ℃,40 h~48 h
36 ℃±1 ℃,18 h~24 h
挑取可疑菌落
TSI,赖氨酸,NA, 靛基质, 尿素 (pH 7.2), KCN
商 品 化 生 化 H2S+靛基质- 尿素- H2S+靛基质+ 尿 H2S-靛基质-尿素 反应结果与左
为了最大可能的检出沙门氏菌,原则上必须使用 两种以上选择性分离培养基。
进口-SS 进口-SS 国产-SS 进口-HE 国产-HE 进口-XLD 国产-XLD 进口-BS 国产-BS CHRO显色 国产-DHL 国产-WS TSA(对照)
65.3 81.0 52.0 83.2 80.0 83.0 86.2 106.6 77.7 68.4 98.4 71.6 100.0
初筛微生 物
沙门氏菌
柠檬酸杆 菌属
变形杆菌
菌落颜色
紫色(直径约 1mm)
蓝色(直径约 1mm)
无色或被抑 制
特异性 灵敏度
89% 100%
---
---
(铜绿假单胞菌也呈紫红色, 可以通过前增菌排除。所以推 荐在检测中的前增菌用TTB。 粉红色、深红色、干燥菌落、 边缘锯齿状等 均非沙门氏菌菌 落。)
被分成2500多个血清型。
Vi抗原 O抗原 H抗原
沙门氏菌命名与书写方式
目前的命名方法规定:
肠道沙门菌肠道亚种(亚种Ⅰ)给予专用名,并采用 标本分离地址的地名。菌名的第一个字母需大写,且 亚种Ⅰ的所用菌名不能用斜体。例如:肠道沙门菌鼠 伤寒血清型应书写为Salmonella enterica subsp.enterica serotype Typhimurium,但在实际工作中,可简写为S. Typhimurium。
细菌鉴定程序流程图
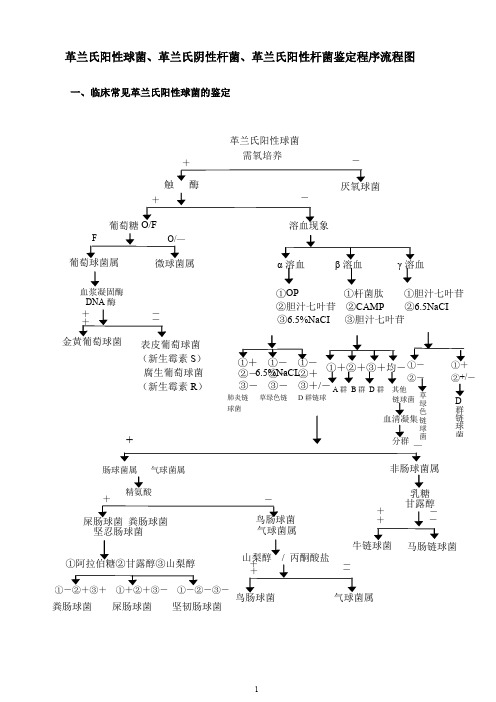
革兰氏阳性球菌、革兰氏阴性杆菌、革兰氏阳性杆菌鉴定程序流程图一、临床常见革兰氏阳性球菌的鉴定6.5%NaCL触葡萄糖分群②- ②+/- 草 绿色链球 菌D 群 链 球 菌血浆凝固酶DNA 酶肠球菌属 气球菌属 精氨酸+-革兰氏阳性球菌 需氧培养 溶血溶血溶血 ①OP ①杆菌肽 ①胆汁七叶苷 ②胆汁七叶苷 ②CAMP ②6.5NaCI ③6.5%NaCI ③胆汁七叶苷②- ②- ②+ ③- ③- ③+/- ①+②+③+均-A 群 B 群 D 群 其他 链球菌肺炎链 草绿色链 D 群链球 球菌气球菌属山梨醇坚忍肠球菌①阿拉伯糖②甘露醇③山梨醇粪肠球菌 屎肠球菌 坚韧肠球菌 表皮葡萄球菌 (新生霉素S ) 腐生葡萄球菌 (新生霉素R )+非肠球菌属乳糖 甘露醇马肠链球菌二、临床常见革兰氏阴性杆菌鉴定见图观察平板上菌落特征(特殊形态、漫延生长、拉丝、溶血、荧光、色素等)②— 革兰氏阴性杆菌 氧化酶(—) KIA 葡萄糖O/FO/-) 肠杆菌科 动力①苯丙氨酸②VP 试验②- ②-②麦芽糖迅速分解 ③甘露醇④DNA 酶 (G-球杆菌) (25%氧化酶+)②+ ②- ③- ③+④+ ④- 嗜麦芽窄 食单胞菌 洋葱伯克 霍尔德氏菌(93%氧化酶阳性)埃希菌属 变形杆属菌 克雷伯氏菌属志贺氏菌属 (漫延生长) (动力-)沙门氏菌属 普罗威登氏菌属 沙雷氏菌属枸橼酸杆菌属 摩根摩根氏菌 (DNA 酶+) 迟缓爱德华菌 (吲哚+,尿素+, 哈夫尼亚菌属耶尔森氏菌属 糖醇反应差) (蜂房哈夫尼亚)(G-短小杆菌 肠杆菌属37℃动力(—)25℃动力(+)尿素(+)4℃生长 糖醇分解/黄色素阴沟肠杆菌聚团多源菌 产气肠杆菌 板畸肠杆菌革兰氏阴性杆菌氧化酶(+) KIA 葡萄糖O/FO/-) 弧菌科动力①嗜盐试验 ②肌醇 ③O/129敏感试验④TCBS 生长 (端鞭毛)(菌落产生 亮黄色色素)莫拉氏菌 (G-球杆菌,SS 不生长, 菌落细小, 不分解任何糖类)①- ①- ①+/- ②- ②+ ②- ④- ④- ④+③R ③S/R ③S 气单胞菌属 邻单胞菌属 弧菌属 (76%有β溶血) (无β溶血)(周鞭毛, 蛋白胨肉汤 中PH8.6以上不分解任何糖 类)三、临床常见革兰氏阳性杆菌鉴定革兰氏阳性杆菌 抗酸染色(18℃--20℃有动力,倒伞形,狭窄溶血环,H 202+)李斯特氏菌+ - +/-++ - 普通血平板生长芽胞杆菌梭状 奴卡氏菌 (血平板呈粉末状 生长,菌落不易挑 起,有菌丝)(G+着色不匀,有异染 颗粒,毒力试验阳性, 结合临床症状考虑 是否为白喉棒状杆菌)红斑丹毒丝菌 (G 染色易脱色,H 2S+ 感染特征)丙酸杆菌棒状杆菌红斑丹毒丝菌糖分解/触酶。
消毒产品检验技术规范

消毒产品检验技术规范Technical Standard for Testing Disinfection Products 1 消毒产品消毒效果检验技术规范1.1 消毒剂杀微生物试验1.1.1 适用范围主要适用于消毒剂鉴定和日常检测,用来评价各种用途的消毒剂对微生物的杀灭效果。
按此方法进行的试验,只是对消毒剂的杀菌能力的重要方面进行验证,侧重反映消毒剂的实用剂量与杀菌能力。
不能反映消毒剂的全面特性。
1.1.2 菌悬液与菌片的制备1.1.3 活菌培养计数技术1.1.4 残留消毒剂的去除方法1.1.5 中和剂鉴定试验1.1.6 物理法去除残留消毒剂试验1.1.7 细菌定量杀灭试验1.1.8 杀灭分枝杆菌试验1.1.9 真菌杀灭试验1.1.10 病毒灭活试验1.1.11 能量试验1.1.12 各种因素对消毒剂杀菌作用影响的测定1.2 消毒剂模拟现场和现场消毒鉴定试验1.2.1 消毒剂对食(饮)具消毒效果的模拟现场鉴定试验1.2.2 消毒剂对医疗器械的消毒模拟现场试验1.2.3消毒剂对医疗器械的模拟现场灭菌试验1.2.4 连续使用稳定性试验1.2.5消毒剂对手消毒的模拟现场试验1.2.6消毒剂对手消毒现场试验1.2.7 消毒剂对皮肤消毒的模拟现场试验1.2.8消毒剂对皮肤消毒现场试验1.2.9消毒剂对其他表面消毒模拟现场鉴定试验1.2.10消毒剂对其他表面消毒现场鉴定试验1.3 空气消毒效果鉴定试验1.3.1 目的检测消毒器械或消毒剂对空气中细菌的杀灭和清除作用,以验证其对空气的消毒效果。
其他方法对空气的消毒效果,亦可参照本试验的有关原则进行。
1.3.2 试验设备和器材1.3.3 试验阶段1.3.4 实验室试验与模拟现场试验操作程序1.3.5 现场试验1.4 水的消毒效果鉴定试验1.4.1生活饮用水消毒效果鉴定1.4.1.1 目的检测生活饮用水消毒剂与消毒器械的杀菌效果,以验证其对生活饮用水消毒能否达到卫生合格标准。
供应室工作流程图07911

供应室工作流程图07911芦圩镇卫生院供应室工作流程管理随着医学科学的迅速发展与医疗质量的不断提高~医院对医院内感染的管理工作更加重视~作为直接关系医院内感染与医疗、护理质量效果的供应室的地位更显其重要性。
供应室工作是医院整体工作的重要组成部分~它担负着为全院提供充足、完好、规格齐全、品质保障的消毒无菌物品的任务~而且与医院各临床一线科室的关系密切~所提供物品质量的好坏直接与医院内感染管理息息相关。
所以供应室质量管理是直接影响临床一线医疗质量与患者安危的一个重要环节。
在供应室制定了各类工作流程图~使工作人员有章可循~可以减少或杜绝了护理缺陷的发生。
工作流程图的制定根据供应工作的性质及特点~组织科室全体护士进行认真讨论~将工作程序以工作流程图的方式分挂在各个工作区域~分为以下几类。
1、护理质量管理流程图护理部?供应室护士长?各小组护理组长?各小组责任护士。
护理质控流程图。
护理部质控组?供应室护士长?质控组组长?质控组成员。
护理质控检查工作安排工作流程图。
护理部、护士长每月检查科室质量?质控组组长每星期检查各小组工作情况?各小组成员每日检查当天的工作情况?提出意见~制定改进措施? 总结分析?改进工作?效果评价。
2、工作环节流程图:包括回收流程、洗涤流程、包装流程、灭菌流程、发放流程、下收下送流程~器械包装流程等。
1、回收流程图:工作人员按防护要求戴帽子、戴口罩、穿手套~每天用专用污物车?科室?清点器械分类放置于防刺的容器?核对、登记?送入洗涤间分类浸泡清洗?下收车用含氯消毒剂抹洗~轮子用含氯消毒剂喷,2、洗涤流程图:分类?清水冲洗?消毒剂浸泡?清水冲洗?酶的浸泡?刷洗?精洗,3、包装流程图:器械干燥?检查器械完好性?上油?配套?核对?放化学指示卡?打包?标识灭菌日期、标识有效期?标识洗涤班、包装班、消毒班人员姓氏,4、灭菌流程图:常规检查灭菌炉?分类?装炉?放监测指示卡带?关炉?预热?灭菌?干燥?出炉?无菌间分类存放,5、发放流程图:按要求更衣、洗手、换鞋?无菌室?根据器械交换表准备用物?传递窗?发放间?无菌车?科室等。
淋球菌临床菌株的收集流程图

淋球菌临床菌株的收集流程图淋球菌临床菌株的收集SOP1、标本的采集、接收与处理1.1标本采集的基本要求1.1.1应使用正规的检查方法和试剂,取材方法要简便,不需要使用特殊的仪器。
1.1.2取标本以不损伤病人为好,尽量使用非侵入性采集方法。
1.1.3所用的器材对病原体的活力无影响或影响很小。
1.1.4操作应规范化。
如取材后需要做细菌培养,应尽快接种。
1.1.5应由医务人员亲自采集标本,一般不应由病人自取。
1.1.6所有标本都应当被视为具有传染性,医务人员应戴手套谨慎操作。
1.2淋球菌培养的标本取材1.2.1男性患者:将男性采样拭子深入到尿道内2—4cm处,轻轻转动并停留10—15秒钟后取出,取出的分泌物带有黏膜细胞。
1.2.2女性患者:从女性患者的宫颈取材时,应先用温水湿润扩阴器(不可用液体石蜡等润滑油),然后将女性采样拭子插入宫颈管1-1.5cm处,轻轻转动并停留20—30秒取出。
为了提高阳性率,可同时取两份标本进行培养。
1.3标本接收的标准1.3.1标本登记:登记内容详见淋球菌菌株来源登记表。
1.3.2 对不合要求的标本,可以拒绝接收。
2、淋球菌的实验室检测2.1分泌物涂片显微镜检查2.1.1原理淋病感染者的泌尿生殖道常见有黄色脓性分泌物,取分泌物作涂片,经过革兰染色后,在显微镜下可见在多形核白细胞内或周围紧相连处有红色的呈双肾形排列的双球菌。
2.1.2方法1)涂片:将拭子在载玻片上轻轻滚动涂片。
2)固定:待涂片在室温中自然干燥,涂片经火焰固定。
3)革兰染色:(BASO珠海贝索快速革兰氏染色液)①第一液(龙胆紫液):染10秒,水洗甩干。
②第二液(碘溶液):染10秒,水洗甩干。
③第三液(脱色液):脱色10-20秒,水洗甩干。
④第四液(沙黄溶液):复染10秒,水洗甩干。
4)镜检:晾干后的载玻片滴加香柏油,先在低倍镜下找到视野后转换到油镜观察结果。
2.1.3结果2.3.1.1结果判读:淋球菌为革兰氏阴性菌,经革兰染色后呈红色,肾形,常呈双排列,两菌接触面扁平或稍凹。
传染病消毒效果检查

【tips】本文由王教授精心编辑整理,学知识,要抓紧!
传染病消毒效果检查
目前检测多仍采用一此条件致病菌为间接指标。
肠道传染病以大肠杆菌为指标,呼吸道传染病以溶血性链球菌为指标。
肝炎病毒近年表面抗原,DNA聚合酶以及电镜观察,甲肝病毒分离等为指标。
如消毒前后均未检出大肠杆菌或溶血性链球菌,则可以消毒后自然菌总数率低的百分率评价,消毒后自然菌总数下降80%以上为效果良好,降低70%为较好。
减少60%以上为一般,减少60%以下为不合格。
具体检查方法:
1.物品表面检查
在消毒物品相邻部位划出2个10cm2范围,消毒前后别以无菌棉签采样,接种后培养24~48小时观察结果。
2.排泄物检查
消毒前后各取0.2ml排泄物的稀释液接种肉汤管,37℃培养24小时后再取样转种相应的培养基,24~48小时后观察结果。
3.空气消毒效果检查
一般用自然沉降法。
医学`教育网搜集整理消毒前后在消毒的空间不同平面和位置。
放置4~5个平面,暴露5~30分钟后盖好,培育24~48小时观察结果。
图解手术室标准工作流程

洗手护士工作流程图巡回护士工作流程图留置针穿刺操作流程图外科手消毒操作流程图穿无菌衣、戴无菌手套操作流程图手术器械清点流程图手术中取血、输血流程图腹腔镜操作流程图高频电刀操作流程图手术室医疗回收处理流程图内镜器械清洗流程图内镜器械包装流程图过氧化氢等离子体低温灭菌器操作流程图手术中缺失物品查找流程1、洗手护士、巡回护士2次核对后确认发生手术物品缺失事件。
2、通知手术医生、麻醉师暂停手术。
3、根据缺失物品类别及发现缺失时段,估计物品可能遗留的区域,分区域查找,洗手护士查找无菌区,手术医生探查切口,巡回护士查找手术间。
4、未及时发现则报告护士长,由其主持全方位查找。
(1)查找手术间内敷料单褶皱内、地面、垃圾桶、料料筐、标本袋、吸引器瓶。
(2)查找与手术间相通的辅助间、刷手间、器械间、准备间,外走廊(3)如缝针等金属器械,可显影敷料缺失寻查:①电话通知放射进行照X片。
②X线结果显示若在切口内,手术医生探查取出;未在切口内,关闭切口,在其它区域继续查找。
(5)手术医生探查、体腔。
(6)与曾进入手术室的相关手术的员、麻醉师沟通,是否取用或将其带出手术间。
5、巡回护士在手术护理记录单上书写事件发生经过及物品未在切口骨的证实结果,由手术医生签字。
6、发现但查找超过30分钟或最终未发现缺失物品的,填写工作缺陷报告单,详细记录事件发生、查找的过程、时间、结果等作为后期责任认定依据。
7、手术室统一保存工作缺陷报告单。
手术中缺失物品查找流程图手术护理不良事件报告及处理流程1判断手术护理不良事件:手术病人识别错误、手术部位错误、手术病人跌倒、用药错误、输血及输液意外、手术病人约束意外、意外针刺伤、管道意外脱落、药物不良反应、其他需要报告的意外事例。
2发生手术护理不良事件后,当事人应第一时间报告护士长;护士长了解情况后立即报告护理部主任,严重不良事件由护理部主任报告相关主管部门,如分管护理院长、医务科。
3妥善保管不良事件的各种记录、检验报告,对造成不良事件的药物、储血袋,输液瓶、器具等,医患双方共同封存并签字。
结核菌药物敏感性测定

结核菌药物敏感性测定标准化操作及质量保证手册国家结核病参比实验室2010年3月前言结核病细菌学检查是结核病控制规划重要的组成部分,随着现代结核病控制策略(DOTS)在我国的广泛实施,以及结核病控制三大目标的全面实现,结核病防治政策与技术策略有了很大的发展,在继续扩展高质量的DOTS的基础上,积极应对耐多药肺结核(MDR-TB)、结核菌/艾滋病病毒(TB/HIV)和其他挑战。
为满足当前结核病防治工作的需要,结核病实验室的工作任务也从之前的以痰涂片镜检发现传染性肺结核病人为重点,扩展到细菌学诊断、耐药结核病诊断等更加广泛的服务领域。
结核分枝杆菌药物敏感性测定(简称)是耐(多)药结核病防治中必不可少的重要工具,其主要作用是诊断耐药结核病、选择和调整耐药结核病治疗方案、开展耐药监测以了解某一地区结核分枝杆菌的耐药水平。
目前耐多药结核病规划性管理(PMDRTB)已在我国部分地区开展了试点,并将以较快的速度在全国扩展。
但在我国公共卫生领域,分枝杆菌药敏试验开展得并不普遍,大部分结核病防治机构的结核病实验室没有相应的经验和技术,缺乏系统的标准化文件,存在标准不一致、操作不规范、质量良莠不齐的问题。
为进一步规范药敏试验的操作,保证工作质量和试验人员安全,国家结核病参比实验室与世界卫生组织合作,编制了本册《结核分枝杆菌药物敏感性测定标准化操作手册》,详细描述结核菌药敏试验各个过程的操作程序。
目前世界卫生组织推荐的药敏试验方法包括比例法、绝对浓度法和液体培养法。
其中比例法为目前我国流行病学监测和耐多药结核病规划管理项目所采用的方法,将在本手册中重点介绍。
绝对浓度法是我国三十多年沿用的药敏试验方法,为目前我国大多数结核病专科医院常规使用的用于临床检测的方法,本手册也有独立章节进行描述,方法引自《中国防痨协会结核病诊断实验室检验规程》。
本手册参考世界卫生组织系列的结核病实验室标准化操作程序(SOP)的主要框架和内容,按照我国结核病规划的实际情况和具体要求进行了调整,并通过在部分省份的试点进一步进行了修改和完善,使之更具有可操作性,供开展药敏试验的实验室使用。
微生物检测

微生物试验检测设备仪器:酶标仪、显微镜、恒温培养箱、干燥箱、冰箱、冰柜、恒温水浴锅、离心机、离心沉淀器、微量振荡器、电子天平、生物天平、高压锅、超净工作台、煤气灶、煤气罐、移液器、酒精灯、手术剪、止血钳、镊子等。
实验检测项目:一、血清学1. 红细胞凝集试验(HA)和红细胞凝集抑制试验(HI)操做方法2.凝集反应⑴鸡白痢和鸡伤寒的诊断⑵鸡霉形体的诊断3.免疫扩散试验(AGP)操作方法⑴鸡传染性囊病的诊断⑵鸡淋巴白血病的诊断二、孵化厅的微生物学检测1.种蛋表面的细菌检测2.绒毛的细菌检测3.终止胚的细菌检测4.一日龄雏鸡的健康检测5.空气中细菌的检测6.设备表面细菌的检测7.水样的细菌的检测三、鸡舍的细菌检测1.空气中细菌的检测2.物体表面细菌的检测3.水样的细菌检测4.垫料的细菌检测5.饲料的细菌检测四、消毒剂及其使用效果的测定五、细菌对药物的敏感性试验检测流程一、血清学1. 红细胞凝集试验(HA)和红细胞凝集抑制试验(HI)操做方法1.1 红细胞凝集试验(HA)1.1.1 在“V”型微量反应板上进行。
每孔加入50微升(用微量进样器或将16号注射针头磨去斜尖,调整针头孔径使每滴恰好25微升)pH 7.2的0.01摩尔/升PBS液或生理盐水,向第1孔滴加新城疫抗原50微升,吸放3~5次混匀,然后从第一孔吸出50微升加入第二孔,以相同方法混匀,再从第二孔吸50微升加入第三孔,如此做倍比稀释至倒数第二孔,再从倒数第二孔吸出50微升弃去,最后一孔不加病毒(抗原)作为红细胞对照。
1.1.2 吸取0.5%鸡红细胞悬浮液,每孔滴加50微升,加毕后在微量振荡器上振荡15~30秒,使其混合均匀,静置室温下或37℃温箱中作用20~40分钟。
1.1.3 当对照孔红细胞全部沉入孔底中间,即可判定各孔的红细胞凝集情况。
以病毒最大的稀释度孔出现100%凝集现象者为这个病毒的凝集价,即一个血凝单位。
1.2 血凝抑制(HI)试验1.2.1 4单位抗原(病毒)的配制如上述血凝试验表中病毒的血凝价为第八孔(256,即1:256倍稀释),4个单位的病毒则除以4,即64倍(64)稀释即可。
细菌内毒素检查法干扰试验

4 预试验 4.1 目的
初步确定供试品的最大不干扰浓度(当限值 以 EU/mg 或 EU/U 表 示 ) 或 最 小 不 干 扰 稀 释 倍 数 (当限值以EU/ml表示),为正式干扰试验提供依 据。
优点:减少摸索过程、节省成本
4.2 操作方法 由于干扰试验检验的是在供试品存在的情况下
内毒素与鲎试剂的反应是否正常,与所用鲎试剂 的灵敏度无关,因此在干扰试验的预试验中原则 上可使用任一灵敏度的鲎试剂。但建议使用较低 灵敏度(0.5或0.25EU/ml)的鲎试剂,可尽量避 免供试品所含的内毒素对干扰试验造成的阳性影 响。
2020220博康wwwzjhycom24然后用样品西咪替丁氯化钠注射液的2倍稀释液稀释该混合液稀释倍数依次为24和8倍将这三支管混合均匀连同该混合液即可得到含内毒素分别为05euml025euml0125euml和006euml含样品西咪替丁氯化钠注射液浓度为2倍稀释液的标准内毒素对照溶液干扰试验系列
Es在0.5λ—2.0λ,且Et在0.5Es—2.0Es (包括
0.5Es和2.0Es),认为供试品在该浓度下无干扰作
用。
7.2 如所用鲎试剂灵敏度为0.25EU/ml,供试品为 XX注射液(稀释4倍)
WSE 对照名称
ES ET
0.5 0.25 0.125 0.06 NC 结果 ++ ++ ++ ++ ++ ++ -- -- - - 0.125 ++ ++ +- -- -- -- -- -- - - 0.42
毒素工作标准品用细菌内毒素检查用水1ml溶解,在 旋涡混合器上混合15分钟,然后制备成1.0EU/ml、 0.5EU/ml、0.25EU/ml、 0.125EU/ml、0.06EU/ml和 0.03EU/ml等6个浓度的内毒素标准溶液,每稀释一 步均应在旋涡混合器上混合30秒钟。
医院消毒供应室操作流程图
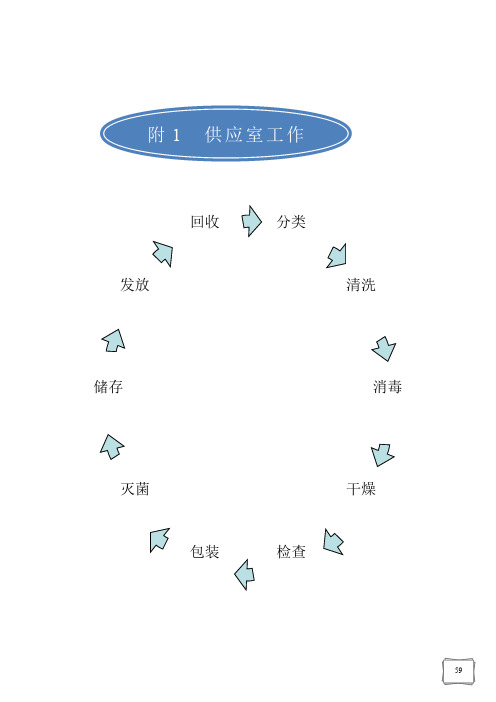
分类消毒干燥检查包装灭菌储存回收清洗发放附1供应室工作附2穿脱防护服流程穿法脱法穿胶鞋脱手套穿第一层手套穿衣结衣领带结好腰带穿第二层手套戴防护面罩进行清洗工作脱防护面罩洗手解开腰带脱防护衣脱胶鞋洗手附3氯消净消毒液使用指引穿好防护桶内加水至指示线(5L)500mg/L有效氯加氯消净1包(20g)1600mg/L有效氯或氯消净1包/水1.5L指示卡监测有效氯浓度浸泡30-45分钟或抹洗注意事项:1.按说明书使用,配制时注意做好个人防护安全。
2.应现配现用,放置于阴凉处。
3.每天使用前指示卡监测有效氯浓度。
4.物品上有大量有机物时应先冲洗后浸泡,减少拮抗作用。
附4器械清洗消毒操作流回收1.封闭包装2.特殊病原体感染器械器具应双层封闭包装并标明疾病名称单独回收处理。
清洗冲洗洗涤漂洗终末漂洗1.在流动水下冲洗。
2.管腔类高压水枪清洗。
3.打开器械轴节并拆开零件。
1.多酶液浸泡后刷洗或擦洗(鲁沃夫多酶清洗剂按1:270稀释,浸泡2-5分钟,室温水即可)。
2.管腔器械应注满多酶液浸泡。
3.超声清洗(时间宜3-5分钟)。
1.在流动水下冲洗或刷洗。
2.管腔器械用高压冲洗。
用软水、纯化水或蒸馏水消毒湿热消毒75%乙醇消毒化学消毒剂1.水温80℃,时间≥10分钟。
2.水温90℃,时间≥1分钟。
浸泡时间>10分钟500mg/L含氯消毒剂浸泡消毒、冲洗或按消毒技术规范及产品说明书要求执行。
干燥1.首先干燥设备进行干燥,金属15-20分钟,70-90℃;塑胶30-40分钟,65-75℃。
2.不耐热物品应使用消毒的低纤维絮布进行干燥处理。
3.管腔类器械应使用高压气枪或95%乙醇进行干燥。
4.禁止使用自然干燥法进行干燥。
检查保养1.目测或者使用带光源放大镜进行检查,检查不合格的应返回重新处理。
2.带电源的应进行绝缘性检查。
3.生锈的器械进行除锈处理(鲁沃夫除锈剂按1:7稀释,浸泡2-10分钟,水温50-80℃)、清洗。
4.使用水溶性润滑剂润滑(鲁沃夫润滑剂1:10稀释,浸泡1-2分钟,室温即可)。
巴氏杀菌工艺流程图

巴氏杀菌工艺流程图巴氏杀菌工艺是一种常用于食品加工的杀菌方法,可以有效杀灭细菌和其他微生物,保证食品的安全和长久保存。
以下是一份巴氏杀菌工艺的流程图,详情如下:巴氏杀菌工艺流程图:接收原料|↓↓↓清洗原料|↓↓↓切割原料|↓↓↓搅拌原料|↓↓↓加热原料|↓↓过热原料 |↓↓↓冷却原料 |↓↓↓过滤原料 |↓↓↓储存原料 |↓↓↓加热杀菌 |↓↓↓冷却杀菌品↓↓↓出口出库接收原料:原料从供应商处接收,检查原料的新鲜程度和品质。
清洗原料:使用水和消毒剂清洗原料,去除表面的污垢和细菌。
切割原料:将原料切割成适当的大小,以便更好地进行搅拌和加热。
搅拌原料:将切割好的原料放入搅拌机中,搅拌均匀。
加热原料:将搅拌好的原料放入加热罐中,通过高温加热杀菌。
过热原料:将加热后的原料放入过热罐中,提高温度和时间,确保彻底杀菌。
冷却原料:经过过热处理的原料通过冷却器进行快速降温,以避免过热后细菌重新生长。
过滤原料:通过过滤设备将原料中的杂质和细菌过滤掉,确保杀菌效果。
储存原料:杀菌后的原料经过包装,储存在冷库或储存室中,准备出库使用。
加热杀菌:将储存的原料放入加热罐中,通过高温加热杀菌。
冷却杀菌品:经过加热杀菌的产品通过冷却器进行快速降温,以保持产品的质量和口感。
出口出库:杀菌后的产品经过包装,准备出库销售。
以上就是巴氏杀菌工艺的简单流程图。
巴氏杀菌工艺是一种常用的食品加工杀菌方法,通过高温加热和冷却处理,可以杀灭细菌和其他微生物,确保食品的安全和长久保存。
同时,也能够保持食品的口感、质量和营养价值。
消毒剂消毒效果验证方案1

消毒剂消毒效果验证方案目录1.目的 (3)2.围 (3)3.职责 (3)3.1. 验证小组组成 (3)3.2. 职责 (3)4.消毒液的配制与使用 (4)4.1. 消毒液的配制 (4)4.2. 消毒液的使用 (4)5.验证容 (4)5.1. 采样部位 (4)5.2. 采样时间 (5)5.3. 取样、检验方法、标准的确定: (5)5.4. 消毒后验证消毒后有效期 (5)6.拟订再验证周期 (5)7.验证结果评定与结论 (5)8.附件 (6)9.培训 (6)消毒剂消毒效果验证方案1.目的验证公司消毒使用的0.1%新洁尔灭、0.2%的新洁尔灭、75%乙醇、3%~5%甲酚皂溶液消毒的效果是否达到要求及消毒后的有效期。
2.围本验证方案适用于车间使用的消毒剂消毒效果的验证。
3.职责3.1.验证小组组成验证小组成员3.2.职责3.2.1.验证小组1.负责起草验证方案。
2.负责本验证的协调工作,以保证本验证方案规定项目的顺利实施。
3.写出验证总结报告。
3.2.2.质量部1.负责审核验证方案。
2.负责取样及对样品的检验。
3.负责生产全过程的监控。
3.2.3.G2制剂车间(G2)1.负责验证方案制定和实施。
2.负责车间洁净区消毒操作。
3.负责收集各项验证记录,并对验证结果进行分析后,起草验证报告,报验证领导小组。
4.消毒液的配制与使用4.1.消毒液的配制4.1.1.75%的乙醇溶液:将95%乙醇与水按重量比为2.7:1混合,搅拌10-20次后,用量筒量取乙醇,用酒精比重计测试,如不在75%,则补加乙醇或水,直至符合所需的规格。
4.1.2.0.1%的新洁尔灭溶液:采购的新洁尔灭溶液一般为5%,配置时,取20ml的5%新洁尔灭溶液,配制成1kg ,搅拌10-20次,即得到0.1%新洁尔灭溶液,密闭保存。
如采购的新洁尔灭溶液的浓度有变化,则按照C浓·V浓=C稀·V 的公式进行计算配制4.1.3.0.2%的新洁尔灭溶液:采购的新洁尔灭溶液一般为5%,配置时,取40ml的5%新洁尔灭溶液,配制成1kg ,搅拌10-20次,即得到0.2%新洁尔灭溶液,密闭保存。
2024版沙门氏菌检验实验解析PPT

增加“无菌量筒:容量50mL、无菌均质杯、无菌均质袋、无菌广口瓶:容量500mL、无菌试管15mm×150mm、18mm×180mm、无菌接种环:10μL(直径约3mm)、1μL以及接种针”
对检验用器具规格明确,方便实验室选用
增加“生物安全柜”
对于实验室开展活菌操作、样本检测实验室生物安全等级需“BSL-2”,因此,增加此设备是生物安全必须。
明确接种菌液浓度为“0.5麦氏浊度”,接种量“2滴~3滴”,避免接种量过大导致假阳性;还有增加"接种混匀后滴加一层无菌液体石蜡进行密封"由于氰化钾不稳定容易分解失效,因此,加石蜡密封避免造成假阳性反应。
“符合表3中A1者,为沙门氏菌典型的生化反应”后面补充“进行血清学鉴定后报告结果”
明确的指出符合沙门氏菌典型的生化反应需要进行血清学鉴定后报告结果
调整可疑菌落初筛流程
流程图更清晰易懂
TTB选择性增菌改为:低背景菌36 ℃±1 ℃,高背景菌42 ℃±1 ℃原因:验证试验发现,对于生鲜样品,TTB 42℃比 TTB 36℃的选择性好,所以继续沿用;对于深加工样品,TTB 36℃比 TTB 42℃生长好,所以低背景菌采用36℃±1℃培养。如有需要,可将预增菌的培养物在2 ℃~8 ℃冰箱保存不超过72h,再进行选择性增菌。
2016版“必要时按表5进行沙门氏菌生化群的鉴定”修改为2024版中“必要时,按表5进行沙门氏菌种和亚种的生化鉴定”
“生化群”用“种和亚种”替代,更易懂;
在表5沙门氏菌种和亚种的生化鉴定中增加“肠炎沙门氏菌、邦戈尔沙门菌种名”以及肠炎沙门氏菌种内对应的6个亚种和生化群分型”;生化反应项增加“明胶酶、L(+)-酒石酸盐、半乳糖醛等8项”
主要变化
章节
新标准变更内容
临床检验科操作SOP

一、检验科检测项目标准操作规程(见附录)A 、临检室A1、血常规检验标准操作规程A2、尿常规标准操作规程B 、生化室B1、糖尿病检测(诊断酶联试剂盒)标准操作规程二、检验室工作流程图大小便体液 血液标本三、检验科各项规章制度(一)生物安全制度1、医务人员1)每1—2年做体检一次,并接受乙肝疫苗接种。
2)每1—2年检查乙肝病毒抗原抗体水平,发现乙型肝炎者应进行隔离治疗。
3)检验人员进入实验室应穿好工作服,不允许在实验室进食和吸烟。
4)检验人员在工作前后和被污染后,应用肥皂和流水清洗,必要时由消毒液浸泡双手,每季度抽查检验人员的手,并做细菌培养一次。
2、环境消毒隔离1)实验室应分为清洁区和操作区,清洁区要注意保护不受污染。
操作有气溶胶可能的标本应配置生物安全柜及其它防护设置,如紫外线灯,排气扇等操作区的工作台及地面每日用消毒液擦拭一次,有污染时随时消毒,每周大扫除一次。
2)采血室每日操作前用清水擦拭操作台一次,采血结束用消毒液擦拭操作台、桌子和地面一次,紫外线每日照射消毒一次,每月空气细菌培养一次,紫外线强度定期测定。
并做记录。
3、各种检验标本的收集,送检必须用相应指定的容器留取,不得外溢污染。
4、静脉及末稍采血,应严格执行消毒隔离措施,静脉抽血做到一人一针一筒一巾一带一消毒,所用止血带及纸垫每日消毒,末稍采血一人一片一管,杜绝交叉污染。
5、一次性医用器具包括采血针,注射器、尿杯、血红蛋白微量吸血吸管,应严格做好领发登记,注射器先浸泡消毒后由供应室一对一调换,统一处理,其余一次性器具浸泡消毒后装入污物袋送焚烧炉焚烧。
6、检验人员在进行静脉抽血时应严格遵守无菌操作技术,操作前必须洗手必须戴好帽子与口罩,操作台和手被污染时应用肥皂和流水认真洗手,必要时用消毒液浸泡双手,酒精、碘酒瓶每周更换消毒两次。
7、凡是肝炎病人和透析病人的血液标本及疑有黄疸的血标本,都视为肝炎的污染标本,应贴上红色危险标记,放在规定区域内,引起警惕和防止扩大污染面。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
包外粘贴化学指标胶带
包装待灭菌物品
包内放置化学指示卡(管) 指示胶带上按要求做好记录
装载灭菌
检查包外化学指示卡胶带颜色
将变色合格的灭菌包储存于无菌间
使用实验室开包检查包内化学指示卡颜色
压力蒸汽灭菌物理监测流程
包装前检查安装在灭菌器上的亮器
检查灭菌物品包装与装载
查看显示屏或打印纸上灭菌过程参数显示
计时,暴露30分钟后将培养皿盖扣上
培养皿编号,在检验报告单上标记
将采集好的培养皿送微生物检测
清洗工作站(迈尔)操作流程图
打开电源、水源
调节好气体处理器压力
初洗
设定好各计时器时间 普通器械清洗区顺序
酶洗 漂洗
末洗 各清洗池操作
初洗 腔镜器械清洗区顺序 酶洗 干燥太开启热烘机、气枪干燥 超声清洗 漂洗 操作结束、关闭电源、水源 末洗
≧ 100cm2,取100cm2
有无菌方法将棉拭子放入装有 无菌营养肉汤的试管中,盖上 试管盖
试管编号,检验报告单上注明 采样者姓名及试管编号,及时 送微生物检测
消毒剂细菌检测操作流程图
准备采样用物
选择待检测的消毒剂
点燃酒精灯
用无菌方法打开吸管,抽吸0.5——1.0ml待检消毒剂
在近酒精灯处打开含有相应中和剂的无菌洗脱液试管,将 吸管内的消毒剂注入试管内,盖紧试管塞
记录每一灭菌批次相关信息
手术部无菌物品灭菌效果常规监测流程图
准备采样用物
点燃酒精灯,检查被检物品灭菌日期
用无菌方法打开被检物品
小件医疗器械分别投入5mL含 营养肉汤的无菌试管中
大的医疗器械在无菌操作下取2 份以上用沾有无菌营养肉汤的 棉拭子反复涂擦
特殊医疗用品,用浸有物理营养肉 汤的棉拭子涂擦,被菜表面 《100cm2,取全部表面,被菜表面
手术部物体表面监测流程图
选择被检查物体表面
根据不同的采样方法准备相应的采样用物
棉拭子法
压印发
将灭菌后的规格板放 在被检物体表面
打开平皿盖,将平皿内培养基 压贴咋物体上
用含有盐水的棉拭子在规格板内 横竖往返均匀涂抹5次,并随之 转动棉试子,连续采样1—4个规 格板面积
用食指轻轻按压培养皿10—2秒 后。盖上平皿盖
用无菌方法将棉拭子放入装有10mL 采样液的试管中,盖上试管盖
连续采样1—4个平板
试管或平皿上编号,检验报告单上注明采样 物品名称及试管或平皿编号,及时送检
洁净手术部空气采样流程图
根据手术间洁净度级别及预计采样房间需要的培养 皿数量(动态、静态),通知微生物室准备
于采样日前1—2日通知手术部准备相应采样房间
根据手术部要求更换专用衣服,带好口罩、帽子如相应的房间
静态
根据手术间洁净度级别按要求手术 区,周边区布点放置好培养皿 将采样架置于每个回风口,在手术 切皮时,手术2小时候手术结束前 将培养皿放于回风口中部
动态
打开所有培养皿,将培养皿盖扣于 培养皿边缘,同时做阳性对照
打开所有培养皿,将培养皿盖扣于 采样架上
在试管上编号,检验报告单上注明被检测消毒剂名称及试 管编号,及时送微生物室检测
外科手消毒效果监测流程
准备采样用物
在洗手后,进行诊疗活动前采样
用浸用相应中和剂的无菌洗脱液的棉拭子在被检者双手指曲往返涂擦2次
用无菌方法将棉拭子放入装有10mL采样液棉拭子的试管中,盖上试管盖
试管编号,检验报告单上注明采样者姓名及试管编号,及时送微生物检测
外来器械发放流程图
CSSD确定灭菌包的物理和化学检测合格
进行生物检测、结果合格后记录
发放到相应手术间
紧急情况下,在生物PCD中加第五类化学指示卡灭菌,合格后发放
进行快速生物检测3小时观察结果检测
结果反馈给主刀医生
