有机化学实验十二醛和酮的鉴定
醛和酮的检验 - 广东嘉应学院

碘代烷。碘代烷遇硝酸汞时生成朱红色碘化汞。ROR'
加热 +HI
ROH+R'I
R'I+HgNO3
R O NO2+HgI
试验方法:在一试管中,加入1g试样,1ml醋酸和1ml57%氢碘
酸(比重约1.7,恒沸点为126℃)。再加入2小粒多孔磁石。取 一制备好的大小合适的纱布塞装入试管口下3-4ml处。布塞上铺 一层2mm厚的棉花。棉花上放一张纵向折迭的滤纸,滤纸用硝 酸汞溶液润湿。
烃类的检验
试验方法:在一小试管中,加入0.1g试样和 2ml四氯化碳溶剂,摇动,使压碎。向些溶 液中滴加入2%溴-四氯化碳的红棕色溶液, 边加边摇动试管。若加入1-2滴以上的溶液 后,溴的红棕色溶液后,溴的红棕色仍继续 退去,则表示试样中可能含有碳-碳不饱和 键。
结果与讨论:
RR本键红' 试和棕C =验共色C用轭褪来双去RH"区键。别,KM烷 能nO烃 迅4 /与 速H+不 地饱 与RR'和 溴C起烃=O加,成绝+反大应多O,数=C使碳溴-RO碳"H的双
试验方N法:溶解N0.1g样品于3ml钒酸溶N液中(由0.N1g钒 酸铵溶于10O0ml水中配制而nR成OH)。加入3滴2O.5%的8-羟 基喹啉在O 6%V 乙O 酸中的溶液。充分摇动后O ,V 再O加入 10ml苯或甲O 苯H,再次摇动后,在苯或甲苯O层中H..显.....(现ROH)n 粉红色或红色者为正结果,呈现灰绿色者为负结果。
R RC
R
R
>
CH > R CH2
R
若卤代烃的分子结构不同,而卤原子相同时,反应的 速度次序为:
RCX>R2CHX>RCH2X
醛和酮的性质原理应用实验

醛和酮的性质原理应用实验一、实验目的掌握醛和酮的性质原理,了解它们的应用实验方法及实验原理。
二、实验器材和试剂1.实验器材:试管、显微镜、玻璃棒、滴管等;2.试剂:甲醛、丙酮、盐酸、碘液等。
三、实验原理醛和酮是常见的有机化合物,它们都含有羰基官能团。
醛分子中,一个碳原子上连接一个氢原子和一个羰基,而酮分子中,两个碳原子直接连接一个羰基。
由于它们的结构差异,醛和酮的性质也有所不同。
醛和酮的性质主要包括物理性质和化学性质两个方面:1. 醛和酮的物理性质•醛和酮的熔点和沸点随碳原子数量的增加而增加,但相对于相应的醇和酸来说,醛和酮的熔点和沸点较低;•醛和酮能溶解在有机溶剂中,如醇、醚和酯等,但不溶于水。
2. 醛和酮的化学性质•氧化性:醛能被氧化为相应的酸,而酮则不容易被氧化;•还原性:醛和酮均可被还原为相应的醇;•亲核加成反应:醛和酮的羰基易于与亲核试剂发生加成反应,生成相应的缩水醇或缩酮。
四、实验步骤1.醛和酮的检验:–将少量待测物与碘液混合,观察颜色变化。
醛试剂能与碘液反应,生成棕红色沉淀,而酮则无反应。
–加入少量盐酸,加热,观察气味。
醛试剂经加热后会发出刺激性气味的蒸汽,而酮则无明显变化。
2.羰基化合物的还原性实验:–取一小量醛和酮试剂分别与盐酸和亚硫酸钠溶液混合,加热反应,观察气体的生成情况。
醛和酮在还原试剂的作用下会生成相应的醇。
3.亲核加成反应实验:–取一小量醛和酮试剂,分别与羟胺或水合肼混合,加热反应,观察颜色变化。
醛和酮的羰基与亲核试剂反应后,会生成颜色明显不同的缩水醇或缩酮。
五、实验注意事项1.实验操作时要注意个人安全,避免接触到有毒有害物质;2.实验过程中要注意加热时的控制,避免发生意外;3.所有废弃物需按规定进行处理,不能随意倒置于垃圾桶。
六、实验总结通过本实验,我们了解了醛和酮的性质原理及其应用实验方法。
醛和酮的物理性质包括熔点、沸点和溶解性,而化学性质则包括氧化性、还原性和亲核加成反应性等。
有机化学实验报告

有机化学实验报告
实验目的,通过本次实验,掌握醛和酮的检验方法,熟悉有机化合物的性质和反应。
实验原理,醛和酮是有机化合物中常见的官能团,它们具有一系列特征性的化学反应。
其中,醛和酮的检验是有机化学实验中的重要内容。
本实验主要通过银镜反应和尿素反应来检验醛和酮的存在。
实验步骤:
1. 银镜反应,取一小部分待检验的化合物溶液,加入等量的银镜试剂,观察是否生成银镜沉淀。
2. 尿素反应,取一小部分待检验的化合物溶液,加入等量的尿素试剂,观察是否生成结晶沉淀。
实验结果:
1. 银镜反应,待检验的化合物溶液加入银镜试剂后,出现银镜沉淀,表明该化合物为醛。
2. 尿素反应,待检验的化合物溶液加入尿素试剂后,未观察到结晶沉淀,说明该化合物不是酮。
实验结论,根据实验结果,待检验的化合物为醛。
实验总结,通过本次实验,我们成功掌握了醛和酮的检验方法,并且对有机化合物的性质和反应有了更深入的了解。
在今后的实验中,我们将进一步应用这些知识,提高自己的实验操作能力和化学分析能力。
实验安全注意事项:
1. 实验中要注意化学试剂的使用量,避免浪费。
2. 实验操作时要戴上实验手套和护目镜,确保实验安全。
实验延伸:
1. 可以尝试使用其他方法来检验醛和酮的存在,比如费林试剂法。
2. 可以进一步研究醛和酮的性质和反应,拓展实验内容。
通过本次实验,我们不仅完成了实验报告的撰写,还深入了解了有机化合物的检验方法和实验操作技巧。
希望在今后的学习中能够更加努力,不断提高自己的实验能力和化学知识水平。
醛与酮的性质实验报告

醛与酮的性质实验报告
《醛与酮的性质实验报告》
实验目的:
通过实验观察和比较醛与酮的性质,了解它们在化学反应中的特点和区别。
实验材料:
醛:甲醛
酮:丙酮
硫酸铜溶液
氢氧化钠溶液
银镜反应试剂
实验步骤:
1. 将甲醛和丙酮分别溶解于水中,得到两种溶液。
2. 分别加入硫酸铜溶液,观察产生的沉淀情况。
3. 分别加入氢氧化钠溶液,观察产生的现象。
4. 进行银镜反应,观察产生的沉淀和颜色变化。
实验结果:
1. 加入硫酸铜溶液后,甲醛产生了蓝色沉淀,而丙酮没有产生沉淀。
2. 加入氢氧化钠溶液后,甲醛产生了白色沉淀,而丙酮没有产生沉淀。
3. 银镜反应中,甲醛生成了银镜沉淀,而丙酮没有发生变化。
实验结论:
通过实验观察和比较,我们发现醛和酮在化学反应中表现出了不同的性质。
醛具有还原性,在加入硫酸铜溶液和氢氧化钠溶液时产生了沉淀,而丙酮没有产
生沉淀。
在银镜反应中,甲醛生成了银镜沉淀,而丙酮没有发生变化。
这表明醛和酮在化学反应中具有不同的还原性和氧化性,这也是它们在有机化学中的重要区别之一。
实验启示:
通过本次实验,我们深入了解了醛和酮的性质,并且能够通过实验观察和比较得出它们在化学反应中的特点和区别。
这对我们在有机化学的学习和应用中具有重要的指导意义,也为我们进一步探索有机化学的奥秘提供了宝贵的经验和启示。
醛和酮的鉴别方法

醛和酮的鉴别方法
醛和酮是有机化合物中的两种常见的官能团。
在化学实验室中,醛和酮的鉴别方法主要分为以下几个方面。
1. 使用Fehling试剂或Benedict试剂
Fehling试剂或Benedict试剂可以区分醛和酮。
这两种试剂包含了铜离子和碱性化合物,可以将醛氧化为相应的酸,但对于酮没有反应。
实验时将待测物和试剂混合在一起,然后加热,在正常情况下,醛会产生红色沉淀,而酮不会有反应。
2.使用Schiff试剂
Schiff试剂可以用于鉴别含有羰基官能团的化合物,这种试剂可以反应出醛但不能反应出酮。
Schiff试剂是一种含有亚硫酸钠和强酸的试剂,首先将试剂加入待测物,然后加热,如果产生了颜色变化,说明该化合物是醛,如果没有颜色变化,则说明是酮。
3.使用Sodium Bisulfite试剂
Sodium Bisulfite试剂可以用于鉴别含有羰基官能团的化合物,醛和酮能够与Sodium Bisulfite形成加合物,但醛的反应迅速而强烈,可以在室温下反应,而酮的反应速度较慢,需要在加热的情况下反应。
在实验中,将待测物和试剂混合,不加热直接放置,如果在30分钟内产生了白色结晶,则反应物为醛,如果没有白色结晶则反应物为酮。
4.使用Lucas试剂
5.使用Jones试剂
以上就是常用的醛和酮的鉴别方法。
实验者需要结合实验情况和实验目的的不同,选择适当的鉴别方法。
用哪些方法可以鉴别醛和酮

用哪些方法可以鉴别醛和酮鉴别醛和酮的方法有以下几种:1. 针对化合物的物理性质进行鉴别:(1)沸点测定:由于醛和酮分子中含有羰基,其沸点较醇和酚相对较高,通过测定化合物的沸点可以初步鉴别是醛还是酮。
一般来说,醛的沸点要比同分子量的酮的沸点更低。
(2)溶解性测定:醛和酮可溶于不同的溶剂中,在一般有机溶剂中酮的溶解性要好于醛。
通过观察化合物在不同溶剂中的溶解情况可以初步鉴别是醛还是酮。
2. 化学试剂进行鉴别:(1)用碘酰胺:碘酰胺(I2/NH3)在醛和酮的存在下产生氨胺。
当有醛存在时,产生的氨会与醛反应生成颜色较深的产品,而酮则不会发生颜色变化。
通过观察反应产物形成的颜色变化可以鉴别是醛还是酮。
(2)用Fehling试剂:Fehling试剂由成人气器A和Fehling溶液B混合后形成,其中Fehling试剂A含有铜离子,可以和醛发生氧化反应生成酸,而与酮没有反应。
通过观察反应管中是否出现红色沉淀可以鉴别是醛还是酮。
(3)用Tollen试剂:Tollen试剂是由氨水和无水AgNO3溶液混合而成,它可以被醛氧化成相应的酸,并同时将无机银离子还原成金属银沉淀。
而酮则不发生反应。
通过观察反应管中是否出现银镜可以鉴别是醛还是酮。
3. 使用红外光谱(IR)进行鉴别:红外光谱是一种常用的检测有机化合物功能团的方法。
在红外光谱中,醛和酮通过C=O红外吸收峰的位置和强度可以进行鉴别。
醛的C=O伸缩振动在1700-1750 cm-1的区域,吸收峰较酮强;而酮的C=O伸缩振动在1700-1725 cm-1的区域,吸收峰较醛弱。
通过比较红外光谱中C=O伸缩振动的位置和强度可以鉴别是醛还是酮。
4. 使用核磁共振波谱(NMR)进行鉴别:核磁共振波谱是一种常用的分析有机化合物结构的方法。
在1H NMR谱和13C NMR谱中,醛和酮的碳和氢的化学位移可以用来进行鉴别。
醛的碳和氢的化学位移一般在较低的范围内,而酮的则较高。
通过观察和对比不同化合物在核磁共振谱中的化学位移可以鉴别是醛还是酮。
醛酮_性质实验报告

一、实验目的1. 加深对醛和酮性质的认识。
2. 掌握醛和酮的鉴别方法。
3. 了解醛和酮的化学性质及其在有机合成中的应用。
二、实验原理醛和酮是含有一个或多个羰基(C=O)的有机化合物。
醛的羰基位于碳链的末端,而酮的羰基位于碳链的中间。
它们具有不同的化学性质,如氧化、还原、亲核加成等。
三、实验仪器与药品1. 仪器:试管、胶头滴管、烧杯、酒精灯、酒精、蒸馏水、碘仿、银氨溶液、斐林试剂、Tollens试剂、亚硫酸氢钠、氢氧化钠、硫酸铜、硫酸锌等。
2. 药品:甲醛、乙醛、丙酮、苯甲醛、苯甲酮、碘化钾、碘、氢氧化钠、硫酸铜、硫酸锌等。
四、实验步骤1. 醛和酮的鉴别a. 取少量醛和酮分别置于试管中,加入少量碘仿,观察是否产生黄色沉淀。
b. 取少量醛和酮分别置于试管中,加入少量银氨溶液,观察是否出现银镜现象。
c. 取少量醛和酮分别置于试管中,加入少量斐林试剂,观察是否出现砖红色沉淀。
2. 醛和酮的氧化反应a. 取少量乙醛和丙酮分别置于试管中,加入少量银氨溶液,观察是否出现银镜现象。
b. 取少量乙醛和丙酮分别置于试管中,加入少量酸性高锰酸钾溶液,观察溶液颜色的变化。
3. 醛和酮的还原反应a. 取少量乙醛和丙酮分别置于试管中,加入少量亚硫酸氢钠溶液,观察是否产生白色晶体。
b. 取少量乙醛和丙酮分别置于试管中,加入少量氢氧化钠溶液,观察是否产生气体。
4. 醛和酮的亲核加成反应a. 取少量乙醛和丙酮分别置于试管中,加入少量氢氰酸,观察是否产生白色沉淀。
b. 取少量乙醛和丙酮分别置于试管中,加入少量水,观察是否产生沉淀。
五、实验结果与分析1. 醛和酮的鉴别a. 碘仿反应:甲醛和乙醛产生黄色沉淀,丙酮不产生沉淀。
b. 银镜反应:甲醛和乙醛产生银镜,丙酮不产生银镜。
c. 斐林试剂反应:甲醛和乙醛产生砖红色沉淀,丙酮不产生沉淀。
2. 醛和酮的氧化反应a. 银镜反应:乙醛和丙酮均产生银镜。
b. 高锰酸钾反应:乙醛溶液颜色由紫色变为棕色,丙酮溶液颜色无明显变化。
鉴别醛 酮的简便方法

鉴别醛酮的简便方法
要鉴别醛和酮这两种有机化合物,可以采用以下几种简便的方法:
1. 用理化性质进行鉴别:
- 熔点:醛和酮的熔点一般较低,但醛的熔点通常比酮的熔点更低。
- 溶解性:醛和酮都可以溶解在水中,但醛的溶解度通常比酮高,因为醛可以形成氢键。
- 稳定性:酮通常比醛更稳定,因为醛中的活泼氢原子容易被氧化剂氧化。
2. 使用化学试剂进行鉴别:
- 用银镜试剂鉴别醛:将醛溶液与银镜试剂反应,如果产生银镜色沉淀,则说明存在还原性醛。
- 用碘仿试剂鉴别酮:将淡黄色的碘仿试剂滴入酮中,如果产生红棕色沉淀,则说明存在酮。
3. 使用氧化剂进行鉴别:
- 使用氢氧化银试剂:将醛或酮与氢氧化银试剂反应,如果产生黑色沉淀,则表明存在醛或酮。
- 使用费林试剂:将醛或酮与费林试剂反应,如果出现绿色溶液,则表明存在醛或酮。
此外,还可以通过红外光谱和核磁共振谱等仪器进一步鉴别和确认醛和酮的结构。
红外光谱可以通过鉴别功能性基团的吸收峰来确定化合物的结构,而核磁共振谱可以提供有关化合物整体结构和取代基位置的信息。
总结起来,要鉴别醛和酮,我们可以通过它们的理化性质、化学试剂反应和仪器分析等多种方法进行辨别。
但需要注意的是,这些方法都有其局限性和特定条件,所以最好在实验室环境下进行鉴别。
第十二章 醛和酮

二.醛酮的化学性质
醛酮的化学性质主要取决于羰基,因为醛、 酮都含有羰基,但醛和酮的结构并不完全相同, 醛基中的羰基与氢原子相连,而酮基则没有与氢 原子相连。因此醛和酮的化学性质上又存在着明 显的差异。醛和酮的主要反应部位如下:
HO
R C CH (R')
H
化学工业出版社
思考:分析醛基的结构,推测其 在化学反应中的断裂方式
化学工业出版社
O R C H(CH3) + HCN
O
OH
R C H(CH3) CN OH
CH3 C H + HCN
CH3 C H
CN
醛、酮与氢氰酸的加成反应是有机合成中增
长碳链的一种方法 。但由于氢氰酸和氰化钾均有
剧毒,实际上很少使用这一方法。α-羟基腈在酸
性条件下可以水解生成α-羟基酸或不饱和烯酸。
CHO
O
化学工业出版社
三、醛、酮的命名
简单的醛、酮使用普通命名法。结构复 杂的醛、酮则使用系统命名法
(一)普通命名法
醛的普通命名法与醇相似,只需根据碳原子数 称为“某醛”。例如:
HCHO CH3CHO CH3CH2CHO
甲醛
乙醛
丙醛
化学工业出版社
酮的普通命名法与醚相似,按酮基所连的 两个烃基来命名。例如:
O CH3 C CH2CH3
O CH3CH2 C CH2CH3
甲(基)乙(基)酮 二乙(基)酮
O
O
C CH2CH3
C
苯(基)乙(基)酮
二苯(基)酮
化学工业出版社
(二)系统命名法
1.脂肪醛、酮命名:
(1).选主链:选择含有羰基的最长碳链为主链,根据 主链碳原子数目称为“某醛”或“某酮”.
有机化学第12章 醛和酮
离反应体系,才得到醛。
CH3CH2OH
K2Cr2O7/ H+ 50℃
CH3CHO
由仲醇氧化制得的酮不易氧化,此法更适宜制备酮。
有机化学
醛酮
16
CH3(CH2)6CH2OH
CrO3 . 吡啶 CH2Cl2 ,25℃
CH3(CH2)6CHO
95%
H3C CH CH CH2OH
巴豆醇
CrO3 . 吡啶 H3C CH CH CHO
O
CHO
CH3O
C CH3
OH
4-甲氧基苯乙酮
2-羟基苯甲醛 水杨醛
CHO
3,8-二甲基-2,7-壬二烯-1-醛
柠檬醛
O
5-甲基-2-异丙基环己酮
有机化学
薄荷醛酮酮
12
二、醛酮的制法
1、烯烃氧化 (双键、H氧化)
R CH
C R' ① O3 R'' ② Zn/ H3O+
R CHO
+
O
R' C
R''
H2C C CH3
命名(羰基碳不计入烃基)。如:
H3C
O C CH2CH3
甲基乙基酮 甲乙酮
O C CH2CH3
苯基乙基酮
苯乙酮
O CH2CH3 苯基乙基醚
苯乙醚
原因:系统命名也有“苯乙酮”,结构与此结构不同。
有机化学
醛酮
7
(2)系统命名法
醛酮的系统命名与醇的系统命名相似。
A: 脂肪族醛酮的命名
脂肪醛的命名与伯醇的命名相似,脂肪酮的命名 与仲醇的命名相似。
环己酮1环己基2丙酮1苯基1乙酮苯乙酮苯基甲基酮巴豆醛肉桂醛chocho3苯基丙烯醛苯基丙烯醛2丁烯醛丁烯醛有机化学124甲基2正丙基戊醛4甲基3乙基26庚二酮4甲氧基苯乙酮2羟基苯甲醛水杨醛choohcho38二甲基27壬二烯1醛5甲基2异丙基环己酮柠檬醛薄荷酮cho有机化学131烯烃氧化ch二醛酮的制法双键h氧化有机化学142由炔制备炔烃水合ohchhgo分子内重排chchchohchcchcocl164含h的醇的氧化和脱氢h氧化常用氧化剂
醛和酮的鉴定实验报告

醛和酮的鉴定实验报告醛和酮的鉴定实验报告实验目的:通过化学实验,鉴定和区分醛和酮化合物。
实验原理:醛和酮是有机化合物中常见的官能团,其区别在于它们的结构中是否存在羰基碳原子两侧的碳原子均为碳氢键。
醛中,羰基碳原子两侧的碳原子至少有一个为氢原子;而酮中,羰基碳原子两侧的碳原子都为碳基团。
实验步骤:1. 实验前准备:准备所需试剂和仪器设备,包括醛和酮化合物样品、试管、试管架、酒精灯、试管夹等。
2. 火焰试验:取少量待测物质,将其滴在镍铝合金丝上,然后将丝放入酒精灯火焰中加热。
若产生明亮的火花并有刺激性气味,表明待测物质为醛;若无火花产生,只有熔化现象,表明待测物质为酮。
3. 试剂试验:a. 用Schiff试剂进行试验:取一小部分待测物质,加入Schiff试剂,观察颜色变化。
若溶液变为红色,表明待测物质为醛;若无颜色变化,表明待测物质为酮。
b. 用碘化银试剂进行试验:取一小部分待测物质,加入碘化银试剂,观察颜色变化。
若溶液变为黄色或白色沉淀,表明待测物质为醛;若溶液无明显变化,表明待测物质为酮。
4. 氧化试验:a. 用氧化银试剂进行试验:取一小部分待测物质,加入氧化银试剂,观察颜色变化。
若溶液变为黑色,表明待测物质为醛;若溶液无明显变化,表明待测物质为酮。
b. 用费林试剂进行试验:取一小部分待测物质,加入费林试剂,观察颜色变化。
若溶液变为深蓝色,表明待测物质为醛;若溶液无明显变化,表明待测物质为酮。
实验结果与讨论:根据实验步骤中的观察结果,我们可以鉴定和区分醛和酮化合物。
通过火焰试验,我们可以初步判断待测物质的性质,但该方法并不十分准确。
而通过试剂试验和氧化试验,可以更加准确地鉴定待测物质是醛还是酮。
在试剂试验中,Schiff试剂的反应原理是醛与Schiff试剂中的亚硫酸钠反应生成具有鲜艳颜色的红色络合物,而酮则不会发生该反应。
碘化银试剂的反应原理是醛与碘化银反应生成黄色或白色的沉淀,而酮则不会发生该反应。
醛,酮性质实验

醛,酮性质实验
醛,酮的性质实验 1.与 2,4 二硝基苯肼的反应:取试管 3 支,分别加入 3 滴甲醛,乙醛和丙酮,在各加入2,4二硝基苯肼试剂10滴,充分震荡,静止片刻,观察,记录并解释发生的现象。
2.碘仿反应:取试管3 支,分别加5 滴甲醛,乙醛和丙酮,再各加入碘试剂10 滴,分别滴加1.25mol/L 氢氧化钠溶液至碘的颜色恰好褪去。
震荡,观察有无沉淀生成,若无沉淀,在温水浴加热数分钟,冷却后再观察,记录并解释发生的现象。
3.与托伦试剂的反应:取大试管 1 支,加入 0.05mol/L 硝酸银溶液2ml,再加入1.25mol/L 氢氧化钠溶液1 滴,然后震荡滴加0.5mol/L 氨水,直至生成的沉淀恰好完全溶解为止,即值得托伦试剂。
取洁净的试管 3 支,各加入配好的托伦试剂,再分别加入 2 滴甲醇,乙醇和丙酮,摇匀后置于60℃左右的水浴溶液中加热,观察,记录并解释发生的现象。
4.与班氏试剂的反应:取试管 3 支,各加入 10 滴班氏试剂,在分别加入 5 滴甲醛,乙醛和丙酮,振荡,置于80℃左右的水浴溶液中加热 2-3 分钟,观察,记录并解释发生的现象。
5.与希夫试剂的反应:取试管2 支,分别滴加5 滴乙醛和丙酮,再加入 10 滴希夫试剂,观察,记录并解释发生的现象。
6.与亚硝酰铁氰化钠的反应:取试管2 支,试管中各加入10滴0.05mol/L 亚硝酰铁氰化钠和 5 滴 1.25mol/L 氢氧化钠,摇匀,再分别加入 10 滴乙醛和丙酮,观察,记录并解释发生的现象。
醛酮的鉴定实验报告

醛酮的鉴定实验报告醛酮的鉴定实验报告引言:醛酮是有机化合物中常见的一类功能团,其结构中含有羰基(C=O)官能团。
醛酮的鉴定实验是有机化学实验中重要的一环,通过该实验可以准确确定化合物中是否含有醛酮官能团,从而为进一步的化学分析和合成提供重要的信息。
本实验通过几种常用的醛酮鉴定方法,对未知化合物进行鉴定与分析。
实验一:用2,4-二硝基苯肼法鉴定醛酮实验原理:2,4-二硝基苯肼(2,4-DNPH)与醛酮反应,可以生成相应的2,4-二硝基苯肼酮(DNPH酮),该酮具有明显的橙红色沉淀。
通过观察产生的沉淀颜色和形态,可以判断样品中是否含有醛酮。
实验步骤:1. 取一小部分未知化合物溶于适量乙醇中。
2. 将溶液滴加入2,4-DNPH溶液中,摇匀。
3. 观察反应产物的颜色和形态。
实验结果:若观察到橙红色沉淀形成,则说明未知化合物中含有醛酮官能团。
实验二:用银镜法鉴定醛酮实验原理:醛酮在碱性条件下与银离子反应,可以生成相应的银镜。
通过观察反应产物的镜面反射性质,可以判断样品中是否含有醛酮。
实验步骤:1. 取一小部分未知化合物溶于适量乙醇中。
2. 加入碱性银氨溶液,摇匀。
3. 观察反应产物的镜面反射性质。
实验结果:若观察到镜面反射出明亮的银镜,则说明未知化合物中含有醛酮官能团。
实验三:用邻氨基苯酚法鉴定醛酮实验原理:醛酮与邻氨基苯酚反应,可以生成相应的酮酸。
通过观察反应产物的颜色变化,可以判断样品中是否含有醛酮。
实验步骤:1. 取一小部分未知化合物溶于适量乙醇中。
2. 加入邻氨基苯酚溶液,摇匀。
3. 观察反应产物的颜色变化。
实验结果:若观察到颜色由无色或淡黄色变为紫色,则说明未知化合物中含有醛酮官能团。
实验四:用巴豆醛试剂法鉴定醛酮实验原理:醛酮与巴豆醛试剂反应,可以生成相应的氧化产物。
通过观察反应产物的颜色变化,可以判断样品中是否含有醛酮。
实验步骤:1. 取一小部分未知化合物溶于适量乙醇中。
2. 加入巴豆醛试剂溶液,摇匀。
有机化学实验十二醛和酮的鉴定

实验十二醛和酮的鉴定一.实验目的:1. 通过实验进一步加深对醛、酮的化学性质的认识;2.通过醛、酮的特征反应,掌握鉴别醛、酮的化学方法;二.实验重点和难点:1. 醛、酮的化学性质的认识;2. 鉴别醛、酮的化学方法;实验类型:基础性实验学时:4学时三.实验装置和药品:主要实验仪器: 试管滴管酒精灯试管夹烧杯锥形瓶布氏漏斗抽滤瓶 pH试纸水浴装置主要化学试剂: 2,4—二硝基苯肼试剂乙醛水溶液丙酮苯乙酮稀硫酸浓硫酸95%乙醇 5%硝酸银浓氨水甲醛苯甲醛铬酸试剂 NaHSO3溶液 10%氢氧化钠溶液碘—碘化钾溶液正丁醛 Schiff试剂托伦试剂费林试剂(I 和 II)淀粉溶液脱脂棉浓H2SO3四.实验原理:(1)醛和酮都含有羰基,可与苯肼、2,4—二硝基苯肼、亚硫酸氢钠、羟胺、氨基脲等羰基试剂发生亲核加成反应。
所得产物经适当处理可得到原来的醛酮,这些反应可用来分离提纯和鉴别醛,酮。
醛和酮在酸性条件下能与2,4—二硝基苯肼作用,生成黄色、橙色和橙红色的2,4—二硝基苯腙沉淀。
2,4—二硝基苯腙是有固定熔点的结晶,易从溶液中析出,即可作为检验醛,酮的定性试验,又可作为制备醛,酮衍生物的一种方法。
(2)鉴于醛比酮易被氧化的性质,选用适当的氧化试剂可以区别,区别醛,酮的一种灵敏的试剂是Tollens试剂,它是银氨络离子的碱性水溶液,反应时醛被氧化成酸,银离子被还原成银附着在试管壁上,故Tollens试验又称银镜反应。
RCHO+2Ag(NH3)2+OH- ——→2Ag↓+RCO2NH4 + H2O + 3NH3铬酸试验也可用来区别醛,酮,由于铬酸在室温下很容易将醛氧化为相应的羧酸,溶液由橘黄色变成绿色,酮在类似条件下不发生反应。
3RCHO+H2Cr2O7+3H2SO4——→3RCO2H+Cr2(SO4)3+4H2O橘黄绿色由于伯醇和仲醇也咳被铬酸氧化,因此铬酸试验不是鉴别醛的特征反应,只有通过用2,4-二硝基苯肼鉴别出羧基后,才能用此法进一步区别醛和酮。
醛和酮的检验 - 广东嘉应学院

反应,生成卤化银沉淀。
乙醇
R
X+AgNO3
R
O
NO2+AgX
试验方法: 在一支小试管中,放置0.5ml饱和的硝酸银乙 醇溶液,加入约30ml(或3滴)试样,强烈摇动后,在室温下静 止2分钟,观察是否有沉淀生成,如无沉淀生成,则将溶液加 热后,再观察结果.如有沉淀产生,在常常中加入3滴5%硝 酸溶液,摇动后,再注意沉淀是否溶解.卤化银不溶于稀硝 酸,而有机酸的银协能溶于稀硝酸中.若溶液仅发生混浊, 可认为是由于微量杂质所引起的,应为负结果
R RC
R
R
>
CH > R CH2
R
若卤代烃的分子结构不同,而卤原子相同时,反应的 速度次序为:
RCX>R2CHX>RCH2X
结果与讨论
双键或芳环的位置,对卤原子的活性也有影响,通常有下 列活性次:
H2C 或
CH CH2X > H2C CH (CH2)n CH2X >H2C
ArCH2X >
Ar (CH2)n CH2X > ArX
蓝色
联苯、菲
紫色
蒽
绿色
各种颜色随时间的变化而有所改变
烃类的检验
溴-四氯化碳试验
绝大多数含有碳碳双键和三键的化合物,很容易与溴起 加成反应,实验时可以观察到溴的四氯化碳溶液褪色。 其反应为:
C
C
+Br2 CCl4
CC
Br Br
CC
+Br2
CCl4 快
CC
Br2 慢
Br Br
Br Br C CH Br Br
结果与讨论
本实验对一般的醇类,不论是水溶性的还是非水溶 性的醇类,均能检验出来。多羟基化合物,如乙二 醇,甘油糖类等均呈负结果,因为这些强极性化合 物不溶于苯,不能与本实验发生溶剂作用。 含有羟基的羧酸、酒石酸、柠檬酸等也无反应,硫 醇及胺类产生绿色或黄色变化。 烃类醚类酮类有卤代烃的存在,对本实验没有干扰。
醛和酮的实验报告

醛和酮的实验报告醛和酮的实验报告引言:醛和酮是有机化学中常见的官能团,它们在生物学、医学、化工等领域中都有着广泛的应用。
为了更好地理解和研究醛和酮的性质和反应特点,本实验通过一系列的实验操作和观察,对醛和酮进行了深入的研究。
实验一:醛的制备与性质研究在这个实验中,我们首先选择了乙醛作为研究对象。
通过将乙醇与酸性高锰酸钾溶液反应,我们成功地制备了乙醛。
实验过程中,我们观察到了高锰酸钾溶液逐渐变浅,同时产生了一种刺激性气味的物质。
这表明乙醇在酸性条件下被氧化成了乙醛。
接下来,我们对乙醛进行了一系列的性质研究。
首先,我们进行了醛的还原反应。
将乙醛与氢气在催化剂的存在下反应,我们观察到了乙醇的生成。
这表明乙醛具有还原性质,可以被还原成醇。
然后,我们对乙醛进行了醛的氧化反应。
将乙醛与氧气在催化剂的存在下反应,我们观察到了乙酸的生成。
这表明乙醛具有氧化性质,可以被氧化成酸。
实验二:酮的制备与性质研究在这个实验中,我们选择了丙酮作为研究对象。
通过将丙醇与酸性高锰酸钾溶液反应,我们成功地制备了丙酮。
实验过程中,我们观察到了高锰酸钾溶液逐渐变浅,同时产生了一种具有刺激性气味的物质。
这表明丙醇在酸性条件下被氧化成了丙酮。
接下来,我们对丙酮进行了一系列的性质研究。
首先,我们进行了酮的还原反应。
将丙酮与氢气在催化剂的存在下反应,我们观察到了丙醇的生成。
这表明丙酮具有还原性质,可以被还原成醇。
然后,我们对丙酮进行了酮的氧化反应。
将丙酮与氧气在催化剂的存在下反应,我们观察到了丙酸的生成。
这表明丙酮具有氧化性质,可以被氧化成酸。
实验三:醛和酮的加成反应在这个实验中,我们研究了醛和酮的加成反应。
我们选择了乙醛和丙酮作为研究对象。
首先,我们将乙醛与氰化钠反应,观察到了产物乙醇腈的生成。
这表明醛可以与氰化物加成生成腈。
接着,我们将丙酮与丙胺反应,观察到了产物N,N-二丙基乙酰胺的生成。
这表明酮可以与胺加成生成酰胺。
实验四:醛和酮的亲核加成反应在这个实验中,我们研究了醛和酮的亲核加成反应。
有机化学:第十二章-醛和酮分析

O
O CH3
H3C C CH2CH3 CH3CH2 C CHCH3
2—丁酮
2-甲基-3-戊酮
不饱和醛酮的命名是从靠近羰基一端给主链编号:
CH3 CH
CH3 O CH CH C CH3
3-甲基-4-己烯-2-酮
羰基在环内的脂环酮,称为环某酮;若羰基在环外,则 将环作为取代基。
O
CH3
4-甲基环己酮
C=O + dR--Mdg+ X 干醚 R-C-OMgX H2O/H+
d+ d烷氧基卤化镁
R-C-OH
RMgX与甲醛反应,水解后得到1°醇; RMgX与其他醛反应,水解后得到2°醇; RMgX与酮反应,水解后得到3°醇。
Cl
用途:制1°、2°、3°醇。例:
CH2OH
Cl Mg
干醚
MgCl HCHO
CH2OMgCl H2O/H+
CH2OH
环己1。基醇甲醇
5. 与氨衍生物的加成
氨的衍生物(NH2Y)(如羟氨(NH2OH)、肼(NH2NH2)、苯肼、2, 4-二硝基苯肼、氨基脲 (NH2NHC(O)NH2) )等由于氮上有孤对电子, 都能作为亲核试剂和醛、酮的羰基发生亲核加成反应。反应是可逆 的。
H+
C O + :NH2Y
C NHY + H2O
O H3C C
CH2CH3
O CH2 CH C CH3
CH3
Cl O CH2 C CH3
甲基乙基酮
甲基乙烯基酮
甲基-α-氯乙基酮
O
二苯酮(二苯甲酮)
2、IUPAC命名法
选含羰基的最长碳链为主链,从靠近羰基一端给主链编 号。醛基因处在链端,因此编号总为1。酮羰基的位置要标 出(个别例外)。
鉴别醛酮的简便方法

鉴别醛酮的简便方法
鉴别醛酮的常用简便方法有以下几种:
1. 使用Schiff试剂:Schiff试剂是一种常用于鉴别醛类化合物的染色试剂。
将样品溶解在乙醇中,加入少量Schiff试剂,观察溶液变成橙红色至紫红色,即可判断为醛类化合物。
2. 使用Fehling试剂:Fehling试剂是常用于鉴别还原性物质中的醛类化合物的试剂。
将样品溶解在水中,加入等量的Fehling A溶液和Fehling B溶液,加热至沸腾。
如果在加热过程中出现红色沉淀,即可判断为醛类化合物。
3. 使用Tollens试剂:Tollens试剂也是一种常用于鉴别醛类化合物的试剂。
将Tollens试剂溶解在碱性溶液中,将样品加入试剂溶液中并加热。
如果溶液中出现银镜反应,即可判断为醛类化合物。
这些方法虽然简便,但也有一定的限制条件和缺点,例如特异性不高、某些醛酮可能无法被特定试剂鉴别等。
因此,在实际应用中,还需结合其他方法进行鉴别确认。
醛酮的化学反应及检验
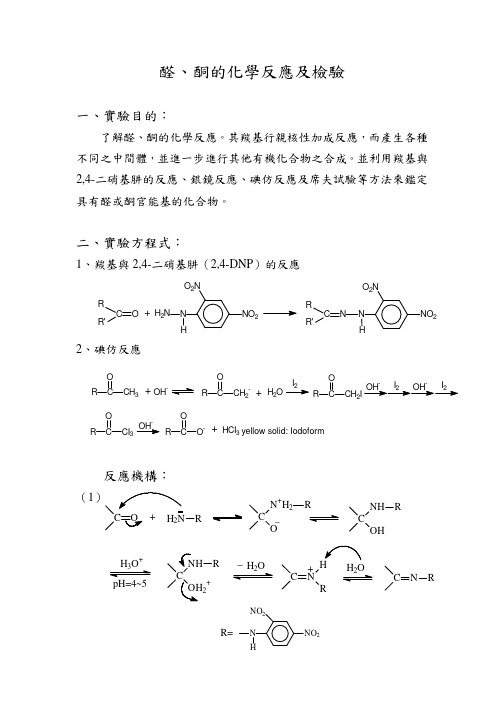
若有黃綠色沉澱,此化合物具有甲基酮官能基; 若無黃綠色沉澱,再加熱 15 分鐘,若仍無黃綠色沉澱則表示此化合 物具有無甲基酮官能基。
Iodoform Samples Structures
O H3C C
Silver mirror +
2,4-DNP test
Ethanal Acetone Benzaldehyde
乙醇
CH3CH2OH
Acetone
無色微香液體,易著火,比重 0.788 ,沸點 56.5 ℃。與水、乙醇、乙醚、氯仿、DMF、油類 互溶。蒸氣能與空氣形成爆炸性混合物,化 學性質活潑,廣泛用作工業溶劑。
丙酮
CH3COCH3 Benzaldehyde
無色油狀液體,有杏仁香味,密度 1.046,沸 點 179℃。稍溶於水,能與乙醇、乙醚或氯仿
_ _ OH ,I2,OH,I2
_ ቤተ መጻሕፍቲ ባይዱ C CI3 + OH
CHI3(碘仿,黃色固體)
三、實驗原理:
1、醛的通式
O R C H
酮的通式
O R C R1
1具有極性的羰基
2醛較酮易進行碳氧雙鍵的親核性加成反應(立體障礙及電子因素) 3沸點較相似分子量的碳氫化合物高(可與水產生氫鍵) ,但較相似 分子量的醇低(不能形成分子間氫鍵) 。 2、醛的製備: 11。醇的氧化(PCC:CrO3.Pyr.HCl;將醇類氧化成醛類最常用的試 劑)
O2N R R' C O O2N R NO2 R' C N N H NO2
+ H2N N
H
2、碘仿反應
O R C O R C CI3 CH3 O I2 R O C CH2I OHI2 OHI2
+ OH
有机化学实验十二-醛和酮的鉴定

实验十二醛和酮的鉴定一.实验目的:1.通过实验进一步加深对醛、酮的化学性质的认识;2.通过醛、酮的特征反应,掌握鉴别醛、酮的化学方法;二.实验重点和难点:1.醛、酮的化学性质的认识;2.鉴别醛、酮的化学方法;实验类型:基础性实验学时:4学时三.实验装置和药品:主要实验仪器: 试管滴管酒精灯试管夹烧杯锥形瓶布氏漏斗抽滤瓶pH试纸水浴装置主要化学试剂: 2,4—二硝基苯肼试剂乙醛水溶液丙酮苯乙酮稀硫酸浓硫酸95%乙醇5%硝酸银浓氨水甲醛苯甲醛铬酸试剂NaHSO3溶液10%氢氧化钠溶液碘—碘化钾溶液正丁醛Schiff试剂托伦试剂费林试剂(I 和II)淀粉溶液脱脂棉浓H2SO3四.实验原理:(1)醛和酮都含有羰基,可与苯肼、2,4—二硝基苯肼、亚硫酸氢钠、羟胺、氨基脲等羰基试剂发生亲核加成反应。
所得产物经适当处理可得到原来的醛酮,这些反应可用来分离提纯和鉴别醛,酮。
醛和酮在酸性条件下能与2,4—二硝基苯肼作用,生成黄色、橙色和橙红色的2,4—二硝基苯腙沉淀。
2,4—二硝基苯腙是有固定熔点的结晶,易从溶液中析出,即可作为检验醛,酮的定性试验,又可作为制备醛,酮衍生物的一种方法。
(2)鉴于醛比酮易被氧化的性质,选用适当的氧化试剂可以区别,区别醛,酮的一种灵敏的试剂是Tollens试剂,它是银氨络离子的碱性水溶液,反应时醛被氧化成酸,银离子被还原成银附着在试管壁上,故Tollens试验又称银镜反应。
RCHO+2Ag(NH3)2+OH- ——→2Ag↓+RCO2NH4+ H2O + 3NH3铬酸试验也可用来区别醛,酮,由于铬酸在室温下很容易将醛氧化为相应的羧酸,溶液由橘黄色变成绿色,酮在类似条件下不发生反应。
3RCHO+H2Cr2O7+3H2SO4——→3RCO2H+Cr2(SO4)3+4H2O橘黄绿色由于伯醇和仲醇也咳被铬酸氧化,因此铬酸试验不是鉴别醛的特征反应,只有通过用2,4-二硝基苯肼鉴别出羧基后,才能用此法进一步区别醛和酮。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
实验十二醛和酮的鉴定
一.实验目的:
1.通过实验进一步加深对醛、酮的化学性质的认识;
2.通过醛、酮的特征反应,掌握鉴别醛、酮的化学方法;
二.实验重点和难点:
1.醛、酮的化学性质的认识;
2.鉴别醛、酮的化学方法;
实验类型:基础性实验学时:4学时
三.实验装置和药品:
主要实验仪器: 试管滴管酒精灯试管夹烧杯锥形瓶布氏漏斗
抽滤瓶pH试纸水浴装置
主要化学试剂: 2,4—二硝基苯肼试剂乙醛水溶液丙酮苯乙酮稀硫酸浓硫酸95%乙醇5%硝酸银浓氨水甲醛苯甲醛铬酸试剂NaHSO3溶液10%氢氧化钠溶液碘—碘化钾溶液正丁醛Schiff试剂托伦试剂费林试剂(I 和II)淀粉溶液脱脂棉浓H2SO3
四.实验原理:
(1)醛和酮都含有羰基,可与苯肼、2,4—二硝基苯肼、亚硫酸氢钠、羟胺、氨基脲等羰基试剂发生亲核加成反应。
所得产物经适当处理可得到原来的醛酮,这些反应可用来分离提纯和鉴别醛,酮。
醛和酮在酸性条件下能与2,4—二硝基苯肼作用,生成黄色、橙色和橙红色的2,4—二硝基苯腙沉
2,4—二硝基苯腙是有固定熔点的结晶,易从溶液中析出,即可作为检验醛,酮的定性试验,又可作为制备醛,酮衍生物的一种方法。
(2)鉴于醛比酮易被氧化的性质,选用适当的氧化试剂可以区别,区别醛,酮的一种灵敏的试剂是Tollens试剂,它是银氨络离子的碱性水溶液,反应时醛被氧化成酸,银离子被还原成银附着在试管壁上,故Tollens试验又称银镜反应。
RCHO+2Ag(NH3)2+OH- ——→2Ag↓+RCO2NH4+ H2O + 3NH3
铬酸试验也可用来区别醛,酮,由于铬酸在室温下很容易将醛氧化为相应的羧酸,溶液由橘黄色变成绿色,酮在类似条件下不发生反应。
3RCHO+H2Cr2O7+3H2SO4——→3RCO2H+Cr2(SO4)3+4H2O
橘黄绿色
由于伯醇和仲醇也咳被铬酸氧化,因此铬酸试验不是鉴别醛的特征反应,只有通过用2,4-二硝基苯肼鉴别出羧基后,才能用此法进一步区别醛和酮。
(3)一个鉴别甲基酮的简便方法是次碘酸钠试验,凡是有CH3CO—基团或其它易被次碘酸钠氧化成这种基团的化合物,如CH3—CH—均能被次碘酸钠作用生成黄色的碘仿沉淀。
RCOCH3+3NaIO——→RCOCI3+3NaOH
RCOCI3+NaOH——→RCOONa+CHI3(黄)
(4)Fehling试剂是由等体积的CuSO4溶液(Fehling I)和酒石酸钾纳的NaOH溶液(Fehling II)组成的。
醛跟氢氧化铜反应(也裴林反应):Cu(OH)2的碱溶液,能把脂肪醛氧化为羧酸,同时Cu(OH)2被还原为红色的Cu2O沉淀。
也是检验醛基的一种方法。
CuSO4+2NaOH→Cu(OH)2↓+Na2SO4
CH 3CHO+2Cu(OH)2CH 3COOH+Cu 2O ↓+2H 2O
酮的重要代表物是丙酮,它易挥发,易燃烧,能溶解许多有机物,是一种重要的有机溶剂,
它没有还原性,不跟银氨溶液起银镜反应。
(5)醛酮能与NaHSO 3溶液反应,生成α-羟基磺酸钠沉淀。
3NaHSO + C R R'(H)O C
R R'(H)OH 3SO Na ↓ 五. 实验內容及步骤:
1.2,4—二硝基苯肼试验:
取3支干燥洁净的试管,各加入1mL 2,4-二硝基苯肼,再依次加入1-2滴试样((1)乙醛、(2)丙酮、
(3)苯乙酮溶液),摇匀静置片刻,观察结晶颜色,若无沉淀,则于水浴中加热。
现象:
结论:
2.Tollens 试验:
取4支洁净的试管中分别加入2mL 5%硝酸银,不断振荡下,逐滴加入浓氨水,开始时生成棕色沉淀,继续加入浓氨水至刚好溶解,再分别加入2滴试样,摇匀,静置,若无变化,50-600C 水浴温热几分钟,观察现象?
试样:(1)甲醛水溶液、(2)乙醛水溶液、(3)丙酮、(4)苯甲醛
现象:
结论:
3.醛、酮а-H 活泼性:碘仿试验:
取4支洁净的试管,分别加入1mL 蒸馏水和3-4滴试样,再分别加入1mL 10%NaOH 溶液,滴加KI-I 2至溶液呈浅黄色,继续振荡至浅黄色消失,析出浅黄色沉淀,若无沉淀,则放在50-600C 水浴中微热几分钟,(可补加KI-I 2溶液)观察结果。
试样:(1)乙醛、(2)正丁醛(3)丙酮、(4)乙醇
现象:
结论:
4. Fehling 试验:
取44支洁净的试管,分别加入Fehling 试剂I 和II 各0.5mL ,然后依次加入3-4滴样品(1)甲醛水溶液(2)乙醛水溶液(3)丙酮(4)苯甲醛,振荡,水浴加热。
现象:
结论:
5.与饱和NaHSO 3溶液反应
取4支洁净的试管,分别加入2mL 新配制的饱和NaHSO 3,分别滴加1mL 试样,振荡置于冰水中冷却数分钟,观察沉淀析出的相对速度。
试样:(1)甲醛水溶液 (2)乙醛水溶液、(3)丙酮、(4)苯甲醛、
现象:
结论:
6.
Schiff 试验
在4支试管中分别加入1ml 品红醛试剂(Schiff 试剂),然后分别滴加2滴试样,振荡摇匀,观察现象?
试样:(1)甲醛、(2)乙醛、(3)丙酮、(4)苯甲醛
现象:
结论:
7.淀粉水解反应:
取一支干净试管,加入约3mL 溶液,0.5mL 稀硫酸,于水浴中加热5min ,冷却加入10%NaOH 溶液中和至中性,取2滴中性液于一干净试管中,加入0.5mLFehling 试剂I 和0.5mL Fehling 试剂II ,振荡,水浴加热。
现象:
结论:
8. 纤维素试验
取小团棉花与一干净试管中,加入2-3滴浓硫酸,用玻璃埲搅拌成糊状,水浴加热,得一亮棕色溶液,取其一半,用10%NaOH溶液中和,再加入2-3滴Fehling试剂I,振荡后,水浴加热。
现象:
结论:
建议性质实验报告的书写:
六.实验注意事项:
1.Tollens试剂必须临时配制,进行实验时切忌用灯焰直接加热,以免发生爆炸。
实验完毕后,应加入少许硝酸,立即煮沸洗去银镜。
2.硝酸银溶液与皮肤接触,立即形成难于洗去的黑色金属银,故滴加和摇荡时应小心操作。
七.思考题:
1.托伦试剂为什么要在临用时才配置?土伦实验完毕后,应该加入硝酸少许,立刻煮沸洗去银镜,为什么?
2. 如何用简单的化学方法鉴定下列化合物?
环己烷环己烯环己醇苯甲醛丙酮
3.成败关键:银镜反应的实验效果主要在银氨溶液的配制和试管的清洁度。
氨水用量的大小也是一
个关键,直接加热或热水浴温度过高都可以造成银镜的质量问题。
另外在新制的Cu(OH)2中碱的用量与实验结果关系也至为密切。
与饱和NaHSO3溶液加成
取4支干燥试管,各加入2mL新配置的饱和亚硫酸氢钠溶液,然后分别滴入8-10滴正丁醛、苯
甲醛、丙酮、苯乙酮,用力振荡,使混合均匀,将试管置于冰水浴中冷却(为什么?),观察有无沉
淀析出。
记录沉淀析出所需时间。
现象:
解释:
结论:
与2,4—二硝基苯肼作用:
取4支干燥试管,各加入2mL2,4—二硝基苯肼试剂,然后分别滴入2-3滴正丁醛、苯甲醛、丙酮、苯乙酮,用力振荡,使混合均匀,观察有无沉淀析出。
如无,静置数分钟后观察;再无,可微热30秒后再振荡,冷却后再观察。
现象:
解释:
结论:
特别注意:2,4—二硝基苯肼的使用,其毒性较大,应该在通风橱内取用。
注意安全!
α-氢原子的反应----碘仿反应
取5支试管,各加入1mL碘—碘化钾溶液,并分别加入5滴40%乙醛水溶液、丙酮、乙醇、正丁醇、苯乙酮。
然后再一边滴加10%氢氧化钠溶液,一边振荡试管,直到碘的颜色接近消失。
反应液呈微黄色为止。
观察有无黄色沉淀。
如无沉淀,可在600C水浴中温热2-3分钟。
冷却后观察。
比较各试管所得结果。
现象:
解释:
结论:
与弱氧化剂反应:
(1)银镜反应
在洁净的试管(试管一定要干净,否则看不到银镜)中,加入4mL 2%硝酸银溶液和2滴5%氢氧化钠溶液,然后一边滴加2%氨水,一边振摇试管,直到生成棕色氧化银沉淀刚好溶解为止。
此即为托伦(Tollens)试剂。
将此溶液平均分置4支干净试管中,分别加入3-4滴甲醛、乙醛、丙酮、苯甲醛,振荡均匀,静置后观察。
如无变化,可在40—500C水浴中温热,有银镜生成,表明是醛类化合物。
现象:
解释:
结论:
(2)与费林试剂反应:
将费林溶液I和费林溶液II各4mL加入到大试管中(费林溶液I和费林溶液II,用时,再等量混合),混合均匀。
然后平均分装到4支小试管中,分别在4支小试管中加入10滴甲醛、乙醛、丙酮、苯甲醛。
振荡混匀,置于沸水浴中,加热3-5分钟,注意观察色变化及有无红色沉淀析出。
现象:
解释:
结论:。
