教学重点苯环上亲核取代反应、芳香族重氮盐的性质和应用、胺的
苯环上的亲电子取代反应及定位效应与反应活性正文

苯环上的亲电子取代反应及定位效应与反应活性一、苯的亲电子取代反应1.简介苯环平面的上下有π电子云①,与σ键②相比,平行重叠的π电子云结合较疏松,因此在反应中苯环可充当一个电子源,与缺电子的亲电试剂③发生反应,类似于烯烃中π键④的性质。
但是苯环中π电子又有别于烯烃,π键共振形成的大π键⑤使苯环具有特殊的稳定性,反应中总是保持苯环的结构。
苯的结构特点决定苯的化学性质,它容易发生亲电子取代反应⑥。
π键σ键电子云2.卤代⑦苯与卤素作用,在三卤化铁(FeX3)的催化下,得到卤代苯,同时放出卤化氢。
(1)与Cl2反应FeCl3+Cl2+HCl反应2FeBr3+ Br2 +HBr(3)与I2反应:碘活性不够,只有与非常活泼的芳香化合物才能发生取代反应。
目前采用氧化剂将碘氧化为碘正离子后直接引入苯环。
HNO3I+I286%)铁屑与卤素反应产生三卤化铁,起到同样的作用。
3Br2+2Fe 2FeBr3苯与氯、溴的取代反应应用十分广泛。
其公认的反应历程是首先缺电子的FeX3与卤素络合,促进卤素之间σ键的极化、异裂。
FeX3+X2X++FeX4-带正电的卤素进攻苯环的π电子。
形成苯碳正离子中间体,类似于烯烃的亲电加成,这一步是速度决定步骤+二卤代烃+X-也可失去质子,恢复苯的骨架。
苯的稳定性起了决定作用,得到取代而不是加成产物。
-H++FeX3+HX3.硝化苯与浓硝酸和浓硫酸的混合物(称混酸)反应,生成硝基苯。
浓H2SO4+HNO3(浓)(98%)+H2O50℃其反应历程如下:浓硫酸的酸性比硝酸的强,它作为酸提供质子(H+),硝酸作为碱提供氢氧根(OH-),去掉一分子水,产生硝基正离子,硝基正离子具有很强的亲电子性,与苯发生亲电子取代反应。
若采用浓硝酸,则反应速度明显减慢,这是由于浓硝酸中仅存在少量的硝基正离子。
4.磺化不同浓度的硫酸与苯反应的速度不同,浓度越高反应越快。
含三氧化硫的发烟硫酸的反+H2SO4(7%SO3(52%)+H2O磺化反应也是亲电取代反应,通常认为亲电试剂是三氧化硫。
教学重点苯环上亲核取代反应芳香族重氮盐的性质和应用胺的

CH3NHCH 3
NH2
H3C
NH 2
2、氮原子上所连有的基团不同时,小的作为基团
CH3CH2NHCH3
N(CH3)2
3、二元或多元伯胺
NH 2CH 2CH 2NH 2
NH 2(CH 2)6NH 2
H2N
NH 2
4、复杂的胺可以看成烃的衍生物
H H3C C CH2CH(CH 3)2
1、红外光谱:伯胺两个尖峰;仲胺单个尖峰
2、宽峰具有仲氢交换实验
14.2.3 胺的立体化学
1、胺上的三个基团均不一样
:
N
N
:
2、季铵盐或碱
R
N+
R'''
R''
R' x-
R
+N R''' R' R'' x-
14.2.4 胺的化学性质 一、胺的碱性
RNH2 + HCl
NaOH RNH3Cl
1、应用:分离和提纯 2、胺的碱性比较
CH2 N(CH3)2 H2O2
OCH2 N(CH3)2
CH2 + (CH3)2NOH
Ph
H
N(CH3)2
H
CH3
Ph
H2O2
Ph OH +N(CH3)2
H
CH3
Ph
H C
Ph
Ph
C
+ (CH3)2NOH
CH3
八、异腈的生成
KOH
RNH2 + CHCl3
RNC
EtOH
九、芳胺的特性
芳香族取代反应

活性药物成分的合成
某些芳香族取代反应可以用于直接合成活性药物成分,如合成抗高血压药物、抗 抑郁药物等。
工业生产中的芳香族取代反应
染料工业
芳香族取代反应在染料工业中应用广泛,如偶氮染料、荧光 染料的合成。
高分子材料
芳香族化合物可用于合成高分子材料,如聚酯、聚酰胺等, 这些高分子材料在工业生产中有广泛应用。
分类
根据取代基和环的大小,芳香族化合 物可以分为苯环化合物、萘环化合物 、蒽环化合物等。
芳香族化合物的结构特点
共轭体系
芳香族化合物具有环状共轭体系,这是其具有特殊性质的关键结构特点。
π电子
芳香族化合物中的π电子数决定了其化学性质,尤其是取代反应的性质。
芳香族化合物的性质
稳定性
芳香族化合物在化学反应中相对稳定,不易发 生氧化或还原反应。
当底物中的取代基具有给电子效应时, 有利于亲核取代反应;而具有吸电子 效应时,则有利于亲电取代反应。
反应条件的影响
温度
01
温度对芳香族取代反应的影响显著,高温有利于提高反应速率,
但可能导致副反应增多。
压力
02
对于某些需要特定压力条件的芳香族取代反应,压力的变化会
对反应产生影响。
溶剂
03
溶剂的极性和酸碱性等性质会影响反应物的溶解度和反应中间
常见的自由基取代反应有烯烃的氧化、烷烃的氧化等。
04构的影响
取代基的性质
底物中取代基的性质对芳香族取代反 应的速度和选择性有重要影响。一般 来说,取代基的电子效应和立体效应 都会影响取代反应的进程。
取代基的电子效应
取代基的立体效应
含氮化合物-芳香族重氮盐

分离提纯
结晶法
利用芳香族重氮盐在特定条件下 结晶析出的特性,通过过滤、洗 涤、干燥等步骤进行分离提纯。
萃取法
利用芳香族重氮盐在不同溶剂中 的溶解度差异,通过萃取剂将芳 香族重氮盐从一种溶剂转移到另 一种溶剂中,从而实现分离提纯。
色谱法
利用色谱原理,通过固定相和流 动相的相互作用,使芳香族重氮 盐在色谱柱上分离,再收集所需 组分。该方法具有分离效果好、
02
CHAPTER
芳香族重氮盐的结构与性质
结构特征
1
芳香族重氮盐是一类含氮的有机化合物,其分子 中含有重氮基团(-N=N-)。
2
重氮基团中的氮原子与芳香环直接相连,芳香烃基和重氮 基团组成,具有平面结构。
物理性质
01
芳香族重氮盐一般为黄色或橙色晶体,具有较高的熔点和沸点。
安全与环保的未来发展
研发新型安全环保的芳香族重氮盐替代品,减少 对环境和健康的危害。
加强生产过程中的安全环保监管,推广清洁生产 技术和循环经济模式。
提高公众对芳香族重氮盐安全环保问题的认识, 加强宣传教育,促进社会共治。
THANKS
谢谢
含氮化合物-芳香族重氮盐
目录
CONTENTS
• 芳香族重氮盐的概述 • 芳香族重氮盐的结构与性质 • 芳香族重氮盐的制备与分离 • 芳香族重氮盐的反应机理与合成应用 • 芳香族重氮盐的安全性与环保问题
01
CHAPTER
芳香族重氮盐的概述
定义与特性
定义
芳香族重氮盐是一类含氮化合物,具 有芳香族结构和重氮盐特性。
芳香族重氮盐的应用领域
有机合成
芳香族重氮盐是重要的有机合成 中间体,可以用于合成多种有机 化合物,如染料、药物、农药等。
《有机化学》课程教学大纲
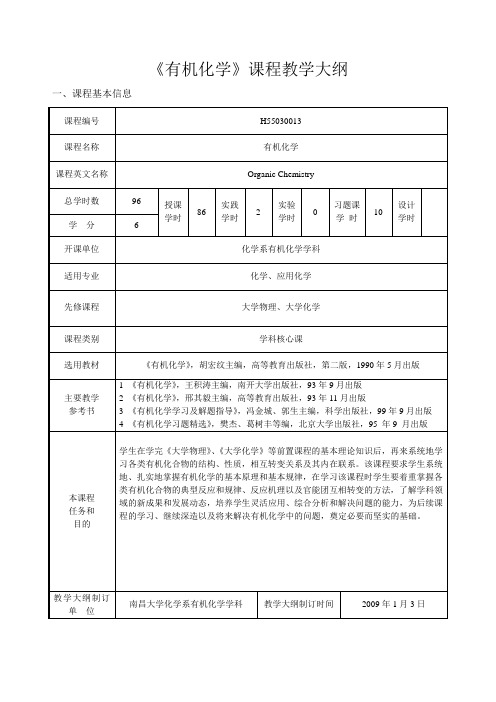
《有机化学》课程教学大纲一、课程基本信息二、课程内容及基本要求说明:1 本大纲主要根据(胡宏纹主编)《有机化学》拟定。
各章要求分“熟悉掌握”“一般掌握”和“了解”三类,分别以符号“* * *”“* *”“*”来表示。
2 本课程分两学期进行,上学期周学时“3”,总学时48学时,下学期周学时“4”,总学时48学时。
第一章绪论(2 学时)基本要求:一、了解有机化学发展史、主要任务和学习方法;二、了解有机化合物的基本特点、分类和反应类型;三、了解共价健的本质,掌握共价健的属性;四、掌握下述名词术语:有机化学;同分异构现象;分子间作用力;Van der walls力;官能团。
§1.1 有机化合物及有机化学 * *§1.2 有机化合物的结构* *§1.3 原子轨道和分子轨道*§1.4 有机化合物的结构* * *§1.5 官能团和有机化合物的分类 * * *第二章烷烃(4学时)基本要求:一、掌握构象的表示方法和典型的构象ap, sp, sc, ac的稳定性分析;二、了解饱和碳原子的sp3杂化轨道与烷基自由基的sp2杂化轨道的形成与构型;三、着重掌握烷烃的自由基取代反应(卤代反应)的基本规律和反应机理,烷烃的物理性质。
四、弄清下列概念:同系列与同分异构;构造异构与链异构;T.S与活泼中间体;扭转张力与Van der Walls张力;Newman投影式与透视式;活性与选择性§2.1 烷烃的同系列和异构* * *§2.2 烷烃的命名* * *§2.3 烷烃的构象* * *§2.4 烷烃的物理性质 * * *§2.5 烷烃的反应* * *§2.6 烷烃的卤代* * *§2.7 烷烃的来源和制备*第三章环烷烃(2学时)基本要求:一、掌握环烷烃的顺反异构现象;二、掌握环烷烃的性质和构象,环丙烷和环已烷的构象及其理论解释;三、掌握下述概念:氢化热与燃烧热;Baeyer张力;船式与椅式构象。
教学重点: 苯环上亲核取代反应、芳香族重氮盐的性 质和应用、胺的

Br
3、磺化反应
NH2 + H2SO4 + NH3HSO4 180-190oC NH2 NH3+
4、硝化反应
NH2 + (CH3CO)2O
SO3H
NHCOCH3
SO3-
NHCOCH3 HNO3/HOAc NHCOCH3 NO2 HNO3/Ac2O NHCOCH3 NO2 OH-/H2O
NH2
NO2 NH2 NO2
PhNO2 NaOH Zn PhNHNHPh H3C NHNH CH3
NO2 NaOH Zn CH3
3、苯环上的亲核取代反应
Cl NO2 OHH2O OH NO2
1、历程
Cl NO2 Nu-
Cl _
Nu NO2
Nu -ClNO2
2、条件:在离去基团的邻位或对位有强的吸电子基时,例如 硝基,离去基团才可以离去顺利发生苯环上的亲核取代反应
OCH3 OH
2、被卤素取代
1)被卤素氟取代
NH2 NaNO2 H2SO4 CH3 N2+HSO4HBF4 CH3 CH3 CH3 N2+BF4F
2)其它卤素
CuX,KX KI ArN2+HSO4ArX ArI
3、被氰基取代
CH3
HCN, CuCN ArN2+HSO4ArCN
Br
COOH Br
CH3
第十四章 含氮化合物
1、重点掌握苯环上亲核取代反应和历程;
2、重点掌握芳香族重氮盐的性质和应用;
3、重点掌握胺的化学性质和制备; 4、重点掌握烯胺的制备和应用; 5、重点掌握常见的分子重排反应和历程和应用; 6、掌握胺的命名;
教学重点: 苯环上亲核取代反应、芳香族重氮盐的性 质和应用、胺的化学性质和制备、烯胺的
芳香族重氮和偶氮化合物

contents
目录
• 芳香族重氮化合物 • 芳香族偶氮化合物 • 芳香族重氮和偶氮化合物的应用 • 芳香族重氮和偶氮化合物的安全性 • 芳香族重氮和偶氮化合物的未来发展
01 芳香族重氮化合物
定义与性质
定义
芳香族重氮化合物是一类含有重氮基 (-N=N-)的有机化合物,通常由芳 香烃与氮气在低温下反应制得。
重氮和偶氮染料在染料工业中占据重要地位,它们可以与其 他染料进行拼色,以获得更丰富的颜色效果。此外,这些染 料还具有良好的耐光、耐气候和耐化学性能,能够保持颜色 的持久性。
荧光材料
荧光材料是利用芳香族重氮和偶氮化合物的发光特性而制成的。这些化合物能够 在紫外光的激发下发出可见光,因此被广泛应用于荧光灯、显示器、夜光涂料等 领域。
性质
芳香族重氮化合物具有不稳定性,容 易分解,同时具有明显的颜色特征, 通常为深红色或紫色。
合成方法
芳香烃与氮气反应
在低温条件下,将芳香烃与氮气反应, 通过重氮化反应制得芳香族重氮化合 物。
重氮盐的转化
通过重氮盐的转化,如取代、加成等 反应,可以得到不同结构的芳香族重 氮化合物。
反应机理
重氮化反应机理
重氮和偶氮荧光材料具有高亮度和高色彩饱和度的特点,能够提供清晰、鲜艳的 显示效果。此外,这些材料还具有良好的化学和热稳定性,能够在不同的环境和 条件下保持稳定的发光性能。
高分子材料
芳香族重氮和偶氮化合物在合成高分子材料方面也具有重 要作用。这些化合物可以通过与其他单体进行聚合反应, 制备出具有特定结构和性能的高分子材料。
重氮和偶氮高分子材料具有良好的耐热、耐腐蚀和耐磨损 性能,被广泛应用于工程塑料、涂料、粘合剂等领域。此 外,这些材料还具有良好的加工性能,能够通过注塑、挤 出、涂覆等工艺进行加工成型。
重氮盐和苯反应

重氮盐和苯反应全文共四篇示例,供读者参考第一篇示例:重氮盐和苯反应是一种重要的有机化学反应,常用于合成芳香胺和其衍生物。
重氮盐是一种含有-N≡N基团的化合物,通常由芳胺和硝酸反应制得。
而苯是一种典型的芳香烃,具有良好的亲电性,容易发生亲电芳香取代反应。
将重氮盐和苯在碱性条件下反应,可以生成芳香胺,是一种重要的合成方法。
在这种反应中,首先需要制备重氮盐。
通常选择在酸性条件下将芳胺和硝酸反应,制备出重氮盐。
硝酸与芳胺反应生成硝基芳胺,而硝基芳胺在强酸或碱性条件下脱去一个羟基,形成重氮盐。
重氮盐是一个亲电试剂,可以参与芳烃的亲电芳香取代反应。
将制备好的重氮盐与苯在碱性条件下反应,会发生重要的SNAr反应。
在反应过程中,重氮盐中的-N≡N基团与苯环发生亲电取代反应,在苯环上引入一个新的取代基。
最常见的情况是在苯环上引入一个氨基取代基,形成芳香胺。
这种反应是在室温下进行的,反应条件温和,适用于各类芳胺和苯衍生物。
重氮盐和苯反应是一个非常重要的合成方法,可以制备各种不同结构的芳香胺。
通过改变芳胺和苯的结构,可以合成出不同取代基的芳胺,具有很好的化学反应性和生物活性。
重氮盐和苯反应也可以制备出含氮杂环的化合物,可用于合成含氮杂环的药物分子。
重氮盐和苯反应在有机合成中具有广泛的应用。
除了制备芳胺外,还可以用于合成具有重要生物活性的化合物,如杀虫剂、染料和药物。
这种反应也为有机化学研究提供了一个重要的手段,可以揭示有机反应的机理及其应用。
重氮盐和苯反应是一种重要的有机合成反应,具有广泛的应用前景。
通过这种反应,可以高效地合成芳香胺和其衍生物,为有机化学合成和生物医药领域带来了新的发展机遇。
希望通过持续的研究和探索,可以进一步拓展这种反应的应用范围,为化学科学的发展做出更大的贡献。
第二篇示例:重氮盐是一种含有-N≡N基团的化合物,通常是通过重氮化反应制备而成的。
重氮盐在有机化学中具有重要的应用价值,可以用于合成各种重要的有机化合物。
《有机化学(1)-1,2》(化学、应化类专业)教学大纲

《有机化学(I)》(化学、应化类专业)教学大纲一、课程基本信息课程名称(中、英文): 有机化学(Ⅰ)-1[Organic Chemistry(Ⅰ)-1]有机化学(Ⅰ)-2[Organic Chemistry(Ⅰ)-2]课程号(代码): 20308730,20308630课程类别: 类级平台课程,必修课学时:48x2学分:3x2先修课程:《无机化学》、《分析化学》基本面向:化学专业、应用化学专业二、教学目的及要求化学,应用化学和材料化学专业的学生,在学完《高等数学》、《普通物理》、《无机化学》、《分析化学》等前置课程的基本理论知识后,进入有机化学的学习。
该课程要求学生系统地、扎实地掌握有机化学的基本原理和基本规律,为后续课程的学习、继续深造以及将来解决有机化学中的问题、奠定必要而坚实的基础,同时能进一步加强解决问题和分析问题能力的培养。
在学习该课程时学生要着重掌握各类有机化合物的结构、命名、物理性质、光谱性质、常用制备方法和用途,尤其是着重掌握各类有机化合物的结构特征和关键反应,把握规律、抓住机理、将官能团互相转变的方法和碳碳键的形成与断裂的方法形成互联网络,同时专注有机化学中的立体化学问题,才能达到有机化学的教学之目的。
三、教学内容1 绪论(4学时)基本要求:一、了解有机化学的发展史、主要任务和学习方法;二、了解有机化合物的基本特点、分类和反应类型;三、了解共价健的本质,掌握共价健的属性,熟悉利用键能数据推算反应的焓变;四、掌握下述名词术语:有机化学;同分异构现象;分子间作用力;Van der walls力;官能团1-1 有机化学的由来和发展1-2 有机化合物的特点:分子结构和组成(同分异构现象,结构的表示方法);理化性质1-3 共价键的键参数:键能、键长、键角;键的极性与诱导效应;键的可极化性1-4 共价键的断裂方式与有机反应的类型1-5 有机化合物的分类1-6 学习有机化学的目的和学习方法2 烷烃(4学时)基本要求:一、掌握构象的表示方法和典型的构象ap, sp, sc, ac的稳定性分析;二、了解饱和碳原子的sp3杂化轨道与烷基自由基的sp2杂化轨道的形成与构型;三、着重掌握烷烃的自由基取代反应(卤代反应)的基本规律(区域选择性)和反应机理(自由基反应),了解烷烃的物理性质。
亲和取代反应总结

亲核取代反应总结1、反应定义:亲核取代反应(Nucleophilic Substitution Reaction)是指有机分子中与碳相连的某原子或基团被作为亲核试剂的某原子或基团取代的反应。
在反应过程中,取代基团提供形成新键的一对电子,而被取代的基团则带着旧键的一对电子离去.2、反应意义:这类反应是有机化学中非常重要的一类反应,不论在理论研究中还是在有机合成实际中都是极其有用的一类反应.3、反应分类:亲核取代反应的主要类型为脂肪族饱和碳上的亲核取代反应,即饱和卤代烃与亲核试剂的取代反应,较特殊结构的有苄基卤代物、烯丙基卤代物亲核反应。
其他类型还包括与酰氯、磺酸酯、磺酰卤、卤代苯等的取代反应.从电荷类型来分,亲核取代反应只能有四种类型:(1)中性底物和负离子亲核试剂反应(2)中性底物和中性亲核试剂反应(3)正离子底物和负离子亲核试剂反(4)正离子底物和中性亲核试剂反应亲核试剂包括有机和无机两类分子或离子:无机类亲核试剂:OH—、CN-、X—、H2O、NH3等有机类亲核试剂:ROH、RO—、PhO-、RS—、RMgX、RCOO-等4、反应机理类型分类:(1)双分子亲核取代反应(S N2)有两种分子参与了决定反应速率关键步骤的亲核取代反应称为双分子亲核取代反应。
反应过程中,亲核试剂从反应物离去基团的背面向与它连接的碳原子进攻,先与碳原子形成比较弱的键,同时离去基团与碳原子的键有一定程度的减弱,两者与碳原子成一条直线,碳原子上另外三个键逐渐由伞形转变成平面,这需要消耗能量,即活化能,当反应进行和达到能量最高状态即过渡态后,亲核试剂与碳原子之间的键开始形成,碳原子与离去基团之间的键断裂,碳原子上三个键由平面向另一边偏转,整个过程犹如大风将雨伞由里向外反转一样,这时就要释放能量,形成产物,S N2反应机理一般式表示为:Nu-+R X[Nuδ-···R···Xδ- ] NuR+X—例如,溴甲烷与OH—的水解反应:(2)单分子亲核取代反应(S N1)只有一种分子参与了决定反应速率关键步骤的亲核取代反应称为单分子亲核取代反应,反应中,反应物首先解离成碳正离子与带负电荷的离去基团,这个过程需要能量,是控制反应速率的一步,即慢的一部.当分子解离后,碳正离子马上与亲核试剂结合,速率极快,是快的一步。
高等有机化学_8.1 芳环上的亲电和亲核取代反应

合成???
Cl
Br
CH3
CH3
CH3
(CH3CO)2Cl
NO2
NH2
NHCOCH3
CH3
CH3
CH3
CuBr
Cl NHCOCH3 CH3
4. Fridel-Crafts反应 (1) 烃基化
亲电试剂产生
R Cl+AlCl3 δ + δ R Cl AlCl3
R++AlCl4-
ROH+H X
X-
ROH2
H2O
R+
R CH CH2+H2SO4
+ HSO RCHCH3 4
催化剂活性
AlCl3>FeCl3>SbCl5>SnCl4>BF3>TiCl4>ZnCl2
第八章 芳环上的亲电 和亲核取代反应
H H C H
C C
C C
H C H H
芳环上离域的π电子的作用,易于发生 亲电取代反应,只有当芳环上引入了强吸电 子基团,才能发生亲核取代反应。
8.1 芳环的亲电取代反应
8.1.1 芳环上的亲电取代历程 1. 亲电试剂的产生
HNO3+2H2SO4 NO2++H3O++2HSO4亲电试剂
O AlCl3
B. 酚的酰化是Fries重排
O PhOH+CH3COOH PhOCCH3
ACl3 PhNO2
OH
C O
CH3
O O
+
CH3 C Cl
AlCl3
C CH3
+
HCl
O CH3 C
O O AlCl3 C CH3 O
+
CH3 C O
+ CH3 C OH
(完整版)苯环上取代反应的定位规则

(完整版)苯环上取代反应的定位规则苯环上原有的取代基对新导入取代基有影响,这种影响包括反应活性和进入位置两个方面。
通常,苯环上原有的第一取代基称为定位基,从大量实验事实的分析总结中发现,定位基的定位作用遵循一定的规律,这一规律称为苯环上亲电取代反应定位规律(又称定位规则)。
下面分别讨论定位基的类型;定位规则的理论解释;二元取代苯的定位规律;定位规律的应用。
(一)定位基的类型1.邻、对位定位基。
这类定位基的结构特征是定位基中与苯环直接相连的原子不含不饱和键(芳烃基例外),不带正电荷,且多数具有未共用电子对。
常见的邻、对位定位基及其反应活性(相对苯而言)如下:强致活基团:―NH2(―NHR,―NR2),―OH中致活基团:―OCH3(―OR),―NHCOCH3(-NHCOR)弱致活基团:―ph(―Ar),―CH3(-R)弱致钝基团:―F,―Cl,―Br,―I这类定位基多数使亲电取代反应较苯容易进行,但卤素例外。
2.间位定位基。
这类定位基的结构特征是定位基中与苯环直接相连的原子一般都含有不饱和键(-CX3例外)或带正电荷。
常见的间位定位基及其定位效应从强到弱顺序如下:―N+H3,―N+R3,―NO2,―CF3,―CCl3,―CN,―SO3H,―CO H,―COR,―COOH,―COOR,―CONH2等。
这类定位基属致钝基团,通常使苯环上亲电取代反应较苯难进行,且排在越前面的定位基,定位效应越强,反应也越难进行。
(二)定位规则的理论解释苯环上的取代反应是亲电取代反应。
因此,从反应活性的角度分析,凡有助于提高苯环上电子云密度的基团,就能使苯环活化,反应活性提高;反之,凡是使环上电子云密度降低的基团,就能使苯环钝化,反应活性降低。
从反应位置的角度分析,当苯环上没有取代基时,环上六个碳原子的电子云密度是均等的;但当苯环上有取代基时,由于取代基的电子效应沿着苯环共轭体系传递。
在环上出现了出现了电子云密度的疏密交替分布现象。
基础有机化学第18章 含氮芳香化合物 芳香亲核取代反应

O
O
两个等价的共振式,结构是对称的。
O
结构示意图
N O
硝基的电子效应 强吸电子基团(吸电子诱导、吸电子共轭) 硝基的同分异构体 芳香硝基化合物与亚硝酸(芳基)酯是同分异 构体。 Ar-NO2,Ar-O-N=O
18.2
1 物理性质:
物理性质、光谱性质和用途
一元芳香硝基化合物是高沸点液体,多数是有机物的良好溶剂。 不溶于水,有毒。 二元和多元芳香硝基化合物为无色或黄色固体。
桑德迈耳的反应机理(自由基取代反应)
N N
+ CuCl
+
络合
N N
+
CuCl
电子转移
+ CuCl2 + N2
CuCl2 提供一个Cl
Cl
+ CuCl
18.9.2 重氮盐的水解(SNlAr)
定义:重氮盐在酸性水溶液中分解成酚和放出氮 气的反应。
[ C6H5-N N ] HSO4 + H2O
+
-
H+
NH3
加压
Br NO2 RNH2
NH2
O2N NH-R NO2
O2N
3 用霍夫曼重排制备
O NH
NaOH + X2
COONa NH2
O
芳胺的化学性质
18.5 芳香胺的氧化
18.6 芳香胺芳环上的亲电取代反应
18.7 联苯胺重排
18.8 重氮化反应
18.5 芳香胺的氧化
N上有氢的芳香胺极易氧化,随氧化剂种类及
NH2
O CH3CCl
NHCOCH 3
O CH3CH2CH2CCl AlCl3 CS2
最新第18章 含氮芳香化合物 芳香亲核取代反应ppt课件

C2H5 NH2
CH3
NH-NH 1C4 H3
CH3
+
NH-NH
CH3
H2N 14CH3
H2N 14CH3
NH2 + H2N
CH3
CH3 NH2
CH3 NH2
极化过渡态理论
NHNH
H+
+
NH2
+
NH2
+
NH 2
+
NH 2
H
+
NH 2
H
+
NH 2
H
H
H
H
- H+
H2N
NH 2
联苯胺
18.8 重氮化反应
NH-OH
苯基羟胺 (中 间还原产物)
Fe + HCl
NH2
苯胺 最终还原产物
(2)双分子还原反应
2PhNO2
Zn
As2O3 NaOH +H2O
O-
+
Ph-N=N-Ph
氧化偶氮苯
NaOH
H2O
Ph-N=N-Ph Zn +NaOH +H2O Ph-NH-NH-Ph
偶氮苯
氢化偶氮苯
18.3.2 芳环上的亲核取代反应(SN2Ar)
芳胺的制备
1 硝基化合物的还原
Fe + HCl (产率 100%)
NO2
or H2/Cu 加压 (产率 95%)
NH2
2 芳环的亲核取代
OH O 2 N
NH3
加压
NH2
R N2H
B r
O 2 N
N O 2
3 用霍夫曼重排制备
含氮化合物-芳香族重氮盐

重氮化反应
通过重氮化反应,芳香胺与硫酸和亚 硝酸钠反应生成芳香族重氮硫酸盐, 再通过放出氮气得到芳香族重氮盐。
02 芳香族重氮盐的化学反应
偶合反应
偶合反应是芳香族重氮盐最重要的反应之一,通常在弱酸性介质中进行。偶合反应 的产物是偶氮化合物,广泛应用于染料、颜料和荧光剂等工业领域。
重氮盐的偶合反应可以通过加入不同的取代基来控制,例如在偶合反应中加入硝基 可以生成具有特定结构的偶氮化合物。
药物合成中的应用
在药物合成中,芳香族重氮盐可用于合成多种药物,如抗菌药、抗炎药、抗肿瘤 药等。
重氮盐参与的药物合成方法具有高选择性、高效率和高产率等特点,为药物研发 和生产提供了重要的技术支持。
其他应用领域
除了上述应用领域外,芳香族重氮盐还可用于合成荧光增 白剂、植物生长调节剂等,以及在分析化学中用于测定芳 香烃和芳香胺等化合物的含量。
来获得所需的产物。
还原反应Biblioteka 还原反应是将芳香族重氮盐中的 重氮基团还原成氨基的过程。
还原反应通常采用化学还原剂或 催化氢化等方法进行,还原剂可 以是硫酸亚铁、亚硫酸氢钠等。
还原反应的产物是芳香族氨基化 合物,具有较高的工业价值,可
用于合成多种有机化合物。
其他反应
1
除了上述三种主要的化学反应外,芳香族重氮盐 还可以发生其他一些反应,例如氧化、水解和光 解等。
致癌性
部分芳香族重氮盐被认为具有致癌 性,可能增加患癌症的风险。
储存与运
储存条件
01
芳香族重氮盐应储存在阴凉、干燥、通风良好的地方,远离火
源和热源。
运输要求
02
在运输过程中,应使用专用的危险品运输工具,并配备安全防
护措施,如防爆设备、灭火器等。
教学重点: 苯环上亲核取代反应、芳香族重氮盐的性 质和应用、胺的42页PPT

56、极端的法规,就是极端的不公。 ——西 塞罗 57、法律一旦成为人们的需要,人们 就不再 配享受 自由了 。—— 毕达哥 拉斯 58、法律规定的惩罚不是为了私人的 利益, 而是为 了公共 的利益 ;一部 分靠有 害的强 制,一 部分靠 榜样的 效力。 ——格 老秀斯 59、假如没有法律他们会更快乐的话 ,那么 法律作 为一件 无用之 物自己 就会消 灭。— —洛克
60、人民的幸福是至高无个的法。— —西塞 罗
66、节制使快乐增加并使享受加强。 ——德 谟克利 特 67、今天应做的事没有做,明天再早也 是耽误 了。——裴斯 泰洛齐 68、决定一个人的一生,以及整个命运 的,只 是一瞬 之间。 ——歌 德 69、懒人无法享受休息之乐。——拉布 克 70、浪费时间是一桩大罪过。——卢梭
芳香族化合物亲核取代反应机理以及在有机合成中的应用

芳香族化合物亲核取代反应机理以及在有机合成中的应用化学化工学院院化学S0702 3071302012 王辰孖我们生活的环境中,有机物随处可见。
可以说,有机物在我们的生活中有着举足轻重的地位。
那么,什么是有机物呢?从定义的角度来说,有机物通常指含碳元素的化合物,或碳氢化合物及其衍生物总称为有机物。
还有几点需要说明的是:1.有机物是有机化合物的简称。
目前人类已知的有机物达3000多万种,数量远远超过无机物。
2.早先,人们已知的有机物都从动植物等有机体中取得,所以把这类化合物叫做有机物。
到19世纪20年代,科学家先后用无机物人工合成许多有机物,如尿素、醋酸、脂肪等等,从而打破有机物只能从有机体中取得的观念。
但是,由于历史和习惯的原因,人们仍然沿用有机物这个名称。
3.有机物一般难溶于水,易溶于有机溶剂,熔点较低。
绝大多数有机物受热容易分解、容易燃烧。
有机物的反应一般比较缓慢,并常伴有副反应发生。
4.有机物种类繁多,可分为烃和烃的衍生物两大类。
根据有机物分子中所含官能团的不同,又分为烷、烯、炔、芳香烃和醇、醛、羧酸、酯等等。
根据有机物分子的碳架结构,还可分成开链化合物、碳环化合物和杂环化合物三类。
5.有机物对人类的生命、生活、生产有极重要的意义。
地球上所有的生命体中都含有大量有机物。
有机物的种类繁多,其中非常重要的一类就是芳香族化合物。
历史上曾将一类从植物胶中取得的具有芳香气味的物质称为芳香族化合物。
但根据气味分类并不科学,现在是指分子中至少含有一个苯环,具有与开链化合物或脂环烃不同的独特性质(称芳香性,aromaticity)的一类化合物。
如苯、萘、蒽及其衍生物。
苯是最简单、最典型的代表。
它们容易发生亲电取代反应、对热比较稳定,主要来自石油和煤焦油。
有些分子中虽然不含苯环但也具有与苯相似的芳香性的化合物,称为非苯芳香化合物,如草盐、薁等。
分子中含有苯环的有机化合物叫做芳香族化合物。
它包括芳香烃及其衍生物,如卤代芳香烃、芳香族硝基化合物、芳香醇、芳香酸等。
第十二章苯环的亲电取代,亲核取代反应及芳环取代基的反应
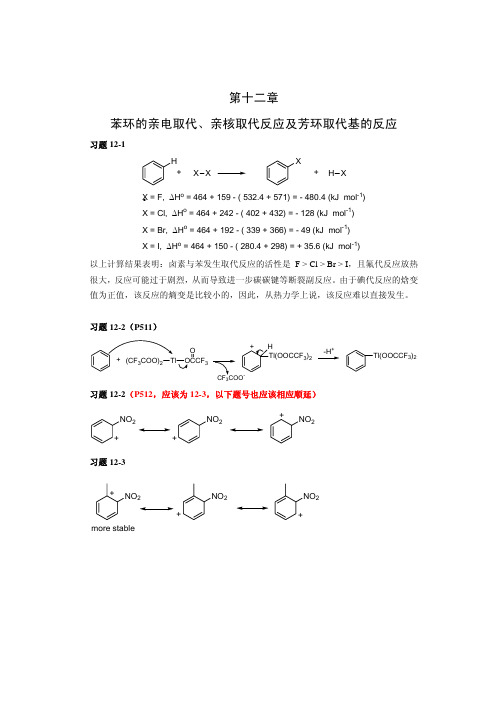
CHO
CHO
(3)
O + (CH3)2CHCH2CCl
AlCl3
O CCH2CH(CH3)2
HNO3 H2SO4
· 248 ·
O
第十一章
氧化还原反应
NH2NH2, OH-
NO2
(4) CH3
Br2
NO2
CH2Br
CN
CH2C N
H2 Pd/C
CH2CH2NH2
(CH3CO)2O
hv
CH2CH2NHCOCH3
OCH2COC2H5 (1) > OCOC2H5 > CH2OC2H5 > COOC2H5
NHCH2CH3 (2) >
NHCH2COCH3 >
NHCOCH3 >
CONHCH3
· 246 ·
CH2OH (3) > COCH3
第十一章
氧化还原反应
NO2 >
CN >
OCOCH3 (4) >
Cl >
COCH3 >
第十二章 苯环的亲电取代、亲核取代反应及芳环取代基的反应
习题 12-1
H + X X X + H X
X = F, ΔHo = 464 + 159 - ( 532.4 + 571) = - 480.4 (kJ mol-1) X = Cl, ΔHo = 464 + 242 - ( 402 + 432) = - 128 (kJ mol-1) X = Br, ΔHo = 464 + 192 - ( 339 + 366) = - 49 (kJ mol-1) X = I, ΔHo = 464 + 150 - ( 280.4 + 298) = + 35.6 (kJ mol-1)
《有机化学Ⅲ》课程教学大纲
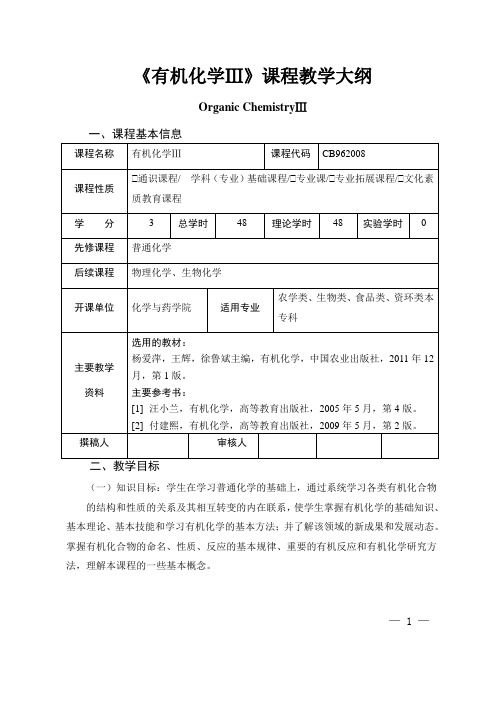
《有机化学Ⅲ》课程教学大纲Organic ChemistryⅢ一、课程基本信息通识课程/学科(专业)基础课程/ 专业课/ 专业拓展课程/ 文化素质教育课程(一)知识目标:学生在学习普通化学的基础上,通过系统学习各类有机化合物的结构和性质的关系及其相互转变的内在联系,使学生掌握有机化学的基础知识、基本理论、基本技能和学习有机化学的基本方法;并了解该领域的新成果和发展动态。
掌握有机化合物的命名、性质、反应的基本规律、重要的有机反应和有机化学研究方法,理解本课程的一些基本概念。
— 1 —(二)能力目标:培养学生具有初步对化学反应的整体轮廓,一定的分析与推理能力,为学习有关后继课程和从事专业技术工作打下坚实的基础。
(三)素质目标:根据“以就业为导向,以教学为中心的”的教育理念,注重培养学生的工程实践能力、技术应用能力和社会适应能力。
三、基本要求1. 了解有机化学发生、发展的历史,认识有机化学与生产、生活的密切关系;2. 掌握各类有机化合物的命名法,同分异构现象、结构和性质,重要合成方法以及它们之间的相互关系;3. 掌握电子效应(诱导效应、共轭效应和超共轭效应)理论,并运用这些理论来说明结构与性能关系;4. 掌握各种活性中间体产生、结构、活性和在有机反应过程中的作用;5. 能应用自由基取代反应、亲核取代、亲电取代、亲核和亲电加成等反应的历程来解释有机反应原理和反应速度;6. 初步掌握立体化学的基本知识和基本理论,能够理解有些有机反应中的立体化学现象;7. 了解各类有机化合物的来源,工业制法及其主要用途。
四、教学内容与学时分配第一章绪论2学时知识点:有机化合物与有机化学;有机化合物的特点;有机化合物结构的表示方法;共价键的基本概念;有机化学中的酸碱理论;有机化合物的分类。
本章小结:1.了解有机化合物和有机化学的涵义;2.掌握有机化合物的特性;有机化合物共价键理论、断裂方式和有机反应的类型;有机化合物的分类方法。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
PhN2+
PhN-NO
ON
N(CH3)2
七、叔胺的氧化和热消除反应
1、定义:叔胺在过氧化氢存在条件下,可以被氧化成氧
化叔胺,有的氧化叔胺在加热条件下生成烯烃和羟基胺
2、历程
H
RC R'
-O + N(CH3)2
C R''
R'''
R C
R'
R''
C
+ (CH3)2NOH
R'''
3、反应的规律:顺式共平面,霍夫曼规则
O
NH2
H2SO4
+ MnO2
NO2
2、卤代反应
O
NH2 + Br2
CH3
NH2
Br
Br
NH2 COOH
Br
如需要单取代的需要降低苯环的活性
NH2 +
(CH3CO)2O
NHCOCH3 Br2
NHCOCH3
NH2
OH-/H2O
Br
Br
3、磺化反应
NH2
+ H2SO4
N+H3HSO4-
NH2
180-190oC
四、酰基化反应
PhNH2 + (CH3CO)2O K2CO3
PhNHCOCH3
1) H3O+ 2)OH-, H2O
PhNH2
应用:保护氨基:例如对溴苯胺的制备(苯)
五、磺酰化反应
Et3N PhSO2Cl + RNH2
应用:鉴别不同的胺
PhSO2NHR
RNH2
TsNHR
TsN- R Na+
R2NH + TsCl
二、命名 1、简单的胺:烃基的名称+胺
CH3NHCH3
NH2
H3C
NH2
2、氮原子上所连有的基团不同时,小的作为基团
CH3CH2NHCH3
N(CH3)2
3、二元或多元伯胺
NH2CH2CH2NH2
NH2(CH2)6NH2
H2N
NH2
4、复杂的胺可以看成烃的衍生物
H H3C C CH2CH(CH3)2
4、硝化反应
NH2 + (CH3CO)2O
SO3H NHCOCH3
NH3+ SO3-
NHCOCH3
HNO3/HOAc NHCOCH3
HNO3/Ac2O
NO2
NHCOCH3 NO2
OH-/H2O
NH2
NO2 NH2
14.1 硝基化合物
14.1.1 脂肪族硝基化合物的性质
1、还原反应:硝基化合物在铁和盐酸作用下可以被还原成胺
HCl
RNO2 + Fe
RNH2
2、α -氢的酸性
O R CH2
OH-
H
O-
O-
R C N+
H
O-
假酸式
酸式结构
3、 有α -氢的硝基化合物与羰基化合物的缩合反应
PhCHO + CH3NO2 3HCHO + CH3NO2
PhCHO + O2N
OH H2O OH -
NO 2
CH 3
PhCH=CHNO 2 (HOCH 2)C-NO 2
OH H2O
H3C
CH 3 CH=CH
14.1.2 芳香族硝基化合物的性质
1、还原反应
HCl
PhNO2 + Fe
PhNH2
2、碱性还原:芳香族硝基化合物在锌粉和氢氧化钠条件
1、红外光谱:伯胺两个尖峰;仲胺单个尖峰
2、宽峰具有仲氢交换实验
14.2.3 胺的立体化学
1、胺上的三个基团均不一样
: :
N
N
2、季铵盐或碱
R
R''' N +
R''
R' x-
R
+N R''' R' R'' x-
14.2.4 胺的化学性质 一、胺的碱性
RNH2 + HCl
NaOH RNH3Cl
RNH2 + H2O + NaCI
NH2
5、季胺化合物的命名
Et4N+Br-
Me3N+C16H33Br-
溴化四乙胺 三甲基十六烷基氢氧化铵
14.2.2 胺的物理和光谱性质
一、物理性质
1、低级的脂肪氨为气体 2、碳原子数目相同的胺沸点伯胺>仲胺>叔胺
CH3CH2CH2NH2
CH3CH2NHCH3
3、芳香族的胺有毒
(CH3)3N
二、光谱性质
CH2 N(CH3)2 H2O2
OCH2 N(CH3)2
CH2 + (CH3)2NOH
Ph
H N(CH3)2 H CH3
Ph
H2O2
Ph OH +N(CH3)2 H CH3
Ph
H C
Ph
Ph
C
+ (CH3)2NOH
CH3
八、异腈的生成
KOH
RNH2 + CHCl3
RNC
EtOH
九、芳胺的特性
1、氧化(在氧化反应中氨基需要保护)
1、应用:分离和提纯 2、胺的碱性比较
1)气态脂肪族胺
(CH3)3N > (CH 3)2NH > CH 3NH2 > NH 3
2)在水溶液中脂肪族胺的比较
H +
OH2
R N H OH2
H OH2
+ H OH2 RN
R H OH2
3)芳香族胺的碱性比较
NH3 > PhNH2 >Ph2NH
R3NH OH2
第十四章 含氮化合物
1、重点掌握苯环上亲核取代反应和历程; 2、重点掌握芳香族重氮盐的性质和应用; 3、重点掌握胺的化学性质和制备; 4、重点掌握烯胺的制备和应用; 5、重点掌握常见的分子重排反应和历程和应用; 6、掌握胺的命名;
教学重点: 苯环上亲核取代反应、芳香族重氮盐的性 质和应用、胺的化学性质和制备、烯胺的 制备和应用分子重排反应和历程和应用。
TsNR2 NaOH
N. R.
R3N
N. R.
该试剂称为兴斯堡试剂
N. R.
六、与亚硝酸的反应
1、脂肪族胺
RNH2 + HNO2 R2NH + HNO2 R3N + HNO2
2、芳香族胺
RN2+ H2O ROH + N2 R2N-NO R3NHNO2
PhNH2 + HNO2 Ph2NH + HNO2 N(CH3)2 + HNO2
下,可以被还原成氢化偶氮苯及其衍生物
PhNO2
NaOH Zn
PhNHNHPh
H3C
NO2 NaOH Zn
CH3
NHNH CH3
3、苯环上的亲核取代反应
Cl NO2
OHH2O
OH NO2
1、历程
Cl
Cl Nu
NO2 Nu-
_ NO2 -Cl-
Nu NO2
2、条件:在离去基团的邻位或对位有强的吸电子基时,例如
硝基,离去基团才可以离去顺利发生苯环上的亲核取代反应
Cl
OCH3
Cl
NO2
CHONa
NO2
NO2
KF
F NO2
NO2
CH3OH
NO2 Cl
NO2
NO2
PhNH2
DMF
NHPh NO2
NO2
14.2 胺
NO2
NO2
14.2.1 胺的分类和命名
一、分类 1、氨的衍生物 伯胺、仲胺、叔胺、季铵盐、季铵碱 2、烃基的不同 3、氨基的数目不同
NH2 >
NH2 >
NH2 >
NH2
NH2
>
OCH3
CH3
H
Cl
NO2
二、一级或二级胺的酸性
(C2H5)2NH + C6H5Li
LiN(C2H5)2 + C6H6
(i-Pr)2NH + C4H9Li
(i-Pr)2NLi
二异丙基氨基锂
三、胺的烷基化
RNH2
+
NaOH R'X
RNHR'
RNR'3OH-
