化学选修四提纲
高二化学知识点总结选修四

高二化学知识点总结选修四高二化学知识点总结选修四目录第一章、化学反应与能量第一节、化学反应与能量的变化第二节、燃烧热、能源第三节、化学反应热的计算第二章、化学反应速率和化学平衡第一节、化学反应速率第二节、影响化学反应速率的因素第三节、化学平衡第四节、化学反应进行的方向第三章、水溶液中的离子平衡第一节、弱电解质的电离第二节、水的电离和溶液的酸碱性第三节、盐类的水解第四节、难溶电解质的溶解平衡第四章、电化学基础第一节、原电池第二节、化学电源第三节、电解池第四节、金属的电化学腐蚀与防护第一章化学反应与能量考点1:吸热反应与放热反应1、吸热反应与放热反应的区别特别注意:反应是吸热还是放热与反应的条件没有必然的联系,而决定于反应物和生成物具有的总能量(或焓)的相对大小。
2、常见的放热反应①一切燃烧反应;②活泼金属与酸或水的反应;③酸碱中和反应;④铝热反应;⑤大多数化合反应(但有些化合反应是吸热反应,如:N2+O2=2NO,CO2+C=2CO 等均为吸热反应)。
3、常见的吸热反应①Ba(OH)2·8H2O与NH4Cl反应;②大多数分解反应是吸热反应③等也是吸热反应;④水解反应考点2:反应热计算的依据1.根据热化学方程式计算反应热与反应物各物质的物质的量成正比。
2.根据反应物和生成物的总能量计算ΔH=E生成物-E反应物。
3.根据键能计算ΔH=反应物的键能总和-生成物的键能总和。
4.根据盖斯定律计算化学反应的反应热只与反应的始态(各反应物)和终态(各生成物)有关,而与反应的途径无关。
即如果一个反应可以分步进行,则各分步反应的反应热之和与该反应一步完成时的反应热是相同的。
温馨提示:①盖斯定律的主要用途是用已知反应的反应热来推知相关反应的反应热。
②热化学方程式之间的“+”“-”等数学运算,对应ΔH也进行“+”“-”等数学计算。
5.根据物质燃烧放热数值计算:Q(放)=n(可燃物)×|ΔH|。
第二章化学反应速率与化学平衡考点1:化学反应速率1、化学反应速率的表示方法___________。
高中选修四化学知识要点总结

高中选修四化学知识要点总结选修四化学基础知识1、化学反应的反应热(1)反应热的概念:当化学反应在一定的温度下进行时,反应所释放或吸收的热量称为该反应在此温度下的热效应,简称反应热。
用符号Q表示。
(2)反应热与吸热反应、放热反应的关系:Q>0时,反应为吸热反应;Q<0时,反应为放热反应。
(3)反应热的测定测定反应热的仪器为量热计,可测出反应前后溶液温度的变化,根据体系的热容可计算出反应热,计算公式如下:Q=-C(T2-T1)式中C表示体系的热容,T1、T2分别表示反应前和反应后体系的温度。
实验室经常测定中和反应的反应热。
2、化学反应的焓变(1)反应焓变物质所具有的能量是物质固有的性质,可以用称为“焓”的物理量来描述,符号为H,单位为kJ·mol-1。
反应产物的总焓与反应物的总焓之差称为反应焓变,用ΔH表示。
(2)反应焓变ΔH与反应热Q的关系。
对于等压条件下进行的化学反应,若反应中物质的能量变化全部转化为热能,则该反应的反应热等于反应焓变,其数学表达式为:Qp=ΔH=H(反应产物)-H(反应物)。
(3)反应焓变与吸热反应,放热反应的关系:ΔH>0,反应吸收能量,为吸热反应。
ΔH<0,反应释放能量,为放热反应。
(4)反应焓变与热化学方程式:把一个化学反应中物质的变化和反应焓变同时表示出来的化学方程式称为热化学方程式,如:H2(g)+O2(g)=H2O(l);ΔH(298K)=-285.8kJ·mol-1书写热化学方程式应注意以下几点:①化学式后面要注明物质的聚集状态:固态(s)、液态(l)、气态(g)、溶液(aq)。
②化学方程式后面写上反应焓变ΔH,ΔH的单位是J·mol-1或kJ·mol-1,且ΔH后注明反应温度。
③热化学方程式中物质的`系数加倍,ΔH的数值也相应加倍。
3、反应焓变的计算(1)盖斯定律对于一个化学反应,无论是一步完成,还是分几步完成,其反应焓变一样,这一规律称为盖斯定律。
选修四知识点(反应热、化学平衡、电化学)
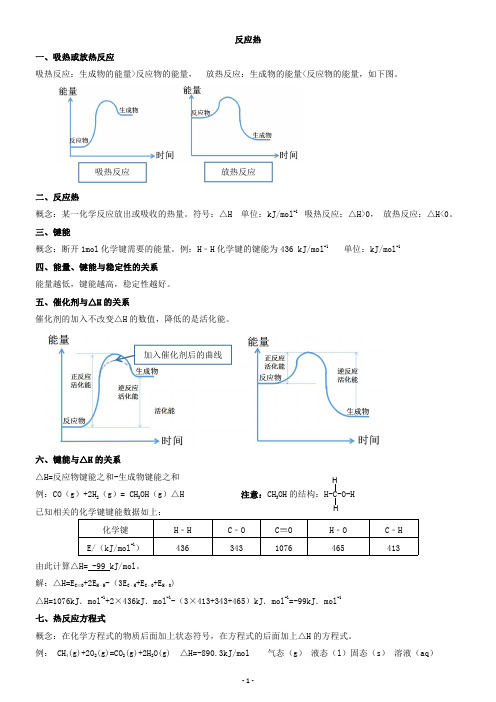
反应热一、吸热或放热反应吸热反应:生成物的能量>反应物的能量,放热反应:生成物的能量<反应物的能量,如下图。
二、反应热概念:某一化学反应放出或吸收的热量。
符号:△H 单位:kJ/mol -1吸热反应:△H>0,放热反应:△H<0。
三、键能概念:断开1mol 化学键需要的能量。
例:H﹣H 化学键的键能为436kJ/mol -1单位:kJ/mol -1四、能量、键能与稳定性的关系能量越低,键能越高,稳定性越好。
五、催化剂与△H 的关系催化剂的加入不改变△H 的数值,降低的是活化能。
六、键能与△H 的关系△H=反应物键能之和-生成物键能之和例:CO(g)+2H 2(g)=CH 3OH(g)△H 注意:CH 3OH 的结构:H-C-O-H已知相关的化学键键能数据如上:化学键H﹣H C﹣O C≡O H﹣O C﹣H E/(kJ/mol -1)4363431076465413由此计算△H=-99kJ/mol。
解:△H=E C≡O +2E H﹣H -(3E C﹣H +E C﹣O +E H﹣O )△H=1076kJ.mol -1+2×436kJ.mol -1-(3×413+343+465)kJ.mol -1=-99kJ.mol -1七、热反应方程式概念:在化学方程式的物质后面加上状态符号,在方程式的后面加上△H 的方程式。
例:CH 4(g)+2O 2(g)=CO 2(g)+2H 2O(g)△H=-890.3kJ/mol气态(g)液态(l)固态(s)溶液(aq)放热反应吸热反应加入催化剂后的曲线HH注意:热反应方程式中可以出现分数的。
例:C 6H 5COOH(s)+15/2O 2(g)=7CO 2(g)+3H 2O(l)△H=-3226KJ/mol八、燃烧热概念:指1mol 物质与氧气进行完全燃烧反应生成稳定氧化物时放出的热量。
例:H 2(g)+1/2O 2(g)=H 2O(l);ΔH=-285.8kJ·mol -1注意:稳定氧化物有:H 2O(l)CO 2(g)SO 2(g)不稳定氧化物有:H 2O(g)CO(g)CO 2(l)SO 2(l)九、盖斯定律计算△H例:利用CO 2和CH 4重整可制合成气(主要成分为CO、H 2),已知重整过程中部分反应的热化学方程式为:①CH 4(g)═C(s)+2H 2(g)△H=+75.0KJ•mol -1②CO 2(g)+H 2(g)═CO(g)+H 2O(g)△H=+41.0KJ•mol -1③CO(g)+H 2(g)═C(s)+H 2O(g)△H=-131.0KJ•mol -1反应CO 2(g)+CH 4(g)═2CO(g)+2H 2(g)的△H=+247KJ/mol.解:盖斯定律利用①+②-③计算得到反应计算过程:①+②:CO 2(g)+H 2(g)+CH 4(g)═C(s)+2H 2(g)+CO(g)+H 2O(g)△H=(75.0+41.0)KJ•mol -1左右各消去一个H 2得到:CO 2(g)+CH 4(g)═C(s)+H 2(g)+CO(g)+H 2O(g)△H=(75.0+41.0)KJ•mol -1上式-③得到:CO 2(g)-CO(g)+CH 4(g)-H 2(g)═H 2(g)+CO(g)△H=(75.0+41.0-131.0)KJ•mol -1整理得到:CO 2(g)+CH 4(g)═2CO(g)+2H 2(g)△H=+247KJ/mol.化学平衡一、活化分子、活化能、单位体积内的活化分子数、活化分子百分数活化分子:普通分子吸收能量后的分子活化能:普通分子变成活化分子需要的能量活化分子百分数:例:容器中含有活化分子数为1O,普通分子数为30,则活化分子百分数为:10/(10+30)×100%=25%单位体积内的活化分子数:例:2L 容器中含有活化分子数为1O,则单位体积内的活化分子数为:10/2=5增大反应速率的本质是:提高活化分子百分数或单位体积内的活化分子数。
【人教版】高中化学选修4知识点总结:第二章化学反应速率和化学平衡

第二章化学反应速率和化学平衡一、化学反应速率(1)化学反应速率的概念化学反应速率是用来衡量化学反应进行的快慢程度的物理量。
(2)化学反应速率的表示方法对于反应体系体积不变的化学反应,通常用单位时间内反应物或生成物的物质的量浓度的变化值表示。
某一物质A的化学反应速率的表达式为:式中——某物质A的浓度变化,常用单位为mol·L-1。
——某段时间间隔,常用单位为s,min,h。
υ——物质A的反应速率,常用单位是mol·L-1·s-1,mol·L-1·s-1等。
(3)化学反应速率的计算规律①同一反应中不同物质的化学反应速率间的关系同一时间内,用不同的物质表示的同一反应的反应速率数值之比等于化学方程式中各物质的化学计量数之比。
②化学反应速率的计算规律同一化学反应,用不同物质的浓度变化表示的化学反应速率之比等于反应方程式中相应的物质的化学计量数之比,这是有关化学反应速率的计算或换算的依据。
(4)化学反应速率的特点①反应速率不取负值,用任何一种物质的变化来表示反应速率都不取负值。
②同一化学反应选用不同物质表示反应速率时,可能有不同的速率数值,但速率之比等于化学方程式中各物质的化学计量数之比。
③化学反应速率是指时间内的“平均”反应速率。
小贴士:①化学反应速率通常指的是某物质在某一段时间内化学反应的平均速率,而不是在某一时刻的瞬时速率。
②由于在反应中纯固体和纯液体的浓度是恒定不变的,因此对于有纯液体或纯固体参加的反应一般不用纯液体或纯固体来表示化学反应速率。
其化学反应速率与其表面积大小有关,而与其物质的量的多少无关。
通常是通过增大该物质的表面积(如粉碎成细小颗粒、充分搅拌、振荡等)来加快反应速率。
③对于同一化学反应,在相同的反应时间内,用不同的物质来表示其反应速率,其数值可能不同,但这些不同的数值表示的都是同一个反应的速率。
因此,表示化学反应的速率时,必须指明是用反应体系中的哪种物质做标准。
【人教版】高中化学选修4知识点总结:第二章化学反应速率和化学平衡

第二章化学反应速率和化学平衡一、化学反应速率课标要求1、掌握化学反应速率的含义及其计算2、了解测定化学反应速率的实验方法要点精讲1、化学反应速率(1)化学反应速率的概念化学反应速率是用来衡量化学反应进行的快慢程度的物理量。
(2)化学反应速率的表示方法对于反应体系体积不变的化学反应,通常用单位时间内反应物或生成物的物质的量浓度的变化值表示。
某一物质A的化学反应速率的表达式为:式中——某物质A的浓度变化,常用单位为mol·L-1。
——某段时间间隔,常用单位为s,min,h。
υ——物质A的反应速率,常用单位是mol·L-1·s-1,mol·L-1·s-1等。
(3)化学反应速率的计算规律①同一反应中不同物质的化学反应速率间的关系同一时间内,用不同的物质表示的同一反应的反应速率数值之比等于化学方程式中各物质的化学计量数之比。
②化学反应速率的计算规律同一化学反应,用不同物质的浓度变化表示的化学反应速率之比等于反应方程式中相应的物质的化学计量数之比,这是有关化学反应速率的计算或换算的依据。
(4)化学反应速率的特点①反应速率不取负值,用任何一种物质的变化来表示反应速率都不取负值。
②同一化学反应选用不同物质表示反应速率时,可能有不同的速率数值,但速率之比等于化学方程式中各物质的化学计量数之比。
③化学反应速率是指时间内的“平均”反应速率。
小贴士:①化学反应速率通常指的是某物质在某一段时间内化学反应的平均速率,而不是在某一时刻的瞬时速率。
②由于在反应中纯固体和纯液体的浓度是恒定不变的,因此对于有纯液体或纯固体参加的反应一般不用纯液体或纯固体来表示化学反应速率。
其化学反应速率与其表面积大小有关,而与其物质的量的多少无关。
通常是通过增大该物质的表面积(如粉碎成细小颗粒、充分搅拌、振荡等)来加快反应速率。
③对于同一化学反应,在相同的反应时间内,用不同的物质来表示其反应速率,其数值可能不同,但这些不同的数值表示的都是同一个反应的速率。
人教版高中化学选修4第二章《化学反应速率和化学平衡》知识点归纳
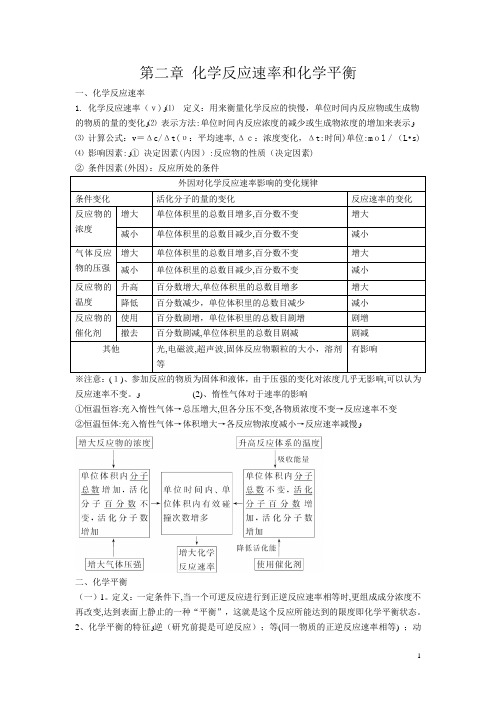
第二章化学反应速率和化学平衡一、化学反应速率1. 化学反应速率(v)ﻭ⑴定义:用来衡量化学反应的快慢,单位时间内反应物或生成物的物质的量的变化ﻭ⑵表示方法:单位时间内反应浓度的减少或生成物浓度的增加来表示ﻭ⑶计算公式:v=Δc/Δt(υ:平均速率,Δc:浓度变化,Δt:时间)单位:mol/(L•s)⑷影响因素:ﻭ①决定因素(内因):反应物的性质(决定因素)②条件因素(外因):反应所处的条件外因对化学反应速率影响的变化规律条件变化活化分子的量的变化反应速率的变化反应物的浓度增大单位体积里的总数目增多,百分数不变增大减小单位体积里的总数目减少,百分数不变减小气体反应物的压强增大单位体积里的总数目增多,百分数不变增大减小单位体积里的总数目减少,百分数不变减小反应物的温度升高百分数增大,单位体积里的总数目增多增大降低百分数减少,单位体积里的总数目减少减小反应物的催化剂使用百分数剧增,单位体积里的总数目剧增剧增撤去百分数剧减,单位体积里的总数目剧减剧减其他光,电磁波,超声波,固体反应物颗粒的大小,溶剂等有影响※注意:(1)、参加反应的物质为固体和液体,由于压强的变化对浓度几乎无影响,可以认为反应速率不变。
ﻭ(2)、惰性气体对于速率的影响①恒温恒容:充入惰性气体→总压增大,但各分压不变,各物质浓度不变→反应速率不变②恒温恒体:充入惰性气体→体积增大→各反应物浓度减小→反应速率减慢ﻭ二、化学平衡(一)1。
定义:一定条件下,当一个可逆反应进行到正逆反应速率相等时,更组成成分浓度不再改变,达到表面上静止的一种“平衡”,这就是这个反应所能达到的限度即化学平衡状态。
2、化学平衡的特征ﻭ逆(研究前提是可逆反应);等(同一物质的正逆反应速率相等) ;动(动态平衡)定(各物质的浓度与质量分数恒定);变(条件改变,平衡发生变化) 3、判断平衡的依据判断可逆反应达到平衡状态的方法和依据例举反应mA(g)+nB(g)C(g)+qD(g)混合物体系中各成分的含量①各物质的物质的量或各物质的物质的量的分数一定平衡②各物质的质量或各物质质量分数一定平衡③各气体的体积或体积分数一定平衡④总体积、总压力、总物质的量一定不一定平衡正、逆反应速率的关系①在单位时间内消耗了mmolA同时生成m molA,即V(正)=V(逆)平衡②在单位时间内消耗了nmolB同时消耗了p molC,则V(正)=V(逆)平衡③V(A):V(B):V(C):V(D)=m:n:p:q,V(正)不一定等于V(逆)不一定平衡④在单位时间内生成nmolB,同时消耗了q molD,因均指V(逆)不一定平衡压强①m+n≠p+q时,总压力一定(其他条件一定) 平衡②m+n=p+q时,总压力一定(其他条件一定) 不一定平衡混合气体平均相对分子质量Mr①Mr一定时,只有当m+n≠p+q时平衡②Mr一定时,但m+n=p+q时不一定平衡温度任何反应都伴随着能量变化,当体系温度一定时(其他不变)平衡体系的密度密度一定不一定平衡其他如体系颜色不再变化等平衡(二)影响化学平衡移动的因素1、浓度对化学平衡移动的影响(1)影响规律:在其他条件不变的情况下,增大反应物的浓度或减少生成物的浓度,都可以使平衡向正方向移动;增大生成物的浓度或减小反应物的浓度,都可以使平衡向逆方向移动(2)增加固体或纯液体的量,由于浓度不变,所以平衡不移动ﻭ(3)在溶液中进行的反应,如果稀释溶液,反应物浓度减小,生成物浓度也减小,V正减小,V逆也减小,但是减小的程度不同,总的结果是化学平衡向反应方程式中化学计量数之和大的方向移动。
化学选修4_水溶液中的离子平衡_知识点归纳

第三章 水溶液中的离子平衡一、弱电解质的电离1、定义:电解质:在水溶液中或熔化状态下能导电的化合物,叫电解质。
非电解质:在水溶液中或熔化状态下都不能导电的化合物。
强电解质:在水溶液里全部电离成离子的电解质。
弱电解质: 在水溶液里只有一部分分子电离成离子的电解质。
2、电解质与非电解质本质区别:电解质——离子化合物或共价化合物 非电解质——共价化合物注意:①电解质、非电解质都是化合物 ②SO 2、NH 3、CO 2等属于非电解质 ③强电解质不等于易溶于水的化合物(如BaSO 4不溶于水,但溶于水的BaSO 4全部电离,故BaSO 4 为强电解质)——电解质的强弱与导电性、溶解性无关。
3、电离平衡:在一定的条件下,当电解质分子电离成 离子的速率 和离子结合成 时,电离过程就达到了 平衡状态 ,这叫电离平衡。
4、影响电离平衡的因素:A 、温度:电离一般吸热,升温有利于电离。
B 、浓度:浓度越大,电离程度 越小 ;溶液稀释时,电离平衡向着电离的方向移动。
C 、同离子效应:在弱电解质溶液里加入与弱电解质具有相同离子的电解质,会 减弱 电离。
D 、其他外加试剂:加入能与弱电解质的电离产生的某种离子反应的物质时,有利于电离。
9、电离方程式的书写:用可逆符号 弱酸的电离要分布写(第一步为主)10、电离常数:在一定条件下,弱电解质在达到电离平衡时,溶液中电离所生成的各种离子物质单质化合物电解质非电解质: 非金属氧化物,大部分有机物 。
如SO 3、CO 2、C 6H 12O 6、CCl 4、CH 2=CH 2……强电解质: 强酸,强碱,大多数盐 。
如HCl 、NaOH 、NaCl 、BaSO 4弱电解质: 弱酸,弱碱,极少数盐,水 。
如HClO 、NH 3·H 2O 、Cu(OH)2、H 2O ……混和物纯净物浓度的乘积,跟溶液中未电离的分子浓度的比是一个常数。
叫做电离平衡常数,(一般用Ka表示酸,Kb表示碱。
高中化学选修4化学反应原理知识点总结(史上最全)

选修4知识点汇总一、焓变反应热1.反应热:一定条件下,一定物质的量的反应物之间完全反应所放出或吸收的热量2.焓变(ΔH)的意义:在恒压条件下进行的化学反应的热效应(1).符号:△H (2).单位:kJ/mol 3.产生原因:化学键断裂——吸热化学键形成——放热放出热量的化学反应。
(放热>吸热)△H 为“-”或△H<0吸收热量的化学反应。
(吸热>放热)△H为“+”或△H>0☆常见的放热反应:①所有的燃烧反应②酸碱中和反应③大多数的化合反应④金属与酸的反应⑤生石灰和水反应⑥浓硫酸稀释、氢氧化钠固体溶解等☆常见的吸热反应:①晶体Ba(OH) 2•8H2O与NH4Cl ②大多数的分解反应③以H2、CO、C为还原剂的氧化还原反应④铵盐溶解等二、热化学方程式书写化学方程式注意要点:①热化学方程式必须标出能量变化。
②热化学方程式中必须标明反应物和生成物的聚集状态(g,l,s分别表示固态,液态,气态,水溶液中溶质用aq表示)③热化学反应方程式要指明反应时的温度和压强。
④热化学方程式中的化学计量数可以是整数,也可以是分数⑤各物质系数加倍,△H加倍;反应逆向进行,△H改变符号,数值不变例:CH4 (g) + 2O2 (g) = CO2 (g) + 2H2O (l) ΔH=-890.3 kJ/mol三、燃烧热1.概念:25℃,101kPa时,1mol纯物质完全燃烧生成稳定的化合物时所放出的热量。
燃烧热的单位用kJ/mol表示。
※注意以下几点:①研究条件:25℃,101kPa ②反应程度:完全燃烧,产物是稳定的氧化物。
(C→CO2,S→SO2,H→H2O,只能在氧气中燃烧。
)③燃烧物的物质的量:1mol④研究内容:放出的热量。
(ΔH<0,单位kJ/mol)四、中和热(常考选择:判断热化学方程式是否正确)1.概念:在稀溶液中,酸跟碱发生中和反应而生成1molH2O,这时的反应热叫中和热。
2.强酸与强碱的中和反应其实质是H+和OH-反应,其热化学方程式为:H+(aq) +OH-(aq) =H2O(l) ,ΔH=-57.3kJ/mol3.弱酸或弱碱电离要吸收热量,所以它们参加中和反应时的中和热小于57.3kJ/mol。
化学必修四知识点概括

化学必修四知识点概括【篇一:化学必修四知识点概括】高中化学选修4知识点总结第1章、化学反应与能量转化化学反应的实质是反应物化学键的断裂和生成物化学键的形成,化学反应过程中伴随着能量的释放或吸收.一、化学反应的热效应1、化学反应的反应热(1)反应热的概念:当化学反应在一定的温度下进行时,反应所释放或吸收的热量称为该反应在此温度下的热效应,简称反应热.用符号q表示.(2)反应热与吸热反应、放热反应的关系.q>0时,反应为吸热反应;q<0时,反应为放热反应.(3)反应热的测定测定反应热的仪器为量热计,可测出反应前后溶液温度的变化,根据体系的热容可计算出反应热,计算公式如下:q=-c(t2-t1)式中c表示体系的热容,t1、t2分别表示反应前和反应后体系的温度.实验室经常测定中和反应的反应热.2、化学反应的焓变(1)反应焓变(3)反应焓变与吸热反应,放热反应的关系:(4)反应焓变与热化学方程式:书写热化学方程式应注意以下几点:①化学式后面要注明物质的聚集状态:固态(s)、液态(l)、气态(g)、溶液(aq).3、反应焓变的计算(1)盖斯定律对于一个化学反应,无论是一步完成,还是分几步完成,其反应焓变一样,这一规律称为盖斯定律.(2)利用盖斯定律进行反应焓变的计算.对任意反应:aa+bb=cc+dd二、电能转化为化学能——电解1、电解的原理(1)电解的概念:在直流电作用下,电解质在两上电极上分别发生氧化反应和还原反应的过程叫做电解.电能转化为化学能的装置叫做电解池.(2)电极反应:以电解熔融的nacl为例:阳极:与电源正极相连的电极称为阳极,阳极发生氧化反应:2cl-→cl2↑+2e-.阴极:与电源负极相连的电极称为阴极,阴极发生还原反应:na++e-→na.总方程式:2nacl(熔)2na+cl2↑的应用(1)电解食盐水制备烧碱、氯气和氢气.阳极:2cl-→cl2+2e-阴极:2h++e-→h2↑总反应:2nacl+2h2o2naoh+h2↑+cl2↑(2)铜的电解精炼.粗铜(含zn、ni、fe、ag、au、pt)为阳极,精铜为阴极,cuso4溶液为电解质溶液.阳极反应:cu→cu2++2e-,还发生几个副反应zn→zn2++2e-;ni→ni2++2e-fe→fe2++2e-au、ag、pt等不反应,沉积在电解池底部形成阳极泥.阴极反应:cu2++2e-→cu(3)电镀:以铁表面镀铜为例待镀金属fe为阴极,镀层金属cu为阳极,cuso4溶液为电解质溶液.阳极反应:cu→cu2++2e-阴极反应: cu2++2e-→cu三、化学能转化为电能——电池1、原电池的工作原理(1)原电池的概念:把化学能转变为电能的装置称为原电池.(2)cu-zn原电池的工作原理:如图为cu-zn原电池,其中zn为负极,cu为正极,构成闭合回路后的现象是:zn片逐渐溶解,cu片上有气泡产生,电流计指针发生偏转.该原电池反应原理为:zn失电子,负极反应为:zn→zn2++2e-;cu得电子,正极反应为:2h++2e-→h2.电子定向移动形成电流.总反应为:zn+cuso4=znso4+cu.(3)原电池的电能若两种金属做电极,活泼金属为负极,不活泼金属为正极;若一种金属和一种非金属做电极,金属为负极,非金属为正极.2、化学电源(1)锌锰干电池负极反应:zn→zn2++2e-;正极反应:2nh4++2e-→2nh3+h2;(2)铅蓄电池负极反应:pb+so42-pbso4+2e-正极反应:pbo2+4h++so42-+2e-pbso4+2h2o放电时总反应:pb+pbo2+2h2so4=2pbso4+2h2o.充电时总反应:2pbso4+2h2o=pb+pbo2+2h2so4.(3)氢氧燃料电池负极反应:2h2+4oh-→4h2o+4e-正极反应:o2+2h2o+4e-→4oh-电池总反应:2h2+o2=2h2o3、金属的腐蚀与防护(1)金属腐蚀金属表面与周围物质发生化学反应或因电化学作用而遭到破坏的过程称为金属腐蚀.(2)金属腐蚀的电化学原理.生铁中含有碳,遇有雨水可形成原电池,铁为负极,电极反应为:fe→fe2++2e-.水膜中溶解的氧气被还原,正极反应为:o2+2h2o +4e-→4oh-,该腐蚀为“吸氧腐蚀”,总反应为:2fe+o2+2h2o=2fe(oh)2,fe(oh)2又立即被氧化:4fe(oh)2+2h2o+o2=4fe(oh)3,fe(oh)3分解转化为铁锈.若水膜在酸度较高的环境下,正极反应为:2h++2e-→h2↑,该腐蚀称为“析氢腐蚀”.(3)金属的防护金属处于干燥的环境下,或在金属表面刷油漆、陶瓷、沥青、塑料及电镀一层耐腐蚀性强的金属防护层,破坏原电池形成的条件.从而达到对金属的防护;也可以利用原电池原理,采用牺牲阳极保护法.也可以利用电解原理,采用外加电流阴极保护法.第2章、化学反应的方向、限度与速率(1、2节)原电池的反应都是自发进行的反应,电解池的反应很多不是自发进行的,如何判定反应是否自发进行呢?一、化学反应的方向1、反应焓变与反应方向2、反应熵变与反应方向3、焓变与熵变对反应方向的共同影响二、化学反应的限度1、化学平衡常数(1)对达到平衡的可逆反应,生成物浓度的系数次方的乘积与反应物浓度的系数次方的乘积之比为一常数,该常数称为化学平衡常数,用符号k表示 .(2)平衡常数k的大小反映了化学反应可能进行的程度(即反应限度),平衡常数越大,说明反应可以进行得越完全.(3)平衡常数表达式与化学方程式的书写方式有关.对于给定的可逆反应,正逆反应的平衡常数互为倒数.(4)借助平衡常数,可以判断反应是否到平衡状态:当反应的浓度商qc 与平衡常数kc相等时,说明反应达到平衡状态.2、反应的平衡转化率(1)平衡转化率是用转化的反应物的浓度与该反应物初始浓度的比值来表示.如反应物a的平衡转化率的表达式为:(2)平衡正向移动不一定使反应物的平衡转化率提高.提高一种反应物的浓度,可使另一反应物的平衡转化率提高.(3)平衡常数与反应物的平衡转化率之间可以相互计算.3、反应条件对化学平衡的影响(1)温度的影响升高温度使化学平衡向吸热方向移动;降低温度使化学平衡向放热方向移动.温度对化学平衡的影响是通过改变平衡常数实现的.(2)浓度的影响增大生成物浓度或减小反应物浓度,平衡向逆反应方向移动;增大反应物浓度或减小生成物浓度,平衡向正反应方向移动.温度一定时,改变浓度能引起平衡移动,但平衡常数不变.化工生产中,常通过增加某一价廉易得的反应物浓度,来提高另一昂贵的反应物的转化率.(3)压强的影响(4)勒夏特列原理由温度、浓度、压强对平衡移动的影响可得出勒夏特列原理:如果改变影响平衡的一个条件(浓度、压强、温度等)平衡向能够减弱这种改变的方向移动.【例题分析】例1、已知下列热化学方程式:写出feo(s)被co还原成fe和co2的热化学方程式 .解析:依据盖斯定律:化学反应不管是一步完成还是分几步完成,其反应热是相同的.我们可从题目中所给的有关方程式进行分析:从方程式(3)与方程式(1)可以看出有我们需要的有关物质,但方程式(3)必须通过方程式(2)有关物质才能和方程式(1)结合在一起.例2、熔融盐燃料电池具有高的发电效率,因而得到重视,可用li2co3和na2co3的熔融盐混合物作用电解质,co为阳极燃气,空气与co2的混合气体为阴极助燃气,制得在650℃下工作的燃料电池,完成有关的电池反应式:阳极反应式:2co+2co32-→4co2+4e-阴极反应式:;总电池反应式: .解析:作为燃料电池,总的效果就是把燃料进行燃烧.本题中co为还原剂,空气中o2为氧化剂,电池总反应式为:2co+o2=2co2.用总反应式减去电池负极(即题目指的阳极)反应式,就可得到电池正极(即题目指的阴极)反应式:o2+2co2+4e-=2co32- .答案:o2+2co2+4e-=2co32-;2co+o2=2co2例3、下列有关反应的方向说法中正确的是( )a、放热的自发过程都是熵值减小的过程.b、吸热的自发过程常常是熵值增加的过程.c、水自发地从高处流向低处,是趋向能量最低状态的倾向.d、只根据焓变来判断化学反应的方向是可以的.答案:bc.化学反应原理复习(二)【知识讲解】第2章、第3、4节一、化学反应的速率1、化学反应是怎样进行的(1)基元反应:能够一步完成的反应称为基元反应,大多数化学反应都是分几步完成的.(2)反应历程:平时写的化学方程式是由几个基元反应组成的总反应.总反应中用基元反应构成的反应序列称为反应历程,又称反应机理. (3)不同反应的反应历程不同.同一反应在不同条件下的反应历程也可能不同,反应历程的差别又造成了反应速率的不同.2、化学反应速率(1)概念:单位时间内反应物的减小量或生成物的增加量可以表示反应的快慢,即反应的速率,用符号v表示.(2)表达式:(3)特点对某一具体反应,用不同物质表示化学反应速率时所得的数值可能不同,但各物质表示的化学反应速率之比等于化学方程式中各物质的系数之比.3、浓度对反应速率的影响(1)反应速率常数(k)反应速率常数(k)表示单位浓度下的化学反应速率,通常,反应速率常数越大,反应进行得越快.反应速率常数与浓度无关,受温度、催化剂、固体表面性质等因素的影响.(2)浓度对反应速率的影响增大反应物浓度,正反应速率增大,减小反应物浓度,正反应速率减小.增大生成物浓度,逆反应速率增大,减小生成物浓度,逆反应速率减小.(3)压强对反应速率的影响压强只影响气体,对只涉及固体、液体的反应,压强的改变对反应速率几乎无影响.压强对反应速率的影响,实际上是浓度对反应速率的影响,因为压强的改变是通过改变容器容积引起的.压缩容器容积,气体压强增大,气体物质的浓度都增大,正、逆反应速率都增加;增大容器容积,气体压强减小;气体物质的浓度都减小,正、逆反应速率都减小.4、温度对化学反应速率的影响(1)经验公式阿伦尼乌斯总结出了反应速率常数与温度之间关系的经验公式:式中a为比例系数,e为自然对数的底,r为摩尔气体常数量,ea为活化能.由公式知,当ea>0时,升高温度,反应速率常数增大,化学反应速率也随之增大.可知,温度对化学反应速率的影响与活化能有关.(2)活化能ea.活化能ea是活化分子的平均能量与反应物分子平均能量之差.不同反应的活化能不同,有的相差很大.活化能 ea值越大,改变温度对反应速率的影响越大.5、催化剂对化学反应速率的影响(1)催化剂对化学反应速率影响的规律:催化剂大多能加快反应速率,原因是催化剂能通过参加反应,改变反应历程,降低反应的活化能来有效提高反应速率.(2)催化剂的特点:催化剂能加快反应速率而在反应前后本身的质量和化学性质不变.催化剂具有选择性.催化剂不能改变化学反应的平衡常数,不引起化学平衡的移动,不能改变平衡转化率.二、化学反应条件的优化——工业合成氨1、合成氨反应的限度合成氨反应是一个放热反应,同时也是气体物质的量减小的熵减反应,故降低温度、增大压强将有利于化学平衡向生成氨的方向移动.2、合成氨反应的速率(1)高压既有利于平衡向生成氨的方向移动,又使反应速率加快,但高压对设备的要求也高,故压强不能特别大.(2)反应过程中将氨从混合气中分离出去,能保持较高的反应速率.(3)温度越高,反应速率进行得越快,但温度过高,平衡向氨分解的方向移动,不利于氨的合成.(4)加入催化剂能大幅度加快反应速率.3、合成氨的适宜条件第3章、物质在水溶液中的行为一、水溶液1、水的电离h2oh++oh-2、溶液的酸碱度3、电解质在水溶液中的存在形态(1)强电解质强电解质是在稀的水溶液中完全电离的电解质,强电解质在溶液中以离子形式存在,主要包括强酸、强碱和绝大多数盐,书写电离方程式时用“=”表示.(2)弱电解质在水溶液中部分电离的电解质,在水溶液中主要以分子形态存在,少部分以离子形态存在,存在电离平衡,主要包括弱酸、弱碱、水及极少数盐,书写电离方程式时用“ ”表示.二、弱电解质的电离及盐类水解1、弱电解质的电离平衡.(1)电离平衡常数在一定条件下达到电离平衡时,弱电解质电离形成的各种离子浓度的乘积与溶液中未电离的分子浓度之比为一常数,叫电离平衡常数.弱酸的电离平衡常数越大,达到电离平衡时,电离出的h+越多.多元弱酸分步电离,且每步电离都有各自的电离平衡常数,以第一步电离为主.(2)影响电离平衡的因素,以ch3coohch3coo-+h+为例.加水、加冰醋酸,加碱、升温,使ch3cooh的电离平衡正向移动,加入ch3coona固体,加入浓盐酸,降温使ch3cooh电离平衡逆向移动. 2、盐类水解(1)水解实质盐溶于水后电离出的离子与水电离的h+或oh-结合生成弱酸或弱碱,从而打破水的电离平衡,使水继续电离,称为盐类水解.(2)水解类型及规律①强酸弱碱盐水解显酸性.②强碱弱酸盐水解显碱性.ch3coona+h2och3cooh+naoh③强酸强碱盐不水解.④弱酸弱碱盐双水解.al2s3+6h2o=2al(oh)3↓+3h2s↑(3)水解平衡的移动加热、加水可以促进盐的水解,加入酸或碱能抑止盐的水解,另外,弱酸根阴离子与弱碱阳离子相混合时相互促进水解.三、沉淀溶解平衡1、沉淀溶解平衡与溶度积(1)概念当固体溶于水时,固体溶于水的速率和离子结合为固体的速率相等时,固体的溶解与沉淀的生成达到平衡状态,称为沉淀溶解平衡.其平衡常数叫做溶度积常数,简称溶度积,用ksp表示.pbi2(s)pb2+(aq)+2i-(aq)(2)溶度积ksp的特点ksp只与难溶电解质的性质和温度有关,与沉淀的量无关,且溶液中离子浓度的变化能引起平衡移动,但并不改变溶度积.ksp反映了难溶电解质在水中的溶解能力.2、沉淀溶解平衡的应用(1)沉淀的溶解与生成根据浓度商qc与溶度积ksp的大小比较,规则如下:qc=ksp时,处于沉淀溶解平衡状态.qc>ksp时,溶液中的离子结合为沉淀至平衡.qc<ksp时,体系中若有足量固体,固体溶解至平衡.(2)沉淀的转化根据溶度积的大小,可以将溶度积大的沉淀可转化为溶度积更小的沉淀,这叫做沉淀的转化.沉淀转化实质为沉淀溶解平衡的移动.四、离子反应1、离子反应发生的条件(1)生成沉淀既有溶液中的离子直接结合为沉淀,又有沉淀的转化.(2)生成弱电解质主要是h+与弱酸根生成弱酸,或oh-与弱碱阳离子生成弱碱,或h+与oh-生成h2o.(3)生成气体生成弱酸时,很多弱酸能分解生成气体.(4)发生氧化还原反应强氧化性的离子与强还原性离子易发生氧化还原反应,且大多在酸性条件下发生.2、离子反应能否进行的理论判据(1)根据焓变与熵变判据(2)根据平衡常数判据离子反应的平衡常数很大时,表明反应的趋势很大.3、离子反应的应用(1)判断溶液中离子能否大量共存相互间能发生反应的离子不能大量共存,注意题目中的隐含条件. (2)用于物质的定性检验根据离子的特性反应,主要是沉淀的颜色或气体的生成,定性检验特征性离子.(3)用于离子的定量计算常见的有酸碱中和滴定法、氧化还原滴定法.(4)生活中常见的离子反应.硬水的形成及软化涉及到的离子反应较多,主要有:ca2+、mg2+的形成.caco3+co2+h2o=ca2++2hco3-mgco3+co2+h2o=mg2++2hco3-加热煮沸法降低水的硬度:ca2++2hco3-caco3↓+co2↑+h2omg2++2hco3-mgco3↓+co2↑+h2o或加入na2co3软化硬水:。
《选修4_化学反应原理》知识点总结整理(超全)

高三化学《化学反应原理》知识清单第一章化学反应与能量变化一、焓变、反应热要点一:反应热(焓变)的概念及表示方法化学反应过程中所释放或吸收的能量,都可以用热量来描述,叫做反应热,又称焓变,符号为ΔH,单位为kJ/mol,规定放热反应的ΔH为“—”,吸热反应的ΔH为“+”。
特别提醒:(1)描述此概念时,无论是用“反应热”、“焓变”或“ ΔH”表示,其后所用的数值必须带“+”或“—”。
(2)单位是kJ/mol,而不是kJ,热量的单位是kJ。
(3)在比较大小时,所带“+”“—”符号均参入比较。
要点二:放热反应和吸热反应1.放热反应的ΔH为“—”或ΔH<0 ;吸热反应的ΔH为“+”或ΔH >0 ∆H=E(生成物的总能量)-E(反应物的总能量)∆H=E(反应物的键能)- E(生成物的键能)2.常见的放热反应和吸热反应①放热反应:活泼金属与水或酸的反应、酸碱中和反应、燃烧反应、多数化合反应。
②吸热反应:多数的分解反应、氯化铵固体与氢氧化钡晶体的反应、水煤气的生成反应、炭与二氧化碳生成一氧化碳的反应3.需要加热的反应,不一定是吸热反应;不需要加热的反应,不一定是放热反应4.通过反应是放热还是吸热,可用来比较反应物和生成物的相对稳定性。
如C(石墨,s) C(金刚石,s)△H3= +1.9kJ/mol,该反应为吸热反应,金刚石的能量高,石墨比金属石稳定。
二、热化学方程式的书写书写热化学方程式时,除了遵循化学方程式的书写要求外,还要注意以下几点:1.反应物和生成物的聚集状态不同,反应热的数值和符号可能不同,因此必须注明反应物和生成物的聚集状态,用s、l、g分别表示固体、液体和气体,而不标“↓、↑”。
2.△H只能写在热化学方程式的右边,用空格隔开,△H值“—” 表示放热反应,△H 值“+”表示吸热反应;单位为“kJ/mol”。
3.△H的值要与热化学方程式中化学式前面的化学计量数相对应,如果化学计量数加倍,△H也要加倍。
化学选修四目录

化学选修四目录第一章:氧化还原反应1.氧化还原反应的基本概念2.氧化还原反应的符号表示法3.氧化还原反应的电子转移过程4.氧化还原反应中的氧化剂和还原剂5.常见氧化还原反应的例子第二章:配位化学1.配位化学的基本概念2.配位化合物的命名方法3.配合物的结构和性质4.配位化学中的配位数和配位键理论5.配位化合物的应用第三章:有机化学基础1.有机化学的基本概念2.有机化合物的命名方法3.有机化学中的结构和性质4.有机化学中的官能团和官能团转化5.有机化合物的应用第四章:聚合物化学1.聚合反应的基本概念和分类2.聚合物的合成方法3.聚合物的结构和性质4.常见的聚合物材料及其应用5.聚合物在环保领域的应用第五章:化学动力学和化学反应速率1.化学动力学的基本概念2.化学反应速率的测定方法3.化学反应速率与反应物浓度的关系4.反应级数和速率常数5.影响化学反应速率的因素第六章:化学平衡和化学平衡常数1.化学平衡的基本概念2.化学平衡的表达式和化学平衡常数的定义3.影响化学平衡的因素4.利用化学平衡常数计算平衡浓度5.平衡常数和平衡位置的关系第七章:电化学和电解质溶液1.电化学的基本概念2.电解质溶液的电离和电离度3.伏安法和法拉第定律4.电解质溶液的电导性和浓度的关系5.电解质溶液在工业生产中的应用第八章:化学分析与仪器分析1.化学分析的基本概念2.化学分析的定性分析方法3.化学分析的定量分析方法4.仪器分析的基本原理和常用仪器5.仪器分析在科学研究和工业生产中的应用以上目录涵盖了化学选修四的主要内容,包括氧化还原反应、配位化学、有机化学基础、聚合物化学、化学动力学和化学反应速率、化学平衡和化学平衡常数、电化学和电解质溶液,以及化学分析与仪器分析。
每章的内容涉及该主题的基本概念、相关理论、实验方法和应用领域等。
人教版高中化学选修4第二章《化学反应速率和化学平衡》知识点归纳
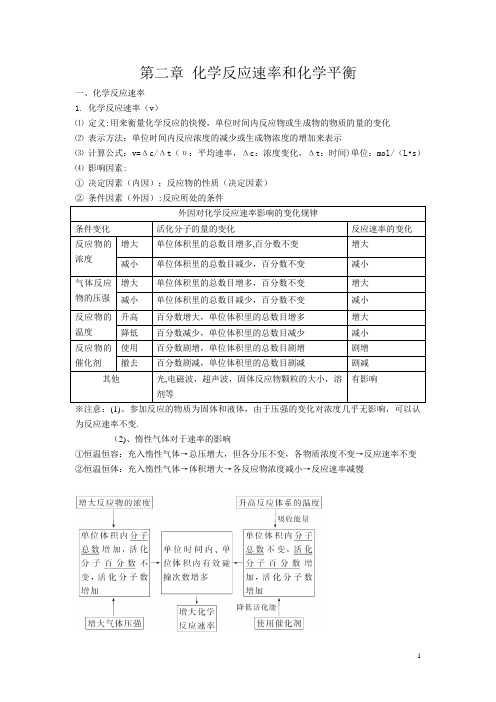
第二章化学反应速率和化学平衡一、化学反应速率1. 化学反应速率(v)⑴定义:用来衡量化学反应的快慢,单位时间内反应物或生成物的物质的量的变化⑵表示方法:单位时间内反应浓度的减少或生成物浓度的增加来表示⑶计算公式:v=Δc/Δt(υ:平均速率,Δc:浓度变化,Δt:时间)单位:mol/(L•s)⑷影响因素:①决定因素(内因):反应物的性质(决定因素)②条件因素(外因):反应所处的条件外因对化学反应速率影响的变化规律条件变化活化分子的量的变化反应速率的变化反应物的浓度增大单位体积里的总数目增多,百分数不变增大减小单位体积里的总数目减少,百分数不变减小气体反应物的压强增大单位体积里的总数目增多,百分数不变增大减小单位体积里的总数目减少,百分数不变减小反应物的温度升高百分数增大,单位体积里的总数目增多增大降低百分数减少,单位体积里的总数目减少减小反应物的催化剂使用百分数剧增,单位体积里的总数目剧增剧增撤去百分数剧减,单位体积里的总数目剧减剧减其他光,电磁波,超声波,固体反应物颗粒的大小,溶剂等有影响※注意:(1)、参加反应的物质为固体和液体,由于压强的变化对浓度几乎无影响,可以认为反应速率不变.(2)、惰性气体对于速率的影响①恒温恒容:充入惰性气体→总压增大,但各分压不变,各物质浓度不变→反应速率不变②恒温恒体:充入惰性气体→体积增大→各反应物浓度减小→反应速率减慢二、化学平衡(一)1。
定义:一定条件下,当一个可逆反应进行到正逆反应速率相等时,更组成成分浓度不再改变,达到表面上静止的一种“平衡”,这就是这个反应所能达到的限度即化学平衡状态。
2、化学平衡的特征逆(研究前提是可逆反应);等(同一物质的正逆反应速率相等);动(动态平衡)定(各物质的浓度与质量分数恒定) ;变(条件改变,平衡发生变化)3、判断平衡的依据判断可逆反应达到平衡状态的方法和依据例举反应mA(g)+nB(g)C(g)+qD(g)混合物体系中各成分的含量①各物质的物质的量或各物质的物质的量的分数一定平衡②各物质的质量或各物质质量分数一定平衡③各气体的体积或体积分数一定平衡④总体积、总压力、总物质的量一定不一定平衡正、逆反应速率的关系①在单位时间内消耗了mmolA同时生成m molA,即V(正)=V(逆)平衡②在单位时间内消耗了n m olB同时消耗了p molC,则V(正)=V(逆)平衡③V(A):V(B):V(C):V(D)=m:n:p:q,V(正)不一定等于V(逆)不一定平衡④在单位时间内生成n molB,同时消耗了q molD,因均指V(逆)不一定平衡压强①m+n≠p+q时,总压力一定(其他条件一定)平衡②m+n=p+q时,总压力一定(其他条件一定) 不一定平衡混合气体平均相对分子质量Mr ①Mr一定时,只有当m+n≠p+q时平衡②Mr一定时,但m+n=p+q时不一定平衡温度任何反应都伴随着能量变化,当体系温度一定时(其他不变)平衡体系的密度密度一定不一定平衡其他如体系颜色不再变化等平衡(二)影响化学平衡移动的因素1、浓度对化学平衡移动的影响(1)影响规律:在其他条件不变的情况下,增大反应物的浓度或减少生成物的浓度,都可以使平衡向正方向移动;增大生成物的浓度或减小反应物的浓度,都可以使平衡向逆方向移动(2)增加固体或纯液体的量,由于浓度不变,所以平衡不移动(3)在溶液中进行的反应,如果稀释溶液,反应物浓度减小,生成物浓度也减小,V正减小,V逆也减小,但是减小的程度不同,总的结果是化学平衡向反应方程式中化学计量数之和大的方向移动。
高中化学选修4-化学反应原理知识点总结

。如 HCl、NaOH、NaCl、BaSO4
化合物
弱电解质:
弱酸,弱碱,极少数盐,水 。如 HClO、NH3·H2O、
非电解质C:u(OH)2、非H2金O…属…氧化物,大部分有机物 。如 SO3、CO2、C6H12O6、CCl4、CH2=CH2……
2、电解质与非电解质本质区别: 电解质——离子化合物或共价化合物 非电解质——共价化合物
注意:①电解质、非电解质都是化合物
②SO2、NH3、CO2 等属于非电解质
③强电解质不等于易溶于水的化合物(如 BaSO4 不溶于水,但溶于水的 BaSO4 全部电
离,故 BaSO4 为强电解质)——电解质的强弱与导电性、溶解性无关。
3、电离平衡:在一定的条件下,当电解质分子电离成 离子的速率 和离子结合成
1
第二章
一、化学反应速率 1. 化学反应速率(v)
⑴ 定义:用来衡量化学反应的快慢,单位时间内反应物或生成物的物质的量的变化 ⑵ 表示方法:单位时间内反应浓度的减少或生成物浓度的增加来表示 ⑶ 计算公式:v=Δc/Δt(υ:平均速率,Δc:浓度变化,Δt:时间)单位:mol/(L·s) ⑷ 影响因素: ① 决定因素(内因):反应物的性质(决定因素) ② 条件因素(外因):反应所处的条件 2.
衡
①m+n≠p+q 时,总压力一定(其他条件一定)
平衡
压强
②m+n=p+q 时,总压力一定(其他条件一定)
不一定平
衡
混 合 气 体 平 均 ①Mr 一定时,只有当 m+n≠p+q 时 相 对 分 子 质 量 ②Mr 一定时,但 m+n=p+q 时
平衡 不一定平
Mr
高中化学选修四的知识点

高中化学选修四的知识点有才智没学问简单陷入空想,一事无成。
有学问没才智,就不要埋怨被人当做工具使用,用毕即弃。
要善用才智来运用学问,以求合理的表现。
下面我给大家共享一些高中化学选修四的学问,盼望能够关心大家,欢迎阅读!高中化学选修四的学问1化学反应速率和化学平衡一、化学反应速率1.化学反应速率(v)⑴ 定义:用来衡量化学反应的快慢,单位时间内反应物或生成物的物质的量的变化⑴ 表示(方法):单位时间内反应浓度的削减或生成物浓度的增加来表示⑴ 计算公式:v=Δc/Δt(υ:平均速率,Δc:浓度变化,Δt:时间)单位:mol/(L·s)⑴ 影响因素:① 打算因素(内因):反应物的性质(打算因素)② 条件因素(外因):反应所处的条件留意:(1)参与反应的物质为固体和液体,由于压强的变化对浓度几乎无影响,可以认为反应速率不变。
(2)惰性气体对于速率的影响①恒温恒容时:充入惰性气体→总压增大,但是各分压不变,各物质浓度不变→反应速率不变②恒温恒体时:充入惰性气体→体积增大→各反应物浓度减小→反应速率减慢二、化学平衡(一)1.定义:化学平衡状态:肯定条件下,当一个可逆反应进行到正逆反应速率相等时,更组成成分浓度不再转变,达到表面上静止的一种“平衡”,这就是这个反应所能达到的限度即化学平衡状态。
2、化学平衡的特征逆(讨论前提是可逆反应)等(同一物质的正逆反应速率相等)动(动态平衡)定(各物质的浓度与质量分数恒定)变(条件转变,平衡发生变化)3、推断平衡的依据(二)影响化学平衡移动的因素1. 浓度对化学平衡移动的影响(1)影响规律:在其他条件不变的状况下,增大反应物的浓度或削减生成物的浓度,都可以使平衡向正方向移动;增大生成物的浓度或减小反应物的浓度,都可以使平衡向逆方向移动(2)增加固体或纯液体的量,由于浓度不变,所以平衡不移动(3)在溶液中进行的反应,假如稀释溶液,反应物浓度减小,生成物浓度也减小,V正减小,V逆也减小,但是减小的程度不同,总的结果是化学平衡向反应方程式中化学计量数之和大的方向移动。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
三水中学高二化学选修4期末复习提纲第一章知识网络常见的吸热反应和放热反应1、活化分子:能够发生 的分子叫做活化分子。
加入反应物,活化分子数目 ,活化分子百分数 (填增大、减小、不变,下同),有气体参加反应的增大容器压强,活化分子数目 ,活化分子百分数 升高容器温度,活化分子数目 ,活化分子百分数2、放热反应:反应物总能量 (填大于、小于或等于,下同)生成物总能量,从微观角度讲,断键吸收的能量 成键放出的能量,△H 0吸热反应:反应物总能量 (填大于、小于或等于,下同)生成物总能量,从微观角度讲,断键吸收的能量 成键放出的能量,△H 0利用反应物和生成物键能之和比较,△H = 。
利用反应物和生成物的总能量比较,△H = 。
3、常见的放热反应类型有: 、 、 、 常见的吸热反应类型有: 、 、 、4、热化学方程式的正确书写:要注明反应的 、 ,若反应是在 和 条件下进行的,可以不予注明。
要注明反应物和生成物的聚集状态或晶形。
常用 、 、 、 分别表示固体、液体、气体和溶液。
一定要注明反应的焓变(△H )。
注意△H 由符号、数值、单位三个部分组成。
而其中数值部分与热化学方程式中的系数有关。
即方程式中的焓变的数值之比等于同意反应的不同方程式中同种物质的系数之比。
热化学方程式中的化学计量数以“mol”为单位,可以是分数,△H 的单位永远是___________。
5、中和反应反应热的测定实验中:用到的玻璃仪器有: 、 、、 、 以及泡沫塑料或纸条、泡沫塑料板或硬纸板。
其中泡沫塑料或纸条、泡沫塑料板或硬纸板的作用是:6、中和热的定义:在测定中和热的实验过程中,为保证数据的测量准确,要用强酸和强碱的稀溶液。
7、燃烧热的定义: 单位:8、现在正在探索的新能源有: 、 、 、 、 、9、盖斯定律的内容:10、在同温同压下,下列各组热化学方程式中,△H 1>△H 2的是( )化学反 应中的 热量变 化 本质原因:化学反应是旧键断裂和新键形成的过程 吸热反应:△H >0 反应热:符号为△H ,单位是kJ/mol 放热反应:△H <0 反应热的测量:一般利用量热计进行测量 反应热的计算:可利用盖斯定律计算无法测量的反应热A、2H2(g)+ O2(g)=2H2O(g) △H1 ; 2H2(g)+ O2(g)=2H2O(l) △H2B、S(g) + O2(g) = SO2(g) △H1 ;S(s) + O2(g) = SO2(g) △H2C、C(s) + 1/2 O2(g) = CO(g) △H1 ; C(s) + 1O2(g) = CO2 (g) △H2D、H2 (g) + Cl2(g) =2HCl(g) △H1 ; 1/2 H2 (g) + 1/2 Cl2(g) = HCl(g) △H211、已知下列热化学方程式:(1)Fe2O3(S) + 3CO (g) = 2 Fe(S) + 3 CO2(g) △H1= —26.7KJ/mol(2) 3Fe2O3(S) + CO (g) = 2 Fe3O4(S) + CO2(g) △H2= —50.75KJ/mol(3) Fe3O4(S) + CO (g) = 3 FeO(S) + CO2(g) △H3= —36.5KJ/mol不用查表,计算反应FeO(s) + CO(g) = Fe (s) + CO2 (g)的焓变。
12、已知H2的燃烧热是285.8 KJ/mol,C3H8的燃烧热是2220 KJ/mol,某H2和C3H8的混合气体共5mol,完全燃烧时放出的热量为3847KJ,则混合气体中H2和C3H8的体积比为13、在一定条件下,CH4和CO燃烧热分别为890 KJ/mol、283 KJ/mol。
在该条件下一定量的CH4和CO混合气体完全燃烧后,放出的热量为262.9KJ,生成的CO2用过量的饱和石灰水完全吸收,可得到50g白色沉淀。
求混合气体中CH4和CO的体积比14.写出下列反应的热化学方程式(1)1摩尔乙醇完全燃烧生成二氧化碳和液态水,放出1366.8 kJ热量(2)1摩尔C(石墨)与适量水蒸气反应生成一氧化碳和氢气,吸收131.3 kJ热量(3)标准状况下将纯净的CH41L在空气中完全燃烧,生成CO2气和液态水,放出39.75kJ 热量,则CH4燃烧热的热化方程式为:________________ 。
(4)由氢气和氧气反应生成1摩尔水蒸气放热241.8 kJ热量,写出该反应的热化学方程式,反应热为。
若1克水蒸气转化为液态水放热2.444kJ,则氢气燃烧生成液态水的热化学方程式为氢气的燃烧热为。
15.已知H-H键的键能为436kJ·mol-1,Cl-Cl键的键能为243kJ·mo l-1,H-Cl键的键能为431kJ·mol-1,则H2(g)+Cl2(g)==2HCl(g)的反应热(△H)等于。
第二章一、化学反应速率1、意义:用来衡量化学反应进行的程度。
2、表示方法:通常用单位时间内或来表示,v= (单位:或或)3、影响因素内因:参加反应物质本身的(最主要因素)外因:对某一确定的反应,外界因素(,,,等)都存在影响。
4、在应用化学反应速率的时候应该注意的几个问题:(1)在中学化学里通常说的化学反应速率一般是指速率。
(2)由于△ c是取浓度的变化的绝对值,故反应速率都取值。
(3)表示一个化学反应的反应速率的时候必须指明是用哪一种反应物或生成物来表示(4)一般不用和表示反应的化学反应速率。
(5)同一个化学反应,在同一段时间内,用不同物质表示反应速率时,数值不同,各物质速率之比等于。
5、化学反应速率的测量6、用于化学反应速率测量的基本性质(1)直接可观察的性质,如释放出气体和体系压强。
(2)依靠科学仪器才能测量的性质,如颜色的深浅、光的吸收、光的发射、导电能力等。
(3)在溶液中,当反应物和产物本身有比较明显的颜色时,常常利用颜色深浅和显色物质浓度间的正比关系来跟踪反应的过程和测量反应速率。
二、化学平衡(一)对化学平衡移动的理解1.定义:可逆反应:在相同条件下,既能向进行,同时又能向进行的反应。
化学平衡状态:在一定条件下,当一个可逆反应进行到时,不再改变,达到表面上静止的一种“”,这就是这个反应所能达到的限度即化学平衡状态。
2、化学平衡的特征____(研究前提是可逆反应)____(同一物质的正逆反应速率相等)____(动态平衡)____(各物质的浓度与质量分数恒定)____(条件改变,平衡发生变化)3、判断平衡的依据(1)各物质浓度、质量分数不再变化(2)同物质:V正=V逆【生成a molX的同时消耗a molX 或b molY】不同物质:异方向,量相当【生成a molX的同时生成c molR】(3)体系温度不再变化(4)a+b≠c+d时,压强不再变化;混合气体密度或平均分子量不再变化(5)颜色(二)影响化学平衡移动的因素1、浓度对化学平衡移动的影响(1)影响规律:在其他条件不变的情况下,增大反应物的浓度或减少生成物的浓度,都可以使平衡向______方向移动;增大生成物的浓度或减小反应物的浓度,都可以使平衡向_______方向移动(2)增加固体或纯液体的量,由于浓度不变,所以平衡______(3)在溶液中进行的反应,如果稀释溶液,反应物浓度____,生成物浓度也____, V 正____,V逆也_____,但是减小的程度不同,总的结果是化学平衡向反应方程式中化学计量数之和_____的方向移动。
2、温度对化学平衡移动的影响影响规律:在其他条件不变的情况下,温度升高会使化学平衡向着_________方向移动,温度降低会使化学平衡向着_________方向移动。
3、压强对化学平衡移动的影响影响规律:其他条件不变时,增大压强,会使平衡向着____________方向移动;减小压强,会使平衡向着__________方向移动。
注意:(1)改变压强不能使无气态物质存在的化学平衡发生移动(2)气体减压或增压与溶液稀释或浓缩的化学平衡移动规律相似(3)在体积恒定的容器内,充入不发生化学反应的气体,由于浓度不变,速率不变,所以平衡_____(4)在恒压容器内,充入不发生化学反应的气体,由于体积变大,各物质的浓度变小,速率变化,所以平衡______(5)气体减压或增压与溶液稀释或浓缩的化学平衡移动规律相似。
4.催化剂对化学平衡的影响:由于使用催化剂对正反应速率和逆反应速率影响的程度是等同的,所以平衡________。
但是使用催化剂可以影响可逆反应达到平衡所需的_____。
5.勒夏特列原理(平衡移动原理):如果改变影响平衡的条件之一(如温度,压强,浓度),平衡向着能够_______这种改变的方向移动三、化学平衡常数(一)定义:在一定温度下,当一个反应达到化学平衡时,________________________比值。
符号:____(二)使用化学平衡常数K应注意的问题:1、表达式中各物质的浓度是________,不是起始浓度也不是物质的量。
2、K只与_____有关,与反应物或生成物的浓度无关。
3、反应物或生产物中有固体或纯液体存在时,由于其浓度是固定不变的,可以看做是“1”而不代入公式。
4、稀溶液中进行的反应,如有水参加,水的浓度不必写在平衡关系式中。
5、非水溶液中的反应,如有水生成或有水参加反应,此时水的浓度不可视为常数,必须表示在平衡关系式中。
6、K 是指某一具体反应的平衡常数。
若反应方向改变,则平衡常数_____。
若方程式中各物质的系数等倍扩大或缩小,尽管是同一反应,平衡常数________。
(三)化学平衡常数K 的应用:1、化学平衡常数值的大小是可逆反应_______的标志。
K 值越大,说明平衡时_____的浓度越大,它的______进行的程度越大,即该反应进行得越_____,反应物转化率越____。
一般地,K>____时,该反应就进行得基本完全了。
2、可以利用K 值做标准,判断正在进行的可逆反应是否平衡及不平衡时向何方进行建立平衡。
(Q :浓度商)Q___K:反应向正反应方向进行;Q___K:反应处于平衡状态 ;Q___K:反应向逆反应方向进行3、利用K 值可判断反应的热效应若温度升高,K 值增大,则正反应为_____反应若温度升高,K 值减小,则正反应为_____反应四、化学反应进行的方向1、在热力学中有两条重要的基本自然规律,控制着所有物质体系的变化方向:(1)物质体系倾向于取得最低的________;(2)物质体系倾向于取得最大的_________。
对于一种物质来说,物质发生着从固态、液态至气态的变化过程,在此过程中,物质的混乱度____,其熵值也在____。
2、自发反应中的焓变和熵变的关系:(1)放热的过程可能是熵____的过程,如铁生锈、氢气燃烧等;也可能是熵_________或______的过程,如甲烷燃烧、氢气与氯气化合等。
