HNMR-2解析
HNMR谱图解析

由在0.9附近三重峰和1.8附 近的四重峰,可推知可能存 在-C-CH2CH3的结构
由在1.1附近三重峰和4.1 附近的四重峰,可推知可 能存在-O-CH2CH3的结构
IR指示其为酯类化合物,
21
(2)再看图的上部分, =6.8处是芳环质子峰,相对峰高表 明有3个质子。脂肪链上质子数为9的单峰 故该化合物为C6H3(CH3)3 且芳环质子峰无裂分现象,说明该化合物为1,3,5-三甲基苯。
22
例4:已知一化合物的化学式为C4H6OF3Br,已测得其核磁共振 波谱图如下,试推断其结构。
24
。 例:某未知物分子式为C5H12O,其核磁共振氢谱如图所示,求其化学结构
H3C
CH3 H2
C C OH
CH3
25
例:某化合物的分子式为C6H10O3,其核磁共振谱见图。试确定该化合 物结构。
CH3CH2OCOCH2COCH3
26
解析实例
例1 某化合物分子式为C8H12O4,根据谱图推其结构。
34
2.分子式为C3H60的某化合物的核磁共振谱如下,试 确定其结构。
谱图上只有一个单峰,说明分子中所有氢核的化学 环境完全相同。结合分子式可断定该化合物为丙酮。 35
3-溴丙炔的1HNMR
36
例4:C10H12O的核磁共振氢谱如下,推导其结构。
S a t A p r 2 2 0 9 :4 3 :0 9 2 0 0 0 : (u n title d ) W 1 : 1 H A xis = p p m S c a le = 4 1 .6 7 H z/ c m
•低δ= 3.87 CH3上氢,低场移动,与电负性强的元素
HNMR2 氢谱核磁共振

3 .2 0 0
3 .0 0 0
2 .8 0 0
2 .6 0 0
2 .4 0 0
2 .2 0 0
2 .0 0 0
1 .8 0 0
1 .6 0 0
1 .4 0 0
1 .2 0 0
1 .0 0 0
例 分子式C8H12O4,1HNMR谱如下, 推导其结构
W e d A p r 1 2 1 1 :1 4 :4 6 2 0 0 0 : (u n title d ) W 1: 1H A x is = p p m S c a le = 3 9 .6 9 H z / c m
Ha Hb
Hc
F
a b c,
a aˊb bˊc ,
Ha R1 Ha R2 R3 Hb X H3C O O C Hb CH2 CH3 CH3 Ha Hb
X Y Hc
O
Hd He CH3 Hb
O
Ha
O
Hf
Hc
Hb
O
Hc
a H3C N H3C b H O
H-NMR of DMF
O N
+
O
-
400 MHz
B0
Be
原子核实际感受到的磁场: B = (1-s) B0 s化学位移常数
2013年7月11日
2
核外电子在与外磁场垂直的平面上
绕核旋转的同时,会产生与外磁场
方向相反的感生磁场。
感生磁场的大小用σ·0 B 表示。σ为屏蔽常数, 与核外电子云的密度有 关。
HNMR 3
自旋偶合现象
e2
n1
n2
CH3 CH2 低分辨
e1
高分辨 J
自旋-自旋偶合
自旋核与自旋核之间的相互作用(干扰)
HNMR氢核磁共振波谱法-文档资料

i 同碳偶合,谐偶(J同, J谐, 2J)
系因相互干扰的两个氢核(如不同构象)处于同一 碳原子上引起。两者之间的偶合常数叫J同。同碳 偶合经过两个C—H键(H—C—H),因此,可用 2J表示。
• 影响电子云密度的一个重要因素,就是与质子相连 接的原子或基团的电负性的大小:
电负性大的取代基(吸电子基团),可使邻近氢核 的电子云密度减少(去屏蔽效应),导致该质子的 共振信号向低场移动,化学位移左移;
电负性小的取代基(给电子基团),可使邻近氢核 的电子云密度增加(屏蔽效应),导致该质子的共 振信号向高场移动,化学位移右移。
Hb Ha Hc
Ha裂分为多少重峰?
Jba Jca
Jca Jba
4
3
210
Ha裂分峰:(3+1)(2+1)=12
实际Ha裂分峰:(5+1)=6
强度比近似为:
1:5:10:10:5:1
偶合常数
• 偶合常数与化学位移值一样,都是解析核磁共振谱 的重要数据。但偶合常数与化学位移值的区别,在 于偶合常数的大小与外加磁场强度无关
7.29 7.21
7.55 8.18
7.27
7.18
CH2CH3 7.68
NO2
7.29 7.21
7.55 8.18
7.27
7.18
CH2CH3 7.68
NO2
7.29 7.21
7.55 8.18
仪器分析课件第五章:HNMR

实验操作步骤
样品装入
将准备好的样品装入样品管中, 确保密封良好。
数据采集
启动仪器进行数据采集,记录 实验结果。
仪器校准
确保仪器处于最佳工作状态, 提高实验精度。
参数设置
根据实验需求设置适当的实验 参数,如频率、扫描宽度等。
结果处理
对采集的数据进行处理和分析, 得出实验结论。
氢原子在分子中的化学环境不同,会导致其自旋磁矩的共振 频率发生变化,通过测定这些频率,可以推断出分子中氢原 子的连接方式和化学环境。
hnmr的原理
氢核磁共振的原理基于核自旋磁矩的存在。当氢原子核处于磁场中时,其自旋磁矩会与磁场相互作用 ,产生能级分裂。当外加射频场以特定频率照射时,低能级上的氢原子核会吸收能量跃迁到高能级上 ,产生共振信号。
谱图解析难度较大
虽然HNMR谱图可以提供丰富的结构信息,但谱图解析需要较高的专 业知识,对解析人员的要求较高。
未来发展
提高检测灵敏度
通过改进检测方法和技术,提高 HNMR的检测灵敏度,使其能够应 用于更广泛的样品分析。
发展便携式设备
随着技术的进步,便携式HNMR设 备的发展将使得现场快速分析成为可 能。
05
hnmr的局限性及未来发 展
局限性
对样品纯度要求高
HNMR分析要求样品具有一定的纯度,否则会产生较大的干扰峰,影 响分析结果的准确性。
对样品量要求大
为了获得较为准确的HNMR谱图,需要一定量的样品。对于某些珍贵 或稀缺的样品,难以满足需求。
对溶剂残留敏感
HNMR分析中,溶剂残留会对谱图产生干扰,影响分析结果的准确性。
03
hnmr实验技术
波谱分析第二章HNMR谱

CH3CH2CH2Br 1.04
CH3(CH2)3Br 0.9
★常见官能团的电负性均大于氢原子的电负性, 因此在烷烃中δCH>δ CH2>δ CH3
2.相连碳原子的SP3和SP2杂化 与氢相连的碳原子从SP3到SP2杂化,S电子的成 分从25%增加到33%,C-H键电子更靠近碳原子, 因而对相连的氢核有去屏蔽作用,δH变大。即共 振位置移向低场。 ★请看下面的区别:
2.1.4 驰豫过程 1.弛豫过程 当大量的原子核在外磁场中取向并达到平衡,高低 能级的分布可利用Boltzman定律来描述。即低能级 的数目略多于高能级的数目,且ΔE极小。当用射频电 磁波照射外磁场中原子核时,低能级的核吸收能量跃 迁至高能级,产生核磁共振信号。由于ΔE极小,高 能级粒子通过自发辐射回到低能级的几率几乎为零。 因此若要在一定时间间隔内持续检测到NMR信号, 必须有某种过程存在,它使高能级的原子核回到低能 级,以保持低能级的粒子数始终略大于高能级的粒子 数。这个过程就是弛豫过程。
弛豫过程示意图(I=1/2的核)
2.2 化学位移
2.2.1化学位移的产生及表示方法 1.化学位移的产生 在磁场强度为B0的磁场中,质子的共振条件 是:
υ共振=γB0/2π
由此式可知对于同一种原子核其核磁共振频率 是一样的,在NMR谱中只在一个地方出峰, 显然毫无用处。
但是事实上并不是这样,由于同种核所处的化 学环境不同,其共振频率也会有变化,这主要 是由核外电子对质子的屏蔽作用不同引起的! 由于核外电子的屏蔽作用,即核外电子运动产 生一种与外磁场相反的感生磁场,削弱了外磁 场B0,因此实际作用于原子核的磁场强度不是 B0而是B0(1-σ)。 σ--屏蔽常数(shielding constant),它反映了 核外电子对核的屏蔽作用的大小,同时也反映 了核所处的化学环境 。
有机波谱分析-NMR3-HNMR2

4)从3)中可知,各峰质子数之和正好与分子式中氢原子数目 符合,所以分子无对称性。
5)解析特征性较强的峰: ① a 峰为单峰,是苯环单取代信号,可能是苯环与烷基碳相连。 因为:ⅰ.化学位移在芳氢范围之内,δ 7.2~7.5 ppm;
ppm 之间。 6)解析低场信号:无大于8 ppm 的信号。 7)重水交换无变化,证明氧原子上无质子相连,即不存在 OH 型
质子。 8)已解析出有 C6H5-和CH3-CO-,还剩下 C2H4O 归属未找到。
从 b组峰和 c 组峰的峰形看,两个亚甲基应相连,即- CH2- CH2-。一端与苯相连,一端与氧相连。
解析具体步骤:
1.区分溶剂峰,杂质峰和旋转边带峰及活泼氢 2.计算不饱和度 UN= n + 1 + a/2 – b/2 3.根据峰积分面积计算各组峰所对应的氢数,注意
分子对称性因素
4.指认单重谱峰 CH3O-, CH3CO-, CH3C 5.确认芳香族化合物峰
, RO-CH2-CN等
6.对简单多重峰进行解析,找出相互耦合的基团
什么是化学位移,化学位移的产生及表示;NMR的标准物 质
自旋自旋偶合现象,耦合常数,一级谱的裂分规律
峰面积积分
2. 应用 a. 影响化学位移的因素(取代基的电负性、磁各向异性) b. 常见官能团的氢谱
c. 烷基:0~2ppm; 烯:4~7ppm;苯环:7.3ppm(无取代基) 对位二取代及简单多取代苯的谱图; 活泼氢(OH, NH, SH, COOH)的特征
HNMR图谱解析

n1)/2
式中n4、n3、n1分别为分子中所含的四价、三价
和一价元素原子的数目。二价原子如S、O等不参和一价元素原子的数目。二价原子如S、O等不参
加计算。当?=0时,表示分子是饱和的,为链状
烃及其不含双键的衍生物。当?=1时,可能有一个
HNMR图谱解析刘和文NMR谱解析步骤检查NMR谱整体:杂质、旋转边带、位移
标定等
看峰的位置:针对δ进行分析
看峰的大小,以确定各峰对应的氢原子数目看峰的大小,以确定各峰对应的氢原子数目
看峰的形状,包括峰数目,J大小等
根据各峰组化学位移和偶合关系的分析,确
定结构单元必须熟记的化学位移大致范围不饱和度不饱和度是表示有机分子中碳原子的不饱和程度。
双键或脂环;当?=2时,可能有两个双键和脂环,
也可能有一个叁键;当?=4时,可能有一个两种不同
羟基氢,位移分别为5.2和10.5ppm两个,
指出其结构例题2秦芄乙素例题3例题4AA’BB’例题5:双照射去偶确定异构体C9H9O2Br结构确定异构体图谱确定两甲基顺反式练习题1:根据图谱确定结构练习题2练习题3练习题4练习题5决定两个取代基的顺反式
10波谱HNMR2耦合与裂分

与质子之间的耦合。 与质子之间的耦合。
质子与质子( H)之间的耦合 质子与质子(1H,1H)之间的耦合
通过两个键之间的耦合 ---同碳质子间的耦合 ---同碳质子间的耦合 通过三个键之间的耦合 ---邻碳质子间的耦合 ---邻碳质子间的耦合 大于三键之间的偶合---远程耦合 大于三键之间的偶合---远程耦合 ---
Cl Ha Hb
Cl H
Cl D
分子中不能通过对称操作进行互换的质子 称之非对映异位 (Diastereotopic) 称之 非对映异位(Diastereotopic) , 无论是在 非对映异位 有手性中心的分子还是无手性中心的分子中。 有手性中心的分子还是无手性中心的分子中。
பைடு நூலகம்
例如
Ha O C H3C O Hb CH2 CH3 a b CH3
−3 ∼ +3 ~2Hz
取代基电负性的影响: 取代基电负性的影响:
取代基电负性增大, 值增大。 取代基电负性增大,2J 值增大。
S Ph Ha Hb −1.38 +0.97 Ph N Ha Hb +5.7 Ph O Ha Hb
2J
应用实例
解释4 HNMR谱 例1 解释4-氧杂环戊酮衍生物的1HNMR谱
φ= 90o
φ= 120o Jab = ~ 3Hz, , φ= 180o Jab = 11 ~ 12Hz
Hb OH
Hb
快速旋转的σ 快速旋转的σ键,3J 6 ~ 8Hz 的平均值) (为60o,180o的平均值)
环己烷: 环己烷:
Ha He Heˊ Ha ˊ
Jaa Jae ˊ ˊ Jea Jeeˊ ˊ
苏式的Newman投影 苏式的Newman投影 Newman
《HNMR图谱解析》课件

HNMR图谱解析的挑战
重叠峰
当氢原子在HNMR图谱上的 峰重叠时,解析和准确解 释峰的位置变得困难。
溶剂峰
HNMR图谱中常常出现溶剂 峰,这些峰会干扰分析, 需要谨慎处理。
溶液浓度
HNMR图谱的解析受到溶液 浓度的影响,因此需要控 制浓度以获得准确的峰值。
HNMR图谱解析的应用领域
有机合成
HNMR图谱解析在有机合成中用于确定反 应产物和研究反应机理。
鸟瞰研究
通过分析HNMR图谱,我们可以了解化合 物的分子结构,从而指导药物设计和分析。
环境监测
HNMR图谱解析可帮助监测环境中的有机 污染物,并识别可能的危险物质。
生物医学
在生物医学领域中,HNMR图谱解析可用 于研究生物大分子结构和代谢产物。
2
仪器设置
将HNMR仪器设置为适当的频率和参数,确保准确测量峰的强度和化学位移。
3
数据解析
通过解读HNMR图谱上的峰值特征,确定化合物的结构,包括官能团和它们的位 置。
常见的HNMR图谱谱线分析
峰形 单峰 双峰 多峰
说明
表明该氢原子环境较简单,附近无其他取 代基。
表明该氢原子受到一个取代基的影响,相 邻位置上存在一个取代基。
《HNMR图谱解析》PPT 课件
欢迎来到本次《HNMR图谱解析》PPT课件。在这个课件中,我们将一起探索 HNMR图谱解析的目的、基本原理、步骤、常见分析方法、实例、挑战以及应 用领域。让我们一起来深入了解吧!
HNMR图谱解析的目的
分析结构
通过HNMR图谱解析,我们可以确定与化合物相关的结构信息,包括它们的有机官能团和它 们的位置。
表明该氢原子受到多个取代基的影响,化 学环境较复杂。
HNMR-2
2.75 ppm HA
JAB
JAB=5.5 Hz
JAC
JBC=4.0 Hz JAC=2.6 Hz
苯基环氧乙烷的氢谱和裂分解析
(5)A3体系 CH3Cl
(6)ABC体系
Hc
Hb
Hb
Ha
Hc
CN
Ha
(a) 60MHz
(b) 300MHz
丙烯腈(H2C=CH—CN)的氢谱
在300MHz核磁共振仪,ABC体系简化为AMX体系。
HA,HB
2
H3C
1 OCHAHBCH3 CH
OCHAHBCH3
CH3(2)
M3C—CH2
5.0 4.5 4.0 3.5 3.0 2.5 2.0 1.5 1.0
二乙基缩乙醛的氢谱(250MHz)
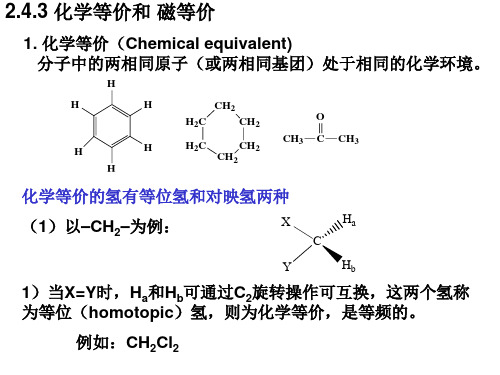
2. 磁等价(Magnetic equivalent)
两个核(或基团)磁等价必须同时满足下列两条件: 1)它们是化学等价的。 2)它们对任意另一核的偶合常数J相同(数值及符号)。
=0
=90
=180
相邻两C-H的键电子轨道示意图
六元环的Jaa > Jae Jee
Ha 2 He
1 He Ha
Ha
C
2 He
1
C
He
Ha
aa = 180,ee = 60°, ae = 60 Jaa =8~12Hz,Jee =1~3Hz,Jae =2~4Hz
练习[2.2] 某葡萄糖样品含有和b两种异构体,根据氢谱 确定两种异构体含量。
(4)tt体系: 有两个不同的J值
A BC
CH2 CH2 CH2
JAB
JBC
HB
1∶2∶1
10波谱HNMR2耦合与裂分

典型例子
AX系统 p.111 AMX系统 p.112
☆二级谱分类及解析
二级谱的特点:
1. 相互耦合产生的多重峰数目多于n+1规律;
2. 多重峰各谱带强度之比不符合二项式展开式 系数之比,内侧峰明显高于外侧峰;
3. 每组裂分峰的化学位移至该组峰的重心位置, 不在该组峰的中心;
5 .0 0 0
4 .5 0 0
4 .0 0 0
3 .5 0 0
3 .0 0 0
2 .5 0 0
2 .0 0 0
1 .5 0 0
1 .0 0 0
邻碳质子间的耦合
Ha—C—C—Hb , 用3J 或J邻表示
饱和型化合物
3J 与两面夹角φ的关系
Karplus方程:
3J = J 0 cos2φ 0.28 (0o ≤φ≤90o) 3J = J 180 cos2φ 0.28 (90o ≤φ≤180o)
Hb Hb
大
苏式
大
小大
小大
小
Hb
大
小
(I)
( II )
( III )
苏式构型的稳定构像以( III )为主,
3Jab 2 ~ 4Hz。
若有分子内氢键存在时,
以形成内氢键的稳定构像为主。
麻黄碱(赤式构型)的稳定构像
Ha
HO
Hb
Ha
Hb
Ph
CH3NH
CH3
Ph ( II )
CH3NH
CH3
OH ( III )
Hf 4.49
5 .0 0 0
4 .6 0 0
4 .2 0 0
3 .8 0 0
3 .4 0 0
H NMR-2

-CH3 , =1.6~2.0,高场; -CH2I, =3.0 ~ 3.5,
-O-H,
-C-H,
大
低场
小
高场
影响化学位移的因素--电负性对化学位移的影
响
3.5 O CH3 3.42-4.02 3.0 N CH3 2.12-3.10 2.5 C CH3 0.77-1.88
H
N
~.8 1 HC C C 3
~3.7 H3C O H C
~0.9 H3C C
O C OH
H C O
C
15 14 13 12 11 10 9
8
7
6
5
4
3
2
1
0
¯ §» Æ » Ñ Î Ò
Ä (ppm) ¦
3.4.1 饱和碳上质子的化学位移 甲基 在核磁共振氢谱中,甲基的吸收峰比较特征,容 易辨认。一般根据邻接的基团不同,甲基的化学 位移在0.7~4ppm之间.
化合物类型 δ (ppm) 化合物类型 δ (ppm)
ROH 0.5~5.5 ArOH(缔合) 10.5~16 ArOH 4~8 RCOOH 10~13 =NH-OH 7.4~10.2 R-SH 0.9~2.5 =C=CHOH(缔合)15~19
RSO3H RNH2, R2NH ArNH2,Ar2NH RCONH2,ArCONH2 RCONHR,ArCONHR RCONHAr, ArCONHAr
云密度↓,屏蔽效应↓,共振信号→低场。例如:
高 场
低 场
高
场
Ha 低 O Hb 场
Hb
β
Ha
HNMR2

间和对-硝基苯乙酸的核磁共振氢 谱
• 由于苯环上两个取代基不同,苯环上四 个氢至少被分成两组。对于对硝基苯乙 酸,苯环上四个氢分成对称的两组,因 而谱图上是对称的两组双峰。而间硝基 苯甲酸,苯环上四个氢不再对称,因而 谱图上峰的分裂也是不规则的。另外, 硝基苯甲酸分子中除了苯环氢外,还有 羧基中羟基氢和一个亚甲基氢,3.8ppm 的单峰是亚甲基氢
双硝基不同位置取代苯的核磁共 振谱图
• 对硝基苯谱图只有单峰,表明苯环上四个 氢一致。间硝基苯谱图有三组分裂的峰, 表明苯环上四个氢在两个硝基的作用下分 成三组各自偶合的峰。而邻硝基苯谱图上 有一个分裂的双重峰,表明苯环上四个氢 分成能偶合的两组。顺便一提:由于两个 硝基强大的吸电子和共轭作用,苯环上氢 的化学位移δ值大大增加,已达到8.0ppm以 上。
Spin System in Pople notation---AMX System notation---AMX
Aromatic substitution pattern: ortho
AA’ XX’ Typical spectra for ortho (symmetrical)
O CH3 O
CH3
A B C B' X A' B Y B' A' A X B B' A' A OH OH B B' A' A Cl Cl
邻二氯苯的谱图如下: 邻二氯苯的谱图如下:
F ri A p r 2 1 2 1 :1 5 :2 3 2 0 0 0 : (u n title d ) W 1: 1H A x is = p p m S c a le = 2 .9 6 H z / c m
AA′BB′ˊ AA′BB′ˊ二级谱
【合成经验】怎样才能拿到一个合格的HNMR谱,一些常见的问题怎么解决?

【合成经验】怎样才能拿到一个合格的HNMR谱,一些常见的问题怎么解决?由于微信更改了订阅号的推送规则,很多朋友不能快速找到我们,其实我们每天都在推送!您可以将有机合成设置为星标(点击右上方“...", 设为星标),就能在微信订阅号中快速找到我们,查看每天订阅。
HNMR谱图是确认化合物结构最重要的数据之一,在有机合成过程中,新合成的化合物必须要HNMR表征,如何得到一个合格的HNMR谱图,是每个合成人必须掌握的技能。
下面小编列出一些常见的问题,抛砖引玉,大家共同学习交流。
问题:产物的峰的不同H直接互相重叠,无法看清峰型,无法精确积分或者不能完全分辨出特定H用于判断HH相关或C-H相关的二维谱图。
解决方法:可以尝试用不同的氘代试剂,化合物在不同的氘代试剂中的峰的位置和峰型会有区别。
问题:产物不溶于氘代氯仿解决方法:氘代氯仿峰型窄,相对便宜,是常用的氘代试剂之一,但是还有其他很多氘代试剂可以选择。
尝试新的氘代试剂,只要氘代试剂不覆盖产物峰,都可以尝试。
要根据样品的极性选择极性相似的溶剂,氘代溶剂的极性从小到大是这样排列的:苯、氯仿、乙腈、丙酮、二甲亚砜、吡啶、甲醇、水。
问题:排除化合物本身的问题,第二次测的HNMR谱图和第一次测的不同。
解决方法:如果只是稍有不同,可能是两次测样的浓度不同,有时更浓的样品中分子的相互作用更加明显,进而影响谱图。
问题:化合物中含有OH或NH等活泼氢,不能确定那个峰是活泼氢的峰?解决方法:在核磁管样品中加一滴氘水,剧烈振荡几分钟,活泼氢会被氘掉,在谱图上消失,或者直接用氘代甲醇送样。
酰胺类的氨基氢交换得很慢,需要长时间放置再测谱。
问题:乙酸乙酯峰盖掉了我的产物峰,油泵拉了几小时还是有溶剂残留解决方法:有时溶剂会包在产物中,无法除去溶剂【【合成经验】如何除去交货产物中的溶剂残留?】。
如果直接想看清峰,可以用二氯甲烷带一下,除去乙酸乙酯后再测。
问题:TLC或LCMS确认产物很纯,但是HNMR谱图非常复杂,明显不是单一的化合物或非对映体的混合物的核磁。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
能量差
磁性核的自旋取向表明
它在外加磁场中的取向 它的某个特定能级状态(用 磁量子数ms表示)。取值为 –I … 0 … +I。
即:每一个取向都代表一个能级状态,有一个ms 。 如:1H核:∵ I=1/2 ∴ ms为 -1/2 和 +1/2
ν= γ H0 高能态 H' ms = _ 1/2 外 场 H' ms = + 1/2
2π E = hν H0
γ — 磁旋比(物质的特征常数)
E = hν = γ
h H0 2π
低能态
自旋核的电荷分布——球形 高能级自旋态(Eb) 1 磁级自旋态(Ea) 磁量子数 m= + 1 2
E
BO=△E=Eb-Ea
结论:
1H受到一定频率(v)的电磁辐射,且提供的能量
CH3CH2OCH2CH3
CH3CH2CH2CH2OH
CH3OCH2CH2CH3
例3. 预测下列化合物有几个NMR信号及裂分情 况,能否用NMR区分
O
三组峰
五重峰
CH2 CH2
CH2 三重峰 O
CH3CH
三重峰 十二重峰
CH2
二重峰
CH3CH2OCH2CH3
二组峰
CH3CH2CH2CH2OH
五组峰
-CH2I, =3.0 ~ 3.5,
-O-H, 大 低场
-C-H, 小 高场
• 电负性影响的规律: 吸电子诱导效应使质子核外电子密度降低, 屏蔽效应减弱,质子的吸收峰就移向低场。 给电子诱导效应使质子核外电子密度增 加, 屏蔽效应增加,质子的吸收峰就移向高场。
2、化学键的磁各向异性效应
H'
1
H'
H 核:
自旋取向数 = 2×1/2 + 1 = 2 一 致 H0 相 反
即:H核在外场有两个自旋方向相反的取向。
讨
论:
1. I=0 的原子核 O(16):C(12);S(32)等 ,无自旋, 无磁性,称为非磁性核,这类核不会发生核磁共振。 不产生共振吸收。
2. I=1 或 I>0的原子核: I=1 : 2H,14N, I=3/2: 11B,35Cl,79Br,81Br I=5/2: 17O,127I
4)化学环境完全相同的原子,虽然它们有很强的偶合作用, 但无裂分现象。 例:-CH3不发生裂分 5)化学等价核:化学位移相同的一组核。 如:CH2=CF2两个氢是化学等价的核。 磁等价核:化学位移相同且核磁性也相同的核。 如:CH2F2中两个氢核的化学位移相同,与两个 19F核的偶合 常数也相同,则这两个氢为磁等价核。 磁等价的核一定是化学等价的,但化学等价的核不一定磁 等价。
整 数 0
半整数 n + 1/2。n = 0,1,2,…
偶 数
偶 数
例如:
H
A (1 ) Z (1 )
C
A (12) Z (6)
N
A (14) Z (7)
奇 - 奇
偶 - 偶
偶 - 奇
I为半整数(1/2)
有共振吸收
I = 0
无
I为整数
有共振吸收
自旋核在外加磁场中的取向 取向数 = 2 I + 1 (在没有外电场时,自旋核的取向是任意的)。
如果氢核邻近有两组偶合程度不等的氢核时,一组有n个, 另一组有n 个,则谱线裂分成(n+1)(n+1)重峰。
a
b
a b CH3CH2I —CH3中的氢核 2个Hb 的自旋取向 外磁场方向 Ha使Hb共振峰 的裂分 各峰面积比 1:2 :1 1 :3 :3 :1 Ha Hb —CH2中的氢核 3个Ha 的自旋取向 外磁场方向 Hb使Ha共振峰 的裂分 各峰面积比
2) 一组氢核多重峰的位置,是以化学位移值为中心左右对称, 并 且各裂分峰间距相等。
3)裂分是因为分子中相邻氢核之间发生了自旋相互作用,自旋偶 合不影响化学位移,但会使吸收峰发生裂分,使谱线增多,简称 自旋裂分。 通常自旋偶合作用传递三个单键
Ha Hb Hc H C H C H C H H
a-b、b-c之间有自旋偶合 a-c之间自旋偶合可忽略 同碳上的自旋偶合最大
B =(1- )B0 :屏蔽常数。 越大,屏蔽效应越大。
由于屏蔽作用的存在,氢核产生共振需要更大的外磁场强 度(相对于裸露的氢核),来抵消屏蔽影响。
在有机化合物中,各种氢核周围的电子云密度不同(结构中 不同位置),屏蔽常数不同,共振频率有差异,即引起共振吸 收峰的位移,这种现象称为化学位移。
如:CH2=CF2(二氟乙烯)分子中,2个1H 和2个19F,化学等价但磁不等价。
反 顺 J烯 J烯 J H1F1 J H2F1 , J H1F2 J H2F2
思考:CH2=CCl2(二氯乙烯)分子中,2个H是否磁等价? 为什么?
②单键带有双键性时,会产生不等价质子。
如:酰胺,由于C—N键带有双键性,不能自由旋 转,因此胺基上的两个H是不等价的。在图谱上会 出现两个不等价质子的单峰信号。
A
A HCHO
C HCOOH
B CH3OH
D CH3COOCH3
下列有机物分子在核磁共振氢谱中只给出一种信号的是 A HCHO C HCOOH B CH3OH D CH3COOCH3
A
例3. 预测下列化合物有几个NMR信号及裂分情 况,能否用NMR区分
CH2 CH2 CH2 O
O CH3CH CH2
价电子产生诱导磁场, 质子位于其磁力线上, 与外磁场方向一致,去 屏蔽。
苯环上的6个电子产生 较强的诱导磁场,质子位 于其磁力线上,与外磁场 方向一致,去屏蔽。
磁各向异性效应(远程屏蔽效应)对化学位移的影响 (烯、炔、羰基、芳香化合物)
H H H H H
7.3
H H
C C
H H
R C C H CH3CH3
• 问题四:什么是自旋偶合常数?{偶合常数(J)}
1.自旋偶合与自旋裂分 每类氢核不总表现为单峰,有时多重峰。 原因:相邻两个氢核之间的自旋相互干扰作用称为自旋偶合。 由自旋偶合引起的谱线增多现象称为自旋裂分。 多重峰的峰间距, 偶合常数(J), 偶合作用的大小。 HA核受到邻近HB 核自旋偶合作用, 吸收峰被分裂为 双重峰。
磁不等价核之间才能发生自旋偶合裂分。如下情况是磁不等价 氢核
A:化学环境不相同的氢核;
B:与不对称碳原子相连的-CH2上的氢核
C:固定在环上的-CH2中的氢核 D:单键带有双键性质时,会产生磁不等价氢核 E:单键不能自由旋转时,也会产生磁不等价氢核。
例1:判断下列化合物有几组峰,几重峰 CH3CH2OH CH2ClCH2CHBr2 Cl-CH2-CH2-Cl
乙炔的各向异性效应
B0
δ=2.0 ~ 3.0
3、氢键和溶剂的影响 分子形成氢键后,使质子周围电子云密度降低,产生去屏 蔽作用而使化学位移向低场移动。形成氢键趋势越大,质子向 低场移动越显著。当存在分子间氢键时,化学位移受到溶液浓 度的影响,若用惰性溶剂稀释溶液,分子间生成氢键的趋势减 小,使化学位移移向高场;而分子内的氢键的形成受溶液浓度 影响极小。 同一试样在不同溶剂中由于受到不同溶剂分子的作用,化 学位移发生变化,称为溶剂效应。溶剂效应主要受溶剂的极性、 形成氢键、形成分子复合物和屏蔽效应。有时几种效应共存一 体,需找出主要影响因素。 有不同类型氢的化学位移表
问题一:核磁共振是如何产生的?(基本原理)
•
让处于外磁场(Bo)中的自旋核(如氢 核)接受一定频率的电磁波辐射,当辐射的 能量恰好等于自旋核两种不同取向的能量 差时,处于低能态的自旋核吸收电磁辐射 能跃迁到高能态,这种现象称为核磁共振。
BO=△E=Eb-Ea
自旋核
原子核象电子一样,有自旋现象,从而有自旋角动量。
大,屏蔽弱,共振需要的磁场强度小,在低场出现,图左侧;
= [( 样 - TMS) / 0 ] ×106 (ppm)
• 问题四:影响化学位移的因素是什么?
1.电负性的影响 与质子相连元素的电负性越强,吸电子作用越强,价电子偏 离质子,屏蔽作用减弱,信号峰在低场出现。
-CH3 , =1.6~2.0,高场;
B0 (1 ) 2
• 问题三:为什么用TMS作为基准?(化学位移 的表示方法)
• 化学位移的数值是一个很小的值,要精确测量 其绝对值很难,通常用相对化学位移来表示。 • 相对标准:四甲基硅烷 Si(CH3)4 (TMS) (内标) • 位移常数 TMS=0
为什么用TMS作为基准?
可用自旋量子数(I)来描述。
h I ( I 1) 2
I=0、1/2、1……
I = 0,ρ =0,无自旋,不能产生自旋角动量,不会产生共 振信号。 ∴ 只有当I > O时,才能发生共振吸收,产生共振
信号。
I 的取值可用下面关系判断:
质量数(A)
奇 数
原子序数(Z)
奇数或偶数 奇 数
自旋量子数(I)
这类原子核的核电荷分布可看作一个椭圆体,电荷 分布不均匀,共振吸收复杂,研究应用较少;
3.I=1/2的原子核:1H,13C,19F,31P
原子核可看作核电荷呈球形分布于核表面, 并象陀 螺一样自旋,有磁矩产生,其核磁共振的谱线窄,最 适宜检测,是核磁共振研究的主要对象,C,H也是有 机化合物的主要组成元素。
旋进轨道 自旋轴
自旋的质子
H0
核的自旋角动量(ρ)是量子化的,不能任意取值,
可用自旋量子数(I)来描述。
外磁场(Bo)
样品管 磁铁 记录器
无线电波 振荡器
接收及 放大器
两种不同取向
原子核象电子一样,有自旋现象,从而有自旋角动量。
旋进轨道 自旋轴
自旋的质子
H0
