中国药典2010年版一部修订说明
中国药典2010版第一部

中国药典2010版第一部摘要:一、引言二、中国药典2010版第一部的概述三、中国药典2010版第一部的主要内容1.药物的分类2.药物的命名规则3.药物的性状、鉴别与检查4.药物的炮制5.药物的制剂四、中国药典2010版第一部的应用与价值五、结论正文:一、引言中国药典是中医药行业的一部权威性法典,对药品的研究、生产、经营、使用、监督管理等方面具有重要的指导作用。
本文将重点介绍中国药典2010版第一部的相关内容。
二、中国药典2010版第一部的概述中国药典2010版第一部,简称2010版药典一部,是按照我国药品监督管理部门的要求,由中国药典委员会组织编纂的。
该书于2010年正式出版,是我国药品标准体系的重要组成部分。
三、中国药典2010版第一部的主要内容1.药物的分类2010版药典一部对药物进行了详细的分类,包括中药材、中药提取物、中药成方制剂、化学药品、生化药品、抗生素、放射性药品等。
2.药物的命名规则药典规定了药物的命名原则,包括通用名、化学名、商品名等,并对药物的命名进行了规范和统一。
3.药物的性状、鉴别与检查药典对药物的性状、鉴别与检查进行了详细的规定,包括外观性状、理化性质、鉴别方法、检查方法等,为药品的真伪鉴别提供了依据。
4.药物的炮制药典对药物的炮制进行了规范,包括炮制方法、炮制程度等,以确保药物的疗效和安全性。
5.药物的制剂药典对药物的制剂进行了详细的规定,包括制剂工艺、处方、质量要求等,以确保药品的质量和疗效。
四、中国药典2010版第一部的应用与价值2010版药典一部的出版,为药品的生产、经营、使用、监督管理等方面提供了重要的依据和指导,对提高我国药品质量、保障人民用药安全有效具有重要意义。
五、结论中国药典2010版第一部是中医药行业的一部权威性法典,对药品的研究、生产、经营、使用、监督管理等方面具有重要的指导作用。
2010版中国药典修改-附录部分

【话题】制剂通则-片剂【2010版页数】附录5-6【2005版页数】附录5-6【区别分析】1. 含片的定义由原来“含于口腔中,药物缓慢溶解产生持久局部作用的片剂”改为“含于口腔中缓慢溶化产生局部或全身作用的片剂”。
指出了含片亦可实现全身作用。
2. 原含片的崩解时限描述为含片的溶化性,测定法仍按照崩解时限检查法,崩解时限由之前“30分钟内应全部崩解”改为“10分钟内不应全部崩解或溶化”,这点修改有些特殊,设定崩解时限的下限主要是为了防止含片在口中迅速溶化,与舌下片区别,但是取消了含片的崩解上限。
3.咀嚼片的定义由原来“口腔中咀嚼或吮服使片剂溶化后吞服,在胃肠道中发挥作用或胃肠道吸收发挥全身作用”修改为了“口腔中咀嚼后吞服的片剂”,定义大大简化。
4. 片剂的注意事项中,增加了“薄膜包衣在必要时检查残留溶剂”,这点规定将更有利于水性包衣技术的应用和推广。
5.分散片分散均匀性的检查方法由之前“取供试品2片,置20±1℃的水中,振摇3分钟,应全部崩解并通过二号筛”,改为“取供试品6片,置250ml烧杯中,加15-25℃的水100ml,振摇3分钟,应全部崩解并通过二号筛”。
新方法增加了供试片剂的数量,特别是规定了进行分散均匀性所需介质的体积,可以充分保证分散均匀性的重现性。
【话题】制剂通则-药用辅料【2010版页数】附录20药用辅料药用辅料系指生产药品和调配处方时使用的赋形剂和附加剂;是除活性成分以外,在安全性方面已进行了合理的评估,并且包含在药物制剂中的物质。
药用辅料除了赋形、充当载体、提高稳定性外,还具有增溶、助溶、缓控释等重要功能,是可能会影响到药品的质量、安全性和有效性的重要成分。
药用辅料可从来源、作用和用途、给药途径等进行分类。
按来源分类可分为天然物、半合成物和全合成物。
按作用与用途分类可分为溶媒、抛射剂、增溶剂、助溶剂、乳化剂、着色剂、黏合剂、崩解剂、填充剂、润滑剂、润湿剂、渗透压调节剂、稳定剂、助流剂、矫味剂、防腐剂、助悬剂、包衣材料、芳香剂、抗黏着剂、抗氧剂、螯合剂、渗透促进剂、pH 调节剂、增塑剂、表面活性剂、发泡剂,、消泡剂,、增稠剂、包合剂、保湿剂、吸收剂、稀释剂、絮凝剂与反絮凝剂、助滤剂等。
中国药典2010年版一部修订说明

709 321 429
12
33 a 3
184 1138 505
14
15
47 8
饮片的定义及质量标准的建立
• 定义:系指药材经过炮制后可直接用于中医临床或制剂生产使用的处方药品。 • 质量标准:由2005年版的13个,增加到439个品种822个饮片标准,基本覆盖了
中医临床常用饮片目录,解决了长期以来饮片缺乏国家标准的问题。 • 定位:明确了中医临床配方和中成药投料所用的均为饮片,并将中成药处方中
二、加强安全性检查项目
• 树脂残留物检查(复脉定胶囊) • 有害元素检查(紫血散)
• 重金属、砷盐检查(黄连上清片等7 个品种)
• 乌头碱限量(二十五味珊瑚丸等32个 品种)
• 三氧化二砷检查(六应丸等10个品种)
a
21
二、加强安全性检查项目
Байду номын сангаас
• 加强中药注射液安全性检查项目
• 如注射用灯盏花素
相关物质、注射剂有关物质、异常 毒性、降压物质、过敏反应、溶血 与凝聚检查
• 一项鉴别同时鉴别二味以上药材,如 桂林西瓜霜、脑得生胶囊、百合固金
口服液
a
10
一、建立中成药专属性鉴别
对照物质
对照品 对照药材 对照提取 物 合计
新增
191 151
5
2010版药 2005版药
典
典
473
282
369
218
16
11
347
858
511
a
11
例如女金丸薄层色谱鉴别
T: 20.8℃, RH: 24.9%
16
47
31
22
499
《中国药典》2010版第一增补本一部修改品种明细
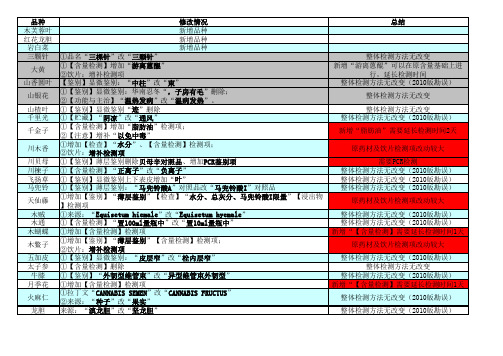
①【鉴别】薄层鉴别:多处修订及订正; ②增加增加【浸出物】【含量检测】检测项; ③饮片:增补检测项 ①【鉴别】薄层鉴别:“加10%盐酸的50%甲醇溶液”改“加10%盐酸的50%甲醇溶液 地榆 50ml” 当归 ①饮片项下酒当归检测项后面的性状删除 ①增加【鉴别】“显微鉴别”粉末、【检查】“水分、总灰分、酸不溶性灰分”【浸 出物】【含量检测】等检测项; 红大戟 ②【鉴别】“薄层鉴别”全新修订,增加对照品 ③饮片:增补检测项 ①【含量检测】羟基红花黄色素A分子式(C27H30O15)改(C27H32O16) 红花 麦芽 ①【鉴别】显微鉴别:多处修订 赤小豆 ①来源:“umbeuata”改“umbellata” ①来源:增加好望角芦荟,习称“新芦荟” 芦荟 ②【检查】“水分、总灰分”标准要求各增加一倍 ③【含量检测】标准要求分库拉索芦荟、好望角芦荟 ①【鉴别】“薄层鉴别”删除对照品 苏木 ②【含量检测】删除 ①拉丁文“HERBA”改“FOLIUM” 巫山淫羊藿 ②【性状】“二回”删除 吴茱萸 ①【含量检测】对照品溶液的制备“0.15mm”改“0.15mg” 佛手 ①【含量检测】对照品溶液的制备“15ul”改“15ug” 诃子 ①【鉴别】薄层鉴别“C18固相萃取小柱”改“C18(300mg)固相萃取小柱” 补骨脂 ①【鉴别】薄层鉴别“显相同的两个蓝白色荧光斑点”删除“蓝白色” ①炮制方法“食用胆巴”删除“食用” 附子 ②【含量检测】“总生物碱”删除 ③饮片项下炮附片【含量检测】“总生物碱”删除 ①增加【检查】“水分、总灰分”检测项 青皮 ②饮片项下相应增加【检查】“水分、总灰分”检测项 苦杏仁 ①【检查】过氧化值(附录ⅨD)改(附录ⅨP) 枇杷叶 ①【鉴别】显微鉴别“中柱”改“束” 京大戟 ①增加【鉴别】“薄层鉴别”、【检查】“水分”【浸出物】【含量检测】等检测项 泽泻 ①来源:“orientalis”改“orientale” ①【含量检测】马兜铃酸I(C17H11O7N)改(C17H11NO7) 细辛 ②【功能主治】“祛风散寒”改“解表散寒” 茺蔚子 ①增加【含量检测】检测项 北豆根
中国药典2010年版一部中成药及相关标准的增修订内容介绍-PPT精品文档

7
气相色谱法
中药指纹图谱分析方法的建立应能体现中药的
整体特征
在满足表征中药化学成分群整体性质的前提下,要求 有较好的重现性。明确了指纹图谱认证、方法验证、 数据处理及计算分析的依据和方法。
提出药典成方制剂原则上不再使用和收载濒危
药材
除规定使用天然麝香、天然牛黄的特殊品种外,其他 使用麝香、牛黄的品种均改为“人工麝香”或“人工 牛黄”; 属于濒危物种或商品匮乏的药材,若需减去或替换应 按相关要求进行并按药品注册管理办法申报,经批准 后方可列入中国药典。
Ⅱ.对原专属性不强的测定方法(紫外、重量法、容 量法)修改为HPLC、GC等专属性强的方法。
戊已丸 05版:UV法测定黄连总生物碱含量 10版:HPLC法测定盐酸小檗碱和芍药苷含量 黄氏响声丸 05版:TLC-S法测定贝母素乙含量 10版:HPLC法测定贝母素甲和贝母素乙含量 HPLC用于乌头碱限量检查 如:原乌头碱限量检查基本用TLC, 二十五味珊瑚丸用HPLC检查乌头碱限量 含量测定增加了较多的新对照品
不收载的原则:
含有濒危药材、国家重点保护的物种、含动物粪便、 有严重安全隐患的品种、处方药材基源不清楚或基础 工作薄弱的品种原则上不收载。
12
新增品种来源:
2019年版药典一部立项情况
专项研究课题 含朱砂、雄黄中成药中游 离砷、汞检测方法研究; 农药多残留检测方法研究; 黄曲霉毒素检测研究; 重金属及有害元素研究;
《中国药典》2019年版一部中成药及相 关标准增修订内容介绍
季 申
2019年
上海市食品药品检验所,上海市张衡路1500号 邮编: 201903 Email: jishen2019gmail
中国药典2010年版中药

原子 TLC-S 滴定 吸收
38 33 1 2 38 53
2010年版 1265
(三)增订剂型品种
新增 露剂品种:金银花露 涂膜剂品种:疏痛安涂膜剂
增修订内容与特点
(一)收载品种数量大幅度增加
2005版收载中成药564种 2010版收载中成药1063种
(一)收载品种数量大幅度增加
2010版药典标准起草技术要求及编写细则 《中国药典》中药质量标准研究技术要求 《中国药典》中药质量标准复核技术要求 《中国药典》中药质量标准起草说明编写 细则 《中国药典》中药质量标准起草与复核工 作规范 《中国药典》中药质量标准正文各论编写 细则
药典编排格式
凡例 正文 附录
2010版药典标准正文内容—药材和饮片
(一)增修订品种
中药材及饮片
种类
药材 饮片
2005版 530 746
2010版 592 809
增幅(%) 12 8
收载标准数量
2005版 530 70 2010版 592 809
种类
药材
增幅(%) 12 1056
饮片
中成药增修订品种
2010年版收载总数: 1063
2010年版新增品种数:499
(三)专项研究课题 (1)含朱砂、雄黄中成药中游离砷、 汞检测方法研究; (2)农药多残留检测方法研究; (3)黄曲霉毒素检测研究; (4)重金属及有害元素研究; (5)生物活性测定法研究。
2010年版药典一部立项情况
不上的原则: (1)品种增加的越多越好,但不降低要求、不破 规矩,质量标准达不到要求的品种不上; (2)含保护动、植物的不上; (3)含龙骨的不上; (4)含人中白、紫河车、五灵脂的不上; (5)含鲜活动物的不上。 (6)处方药材基源不清楚或基础工作薄弱的品种 原则上不收载。
中国药典2010版第一部

中国药典2010版第一部
摘要:
1.介绍《中国药典2010 版第一部》
2.该版本的主要内容和更新
3.《中国药典》的历史和作用
4.《中国药典》对中医药发展的影响
正文:
《中国药典2010 版第一部》是我国国家级的药品标准规范,对药品的研发、生产、质量控制以及药品的流通和使用等方面具有重要的指导意义。
《中国药典》是我国药品标准的核心,它的每一次更新都受到广泛的关注。
2010 版第一部的《中国药典》是对前一版的修订和完善,主要包括了中药、化学药品、生物制品等各类药品的标准。
此次修订,对药品的收载数量、质量标准、检验方法等方面都进行了大幅度的提升和改进,以适应我国药品研发和生产的新需求。
《中国药典》的历史可以追溯到1953 年,其初衷是为了规范药品的生产和使用,保障人民的用药安全。
从那时起,《中国药典》已经经历了多次修订,每一次修订都反映出我国药品标准的进步,以及药品研发和生产技术的提升。
《中国药典》对我国中医药的发展起到了重要的推动作用。
一方面,它规范了中医药的生产和使用,保障了人民的用药安全。
另一方面,它推动了中医药的现代化进程,促进了中医药与国际接轨。
《中国药典》2010年版(一部)药材及饮片拟收载品种中医标准修订内容
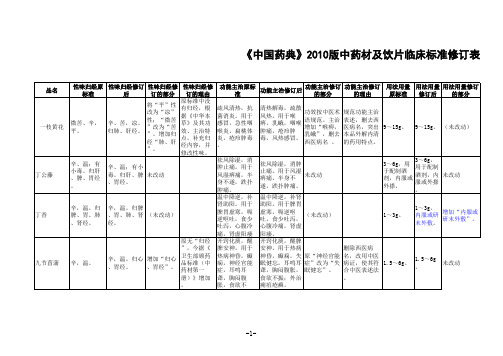
功能主治原标 准 行气止痛,活 血散瘀。用于 胃痛,风湿痹 痛;外治牙 痛,跌扑肿 痛,虫蛇咬伤 理气止痛,温 中助阳。用于 胃寒胀痛,肝 胃气痛,肾虚 阳痿,腰膝酸
功能主治修订后
功能主治修订 功能主治修订 用法用量 用法用量 用法用量修订 的理由 的部分 原标准 修订后 的部分 6~12g。 6~12g。 外用鲜品 外用鲜品适 适量,捣 (未改动) 量,捣烂敷 烂敷患处 患处。 。
用法用量 用法用量 用法用量修订 修订后 原标准 的部分
1~3g, 1~3g,包 包煎。多 煎。多入丸 入丸散 (未改动) 散服。外用 服,外用 适量。 适量。
3~6g。
3~6g。
(未改动)
Байду номын сангаас
八角莲
苦、辛, 平;有毒。
将“平”性 苦、辛,凉; 改为“凉” 有毒。归肺、 性;增加归 肝经。 经“肺、肝 ”。 甘,温。归胃 (未改动) 、肾经。
3~9g。
3~9g。
(未改动)
了哥王
苦、辛,微 温;有毒。
将“微温” 苦、辛,寒。 之性改为“ 有毒。归肺、 寒”性。增 肝经。 加“归肺、 肝经。”
消炎解毒,散 瘀逐水。用于 支气管炎,肺 炎,腮腺炎, 淋巴结炎,风 湿痛,晚期血 吸虫病腹水, 疮疖痈疽。
清热解毒,散瘀 逐水。用于肺热 咳嗽,痄腮,发 颐,疮疖痈疽, 风湿痹痛,臌胀 。
功能主治原标 功能主治修订 功能主治修订 用法用量 用法用量 用法用量修订 功能主治修订后 准 的部分 的理由 原标准 修订后 的部分 根据《本草正 》、《本草汇 言》和《中华 临床中药学》 增加“养血” 功效,根据《 神农本草经》 增加“益智” 功效。原“主 治”中的心力 衰竭,心原性 休克属于西医 名称,而主治 中的中医病名 已经有“体虚 欲脱,肢冷脉 微”,故直接 删除“心力衰 竭,心原性休 克”。
中国药典2010年版
年版截图:中国药典20102010版中国药典word版pdf版exe版电子书2010版中国药典word版pdf版exe版电子书中国药典2010年版一部正文一枝黄花(p3)YizhihuanghuaSOLIDAGINIS HERBA本品为菊科植物一枝黄花Solidago decurrens Lour.的干燥全草。
秋季花果期采挖,除去泥沙,晒干。
【性状】本品长30~lOOcm。
根茎短粗,簇生淡黄色细根。
茎圆柱形,直径0.2~0.5cm;表面黄绿色、灰棕色或暗紫红色,有棱线,上部被毛;质脆,易折断,断面纤维性,有髓。
单叶互生,多皱缩、破碎,完整叶片展平后呈卵形或披针形,长1~9cm,宽0.3~1.5cm;先端稍尖或钝,全缘或有不规则的疏锯齿,基部下延成柄。
头状花序直径约0.7cm,排成总状,偶有黄色舌状花残留,多皱缩扭曲,苞片3层,卵状披针形。
瘦果细小,冠毛黄白色。
气微香,味微苦辛。
【鉴别】 (1)叶表面观:上表皮细胞多角形,垂周壁略呈念珠状增厚。
下表皮细胞垂周壁波状弯曲,气孔不定式,略下陷。
非腺毛有两类:表皮非腺毛由3个细胞组成,壁薄,顶端1个细胞常萎缩成鼠尾状,较小;叶缘非腺毛睫毛状由3~7个细胞组成,壁稍厚,长180~500μm。
(2)取本品粉末2g,加石油醚(60~90℃)50ml,超声处理30分钟,放冷,滤过,弃去石油醚液,药渣挥干溶剂,加70%乙醇30ml,加热回流1小时,放冷,滤过,滤液蒸干,残渣加甲醇1ml使溶解,作为供试品溶液。
另取一枝黄花对照药材2 g,同法制成对照药材溶液。
再取芦丁对照品,加甲醇制成每1ml含0.5mg的溶液,作为对照品溶液。
照薄层色谱法(附录ⅥB)试验,吸取供试品溶液5~10μl、对照药材溶液和对照品溶液各5μl,分别点于同一以含4%磷酸氢二钠溶液制备的硅胶G薄层板上,以乙酸乙酯-甲醇-甲酸-水(8:1:2010版中国药典word版pdf版exe版电子书1:1)为展示剂,展开,取出,晾干,喷以3%三氯化铝乙醇溶液,晾干,置紫外光灯(365nm)下检视,供试品色谱中,在与对照药材色谱和对照品色谱相应的位置上,显相同颜色的荧光斑点。
2010年版中国药典增补本修订内容
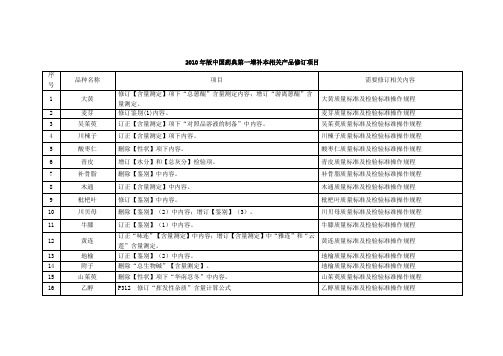
14
银黄片
新增品种
工艺规程、成品检验标准操作规程
15
石斛夜光丸
(重大变更)
P118修改“处方”和“制法”,修订鉴别(2)(3),增订鉴别(4);修订鉴别(5);删除原鉴别(5),修订鉴别(6);修订“含量测定”项(流动相、对照品配制、含量限度0.33变更为0.27)
工艺规程、成品检验标准操作规程、处方文件、包装材料相关文件及备案
P555订正“检查法”
QC文件
2010年版中国药典第二增补本相关产品修订项目
序号
品种名称
项目
需要修订相关内容
1
干姜
修订饮片项下的【浸出物】
干姜质量标准及检验标准操作规程
2
山药
药材及饮片品种项下增订“二氧化硫残留量”检查项目,限度为“二氧化硫残留量不得过400mg/kg
山药质量标准及检验标准操作规程
3
4
川楝子
订正【含量测定】项下内容。
川楝子质量标准及检验标准操作规程
5
酸枣仁
删除【性状】项下内容。
酸枣仁质量标准及检验标准操作规程
6
青皮
增订【水分】和【总灰分】检验项。
青皮质量标准及检验标准操作规程
7
补骨脂
删除【鉴别】中内容。
补骨脂质量标准及检验标准操作规程
8
木通
订正【含量测定】中内容。
木通质量标准及检验标准操作规程
QC文件
药材项下订正【含量测定】项
黄连质量标准及检验标准操作规程
12
酸枣仁
订正饮片项下的【炮制】项、【鉴别】项、【检查】中的水分项、【含量测定】项。
酸枣仁质量标准及检验标准操作规程
中国药典 2010 年版一部附录

中国药典2010 年版一部附录附录Ⅰ A 丸剂丸剂系指饮片细粉或提取物加适宜的黏合剂或其他辅料制成的球形或类球形制剂,分为蜜丸、水蜜丸、水丸、糊丸、蜡丸和浓缩丸等类型。
蜜丸系指饮片细粉以蜂蜜为黏合剂制成的丸剂。
其中每丸重量在0.5g(含0.5g)以上的称大蜜丸,每丸重量在0.5g 以下的称小蜜丸。
水蜜丸系指饮片细粉以蜂蜜和水为黏合剂制成的丸剂。
水丸系指饮片细粉以水(或根据制法用黄酒、醋、稀药汁、糖液等)为黏合剂制成的丸剂。
糊丸系指饮片细粉以米粉、米糊或面糊等为黏合剂制成的丸剂。
蜡丸系指饮片细粉以蜂蜡为黏合剂制成的丸剂。
浓缩丸系指饮片或部分饮片提取浓缩后,与适宜的辅料或其余饮片细粉,以水、蜂蜜或蜂蜜和水为勤合剂制成的丸剂。
根据所用黏合剂的不同,分为浓缩水丸、浓缩蜜丸和浓缩水蜜丸。
丸剂在生产与贮藏期间应符合下列有关规定。
一、除另有规定外,供制丸剂用的药粉应为细粉或最细粉。
二、蜜丸所用蜂蜜须经炼制后使用,按炼蜜程度分为嫩蜜、中蜜和老蜜,制备蜜丸时可根据品种、气像等具体情况选用。
除另有规定外,用塑制法制备蜜丸时,炼蜜应雄热加入药粉中,混合均匀;处方中有树脂类、胶类及含挥发性成分的药味时,炼蜜应在60℃左右加入;用泛制法制备水蜜丸时,炼蜜应用沸水稀释后使用。
三、浓缩丸所用提取物应按制法规定,采用一定的方法提取浓缩制成。
四、除另有规定外,水蜜丸、水丸、浓缩水蜜丸和浓缩水丸均应在80℃以下干燥;含挥发性成分或淀粉较多的丸剂(包括糊丸)应在60℃以下干燥;不宜加热干燥的应采用其他适宜的方法干燥。
五、制备蜡丸所用的蜂蜡应符合本版药典该饮片项下的规定。
制备时,将蜂蜡加热熔化,待冷却至60℃左右按比例加入药粉,棍合均匀,趁热按塑制法制丸,并注意保温。
六、凡需包衣和打光的丸剂,应使用各品种制法项下规定的包衣材料进行包衣和打光。
七、丸剂外观应圆整均匀、色泽一致。
蜜丸应细腻滋润,软硬适中。
蜡丸表面应光滑无裂纹,丸内不得有蜡点和颗粒。
中国药典2010年版修订简介

《中国药典》版增补本增补内容

序号《中国药典》2010年版第一增补本(一部)《中国药典》2010年版第一增补本(二部)新增品种乙醇丹七片头孢氨苄对乙酰氨基酚修订品种肌苷大黄安乃近山银花安乃近片川木香苯甲酸川贝母木通明胶龙胆牛膝枸橼酸钠当归补骨脂附子重质碳酸镁麦芽氧化镁苦杏仁诺氟沙星胶囊枇杷叶泽泻修订附录酸枣仁重金属检查法黄连滴定液酸枣仁牛黄解毒片订正附录妇康宁片最低装量检查法抗病毒口服液补中益气丸(水丸)修订附录重金属检查法酸败度检查法滴定液序号《中国药典》2010年版第二增补本(一部)《中国药典》2010年版第二增补本(二部)修订品种干姜修订附录山药一般鉴别试验牛膝铵盐检查法天冬粒度和粒度分布测定法丹参溶出度测定法白及白术白芍粉葛黄连酸枣仁龙胆泻肝丸板兰根颗粒复方鱼腥草片清火栀麦片修订附录药材和饮片检定通则显微鉴别法一般鉴别试验炽灼残渣检查法膨胀度测定法鞣质含量测定法序号《中国药典》2005年版增补本《中国药典》2005年版增补本一部修订品种一部修订附录三七药材检定通则大青叶杂质检查法牛蒡子砷盐检查法丹参微生物限度检查法甘草对照品对照药材对照提取物石膏龙胆白术二部修订品种白芍马来酸氯苯那敏百部头孢氨苄连翘明胶苦杏仁盐酸小檗碱片郁金诺氟沙星胶囊金钱草淀粉金银花糊精荆芥茵陈茯苓二部修订附录栀子砷盐检查法粉葛崩解时限检查法浙贝母微生物限度检查法桑白皮试液黄芪滴定液炙黄芪标准品与对照品表黄连黄柏菟丝子酸枣仁罂粟壳甘草浸膏黄芩提取物六味地黄丸石淋通片板兰根颗粒。
2010年版《中国药典》(一部)增补本品种临床标准

品名:千金子 【性味与归经】辛,温;有毒。归肝、肾、大肠经。 【功能与主治】泻下逐水,破血消癥,外用疗癣蚀疣。用于二便不通,水肿,痰饮,积滞胀 满,血瘀经闭;外治顽癣,赘疣。 【用法与用量】1~2g;去壳,去油用,多入丸散服。外用适量,捣烂敷患处。 【注意】孕妇禁用。以免中毒。
鼻炎通喷雾剂(鼻炎滴剂) 【功能与主治】 散风清热,宣肺通窍。用于风热蕴肺所致的鼻塞,鼻流清涕或浊涕, 发热,头痛;急、ቤተ መጻሕፍቲ ባይዱ性鼻炎见上述证候者。
痹祺胶囊 【功能与主治】 益气养血,祛风除湿,活血止痛。用于气血不足,风湿瘀阻,肌肉关 节酸痛,关节肿大、僵硬变形或肌肉萎缩,气短乏力;风湿、类风湿性关节炎,腰肌劳损, 软组织损伤属上述证候者。 【注意】 孕妇禁服;高血压患者禁服。
品名:红大戟 【性味与归经】苦,寒;有小毒。归肺、脾、肾经。 【功能与主治】泻水逐饮,消肿散结。用于水肿胀满,胸腹积水,痰饮积聚,气逆咳喘,二 便不利,痈肿疮毒,瘰疬痰核。 【用法与用量】1.5~3g,入丸散服,每次 1g;内服醋制用。外用适量,生用。 【注意】孕妇禁用。
品名:拳参 【性味与归经】苦、涩,微寒。归肺、肝、大肠经。 【功能与主治】清热解毒,消肿,止血。用于赤痢热泻,肺热咳嗽,痈肿瘰疬,口舌生疮, 血热吐衄,痔疮出血,蛇虫咬伤。 【用法与用量】5~10g。外用适量。
加减地黄丸 【功能与主治】 滋补肝肾。用于肝肾不足,头晕耳鸣,潮热,盗汗,遗精。
加味八珍益母膏 【功能与主治】 活血养血,补气调经。用于瘀血内阻,气血不足所致的月经不调、闭 经、痛经、产后恶露不绝,症见月经期错后、经水量少、有血块或淋漓不净、经闭不行、行 经腹痛、拒按、产后恶露不净。 【注意】 孕妇禁服;月经过多、月经提前者慎服。
《中国药典》2010年版一部凡例和中成药及相关标准增修订内容

鉴 别
HP LC 25 11 3 GC 理化 通则
检 查
重金属 有害元 素 8 8 11 12 12 17 31 37 1 14 17 40 28 毒性 成分 32 10 其 他 162 90 50 56 31 71 243 217
特征 或指 纹图 谱 6 1 16
含量测定
HPLC TL CS 12 33 UV GC 其 他 1 4
17
2010版中国药典标准制定基本原则
坚持“科学、实用、规范”、质量可控性和标准先进性的 原则
18
建立符合中医药特点的质量标准体系 逐步由单一指标性成分定性定量向活性、有效成 分及生物测定的综合检测过渡,向多成分及指纹 或特征图谱整体质量控制模式转化 增加和完善中药安全性检测方法 增强检测方法的专属性 建立科学合理的控制指标
9 16 2
54 102 5 17 26 179 134 298
426 627 1 10 1127 726 1554 1363
709 321 17 9 412 175
8 16
24 19 7
中成药
提取物
1 3 13 15 47
1 17 20 25 37
5 9 7 16 31 34 30 32 34
中药材
25
增修订品种
2010年版收载总数: 1063 2010年版新增品种数:499 2010年版修订品种数:254
26
1、鉴别项--新增各项鉴别2165项
显微 TLC HPLC GC 特征图 谱 2 1
2010年版 收载总数 2005年版 收载总数 新增
540
281
2962
1144
《中国药典》2010年版附录部分内容

通用检测方法和指导原则主要增修订内容
❖ 电位滴定 1、作图法 零阶 E~V曲线突跃部的中点或拐点所 对应的滴定液体积 一阶导数 一级微商(△E/△V)的极值 所对应的滴定液体积 二阶导数 二级微商(△2E/△V2)等于 零时所对应的滴定液体积
通用检测方法和指导原则主要增修订内容
❖ 2、计算法
二阶导数法较一阶导数法更准确,故最常用
通用检测方法和指导原则主要增修订内容
❖ 酸败度检查法 羰基值的原计算公式有误 羰基值= A
V2 ×1000 854 ×W
1、854的各种V1 醛的2,4-二硝基苯腙的ε,而不是mε 2、V1 供试品稀释总体积
V2 测定用供试品稀释液体积 S 25ml
5ml 25ml
3、修改为 羰基值= 125 ×A ×1000
c、具有足够的灵敏度(0.05mg/L) (3)TOC测量的意义 控制化学污染与微生物污染
通用检测方法和指导原则主要增修订内容
❖ 紫外-可见分光光度法 1、波长校正 增加了高氯酸钬溶液的校正(以10% 高氯酸为溶剂,配制含4%氧化钬的溶液) λmax nm:241.13,278.10,287.18,333.44, 345.47,361.31,416.28,451.30, 485.29,536.64,640.52nm。 2、波长允差 紫外区 ±1nm 500nm ±2nm 700nm ±4.8nm
采用线性内插法
V0=V+
a a+ b
△V
式中 V0:终点时的滴定液体积
a:二级微商为零前的二级微商值
b:二级微商为零后的二级微商值
V:二级微商为a时的滴定液体积
通用检测方法和指导原则主要增修订内容
❖ 不溶性微粒检查法
中国药典2010年版中成药标准的介绍

药味改用饮片名表述 例如:香附(醋制) →醋香附 例如:香附(醋制) 麦芽( 麦芽(炒) →炒麦芽 百部(蜜炙) 百部(蜜炙) →蜜百部 山楂( 山楂(焦) →焦山楂 药典未收载的炮制品仍沿用原名称 例如:杜仲叶(盐炙) →杜仲叶(盐炙) 例如:杜仲叶(盐炙) 杜仲叶(盐炙) 处方中的炮制品如药典未收载的特殊炮制方法将 附在该品种项下
4
技术要求
中药成分复杂, 中药成分复杂,应根据所含成分的化学 性质选择适宜的专属性方法。 性质选择适宜的专属性方法。对于不宜达 到专属性要求的一般理化鉴别、 到专属性要求的一般理化鉴别、荧光鉴别 及光谱鉴别,一般不宜采用。 及光谱鉴别,一般不宜采用。 检查项主要包括安全性、有效性、 检查项主要包括安全性、有效性、均一 性与纯度要求四个方面, 性与纯度要求四个方面,应根据中药制剂 的具体情况,研究建立合理的检查项目。 的具体情况,研究建立合理ቤተ መጻሕፍቲ ባይዱ检查项目。 5
气相色谱法
中药指纹图谱分析方法的建立应 中药指纹图谱分析方法的建立应能体现中药的 整体特征
在满足表征中药化学成分群整体性质的前提下, 在满足表征中药化学成分群整体性质的前提下,要求 有较好的重现性。明确了指纹图谱认证、方法验证、 有较好的重现性。明确了指纹图谱认证、方法验证、 数据处理及计算分析的依据和方法。 数据处理及计算分析的依据和方法。
应选择专属性成分、 应选择专属性成分、活性成分作为含量测定的 指标
避免选择无专属性的指标成分、 避免选择无专属性的指标成分、低活性的微量成分或水 解产物作为测定指标。 解产物作为测定指标。当单一成分不能反映该药的整体 活性时,应采用多成分或多组分的检测方法。 活性时,应采用多成分或多组分的检测方法。
14
1、鉴别项 新增各项鉴别 、鉴别项--新增各项鉴别 新增各项鉴别2165项 项
2010年中国药典制剂通则

(二)无菌与灭菌制剂 无菌与灭菌制剂 与灭菌
基本定义: 基本定义:系指直接注射于体内或直接用于创伤面、
粘膜等的一大类制剂。
灭菌制剂:系指采用物理、化学方法杀灭或除去所
有活的微生物繁殖体和芽孢的一类制剂。
无菌制剂:系指采用无菌操作方法或制备技术的不
含任何活的微生物繁殖体和芽孢的一类制剂。
基本分类:注射制剂(注射剂、粉针等)、眼用
注射用浓溶液
附录ⅠB注射剂增修概况介绍( 附录ⅠB注射剂增修概况介绍(二) ⅠB注射剂增修概况介绍
注射剂在生产与贮藏期间(一般要求) 注射剂在生产与贮藏期间(一般要求)
第一点: 除另有规定外 混悬型注射液中药物粒度应控制在15μm 除另有规定外, 第一点:…除另有规定外,混悬型注射液中药物粒度应控制在15μm 以下, 15~20μm(间有个别20 50μm) 20~ 不应超过10 10% 。 以下,含15~20μm(间有个别20~50μm)者,不应超过10%…。混 悬型注射液不得用于静脉注射或椎管注射 乳状液型注射液应稳定, 不得用于静脉注射或椎管注射; 悬型注射液不得用于静脉注射或椎管注射;乳状液型注射液应稳定, 不得有相分离现象,不得用于椎管注射。静脉用乳状液型注射液中乳 不得有相分离现象,不得用于椎管注射。静脉用乳状液型注射液中乳 分散相球粒)的粒度90%应在1μm以下,不得有大于5μm 90%应在1μm以下 5μm的 滴(分散相球粒)的粒度90%应在1μm以下,不得有大于5μm的乳滴 球粒) 除另有规定外,静脉输液应尽可能与血液等渗。 (球粒)。除另有规定外,静脉输液应尽可能与血液等渗。 第二点: 第二点:注射剂所用的原辅料应从来源及工艺等生产环节进行严格控 制并应符合注射用的质量要求。注射剂所用溶剂必须安全无害, 制并应符合注射用的质量要求。注射剂所用溶剂必须安全无害,并不 得影响疗效和质量。一般分为水性溶剂和非水性溶剂。 得影响疗效和质量。一般分为水性溶剂和非水性溶剂。 非水性溶剂:常用的为植物油, 等溶剂 等溶剂。 (2)非水性溶剂:常用的为植物油,…等溶剂。供注射用的非水性 溶剂,应严格限制其用量,并应在品种项下进行相应的检查。 溶剂,应严格限制其用量,并应在品种项下进行相应的检查。
《中国药典》2010年版增、修订情况简介

增多 ,特别是心功能 Ⅲ级与Ⅳ级患者。 参考文献
1 An h n s n NR, Ma fe a J, W a r n C t o ie nr d r e PW , e 1 tb — ta . i i An
b tuci e p m o a y tehe a y i x c r t on o hr n c o sr tv ul n r
・
药 事 管 理
・
《 中国药典 》2 1年版增 、修订情况简介 00
陈桂 良 王麟达 2 10 ) 02 3 ( 上海市食 品药品检验所 上海
中图分类号 :R 2 . 9 12
文献标识码 :C
文章编号 :1 0 — 3 (0 )9 0 2 — 3 6 1 32 1 0 — 4 2 0 0 5 0 正 文及 其引用 的附录共 同构 成。本部 药典 收载 的凡例 、 附录对药典 外其他 的 国家 药品标 准具 同等 法定约束 力 ; 着重强调 药品生产必须符合 G ,违反者即使按 《 MP 中国 药典 》检验合格 ,亦 不能认为符 合药典规定 ; 首次明确 药 品标 准正文 的定 义与 内涵 ,即系根据 自身 的理化与生 物学特 性 ,按处方来 源 、生产丁艺 、贮藏运输 等各 环节 制定 的 、用 以检测 药品质量是 否达到用药要 求并衡量其
探讨 [ ] J .四』I I 医学 ,2 0 , 2): 3 0 71 8 4 . (
性肺疾病诊治指南 ( 0 2 7年修订 )[ ] 0 J .巾华结核和呼吸杂
活工艺等 。
针 对有机溶剂 引入 了多层 意义 : 如凡生产过程 中引 入有机 溶剂 ,应在后 续工艺 中去 除 ,其残 留量应符 合附 录规定 ; 正文 中列 出的按正文方法 检测 ,正文 中未规定 检测 的也需要符合规 定。一部凡例还 针对大量 收载的饮
中国药典2010版第一部

中国药典2010版第一部
(原创版)
目录
1.引言:介绍《中国药典》及其 2010 年版的基本信息
2.《中国药典》2010 年版的主要内容
3.第一部的特点与重要性
4.第一部的主要章节和规定
5.结论:总结《中国药典》2010 年版第一部的主要贡献和影响
正文
《中国药典》是我国药品和药用辅料、直接接触药品的包装材料和容器的法定标准,是药品研发、生产、经营、使用和监管的重要依据。
2010 年版是该药典的第五版,其第一部是其中最重要的部分,涵盖了中药的基本要求、质量标准和检验方法等内容。
第一部的主要内容包括中药的来源、性状、鉴别、检查、浸出物测定、含量测定等。
其中,来源主要规定了中药材的采收、加工、贮存等环节,以保证其质量;性状则详细描述了中药的外观、气味、味道、水试、火试等特征,以便鉴别真伪;鉴别主要通过宏观和微观特征,如形状、大小、颜色、质地、组织结构等,以及理化和生物学特性,如旋光性、折光率、硬度、黏度、PH 值、酶谱、DNA 指纹等,来判断中药的真伪和品质;检查则规定了中药的重金属、农药残留、真菌毒素、杂质等污染物的限量,以保障用药安全;浸出物测定和含量测定则是评价中药有效成分含量的重要方法。
第一部的特点在于其全面性和严谨性。
全面性体现在它对中药的全过程进行了规定,从源头到成品,从质量到安全,涵盖了中药的各个方面;严谨性则体现在它对中药的鉴别和检查等环节的规定上,采用了现代科技手段,使得中药的质量控制更加科学和准确。
第一部的主要章节有中药的来源、性状、鉴别、检查、浸出物测定、含量测定等,规定了中药的基本要求、质量标准和检验方法。
其中,鉴别章节是第一部的重点,因为它是判断中药真伪和品质的关键。
