警惕含钆磁共振造影剂引起的肾源性系统纤维化
钆造影剂与肾源性系统性纤维化

肾源性 系统 性 纤 维 化 ( S ) 最 初认 为 是一 种 皮 慢性期可出现肢体水肿 ( NF , 多发生于下肢 ) 弥漫性皮肤 , 肤 疾 病 ,因 此 被 称 作 为 肾 源 性 纤 维 化 性 皮 肤 病 色素 沉着 , 硬结 , 下脂 肪纤 维 化 , 皮 组织 内还 可 出现
此将 N D 更 名 为 N F3。20 F S【 0 6年 , r nr4提 出 状 极 其相 似 , J Go e_ b 可通 过全 层皮肤 活 检进 行鉴 别诊 断 。
N F与磁共振血管造影成像 中使用钆对 比剂 (ao n S gdl — i
NF S 有其特殊组织病理学特征 , 目前可以通过皮 肤活检明确诊断 。 。。组织病理学可见真皮层胶原束 im—bsdcnrsaet,B A ) 关 。本文 就 N F u ae ot t gnsG C s有 a S 的临床特征 、 发生机制以及钆造影剂的分类特点进行 的排列增厚 , 黏蛋 白沉积 , D C 和 I 型前胶原束 的梭
宋立群 , 教授 , 士 生导 师 。首 届 国家 中医 药管理 局 优 秀 中 医临床 人 才 ; 博 黑龙 江省
名 中医。现为黑龙江中医药大学附属第一 医院肾内科主任。兼任 中华 中医药学会 肾病 分会委 员; 世界 中医药学会联合会第一届 内科 肾脏病专业委 员会常务理事 ; 中国中西医 结合 学会 肾脏疾病专业委 员会委 员; 黑龙 江省 中西 医结合 医学会 肾病专业委 员会副主 任委 员 ; 黑龙 江省 中 医药学会 肾病 专 业委 员会 副主 任委 员。 从事 中医教 学、 医疗、 科研近 3 年 , 0 以中医药治疗 肾脏疾病为研 究方向。依据 中医 药诊 治 肾 系疾病 的 长期 经验 , 结 和 凝 炼 出 肾 系疾 病 关键 病 机 是 “ ” “ ” “ ” 总 虚 、瘀 、水 、 “ 、 毒 ” 大环节 。提 出 了“ 本 兼 治 、 邪 为 先 ” 治 疗原 则 。并 承 担 和 完成 的科 浊” “ 五 标 祛 的 研课题 2 0余项 , 出版专著 1 , 0部 发表论文 10余篇 , 中3篇 S I 1 其 C 文章。获得省部级科研奖励 2 余项 , 0 培 养研 究 生 10余 人 。 1
肾源性系统性纤维化与磁共振含钆对比剂

nneago rpy MR 。部 分 学 者 已 开 始 尝 试 将 G C 作 a c n iga h , A) BA
为 X线 碘 对 比剂 的替 代 品 , 于对 碘 对 比 剂过 敏 或 肾 功 能 不 全 用
患 者 的 C DS 检 查 中。。 T、 A 。但 随 着 对 肾 源 性 系 统 性 纤 维 化
认识 。 NS 概 况 F
时 , 纤 维 细 胞 和 各 种 骨 髓 源 性 细 胞 ( o em r w dr e 成 b n a r —e i d o v
c l ) 如 造 血 干 细胞 、 el , s 内皮 祖 细 胞 、 质 母 细胞 及 单 核 纤维 细胞 间
Байду номын сангаас
等 , 组织 损 伤 和 各 种 细 胞 因 子 做 出 反 应 性 增 生 , 而 导 致 组 对 进
【中图 分 类号 1R4 5 2 4 . ;R6 2 9 ;R5 7 【 献 标 识码 】A 9 文 【 文章 编 号】1 0 3 3 2 1 7 2 0 1 —3 0 00 1 ( 0 0 0 — 2 90
自二 卜世 纪 八 1 年 代 第 一 种 钆 对 比 剂 ( a oi u b sd 一 g d l im— ae n c n rs a e t , B A) o t t g n s G C 马根 维 显 ( g e i ) 用 于 临床 以来 , a Ma n vs 应 t GB A 一 直被 认 为 是 一 种 安 全 可 靠 、 肾 毒 性 的 对 比 剂 , 广 C 低 而 泛应 用 于磁 共 振 增 强 扫 描 和 磁 共 振 血 管 成 像 ( g ei rs — ma n t eo c
织纤维化[ 。
NS F通 常 起 病 隐 匿 ,进 行 性 加 重 , 5 的 患 者 呈 暴 发 性 约 发病 并 迅 速 死亡 J 临床 上 NS 。 F是 一 种 以 组织 广 泛 进 行 性纤
MR增强检查注意事项说明

MR增强检查注意事项说明
MR增强检查时,需经静脉注射含钆对比剂,这样可提高检查的敏感性和特异性,有助于提高诊断的准确性。
目前研究表明,磁共振对比剂具有良好的耐受性,很少发生全身副反应,偶有轻微的局部反应。
*重度肾功能不全的患者(GFR<30ml/min1.73m2)不宜注射含钆对比剂。
目前的研究表明,重度肾功能不全的患者注射含钆对比剂与肾源性系统性纤维化的发生相关。
肾源性系统性纤维化可能累及心脏等重要器官,导致死亡。
因此重度肾功能不全是注射含钆对比剂的禁忌症。
*对有过敏倾向的患者,使用磁共振对比剂需慎重,因为产生过敏反应的机会较其他患者为高。
注射对比剂后,偶有恶心、呕吐及过敏性皮肤粘膜反应等。
注射过程中注射部位可出现短暂温热感或疼痛。
由于造影剂为高渗性,故注入血管旁组织可引起疼痛,20分钟左右消失,无其他组织反应。
极少数情况下可出现过敏样反应甚至休克,此种情况下MRI室会全力采取抢救措施。
*迄今所知,磁共振对比剂对肾功能不会产生影响,但肾功能不全者对比剂的排出会受到延迟。
* 在注射对比剂前一般要求禁食2小时。
一般过敏反应在注药后20分钟左右出现,故希望患者检查完成半小时后再离院,以便观察。
若离院后出现不适,请速就近医院诊治。
以上情况,在MRI增强检查前都应仔细认真了解工作人员会详细说明。
含钆对比剂引起肾源性系统纤维化的机理及防治

2006年5月,丹麦医药管理局首次报告25例使用钆对比剂后 发生NSF病例 2006年12月,美国FDA认为含钆对比剂与NSF有一定相关性 2007年5月23日,美国FDA要求企业对所有含钆对比剂加入一 黑框警告:
警告:有严重肾功能不全的患者使用含钆对比剂有发生NSF风险
1. 概论—NSF报道情况
Cowper S E, Robin H S, Steinberg S M, et al. Scleromyxoedema-like cutaneous diseases in renal-dialysis patients. Lancet, 2000,356:1000-1001.
1. 概论—NSF报道情况
含钆对比剂的类别、结构和NSF关系
含钆对比剂药代动力学
NSF发病机理
9. 小结
病理改变
纤维母细胞增生、胶原质重组及粘蛋白沉积
四肢皮肤变厚变硬,关节固定和挛缩,甚至导致死亡 病变皮肤广泛增厚,皮下组织弥漫性纤维化表现 严格掌握含钆对比剂使用禁忌症,使用前签署知情同意书 使用能达到诊断需求的最低剂量,不能超过推荐剂量 主要治疗手段为改善肾功能,辅以对症治疗
使用时剂量要求
肾功能不全患者在确有必要时才能使用钆对比剂 建议使用达到诊断需求的最低剂量 不能超过对比剂产品说明书推荐的剂量
7. 含钆对比剂NSF的预防
剂使用的适应证、禁忌证、 可能发生的不良反应和注意事项 使用钆对比剂的价值、危险性和可能的替代检查方法 如果出现异常反应,及时与相关医师联系 建议需要血液透析维持的患者,使用钆对比剂3h内行血透, 在临床安全允许条件下24h内行第2次血透
NSF

关于含钆磁共振造影剂与肾源性纤维化皮肤病的更新FDA已获悉一种新的疾病,肾源性系统性纤维化(Nephrogenic Systemic Fibrosis NSF)或称作肾源性纤维化皮肤病(Nephrogenic Fibrosing Dermopathy NFD),该病可发生于在MRI或MRA中使用钆造影剂的中晚期肾脏疾病患者中。
MRI扫描提供了内脏器官详尽清晰的图像。
MRA则利用钆造影剂获得更清楚的血管图像。
在一些MRI及所有MRA扫描中,都要将含钆造影剂注入患者血管来与其周边组织区别。
截至2006年12月21日,FDA已收到90例中晚期肾病患者在MRI或MRA钆造影检查后发生NSF/NFD 的报告。
NSF/NFD的发作时间在造影后2天至18个月不等。
许多患者(非所有患者)接受了高剂量的造影剂;部分只接受了一次造影。
鉴于这些报告,FDA向各卫生机构和患者作如下通告:l 中晚期肾病患者在接受MRI或MRA钆造影剂检查后,有可能出现导致健康衰竭,甚至死亡的NSF/NFD。
l 相信自己可能有NSF/NFD的患者应告知你的医生。
患有NSF/NFD的患者会出现局部皮肤僵硬、紧绷的感觉,以及可能出现局部器官疤痕。
NSF/NFD的症状还包括:皮肤烧灼感、发痒、水肿、变硬、变紧;红色或黑色斑块;巩膜黄斑;关节强直,行走、伸手、伸腿困难;髋骨、肋骨疼痛;肌无力。
l 中晚期肾病患者作影像检查时,尽可能选择MRI或MRA含钆造影剂检查以外的影像检查,如果病人确实需要钆造影剂检查,在做完MRI或MRA后应及时进行透析。
l FDA要求各卫生专业人员和病人对NSF/NFD可疑病例进行报告,按照MedWatch程序通过电话或internet 告知FDA。
全世界范围内,共约有215例病例报告。
在这些报告中,其中75例病例有详尽的病史回顾,这些病例均接受过MRI或MRA钆造影剂检查。
研究者已在这些患者的皮肤发现了钆。
为什麽接受MRI或MRA钆造影剂检查的中晚期肾病患者会出现NSF/NFD尚不清楚。
钆对比剂临床安全性应用中国专家建议
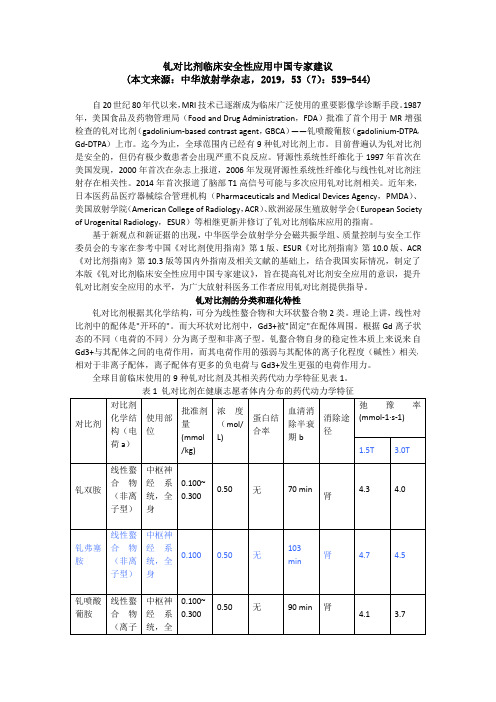
钆对比剂临床安全性应用中国专家建议(本文来源:中华放射学杂志,2019,53(7):539-544)自20世纪80年代以来,MRI技术已逐渐成为临床广泛使用的重要影像学诊断手段。
1987年,美国食品及药物管理局(Food and Drug Administration,FDA)批准了首个用于MR增强检查的钆对比剂(gadolinium-based contrast agent,GBCA)——钆喷酸葡胺(gadolinium-DTPA,Gd-DTPA)上市。
迄今为止,全球范围内已经有9种钆对比剂上市。
目前普遍认为钆对比剂是安全的,但仍有极少数患者会出现严重不良反应。
肾源性系统性纤维化于1997年首次在美国发现,2000年首次在杂志上报道,2006年发现肾源性系统性纤维化与线性钆对比剂注射存在相关性。
2014年首次报道了脑部T1高信号可能与多次应用钆对比剂相关。
近年来,日本医药品医疗器械综合管理机构(Pharmaceuticals and Medical Devices Agency,PMDA)、美国放射学院(American College of Radiology,ACR)、欧洲泌尿生殖放射学会(European Society of Urogenital Radiology,ESUR)等相继更新并修订了钆对比剂临床应用的指南。
基于新观点和新证据的出现,中华医学会放射学分会磁共振学组、质量控制与安全工作委员会的专家在参考中国《对比剂使用指南》第1版、ESUR《对比剂指南》第10.0版、ACR 《对比剂指南》第10.3版等国内外指南及相关文献的基础上,结合我国实际情况,制定了本版《钆对比剂临床安全性应用中国专家建议》,旨在提高钆对比剂安全应用的意识,提升钆对比剂安全应用的水平,为广大放射科医务工作者应用钆对比剂提供指导。
钆对比剂的分类和理化特性钆对比剂根据其化学结构,可分为线性螯合物和大环状螯合物2类。
磁共振钆对比剂的不良反应

磁共振钆对比剂的不良反应对比剂是医学影像检查中最常使用的药物之一,其不良反应的发生越来越受到重视。
对比剂不良反应包括肾脏外不良反应及肾脏不良反应。
按发生时间长短可分为急性不良反应、晚期不良反应及超晚期不良反应。
含钆对比剂在磁共振检查中被广泛使用,相对于碘对比剂,其不良反应的发生率较低,但程度可能很严重。
静脉注射0.1mmol/kg 或0.2mmol/kg含钆对比剂急性的肾脏外全身不良反应的发生率约0.07%-2.4%。
绝大多数程度很轻。
类过敏反应非常少见,发生率大约为0.004% -0.7%,最常见的症状是风疹或荨麻疹,气管痉挛罕见。
严重的、危及生命的过敏反应十分少见,发生率约0.001%~0.01%。
致死性不良反应有发生但十分罕见。
根据病情严重程度将不良反应分为轻度、中度及重度:•轻度不良反应症状及体征轻、可自限。
症状包括出汗、瘙痒、皮疹、荨麻疹、皮肤苍白或潮红、恶心、咳嗽、头痛、头晕、颜面部肿胀、发热、寒战、焦虑。
发生轻度不良反应的需观察着直至确认症状缓解或者没有进展,一般不需治疗。
•中度不良反应的症状和体征更显著。
表现为全身性或弥漫性红斑、心动过速或心动过缓、轻度低血压、高血压、支气管痉挛、喉头水肿。
病情可能进展,甚至危及生命,必须立即治疗,密切监测生命体征,开放静脉通道。
•重度不良反应常常危及生命。
表现为严重低血压、严重心律失常、心脏骤停、意识丧失、喉头水肿、惊厥。
需马上识别并立即积极抢救,密切监测生命体征,开放静脉通道。
对比剂急性不良反应的一般处理方法包括密切观察,监测生命体征,开放静脉通道,面罩吸氧(6~10L/min)。
静脉补液0.9%的生理盐水或林格乳酸液(儿童:10~20ml/kg,最大量不超过500-1000mL。
成人:1000mL,快速注射)。
特殊的处理:意识丧失及心脏骤停立即进行心肺复苏操作及心脏除颤。
出现荨麻疹可考虑使用苯海拉明。
儿童:口服、肌肉注射或静脉注射,剂量为1mg/kg体重,最高不超过50mg,静脉注射需缓慢,至少注射1~2min。
钆造影剂在肾病患者的应用2

肾性系统性纤维化(NSF)
• 最早报道于2000 • 没有年龄、性别、人种(?)差异 • 肾功能不全患者发生率0-7%(根据造影剂不同) • 主要发生于肾功能不全+接受钆造影剂患者,尤其是三类高危钆
造影剂使用后 • 可能机制:在肾损害患者中, 三价钆离子可能从鳌合物中通过机
体内离子的金属转移作用释放出来,游离的钆离子能刺激组织和 器官发生纤维化/刺激骨髓产生CD34+循环纤维细胞,从而导致 NSF。
钆在骨组织&脑组织沉积
• 肾功能正常者亦发生 • 静脉用药后8年钆仍可在骨组织中检测到 • 尸体解剖中发现钆造影剂在脑部神经核团(齿状核、桥脑、苍白
球、丘脑)中聚集 • 目前没有可靠的临床证据支持这种沉积带来的后果
Layne, K. A., et al. (2018). Br J Clin Pharmacol.
• Girardi, M., et al. (2011). "Nephrogenic systemic fibrosis: clinicopathological definition and workup recommendations." J Am Acad Dermatol 65(6): 1095-1106 e1097.
主要标准
特征性斑块
卵石样皮肤
关节挛缩
皮肤硬化
次要标准
浅表斑块
真皮丘疹
皮肤褶皱
巩膜斑块
病理改变
真皮细胞增多(+1)
小叶间隔受累(+1·)
弹性纤维保留(-1)
粗、细胶原蛋白束(+1)
异位骨化(+3)
CD34+细胞“电车轨道”样排列(+1)
含钆对比剂与肾源性系统性纤维化

放射学实践 20 0 8年 1月 第 2 3卷 第 1期
Ra il r ci ,a 0 8 Vo 3 No 1 do P a t e J n 2 0 , l , . c 2
・
对 比 剂 研 究 ・
含 钆 对 比剂 与 肾源 性系统 性纤 维化
i emo ah , D) 然 而 , 些 患 者 临 床 上 出 现 其 它 组 n d r p ty NF 。 g 有
织 [ 受 累 ( 、 骼 肌 肉 、 脏 隔 膜 和 食 管 等 ) 因 此 现 在 更 多 被 3 3 肺 骨 心 ,
协 作 修 改 的 新标 签 还 规 定 , 有 在 经 过 慎 重 考 虑 后 , 能 用 于 只 才
成 熟 本 身 导 致 发 生 NS F的风 险增 加 。
虽 然 N F 的 确 切 病 因 尚 在 研 究 中 , 有 报 道 使 用 含 钆 S 已
是 正 式 的 A R方 针 。 20 年 F C 07 DA指 出 , 尚未 收 到 任 何 中 度 肾 功 能不 全患 者发 生 NS F的 报 告 『 。 由于 新信 息 的 出 现 , 计 可 j 预 能会 重 新 考 虑 和修 改 蓝 丝 带 委 员 会 的 指 导 文件 。E U 最 近 发 SR 布 了“ S E UR指 南 : G 含 d对 比剂 与 肾 源 性 全 身性 纤 维 变 性 ”『 。 】 这 些指 南 的关 键 特征 是 区分 各 种 含 G d对 比 剂 。E UR 提 出 ” S 强
肝 移 植 围手 术 期 的任 何 严 重 程 度 的 急 性 肾 功 能 不 全 。 这 些 患 者 应 避 免 使 用 含 钆 类 制 剂 , 给 予 含 钆 对 比 剂 时 , 要 超 过 推 当 不 荐 剂 量 , 次 给 药 前 要 有 足 够 的 时 间 间 隔 使 该 对 比 剂 从 人 体 清 再
关于含钆造影剂的风险评估报告

大 约有 5 %的 患者 呈现 出快速 进展 的严 重发病
部、 脊柱和全身 MR 检 查 , I 通过静脉注射入体 内。 在心 过 程。NS F引起 的身体器 官纤维化 ( 损伤机体 正常生 脏 MR 检 查 中 ,钆 双 胺 可 以检 测 冠 状 动 脉 疾 病 理功能 ) I 可能会 导致死亡 。 呼吸抑制或行动障碍 ( 易引 ( A 。成人 中枢神经 系统 、 身 、 C D) 全 心脏和胸 部成 像 起意外摔伤而导 致骨折 ) 所致并发症 可使病情进一步 的推荐 剂量按 人体体 重 比例为 0] mo/g( 当 于 恶化 。部分患者 因肾脏疾病 或移植手术 已经死亡 。 . m l k 相 02 l g 最大 至 lO mo k )心脏 灌 注检 查推 荐 . / ), mk Om lg ; /
在一定 的联系 。 06年 1 月 , P V 20 1 在 h WP会议上讨论 信号强度 。
了更多的病例数据 ,其 中已核实的 4 例和待核 实的 8
游离 的钆具 有高毒性 ,在体 内分布 于骨骼 和肝
4 0例 N F与钆双胺 有关 , 例可 能与钆 喷酸葡胺 ( S 2 马 脏 , 并可迅速导致肝脏坏死 。 所有 的含钆 MR 造影剂 I 根维显 ) 有关 , 与其他含钆造 影剂相 关的病 例尚未 发 都是螯合物 , 螯合后能改变其在体 内的分布以确保图
性系统纤维化 (e h—oe iss mif rs , F 有 于如何避 免这种使人极其虚弱甚至致 命疾病 的指导 。 npr g n t c boi NS ) cye i s
关 。 97年 , 19 首次在美国发现了肾源性纤维化皮肤病 ,
本报 告就 当前有 价值 的数据进 行 了讨论 ,并对
维普资讯
含钆MR对比剂与肾源性系统性纤维化的关系

马春 忠 , 高继 斌
( 津 市 第 五 中心 医 院 放射 科 , 津 天 天 305 ) 04 0
MA h n z o g C u -h n ,GA0 ibn J— i —
(eate to a ioy i jn N . e t sil i j 04 0 hn) D p r n f R do g,T ni o C ne Ho t ,Ta i 3 0 5 ,C i m l a 5 r pa nn a
() 92 9 . 2 :2 -2 9
l 67 .
・
5 ・ 3
[7李 剑 明 , 军 , 晓 明 , . F F G P TC 11 辛 王 等 8— D E / T全 身 显 像 在 寻 找 肿 瘤 原 发 灶 中 的 临 床 价 值 [_中 国 肿 瘤 I ,0 7,4 1 ) 10 — J ] 临床 2 0 3 (7 :0 1
[8陈 钊பைடு நூலகம், 容 , 宁. F F E /T 的主 要 局 限性 和相 应 处 理 措 1] 郑 吴 — DG P TC
施 [ .中 国医 学 影 像 技 术 ,0 6,2 2 :2 — 2 . J 】 20 2 ( )3 0 33
【9Nan ,R b l D at lci , e 1 R l o F- D 1] a i C u el ,C s l c o e u P t . o a e f F G
黏 液 水 肿 样 皮 肤 病 ”2 0 年 又 对 其 临 床 和 组 织 学 特 点 进 行 ,0 1
【 键词】 纤维化 ; 疾病 ; 影剂 ; 关 肾 造 钆 【 图分 类 号】 R 9 ; 4 5 中 62R 4 . 2 [ 献 标 识 码】 B 文 【 章 编 号】 1 0 — 0 2 2 0 ) 1 0 5 — 2 文 0 8 1 6 (0 9 0 — 0 3 0
药品不良反应通报警惕含钆磁共振造影剂引起的肾源性系统纤维化

药品不良反应通报警惕含钆磁共振造影剂引起的肾源性系统纤维化作者:国家药品食品监督管理局来源:《中国社区医师》2008年第05期产品基本情况含钆造影剂用以提高图像的对比度。
使身体各部分的异常组织或患处显像。
静脉注射后,主要用于头部、脊髓和身体等一般MRI造影。
游离的钆具有高毒性,在体内分布于骨骼和肝脏,并可迅速导致肝脏坏死。
所有的含钆造影剂都是螯合物,螯合后能改变其在体内的分布以确保图像对比强度,同时改善其毒副作用。
与X线增强剂不同,钆螯合物对肾脏没有毒性。
因此。
近年来对严重肾损伤或曾对含碘造影剂严重过敏的患者。
推荐使用含钆造影剂来替代传统的放射成像用造影剂。
在我国,含钆造影剂钆喷酸葡胺注射液(商品名:马根维显)首先于1988年获得进口批准,目前我国上市的含钆类造影剂有钆贝葡胺注射液(商品名:莫迪司)、钆双胺注射液(商品名:欧乃影)、钆喷酸葡胺注射液和钆特酸葡胺注射液(商品名:多它灵)。
含钆造影剂引起NSF/NFD 的风险分析钆双胺(商品名:欧乃影)是第一个被报道与NSF有关的含钆造影剂。
目前全球有关含钆造影剂引起NSF病例的报告有200多例,其中欧乃影180例,马根维显78例,钆氟塞胺(opti-MARK)2例,莫迪斯1例(该患者也使用过欧乃影)(英国2007年6月和美国2007年3月公布数据),其他含钆造影剂还未收到类似的报告。
2006年1月,一项奥地利的研究认为含钆造影剂可能是诱发NSF的因素。
9例重症肾病患者中有5例(平均年龄58岁)在使用含钆造影剂进行磁共振血管造影后2~4周患上了NSF。
这5例患者开始表现为下肢和足部皮肤变厚硬结,然后蔓延至躯干和身体上部。
NSF患者与其他患者相比具有更长的血液透析史,但年龄、性别、用药、潜在肾病、透析阶段或并存疾病方面未表现出差异。
一项来自丹麦的大型研究也显示含钆造影剂与NSF的发生相关。
在2005年8月~2006年5月期间,哥本哈根的肾病中心回顾分析了所有NSF的病例后发现,所有13例严重肾病患者(平均年龄50岁)在第1次出现NSF的症状前均使用过钆双胺,7例发展成严重残疾(其中1例在使用含钆造影剂后21个月死亡),其余的6例没有产生严重的影响。
肾功能不全什么情况能做MRI增强扫描?

肾功能不全什么情况能做MRI增强扫描?嗨,⼤家好!
磁共振增强与平扫相⽐,能获得更多的病灶信息,有助于不同疾病的鉴别诊断。
磁共振增强所⽤造影剂多为含钆造影剂,⽽且多为⾮离⼦型顺磁性造影剂,静脉注射后可使磁共振发⽣T1对⽐增强,有助于医师获得更多信息,进⼀步明确病变性质。
简单介绍
排泄半衰期约为70-80分钟,静脉注射钆对⽐剂进⼊⼈体后,通过肾⼩球过滤后经肾脏排泄,排泄半衰期约为
那么,肾功能不4⼩时后约有80%的注射剂量通过尿液排泄,24⼩时后有95%-98%被排泄。
那么,肾功能不全患者能否⾏钆造影剂增强检查?
钆造影剂在严重肾功能不全患者体内清除时间延长,甚⾄在⼈体组织中沉积⽽导致肾源性系统纤维化。
研究表明,急性或慢性重度肾功能不全,即GFR<30ml/ (min. 1.73 m2),可能出现肾源性系统纤维化相关风险,使⽤剂量越⾼,风险越⾼。
简单总结
1、轻中度肾功能不全、GFR⽆明显异常者,⼤部分情况下可正常⾏磁共振增强检查,协助疾病诊断。
2、若肾功能严重不全,GFR<30ml/ (min. 1.73 ㎡),医师应权衡磁共振增强检查的利弊,并积极预防NSF发⽣。
3、GFR<15ml/ (min. 1.73 ㎡)的终末期肾病患者应禁⽤含钆造影剂,中度肾功能不全、
GFR<60ml/ (min. 1.73 ㎡)者,应权衡检查利弊,且最好使⽤低剂量)。
临床部分在申请MRI检查时并未提供具体eGFR值,可根据下⾯程序⽤肌酐值进⾏换算。
临床部分在申请MRI检查时并未提供具体eGFR值,可根据下⾯程序⽤肌酐值进⾏换算。
磁共振钆对比剂的不良反应

磁共振钆对比剂的不良反应对比剂是医学影像检查中最常使用的药物之一,其不良反应的发生越来越受到重视。
对比剂不良反应包括肾脏外不良反应及肾脏不良反应。
按发生时间长短可分为急性不良反应、晚期不良反应及超晚期不良反应。
含钆对比剂在磁共振检查中被广泛使用,相对于碘对比剂,其不良反应的发生率较低,但程度可能很严重。
静脉注射0.1mmol/kg或0.2mmol/kg含钆对比剂急性的肾脏外全身不良反应的发生率约0.07%-2.4%。
绝大多数程度很轻。
类过敏反应非常少见,发生率大约为0.004%-0.7%,最常见的症状是风疹或荨麻疹,气管痉挛罕见。
严重的、危及生命的过敏反应十分少见,发生率约0.001%~0.01%。
致死性不良反应有发生但十分罕见。
根据病情严重程度将不良反应分为轻度、中度及重度:轻度不良反应症状及体征轻、可自限。
症状包括出汗、瘙痒、皮疹、荨麻疹、皮肤苍白或潮红、恶心、咳嗽、头痛、头晕、颜面部肿胀、发热、寒战、焦虑。
发生轻度不良反应的需观察着直至确认症状缓解或者没有进展,一般不需治疗。
中度不良反应的症状和体征更显著。
表现为全身性或弥漫性红斑、心动过速或心动过缓、轻度低血压、高血压、支气管痉挛、喉头水肿。
病情可能进展,甚至危及生命,必须立即治疗,密切监测生命体征,开放静脉通道。
重度不良反应常常危及生命。
表现为严重低血压、严重心律失常、心脏骤停、意识丧失、喉头水肿、惊厥。
需马上识别并立即积极抢救,密切监测生命体征,开放静脉通道。
对比剂急性不良反应的一般处理方法包括密切观察,监测生命体征,开放静脉通道,面罩吸氧(6~10L/min)。
静脉补液0.9%的生理盐水或林格乳酸液(儿童:10~20ml/kg,最大量不超过500-1000mL。
成人:1000mL,快速注射)。
特殊的处理:意识丧失及心脏骤停立即进行心肺复苏操作及心脏除颤。
出现荨麻疹可考虑使用苯海拉明。
儿童:口服、肌肉注射或静脉注射,剂量为1mg/kg体重,最高不超过50mg,静脉注射需缓慢,至少注射1~2min。
磁共振检查以及体内植入物的安全性

磁共振检查以及体内植入物的安全性陈克敏;潘自来;姚侃敏;宋琦;杨燕敏【摘要】随着磁共振设备和技术的进展,其在临床上的应用已较前明显增加,体内植入物在临床治疗中的应用也已相当常见,磁共振检查和体内植入物的安全性已更多地受到了关注.本文就磁共振检查和对比剂使用的安全性及体内植入物,如支架、弹簧圈、滤器、动脉夹、骨科植入物、输液泵、起搏器等的安全性及相关事项进行了介绍和讨论.【期刊名称】《中国医学计算机成像杂志》【年(卷),期】2014(020)005【总页数】5页(P430-434)【关键词】磁共振;安全性;对比剂;植入物;装置【作者】陈克敏;潘自来;姚侃敏;宋琦;杨燕敏【作者单位】上海交通大学医学院附属瑞金医院北院放射科;上海交通大学医学院附属瑞金医院放射科【正文语种】中文【中图分类】R814.42磁共振检查自1980年代初期开始应用于临床后,由于其无X线辐射,软组织分辨率高,可直接进行多平面成像,特别是所用检查序列和参数多,信息量大,并可进行相关的功能性检查,使其应用逐年增加,使用范围不断扩大。
近年来随着磁共振设备和技术的进展和普及程度的增加,特别是3.0T MR的大量应用,磁共振检查的数量和应用范围将进一步增加,另一方面随着临床治疗的进展,各种新技术不断涌现,特别是支架等体内植入物应用的增多,磁共振检查的安全性已越来越受到关注和重视。
磁场对人体的影响目前临床上常用的MR设备多为0.2~3T场强,美国FDA的指南认为临床上使用的MR设备在8T及以内,对成人无明显的危险性和不良影响,超过8T场强的人体检查应获相关的伦理通过和有被检查者的知情同意,目前已有一些志愿者在9.4T MR上进行检查的相关报道,也未见明显的不良反应[1]。
人体在上述允许的静磁场短期暴露观察中无明显的生物效应损害发生,但目前尚无长期暴露在静磁场中对人体影响的系统报告。
由于梯度场的快速切换,将产生导电组织的感应电流,并可刺激神经和肌肉及产生一定的影响。
关于含钆造影剂的风险评估报告

关于含钆造影剂的风险评估报告
钟露苗
【期刊名称】《中国药物警戒》
【年(卷),期】2007(004)003
【摘要】2006年1月,含钆磁共振成像(MRj)造影剂被推测与一种罕见、甚至致命的疾病——肾源性纤维化皮肤病(nephrogenic fib—rosing dermopathy,NFD)/肾源性系统纤维化(nephr—ogenic systemic fibrosis,NSF)有关。
1997年,首次在美国发现了肾源性纤维化皮肤病,它作为一种特发性皮肤疾病,其主要特征为:四肢皮肤变厚变硬,有时会发生在躯干部,同时伴有皮肤纤维母细胞样细胞的增生、胶原质重组及粘蛋白沉积。
【总页数】6页(P180-185)
【作者】钟露苗
【作者单位】湖南省药品审评认证及不良反应监测中心,湖南,长沙,410001
【正文语种】中文
【中图分类】R915.5;R814.43
【相关文献】
1.黄葵胶囊在预防钆造影剂诱导的肾源性系统纤维化中的作用黄葵胶囊在预防钆造影剂诱导的肾源性系统纤维化中的作用 [J], 张艳;王琳
2.从通报含钆磁共振造影剂看我国的药品风险管理 [J], 吴桂芝;田春华;陈易新
3.含钆造影剂脑内沉积的研究现状 [J], 刘金沙;伍建林
4.半剂量含钆造影剂T2-FLAIR增强在脑膜瘤病灶强化中的应用价值 [J], 于秀英;
何勇;姚振威;韩广;韩召春;刘松国;陈晓军
5.EMA采取措施减小含钆造影剂的使用风险 [J],
因版权原因,仅展示原文概要,查看原文内容请购买。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2008-1-7
药品不良反应信息通报(第13期)
7
NSF仅发生在肾功能损害的患者身上。 NSF的发病时间为几天到几个星期。皮肤变 化首先是发红或发黑、出现丘疹斑块,随后 皮肤麻木,表皮呈现桔黄色条形纤维状。疾 病诊断根据皮肤活体组织检查的特定组织学 病理特征来确定:胶原束增厚且周围出现裂 缝,粘蛋白沉积,纤维母细胞样细胞和弹性 纤维增生而无发炎症状。
2008-1-7
药品不良反应信息通报(第13期)
8
皮肤损害一般发生在踝关节至大腿之间, 呈对称状。疾病后期,损害部位会扩展到腕 关节和上臂之间。病人感到患部烧灼、瘙痒 或剧烈刺痛,也可能出现手脚浮肿并呈水泡 状。另外,有些患者眼睛或附近出现黄色丘 疹、斑块;也曾有病例在皮肤损害前出现不 明原因血压快速波动的情况。
部。NSF患者与其他患者相比具有更长的血
液透析史,但年龄、性别、用药、潜在肾病、
透析阶段或并存疾病方面未表现出差异。
2008-1-7
药品不良反应信息通报(第13期)
14
一项来自丹麦的大型研究也显示含钆造 影剂与NSF的发生相关。在2005年8月至 2006年5月期间,哥本哈根的肾病中心回顾 分析了所有NSF的病例后发现,所有13例严 重肾病患者(平均年龄50岁)在第一次出现 NSF的症状前均使用过钆双胺,7例发展成 严重残疾(其中1例在使用含钆造影剂后21 个月死亡),其余的6例没有产生严重的影 响。自2006年3月该中心停用钆双胺后,未 再发现NSF病例。
相关研究,同时密切关注我国含钆造影剂的不良反
应发生情况,虽然我国目前尚未发现含钆造影剂诱 发NSF的报告,但是为了广大医护人员和患者及时 了解含钆造影剂可能诱发NSF的风险,保障临床用 药安全,国家药品不良反应监测中心特通报此安全 信息。
2008-1-7
药品不良反应信息通报(第13期)
3
二、产品基本情况
含钆造影剂用以提高图像的对比度,使身体各部分 的异常组织或患处显像。静脉注射后,主要用于头
部、脊髓和身体等一般MRI造影。游离的钆具有高 毒性,在体内分布于骨骼和肝脏,并可迅速导致肝
脏坏死。所有的含钆造影剂都是螯合物,螯合后能 改变其在体内的分布以确保图像对比强度,同时改 善其毒副作用。
与X射线增强报(第13期)
13
2006年1月,一项奥地利的研究认为含 钆造影剂可能是诱发NSF的因素。9例重症 肾病患者中有5例(平均年龄58岁)在使用 含钆造影剂进行磁共振血管造影后2~4周患 上了NSF。这5例患者开始表现为下肢和足
部皮肤变厚硬结,然后蔓延至躯干和身体上
2008-1-7
药品不良反应信息通报(第13期)
9
许多患者皮肤增厚阻碍了关节的弯曲和伸 展,导致挛缩变形,严重的患者有可能不能 行走,甚至手臂、手部、腿和脚关节不能活 动。患者一般均呈现肌肉虚弱的症状。X射 线检查显示软组织钙化,髋骨、肋骨出现深 部骨痛。
2008-1-7
药品不良反应信息通报(第13期)
2008-1-7
药品不良反应信息通报(第13期)
17
五、含钆造影剂诱发NSF的机理
含钆造影剂引起NSF的机制目前还在研 究阶段。目前认为:肾损伤是一个重要的因 素,因为NSF只发生在严重肾功能不全的患 者身上,他们需要花费更长的时间排除体内 的造影剂。在肾损害患者中, 三价钆离子 可能从鳌合物中通过机体内离子的金属转移 作用释放出来,游离的钆离子能刺激组织和 器官发生纤维化,从而导致NSF。
2008-1-7
药品不良反应信息通报(第13期)
18
钆在人体组织内沉积已在NSF患者组织中得到
核实。High等人检测了7例发生NSF前使用过含钆
造影剂的患者体内的13个组织,其中有4个组织出
现了钆沉积现象。而且患者在使用含钆造影剂11
个月后仍能在其组织样本中检测到钆,而未发生
NSF的患者组织样本中未检测到钆。Boyd等人也
警惕含钆磁共振造影剂引起的肾 源性系统纤维化
2008-1-7
药品不良反应信息通报(第13期)
1
一、背景
2006年1月,奥地利一项研究中报道5名NSF患者 可能与使用过含钆造影剂相关。随后丹麦医药管理 局于2006年5月报告了25例使用含钆造影剂后发 生NSF的病例,其中20例发生在丹麦,5例发生在 奥地利。同年6月美国也通告了此信息。随着与含 钆造影剂有关的NSF病例报告逐渐增多,多项相关 研究的陆续发表,美国FDA于2006年12月更新了 含钆造影剂可能会诱发NSF的信息,认为含钆造影 剂与NSF有一定的相关性。英国等欧盟国家于 2007年2月警告了含钆造影剂可能引起NSF的风险, 并修改了含钆造影剂的说明书。
证实了NSF患者体内钆的沉积现象,发现沉积的发
生一般有区域性限制,且该区域内也出现磷酸钙的
沉积。钆在组织中沉积可以通过多种机制诱发NSF,
如循环成纤维细胞和转化生长因子的介入等。
2008-1-7
药品不良反应信息通报(第13期)
19
六、建议
鉴于含钆造影剂具有可能诱发NSF的风 险,建议广大医护人员严格按照适应症使用, 不要超剂量使用,并在使用前应注意患者肾 功能情况,并且应在体内的造影剂清除后, 才可再次使用。严重肾功能不全的患者使用 含钆造影剂后,应及时进行血液透析,以帮 助患者尽快排出体内的钆,减少钆在患者体 内停留的时间。
10
大约有5%的患者呈现出快速进展的严 重发病过程。NSF引起的身体器官纤维化 (损伤机体正常生理功能)可能会导致死亡, 呼吸抑制或行动障碍(易引起意外摔伤,而 导致骨折)所致并发症使病情进一步恶化。
2008-1-7
药品不良反应信息通报(第13期)
11
目前,对NSF尚无有效的治疗方法。物 理治疗或局部、系统类固醇药物疗法都具有 不确定的疗效。免疫抑制疗法是无效的。血 浆去除法、光量子疗法和镇静剂对某些患者 的症状有些改善。有些患者在自然条件或在 肾移植恢复正常肾功能后症状得到改善。
2008-1-7
药品不良反应信息通报(第13期)
2
自2006年报道含钆造影剂可能诱发NSF以来,国 家药品不良反应监测中心一直对含钆造影剂引起 NSF的风险保持高度关注,及时跟踪国外最新的安 全性信息,并在中心网站()和 《中国药物警戒》杂志等载体中刊载了相关信息及
2008-1-7
药品不良反应信息通报(第13期)
15
Broome等人的研究结果表明肾透析患 者使用钆双胺后有发生NSF的风险。研究中 使用过钆双胺的301例肾透析患者中有12例 已确诊患有NSF,而未使用过钆双胺的258 例中未发现NSF病例,使用钆双胺后发生 NSF的比数比为22.3[95%,CI 1.3~ 378.9]。另外,研究还表明当钆双胺使用 剂量为推荐剂量的2倍时,其风险度将明显 增加。
2008-1-7
药品不良反应信息通报(第13期)
5
三、肾源性纤维化皮肤病/肾源性系统纤 维化(NFD/NSF)
1997年,肾源性纤维化皮肤病 (Nephrogenic Fibrosing Dermopa- thy, NFD)首次在美国被发现,于2000年 首次在杂志上公开发表。NFD作为一种特发 性皮肤病,其主要特征为:四肢皮肤变厚变 硬,有时会发生在躯干部,同时伴有皮肤纤 维母细胞样细胞的增生、胶原质重组及粘蛋 白沉积。
2008-1-7
药品不良反应信息通报(第13期)
20
2008-1-7
药品不良反应信息通报(第13期)
6
NFD较NSF具有更明显和可见的皮肤病变 特征,NSF涉及到肺、肝、肌肉和心脏等器 官[3]。国际肾源性纤维化皮肤病研究中心 ()认为,NSF这 一术语比NFD更确切,它能更准确地反应目 前人们对此疾病的理解。因此,在本通报中 用NSF来表示NFD和NSF。
性。因此,近年来对严重肾损伤或曾对含碘造影剂
严重过敏的患者,推荐使用含钆造影剂来替代传统
的放射成像用造影剂。
2008-1-7
药品不良反应信息通报(第13期)
4
在我国,含钆造影剂钆喷酸葡胺注射液 (商品名:马根维显)首先于1988年获得 进口批准,目前我国上市的含钆类造影剂有 钆贝葡胺注射液(商品名:莫迪司)、钆双 胺注射液(商品名:欧乃影)、钆喷酸葡胺 注射液和钆特酸葡胺注射液(商品名:多它 灵)。
2008-1-7
药品不良反应信息通报(第13期)
12
四、含钆造影剂引起NSF/NFD的风险分 析
钆双胺(商品名:欧乃影)是第一个报 道与NSF有关的含钆造影剂。目前全球有关 含钆造影剂引起NSF病例报告有200多例, 其中欧乃影:180例;马根维显:78例;钆 氟塞胺(optiMARK):2例;莫迪斯:1例 (该患者也使用过欧乃影)(英国2007年6 月和美国2007年3月公布数据),其他含钆 造影剂还未收到类似的报告。
2008-1-7
药品不良反应信息通报(第13期)
16
在另一项研究中,254例肾功能不全的 患者在使用含钆造影剂后有7例发生了NSF, 发生率为3%。在Broome的研究中,透析 患者使用含钆造影剂后NSF的发生率为4%。 接受过肝移植手术的患者也报道存在NSF发 生的风险。
综上所述,含钆造影剂存在诱发 NSF/NFD的风险。
