第四章 重排反应
重排反应——精选推荐

重排反应有机化学中重排反应很早就被⼈们发现,研究并加以利⽤。
第⼀次被Wohler 发现的,由⽆机化合物合成有机化合物,从⽽掀开有机化学神秘⾯纱的反应—加热氰酸铵⽽得到尿素,今天也被化学家归⼊重排反应的范畴。
⼀般地,在进攻试剂作⽤或者介质的影响下,有机分⼦发⽣原⼦或原⼦团的转移和电⼦云密度重新分布,或者重键位置改变,环的扩⼤或缩⼩,碳架发⽣了改变,等等,这样的反应称为是重排反应。
按照反应的机理,重排反应通常可分为亲核反应、亲电反应、⾃由基反应和周环反应四⼤类。
也有按照不同的标准,分成分⼦内重排和分⼦间重排,光学活性改变和不改变的重排反应,等等。
⼀、亲核重排重排反应中以亲核重排为最多,⽽亲核重排中⼜以1,2重排为最常见。
(⼀)亲核1,2重排的⼀般规律1.亲核1,2重排的三个步骤:离去基团离去,1,2基团迁移,亲核试剂进攻2.发⽣亲核1,2重排的条件(1)转变成更稳定的正离⼦(在⾮环系统中,有时也从较稳定的离⼦重排成较不稳定的离⼦)(2)转变成稳定的中性化合物(3)减⼩基团间的拥挤程度,减⼩环的张⼒等⽴体因素。
(4)进⾏重排的⽴体化学条件:带正电荷碳的空p轨道和相邻的C-Z 键以及α碳和β碳应共平⾯或接近共平⾯(5)重排产物在产物中所占的⽐例不仅和正电荷的结果有关,⽽且和反应介质中存在的亲核试剂的亲核能⼒有关3.迁移基团的迁移能⼒(1)多由试验⽅法来确定基团的固有迁移能⼒(2)与迁移后正离⼦的稳定性有关(3)邻位协助作⽤(4)⽴体因素4.亲核1,2重排的⽴体化学:(1)迁移基:构象基本保持,没有发现过构型反转,有时有部分消旋(2)迁移终点:取决于离去及离去和迁移基进⾏迁移的相对时机5.记忆效应:后⼀次重排好像和第⼀次重排有关,中间体似乎记住了前⼀次重排过程(⼆) 亲核重排主要包括基团向碳正离⼦迁移,基团向羰基碳原⼦迁移,基团向碳烯碳原⼦迁移,基团向缺电⼦氮原⼦转移,基团向缺电氧原⼦的迁移,芳⾹族亲核重排,下⾯就这六种迁移作简要介绍:1.基团向碳正离⼦迁移:(1)Wagner-Meerwein重排:烃基或氢的1,2移位,于是醇重排成烯(2)⽚那醇重排:邻⼆醇在酸催化下会重排成醛和酮(3)Demyanov重排,Tiffeneau-Demyanov扩环以及有关反应(4)⼆烯酮-酚重排:4,4-⼆取代环⼰⼆烯酮经酸处理重排成3,4-⼆取代酚的反应(5)醛酮同系物的合成:醛或酮和重氮甲烷作⽤⽣成⾼⼀级的同系物(6)烯丙基重排:烯丙基系统中双键发⽣位移的反应2.基团向羰基碳原⼦迁移:(1) Benzil-Benzilic Acid重排:α-⼆酮经强碱处理会发⽣重排,⽣成α-羟基⼄酸盐(2) 酸催化下醛酮的重排:在烃基的交换后,醛重排成酮,酮则重排成另⼀种酮3.基团向碳烯碳原⼦迁移:(1) Arndt-Eistert合成和Wolff重排:由羧酸经酰卤,重氮酮合成⾼⼀级同系物的⽅法(2) 其他的碳烯重排反应,主要是1,2氢迁移⽣成烯4.基团向缺电⼦氮原⼦转移:(1)Beckmann重排:醛肟或酮肟重排成酰胺(2)Hoffmann重排:氮上⽆取代基酰胺经溴及碱处理,脱羰⽣成伯胺(3)Curtius重排:酰基叠氮热分解⽣成异氰酸酯(4)Schmidt重排:酸、醛和酮在酸催化下和叠氮酸反应,⽣成胺、酰胺等的反应(5)Lossen重排:异羟肟酸及O-酰基衍⽣物经类似Hoffmann的重排⽣成少⼀个碳的胺(6)Neber重排:肟酮的磺酸酯在⼄醇钾处理后⽔解⽣成α-氨基酮5.基团向缺电氧原⼦的迁移:(1)氢过氧化物的重排:氢过氧化物在酸催化下,O-O键断裂,同时烃基从碳原⼦迁移到氧原⼦上(2)Baeyer-Villiger重排:酮在酸催化下与过酸作⽤,在分⼦中插⼊氧⽣成酯的反应6.芳⾹族亲核重排:(1)芳羟胺重排(Bamberger重排):经硫酸处理重排成氨基酚(2)Sommelet-Hauser重排:苄基季胺盐经氨基钠等强碱处理重排成邻位取代的苄基叔胺⼆、⾃由基重排反应1.1,2迁移:⽐正离⼦重排反应少得多,主要发⽣在:(1)某些双⾃由基的1,2-烷基和氢(2)烯基(迁移的⼄烯基若是环的⼀部分,则发⽣重排)2.⾮1,2迁移:多发⽣1,5迁移3.Barton反应:处于羟基δ位上的甲基氧化成醛基的反应4.Hofmann-loffler-freytag反应:质⼦化N-卤化胺经热分解或光解形成六氢吡啶等的反应。
第四章重排反应解读

R2
R1 R3 C C R4 OH OH
H
R2
R1 C C R4 R3 O
1. 反应机理:
II
H 3C CH3 C CH3 C CH3 H+ H 3C CH3 C CH3 C CH3 -H 2O H 3C CH3 C OH CH3 CH3 C O C CH3 CH3 C + CH3
HO OH CH3 重排 CH3 C C CH3
HO
CH2
O (4)
OH
OH
三、苯偶酰-二苯乙醇酸型重排
• 二苯基乙二酮(苯偶酰)类化合物用碱处理,生成二苯基-羟 基酸(二苯乙醇酸)的反应称为苯偶酰-二苯乙醇酸型重排反 应。
O Ar C
O C Ar
OH O KOH
△
Ar
C Ar
C
OK
1. 反应机理
C6H5 C C C6H5 + OH O O O O C C OH C6H5
HO +OH2 -H+
HO + CH3
CH3
III 重排反应的动力是:由三级C+生成更加稳定的质子化的酮
注意问题:
1)驱动力? 2)两个羟基中谁先离去?(生成的正碳离子稳定性) 3)哪个基团迁移? 4)立体化学上离去基与迁移基成反式共平面
5)扩展反应
6)应用
羟基位于脂环上的邻二叔醇化合物在酸或Lewis酸的催 化下发生重排,生成扩环脂肪酮、螺环酮
H+ -H2 O H+
(CH3)3C-CH2 (CH3)3C-CH-CH3
2. 迁移基团迁移顺序 易带负电荷或带负电荷后相对稳定、且易给出电子的基团容易
迁移。据此, 可得出一般情况下迁移基团的活性顺序。
第四章 重排反应

重排开始 O 环丙酮
R1 R3
R1 R3
A
R2 C C.. R4 ROH R2 C CHR4
OC OR
重排结束O
C OR
R1 R3
R1 R3
B
R2 C.. C R4 CO
ROH
R2CH C R4 RO 中R=H C O 时则得到羧酸
OR
OR
反应中究竟以A方式开环,还是以B方式开环,
则决定于碳负离子的稳定性。
• 酸催化质子化脱水后重排 • 酰卤催化剂则是将羟基酯化后脱去酰氧基
R
OH R''COCl
CN
R'
O
R C
O N
C R'' -CH3COO-
R'
[ R C N R'
R C N R' ]
H2O
-H+
R C NH R' O
• 空间结构的影响
O2N
Ph N
PClO5 2N
O
O2N
NHPh H2O
Br OH
对甲氧基苯基 > 对甲基苯基 > 苯基 > 对溴苯基 > 烷基 > 氢
优先产生稳定
碳正离子
Ph2C CH2 H+ Ph2C+ CH2
OH OH -H2O
OH
Ph2CH CH +OH
H+
Ph2CH
CH O
PhHC CHPh H+ PhHC CHPh
OH OH -H2O
+
OH
Ph2CH CH +OH
H+
1、片呐醇(Pinacol)重排—分子内C→C重排
第四章 重排反应

二、Pinacol重排反应 重排反应
若反应中形成正离子,除了上面的相应双键进行亲电加成外, 若反应中形成正离子 , 除了上面的相应双键进行亲电加成外 ,还 可以由迁移H原子、烃基、芳基或其它带有一对电子的基团而变得稳定。 可以由迁移 原子、烃基、芳基或其它带有一对电子的基团而变得稳定。 原子 当这些迁移进行十分顺利时,在合成上就有应用价值。 当这些迁移进行十分顺利时,在合成上就有应用价值。特别是与形成正 离子的相邻碳原子上带有羟基时, 离子的相邻碳原子上带有羟基时,由羟基转变为羰基化合物是一个有利 的重排方式。由酸催化邻二醇形成酮的反应,称为“ 重排。 的重排方式。由酸催化邻二醇形成酮的反应,称为“Pinacol”重排。 重排
O TFA, C6H6
O
∆
H 2400C
100% H
H
H 83%
2、Claisen 重排 、
其与Cope重排完全相似, 只不过将其中的一个 重排完全相似,只不过将其中的一个CH2 变为氧 。 在有 变为氧。 其与 重排完全相似 机合成中常用于构建一些难以合成的官能团,具有非常重要的应用价值。 机合成中常用于构建一些难以合成的官能团,具有非常重要的应用价值。
烯烃 异丁烯 苯乙烯
.CCl3 1.00 >19
:CBr2 1.00 0.4 3.2
Br2 1.00 0.6 1.9
环氧化反应 1.00 0.1 13.5
3-甲基 丁烯 0.17 甲基1-丁烯 甲基
一些与环状共轭体系相连的卡宾如环丙烯卡宾和环庚三烯卡宾, 一些与环状共轭体系相连的卡宾如环丙烯卡宾和环庚三烯卡宾,在 这些分子中,空的P轨道参与共轭体系 不显示明显的缺电子特征, 轨道参与共轭体系, 这些分子中,空的 轨道参与共轭体系,不显示明显的缺电子特征,实 际上是环丙烯正离子和卓鎓离子的共轭碱。 际上是环丙烯正离子和卓鎓离子的共轭碱。
重排反应总结

重排反应总结1、什么叫重排反应?一般地,在进攻试剂作用或者介质的影响下,有机分子发生原子或原子团的转移和电子云密度重新分布,或者重键位置改变,环的扩大或缩小,碳骨架发生了改变等等,这样的反应称为重排反应。
简单的理解:重排反应是指反应中烃基或氢原子或别的取代基从分子中的一个原子迁移到该分子中的另一个原子上的变化。
(指分子内重排)2、重排的分类按反应机理 ,重排反应可分为:基团迁移重排反应和周环反应中的重排。
基团迁移重排反应 即反应物分子中的一个基团在分子范围内从某位置迁移到另一位置的反应。
常见的迁移基团是烃基。
基团迁移重排反应又包括缺电子重排(亲核重排),富电子重排(亲电重排)和自由基重排.。
周环反应中的重排包括电环反应、σ键迁移。
也可按照不同的标准,分成分子内重排和分子间重排,光学活性改变和不改变的重排反应等等。
本讲义把重排分为以下几类:a.从碳原子到碳原子的重排 b.从碳原子到杂原子的重排 c.从杂原子到碳原子的重排 d.其它重排一、从碳原子到碳原子的重排反应1、Wangner-Meerwein 重排(瓦格纳尔—米尔外英重排,简称瓦—米重排)两个相邻原子之间发生的重排叫1,2重排,也叫Wangner-Meerwein 重排。
如:醇或卤代烃在酸催化下进行亲核取代或消除反应时,烯烃进行亲电加成时发生的重排。
例如:a.亲电加成时发生的重排如果反应液中同时存在两种或是两种以上的亲核试剂,则通过中间体碳正离子,能够生成混合加成产物。
R 2C R 3R 1C OHR 4R 5R 2C R 3R 1CR 4R 5R 1CR 2C R 3R4R 5R1CR 2CR 3R 4R 5OH H +(-H O)重排H O(-H +)b.醇进行亲核取代和消除时的重排亲核取代时,除大多数伯醇难以形成正碳离子而按S N 2反应外,仲醇或叔醇反应常伴随着重排产物的产生。
(S N 1)消去时(S N 1):c.卤代烃进行亲核取代和消除时的重排亲核取代按S N 1机理反应时伴随着碳正离子的重排 消去时注意:有碳正离子形成时,就有可能伴随着重排反应 形成C +的方式总结: (a)卤代烃 (AgNO 3醇溶液) (b)含-NH 2,重氮化放氮气(c)-OH ,加 H + (失H 2O),烯烃加H +基团迁移顺序:对迁移顺序的理解:迁移基团的电子云密度越大越容易迁移(但具体情况下,要具体分析)(CH 3)3C-CH 2Cl(CH 3)32Ag (AgNO 3(CH 3)3C-CH 2N 2Cl-N 2(CH 3)3C-CH 2(CH 3)3C-CH 3NH 2NaNO 2△(CH 3)3C-CH 2OH (CH 3)3C-CH 2=CH 2(CH 3)32(CH 3)33H +2H +ClR 3C-R 2CH-RCH 3-CH 3-H->>>>>>OCH 3>反应举例:2、Pinacol (频哪醇)重排(邻二醇重排)当起始物的脱水产物能产生两种不同的正离子时,总是生成更稳定的正碳离子为主,有不同迁移基团时,按迁移的难易程度进行。
重排反应

重排反应(rearrangement reaction)是分子的碳骨架发生重排生成结构异构体的化学反应,是有机反应中的一大类。
重排反应通常涉及取代基由一个原子转移到同一个分子中的另一个原子上的过程。
以下例子中取代基R由碳原子1移动至碳原子2:分子间重排反应也有可能发生。
按反应机理,重排反应可分为:基团迁移重排反应和周环反应。
基团迁移重排反应反应物分子中的一个基团在分子范围内从某位臵迁移到另一位臵的反应。
常见的迁移基团是烃基。
迁移基团的原来位臵称为迁移起点,迁移后的位臵称为迁移终点,这类反应又可按价键断裂方式分为异裂和均裂,前者重要得多,其中尤以缺电子重排最为重要。
缺电子重排反应是反应物分子先在迁移终点形成一个缺电子活性中心,从而促使迁移基团带着键裂的电子对发生迁移,并通过进一步变化生成稳定产物。
以频哪酮重排反应为例,反应物分子中的一个羟基与酸作用形成锌盐后失水变为缺电子活性中心正碳离子,促使邻位带羟基碳原子上的一个甲基带着电子对发生1,2-迁移,同时羟基氧原子上未共用电子对转移至碳?氧之间构成双键,最后失去质子而得产物(见上反应式)。
在迁移终点形成一个富电子活性中心后,促使迁移基团不带键裂电子对而转移,叫富电子重排反应,例如法沃斯基重排:a - 卤代酮在强碱作用下重排,生成碳架不同的羟酸酯,反应通过富电子活性中心负碳离子进行:环反应反应物因分子内共价键协同变化而发生重排Favorsky重排反应的反应,有电环化反应和δ迁移反应。
例如环丁烯经加热发生逆向电环化而得1,3-丁二烯,1,3-己二烯经加热发生氢原子1,5-迁移而得2,4-己二烯。
这类重排在合成中应用最多的是属于3,3-迁移的科普重排和克莱森重排。
科普重排是1,5-二烯受热重排为另一个1,5-二烯的反应。
例如内消旋-3,4-二甲基-1,5-己二烯经加热几乎定量地转变为(Z ,E)-2,6-辛二烯:克莱森重排反应是参与反应的体系中有一个氧原子代替了碳原子。
第二部分 第四章 重排反应

H2O
CH3CH2CHCH2
CH3CH2CH+CH3
CH3CH=CHCH3
亲电重排: 亲电重排:
Ph CH2 O CH3 PhLi C6H6
Ph CH O CH3
Li+
CH3 - + H2O Ph CH O Li
自由基重排
Cl Cl C CH=CH2 Cl Br
CH3 Ph CH OH
Cl Cl C CH CH2Br Cl
本课程按照活泼中间体或机理进行分类讲解, 本课程按照活泼中间体或机理进行分类讲解, 着重介绍以下几类型反应: 着重介绍以下几类型反应: 1、经过正离子重排 、 2、经过负离子重排 、 3、经过卡宾Carbene 、氮宾 、经过卡宾 氮宾Nitrene重排 重排 4、σ-迁移反应(属于周环重排) 、 迁移反应 属于周环重排) 迁移反应(
H2O
R C N R' OH2
-H+
R C N R' OH
互变 异构
R C NH R' O
脱羟、重排、夺羟、 脱羟、重排、夺羟、互变
举例
Et 例 1 n-Bu C C Me H N OH
H2SO4 乙醚
Et O n-Bu C N C CH3 H H
例2 C N OH
NO2
PCl5
NO2 N C OH HN C O
NH2 HNO2 OH
CHO
试分析
CH2NH2 OH
HNO2
O
• 通常经过三元环碳正离子历程,迁移基团从离去基 通常经过三元环碳正离子历程, 三元环碳正离子历程 团背后迁移。 团背后迁移。
CH3 H ph NH2 OH HO Me NH2 H OCH3
《有机化学重排反应》课件

THANKS
感谢观看
详细描述
重排反应通常涉及分子内部的重排,包括电子、质子和原子的重新排列,这种 重排可以发生在分子内或分子间,并伴随着键的断裂和形成。重排反应通常伴 随着键能的变化,需要一定的活化能来启动反应。
重排反应的重要性
总结词
重排反应在有机化学中具有重要的意义,它涉及到许多有机化合物的合成、转化和降解过程。
详细描述
重排反应的动力学与热力学
动力学研究
分析重排反应的动力学特征,如反应 速率常数、活化能等,以及如何影响 反应进程。
热力学研究
探讨重排反应的热力学性质,如反应 熵变、焓变等,以及与反应条件的关 系。
重排反应的历程与过渡态
历程研究
揭示重排反应的具体步骤和中间体,以及各 步骤之间的相互转化。
过渡态研究
分析重排反应过程中的过渡态结构,以及如 何影响反应活化能和产物形成。
贝克重排反应是一种有机化学反应,涉及环丙烷环系的重排过程。在反应中,环丙烷环系通过加热或 其他能量源的激发,发生重排,生成新的化合物。
沃尔夫-凯惜纳重排反应
总结词
涉及芳香族化合物的重排反应
详细描述
沃尔夫-凯惜纳重排反应是一种有机化学反应,涉及芳香族化 合物的重排过程。在反应中,芳香族化合物通过加热或其他 能量源的激发,发生重排,生成新的化合物。
计算化学的应用
利用计算化学方法预测和优化 重排反应的途径和产物,提高
反应效率。
06
参考文献
参考文献
《有机化学重排反应》第二版,作者
01
XXX,出版社:XXX。
《有机化学重排反应》第三版,作者
02
XXX,出版社:XXX。
"有机化学重排反应研究进展",作者
04第四章 重排反应 2

RHC
CHCONH2
RHC
若α,β-位含炔键的酰胺,重排则得腈类:
RC CCONH2 RCH2CN
c.芳环邻位有-NH2、-OH等亲核基团时,形成异氰 酸酯中间体可进行分子内环合,形成新杂环:
H
C 6H5OCH3 Ph
P
P
C C O Ph C 6H5OCH3 P + 94% Ph CH3OC 6H5 C C Ph
6%
O C 6H5OCH3 p
b.不对称的连二乙醇
R1 R1 C
R2 C R2
OH OH
☆ 重排的方向决定于羟基失去的难易;
☆ 羟基离去后碳正离子的稳定性:叔碳>仲碳>伯碳; ☆ 与基团迁移能力的大小无关。
O R C N R' R C N H R'OH R C H N R'
(2)肟的立体异构化
由于Beckmann重排中迁移基团位于肟羟基反位, 故当肟基C原子上连有不同烃基时,会有Z /E异构体, 重排后产物酰胺也为混合物,这是不希望的结果。 为此,应了解造成肟异构化的可能性:
a.在质子极性溶剂中易发生异构化
P CH3OC 6H5 Ph H2SO4 P CH3OC 6H5 C C Ph OH OH P CH3OC 6H5 P CH3OC6H5 C Ph + P CH3OC 6H5 C O 28% C Ph O Ph C Ph C 6H5OCH3 P
72%
CH3 Ph H2SO4 Ph C C CH3 Ph C Ac O 2 OH OH Ph Ph C C CH3
有机化学重排反应讲解
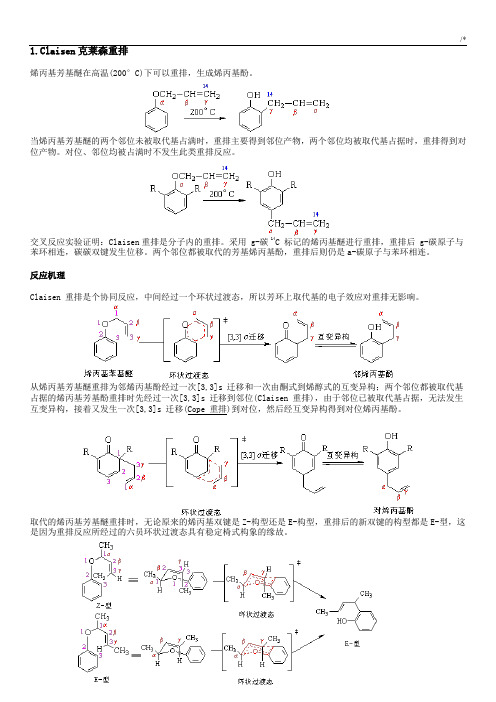
1.Claisen克莱森重排烯丙基芳基醚在高温(200°C)下可以重排,生成烯丙基酚。
当烯丙基芳基醚的两个邻位未被取代基占满时,重排主要得到邻位产物,两个邻位均被取代基占据时,重排得到对位产物。
对位、邻位均被占满时不发生此类重排反应。
交叉反应实验证明:Claisen重排是分子内的重排。
采用 g-碳 14C 标记的烯丙基醚进行重排,重排后 g-碳原子与苯环相连,碳碳双键发生位移。
两个邻位都被取代的芳基烯丙基酚,重排后则仍是a-碳原子与苯环相连。
反应机理Claisen 重排是个协同反应,中间经过一个环状过渡态,所以芳环上取代基的电子效应对重排无影响。
从烯丙基芳基醚重排为邻烯丙基酚经过一次[3,3]s 迁移和一次由酮式到烯醇式的互变异构;两个邻位都被取代基占据的烯丙基芳基酚重排时先经过一次[3,3]s 迁移到邻位(Claisen 重排),由于邻位已被取代基占据,无法发生互变异构,接着又发生一次[3,3]s 迁移(Cope 重排)到对位,然后经互变异构得到对位烯丙基酚。
取代的烯丙基芳基醚重排时,无论原来的烯丙基双键是Z-构型还是E-构型,重排后的新双键的构型都是E-型,这是因为重排反应所经过的六员环状过渡态具有稳定椅式构象的缘故。
反应实例Claisen 重排具有普遍性,在醚类化合物中,如果存在烯丙氧基与碳碳相连的结构,就有可能发生Claisen 重排。
2.Beckmann贝克曼重排肟在酸如硫酸、多聚磷酸以及能产生强酸的五氯化磷、三氯化磷、苯磺酰氯、亚硫酰氯等作用下发生重排,生成相应的取代酰胺,如环己酮肟在硫酸作用下重排生成己内酰胺:反应机理在酸作用下,肟首先发生质子化,然后脱去一分子水,同时与羟基处于反位的基团迁移到缺电子的氮原子上,所形成的碳正离子与水反应得到酰胺。
迁移基团如果是手性碳原子,则在迁移前后其构型不变,例如:反应实例3.Bamberger,E.重排苯基羟胺(N-羟基苯胺)和稀硫酸一起加热发生重排成对-氨基苯酚:在H2SO4-C2H5OH(或CH3OH)中重排生成对-乙氧基(或甲氧基)苯胺:其他芳基羟胺,它的环上的o-p位上未被取代者会起类似的重排。
最新第四章--重排反应

C6H5
C C C6H5 KOH/C2H5OH
OO C6H5 OH C6H5 C COO
C6H5 C C C6H5 + OH OO
O C6H5 C C OH
O C6H5
OO C6H5 C C OH
C6H5
OHO C6H5 C C O
RCCR Y RCCR
OH Y
OH
R R C C R Y为
OR
NH2 X
OSO2R
Tiffeneau环扩大反应
1-氨基甲基环烷醇用亚硝酸处理,经重排形成 多一个碳的环烷酮的反应,称为Tiffeneau环 扩大反应。
(CH2)n
OH C
HNO2 (CH2)n
CH2NH2
O C CH2
三、 二苯乙醇酸重排
异冰片 -H
CH2 CH2
莰烯
Ph
C H3 OTs C CH CH3
P hH
CH3 *
H 3 C C C* P h CH3 CH3
C H3 P h C C*H C H 2
H
C H3
P h C C* C H 3 CH3 CH3 +
H 3 C C C* P h CH3 CH3
CH2 CH3
CH3
CH3
反应包括下列三个步骤: 1.酰氯的形成; 2.酰氯和重氮甲烷作用生成重氮酮; 3.重氮酮经Wolff重排变为烯酮,再转变 为羧酸或衍生物。
H3CO H3CO
P C H3OC 6H5 C C Ph
OH OH
P C H3OC 6H5
P C H3OC 6H5 C Ph
+ห้องสมุดไป่ตู้
有机重排反应详尽总结

有机重排反应详尽总结重排反应(rearrangement reaction)是分⼦的碳⾻架发⽣重排⽣成结构异构体的化学反应,是有机反应中的⼀⼤类。
重排反应通常涉及取代基由⼀个原⼦转移到同⼀个分⼦中的另⼀个原⼦上的过程,现将有机重排反应进⾏⼀个详尽的总结。
(1)Amadori重排反应酸或碱催化下醛糖的N-糖苷(糖胺,glycosylamines)异构化⽣成1-胺基-1-脱氧酮糖的反应被称为Amadori重排反应。
此反应的底物和产物都称为“Amadori化合物”。
各种Lewis酸都已应⽤于此反应:CuCl2 , MgCl2 , HgBr2 , CdCl2 , AlCl3 , SnCl4 , etc。
此反应中只需催化量的酸就可以催化胺和醛糖反应,进⽽重排。
伯胺,仲胺,脂肪胺或芳⾹胺都可以发⽣此反应。
糖胺类化合物会发⽣复杂的美拉德反应(⾷物在烹饪或储藏过程中糖,胺,氨基酸和蛋⽩质等进⾏重排和降解)。
此反应中⽣成的⿊⾊产物是由于发⽣了此类⾮酶褐变反应。
(2)Baker-Venkataraman重排贝克-⽂卡塔拉曼重排反应(Baker-Venkataraman重排)是2-⼄酰氧基苯⼄酮衍⽣物在碱作为催化剂之下⽣成1,3-⼆酮的反应。
这个反应常⽤于制造⾊酮和黄酮类化合物。
(3)Bamberger RearrangementN-芳基羟胺在强酸⽔溶液作⽤下重排为氨基苯酚的反应。
(4)Beckmann Rearrangement贝克曼重排反应(Beckman rearrangement)指醛肟或酮肟在酸催化下⽣成N-取代酰胺的亲核重排反应,反应中起催化作⽤的酸常⽤五氯化磷。
此反应是由德国化学家恩斯特·奥托·贝克曼发现并由此得名。
(5)Brook RearrangementC-Si→O-Si的离⼦性重排反应,从羟基硅烷到硅醚的转化。
Brook 重排反应的推动⼒是产物中键能较⾼的 Si-O 键的⽣成。
有机化学中的重排反应

OH Ph Ph
O
Ph Ph
3. 碳烯(Carbene)重排
⑴ Wolff重排
α- 重氮甲酮在水、醇、或胺存在下,用Ag, Ag2O或光照 下催化,分解生成羧酸或酸酸衍生物——Wolff重排.
NO2 COCHN2 Ag2O H2O NO2 CH2CO2H
R C C L R C C -L R C C +H
+
Nu-
R Nu C C
R C C 重排 R C C -H
+
(CH3)3CCHCH3 OH
无水草酸 100—110 ℃
(CH3)3CCH=CH2 + (CH3)2CHC=CH2 CH3 31% 3%
+ (CH3)2C=C(CH3)2
反应机理是: 醇首先在酸作用下脱去羟基形成碳正离子,
CH2CH2CO2H H SO + HN3 2 4 CH2CH2CO2H
羧酸可以是直链脂肪族的一元或二元羧酸、脂环酸、芳香 酸等;与Hoffmann重排、Curtius反应相比,本反应胺的 收率较高。
例:
⑷.贝克曼(Beckmann)重排
①定义:醛或酮肟在 酸性条件下,重 排生成酰胺的反 应。(质子酸
H2SO4 , HCl, H3PO4 非质子酸PCl5, SOCl2, TsCl, AlCl3等)
C N
R C N
R' OH
H+ or PCl5
R'CONHR
OH
H+
+
C N
OH2
② 机理:反应被认 为是通过缺电子氮 进行的:
R C N R'
第四章 重排反应

H O 2 H C 3 C C H 3 C H +2
C H 3
C H 3
C H 3
CH3
CH3
+ H3C C CH2
Br
H3C C CH2Br
极不稳定
较稳定
CH3
重排
CH3
CH3
Br
H3C
C +
CH2CH3
H3C
CH3 C CH2CH3 Br
主要产物
1. 形成C+ 形式
(1) 卤代烃 Ag+、AgCl或Lewis酸催化
H
R2 C C R4
OH OH
R1 R2 C C R4
R3 O
1. 反应机理:
II
H3C CH3 CH3 C C CH3
HO OH
H3C CH3 H+ CH3 C C CH3
CH3
HO +OH2
H3C CH3
-H 2O CH3 C C CH3 +
OH CH3
重排 CH3 C C CH3 -H+ CH3 C C CH3
H H 3C C C Ph
C H 3C H 3
OH NHTs Ph3P/DEAD
OPPh3
NHTs -Ph3P=O
NHTs
NHTs
NHTs
二、Pinacol重排
在酸催化作用下,取代的邻二醇失去一分子水,重排生成醛 或酮的反应称Pinacol重排。取代的邻二醇称为频呐醇,重排 生成的酮称为频呐酮
R1 R3
• 重排生成的脂环烯酮在氧气的存在下经光照,释放出CO2, 生成环酮。
• 抗HⅣ病毒药物Oxetanocin可通过该重排而制得中间体, 经还原、脱保护而制得产品。
有机化学中重排反应

有机化学中重排反应有机化学中重排反应很早就被人们发现,研究并加以利用。
第一次被Wohler发现的,由无机化合物合成有机化合物,从而掀开有机化学神秘面纱的反应—加热氰酸铵而得到尿素,今天也被化学家归入重排反应的范畴。
一般地,在进攻试剂作用或者介质的影响下,有机分子发生原子或原子团的转移和电子云密度重新分布,或者重键位置改变,环的扩大或缩小,碳架发生了改变,等等,这样的反应称为是重排反应。
按照反应的机理,重排反应通常可分为亲核反应、亲电反应、自由基反应和周环反应四大类。
也有按照不同的标准,分成分子内重排和分子间重排,光学活性改变和不改变的重排反应,等等。
一、亲核重排重排反应中以亲核重排为最多,而亲核重排中又以1,2重排为最常见。
(一)亲核1,2重排的一般规律1.亲核1,2重排的三个步骤:离去基团离去,1,2基团迁移,亲核试剂进攻2.发生亲核1,2重排的条件(1)转变成更稳定的正离子(在非环系统中,有时也从较稳定的离子重排成较不稳定的离子)(2)转变成稳定的中性化合物(3)减小基团间的拥挤程度,减小环的张力等立体因素。
(4)进行重排的立体化学条件:带正电荷碳的空p轨道和相邻的C-Z键以及α碳和β碳应共平面或接近共平面(5)重排产物在产物中所占的比例不仅和正电荷的结果有关,而且和反应介质中存在的亲核试剂的亲核能力有关3.迁移基团的迁移能力(1)多由试验方法来确定基团的固有迁移能力(2)与迁移后正离子的稳定性有关(3)邻位协助作用(4)立体因素4.亲核1,2重排的立体化学:(1)迁移基:构象基本保持,没有发现过构型反转,有时有部分消旋(2)迁移终点:取决于离去及离去和迁移基进行迁移的相对时机5.记忆效应:后一次重排好像和第一次重排有关,中间体似乎记住了前一次重排过程(二) 亲核重排主要包括基团向碳正离子迁移,基团向羰基碳原子迁移,基团向碳烯碳原子迁移,基团向缺电子氮原子转移,基团向缺电氧原子的迁移,芳香族亲核重排,下面就这六种迁移作简要介绍:1.基团向碳正离子迁移:(1)Wagner-Meerwein重排:烃基或氢的1,2移位,于是醇重排成烯(2)片那醇重排:邻二醇在酸催化下会重排成醛和酮(3)Demyanov重排,Tiffeneau-Demyanov扩环以及有关反应(4)二烯酮-酚重排:4,4-二取代环己二烯酮经酸处理重排成3,4-二取代酚的反应(5)醛酮同系物的合成:醛或酮和重氮甲烷作用生成高一级的同系物(6)烯丙基重排:烯丙基系统中双键发生位移的反应2.基团向羰基碳原子迁移:(1) Benzil-Benzilic Acid重排:α-二酮经强碱处理会发生重排,生成α-羟基乙酸盐(2) 酸催化下醛酮的重排:在烃基的交换后,醛重排成酮,酮则重排成另一种酮3.基团向碳烯碳原子迁移:(1) Arndt-Eistert合成和Wolff重排:由羧酸经酰卤,重氮酮合成高一级同系物的方法(2) 其他的碳烯重排反应,主要是1,2氢迁移生成烯4.基团向缺电子氮原子转移:(1)Beckmann重排:醛肟或酮肟重排成酰胺(2)Hoffmann重排:氮上无取代基酰胺经溴及碱处理,脱羰生成伯胺(3)Curtius重排:酰基叠氮热分解生成异氰酸酯(4)Schmidt重排:酸、醛和酮在酸催化下和叠氮酸反应,生成胺、酰胺等的反应(5)Lossen重排:异羟肟酸及O-酰基衍生物经类似Hoffmann的重排生成少一个碳的胺(6)Neber重排:肟酮的磺酸酯在乙醇钾处理后水解生成α-氨基酮5.基团向缺电氧原子的迁移:(1)氢过氧化物的重排:氢过氧化物在酸催化下,O-O键断裂,同时烃基从碳原子迁移到氧原子上(2)Baeyer-Villiger重排:酮在酸催化下与过酸作用,在分子中插入氧生成酯的反应6.芳香族亲核重排:(1)芳羟胺重排(Bamberger重排):经硫酸处理重排成氨基酚(2)Sommelet-Hauser重排:苄基季胺盐经氨基钠等强碱处理重排成邻位取代的苄基叔胺二、自由基重排反应1.1,2迁移:比正离子重排反应少得多,主要发生在:(1)某些双自由基的1,2-烷基和氢(2)烯基(迁移的乙烯基若是环的一部分,则发生重排)2.非1,2迁移:多发生1,5迁移3.Barton反应:处于羟基δ位上的甲基氧化成醛基的反应4三、亲电重排第一步是在亲核试剂作用下,离去基脱离形成富电中心,离去基以氢及金属原子居多;第二步是迁移基团留下一对成键电子,以正离子的形式向富电中心迁移,重排结果是形成新的富电中心。
有机化学重排反应 的总结

有机化学重排反应总结1.Claisen克莱森重排烯丙基芳基醚在高温(200°C)下可以重排,生成烯丙基酚。
当烯丙基芳基醚的两个邻位未被取代基占满时,重排主要得到邻位产物,两个邻位均被取代基占据时,重排得到对位产物。
对位、邻位均被占满时不发生此类重排反应。
交叉反应实验证明:Claisen重排是分子内的重排。
采用 g-碳 14C 标记的烯丙基醚进行重排,重排后 g-碳原子与苯环相连,碳碳双键发生位移。
两个邻位都被取代的芳基烯丙基酚,重排后则仍是a-碳原子与苯环相连。
反应机理Claisen 重排是个协同反应,中间经过一个环状过渡态,所以芳环上取代基的电子效应对重排无影响。
从烯丙基芳基醚重排为邻烯丙基酚经过一次[3,3]s 迁移和一次由酮式到烯醇式的互变异构;两个邻位都被取代基占据的烯丙基芳基酚重排时先经过一次[3,3]s 迁移到邻位(Claisen 重排),由于邻位已被取代基占据,无法发生互变异构,接着又发生一次[3,3]s 迁移(Cope 重排)到对位,然后经互变异构得到对位烯丙基酚。
取代的烯丙基芳基醚重排时,无论原来的烯丙基双键是Z-构型还是E-构型,重排后的新双键的构型都是E-型,这是因为重排反应所经过的六员环状过渡态具有稳定椅式构象的缘故。
反应实例Claisen 重排具有普遍性,在醚类化合物中,如果存在烯丙氧基与碳碳相连的结构,就有可能发生Claisen 重排。
2.Beckmann贝克曼重排肟在酸如硫酸、多聚磷酸以及能产生强酸的五氯化磷、三氯化磷、苯磺酰氯、亚硫酰氯等作用下发生重排,生成相应的取代酰胺,如环己酮肟在硫酸作用下重排生成己内酰胺:反应机理在酸作用下,肟首先发生质子化,然后脱去一分子水,同时与羟基处于反位的基团迁移到缺电子的氮原子上,所形成的碳正离子与水反应得到酰胺。
迁移基团如果是手性碳原子,则在迁移前后其构型不变,例如:反应实例3.Bamberger,E.重排苯基羟胺(N-羟基苯胺)和稀硫酸一起加热发生重排成对-氨基苯酚:在H2SO4-C2H5OH(或CH3OH)中重排生成对-乙氧基(或甲氧基)苯胺:其他芳基羟胺,它的环上的o-p位上未被取代者会起类似的重排。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
C C O
Br(CH2)9 C CHN2 O
NH3.H2O/AgNO3 Br(CH2)9CH2CONH2
49%
O N2
hν CH3OH
H
75%
H3COOC
RCOOH
RCOCl
CH2N2
RCOCHN2
RCH C O COCl
H2O
RCH2COOH
1. CH2N2 2. PhCOOAg/EtOH/TEA CH2COOC2H5
84~92%
Arndt-Eistert同系列羧酸的合成反应 同系列羧酸的合成反应
Arndt-Eistert合成是将一个酸变成它的高一级同系 合成是将一个酸变成它的高一级同系 物或转变成同系列酸的衍生物, 如酯或酰胺 如酯或酰胺)的反 物或转变成同系列酸的衍生物,(如酯或酰胺 的反 该反应可应用于脂肪族酸和芳香族酸的制备。 应。该反应可应用于脂肪族酸和芳香族酸的制备。 反应包括下列三个步骤: 反应包括下列三个步骤: 1.酰氯的形成 酰氯的形成; 1.酰氯的形成; 2.酰氯和重氮甲烷作用生成重氮酮 酰氯和重氮甲烷作用生成重氮酮; 2.酰氯和重氮甲烷作用生成重氮酮; 3.重氮酮经Wolff重排变为烯酮 重氮酮经Wolff重排变为烯酮, 3.重氮酮经Wolff重排变为烯酮,再转变 为羧酸或衍生物。 为羧酸或衍生物。
R1 C C R2 OH OH
羟基离去后碳正离子的稳定性:叔碳 仲碳 仲碳>伯碳 羟基离去后碳正离子的稳定性:叔碳>仲碳 伯碳
P CH3OC6H5 Ph P CH3OC6H5 C C Ph OH OH P CH3OC6H5 P CH3OC6H5 C Ph + P CH3OC6H5 C O C Ph O Ph C Ph C6H5OCH3 P H2SO4
O OH O ref. COOH OH
O
O K OH
HO HO O C
79%
C 8H17 KOH/C3H7OH.H2O C8H17 O HO HOOC O HN O H N O O 2) H2O
O
92~100% 甾体缩环
H N OH COOH O
1)CH3O /CO OH-
O
H
H3C
CH3 CH3 H3C CH3
O
1. CH3NO2/OH 2. H2/Ni
-
OH CH2NH2
NaNO2/HOAc
O
CH2 CH3 TsOH CH3 H3C C6H6
1,2- 迁移是其基本要求
O
OH HO OH
1,2- 迁移是其基本要求
Tiffeneau环扩大反应 环扩大反应
1-氨基甲基环烷醇用亚硝酸处理,经重排形成 氨基甲基环烷醇用亚硝酸处理, 用亚硝酸处理 多一个碳的环烷酮的反应,称为Tiffeneau Tiffeneau环扩 多一个碳的环烷酮的反应,称为Tiffeneau环扩 大反应。 大反应。
COOCH3 CH2COOH 1. SOCl2 2. CH2N2 COOCH3 (CH2)2COOCH3
H H3CO
H H3CO
84%
第二节 从碳原子到杂原子的重排
• • • • Beckmann重排 重排 Hofmann重排 重排Curtius重排 重排 重排 Schmidt反应 反应 Baeyer-Villiger重排 重排
适用范围: R N C O 适用范围 本重排的酰胺包 括脂肪、脂环、芳脂、 括脂肪、脂环、芳脂、芳香 及或杂环等的单酰胺, 及或杂环等的单酰胺,用以 制备各类伯胺。 制备各类伯胺。 2 RNH2 + CO3
65~71%
芳环邻位有-NH2,-OH等亲核试剂时,可成新环 等亲核试剂时, 芳环邻位有 等亲核试剂时
主产物
次产物
Ph Ph P CH3OC6H5 C C C6H5OCH3 P OHOH
H
C 6H5OCH3 P Ph C C O Ph C 6H5OCH3 P + Ph P CH3OC6H5 C C Ph O C6H5OCH3 p
94%
6%
2.不对称的连二乙醇 不对称的连二乙醇
R1
R2
重排的方向决定于羟基失去的难易
第四章 重排反应
定义:受试剂或介质的影响, 定义:受试剂或介质的影响,同一有机分子内的一个基团 或原子从一个原子迁移到另一个原子上,使分子构架发生 或原子从一个原子迁移到另一个原子上 使分子构架发生 改变而形成一个新的分子的反应称为重排反应。 改变而形成一个新的分子的反应称为重排反应。 重排反应类型(按终点原子电荷分 重排反应类型 按终点原子电荷分) 按终点原子电荷分 缺电子重排 富电子重排 自由基重排 • • • • 从碳原子到碳原子的重排 从碳原子到杂原子的重排 从杂原子到碳原子的重排 σ-键迁移重排 键迁移重排 重排反应的应用 1. 形成 形成C-C、C-N、C-O键 、 、 键 2. 定向引入官能团 3. 形成环状化合物
RCONH2 + Br2 + 4 OH + CO2 + 2 Br + 2 H2O RNH2 3
机理
R C NH2 O OH Br2 R C NHBr O
1、供电性R速度快于吸电性 、供电性 速度快于吸电性 速度快于吸电性R 2、重排后 构型保留 构型保留 、重排后R构型
R C N Br O
H2O/OH
O
COOH Cl KOH/C2H5OH
64%
(CH3)2CH CH C CH(CH3)2 Br O (CH3)2CH CHCOOCH3 CH(CH3)2 O 1. NaOH/C2H5OH Br 2. H
91% 83%
CH3O
COOH
五、Wolff重排 重排
重氮酮在银、银盐或铜存在条件下, 重氮酮在银、银盐或铜存在条件下,或用光照射 在银 或热分解消除氮分子而重排为烯酮 消除氮分子而重排为烯酮, 或热分解消除氮分子而重排为烯酮,生成的烯酮 进一步与羟基或胺类化合物作用得到酯类、 进一步与羟基或胺类化合物作用得到酯类、酰胺 或羧酸的反应称为Wolff重排反应。 重排反应。 或羧酸的反应称为 重排反应
Cl O
Cl RO O OR O O
COOR
ROH
+ RO COOR
PhCH2 C CH2Cl O PhCH C CH3 Cl O
RO ROH
PhCH2CH2COOR
Favorski卤代酮重排应用 卤
•大环类化合物的缩合 大环类化合物的缩合 大环类化合物的缩 •制备α碳上多烃基取代羧酸衍生物 制备α碳上多烃基取代羧酸衍生物 制备 •合成有张力的脂环烃羧酸衍生物 合成有张力的脂环烃羧酸衍生物 合成有张力的脂环烃
机理
基团的迁移能力
1.对称的连二乙醇 对称的连二乙醇
R1
R2 R2 C C R1 OH OH
CH3 CH3 Ph C C Ph OH OH
芳基>烃基 芳基 烃基 供电子取代芳基>吸电子取代芳基 供电子取代芳基 吸电子取代芳基
H
H3C C O
CH3 C Ph + Ph C Ph O
CH3 C CH3 Ph
C6H5 C C C6H5 + OH O O O O C6H5 C C OH C6H5
C6H5
O C C OH O C6H5
OHO C6H5 C C O C6H5
Ar C C Ar' O O
Ar' Ar C C OH OHO + Ar HO C C Ar' O OH
迁移能力:吸电子基芳环> 迁移能力:吸电子基芳环> 供电子基芳环
HO
Favorski卤 四、Favorski卤代酮重排
卤代酮在亲核碱(NaOH,RONa等)存在的条件 α-卤代酮在亲核碱 卤代酮在亲核碱 等 存在的条件 发生重排得到羧酸盐、 下,发生重排得到羧酸盐、酯或酰胺的反应称为 Favorski卤代酮重排反应。 卤 酮重排反应。
PhCH2 C CH2Cl O NaOH PhCH2CH2COO
关注1,2重排 构型保留
一、Beckmann重排 重排 酮肟类化合物在酸性催化剂的作用下, 类化合物在酸性催化剂的作用下 酮肟类化合物在酸性催化剂的作用下,重排成取 酰胺的反应称为 的反应称为Beckmann重排。 重排。 代酰胺的反应称为 重排
R OH C N R'
H
O R C NHR'
机理
Beckmann重排的应用 Beckmann重排的应用 重排的
(CH2)n
C
OH CH2NH2
HNO2
(CH2)n
C
O
CH2
三、 二苯乙醇酸重排
二苯基乙二酮类化合物用碱处理,生成二苯 二苯基乙二酮类化合物用碱处理,生成二苯 用碱处理 乙醇酸的反应称为二苯乙醇酸重排反应。 乙醇酸的反应称为二苯乙醇酸重排反应。
KOH/C 2H5OH
C6H5 C C C6H5 O O C 6H5 OH C COO C 6H5
N F3C N CONH2 NH2 Br2/KOH
0~5, 105min N N C O N NH2
F3C N F3C N N
OH N H
72%
三、Curtius重排 重排
酰基叠氮化合物在惰性溶液中加热分解为 酰基叠氮化合物在惰性溶液中加热分解为 化合物在惰性溶液中加热分解 异氰酸酯的反应称为Curtius重排反应。 异氰酸酯的反应称为 重排反应。 重排反应
第一节 从碳原子到碳原子的重排
1. Wagner-Meerwein重排 重排 2. Pinacol重排 重排 3. 苯偶酰-二苯乙醇酸型重排 苯偶酰 二苯乙醇酸型重排 4. Favorski重排 重排 5. Wolff重排 重排
