大肠杆菌表达系统与蛋白表达纯化
综述:大肠杆菌中重组蛋白的表达:进展与挑战

大肠杆菌中重组蛋白的表达:进展与挑战毫无疑问,重组蛋白在微生物中的表达革新了生物化学领域。
以前,纯化少量的目的蛋白需要处理几千克的动物或植物组织,或是大量的生物体液,这个时代已经一去不返了。
对于每个研究者来说,如果他要开始一个项目,需要某种纯化的蛋白。
他马上就会想到,怎样通过重组表达的方式获得这种蛋白。
目的重组蛋白的大量表达使人们能够对其生物化学性质进行分析,将其应用于工业并发展成为商业化产品。
从理论上来讲,获得重组蛋白的过程相当直接:获得目的基因,克隆到表达载体,转入表达宿主,诱导,纯化。
然而,实际上,事情通常并不是这样。
宿主菌生长差,包涵体的形成,蛋白无活性,甚至无法获得任何蛋白,这些都是实验中会遇到的问题。
在过去,有许多综述详细地介绍了这个课题。
综合来说,这些论文收集了2000多个例子。
然而在重组蛋白表达纯化领域,一直都在进步着。
因此,在本综述中,我们对本领域最近取得的进展做了评述。
同时,对于那些那些对异源表达还不大熟练的研究人员,我们通过回答项目开始就需要解决的问题,提供的许多选择和方法,。
这些选择和方法,在过去的几十年里,曾被成功的用来表达一系列的蛋白。
问题一:选择哪种生物体作为表达宿主?整个过程的开始就是要选择宿主细胞,利用它的蛋白合成机制来获得珍贵的蛋白。
宿主的选择决定了我们以后所需要的技术,包括各种分子工具,仪器或者试剂。
在这些微生物体中,现有的宿主系统包括细菌,酵母,filamentous fungi, 和 unicellular algae。
他们各有优点和缺点,宿主的选择可能取决于我们要表达的蛋白。
例如,如果目的蛋白需要翻译后的修饰,那么我们就要选择真核表达系统。
在本篇综述里,我们主要详细介绍大肠杆菌表达系统。
众所周知,利用大肠杆菌作为宿主具有很多优点。
1.它有无可比拟的快速生长机制,在glucose-salts培养基中,以及在最优的环境条件下,它扩增一倍的时间大约是20分钟。
蛋白质的表达、纯化及检测-分子实验报告

实验目的1.了解外源基因在大肠杆菌细胞中的诱导表达情况2.学会用SDS-PAGE电泳法分离不同分子量的蛋白质3.学习通过亲和层析法纯化目的蛋白4.学会考马斯亮蓝染色法和蛋白质杂交法检测蛋白质实验原理1.外源基因在大肠杆菌细胞中的诱导表达:将外源基因克隆在特殊的表达载体中,让其在E. coli中表达,该表达载体上含有lac操作子的启动子。
在不加诱导剂的条件下培养宿主菌,lacI基因表达的阻遏蛋白LacI与lac操作子结合,使外源基因不能表达;向培养基中加入诱导物IPTG后,LacI阻遏蛋白变构失活,不能与lac操作子结合,外源基因就表达。
2.蛋白质SDS-PAGE电泳分离:SDS-PAGE是最常用的定性分析蛋白质的电泳方式,特别是用于蛋白质纯度检测和测定蛋白质分子量。
其分离原理是根据蛋白质分子量的差异,因为SDS-PAGE的样品处理液及缓冲液的加入破坏了蛋白质的二级、三级、四级等结构,并使SDS与蛋白质充分结合形成SDS-蛋白质复合物,稳定地存在于均一的溶液中,SDS与蛋白质结合后使SDS-蛋白质复合物上带有大量的负电荷,远远超过其原来所带的电荷,从而使蛋白质原来所带的电荷可以忽略不计,消除了不同分子之间原有的电荷差别,其电泳迁移率主要取决于亚基分子质量的大小,这样分离出的谱带也为蛋白质的亚基。
3.考马斯亮蓝法检测蛋白质:考马斯亮蓝是一种蛋白质染料,主要有R-250和G-250两种类型。
考马斯亮蓝可以和蛋白肽链中碱性氨基酸残基或芳香族氨基酸残基(Arg,Trp,Tyr,His,Phe)结合。
考马斯亮蓝R250多用于聚丙烯酰胺凝胶电泳后蛋白质条带的染色;因为考马斯亮蓝R250中的R代表Red,偏红,红蓝色,与蛋白质结合虽然比较缓慢,但是染料可以穿透凝胶,染胶效果好,染色后为蓝色,且与胶的结合可以被洗脱下去,所以可以用来对电泳条带染色。
4.基因融合就是将两个或多个开放读码框按一定顺序连接在一起,融合阅读框架的表达产物是一个杂和蛋白。
大肠杆菌系统表达和纯化流程
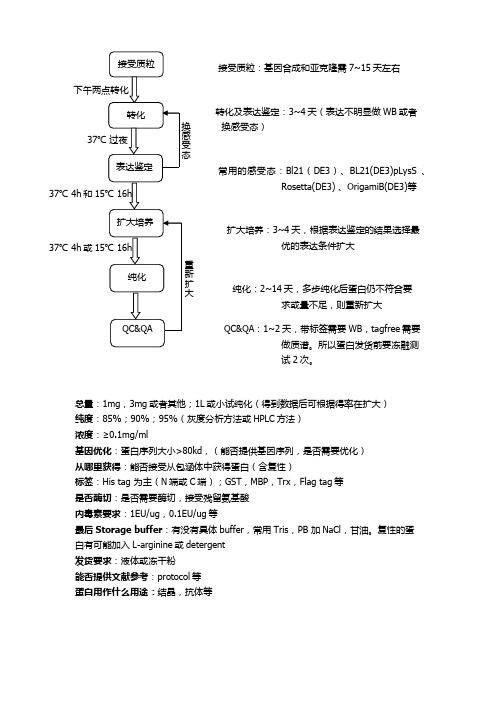
转化及表达鉴定:3~4天(表达不明显做WB或者
换感受态)
常用的感受态:Bl21(DE3)、BL21(DE3)pLysS 、
Rosetta(DE3) 、OrigamiB(DE3)等
扩大培养:3~4天,根据表达鉴定的结果选择最
优的表达条件扩大
纯化:2~14天,多步纯化后蛋白仍不符合要
求或量不足,则重新扩大
:1~2天,带标签需要WB,tagfree需要
做质谱。
所以蛋白发货前要冻融测
试2次。
总量:1mg,3mg或者其他;1L或小试纯化(得到数据后可根据得率在扩大)
纯度:85%;90%;95%(灰度分析方法或HPLC方法)
浓度:≥0.1mg/ml
基因优化:蛋白序列大小>80kd,(能否提供基因序列,是否需要优化)
从哪里获得:能否接受从包涵体中获得蛋白(含复性)
标签:His tag 为主(N端或C端);GST,MBP,Trx,Flag tag等
是否酶切:是否需要酶切,接受残留氨基酸
内毒素要求:1EU/ug,0.1EU/ug等
最后Storage buffer:有没有具体buffer,常用Tris,PB 加NaCl,甘油。
复性的蛋
白有可能加入L-arginine或detergent
发货要求:液体或冻干粉
能否提供文献参考:protocol等
蛋白用作什么用途:结晶,抗体等。
在大肠杆菌中表达重组蛋白的流程

在大肠杆菌中表达重组蛋白的流程
在大肠杆菌中表达重组蛋白的流程通常包括以下步骤:
1. 克隆:首先需要将目标基因克隆到适当的表达载体中。
这可以通过PCR扩增目标基因,然后将其与表达载体连接,形成重组质粒。
2. 转化:将重组质粒转化到大肠杆菌细胞中。
可以使用化学方法(如热冲击法)或电穿孔法将质粒导入细胞。
3. 选择:转化后,将细胞分散在含有适当抗生素的琼脂平板上培养。
只有带有重组质粒的细胞能够存活并形成菌落。
4. 培养:将含有重组细胞的培养液转移到适当的培养基中,并在适当的条件下培养。
这可能包括调节温度、pH值和搅拌速度等。
5. 表达:在培养期间,目标基因会被大肠杆菌细胞转录和翻译为蛋白质。
使用适当的启动子和调控序列,可实现目标蛋白的高效表达。
6. 细胞破碎:一旦细胞达到最佳表达水平,就需要破碎细胞以释放目标蛋白。
这可以通过多种方法实现,如超声波、高压破碎或化学方法。
7. 纯化:通过使用各种分离和纯化技术(如亲和层析、凝胶过滤、离子交换层析等),从细胞裂解液中纯化目标蛋白。
以上是在大肠杆菌中表达重组蛋白的一般流程。
具体的步骤和条件可能因实验设计和目标蛋白的特性而有所不同。
大肠杆菌表达纯化蛋白

大肠杆菌表达纯化蛋白大肠杆菌是一种常见的细菌,被广泛用于表达和纯化蛋白的研究中。
本文将探讨大肠杆菌表达纯化蛋白的方法和应用。
一、大肠杆菌表达纯化蛋白的方法大肠杆菌表达纯化蛋白的方法主要包括以下几个步骤:1. 质粒构建:首先需要构建包含目标蛋白基因的质粒。
这通常包括选择一个适当的表达载体,将目标蛋白基因克隆到质粒中,并添加相应的启动子和信号序列,以实现高效的蛋白表达。
2. 转化大肠杆菌:将质粒导入大肠杆菌中,使其成为宿主细胞。
常用的转化方法包括化学转化、电转化和热激转化等。
3. 诱导表达:通过添加适当的诱导剂,如IPTG(异丙基β-D-硫代半乳糖苷),诱导大肠杆菌开始表达目标蛋白。
4. 细胞培养:大肠杆菌在适当的培养基中进行培养,以提供足够的营养物质和条件来支持蛋白的表达。
5. 细胞破碎:培养达到一定密度后,通过破碎细胞膜的方法将细胞内的目标蛋白释放出来。
常用的方法包括超声波破碎、高压破碎和化学破碎等。
6. 蛋白纯化:通过一系列的层析、过滤和浓缩等步骤,从细胞裂解液中纯化目标蛋白。
常用的纯化方法包括亲和层析、离子交换层析和凝胶过滤层析等。
大肠杆菌表达纯化蛋白的方法被广泛应用于生物医学研究、药物开发和工业生产等领域。
1. 生物医学研究:通过大肠杆菌表达纯化蛋白,可以获得大量高纯度的目标蛋白,用于研究其结构、功能和相互作用等。
这对于研究蛋白质的生物学特性、疾病机制以及药物研发具有重要意义。
2. 药物开发:大肠杆菌表达纯化蛋白广泛应用于药物的筛选和研发。
通过表达和纯化目标蛋白,可以用于药物靶标的筛选、药物的活性评价以及药物的结构优化等。
3. 工业生产:大肠杆菌表达纯化蛋白的方法也被应用于工业生产中。
通过大肠杆菌表达大量的目标蛋白,可以用于生产酶类、抗体和其他重要蛋白制剂。
三、大肠杆菌表达纯化蛋白的优势和挑战大肠杆菌作为常见的宿主细胞,表达纯化蛋白具有以下优势:1. 高表达水平:大肠杆菌能够高效表达目标蛋白,产量较高。
重组蛋白质的表达与纯化技术

重组蛋白质的表达与纯化技术蛋白质是生命体活动的重要组成部分,对于生命体的生长、繁殖和免疫功能起着至关重要的作用。
而重组蛋白质则是利用基因工程技术,将人工合成的外源基因导入到特定的宿主细胞中,通过细胞表达和纯化技术得到的转录翻译产物。
这种技术不仅可以生产天然蛋白质,还可以生产人工合成的新型蛋白质,对于疾病的治疗和新药的研发有着重要的意义。
一、蛋白质表达技术蛋白质表达是获得大量重组蛋白质的重要方法。
选择适当的宿主细胞和表达载体是获得高水平表达的关键。
常用的宿主细胞包括大肠杆菌、酵母菌、昆虫细胞、哺乳动物细胞等。
1.大肠杆菌表达系统大肠杆菌表达系统具有生长快、表达量高等优点,广泛应用于重组蛋白质的表达和纯化。
其表达载体主要有pET和pBAD两种,pET系统一般用于产生可以形成包涵体的重组蛋白,pBAD系统用于在分泌表达中产生滞留蛋白。
2.昆虫细胞表达系统昆虫细胞表达系统包括SF9、Sf21、HighFive等细胞系,常用的表达载体为pIB/V5-His、pFastBac等。
昆虫细胞表达系统通常用于表达大分子蛋白质,如糖蛋白、膜蛋白等。
3.哺乳动物细胞表达系统哺乳动物细胞表达系统是目前表达规模最大、表达产物最接近人体蛋白质的一种表达系统。
其表达载体主要有pCDNA3.1、pCI 等,常用于表达与人体有关的蛋白质,如抗体、生长因子等。
二、蛋白质纯化技术蛋白纯化是重组蛋白质生产的重要环节,其目的是得到高质量的、纯度较高的蛋白质样品。
常见的纯化方法包括亲和层析法、离子交换层析法、凝胶过滤层析法、逆流式层析法等。
1.亲和层析法亲和层析法是指因与载体中固定的亲和剂相互结合而纯化目标蛋白质的一种方法。
亲和剂通常是与目标蛋白质有特异性结合作用的化合物,如亲和标签、酶底物、抗体等。
常见的亲和层析方法有亲和柱层析、亲和膜层析等。
2.离子交换层析法离子交换层析法是根据蛋白质带有正或负电荷的差异性进行分离的一种方法。
离子交换层析的柱填充物常为离子交换树脂,其一般分为阴离子交换树脂和阳离子交换树脂两种。
大肠杆菌表达纯化蛋白

大肠杆菌表达纯化蛋白大肠杆菌是一种常见的细菌,广泛应用于生物学研究中。
它具有较高的生长速度、易于培养和操作的特点,被广泛用于表达和纯化蛋白。
本文将从大肠杆菌的选择、蛋白表达、纯化等方面介绍如何利用大肠杆菌表达纯化蛋白。
一、大肠杆菌的选择在大肠杆菌中选择合适的表达宿主菌株至关重要。
一般而言,常用的宿主菌株有BL21(DE3)、Rosetta(DE3)、Origami(DE3)等。
这些菌株具有较高的蛋白表达能力和稳定性,适合用于表达多种蛋白。
根据所需表达的蛋白的特点(例如毒性、折叠状态等),选择合适的宿主菌株是必要的。
二、蛋白表达蛋白表达是指通过转化目标基因到大肠杆菌中,使其表达目标蛋白。
一般采用的方法有原核表达和真核表达两种。
原核表达是将目标基因插入表达质粒,然后转化到大肠杆菌中,利用大肠杆菌的细胞机制进行蛋白表达。
真核表达则是将目标基因转化到真核细胞中,利用真核细胞的转录和翻译系统进行蛋白表达。
在大肠杆菌中进行蛋白表达时,需要选择适当的表达质粒。
常用的表达质粒有pET系列、pGEX系列等。
这些质粒通常含有启动子、多克隆位点、选择标记等功能元件,能够实现高效的蛋白表达。
在构建表达质粒时,需要将目标基因插入适当的位点,确保目标蛋白能够被正常表达。
三、蛋白纯化蛋白表达后,需要对目标蛋白进行纯化。
常用的纯化方法包括亲和层析、离子交换层析、凝胶过滤层析等。
亲和层析是利用蛋白与亲和树脂之间的特异性相互作用进行纯化的方法。
离子交换层析则是利用蛋白与离子交换树脂之间的电荷相互作用进行纯化的方法。
凝胶过滤层析则是利用蛋白在凝胶中的分子大小差异进行纯化的方法。
在进行蛋白纯化时,需要根据目标蛋白的特性选择合适的纯化方法。
不同的纯化方法具有不同的选择条件和操作步骤,需要根据实际情况进行选择。
此外,为了提高纯化效果,还可以采用多步骤的纯化策略,如串联多个纯化方法,以获得更高纯度的蛋白。
四、蛋白质结构分析在蛋白纯化后,可以对目标蛋白进行结构分析。
大肠杆菌表达

大肠杆菌表达引言大肠杆菌(Escherichia coli)是一种常见的细菌,广泛应用于基因工程和蛋白质表达领域。
大肠杆菌表达系统具有高效、经济且易于操作的特点,因此被广泛用于重组蛋白的生产。
本文将介绍大肠杆菌表达系统的基本原理及其在蛋白质表达中的应用。
大肠杆菌表达系统的基本原理大肠杆菌表达系统采用重组DNA技术,将外源基因插入到大肠杆菌的表达载体中。
表达载体通常包含一个启动子、一个转录终止子、一个选择性抗生素抗性基因和一个参考基因。
启动子能够促使外源基因的转录,转录终止子能够终止转录过程,选择性抗生素抗性基因则能够确保只有带有外源基因的细菌存活下来。
参考基因用于对比表达水平,以评估外源基因的表达效果。
大肠杆菌表达系统的步骤大肠杆菌表达系统的基本步骤如下:1.选择适当的表达载体:根据需要选择合适的表达载体,包括质粒和噬菌体。
2.插入目标基因:将目标基因插入到表达载体中,通常使用限制酶切和连接酶法完成插入。
3.转化大肠杆菌:将重组载体导入大肠杆菌细胞中,通常使用热激转化或电转化的方法。
4.选择性培养:将转化后的菌液接种到选择性培养基上,以筛选含有外源基因的细菌。
5.表达蛋白质:使用适当的培养条件和诱导方法,促使含有外源基因的细菌表达目标蛋白质。
6.蛋白质纯化:利用亲和层析、离子交换层析等技术,对目标蛋白质进行纯化。
大肠杆菌表达系统的应用大肠杆菌表达系统在蛋白质表达领域具有广泛的应用。
以下是一些常见的应用领域:1.重组蛋白质的生产:大肠杆菌表达系统可用于大规模生产重组蛋白质,如重组人胰岛素等。
2.蛋白质结构和功能研究:通过大肠杆菌表达系统,可以表达和纯化具有特定结构和功能的蛋白质,用于研究其结构和功能。
3.抗原制备:大肠杆菌表达系统可以用于表达和纯化目标蛋白质,作为疫苗的抗原。
4.酶的生产:利用大肠杆菌表达系统表达酶,可以实现酶的大规模生产,用于工业生产和生物催化等领域。
总结大肠杆菌表达系统是一种高效、经济且易于操作的蛋白质表达系统。
大肠杆菌系统蛋白表达纯化流程

大肠杆菌系统蛋白表达纯化流程英文回答:Introduction:The expression and purification of proteins in Escherichia coli (E. coli) is a commonly used method in molecular biology research. E. coli is a well-studied and easily manipulated organism, making it an ideal host for protein expression. In this article, we will discuss the general workflow for the expression and purification of proteins in E. coli.Expression of the target protein:1. Gene cloning: The first step is to clone the gene encoding the target protein into an expression vector. This vector contains a promoter that drives the expression of the gene in E. coli.2. Transformation: The recombinant expression vector is then introduced into E. coli cells through a process called transformation. This results in the production of many E. coli cells carrying the target gene.3. Expression induction: The transformed E. coli cells are grown in a suitable culture medium until they reach a specific growth phase. At this point, expression of the target gene is induced by adding a chemical inducer or by changing the growth conditions.4. Protein expression: The induced E. coli cells produce the target protein, which can either be present in the soluble fraction or form insoluble aggregates called inclusion bodies.Protein purification:1. Cell lysis: The E. coli cells are harvested by centrifugation and then lysed to release the proteins. Various methods can be used for cell lysis, such as sonication, freeze-thaw cycles, or enzymatic digestion.2. Removal of cell debris: The cell lysate is then clarified by centrifugation to remove cell debris and insoluble material. The resulting supernatant contains the target protein along with other cellular components.3. Protein purification: Different purification techniques can be employed to isolate the target protein from the crude lysate. These techniques include affinity chromatography, ion exchange chromatography, size exclusion chromatography, and hydrophobic interaction chromatography. The choice of purification method depends on the properties of the target protein.4. Protein concentration: After purification, thetarget protein is often in a dilute solution. Concentration can be achieved by using techniques such as ultrafiltration or precipitation with ammonium sulfate.5. Protein characterization: The purified protein should be characterized to confirm its identity and purity. Techniques such as SDS-PAGE, western blotting, and massspectrometry can be used for protein analysis.Conclusion:The expression and purification of proteins in E. coli is a well-established and widely used technique in molecular biology research. The workflow involves gene cloning, protein expression, cell lysis, protein purification, concentration, and characterization. By following this general procedure, researchers can obtain purified proteins for further analysis and functional studies.中文回答:简介:大肠杆菌(E. coli)中的蛋白表达和纯化是分子生物学研究中常用的方法。
大肠杆菌蛋白表达体系的构建实验报告

⼤肠杆菌蛋⽩表达体系的构建实验报告⼤肠杆菌蛋⽩表达系统的构建与蛋⽩质的分离纯化●实验⽬的:1.学会氯化钙制备⼤肠杆菌DH10B感受态细胞及掌握质粒转化感受态细胞的操作⽅法2.转化BL21(DE3)并在合适条件下诱导表达蛋⽩,掌握蛋⽩质诱导表达的原理,学习蛋⽩质诱导表达的⽅法3. 学会使⽤镍柱分离纯化蛋⽩质,利⽤PEPC试剂盒测定PEPC的活⼒。
●实验原理:1. 钙转法:Ca2+能与加⼊的DNA分⼦结合,形成抗DNA酶(DNase)的羟基-磷酸钙复合物,并黏附在细菌细胞膜的外表⾯上。
当42℃热刺激短暂处理细菌细胞时,细胞膜的液晶结构发⽣剧烈扰动,并随之出现许多间隙,为DNA分⼦提供了进⼊细胞的通道。
2. 诱导BL21(DE3)表达蛋⽩质的原理:E. coli BL21(DE3)其DE3是整合在细菌基因组上的⼀种携带T7 RNA聚合酶基因和lacI 基因的λ噬菌体,lacI编码的阻遏蛋⽩与lac操纵基因结合,从⽽不能进⾏外源基因的转录和表达,此时宿主菌正常⽣长。
IPTG 为乳糖类似物,不能被细胞利⽤,可以特异结合阻遏蛋⽩,阻遏蛋⽩不能与操纵基因结合,则外源基因⼤量转录并⾼效表达。
3. 六聚组氨酸纯化蛋⽩的原理:亲和层析是⼀种通过⽣物分⼦之间的特异性的相互作⽤来分离物质的层析⽅法。
组氨酸是具有杂环的氨基酸,每个组氨基酸含有⼀个咪唑基团,这个化学结构带有很多额外电⼦,对于带正电的化学物质有静电引⼒,亲和层析是利⽤这个原理来进⾏吸附的,亲和配体(也就是填料)上的阳离⼦(⼀般是镍离⼦)带正电对组氨酸有亲和作⽤。
组氨酸标签是原核表达载体上6个组氨酸的区段,这个标签在PH8.0时不带电,且⽆免疫原性,对蛋⽩质的分泌,折叠,功能基本上⽆影响.能⾼度亲和镍离⼦,⽤于蛋⽩质的亲和纯化.4. ⽬标蛋⽩:磷酸烯醇丙酮酸羧化酶(Phosphoenolpyruvate carboxykinase,PEPC.酸羧化酶的催化下,草酰⼄酸转变为磷酸烯醇式丙酮酸和⼆氧化碳。
重组蛋白IFNGA在大肠杆菌中的表达与纯化

高中组11年级生物化学3人项目重组蛋白IFNGA在大肠杆菌中的表达与纯化重组蛋白IFNGA在大肠杆菌中的表达与纯化摘要:干扰素γ(Interferon gamma,IFN-γ)是体内重要的细胞因子,能够通过调控免疫相关基因的转录协调机体的免疫反应,具有抗病毒、抗肿瘤、增强免疫力能功能。
目前对于IFN-α、IFN-β重组表达的较多,而关于IFN-γ 蛋白的纯化表达较少.因此,本研究使用PCR方法扩增IFN-γ基因,将IFN-γ基因分别插入原核表达载体pET-30构建重组表达质粒pET-30--IFN-γ,转化大肠杆菌BL21和Rosetta菌株,在IPTG诱导下表达IFN-γ,SDS-PAGE分析重组表达蛋白。
结果表明:成功构建重组表达质粒pET-30-IFN-γ;表达产物主要以包涵体形式存在;经Ni2+-NTA亲和层析纯化,获得高纯度重组蛋白。
本实验纯化的蛋白有望在今后用于医学和生物学研究中。
关键词:干扰素;IFN-γ 蛋白;大肠杆菌表达系统;重组表达;蛋白纯化;一、研究背景干扰素(IFN)是一种广谱抗病毒剂,并不直接杀伤或抑制病毒,而主要是通过细胞表面受体作用使细胞产生抗病毒蛋白,从而抑制病毒(比如:乙肝病毒)的复制。
其类型分为三类,α-(白细胞)型、β-(成纤维细胞)型,γ-(淋巴细胞)型;同时还可增强自然杀伤细胞(NK细胞)、巨噬细胞和T淋巴细胞的活力,从而起到免疫调节作用,并增强抗病毒能力。
干扰素是一组具有多种功能的活性蛋白质(主要是糖蛋白),是一种由单核细胞和淋巴细胞产生的细胞因子。
它们在同种细胞上具有广谱的抗病毒、影响细胞生长,以及分化、调节免疫功能等多种生物活性。
其中,IFN-γ是体内重要的免疫调节因子,能通过与细胞表面受体结合,诱导病毒感染细胞产生多种抗病毒蛋白,使细胞内产生抗病毒状态而发挥抗病毒作用。
在诱导效应因子表达的同时,由于IFN-γ能够提高细胞表面MHC分子的表达,增强免疫活性细胞对病原体的杀伤作用,从而协同促进了机体对病毒感染细胞的杀灭,而使机体处于抗病毒状态。
蛋白体外表达与纯化

蛋白体外表达与纯化随着后基因组时代的到来,蛋白质组成为科学研究的热点。
蛋白质作为生命机体的主要活动的承担者,其体外表达与纯化在研究相应基因的功能上有重要意义。
蛋白体外表达系统按其表达宿主可分为原核表达系统,真核表达系统和哺乳动物细胞表达系统。
一:原核表达系统原核表达系统的宿主菌主要以大肠杆菌为代表,大肠杆菌表达体系是目前应用最广泛的外源基因表达体系,这也是外源基因表达的首选体系。
该表达体系的优点:遗传学和生理学背景清楚;容易培养;外源基因经常可以高效表达及操作简单、周期短、成本低等。
其不足之处是不能进行典型真核细胞所具有的复杂的翻译后修饰;广泛的二硫键的形成及外源蛋白组装成蛋白复合体的能力也受到限制;另外外源基因产物在大肠杆菌中易形成不溶的包涵体;有时由于真核mRNA的结构特性及密码子使用频率与大肠杆菌的差异,而的不到足够的产物。
二:真核表达系统真核表达系统的宿主菌主要以酵母表达系统为代表,酵母基因表达系统的载体通常既能在酵母中进行复制也能在大肠杆菌中进行复制,形成所谓酵母菌――大肠杆菌穿梭载体。
因以大肠制备质粒DNA较方便,通常利用大肠杆菌系统构建酵母载体以简化手续,缩短时间。
作为基因表达系统的宿主应该具备以下条件:安全无毒,不致病;遗传背景较清楚,容易进行遗传操作;容易进行载体DNA的导入;培养条件简单;有良好的蛋白分泌能力;有类似高等真核生物的蛋白翻译后修饰功能。
三:哺乳动物细胞表达系统由于本专业不涉及哺乳动物细胞表达系统的应用,故此不赘述。
表达载体的种类及相应的分离纯化方法作为表达载体必须具备以下特征:稳定的遗传复制、传代能力,无选择压力下能存在于宿主细胞内;具有显性的筛选标记;启动子的转录是可调控的;启动子的转录的mRNA能够在适当的位置终止;具有外源基因插入的多克隆位点。
在原核表达系统中常用的表达载体有:PET-载体系列,用这类载体表达出的外源蛋白在N 端或C端或两端均具有his tag。
大肠杆菌表达载体,构建方法及其应用

大肠杆菌表达载体,构建方法及其应用大肠杆菌(Escherichia coli)是一种常见的肠道细菌,也是常用的表达宿主。
利用大肠杆菌表达载体,可以将目标基因导入大肠杆菌中进行表达,从而产生大量目标蛋白。
本文将介绍大肠杆菌表达载体的构建方法及其应用。
一、大肠杆菌表达载体的构建方法1. 选择适合的表达载体:常见的大肠杆菌表达载体包括pET系列、pBAD系列和pGEX系列等。
选择适合的表达载体主要考虑载体的复制起源、选择标记、表达调控元件和蛋白纯化标记等因素。
2. 克隆目标基因:将目标基因通过PCR扩增得到目标基因片段,然后利用限制性内切酶切割载体和目标基因片段,将目标基因片段插入载体中。
3. 进行质粒转化:将构建好的重组质粒导入大肠杆菌中。
可以通过化学法、电穿孔法或热冲击法等方法将质粒导入大肠杆菌中。
4. 筛选与鉴定:经过转化后,利用选择性培养基筛选出含有目标基因的重组大肠杆菌。
通过PCR、限制性酶切和测序等方法对重组菌株进行鉴定,确认目标基因已经成功插入载体。
二、大肠杆菌表达载体的应用1. 蛋白表达:利用大肠杆菌表达载体,可以将目标基因导入大肠杆菌中进行表达,从而大量产生目标蛋白。
这对于研究蛋白的结构、功能及其在生物学过程中的作用具有重要意义。
2. 蛋白纯化:大肠杆菌表达载体常含有蛋白纯化标记,如His标签、GST标签等。
通过这些标记,可以方便地对目标蛋白进行纯化和检测,为后续研究提供了便利。
3. 蛋白互作研究:大肠杆菌表达载体可以用于蛋白互作研究。
通过将目标蛋白与其他蛋白共同表达,可以研究它们之间的相互作用关系,揭示生物学过程中的分子机制。
4. 疫苗研究:大肠杆菌表达载体可以用于疫苗研究。
将目标抗原基因导入大肠杆菌中进行表达,可以获得大量的抗原蛋白,从而用于疫苗的开发和研究。
5. 酶工程:大肠杆菌表达载体可以用于酶工程研究。
通过将目标酶基因导入大肠杆菌中表达,可以进行酶的产量优化、酶的工艺改造等研究,提高酶的生产效率和稳定性。
大肠杆菌重组蛋白表达存在的问题

大肠杆菌重组蛋白表达存在的问题一、概述大肠杆菌(Escherichia coli)是一种广泛存在于土壤和水中的革兰氏阴性细菌,是重要的生物工程表达系统。
大肠杆菌重组蛋白表达系统因其高效、简便和成本低廉而被广泛应用于生物制药、基因工程和研究领域。
然而,大肠杆菌重组蛋白表达过程中存在一系列问题,限制了其在实际应用中的发展。
二、表达负荷过大在大肠杆菌重组蛋白表达系统中,由于外源基因的表达和蛋白质合成会对细胞的正常代谢和生理过程造成负担,因此表达负荷过大是一个常见问题。
这会导致目的蛋白无法高效表达,或者甚至导致细胞逝去,影响蛋白表达的稳定性和可靠性。
三、蛋白质结构错误大肠杆菌重组蛋白表达系统中,外源基因的表达受到诸多因素的影响,例如启动子的选择、转录水平、翻译后修饰等,这些都可能导致目的蛋白结构错误。
蛋白质结构错误会降低蛋白活性和稳定性,影响其在实际应用中的效果。
四、蛋白质纯度较低在大肠杆菌重组蛋白表达系统中,外源基因的表达会导致大量的杂蛋白和热蛋白的产生,这些都会降低目的蛋白的纯度。
低纯度的蛋白在实际应用中无法满足质量标准,限制了其广泛应用。
五、蛋白聚集和包含体形成在大肠杆菌重组蛋白表达系统中,外源基因的表达会导致蛋白聚集和包含体形成,这些都会影响蛋白的溶解性和稳定性。
蛋白聚集和包含体形成是影响大肠杆菌重组蛋白表达系统应用的重要问题之一。
六、表达宿主毒性外源基因的表达可能会产生毒性蛋白,例如膜蛋白、毒素等,这些都会对大肠杆菌宿主细胞产生毒性作用,甚至导致细胞逝去。
表达宿主毒性的问题不仅影响了目的蛋白的表达效率,还可能对表达宿主细胞的健康造成影响。
七、解决方案及展望针对以上存在的问题,研究人员提出了一系列解决方案。
例如通过优化启动子和调整转录水平,减轻表达宿主的负荷;设计合适的蛋白结构域,提高蛋白质结构的稳定性;采用亲和纯化技术和蛋白纯化缓冲液,提高蛋白质的纯度;利用融合蛋白和分子筛等技术,降低蛋白聚集和包含体的形成;通过调整表达条件和优化表达宿主,减轻表达宿主的毒性等。
用于蛋白质表达和纯化的高通量方法

用于蛋白质表达和纯化的高通量方法蛋白质表达和纯化是生物技术研究中非常关键的步骤。
随着科学技术的不断进步,高通量方法已经成为许多研究实验室的首选。
本文将介绍一些常用的用于蛋白质表达和纯化的高通量方法。
1.蛋白质表达的高通量方法在蛋白质表达中,高通量方法可以实现同时表达多个蛋白质的需求。
以下是几种常见的高通量蛋白质表达方法:a.原核系统:原核表达系统(如大肠杆菌)是最常用的蛋白质表达系统之一。
通过构建表达载体和优化表达条件,可以实现高效的蛋白质表达。
此外,也有一些专门用于高通量表达的原核表达系统被开发出来,如自动化液体处理系统。
b.酵母系统:酵母系统也被广泛应用于蛋白质表达。
其中,酿酒酵母和毕赤酵母是常用的表达宿主。
通过高通量方法,可以轻松地表达多个蛋白质,并且可以方便地进行后续的纯化步骤。
c.昆虫细胞系统:昆虫细胞系统通常用于表达复杂的重组蛋白质。
虽然昆虫细胞表达系统相对于其他系统来说表达量较低,但通过高通量方法,可以实现多个蛋白质的高效表达。
2.蛋白质纯化的高通量方法蛋白质纯化是高通量方法的另一个重要应用领域。
以下是几种常见的高通量蛋白质纯化方法:a.亲和层析:亲和层析是常用的蛋白质纯化方法之一。
通过构建带有亲和标签的蛋白质,并利用亲和基质与其结合,可以高效地纯化目标蛋白质。
高通量方法可以实现同时纯化多个蛋白质,提高工作效率。
b.离子交换层析:离子交换层析是使用离子交换基质对蛋白质进行分离纯化的方法。
通过调节溶液中盐浓度和pH值,可以实现不同蛋白质的选择性吸附和洗脱。
高通量方法可以将多个蛋白质同时进行纯化,提高处理量。
c.凝胶过滤层析:凝胶过滤层析是根据蛋白质分子量的差异进行纯化的方法。
通过选择合适的孔径,可以将不同分子量的蛋白质进行分离。
高通量方法可以同时处理多个样品,提高纯化效率。
3.高通量方法的优势与挑战高通量方法的优势在于大大提高了实验效率,节约了时间和资源。
通过同时处理多个样品,可以快速筛选最有效的条件和方法。
大肠杆菌系统蛋白表达纯化流程

大肠杆菌系统蛋白表达纯化流程下载温馨提示:该文档是我店铺精心编制而成,希望大家下载以后,能够帮助大家解决实际的问题。
文档下载后可定制随意修改,请根据实际需要进行相应的调整和使用,谢谢!并且,本店铺为大家提供各种各样类型的实用资料,如教育随笔、日记赏析、句子摘抄、古诗大全、经典美文、话题作文、工作总结、词语解析、文案摘录、其他资料等等,如想了解不同资料格式和写法,敬请关注!Download tips: This document is carefully compiled by theeditor. I hope that after you download them,they can help yousolve practical problems. The document can be customized andmodified after downloading,please adjust and use it according toactual needs, thank you!In addition, our shop provides you with various types ofpractical materials,such as educational essays, diaryappreciation,sentence excerpts,ancient poems,classic articles,topic composition,work summary,word parsing,copy excerpts,other materials and so on,want to know different data formats andwriting methods,please pay attention!大肠杆菌是一种广泛用于蛋白质表达和纯化的微生物。
下面是一个详细的大肠杆菌系统蛋白表达纯化流程:1. 设计并合成目的基因:首先,需要根据所需的蛋白质序列设计并合成相应的基因序列。
原核表达实验报告

原核表达实验报告
一、实验目的
本实验旨在通过原核表达系统将目标蛋白在大肠杆菌中进行表达,并对其进行纯化和鉴定。
二、实验材料
1. 目标蛋白基因克隆质粒;
2. 大肠杆菌感受态细胞;
3. 抗生素(如氨苄青霉素);
4. IPTG诱导剂;
5. SDS-PAGE凝胶电泳试剂盒;
6. 蛋白质纯化试剂盒。
三、实验步骤
1. 大肠杆菌转化:将目标蛋白基因克隆质粒转化到大肠杆菌感受态细胞中,加入抗生素(如氨苄青霉素)筛选阳性克隆。
2. 诱导表达:将阳性克隆的大肠杆菌接种到含有IPTG诱导剂的培养基中,使其表达目标蛋白。
3. 收集菌体:培养一定时间后,收集大肠杆菌菌体。
4. 裂解菌体:将收集到的大肠杆菌菌体进行裂解,释放目标蛋白。
5. 纯化目标蛋白:使用蛋白质纯化试剂盒对目标蛋白进行纯化。
6. 鉴定目标蛋白:通过SDS-PAGE凝胶电泳分析目标蛋白的表达情况和纯度。
四、实验结果与分析
1. 大肠杆菌转化结果:通过抗生素筛选,获得阳性克隆。
2. 诱导表达结果:在含有IPTG诱导剂的培养基中,目标蛋白得到了有效表达。
3. 菌体收集结果:成功收集到大肠杆菌菌体。
4. 裂解菌体结果:菌体裂解后,释放出目标蛋白。
5. 纯化目标蛋白结果:通过蛋白质纯化试剂盒,成功纯化了目标蛋白。
6. 鉴定目标蛋白结果:通过SDS-PAGE凝胶电泳分析,目标蛋白得到了高纯度的表达。
五、实验结论
本实验通过原核表达系统成功表达了目标蛋白,并通过纯化和鉴定获得了高纯度的目标蛋白。
这为进一步研究该蛋白的功能和应用提供了基础。
生物化学中的蛋白质表达和纯化

生物化学中的蛋白质表达和纯化蛋白质是细胞中最基本的生物大分子之一,具有重要的结构和功能作用。
在生化实验研究中,常常需要大量的蛋白质作为实验材料。
蛋白质表达和纯化技术是生物化学研究中的关键技术之一。
本文将简要介绍蛋白质表达和纯化的原理和方法。
一、蛋白质表达技术蛋白质表达是将目的基因转录成RNA后再翻译成蛋白质的过程。
蛋白质表达主要有原核细胞和真核细胞两种方法。
原核细胞表达系统主要利用大肠杆菌,真核细胞表达系统则使用哺乳动物细胞,其主要的表达技术有以下几种:(一)重组蛋白质大规模表达重组蛋白质是指人为构建的同源或异源蛋白序列,利用基因工程技术将其导入到表达宿主中进行高效表达的蛋白质。
大肠杆菌是目前最常用的宿主。
一般来说,要将目的基因插入到选择性表达载体中,选用合适的启动子和终止子,将目的蛋白质与标签结合。
表达宿主随后被转化,蛋白质在生长过程中表达出来,随后进行纯化和鉴定。
(二)GST融合蛋白表达GST融合蛋白是利用GST (glutathione S-transferase)标签的蛋白质,将GST和目的蛋白质融合在一起表达,然后通过Glutathione 亲和层析纯化方法纯化目的蛋白质。
GST融合蛋白可以提高目的蛋白质的稳定性和可溶性,使得其在细胞内表达更加稳定。
(三)His标签蛋白表达His标签是一种聚组氨酸标签,可以与Ni2+螯合,因此可采用Ni2+亲和层析的方法纯化。
His标签融合蛋白表达时选择了较少的氨基酸标签,对目标蛋白的生物学性质和功能影响较小。
二、蛋白质纯化技术蛋白质表达和纯化是蛋白质生物化学研究的关键。
通常情况下,表达宿主细胞中的蛋白质必须经过纯化才能得到纯净的蛋白质,获得足够高纯度的蛋白质可用于测定其结构和功能。
(一)离子交换层析法离子交换层析法是利用蛋白质负荷(或正荷)的离子性质与相应的离子交换质团之间进行选择性结合的纯化方法。
离子交换层析法分为阴离子交换层析和阳离子交换层析两种。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
8.大肠杆菌表达系统与蛋白表达纯化大肠杆菌表达系统遗传背景清楚,目的基因表达水平高,培养周期短,抗污染能力强等特点, 是分子生物学研究和生物技术产业化发展进程中的重要工具。
因此熟练掌握并运用大肠杆菌表达系统的基本原理和常规操作是对每一个研究生来说是非常必要的。
本章节介绍了实验室常用的大肠杆菌表达系统的构成特点,归纳了利用大肠杆菌表达系统纯化重组蛋白的基本流程和详细操作步骤,并且结合笔者的操作经验,总结了初学者在操作过程中可能遇到的问题和解决策略。
8.1大肠杆菌表达系统的选择与构建8.1.1表达载体的选择根据启动子的不同这些载体大致可以分为热诱导启动子,如λPL,cspA 等和另外一类就是广泛使用的IPTG诱导的启动子,如lac,trc,tac,T5/lac operator,T5/lac operator等。
根据表达蛋白质的类型可分为单纯表达载体和融合表达载体。
融合表达是在目标蛋白的N端或C端添加特殊的序列,以提高蛋白的可溶性,促进蛋白的正确折叠,实现目的蛋白的快速亲和纯化,或者实现目标蛋白的表达定位。
常用的用于亲和纯化融合标签包括Poly-Arg,Poly-His, Strep-Tag Ⅱ,S-tag,MBP等。
其中His-Tag 和GST-Tag 是目前使用最多的。
His Tag 大多数是连续的六个His 融合于目标蛋白的N端或C端,通过His 与金属离子:Cu2+>Fe2+>Zn2+>Ni2+ 的螯合作用而实现亲和纯化,其中Ni2+是目前使用最广泛的。
His 标签具有较小的分子量,融合于目标蛋白的N端和C端不影响目标蛋白的活性,因此纯化过程中大多不需要去除。
目前常使用的表达载体主要是由Novagen 提供的pET 系列和Qiagen 公司提供的pQE 系列。
除了His 标签外,还原性谷胱甘肽S-转移酶是另一种实验室常用的融合标签。
它可以通过还原性谷胱甘肽琼脂糖亲和层析而快速纯化。
此外,与His 相比,GST 很多时候能够促进目标蛋白的正确折叠,提高目标蛋白表达的可溶性,因此,对于那些用his 标签表达易形成包涵体的蛋白,可以尝试用GST融合表达来改进。
当然,GST 具有较大的分子量(26kDa),可能对目的蛋白的活性有影响,因此很多时候切除GST是必须的。
目前,GST融合表达系统主要是由GE Healthcare(原Amersham)提供。
8.1.2宿主菌的选择重组质粒的构建一般选择遗传稳定,转化效率高,质粒产量高的菌株作为受体菌,常用的有E.coli DH5α,E.coli JM 109,E.coli DH 10B ,E.coli NovaBlμe等rec A–和end A–型细胞。
作为表达宿主菌必须具备几个基本特点:遗传稳定,生长速度快,表达蛋白稳定。
具体操作过程中,根据所使用的表达载体的特点,目的基因密码子的组成等选择特定的表达宿主菌。
以下是实验室常用的几种表达宿主:BL2:lon和ompT 蛋白酶缺陷型,避免了宿主对外源蛋白的降解。
是经典的使用最广泛的表达受体。
适用于Tac,Trc,Lac,λPL,cspA等作为启动子的载体。
BL21(DE3):DE3噬菌体溶源于BL21 形成的带有染色体T7 RNA 聚合酶基因大肠杆菌。
IPTG 诱导的lacΜV5 启动子控制T7 RNA 聚合酶基因表达T7 RNA 聚合酶,进而控制T7 表达系统表达目的蛋白。
BL21(DE3)衍生系列:在经典的T7表达系统BL21(DE3)的基础上,Novagen 公司开发了一些特殊的表达宿主细胞。
比如:Origami (DE3),Origami B(DE3)和Rosetta-gami (DE3)菌株带有trxB和gor双突变。
拥有trxB和gor突变的菌株比单具,trxB突变的菌株更有可能促进二硫键的形成,使蛋白可溶性更好,活性更高。
Rosetta™系列:是经过修饰,专用于带有大肠杆菌稀有密码子的真核蛋白表达的菌株。
经提高稀有tRNA 水平,可以提高一些真核基因表达效率(更多信息可参考相应公司的资料)。
BL21-Codon Plus系列:包括BL21-CodonPlus®(DE3)-RIPL,BL21-CodonPlμs®-RIL,BL21-CodonPlμs®(DE3)-RIL, BL21-CodonPlμs®-RP,BL21- CodonPlus®(DE3)-RP等。
这些受体菌添加了大肠杆菌中编码精氨酸(R),亮氨酸(L),异亮氨酸(I)和脯氨酸(P)稀有密码子的tRNA 基因,更多用于表达一些真核生物的基因。
其中RIL系列常用于AT 含量高的基因,而RP系列主要用于GC含量高的基因(更多信息参考Stratagene 公司资料)。
M15/SG13009:自身表达T5 RNA polymerase,主要用于pQE系列载体的表达。
另一个需要考虑的是大肠杆菌的密码子及其偏爱性。
表1 大肠杆菌密码子使用频率统计8.2表达条件的建立为了方便后续的纯化操作, 保持目标蛋白的活性,提高蛋白的得率,我们在进行蛋白的大量制备之前应该首先确定目标蛋白的最佳表达条件。
首先,保证表达蛋白稳定,尽量避免蛋白酶的降解,我们可以通过使用一些蛋白酶缺陷性的表达宿主,其次在表达的过程中可以在培养体系中添加一些蛋白酶抑制剂等来解决。
与实现外源蛋白的稳定表达相比,更多时候保证目标蛋白的可溶性表达,是建立表达条件的主要工作。
很多外源基因在大肠杆菌表达时很容易形成不可容的包涵体,其原因可能有:表达量过高,研究发现在低表达时很少形成包涵体,表达量越高越容易形成包涵体;蛋白合成速度太快,以至于没有足够的时间进行折叠,二硫键不能正确配对;过多蛋白间的非特异性结合,蛋白质无法达到足够的溶解度等。
目前对包涵体的形成和复性过程中发生聚集的机制尚不清楚, 但已经报道了很多用于优化表达以增加目标蛋白可溶性的方法。
8.2.1确定表达状况转化构建好的质粒至表达宿主感受细胞,挑取单克隆子至5ml 含有相应抗性的LB 培养基中,37℃,200 rpm,培养至OD600=0.5左右,加入IPTG至终浓度0.2mM,转移至28℃,200 rpm 继续诱导培养,可以在2h,4h,6h分别取样以分析表达状况。
将取出的1ml 菌液12000 rpm 离心1min,收集菌体,加入1ml PBS 缓冲液重悬沉淀,同样离心1min。
再加入300~500ml PBS重悬细胞。
超声破碎细胞(具体见操作细胞破碎)将破碎液体4℃,12000 rpm 离心10min,分离上清和沉淀。
SDS-PAGE 分析上清和沉淀的蛋白分布(具体操作参考SDS-PAGE)。
若在上清中有明显的目的蛋白的条带,即可以放大培养进而纯化目标蛋白。
若目标蛋白的表达主要分布于沉淀,则可以尝试一下几种方法来改善表达。
改变表达载体下手,像GST,NΜS,MBP, TrxA等融合标签能够提高很多蛋白在大肠杆菌中表达的可溶性,此外一些分泌标签如ompA,Pet-22b上的pelB也能够将目标蛋白运输至细胞的周质空间,从而提高目标蛋白的可溶性。
降低表达速度,可采取低温诱导,如15℃诱导过夜,或者采用弱启动子表达载体。
尝试一些特殊设计的表达宿主Origami:thioredoxin redμctase/glμtathione redμctase 双突变适合带thioredoxin redμctase的融合表达载体,帮助形成更多的二硫键。
对于一些蛋白可能无法实现可溶性表达,这时候溶解包涵体后再纯化是唯一的解决办法。
8.2.2聚丙烯酰胺凝胶电泳(SDS-PAGE)大肠杆菌表达纯化外源蛋白,SDS-PAGE是必不可少的操作。
可以用来检测蛋白的表达情况(表达量,表达分布等),用来分析纯化的目的蛋白的纯度。
本小节列出SDS-PAGE 操作中一些试剂的配置及其基本的操作过程。
8.2.2.1主要试剂的配置(1)30%丙烯酰胺贮存液:29g丙烯酰胺和1g N,N’-亚甲双丙烯酰胺溶于100ml热水中,验证其pH值不大于7.0。
置棕色瓶中,4℃保存。
丙烯酰胺具有很强的神经毒性并可以通过皮肤吸收,其作用具累积性。
称量丙烯酰胺和亚甲双丙烯酰胺时应戴手套和面具。
可认为聚丙烯酰胺无毒,但也应谨慎操作,因为它还可能会含有少量未聚合材料。
建议实验室划出专门的台面,设置单独的配置器皿进行SDS-PAGE 的相关实验。
(2)1.5mol/L Tris(pH8.8)溶液。
(3)10% SDS溶液:SDS 10.0g 加入ddH2O ToTo100。
(4)10%过硫酸铵:新鲜配制。
(5)TEMED溶液:4℃保存。
(6)1.0 mol/L Tris(pH6.8)溶液。
(7)2×样品溶解液:2%SDS,5%巯基乙醇,10%甘油,0.02%溴酚蓝,0.01mol/L Tris-HCl(pH8.0)缓冲液。
(8)5×Tris-甘氨酸电极缓冲液:15.1g Tris,94g甘氨酸和5g SDS定容到1000ml(建议每次电泳用新稀释的缓冲液)。
(9)考马斯亮蓝R染色液:每100ml甲醇、水、冰乙酸混合物(9:9:2)中,溶解0.25g考马斯亮蓝R,搅拌溶解。
(10)脱色液:10%冰醋酸(可加如乙醇,建议不要使用甲醇)。
8.2.2.2主要操作步骤1、凝胶制备(1)安装洗涤干净的玻璃板、板条,并将玻璃板固定在电泳槽中。
(2)配制10%的分离胶(具体参考表2):迅速在两玻璃板间隙中灌注分离胶,直至剩余的板宽比梳子长度多1cm。
小心在胶上覆盖一薄层异丙醇或水。
(3)在分离胶聚合的过程(可置于37℃,约10min)中,配制5%的积层胶(参考表格3)。
(4)分离胶聚合完全后,倒去异丙醇或水,用滤纸吸干胶面上的残余。
(5)灌注积层胶,立即插入干净的梳子,避免产生气泡。
(6)积层胶聚合完全后,小心拔出梳子,拨去封胶用的塑料条,固定于电泳槽。
(7)在上下电泳槽中加入足够的电泳缓冲液。
2、样品的制备在蛋白溶液中加入等体积的2×样品溶解液,混合液在沸水浴中加热5min,冷却后即可上样。
3、上样用微量移液器上样,每加入一种样品,上样量根据根据具体的样品浓度确定,未知浓度一般用10微升。
4、电泳对于一块胶,在浓缩胶中电流设置在15~20mA,当染料进入分离胶后可设置电压至电流约为25~30mA,继续电泳直至染料到达离凝胶底部1cm处。
5、后处理(1)染色:加入染色液(用量同上),室温染色30min~1h。
Tip:染色前可将染色液在微波炉里加热至沸,然后摇床震荡染色约10min即可。
(2)脱色:将染色后的胶块用水洗涤三次去除表面染料,然后加入脱色液脱色,其间更换脱色液3~4次至条带清晰。
