金刚烷胺的鉴别反应
药物分析:金刚烷胺

药物分析:金刚烷胺
俗称:金刚胺,三环癸胺,symmetrel
药物简介(考试大网站整理)
【性状】常用其盐酸盐,为白色闪光结晶或结晶性粉末;无臭,味苦。
在水或乙醇中易溶,在氯仿中溶解。
水溶液ph3.5~5。
【药理】
(1)进入脑组织后可促进释放多巴胺,或延缓多巴胺的代谢而发挥抗震颤麻痹作用。
对震颤麻痹有明显疗效,缓解震颤、僵直效果好。
起效快,用药后48小时作用明显,2周后达高峰,t1/210~28小时,药物以原形由肾排出,酸性尿排泄加速。
(2)抗亚洲a-Ⅱ型流感病毒作用。
对该型流感接触者保护率约70%。
(3)退热作用,对多种炎症、败血症、病毒性肺炎等与抗生素合用退热作用比单用抗生素好。
【应用】用于不能耐受左旋多巴治疗的震颤麻痹患者;用于亚洲a-Ⅱ型流感、病毒性感染发热患者。
【用法】口服:成人每次0.1g,早晚各1次,剂量每日400mg。
小儿用量酌减,可连用3~5日,最多10日。
1~9岁小儿每日3mg/kg,用量不超过150mg /日。
【注意】
(1)不良反应少,少数病人服后可有嗜睡、眩晕、抑郁、食欲减退等,亦可出现四肢皮肤青斑,踝部水肿等。
(2)震颤麻痹患者超过200mg/d时,疗效不增,毒性渐增。
老年患者耐受性低,可出现幻觉谵妄。
(3)精神病、脑动脉硬化、癫痫、哺乳妇女慎用。
可致畸胎,孕妇禁用。
肾功不良者酌减剂量。
盐酸金刚烷胺肝肾毒性

盐酸金刚烷胺肝肾毒性
盐酸金刚烷胺片的副作用有眩晕、失眠、神经质、恶心、呕吐、厌食、口干、便秘,偶尔可以见到抑郁、焦虑、幻觉、精神错乱、共济失调、头痛,罕见的是惊厥,少见白细胞减少以及中性粒细胞的减少。
这个药物是抗帕金森氏病的药物,可以用于帕金森病、帕金森综合征,还有药物诱发的锥体外系疾患、一氧化碳中毒后,帕金森综合征以及老年人合并有脑动脉硬化的帕金森综合征,也可以用于防止a 型流感病毒引起的呼吸道的感染。
它的有效期是36个月,在服用的时候,像帕金森病和帕金森综合征的患者,一次是100毫克,一天1到2次,一天最大的剂量是400毫克;在用于抗病毒的时候,成人一次是200毫克,一天一次或者一次100毫克,每12小时一次,1到9岁的小儿,要按体重,一次是1.5到3毫克每千克,八个小时一次或者是一次2.2到4.4毫克每千克,12小时一次。
以上方案仅供参考,具体使用情况请按药品说明或到正规医院按医嘱用药。
一种快速灵敏检测金刚烷胺的方法

一种快速灵敏检测金刚烷胺的方法摘要:目的:建立荧光法检测金刚烷胺的分析方法。
方法:合成一种具有荧光增强效应的环糊精聚合物,并制备了芘/环糊精聚合物复合探针。
结果:考察了复合探针用于检测金刚烷胺含量的可行性,并实现了水溶液中金刚烷胺含量的灵敏快速的检测。
结论:光化学检测金刚烷胺含量的方法,检测下线低,重现性好,有望用于更复杂体系中金刚烷胺的快速检测。
关键词:环糊精聚合物;金刚烷胺;测定[Abstract]Objective:Utilized a fluorescent method for quantitative detection of amantadine.Methods:Synthesized a kind of cyclodextrin polymer with fluorescence enhancement effect,and prepared the pyrene/cyclodextrin polymer composite probe.Results:The results showed that the prepared complex probe has the highest detection sensitivity for amantadine.The detection limit was 0.1 mmol/L. Conclusion:The method showed good reproducibility and low detection limit.The composite probe in future is expected to be used for more complex systems in the rapid detection of amantadine.[Keywords]cyclodextrin polymer;amantadine;determination金刚烷胺是一种具有对称结构的三环癸胺[1],原为抗病毒药,其抗帕金森病机制主要是促进纹状体多巴胺的合成和释放,减少神经细胞对多巴胺的再摄取,并有抗乙酰胆碱作用,从而改善帕金森病患者的症状。
HPLC法测定复方氨酚烷胺胶囊中盐酸金刚烷胺的含量word精品文档5页

HPLC法测定复方氨酚烷胺胶囊中盐酸金刚烷胺的含量复方氨酚烷胺胶囊由对乙酰氨基酚、盐酸金刚烷胺、马来酸氯苯那敏、人工牛黄、咖啡因几种主要成分组成,是临床常用的解热镇痛药。
中国药典中盐酸金刚烷胺的含量测定方法采用的是滴定法[1],该方法操作较为繁琐,认为误差较大。
为更有效、快速、可靠的测定盐酸金刚烷胺含量,2006年修虹等[2]建立了HPLC-ELSD方法测定复方氨酚烷胺胶囊中盐酸金刚烷胺的含量。
笔者在此基础上对盐酸金刚烷胺的测定方法进行了适当的改进,经过方法学验证,该方法回收率、准确度及重现性均为良好,且灵敏度与峰形更好,现报告如下。
1 实验材料1.1 仪器与设备Agilent 1260型高效液相色谱仪(配有脱气机、自动进样器、恒温箱、液相色谱泵、柱温箱及蒸发光散射检测器),由Chemstation化学工作站系统控制(Agilent,德国); METTLER TOLEDO AB135-S型十万分之一天平(METTLER,瑞士);XW-80A涡旋混合器(上海沪西分析仪器厂);TGL16M 型冷冻离心机(长沙英泰仪器有限公司);AHL-2001-P痕量型分析型超纯水机(艾科浦,重庆颐洋企业发展有限公司)。
1.2 试药与材料盐酸金刚烷胺对照品:由中国药品生物制品检定研究院提供,批号:100426-200301;复方氨酚烷胺胶囊:由四川某制药有限公司提供,批号:130408、1304010、130412、130415、130417;醋酸铵:天津科密欧化学试剂有限公司,分析纯,批号:120315;醋酸:天津科密欧化学试剂有限公司,分析纯,批号:121009;甲醇:美国Tedia公司,色谱纯,批号:1202257;纯水:自制去离子超纯水。
2 方法2.1 色谱条件色谱柱:Agilent TC-C18柱(4.6 mm×250 mm,5 μm,Agilent,美国);保护柱:Gemini C18(4 mm×3.0 mm,10 μm,Phenomenex,美国);流动相:甲醇-1%醋酸铵缓冲溶液(用醋酸调至pH 3.5)(22∶78);流速:1 ml/min;蒸发光散射检测器检测温度为104 ℃,雾化气(N2)流速:3.0 L/min;柱温:35 ℃;进样量:10 μl。
HPLC-ELSD法测定盐酸金刚烷胺片的含量

5 5℃ , 雾化气体 : 空气 ; 流速 2 0L mn . / i。对照 品及 样品色谱图见图 1 2 目录后 ) — ( 。在该色谱条件下 ,
理 论 塔板数 按 金 刚烷胺 峰计算 应 不低 于 400 0 。
1 3 4 方法 学 考察 ..
药 品生物 制 品检定 所 , 号 :04 6— 0 3 1 , 酸 批 102 20 0 ) 盐 金刚烷 胺 片 为 市 售 , 为 纯 化 水 , 腈 、 氟 乙 酸 均 水 乙 三 为分 析纯 。
134 4 重 复性试 验 : 密称 取 同 一批 盐 酸 金刚 烷 .. . 精 胺 片细 粉 , “ .. .” 按 134 1 的方 法制 备 , 录色谱 图 , 记 结
果 R D为 16% . S .
各 3份 , 加水 稀 释 至 刻 度 , 匀 , 摇 即得 加 样 回 收样 品
l , 重复进样 6次 , 记录色谱图。平均峰面积的对数
为 320 ,S .3 3 R D为 0 2% 。 .
1 3 4 6 加 样 回 收 率 试 验 : 密 称 取 已 知 含 量 . .. 精 (55 ) 9 .% 的盐 酸金 刚 烷 胺 片 ( 苏 鹏鹞 药业 有 限 公 江
司 , 号 :9 2 9 ) 批 0 1 1 2 细粉 9份 , 10ml 瓶 中 , 水 置 0 量 加
试 验 方 法
金刚烷胺标准品中纯度受限的杂质分析

化学分析计量CHEMICAL ANALYSIS AND METERAGE第24卷,第1期2015年1月V ol. 24,No. 1Jan. 20155doi :10.3969/j.issn.1008–6145.2015.01.002金刚烷胺标准品中纯度受限的杂质分析张立华,周剑,陈洁,王敏(中国农业科学院农业质量标准与检测技术研究所,农业部农产品质量安全重点实验室,北京 100081)摘要 为确定购买的金刚烷胺标准品中使纯度受限的主要杂质成分,用质量平衡法对标准品中主成分含量进行定值分析。
采用红外光谱、质谱等方法对金刚烷胺标准品的主成分进行定性,用气相色谱–质谱法、顶空气相色谱法、卡尔费休法对其主要杂质进行确证并定量。
结果表明金刚烷胺标准品中主要杂质成分为溴代金刚烷胺、甲醇、乙苯和水,含量分别为1.53%,0.0376%,0.0045%,0.41%,经计算金刚烷胺标准品的纯度为98.16%。
该方法可用于金刚烷胺标准品主要杂质的定性、定量分析,对其纯度值进行验证。
关键词 金刚烷胺标准品;气质联用法;顶空气相法;卡尔费休法;杂质分析中图分类号:O658 文献标识码:A 文章编号:1008–6145(2015)01–0005–05Determination and Indentification of Related Substances of Amantadine StandardZhang Lihua ,Zhou Jian ,Chen Jie ,Wang Min(Key Laboratory of Agrifood Safety and Quality ,Ministry of Agriculture ,Institute of Quality Standards and Testing Technology for Agro-products ,Chinese Academy of Agricultural Sciences ,Beijing 100081,China)Abstract To determine the related substances which limit the purity of the amantadine standard and the mass balance method was adopted to definite the value of component content of amantadine standard. Infrared spectrum and mass spectrum method were adopted to determine the nature of the main component of amantadine standard. At the same time ,the gas chromatography–mass spectrometry ,headspace gas chromatography and Karl Fischer method were applied to identify and quantify the related substances. Ultimately ,1-bromoadamantane ,methanol ,ethylbenzene and water were the main impurities in amantadine standard , and the content of which were 1.53%,0.037 6%, 0.004 5% and 0.41%. The purity of the amantadine standard was 98.16%. This method can be used for qualitative and quantitative analysis of main impurities in amantadine ,and verification of amantadine purity.Keywords amantadine standard; GC–MS; headspace–GC; Karl Fischer method; impurity标准物质在分析实验中广泛用于校准仪器、评价测试方法及为材料赋值,其正确使用对保证分析结果的准确性、溯源性有重要意义[1]。
内标法测定鸡肉中金刚烷胺含量方法的优化--高效液相色谱-串联质谱法

内标法测定鸡肉中金刚烷胺含量方法的优化--高效液相色谱-串联质谱法
金刚烷胺是一种重要的抗菌剂,由于其疗效稳定、抗菌作用全面,因此被广泛
应用于兽医药领域。
为了精确测定其在鸡肉中的含量,研究者在不断优化方法的基础上,提出了利用高效液相色谱-串联质谱法测定鸡肉中金刚烷胺含量的方法。
首先,采用Classic L-column柱色谱,在80%甲苯-0.5%甲醛溶剂组合中以
0.5mL/min流速进行分离。
通过调节柱温度、流速和流量,可以提高样品的灵敏度
和稳定性,避免非特异性偏离波现象的出现。
分离完成后,采用MS/MS技术,利用温度端控即可进行鉴定,该技术可以克服分子相互间的结合和避免峰的失效,实现精准风准的检测目标。
此外,还研究了各种条件,包括柱温、ELUTION溶剂、流速和流量,以及使用MS/MS技术进行定性和定量。
结果表明,在测定条件下,该方法可以有效识别和定
量金刚烷胺,且质谱峰强度稳定,重复性和精密度良好。
使用高效液相色谱-串联质谱法测定鸡肉中金刚烷胺含量的方法具有以下优点:首先,可以实现高灵敏性和精确性的检测;其次,能够同时实现定量和定性;最后,条件的优化能够有效地解决准精安等检测困难。
总而言之,使用高效液相色谱-串联质谱法测定鸡肉中金刚烷胺含量的方法实
现了快速精准的金刚烷胺测定,为优质的兽医制造提供了可靠的测量依据。
DB22T 2268-2015 饲料中金刚烷胺的测定 液相色谱-质谱质谱法.pdf

准仅 8 结果计算和表述
供内 按(1)式计算试样中金刚烷胺含量,计算结果需扣除空白值。
部使用 式中:
X = c ×V ...............................................................................................(1) m
4.14 乙腈-0.1 %甲酸混合溶液(40+60):量取 40mL 乙腈与 60 mL 的 0.1 %甲酸溶液(4.12),混匀。
4.15 金刚烷胺标准储备液:100.0 mg/L。准确称取适量金刚烷胺标准物质(4.2)用甲醇溶解并全部
转移至 50 mL 容量瓶中,用甲醇定容至刻度,混匀。
1
DB22/T 2268—2015
使用 表2 定性分析时相对离子丰度的最大允许偏差
相对离子丰度 允许的相对偏差
7.4.5 定量测定
>50% ±20%
>20%至50% ±25%
>10%至20%
不得翻印 ±30%
≤10% ±50%
做两份试料的平行测定。根据试样中被测样液中被测组分的含量情况,选取响应值相近的标准工作
液进行分析,对于高浓度样品须适当进行系列稀释。标准工作液和样液中被测组分的响应值均应在仪器
h) i) j)
碰撞气:0.15 MPa;
不 离子源温度:550.0 ℃; 得 定性离子对、定量离子对、去簇电压、碰撞能量见表 1。
翻印 表1 金刚烷胺的监测离子对、去簇电压和碰撞能量
化合物名称 金刚烷胺 a 定量离子。
食品中金刚烷胺类化合物检测方法的研究

金刚烷胺、金刚乙胺、美金刚胺是母体结构为饱和环癸烷的金刚烷胺类化合物。
金刚烷胺、金刚乙胺都是FDA批准的抗甲型流感病毒的药物,能在极低浓度下通过M2蛋白质子通道抑制甲型流感病毒的复制[1-3]。
美金刚胺是金刚乙胺的同分异构体,作用机理相似。
虽然许多国家禁止在家禽养殖中使用金刚烷胺和金刚乙胺[4-5],但在中国和美国,这类化合物仍被非法用于家禽(尤其是鸡)养殖中[6],原因可能是:①金刚烷胺类化合物价格低廉,抗流感病毒活性好;②农户为减少在禽流感肆虐流行期间的经济损失,不顾法律法规定期给禽类喂食药物;③饲料厂家在产品中添加药物,从而吹嘘该产品具有增强机体抵抗力的功效。
金刚烷化合物的滥用,使得耐药菌株出现,并呈增加的趋势[7]。
在我国,兽药已从传统线下营销模式慢慢转向互联网营销模式,2019年9月,在“某”宝、“某”多多、“某”巴巴等APP上搜索“金刚烷胺兽用”“金刚乙胺兽用”,发现不少商家销售金刚烷胺类化合物。
同时,还有部分商家宣传金刚烷胺类化合物具有预防和治疗畜禽及家禽流感病毒的功效。
鉴于金刚烷胺类化合物在我国的滥用情况,本文对近年来金刚烷胺类化合物的检测方法进行综述,希望为监管检验研究人员提供参考和借鉴。
1 色谱分析法1.1 高效液相色谱技术高效液相色谱技术(HPLC)是有机化合物分析运用中最普遍的一种检测方法。
HPLC法的检测器有紫外检测器(包括UV、DAD)、电化学检测器(ECD)。
金刚烷胺类化合物是稳定饱和的三环胺化合物,仅吸收小于200 nm的波长辐射,紫外响应极小,需经衍生化才能通过紫外检测器测定。
F.A.L.Van Der Horst等[8]采用十六烷基三甲基溴化铵(CTAB)胶束介导,研究了尿中金刚烷胺柱前衍生结合反相高效液相色谱的在线测定方法。
在60 ℃和pH为11条件下,金刚烷胺与1-氟-2,4-二硝基苯进行衍生化,4min内完全转化为含有色基团的衍生物,从而产生紫外检测信号。
金刚烷胺

适用于原发性帕金森病、脑炎后的帕金森综合征、药物诱发的锥体外系反应、一氧化碳中毒后帕金森综合征 及老年人合并有脑动脉硬化的帕金森综合征。也可用于预防或治疗亚洲甲-Ⅱ型流感病毒所引起的呼吸道感染。本 品与灭活的甲型流感病毒疫苗合用时可促使机体产生预防性抗体。
1、抗震颤麻痹口服,成人常用量:一次100mg,每日1~2次,每日最大量为400mg。肾功能障碍者应减量。 小儿不用。
摩尔折射率:45.67 摩尔体积(cm3/mol):141.7 等张比容(90.2K):370.8 表面张力(dyne/cm):46.7 极化率(10 -24cm 3):18.10
疏水参数计算参考值(XlogP):无 氢键供体数量:1 氢键受体数量:1 可旋转化学键数量:0 互变异构体数量:0 拓扑分子极性表面积:26 重原子数量:11 表面电荷:0 复杂度:144 同位素原子数量:0 确定原子立构中心数量:0
(6)逾量中毒的表现:惊厥,见于用4倍于常用量时;严重的情绪或其他精神改变,严重的睡眠障碍或恶梦。 眩晕,嗜睡,抑郁,食欲减退,四支皮肤青斑,踝部水肿,老年患者可出现幻觉谵妄、精神失常或错乱,个别病 例有充血性心力衰竭,可引起肾损害。
1、金刚烷胺有退热作用,与多种抗炎药及抗菌药合用时,疗效比单用抗菌药好。 2、其他抗帕金森药、抗组胺药、吩噻嗪类或三环类抗抑郁药与金刚烷胺合用,可增强抗胆碱作用,特别是有 精神错乱、幻觉及恶梦的患者更明显。合用时需调整这些药物或金刚烷胺的用量。 3、与中枢神经兴奋药合用时,可增强中枢神经的兴奋作用,严重者可引起惊厥或心律失常等不良反应。 4、与氨苯蝶啶合用,金刚烷胺的肾脏清除率降低,中毒反应的发生率升高。如两药必须合用,应监测金刚烷 胺的毒性反应。 5、颠茄和金刚烷胺均有抗胆碱作用,合用时可产生过度的抗胆碱作用。 6、复方新诺明与金刚烷胺合用,可导致二者经肾小管分泌的量均减少,故可增加中枢毒性,出现失眠,精神 错乱等症状。 7、槟榔有拟胆碱作用,与金刚烷胺合用时两者的胆碱及抗胆碱作用相互拮抗,造成二者的效应降低。 8、溴哌利多可对抗金刚烷胺的药理作用,故会降低金刚烷胺的疗效。 9、从理论上讲,卡法根可对抗金刚烷胺的多巴胺作用,降低金刚烷胺的疗效。
气相色谱法测定饲料中金刚烷胺药物的含量

摘 要 :实验 建 立 了 气相 色谱 法检 测饲 料 中金 刚 烷 胺 含 量 的 方 法 ,饲 料 中 的金 刚烷 胺 用 甲 醇 :三 氯 乙酸 一 1:1提 取 ,取 上 层 提 取 液 经 MCX 阳 离子 交换 柱 净 化 ,用 氨 水 + 异 丙 醇 + 甲 醇 一 5+25+ 70混 合 液 5 ml洗 脱 ,经 氮 吹 浓 缩 ,浓 缩 物 在碱 性 条 件 下 用三 氯 甲烷 溶 剂 复溶 ,取 有机 层 进 行 气相 色谱 仪一FID测 定 ,外 标 法定 量 ,方 法检 出 限 达 到 1.0 mg/kg,方 法 回 收 率 达 到 76.7 ~98.3 ,相 对 标 准 偏 差 小 于 5 。 关 键 词 :饲 料 ;金 刚 烷 胺 ;气相 色谱 法 中 图分 类 号 :¥816.17 文 献 标 志 码 :A 文 章 编 号 :1003— 6202(2O18)02—0037—04
Determ ination of am antadine by gas chrom atography in feed ZH A N G Cui—fen D ON G W ei feng。 (1.Dalian Vocational and Technical College,Dalian 116035,China;2.Liaoning Entry Exit Inspection and Quarantine Bureau, Dalian 1 l6001,China) ABSTRACT :The determ ination m ethod of am antadine by gas chrom atography in feed was established. A mantadine in feed w as extracted w ith 1 : 1 ratio of m ethanol to trichloroacetic acid ,T he upper extract was purified by M CX cation exchange colum n, w hich eluted by 5 m l m ixed liquor (com posed of am m onia 5,isopropanol 25 and m ethanol 70),it w as concentrated by nitrogen concentration,the concentrate is redissolve by trichlorom ethane in alkaline conditions,and the organic layer was determined by the gas chromatograph FID ,By means of the external standard m ethod,the detection limit reached 1.0 mg/kg,the recovery rate of the m ethod reached 76.7 一98.3 , and the relative standard deviation was less than 5 . KEYW ORDS:feed;amantadine;gas chromatography
高效液相色谱-质谱法分析(金刚烷胺)原始记录
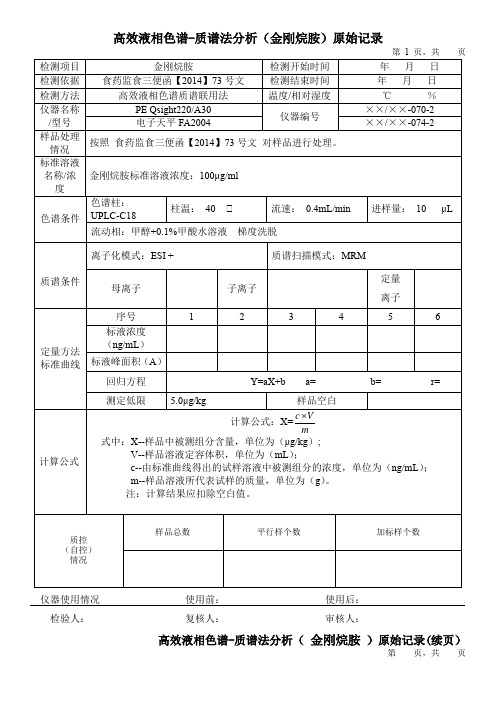
按照食药监食三便函【2014】73号文对样品进行处理。
标准溶液名称/浓度
金刚烷胺标准溶液浓度:100μg/ml
色谱条件
色谱柱:UPLC-C18
柱温:40 ℃
流速:0.4mL/min
进样量:10 μL
流动相:甲醇+0.1%甲酸水溶液梯度洗脱
质谱条件
离子化模式:ESI +
质谱扫描模式:MRM
平均值
(μg/kg)
相对偏差
(%)
仪器使用情况使用前:使用后:
检验人:复核人:审核人:
母离子
子离子
定量
离子
定量方法标准曲线
序号
1
2
3
4
5
6
标液浓度(ng/mL)
标液峰面积(A)
回归方程Байду номын сангаас
Y=aX+b a= b= r=
测定低限
5.0μg/kg
样品空白
计算公式
计算公式:X=
式中:X--样品中被测组分含量,单位为(μg/kg);
V--样品溶液定容体积,单位为(mL);
c--由标准曲线得出的试样溶液中被测组分的浓度,单位为(ng/mL);
m--样品溶液所代表试样的质量,单位为(g)。
注:计算结果应扣除空白值。
质控
(自控)
情况
样品总数
平行样个数
加标样个数
仪器使用情况使用前:使用后:
检验人:复核人:审核人:
高效液相色谱-质谱法分析(金刚烷胺)原始记录(续页)第页,共页
样品编号
试样质量
( g )
定容体积
(mL)
组分浓度
(ng/mL)
用酶联免疫试剂盒检测鸡肉中的金刚烷胺

2018年第3期金刚烷胺为禁止用于兽用的抗病毒药品。
金刚烷胺具有神经毒性,能使中枢神经系统受刺激或中毒,在食品中残留,对心肺及肾功能不全者,还容易导致蓄积毒性。
1酶联免疫试剂盒准备金刚烷胺酶联免疫试剂盒(Ⅳ型)。
北京维德维康生物技术有限公司生产。
2原理鸡肉中的金刚烷胺与酶标板上固定的金刚烷胺特异性竞争抗体,当鸡肉中不含金刚烷胺或金刚烷胺含量很少时,更多的抗体就会与酶标板上的金刚烷胺结合,结合物被固定在酶标板上,加入酶标记物以后,底物被催化显色,根据显色的深浅来判断鸡肉中金刚烷胺的含量。
显色越深,含量越少,显色越浅,含量越多。
3工作液准备1份浓缩样品提取液加19份去离子水。
1份浓缩样品稀释液加9份去离子水。
1份浓缩洗涤液加19份去离子水。
1份酶标记物浓缩液加10份酶标记物稀释液。
4鸡肉前处理称取2±0.05g 均质后的鸡肉于50mL 离心管中。
加入4mL 样品提取液充分涡动5min 。
离心机4000g 以上,离心5min 。
取0.2mL 上清液于干净离心管中,加入0.2mL 样品稀释液充分涡动10s 。
取50μL 进行检测。
5检测根据样品数量的多少取出相应数量的酶标板条固定在酶标板架上,要求做两个平行样,标记清楚标准品和样品的滴加位置。
未使用的酶标板条用自封袋密封后,立即保存期于2~8℃环境中。
将50μL 各标准品工作液(0、0.1、0.3、0.9、2.7、8.1ppb )和50μL 各样品溶液分别加入对应的酶标板孔中。
各孔均加入50μL 酶标记物工作液,枪头不能接触到酶标板孔中的液体。
把酶标板用盖板膜盖好,轻轻振荡酶标板10s ,使溶液充分混匀,在室温(25±2℃)下避光反应30min 。
揭开盖板膜,把酶标板孔中的液体倒净,在每个孔中分别加入260μL 洗涤工作液,充分洗涤4次,每次浸泡10~20s 。
洗涤完毕后,倒掉酶标板孔中洗涤工作液,将酶标板倒倒置于吸水纸上,轻轻拍打到拍干。
荧光法测定片剂中金刚烷胺的含量

荧光法测定片剂中金刚烷胺的含量张文伟3 杨 梅 施 杰 王立艳(辽宁师范大学化学系,大连116029) 2001205226收稿;2001211228接受1 引 言金刚烷的衍生物金刚烷胺是临床应用已久的抗病毒、抗震颤麻痹的药物,也是预防治疗甲型流感病毒引起的上呼道疾病的抗感冒药。
测定金刚烷胺的方法有电化学方法1和气相色谱法2以及中国药典3采用的银量法。
采用荧光分光光度法直接测定金刚烷胺的方法未见报道。
作者详细地研究了金刚烷胺的荧光光谱,发现金刚烷胺有较强的荧光性质,据此建立了金刚烷胺的测定方法。
荧光强度与金刚烷胺含量在0.5~30.0mg/L 的质量浓度范围内呈良好的线性关系,检出限为0.26mg ΠL 。
对质量浓度为0.5mg ΠL 的金刚烷胺标准溶液进行了11次平行测定的相对标准偏差为1.46%。
方法简便、快速、灵敏度高。
用于药物中金刚烷胺片剂含量的测定,结果满意。
2 实验部分2.1 仪器和试剂 RF 2540型荧光分光光度(日本岛津公司);PHI 2F L 型酸度计(杭州樊隆仪器制造厂)。
金刚烷胺(东北制药厂提供)储备液500.0mg ΠL ;缓冲溶液为伯瑞坦2罗比森(Britton 2R obins on )缓冲体系,pH 11.0;其它试剂均为分析纯,实验用水为去离子水经石英亚沸蒸馏器蒸馏所得。
2.2 实验方法 取一定量的金刚烷胺标准溶液于25m L 比色管中,加入10m L 缓冲溶液,用水稀释至刻度,摇匀,放置10min 后。
在λex =305nm 、λem =415nm 处,以试剂为空白测定溶液的相对荧光强度值ΔF 。
3 结果与讨论3.1 荧光光谱 在RF 2540型荧光分光光度计上扫描质量浓度为1.0mg ΠL 的金刚烷胺溶液的激发光谱和发射光谱。
发现金刚烷胺的最大激发波长λex =305nm ,最大发射波长λem =415nm 。
3.2 条件实验 (1)酸度的影响 用Britton 2R obins on 缓冲体系控制酸度,研究在不同酸度条件下金刚烷胺的荧光强度,依次以pH =2~12缓冲溶液为空白,测定1.0mg ΠL 金刚烷胺溶液相对荧光强度ΔF 。
金刚烷胺判定依据

金刚烷胺判定依据
金刚烷胺(Diamondoid amine)是一种有机化合物,它是金刚
烷(Diamondoid)与胺(Amine)官能团结合形成的化合物。
金刚烷胺的判定依据可以从其化学性质和物理性质入手。
化学性质:
1. 金刚烷胺是一种有机化合物,可用有机合成方法合成,比如金刚烷与胺的反应。
2. 它含有胺基官能团,具有碱性,可以和酸反应生成盐。
3. 它在一定条件下可以发生酰化、烷基化、烯化等常见有机反应。
物理性质:
1. 金刚烷胺是一种固体,通常是白色晶体或结晶粉末的形式。
2. 它在常温下无味无臭,有时具有特殊的化学气味。
3. 它的熔点、沸点、密度等物理性质可以用于判定和鉴定。
当然,准确的判定金刚烷胺还需要通过化学分析方法,如质谱、红外光谱、核磁共振等技术手段进行进一步的鉴定确认。
盐酸金刚烷胺检验操作规程

制药有限公司GMP管理文件一、范围:本标准规定了盐酸金刚烷胺检验操作规程;适用于本公司对盐酸金刚烷胺的质量检测。
二、引用标准:中华人民共和国药典(2000年版)三、质量指标:四、试剂1、盐酸(AR)2、硅钨酸(AR)3、冰醋酸(AR)4、醋酸汞(AR)5、高氯酸(AR)五、仪器与用具1、红外分光光度计2、酸度计六、结构式和分子量NH2HC lC10H17N·HCl 187.71本品为三环[3.3.1.13,7]癸烷-1-胺盐酸盐。
按干燥总计算,含C10H17N·HCl不得少于99.0%。
七、操作步骤:1、性状:本品为白色结晶或结晶性粉末,无臭,味苦。
本品在水或乙醇中易溶,在氯仿中溶解。
2、鉴别:(1)取本品10mg,加水2ml溶解后,加盐酸使成酸性,滴加硅钨酸试液,即析出白色沉淀。
(2)本品的红外光吸收图谱应对照的图谱(光谱集369图)一致。
(3)本品的水溶液显氯化物的鉴别反应(附录III)。
3、检查:3.1 酸度:取本品2.0g,加水10ml使溶解,依法规定(见PH测定操作规程),PH值应为3.5~5.0。
3.2 溶液的澄清度与颜色:取本品1.0g,加水10ml溶解后,溶液应澄清,无色;如显浑浊,与1号浊度标准液(见溶液的澄清度与颜色检查对操作规程)比较,不得更浓;如显色,与黄色2号标准比色液比较,不得更深。
3.3 干燥失重:取本品,在105℃干燥至恒重,减失重量不得过0.5%(见干燥失重测定操作规程)。
3.4 炽灼残渣:不得过0.1%(见炽灼残渣检查操作规程)。
3.5 重金属:取本品2.0g,加水23ml溶解后,加醋酸盐缓冲液(pH3.5)2ml,依法检查(见重金属检查操作规程),含重金属不得过百分之五。
4、含量测定:HCL 4.1 原理:本品在冰醋酸中,与醋酸汞试液,反应生成醋酸金刚烷胺和难电离的氯化汞,用高氯酸液滴定,生成高氯酸金刚烷胺和醋酸,微过量的高氯酸使结晶紫显蓝色为终点。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
盐酸金刚烷胺的鉴别反应(2005年版中国药典):
1、取本品10 mg,加水2 mL溶解后,加盐酸使成酸性,滴加硅钨酸试液,即析
出白色沉淀。
2、本品的红外光吸收图谱应与对照的图谱(光谱集369图)一致。
3、本品的水溶液显氯化物的鉴别反应。
氯化物鉴别反应:
(1)取供试品溶液,加稀硝酸使成酸性后,滴加硝酸银试液,即生成白色凝乳状沉淀;分离,沉淀加氨试液即溶解,再加稀硝酸酸化后,沉淀复生成。
如供试品为生物碱或其他有机碱的盐酸盐,须先加氨试液使成碱性,将析出的沉淀滤过除去,取滤液进行试验。
(2)取供试品少量,置试管中,加等量的二氧化锰,混匀,加硫酸湿润,缓缓加热,即发生氯气,能使用水湿润的碘化钾淀粉试纸显蓝色。
检查:
酸度取本品2.0 g,加水10 mL溶解后,依法测定,pH值应为3.5~5.0。
含量测定取本品约0.15 g,精密称定,加0.01 mol/L盐酸5 mL与乙醇50 mL 使溶解,照电位滴定法(附录ⅦA),用氢氧化钠滴定液(0.1mol/L)滴定,读取两突跃点的体积之差。
每1ml的氢氧化钠滴定液(0.1mol/L)相当于18.77mg 的C10H17N·HCl(2010年版中国药典修订方法)。
莽草酸检测出现类似金刚烷胺反应的解释:
1、盐酸金刚烷胺鉴别反应有3项,其中第1项和第3项为非特异性反应,化合物中只要有Cl-、-NH2存在,很容易发生相关反应。
因此,检测莽草酸时出现了第1项和第3项的反应,不能立即下定论说莽草酸中含金刚烷胺。
可进行第2项,即比对两者的红外图谱,能直接说明问题。
2、针对上述的解释,有人会提出,莽草酸中含有Cl-,为何公司产品资料中莽草酸结构式中没有显示?答案是:由于市场上盗版猖獗,公司处于保密考虑,只公示了莽草酸的通用结构式,而将结构修饰后的莽草酸结构式隐藏。
莽草酸的工艺
中有Cl-、-NH2存在,所以会有第1项和3项的类似反应,但莽草酸是安全的。
3、有客户反应:用滴定法能检测到金刚烷胺的含量,那么动物食品中也能检测到金刚烷胺残留,即使上述两条解释能说明问题,那么残留问题如何解释?回答:目前动物性食品中金刚烷胺的主流检测方法是LC-MS/MS方法,是一种灵敏度更高的检测方法。
该方法能根据定性定量离子帮助确定莽草酸是否含金刚烷胺。
可以肯定的说,莽草酸无残留问题,检测安全,可放心使用。
